Влияние содержимого кишечника на гены эпителиальных клеток кишечника
Добавил пользователь Евгений Кузнецов Обновлено: 28.01.2026
Для цитирования: Нарушение нормального состава кишечных бактерий: клиническое значение и вопросы терапии. РМЖ. 2008;2:41.
Микрофлора пищеварительного тракта представляет собой сложную экологическую систему, включающую наряду с кишечными бактериями слизистые оболочки хозяина, компоненты пищи, вирусы, грибы. Основная масса нормальных кишечных бактерий фиксирована к специфическим рецепторам энтероцитов слизистой оболочки желудочно-кишечного тракта, образуя микроколонии (мукозная, пристеночная микрофлора), и лишь незначительная ее часть находится в свободном состоянии в просвете кишки (внутрипросветная микрофлора). Кишечная микрофлора подразделяется на облигатную (синонимы: главная, резидентная, индигенная, аутохтонная), факультативную (сапрофитная и условно-патогенная) и транзиторную (случайная). В состав облигатной микрофлоры входят анаэробы: бифидобактерии, пропионобактерии, пептострептококки и аэробы (лактобактерии, энтерококки и эшерихии). Факультативная микрофлора представлена сапрофитами (бактериоиды, пептококки, стафилококки, стрептококки, бациллы, дрожжевые грибы) и аэробными и анаэробными бациллами. К условно патогенным энтеробактериям относятся представители семейства кишечных бактерий: клебсиеллы, протеи, цитробактеры, энтеробактеры и др.
Литература
1. Григорьев П.Я., Яковенко Э.П. Нарушение нормального состава кишечной микрофлоры, клиническое значение и вопросы терапии. Методическое пособие. М., 2000. 15 с.
2. Gibson G.R., Macbarlane G.T. Human colonic bacteria: role in nutrition, physiolody and pathology. Boca Ratoh: CRC Press. - 1995. - 250 Р.
3. Белоусова Е.А., Никитина Н.В., Мишуровская Т.С., Златкина А.Р. Возможности препаратов на основе микробных метаболитов для восстановления кишечной микробиоты.// Consilium medicum. 2005. Выпуск № 1. С. 9-13.
4. Грачева Н.М., Ющук Н.Д., Чупринина Р.П., Мацулевич Т.В., Пожалостина Л.В. Дисбиозы кишечника, причины возникновения, диагностика, применение бактерийных биологических препаратов. Пособие для врачей и студентов. М. 1999. 44 с.
5. Rose S. Gastrointestinal and Hepatobiliary pathophysiology. Fence Greek Publishing, LLC, Madison. 1998. 475 p.
6. Шендеров Б.А. Медицинская микробная экология и функциональное питание // Микрофлора человека и животных и ее функции. - Т. 1. - М.: Грантъ, 1998.
7. Yakovenko E., Grigoriev P., Tcherenchimediins at all. Is irritable bowel syndrome (IBS) related to altered gut flora? // Gut.-1997. Vol.41, suppl.3.-P.A.-123.
8. Яковенко Э.П., Агафонова Н.А. Схемы профилактики и коррекции нарушений баланса кишечной микрофлоры при проведении антибиотикотерапии. Применение пробиотических препаратов. //Consilium medicum. 2002. № 11. С. 6-7.
9. Bouvier M. et al. Effects of consumption of a milk fermented by the probiotic Bifidobacterium animalis DN 173 010 on colonic transit time in healthy humans // Bioscience and Microflora. - 2001. - Vol 20 (2). - P. 43-48.
10. Шостакович Корецкая Л.Р., Кривуша Е.Л.,Чергинец А.В. Тактический подход к коррекции дисбиоза кишечника у детей пробиотическими препаратами. Опыт применения препарата Линекс. //Украинский медицинский журнал.1999.№ 2. С. 61-64.
11. Ушкалова Е.А. Роль пробиотиков в гастроэнтерологии. //Фарматека. 2007. № 6. С.16-23.
Молекулярно-генетические аспекты канцерогенеза в толстой кишке
Колоректальный рак (КРР), или карцинома толстой кишки (ТК), — это злокачественная опухоль, состоящая из эпителиальной ткани и поражающая слепую, ободочную и/или прямую кишку, включая ее анальный отдел [1].
Данная форма рака наиболее часто встречается в развитых странах, занимая в структуре онкологической заболеваемости третье место у мужчин и второе — у женщин [2]. Опухоли толстой и прямой кишки по своей распространённости уступают лишь раку легкого. Ежегодно в мире диагностируется более 1 млн. 200 тыс. карцином толстой кишки и отмечается около 700 тыс. смертей от данной патологии. При этом в Германии ежегодно диагностируют 50 тыс. первично обнаруженных заболеваний КРР. Много таких больных в Дании, Ирландии и Нидерландах: 40-61 случай на 100 тыс. В России за последние 50 лет (с 1960 по 2010 г.) количество первичных заболеваний КРР выросло в 7 раз. За 10 лет число больных увеличилось на 22 % и достигло 46 тыс. в год. В США ежегодно выявляют 150 тыс. новых случаев КРР, из них 55-60 тыс. заканчиваются смертельным исходом [1].
Таким образом, проблема КРР стала в последнее время одной из наиболее актуальных медико-социальных проблем, требующей самого пристального внимания исследователей.
Эпидемиологическими исследованиями в большинстве развитых стран была установлена тесная корреляционная связь увеличения заболеваемости с тремя основными факторами [3]:
‒ увеличением потребления в пищу животных жиров и белков. Известно, что продукты распада белков могут быть материалом для кишечного синтеза N-нитрозаминов и других метаболитов, которые обладают канцерогенной активностью;
‒ снижением потребления в пищу волокнистой клетчатки. Чрезмерная очистка углеводов приводит к снижению массы невсасываемой целлюлозы, являющейся своего рода адсорбентом для экзогенных и эндогенных канцерогенов. Также удлиняется время пассажа по кишечнику;
‒ наличие кишечном содержимом эндогенных канцерогенов: индола, скатола, гуанидина, метаболитов стероидных гормонов;
‒ менее подвижным образом жизни современного человека, что также ведёт к замедлению пассажа по кишечнику.
Также факторами риска являются ожирение, возраст старше 50 лет, гипотония и атония кишечника (приводит к хроническим запорам и воздействию на слизистую толстой кишки канцерогенов в условиях длительного застоя каловых масс, и как следствие, её травматизация в местах физиологических изгибов) [3].
Существует 4 класса генов, которые задействованы в процессе канцерогенеза [1]:
1) протоонкогены — это нормальные гены клеток, участвующие в регуляции процессов их роста и дифференцировки. В зрелых тканях они, как правило, неактивны. Активация протоонкогенов и превращение их в клеточные онкогены происходят при опухолевом росте и в ходе эмбриогенеза. Некоторые клеточные онкогены активируются также при пролиферации и дифференцировке клеток в очагах репаративной регенерации;
2) гены-супрессоры опухолей (антионкогены), ингибирующие пролиферацию клеток;
3) гены, участвующие в гибели клеток путем апоптоза. Известно, что апоптоз — генетически запрограммированная смерть клеток в живом организме. Основная биологическая роль апоптоза в норме — установление нужного равновесия между процессами пролиферации и гибели клеток;
4) гены, отвечающие за процессы репарации ДНК.
В соответствии с наличием или отсутствием наследственной предрасположенности к КРР выделяют 3 его формы:
‒ наследственный семейный неполипозный КРР (синдром Линча);
‒ наследственный КРР при семейном аденоматозе;
‒ спорадический (ненаследственный) КРР.
На долю наследственных форм КРР приходится не более 4-6 %, а спорадического КРР — 94-96 % [1].
Наследственный неполипозный КРР (Hereditary Nonpolyposis Colorectal Cancer — HNPCC) составляет около 2-3 % всех случаев КРР, происходит вследствие мутации в одном из нескольких генов, участвующих в репарации ДНК, а это в 50 % случаев обусловливает риск развития КРР. HNPCC-синдрому присуще существование фенокопий, т. е. наличие нескольких генов (hMLH1, hMSH2, hMSH3, hMSH6, hPMS2), мутация в которых вызывает идентичные фенотипические отклонения наследственного неполипозного рака ТК. Все перечисленные гены отвечают за репарацию непарных оснований ДНК (mismatch repair). Их инактивация характеризуется картиной так называемой «микросателлитной нестабильности» (MSI — microsatellite instability) [1].
Семейный аденоматозный полипоз (FAP — familial adenomatous polyposis) — аутосомно-доминантное заболевание со 100 % риском возникновения КРР. Он проявляется возникновением сотен полипов ТК, некоторые из которых неминуемо трансформируются в злокачественную опухоль. У 5 % больных озлокачествление полипов происходит уже к 20-летнему возрасту. Встречаемость FAP в популяции составляет приблизительно 1 на 8 тыс. FAP-синдром чаще всего связан с инактивирующей мутацией в гене опухолевой супрессии АРС (adenomatous polyposis coli), хотя сходные по клиничecкoй картине проявления могут вызываться повреждением и других генов, в частности гена MYH — MUTY-гомолога. FAP-синдром составляет менее 1 % всех случаев КРР [1].
Что касается спорадического КРР, выделяют два основных пути развития рака. Один из них «канонический», или супрессорный, путь, который сопровождается хромосомной нестабильностью (CIN — chromosomal instability). Супрессорный путь присутствует в 80-85 % случаев колоректальных карцином. В данном случае развитию карциномы предшествует аденома. Патогенез КРР включает как активацию онкогенов, так и инактивацию супрессорных генов. Данный вариант характеризуется потерей аллельных локусов в хромосомах 5q (APC), 17p (p53) и 18q (DCC/SMAD4) и мутацией в гене KRAS.
В “классической” модели прогрессии колоректального рака исходным событием является инактивация гена АРС (ген аденоматозного полипоза толстой кишки), который в норме является опухолевым супрессором. Молекулярно-генетические исследования выявили делецию в длинном плече 5-й хромосомы, затрагивающую ген APC, как в опухолевых, так и в нормальных клетках. Полагают, что эта делеция приводит к потере генов-супрессоров опухолевого роста, а, следовательно, и кодируемых ими белков, которые в норме подавляют рост опухоли. Ген APC контролирует специфическое сцепление клеток эпителия кишечника, нарушение которого необходимо для возникновения полипа, но недостаточно для возникновения клона раковой опухоли. APC содействует деградации β‑катенина, что ограничивает транскрипцию генов, участвующих в регуляции клеточного цикла. Этот путь является неотъемлемой частью патогенеза рака толстой кишки [4].
KRAS — представитель белков семейства Ras, которые кодируют малые G-белки (малые ГТФазы). Белки семейства Ras являются мембраносвязанными и участвуют в передаче сигнала. В норме белки семейства Ras существуют в неактивной форме. Они активируются, когда находящийся рядом трансмембранный рецептор (например, EGRF, Toll-рецептор, G-белок) связывается с соответствующим лигандом. Дальнейший внутриклеточный сигнальный каскад включает в себя переход ГДФ в ГТФ. После активации RAS происходит поток активации широкого круга эффекторов, включая серин/треонин киназы, ГТФ-активирующий белков (GAPs), фосфоинозитид 3-киназы (PI3K), и GEFs. Ras отключаются, когда молекула ГТФ обратно преобразуется в молекулу ГДФ. В случае мутации, они остаются в состоянии ГТФ. Ошибки в регуляции KRAS могут привести к росту опухоли и метастазированию [5]. Таким образом, в опухолях с мутированным типом гена KRAS белок постоянно находится во «включенном» состоянии даже без активации восходящим сигналом от EGFR. В результате продолжается стимуляция находящихся ниже по сигнальной цепи эффектов, ведущих к росту и распространению опухоли.
В опухолях выявляют разные типы гена KRAS, которые кодируют “нормальный”, не мутированный белок KRAS (дикий тип), или патологический мутантный KRAS. «Статус» KRAS (дикий или мутантный тип) может указывать на прогноз заболевания и позволяет предсказать ответ опухоли на некоторые препараты [6]. Мутации в кодоне 12 фиксируются у 27.7 % больных, в кодоне 13 — у 6.6 %. Реже встречаются мутации в 61, 117, 146 и других кодонах. Самое распространённое изменение в 12 кодоне — замена глицина на аспартат и глицина на валин. Замена глицина на валин отрицательно влияет на патогенез, течение КРР и общую структуру выживаемости пациентов. Помимо вышесказанного, мутации KRAS связаны с более быстрым и агрессивным развитием метастазов в печень. Было доказано, что эти мутации вместе с высокой экспрессией маркера клеточной пролиферации Ki-67 ассоциированы с множественными метастазами печени, лёгких, более короткими интервалами их обнаружения и плохой выживаемостью больных после резекции ободочной кишки.
BRAF представляет собой RAS-регулируемую серин/треонин киназу, которая наряду с KRAS является еще одним участником сигнального пути, контролирующего клеточную пролиферацию, дифференцировку и апоптоз [5]. Мутации в гене BRAF часто обнаруживаются в злокачественных опухолях человека, таких как метастатический колоректальный рак, немелкоклеточный рак легких, меланомы и папиллярный рак щитовидной железы.
Малигнизация полипа связана с делецией генов в ножке хромосомы 18q, в частности SMAD2 и SMAD4. Каждый рецептор взаимодействует со своим собственным членом семейства ростовых факторов TGFбета. И таким образом внутри клетки возникает специфический для данного ростового фактора отклик. Разные SMAD после активации связываются и образуют гетеродимерные комплексы с одной и той же медиаторной молекулой, известной как SMAD4.Белок SMAD4 принадлежит к супрессорам опухолеобразования. Этот комплекс транслоцируется в ядро, где он прямо или в комплексе с другими компонентами аппарата транскрипции регулирует (активирует или репрессирует) экспрессию определенных генов.
Ген p53 является одним из ключевых генов-супрессоров опухолевого роста, функция которого направлена на ограничение вероятности возникновения генетически нестабильных клеток. Белок р53 контролирует состояние генома и устраняет потенциально опасные в плане злокачественной трансформации клетки [4].
Таким образом, канцерогенез в толстой кишке представляет собой последовательную цепь генетических изменений, включающих активацию нескольких онкогенов и потерю двух или более опухолевых супрессорных генов. Эти процессы отражаются в морфологически распознаваемых стадиях: толстокишечная эпителиальная гиперплазия, эпителиальная дисплазия с формированием аденом различной степени с последующим прогрессивным увеличением и злокачественных трансформаций.
Схему канцерогенеза в толстой кишке можно представить как последовательность «аденома-карцинома»: первоначально инактивируется APC, затем активируется онкоген KRAS, далее происходит потеря генов на 18q (SMAD2 и SMAD4) и в конечном итоге происходит потеря гена Ps34 TGF рецепторов II генов [4].
При выборе тактики лечения пациентов с КРР особое значение имеет ген KRAS [7]. Помимо хирургического лечения, пациентам обычно назначается химиотерапия или радиотерапия в сочетании с таргетными препаратами. Наиболее перспективными мишенями представляются рецепторы ростовых факторов — эпидермального фактора роста (EGFR). Моноклональные антитела специфически нацелены и связываются с EGFR. В случае мутации KRAS, имеющей место у приблизительно 40 % больных колоректальным раком (КРР), этот ген способен самостоятельно продуцировать активирующие ростовые сигналы, и мутированный КRAS находится в состоянии постоянной активации вне зависимости от статуса EGFR. Блокада EGFR в этой ситуации неэффективна. Таргетная терапия антиEGFR также неэффективна при лечении опухоли с мутантным BRAF [8].
Таким образом, в настоящее время накоплено достаточно знаний о генетических изменениях, сопровождающих КРР. Однако исследования в этом направлении продолжаются. Конечная цель данных исследований — разработка новых методов профилактики и лечения КРР, направленных на замещение или подавление мутированных генов.
Основные термины (генерируются автоматически): KRAS, APC, EGFR, ген, BRAF, толстая кишка, FAP, мутация, опухолевый рост, злокачественная опухоль.
Лимфоидная ткань кишечника как основа иммунной системы пищеварительного тракта
Желудочно-кишечный тракт — высокоспециализированный орган, которой участвует в поглощении переработки и усвоении питательных веществ. Кроме этого он выполняет другие не менее важные функции. Кишечник — важный орган иммунной системы: он постоянно контактирует с большим количеством веществ и агентов внешней среды, а также факторов, влияющих на жизнедеятельность всего организма. В статье представлена характеристика составных частей иммунной системы пищеварительного тракта и их роль в формировании иммунного ответа организма на антигенное воздействие.
Ключевые слова: антигены, иммуноглобулины, иммунокомпетентные клетки, иммунный ответ, лимфоидная ткань, пищеварительный тракт
Воздействие антигенов внешней среды является ключевым фактором в развитии защитных реакций против различных патогенных микроорганизмов и многих органических и неорганических веществ, в том числе канцерогенов [7].
Кишечник является основной зоной, где происходит сенсибилизация иммуноцитов, которые затем заселяют другие слизистые оболочки и служат отправной точкой для циркуляции клеток между различными органами. Иммунокомпетентные ткани пищеварительного тракта получили название лимфоидной ткани. Этой ткани принадлежит важная роль защите организма от антигенов. Следует заметить, что к механизмам защиты принадлежат так же секреция слизи и перистальтика кишечника.
Лимфоидная ткань в стенке пищеварительного тракта существует в четырех анатомических зонах: 1) лимфоциты, расположенные базально, между эпителиальными клетками слизистой оболочки — интраэпителиальные лимфоциты; 2) лимфоциты, расположенные в соединительной ткани собственного слоя слизистой оболочки-лимфоциты собственного слоя; 3) специфические скопления лимфоидных клеток в слизистой оболочке тонкой кишки в частности в тощей кишке — пейеровы бляшки; 4) солитарные лимфоидные фолликулы слизистой оболочки [1, 5].
Важными составными частями иммунной системы пищеварительного тракта являются слюнные железы, лимфоидная ткань глотки, региональные лимфатические узлы и ретикуло-эндотелиальная ткань печени.
Интраэпителиальные лимфоциты локализуются базально между эпителиальными клетками слизистой оболочки, в особенности в тех местах, которые соприкасаются с внешней средой. Количество лимфоцитов данного типа в среднем составляет 21 на 100 эпителиальных клеток. Эти лимфоциты различны по своей форме и размерам, а также по содержанию гранул в цитоплазме. Они могут мигрировать в обоих направлениях через базальную мембрану. Гранулы интраэпителиальных лимфоцитов и тучных клеток сходны по своему строению и химическому составу, поэтому высказывается некое предположение эти лимфоциты это Т-лимфоциты, которые особым образом связаны с тучными клетками слизистой оболочки кишечника. Среди интраэпителиальных лимфоцитов выделены Т- и В-лимфоциты, но их точное подразделение на группы до сих пор неизвестно [1].
Лимфоциты собственного слоя хоть и изучались многими специалистами более интенсивно, чем интраэпителиальные лимфоциты, но данные о них весьма разрозненные и содержат много противоречий. Установлено что в слизистой оболочке тонкого кишечника человека их содержится до 11000 на мм. Среди лимфоцитов преобладают В-клетки, их численность более 50 %, содержащие поверхностный IgA. Оставшаяся часть В-лимфоцитов представлена клетками с поверхностными IgM и IgG. Т-лимфоциты тоже присутствуют, но об их подклассах практически ничего неизвестно, кроме того что они продуцируют антитела и могут проникать в слизистую кишки находящуюся в непосредственном контакте с бляшками [3].
Важнейшее свойство кишечника — феномен рециркуляции лимфоцитов. Сенсибилизированные антигенами (как пищевыми, так и инфекционными) лимфоциты пейеровых бляшек мигрируют в брыжеечные лимфатические узлы, а оттуда по лимфатическим сосудам через грудной проток и систему кровообращения направляются к собственному слою слизистой оболочки кишечника, главным образом в качестве клеток, секретирующих IgA. Этот механизм обеспечивает формирование клонов лимфоцитов и образование специфических антител в участках слизистой оболочки, отдаленных от очага первичной сенсибилизации. В процессе сенсибилизации плазматических клеток с последующим клонированием лимфоцитов, вырабатывающих антитела с определенными свойствами (аналогичными тем, которые выступили матрицей), участвуют не только нативные молекулы иммуноглобулинов.
Попавшие в просвет кишечника или на слизистые оболочки антигены распознаются иммуноглобулинами памяти (IgG), после чего информация передается в иммунокомпетентные клетки слизистой оболочки, где из сенсибилизированных лимфоцитов клонируются плазматическими клетками, ответственными за синтез IgА и IgМ. В результате защитной деятельности этих иммуноглобулинов включаются механизмы иммунореактивности или иммунотолерантности. Иммунная система «запоминает» антигены, чему способствуют генетические факторы, а также антитела класса IgG, передающиеся, например, от матери плоду во время беременности, и иммуноглобулины, поступающие в ЖКТ ребенка с грудным молоком. В результате рециркуляции лимфоцитов и клонирования иммунный ответ охватывает все слизистые ЖКТ [3, 4].
Главная функция кишечных иммуноглобулинов (Ig) — иммунное отторжение у поверхности слизистой оболочки. Известно, что IgA преобладает среди иммуноглобулинов во всех секретах и в собственной пластинке кишечника. Секреторный IgA, выполняющий роль главного уничтожителя антигенов и иммуномодулятора слизистой оболочки ЖКТ, удерживается около эпителиальных клеток в результате взаимодействия с гликокаликсом, во многом благодаря присутствию микрофлоры кишечника. IgA занимает благоприятную позицию, препятствующую поглощению антигенов. Двумерная молекула IgA может функционировать как агглютинин, уменьшая прилипание бактерий к энтероцитам.
Особое значение в иммунологических функциях желудочно-кишечного тракта придается тонкой кишке, в которой организованная лимфоидная ткань представлена сгруппированными лимфатическими узелками, аппендиксом и лимфатическими узлами брижейки. Эти органы включают зону с фолликулярными структурами, содержащую в основном В-лимфоциты и интрафолликулярную (паракортикальную) зону, состоящую в основном из Т-лимфоцитов, расположенных вокруг высокоэндотелиальных венул. Эпителиальные структуры сгруппированных лимфатических узелков специализированы на поглощении антигенов макрофагами [2].
Пейеровы бляшки это структурно организованные и оформленные скопления лимфоидных клеток в подслизистом слое тонкой кишки. Так у человека они появляются по ходу всей тонкой кишки уже на 24-й недели внутриутробного развития. Пейеровы бляшки окружены М-клетками, которые лишены ворсинок и ответственны за транспортные и частично метаболические процессы. К ним относят способность транспортировать макромолекулы и частицы из просвета кишки в лимфоциты пейеровых бляшек. Бляшки плохо развиты у животных, выращиваемых в стерильных условиях. В пейеровых бляшках содержится до 40 % Т-лимфоцитов, которые располагаются в межфолликулярном пространстве [5, 6].
Наибольшая концентрация пейеровых бляшек отмечена в аппендиксе — червеобразном отростке слепой кишки. Известно, что он имеется далеко не у всех животных, например, его нет у кошек, но он присутствует у человека, обезьян, кроликов и ряда жвачных животных. Главная функция этого органа — это защита кишечника и его микрофлоры от патогенных агентов. Аппендикс выполняет так же ряд второстепенных функций: синтетическую (продуцирует амилазу и липазу) и гормональную (производит гормоны, участвующие в сокращении сфинктеров кишечника и регулирующие его перистальтику) [2, 4].
Солитарные лимфоидные фолликулы содержатся в слизистой оболочке и подслизистой основе кишечника. Но в отличие от пейеровых бляшек не имеют тесной связи с эпителием. Этот вид лимфатических образовании содержит Т-клетки, В-клетки, а также макрофаги. Сенсибилизированные лимфоциты в дальнейшем мигрируют в брыжеечные лимфатические узлы, а оттуда в грудной проток и систему кровоснабжения к собственному слою кишечника.
Важную роль играет система иммуногенеза в деятельности толстой кишки, непосредственно соприкасающейся с различными бактериальными антигенами. В ней содержится большое количество клеток, несущих Ig. Клетки, несущие IgА и IgМ, располагаются преимущественно в поверхностном эпителии, а несущие IgG — в базальных отделах слизистой оболочки толстой кишки. В собственной пластинке слизистой оболочки выявляют в основном IgG-секретирующие клетки [2].
Слизистая оболочка здорового млекопитающего не может полностью заблокировать проникновение антигенов из полости кишечника в его стенку, а затем в циркулирующую кровь. Например, ботулинистический токсин, попав в кишечник, не задерживается в просвете кишки, а проходит через кишечную стенку в интерстинальную лимфу. Предполагают, что такой обходной путь миграции антигенов в обход системы IgA может быть неким приспособлением кишечника к защите от антигенов либо проявлением сложной многоступенчатой стратегии защиты кишечника от антигенов [4].
Таким образом, на всем протяжении кишечника лимфатические ткани и их элементы представлены весьма широко. Они разнообразны строению и функциям. Клеточный иммунитет кишечника в отличие от системы секретируемых им антител изучен недостаточно. Известно, что после перорального воздействия антигенов системные клеточные иммунные реакции выявляются редко. Возможно, когда здоровый организм получают безвредные антигены (например, антигены нормальной микрофлоры), в слизистой оболочке кишечника не развиваются реакции клеточного иммунитета. Или если иммунная реакция происходит, то иммунные клетки кишечника не могут сохранять в клетках памяти информацию об антигене. Это свидетельствует о наличии в кишечнике механизмов иммунной памяти, но они, в отличие от системного иммунного ответа, не носят долговременного характера.
- Галактионов В. Г. Эволюционная иммунология: учеб. пособие для вузов. М.: ИКЦ «Академкнига», 2005. 407 с.
- Кузник Б. И. Иммуногенез, гомеостаз и неспецифическая резистентность организма / Б. И. Кузник, Н. В. Васильев, Н. Н. Цыбиков. М.: Медицина, 1989. С. 191-200.
- Ройт А., Бростофф Дж., Мейбл Д. Иммунология. М.: Мир, 2000. 592 с.
- Скопичев В. Г. Физиолого-биохимические основы резистентности животных / В. Г. Скопичев, Н. Н. Максимюк. С.-Петербург: изд-во «Лань», 2009. 352 с.
- Тейлор Д. Биология = Biological Science 1&2: В З т. Т.1 / Под ред. Р. Сопера; Пер.с англ.: Ю. Л. Амченкова и др. 3-е изд. М.: Мир, 2004. 454 с.
- Хаитов Р. М. и др. Иммунология: Учебник для вузов. М.: ГЭОТАР-Медиа, 2011. 311 с.
- Ребезов М. Б., Чупракова А. М., Зинина О. В., Максимюк Н. Н., Абуова А. Б. Оценка методов исследования ксенобиотиков.. Уральск, 2015.
Основные термины (генерируются автоматически): слизистая оболочка, лимфоцит, пищеварительный тракт, антиген, иммунная система, клетка, тонкая кишка, бляшка, внешняя среда, главная функция.
Влияние содержимого кишечника на гены эпителиальных клеток кишечника
ОГБУЗ «Смоленcкий областной институт патологии», Смоленск, Россия
ОГБУЗ «Смоленcкий областной институт патологии», Смоленск, Россия;
Кафедра патологической анатомии Смоленского государственного медицинского университета Минздрава России, Смоленск, Россия
Гипоэстрогенемия, вызванная нарушением кишечной микробиоты, как возможный фактор риска малигнизации эндометриоидной гетеротопии
Журнал: Архив патологии. 2020;82(2): 57‑61
В работе раскрываются патогенетические особенности влияния нарушения микробиоты кишечника на развитие заболеваний женской репродуктивной системы. Появление динамического дисбаланса между измененной микробиотой и макроорганизмом имеют множество проявлений в виде нарушений гормонального гомеостаза, одно из которых дисбиозиндуцированная гипоэстрогенемия. На примере эндометриоидной гетеротопии прослеживается возможность ее прогрессирования и малигнизации за счет возникновения на фоне гипоэстрогенемии первичной поломки гена-онкосупрессора PTEN с последующими генетическими аномалиями в генах ARID1A и ТР53. Наличие мутации PTEN как при самом эндометриозе, так и при его малигнизации указывает на возможность участия дисбиозиндуцированной гипоэстрогенемии в патогенезе эндометриоза. Таким образом, связь между заболеваниями женской репродуктивной системы и нарушением кишечного микробиома может быть более значительной, а возможность коррекции кишечной микробиоты при помощи пре- и пробиотиков открывает новые горизонты не только для профилактики, но и лечения многих гинекологических заболеваний, связанных с нарушением гормонального статуса.
Симбиоз микробиоты с макроорганизмом, а также последствия нарушений их отношений — предмет обсуждения и исследования, необходимый для понимания регуляции структурных основ гомеостаза. Проблема дисбиоза также мало изучена, а некоторые исследователи и вовсе отрицают клиническое значение этого понятия [1]. В настоящее время многие аспекты влияния кишечной микрофлоры на человеческий организм неизвестны. Этиологическая, патогенетическая и морфофункциональная роль микробиоты в становлении и развитии отдельных заболеваний проблематична, несмотря на пристальный интерес ученых к данному направлению [2—4]. В нашей работе обобщаются результаты исследований, показывающие участие кишечной микробиоты в контроле гормонального фона путем метаболизма эстрогенов и перевода их в активные формы. Нарушение этой функции при нарушении кишечного микробиома приводит к развитию гипоэстрогенемии, роль которой рассмотрена в рамках патогенеза заболеваний женской репродуктивной системы, а именно эндометриоза и риска малигнизации эндометриоидных гетеротопий, так как распространенность и социальная значимость этих патологий в популяции велика [5]. Цель работы — уточнить возможную роль кишечной микрофлоры в малигнизации очагов эндометриоза.
Влияние кишечной микробиоты на гормональный фон женщины
С увеличением объема знаний о кишечной микробиоте и ее влиянии на человеческий организм все больше фактов говорят в пользу того, что нарушение ее сбалансированной работы может быть фоном или даже непосредственным этиологическим фактором развития многих заболеваний, будь то метаболические нарушения или же активация опухолевого роста [6]. Некоторые исследователи связывают проблему дисбиоза даже с риском невынашивания беременности [7]. Одной из наиболее важных функций кишечного микробиоценоза, влияющей на гомеостаз макроорганизма, является поддержание уровня гормонов, в том числе эстрогена и его производных в сыворотке крови на физиологическом уровне [8]. Каким же образом это происходит?
На сегодняшний день известно, что микробиота кишечника, находящаяся в динамическом балансе с организмом женщины, косвенно отражает генетическую индивидуальность ее организма, а также особенности ее образа жизни [8]. Состав кишечного микробиома имеет и гендерные различия, становление которых наблюдается одновременно с половым созреванием, что указывает на связь бактерий с гормональным фоном [9]. Одни виды микроорганизмов способны лишь только реагировать на гормоны хозяина, тогда как другие самостоятельно секретируют их и оказывают тем самым не только местное, но и системное действие на макроорганизм [10]. Показано, что кишечная микробиота обладает особой ферментативной активностью, принимающей участие в метаболизме эстрогена [8] (например, фермент β-глюкуронидаза [11]), за счет которой возможно преобразование полициклических ароматических углеводородов [12] и поступающих с пищей фитоэстрогенов [13] в активные метаболиты эстрогена, тем самым регулирует уровень эстрогена вместе с эндокринной системой. Однако и сам макроорганизм активно способствует созданию оптимальных условий для существования кишечных комменсалов путем синтеза необходимых гормонов [8]. Интересно, что кишечник является органом-мишенью для эстрогена, который опосредованно через рецептор ER-β способствует повышению микробного разнообразия, с чем исследователи связывают снижение риска формирования хронического воспаления в толстой кишке и последующего возникновения колоректального рака [14]. Также показано влияние микрофлоры кишечника непосредственно на органы, продуцирующие гормоны. В 2019 г. опубликовано исследование, целью которого было определить возможность влияния кишечной микробиоты на женскую репродуктивную систему, используя в качестве модели крыс с дигидротестостерон (DHT)-индуцированным синдромом поликистозных яичников (СПКЯ). При помощи пробиотиков исследователи пытались создать наиболее подходящие условия для жизнедеятельности нормального кишечного микробиоценоза и получили неожиданные результаты. У крыс с СПКЯ на фоне данной терапии последовало заметное улучшение репродуктивной функции, что доказывает опосредованное влияние кишечной микробиоты на яичники, а также тот факт, что нарушение состава кишечной микрофлоры может быть одним из индукторов развития многих заболеваний женской репродуктивной системы [15]. Интересно, что в более ранних работах уже предлагалось использование пре- и пробиотиков в качестве лечения заболеваний, связанных с менопаузой, что подчеркивает связь кишечных микроорганизмов и гормонального фона женщин [9].
Таким образом, стоит задуматься над важным на сегодняшний день вопросом: имеются ли патогенетические связи между дисбиозом и заболеваниями женской репродуктивной системы?
Дисбиозиндуцированная гипоэстрогенемия и ее связь с канцерогенезом
Известно, что снижение микробного многообразия при дисбиозе неотвратимо ведет к изменению метагенома кишечной микрофлоры, что, в свою очередь, может негативно сказаться на макроорганизме [16]. Так, в некоторых работах, посвященных раку молочной железы, исследователи отмечают явное отличие состава кишечной микробиоты в качественном и количественном отношении у здоровых женщин и пациенток, страдающих раком молочной железы [8, 16]. Замечено, что при дисбиозе вследствие потери части микробных популяций, участвующих в метаболизме стероидных гормонов, снижается уровень эстрогена в крови, с чем многие исследователи связывают повышение риска возникновения таких процессов, как ожирение, гиперплазия эндометрия, СПКЯ, а также опухолевый рост [11]. Опираясь на подобные результаты, можно сделать вывод о существовании дисбиозиндуцированной гипоэстрогенемии и рассматривать ее не только в качестве возможного проявления нарушений кишечной микрофлоры, но и фона для других патологий. Проявления гипоэстрогенемии в первую очередь характерны для менопаузы, когда уровень эстрогена снижается ввиду структурно-физиологического истощения яичников. Гипоэстрогенемия наблюдается и как следствие тотальной овариоэктомии. Стоит заметить, что клинические, гормональные и биохимические нарушения у женщин с физиологической гипоэстрогенемией в период менопаузы аналогичны таковым у молодых женщин с нефизиологической гипоэстрогенемией (например, при центральном гипогонадизме) [17]. Таким образом, дисбиозиндуцированная гипоэстрогенемия, наиболее вероятно, будет иметь те же последствия для организма, но менее выраженные в сравнении с вышеописанными состояниями.
Несмотря на общепризнанную значимость гиперэстрогенемии в канцерогенезе опухолей женской репродуктивной системы, вопрос о ее роли в этом процессе до сих пор остается недостаточно изученным. Принимая во внимание возможность малигнизации эндометриоидной гетеротомии, большинство данных говорит об эстрогене как о триггере малигнизации этой патологии [18]. И действительно, из всех возможных локализаций эндометриоидных гетеротопий в 80% случаев подвергается озлокачествлению именно эндометриоз яичников — органов, синтезирующих эстрогены [19]. Однако стоит заметить, что малигнизация эндометриоидных гетеротопий других локализаций достаточно часто возникает после тотальной овариоэктомии. В литературе описано большое количество клинических случаев, где малигнизация наступала при локализации гетеротопии на брюшине [20], сигмовидной кишке [21], послеоперационном рубце [22]. Все эти случаи объединяет то, что в анамнезе у таких пациенток была операция по удалению матки и придатков, что явно приводит к гипоэстрогенемии.
Таким образом, затрагивается еще один важный вопрос: может ли гипоэстрогенемия, в том числе и обусловленная дисбиозом, запустить малигнизацию в эндометриоидной гетеротопии?
Зависимость дефекта гена-супрессора опухолей PTEN от эстрогена
При малигнизации эндометриоидных гетеротопий был обнаружен целый ряд генетических изменений. Работы многих исследователей показали, что в первую очередь для этой злокачественной опухоли характерно нарушение функционирования гена-супрессора PTEN вследствие его потери в результате делеции [23] либо мутации [24]. Задачей данного гена является подавление опухолевого роста за счет синтеза антионкобелка PTEN (phosphatase and tensin homolog deleted on chromosome 10) — фосфатазы с двойной субстратной специфичностью, которая является одним из регуляторов сигнального пути PI3K/AKT/mTOR. Этот механизм участвует в контроле клеточной пролиферации и инвазии опухолевых клеток [25]. Мутация гена PTEN является частой находкой при эндометриозе, а также при эндометриоз-ассоциированном раке [26] и, по мнению некоторых авторов, является первичной, запуская другие генетические изменения [27], что представляется одним из первых проявлений малигнизации эндометриоидной гетеротопии [28].
Учитывая данные, описанные выше, стоит предположить, что PTEN находится под контролем со стороны эстрогена, и нарушения в его работе становятся следствием гормонального сбоя. И действительно, эстроген способен влиять на экспрессию данного гена-супрессора опосредованно с помощью микро-РНКmiR-200c [29], а также через сигнальный путь GPR30 с последующей активацией малатдегидрогеназы-2 (MDH2) [30]. Из этого следует, что поломка PTEN в ткани эндометрия возникает на фоне гиперэстрогенемии, что и описывают M. Scully и соавт. [31]. Однако результаты исследований в данной области оказались неоднозначными. Было замечено, что малигнизация эндометриоидных гетеротопий возникает именно на фоне гипоэстрогенемии, а в 2011 г. F. Saito и соавт. [32] показали в эксперименте, что эстроген провоцирует пролиферацию эпителиальных клеток эндометрия, а снижение уровня эстрогена провоцирует именно пролиферацию PTEN-null cells с эстрогеннезависимыми способностями, вызывая рост аномальных желез с последующим развитием неоплазии, что объясняет повышение частоты встречаемости рака эндометрия в пери- и постменопаузальном периоде. Аналогичные результаты в 2012 г. опубликованы и другими исследователями [33]. Таким образом, была показана возможность активации и прогрессии канцерогенеза в ткани эндометрия в отсутствие влияния со стороны эстрогена, что подтверждает множество клинических наблюдений малигнизации эндометриоидных гетеротопий в период менопаузы и дает право на существование гипотезы о роли гипоэстрогенемии различного генеза в малигнизации эндометриоидных гетеротопий, в том числе дисбиозиндуцированной.
Вторичные генетические нарушения, обусловливающие малигнизацию эндометриоидной гетеротопии
Первичная мутация PTEN как гена-онкосупрессора неизбежно влечет за собой и другие генетические нарушения, обусловливающие прогрессию опухолевого роста. Так, мутация гена ARID1A наблюдается как при эндометриозе, так и при эндометриоз-ассоциированных опухолях, что сопровождается снижением синтеза соответствующего белка [23]. Белок ARID1A регулирует транскрипцию некоторых генов путем изменения структуры хроматина вокруг них, что может способствовать нарушению регуляции экспрессии генов [34], а следовательно, и прогрессированию малигнизации эндометриоидной гетеротопии. Выяснено, что потеря белка ARID1A приводит к нарушению работы транскрипционно-регуляторных комплексов SWI/SNF, что часто встречается при эндометриозе и эндометриоз-ассоциированных опухолях [35]. Потеря контроля над опухолевым ростом со стороны генов PTEN и ARID1A, по мнению исследователей, связана с изменением соотношения рецепторов к эстрогену (ER-α/ER-β) в клетках эндометриоидной гетеротопии [36], что снова подтверждает зависимость данного процесса от стероидных гормонов.
Одновременно с мутациями генов PTEN и ARID1A достаточно часто обнаруживается и генетическая поломка со стороны антионкогена ТР53, что расценивается как более поздняя генетическая поломка, возникающая после мутации PTEN в очагах эндометриоидных гетеротопий [27], и также является наиболее часто встречающейся при малигнизации такой патологии [26]. Продукт гена ТР53 белок р53 известен под именем «страж генома». В его задачу входят своевременная остановка клеточного цикла и репарации ДНК в потенциально опасных в отношении озлокачествления клетках, а также запуск программы их апоптоза [37]. Интересно, что мутации белка р53 встречаются при эндометриозе без злокачественной трансформации, что в совокупности с известными для этой патологии такими свойствами, как способность избегать апоптоз, высокая пролиферативная активность, способность к инвазивному росту и выраженный ангиогенный потенциал, делают ее весьма схожей со злокачественными новообразованиями [38].
Итак, изучая механизмы малигнизации эндометриоидных очагов, многие исследователи обращают внимание именно на совокупность генетических повреждений со стороны антионкогенов PTEN, ARID1A и ТР53. Эти мутации присутствуют поодиночке и с менее выраженной экспрессией в эндометриоидных гетеротопиях с доброкачественным течением, но наблюдаются в полном составе с более активной экспрессией при малигнизации данной патологии [18, 27, 39]. Показано, что эндометриоз и ассоциированный с ним рак изначально генетически связаны [40], а запуск первичной генетической поломки PTEN возникает задолго до менопаузы, когда физиологическая гипоэстрогенемия еще не наступила. Таким образом, можно предположить этиопатогенетическую значимость дисбиоз-ассоциированной гипоэстрогенемии не только для малигнизации эндометриоидной гетеротопии, но и возможную ее роль в возникновении этой патологии еще до озлокачествления.
Заключение
Исходя из проанализированных данных литературы, можно с уверенностью говорить о наличии патогенетической связи между нарушением кишечного микробиома и заболеваниями женской репродуктивной системы за счет нарушения динамического баланса между измененной микробиотой и макроорганизмом, одним из проявлений которого является нарушение гормонального гомеостаза в виде гипоэстрогенемии. Основываясь на результатах ряда оригинальных исследований, мы проследили возможность прогрессирования канцерогенеза в ткани эндометриоидных гетеротопий на фоне отсутствия контроля последней со стороны эстрогена, а именно первичной поломки гена-онкосупрессора PTEN с последующими генетическими аномалиями в генах ARID1A и ТР53. Схожесть поломки PTEN как при доброкачественно протекающем эндометриозе, так и при малигнизации его очага указывает на возможность участия дисбиоз-индуцированной гипоэстрогенемии в патогенезе эндометриоза. Таким образом, возможность влияния на женскую репродуктивную систему опосредованно через кишечную микрофлору при помощи пре- и пробиотиков открывает новые горизонты как в профилактике, так и в лечении многих гинекологических заболеваний.
Авторы заявляют об отсутствии конфликта интересов.
The authors declare no conflicts of interest.
Сведения об авторах
Как нарушение кишечного барьера влияет на биологию микроглии
С течением времени открываются все новые функции микробиома в организме человека и его роль в патогенезе болезней. В новых исследованиях выводится связь функционирования микробиома с процессом старения. Моссад с соавт. демонстрируют, что связанное со старением нарушение целостности тканевого барьера в кишечнике, опосредованное микробиомом, может способствовать дисфункции микроглии у мышей.
По мере увеличения продолжительности жизни человека возрастные заболевания становятся все большим бременем для общества и экономики по всему миру. Тем не менее, многие особенности процесса старения остаются плохо изученными. В их число входит и то, как на него воздействуют факторы окружающей среды и образ жизни. В последнее время исследования влияния кишечных бактерий на здоровье человека и их роль в патогенезе различных заболеваний стали предметом особого интереса. В нескольких фундаментальных исследованиях была показана роль микробиома в развитии возрастных заболеваний, таких как болезнь Альцгеймера и болезнь Паркинсона [1, 2], а также выявлены некоторые клеточные и молекулярные признаки старения и снижения когнитивных функций [3, 4]. Однако остается неясной взаимосвязь между состоянием кишечника и микроглии.
В новом исследовании, проведенном Моссадом с соавт. [5] и опубликованном в Nature Neuroscience, демонстрируется, что опосредованные микробиомом изменения проницаемости кишечника во время старения могут способствовать перемещению промежуточных продуктов обмена веществ из кишечника, в кровоток и, возможно, в мозг. Эти метаболиты, в свою очередь, могут изменять функцию микроглии и нарушать ее гомеостаз в сторону патогенеза [5] (рис. 1). В частности, чтобы изучить влияние микробиома на дисфункцию микроглии при старении, Моссад с соавт. [5] исследовали экспрессию генов клетками микроглии у молодых (6-10 недель) и старых (96-104 недель) мышей. Животные пребывали в стерильных (GF, от англ. germ-free) или же свободных от специфической патогенной микрофлоры (SPF, от англ. specific-pathogen-free) условиях содержания. В процессе сравнения экспрессии генов у мышей из группы GF (т. е. тех, у которых отсутствовал микробиом) с мышами группы SPF авторы предположили, что наблюдаемые различия в функции микроглии обусловлены биологией кишечных бактерий, хотя использованный в исследовании подход не предполагает какое-либо влияние отдельных микроорганизмов. Авторы сообщают, что в клетках микроглии мышей обеих групп (и GF, и SPF) выявлена зависимая от возраста транскриптомная сигнатура, определенная с помощью секвенирования РНК. Однако степень различий в экспрессии генов, связанных со старением, оказалась более выраженной в микроглии мышей группы SPF по сравнению с животными из группы GF. Примечательно, при сравнении старых мышей обеих групп самые большие различия были обнаружены в экспрессии тех генов, которые вовлечены в организацию цитоскелета, реализацию иммунных функций и регуляцию работы митохондрий. Митохондрии — крайне важные клеточные органеллы, ответственные за в процесс выработки энергии, которые участвуют в старении клеток благодаря модуляции выработки активных форм кислорода (АФК) и реакций на окислительный стресс. Удивительные изменения в экспрессии генов, связанных с функциями митохондрий, побудили авторов исследовать воздействие микробиома на эти органеллы.
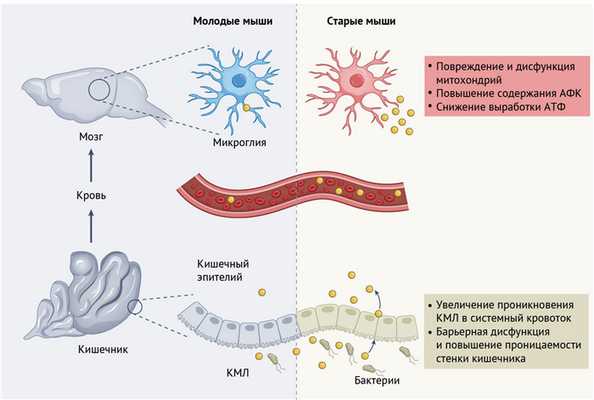
Увеличение кишечной проницаемости с возрастом усиливает проникновение кишечных метаболитов в системный кровоток и накопление их в тканях, что способствует нарушению функции микроглии. Повышенная проницаемость кишечного барьера, опосредованная микробиомом кишечника и связанная со старением, приводит к увеличению проникновения метаболитов (например, N(6)-карбоксиметиллизина (КМЛ)) в кровоток и головной мозг. КМЛ накапливается в головном мозге и может повреждать митохондрии, что выражается в дисфункции микроглии (при старении мышей; верхняя правая часть рисунка).
В ходе пристального изучения генов, участвующих в выработке АФК, повышенная экспрессия таких генов, а также генов, задействованных в ответе на накопление кислородных радикалов, была обнаружена только в клетках микроглии у старых мышей группы SPF. Это указывает на то, что содержание АФК в микроглии зависит и от процесса старения, и от присутствия микробиоты. Действительно, при старении мышей группы SPF концентрация АФК в микроглии повышалась по сравнению с более низкими аналогичными значениями у мышей группы GF. Помимо этого, в микроглии старых мышей из группы SPF авторы обнаружили признаки повреждения и дисфункции митохондрий (в них была снижена выработка АТФ), что указывает на то, что обильная микробиота влияет на функцию микроглии у старых мышей. Хотя сравнение с мышами, лишенными кишечных бактерий, приводит к бинарным результатам, которые нельзя назвать естественными (т. е. в природе не существует животных или людей со стерильным кишечником), данный метод формирует базу для дальнейшего изучения влияния микроорганизмов в кишечнике на функцию митохондрий микроглии.
Кишечные микроорганизмы используют множество биосинтетических путей для преобразования и расщепления пищевых соединений до малых и крупных молекул, которые могут влиять на функции макроорганизма. В число последних входят короткоцепочечные жирные кислоты (КЦЖК), которые модулируют энергетический обмен в эпителиоцитах кишечника и играют роль в регуляции функционирования иммунной системы [6]. Эти молекулы могут попадать в кровоток и достигать тканей головного мозга. Согласно исследованиям, микробиом и метаболиты, связанные с его жизнедеятельностью (такие как КЦЖК), могут влиять на течение болезней Альцгеймера или Паркинсона (что было продемонстрировано на мышиных моделях) [1, 2, 7]. Моссад с соавт. [5] применили методики таргетной и нетаргетной метаболомики для изучения ряда метаболитов в сыворотке крови и мозге, содержание которых изменялось с возрастом. Метаболизм нескольких соединений как в сыворотке, так и в ткани мозга у старых мышей был в значительной степени усилен. В число этих веществ входят ацетат, пропионат, пальмитолеат (16:1n7), N-оксид триметиламина (ТМАО), 1-олеоил-2-242 докозагексеноил-ГФХ (18:1/22:6), стахидрин и N(6)-карбоксиметиллизин (КМЛ). С помощью нетаргетной метаболомики образцов крови человека удалось выявить, что с возрастом содержание двух метаболитов (TMAO и КМЛ) возрастает. КЦЖК (ацетат и пропионат) синтезируются микробиотой из пищевых волокон и могут влиять на активацию микроглии в мозге мыши [2]. ТМАО образуется в результате окисления микроорганизмами в кишечнике аминов пищи и последующих ферментативных реакций в печени; в более ранних работах на примере моделей инсульта у грызунов было показано, что данное соединение отрицательно влияет на исход заболевания [8]. КМЛ — представитель молекулярного класса, известного как конечные продукты глубокого гликирования, которые образуются в результате реакций окисления и гликирования белков (например, реакции Майяра). Возникновение конечных продуктов глубокого гликирования связывают с реакцией на стресс, и ранее предполагалось, что эти метаболиты вовлечены в патогенез болезни Альцгеймера [9]. Однако требуются дополнительные исследования, чтобы воспроизвести изначальные наблюдения и выявить потенциальное влияние на функции организма, оказываемое этими метаболитами.
В исследованиях для проверки этой концепции были использованы ацетат, пропионат, ТМАО и КМЛ. В ходе эксперимента путем внутрибрюшинной инъекции у молодых мышей повышали концентрации этих соединений (такой способ введения облегчает распространение вещества по системному кровотоку). Из четырех анализируемых метаболитов только введение КМЛ частично воспроизводило усиление окислительного стресса, снижение функционирования митохондрий и повреждение их структуры, которые наблюдались в микроглии мозга у старых мышей. Это побудило ученых искать причину повышения концентрации КМЛ в головном мозге; изначально была выдвинута соответствующая гипотеза, согласно которой на повышение содержания КМЛ в головном мозге может влиять микробиота. Поразительно, но у мышей из группы GF содержание КМЛ в фекалиях оказалось выше, чем у мышей группы SPF. Это свидетельствует о том, что метаболизм бактерий не является причиной повышения содержания КМЛ.
Кишечный эпителий служит системой защиты между организмом животного и его кишечным микробиомом, и, согласно предыдущим исследованиям, бактерии микробиома также представляют собой ключевые регуляторы кишечной проницаемости (т. е. нарушения функции кишечника как биологического барьера), вследствие чего могут изменяться системные концентрации кишечных метаболитов [10]. Авторы оценивали кишечную проницаемость путем определения перехода молекул с флуоресцентной меткой из кишечника в кровоток после перорального приема. Было обнаружено, что у старых мышей группы SPF повысилась проницаемость кишечника, чего не наблюдалось у старых мышей группы GF. Кроме того, у молодых мышей группы GF, кишечник которых путем фекального переноса от старых мышей был колонизирован микроорганизмами, выявлена более высокая степень утечки флуоресцентного красителя из кишечника по сравнению с молодыми мышами группы GF, кишечник которых был колонизирован микроорганизмами от молодых мышей-доноров. Лучшим объяснением этих наблюдений служат изменения микробиома с возрастом, которые в большей степени влияют на транслокацию КМЛ, чем непосредственно на содержание метаболитов, сопровождающиеся накоплением КМЛ в системном кровотоке и ткани мозга мышей (по крайней мере, такое наблюдалось в настоящем эксперименте). Как старение изменяет влияние микробиоты на проницаемость кишечника, остается неизвестным.
Соответственно, авторы изучили, как способ введения КМЛ влияет на его накопление в микроглии. У молодых мышей группы SPF концентрация КМЛ в микроглии повышалась только после внутрибрюшинной инъекции (по сравнению с пероральным введением, после которого достигались лишь низкие значения). Напротив, у старых мышей группы SPF после системного и перорального введения метаболита наблюдалось усиление накопления КМЛ. Это указывает на то, что повышенная проницаемость кишечника может способствовать облегчению перемещения метаболита из кишечника в мозг. Наконец, чтобы проверить, влияет ли кишечная проницаемость на концентрацию КМЛ в периферическом и системном кровотоке, авторы перорально вводили мышам вещества, которые либо предотвращают накопление КМЛ (эллаговая кислота), либо усиливают барьерную функцию кишечника (кишечная щелочная фосфатаза) [11, 12]. Оба соединения привели к снижению накопления КМЛ в головном мозге. Хотя эллаговая кислота не оказывала влияния на проницаемость кишечника, введение ее снижало накопление КМЛ в головном мозге, что указывает на кишечник как ключевой источник этого метаболита. Повышение барьерной функции кишечника посредством введения кишечной щелочной фосфатазы показало, что путь от кишечника к системному кровотоку, по-видимому, влияет на возрастное накопление КМЛ в головном мозге.
Моссад с соавт. [5] определили важный опосредованный микробиотой процесс в ходе старения, при котором потенциально патогенные молекулы в кишечнике, по-видимому, влияют на клеточные реакции в мозге мышей. Многие аспекты остаются нераскрытыми; например, каким образом КМЛ изменяет функцию микроглии и является ли его воздействие на эти клетки прямым или опосредованным другими клеткам; существуют ли другие метаболиты кишечного происхождения с аналогичными, синергическими или антагонистическими функциями, как микробиота стареющего организма влияет на проницаемость кишечника и можно ли обратить данный процесс вспять (возможно, путем применения фекальных трансплантатов от молодых мышей или пробиотиков). Взаимное влияние стареющего макроорганизма и микробиома может влиять на проницаемость кишечника. Барьерная функция кишечника опосредуется физическими, химическими и клеточными компонентами, такими как кишечный эпителий, иммунокомпетентные клетки, слой слизи и секретируемые молекулы. Нарушение функции любого из этих важных компонентов может привести к повышению проницаемости кишечника. Имеющиеся данные говорят о том, что функция этих компонентов регулируется кишечными микроорганизмами; однако влияние старения на этот процесс было изучено лишь недавно. В будущем необходимы дальнейшие исследования для выявления клеточных и молекулярных изменений, связанных со старением, которые могут изменять барьерную функцию кишечника.
Если эти результаты получится воспроизвести у человека, они могут открыть новые перспективы влияния старения и факторов окружающей среды на функцию мозга, а также потенциально связанные с возрастом патологии и аспекты поведения. Ранее уже проводили связь между повышенной кишечной проницаемостью («дырявым кишечником») и некоторыми патологиями нервной системы (такими как болезнь Альцгеймера, болезнь Паркинсона, депрессия и расстройства аутистического спектра), хотя роль первой не удалось точно подтвердить. Кроме того, появились свидетельства накопления других нейроактивных кишечных метаболитов в мозге мышей. Все эти данные показывают, что химические соединения из пищи, микроорганизмы и/или кометаболизм между микробиомом и организмом хозяина могут влиять на определенные функции мозга. Примерами последнего взаимодействия служат кишечные метаболиты (КЦЖК обладает протективным действием, а КМЛ — патогенным). Обеспечение целостности кишечного барьера для регуляции проникновения метаболитов из кишечника в системный кровоток представляет собой новый подход к укреплению здорового функционирования тканей мозга.
Читайте также:
