Возрастание гидростатического давления в клубочках. Кровоток в почке
Добавил пользователь Дмитрий К. Обновлено: 21.01.2026
Гидронефроз - это функциональное нарушение чашечно-лоханочной системы почки. В результате стеноза усложняется отток мочи и повышается гидростатическое давление. Такие изменения приводят к трансформации паренхимы, ухудшают работу почки. Различают три стадии: начальную, раннюю, терминальную. Нарушение чаще встречается у женщин.
Этиология и патогенез гидронефроза
Различают врожденный и приобретенный гидронефроз. Патология всегда сопровождается сужением ЛМС (лохано-мочеточникового сегмента), аномалию могут вызывать следующие факторы.
Сдавление и пульсовое воздействие со стороны добавочного нижнесегментарного артериального сосуда.
Отклонение в развитии семенных и почечных вен.
Сегментарная дисплазия ЛМС.
Педункулит из-за вытекания мочи в почечный синус.
К провоцирующим факторам относятся: подвижность почки, аномальная работа парапельвикальной клетчатки, дисфункция почечных кровеносных сосудов.
Клиническая картина гидронефроза
Различает два этапа. Первый характеризуется образованием обструкции ЛМС, симптоматика невыражена. Для второго характерны основные признаки почечной недостаточности:
тупая боль в области поясницы;
наличие крови в моче;
При обострении возможна картина почечной колики. Специфичным симптомом для гидронефроза является выбор больного спать на животе, поскольку перераспределение внутрибрюшного давления облегчает отток мочи.
Диагностика гидронефроза
Для постановки диагноза пациентам проводят клинико-лабораторные исследования. Кроме анализов мочи и крови используют инструментальные методы. Если необходима операция, обязательно проводят гистологический анализ пораженной ткани.
Физикальный осмотр
На ранних стадиях малоинформативен, заметить нарушение при пальпации и перкуссии возможно на последних этапах болезни.
Ультразвуковое исследование
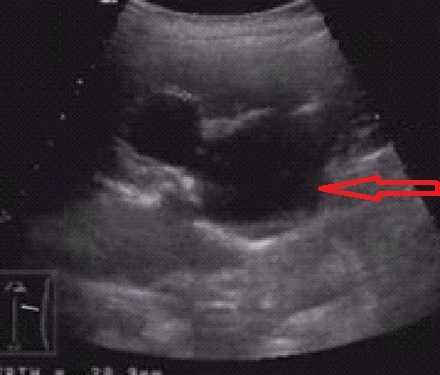
Ультразвуковое исследование. Диалатация чашечно-лоханочной системы.
При подозрении на данную патологию исследования проводят полипозиционно, оценивают состояние почки, лоханок, мочеточника, сосудов. Для корректного диагноза используют сравнение со здоровой почкой.
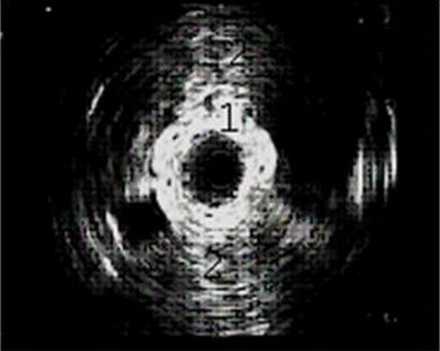
Эндолюминальная эхосонограмма зоны лоханочно-мочеточникового сегмента.
1. Стенка мочеточника.
2. Склероз парауретеральной клетчатки
Состояние парауретеральной клетчатки показывает эндолюминальный датчик, который заводят через мочеточник. Для оценки функциональных возможностей используют фармакоэкографию с мочегонными препаратами.
Эходоплерография сосудов почек.
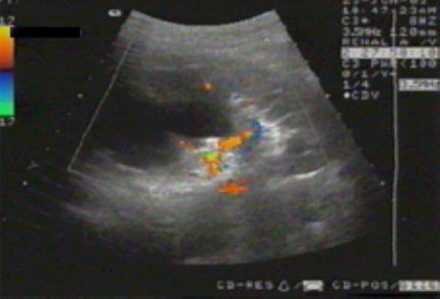
Эходопплерограмма. Снижение интенсивности кровотока в области истонченной паренхимы верхнего и среднего сегментов почки.
Исследование актуально для оценки гемодинамических отклонений. Патология приводит к трансформации органа и растяжению артериальных и венозных сосудов. По их размерам можно судить о стадии и корректно выбирать лечение.
Рентгенологические методы обследования
Если нет противопоказаний, то рентгенологические исследования с контрастом являются приоритетными в диагностике гидронефроза.
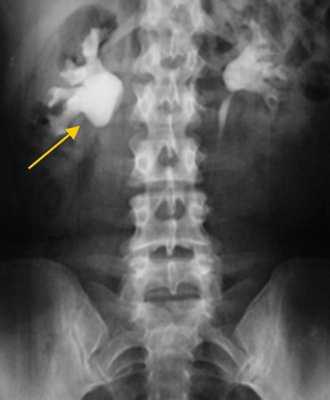
Экскреторная урограмма. Стеноз лоаночно-мочеточникового сегмента, гидронефроз справа.
Благодаря рентгеноконтрастным препаратам метод дает оценку экскреторным функциям почек. Он эффективен на начальных стадиях заболевания, по мере нарастания патологии диагностическая эффективность снижается.
Применяется для обследования мочевых путей, показывает их структурное состояние, но не отражает функционального.
Применяется при непереносимости йодсодержащих контрастов. Актуальна для пациентов со значительным угнетением почечной функции. Результативность исследования повышает видеозапись.
Антероградная чрескожная пиелография.
Назначается, когда уретеропиелография невозможна и когда почка не выделяет контрастное вещество.
Диагностирует нарушения в развитии почек и сосудов. Для уровазального конфликта характерна патология наполнения ЛМС. Метод позволяет оценить трансформацию органа и прилегающих сосудов.
КТ
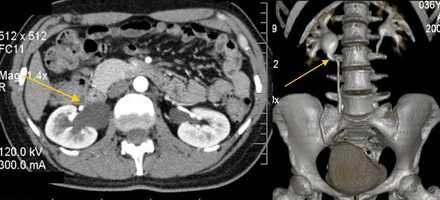
Мультиспиральная компьютерная томография. 3D реконструкция. Стеноз лоханочно-мочеточникового сегмента, гидронефроз справа.
Исследование неинвазивно и с высокой точностью показывает структурные изменения мочеполовой системы. На основании снимков проводится трехмерная реконструкция, что позволяет увидеть объем поражения и протяженность деформированного участка мочеточника. Не отражает функциональных изменений.
МРТ
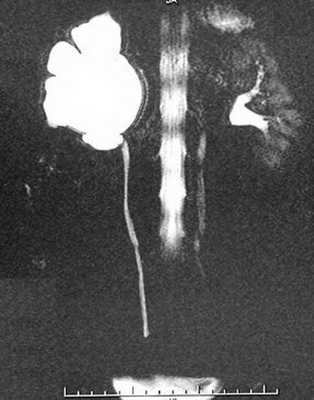
Магнитно-резонансная урография. Стеноз лоханочно-мочеточникового сегмента, гидронефроз справа.
Современный и наиболее информативный метод. Используется магнитно-резонансная урофагия с контрастом и без. В результате получают динамические изображения, которые демонстрируют все этапы эвакуации жидкости. Для более четкой визуализации мочевых путей используют фармакологические агенты. При большом количестве томографических срезов возможна 3D-реконструкция изображения.
Радионуклидные исследования
Для диагностики используют динамическую нефросцинтиграфию, в ходе которой оценивают транспорт радиоактивного вещества. Выделяют три сегмента исследования, каждый со своим временным течением. Первый отражает кровенаполнение почечных сосудов, второй - транспорт через клетки эпителия проксимальных канальцев, третий - уродинамику верхних мочевых путей. Метод показывает функциональные изменения, не дает информации о структурных деформациях.
Лечение гидронефроза
Сложность обнаружения патологии на начальных стадиях делает основным методом лечения реконструктивную операцию.
Подготовка к операции
Предусматривает комплекс мер по устранению патологических состояний и нормализации физиологических отклонений, что позволяет увеличить резерв функциональных возможностей почек. Для ликвидации воспалительного процесса используют НПВС, антигистамины, антибиотики. Для оздоровления соединительной ткани назначают солкосерил и вобэнзим.
Для снижения функциональной дегенерации назначают β2-адреномиметик гинипрал, на начальных стадиях это позволяет избежать операции. Также выполняется дренирование нефростомой или катетером-стентом.
Реконструктивные операции
Показаниями являются прогрессирование патологии, разрушение ткани, ведущее к функциональной и структурной гибели почки, сопутствующий гнойный пиелонефрит, состоявшееся почечное кровотечение.
Уретеропиелопластика (операция Андерсена-Хайнса) предусматривает резекцию больной зоны мочеточника и лоханки и создание пиелоуретерального анастомоза. Успешность операции обусловлена правильным определением зоны афункционального участка, резекция проводится на 5-6 мм дистальней пораженной ткани..
При стенозе ЛМС и наличии добавочного сосуда выполняется резекция, которая позволяет привести в соответствие просвет сосуда и паренхимы.
Важной частью вмешательства является эффективное дренирование, различают: нефростомию, установку мочеточникового катетера, катетера-стента. Важно предупредить воспалительные осложнения и внешнее инфицирование.
Включают два вида вмешательства: антеградную чрескожную эндопиелотомию и баллонную дилатацию. Операции показаны при небольших изменениях лоханки и отсутствии добавочного сосуда из-за высокого риска кровотечения. Эффективность составляет 72% против 89% открытого метода.
Сочетают в себе методы предыдущих двух. Позволяют проводить резекцию и наложение анастомоза, при этом характеризуются малой травматичностью и уменьшают сроки госпитализации
Послеоперационное ведение
Для нормального отведения мочи устанавливается катетер Фоли № 12-14. Чтобы уменьшить отек, назначают НПВС и уросептики. Для улучшения питания тканей используют венорутон, трентал. Для восстановления слизистой применяют вобэнзим и солкосерил. Длительность терапии в каждом случае определяется индивидуально, но ее срок составляет не менее 10 дней.
Антибиотики назначают после удаления дренажа с целью предупредить формирования мультирезистентной флоры, исключением является стойкое воспаление в первые сутки после операции.
После нефростомии обязательно проводят антеградную рентгенотелевизионную уроскопию и пиеломанометрию для проверки состоятельности верхних мочевых путей.
Заключение
Правильная диагностика и выбор метода коррекции определяют успешность терапии. Не менее важны предоперационная подготовка и послеоперационное обследование, оно позволяет определить успешность вмешательства, на ранних стадиях скорректировать осложнения.
Акопян Гагик Нерсесович - врач уролог, онколог, д.м.н., врач высшей категории, профессор кафедры урологии ФГАОУ ВО Первый МГМУ им. И.М. Сеченова
Застойная почка ( Нефрогенная венозная гиперемия , Сердечная почка , Хронический кардиоренальный синдром )
Застойная почка - это комплекс изменений в структуре тканей почек, который развивается на фоне недостаточности кровообращения, включает венозную гиперемию и дистрофию извитых канальцев. Выраженность симптомов коррелирует со степенью расстройств кровообращения. Для явной стадии типично уменьшение суточного диуреза, преобладание ночного мочеиспускания над дневным, изменение качества выделяемой мочи. Диагноз устанавливают на основании лабораторных (ОАМ, биохимия крови, суточная протеинурия) и инструментальных (УЗИ почек, КТ или МРТ-ангиография) исследований. Лечение направлено на коррекцию сердечно-сосудистых нарушений, поддержку функции почек.
МКБ-10

Общие сведения
Застойная почка (сердечная почка, нефрогенная венозная гиперемия, хронический кардиоренальный синдром) развивается при прогрессировании хронической сердечной недостаточности. В возрасте до 45-50 лет патология чаще встречается у мужчин, поскольку они более подвержены кардиологическим заболеваниям. После 65 лет застойная почка одинаково часто регистрируется у обоих полов. Нефрологи указывают, что адекватный контроль конгестивных явлений с одновременным улучшением или сохранением работы почек является основной целью в терапии ХСН и кардиоренального синдрома. По данным различных источников, распространенность нарушения функций почек при ХСН составляет 20-65%.

Причины
При хроническом застойном кардиоренальном синдроме II типа изменения изначально наблюдаются в сердечно-сосудистой системе, и только потом присоединяются нарушения со стороны почек. Основная причина - нарушение почечного кровотока на фоне снижения объема сердечного выброса при ряде кардиологических заболеваний: декомпенсированной гипертонии, легочном сердце, генерализованном кардиосклерозе и пр. При изменении насосной функции сердца любой этиологии выявляются общие морфологические и функциональные изменения в почках. В основе патологического процесса может лежать:
- Слабость миокарда. Повреждение сердечной мышцы проявляется слабыми сокращениями из-за снижения внутрижелудочкового давления. В результате отмечается недостаточный выброс притекающей крови в артерии большого и малого кругов. ИБС и инфаркт миокарда в 70% осложняются уменьшением насосной функции.
- Кардиальные пороки. При декомпенсированных пороках сердечные сокращения также ослаблены, мышечной энергии не хватает на продвижение крови через суженные отверстия. Неполное смыкание клапанного аппарата приводит к частичному возврату крови обратно в сердечную камеру и венозные сосуды.
- Уменьшение вместимости полостей сердца. Ограничение емкостей кардиальных полостей из-за субэндокардиального тромбоза, фиброэластоза, утолщения стенок желудочков и перегородки с субаортальным стенозом проявляется уменьшением сердечного выброса и снижением кровотока. Наблюдается при эндокардите Леффлера, гипертрофической кардиомиопатии, других патологиях.
- Скопление жидкости в полости перикарда. Отсутствие достаточного расширения кардиальных полостей в диастолу из-за скопления жидкости в результате воспаления часто заканчивается облитерацией за счет организации фиброзного экссудата. Фиброзные массы прорастают грануляциями и сосудами, соединительная ткань постепенно грубеет, сердце оказывается погруженным в пласт коллагена. Это препятствует сократительной деятельности миокарда.
К факторам, способствующим прогрессу застойного кардиоренального синдрома, относят сахарный диабет, бронхиальную астму, гиперфункцию щитовидной железы и ряд других заболеваний. У 25% больных с кардиоваскулярной недостаточностью диагностируют хроническую обструктивную болезнь легких на фоне бронхиальной астмы, что является предвестником неблагоприятного течения патологии. Переизбыток тиреотропных гормонов увеличивает нагрузку на миокард с его последующим ослаблением.
Сопутствующие тревожно-депрессивные расстройства отражают тяжесть симптомов застойной ХСН. Они могут негативно влиять на общий процесс через поведенческие факторы, увеличивающие сердечно-сосудистый риск. К таковым относят курение, злоупотребление спиртным, малоподвижность. Доказано, что пациенты с депрессией менее привержены терапии, что может способствовать более быстрому наступлению декомпенсированной стадии ХПН при застойной почке.
Патогенез
Застойное сердце не может обеспечить достаточный выброс крови в сосудистое русло, что проявляется уменьшением почечного кровотока преимущественно в корковом слое за счет спазма артериол и венозного полнокровия. В результате нарушается клубочковая фильтрация, вода и натрий накапливаются в организме. Капиллярно-паренхиматозный блок усиливает гипоксию тканей. Резкое спазмирование внутрипочечных артериальных сосудов порождает дистрофические нарушения с вовлечением канальцевого эпителия, развитием склерозирования стромы почек.
Гиперстимуляция ренин-ангиотензин-альдостероновой системы (РААС) проявляется вторичным гиперальдостеронизмом, что усугубляет гипернатриемию. Задержка натрия и воды способствует скоплению транссудата в органах и межуточной ткани, включая почку. При морфологическом исследовании визуализируются расширенные из-за гиперволемии вены и капилляры, включая клубочковые. Имеет место отек, пролиферация соединительнотканных структур, что получило название цианотической индурации. У 50% людей с сердечной почкой, особенно при гипертонической болезни, артериолы склеротически изменены.
Симптомы застойной почки
Симптомы сердечной почки появляются при выраженной кардиоваскулярной недостаточности. Основная клиника - уменьшение выделяемого количества мочи в течение суток, позывы на мочевыделение преимущественно в ночные часы (в норме дневной диурез составляет 80%, а ночной - 20%).Отеки могут уменьшаться или исчезать после сна. У некоторых пациентов повышается артериальное давление (больше - систолическое), что обусловлено активизацией РААС, увеличением объема циркулирующей жидкости, артериоспазмом. За счет задержки воды возможны жалобы на увеличение веса, чувство распирания, отеки.
У большинства больных с застойной гиперемией на раннем этапе азотемии нет, но стойкая олигурия (уменьшение диуреза до критических значений менее 200-300 мл мочи в сутки) может привести к накоплению азотистых оснований, увеличению уровня креатинина и мочевины. В этом случае появляются жалобы на выраженную слабость, тошноту, потерю аппетита. Количество мочи уменьшено, больного беспокоит изнуряющий кожный зуд. Нарастающая слабость, утомляемость и бледность объясняются анемией, что характерно для ХПН.
Осложнения
Основное осложнение застойной гиперемии - полная утрата функциональной способности почек с присоединением терминальной стадии ХПН. Ренальная дисфункция встречается у 2/3 пациентов с сердечной недостаточностью. Тяжелая форма ХПН значительно утяжеляет течение кардиоваскулярной патологии, при их одновременном прогрессировании часто наступает летальный исход. Гибели нефронов способствует ишемия почек, она же приводит к присоединению вторичной микробной флоры, что вызывает воспалительный процесс.
Ряд заболеваний (ревматизм, атеросклероз, гипертоническая болезнь) сами по себе изменяют морфологическую структуру почек и их функционирование, ХСН и развитие венозного полнокровия усугубляют утрату функций. Если сократимость миокарда нарушена значительно, кроме снижения СКФ регистрируют увеличение плазменной концентрации натрийуретических пептидов. Это приводит к острой декомпенсации ХСН. У 25-70% таких больных диагностируют острое повреждение почек, что создает условия для дальнейшего прогрессирования ХБП.
Диагностика
Симптомокомплекс «застойная почка» устанавливают при оценке жалоб, сопутствующей кардиоваскулярной патологии, данных лабораторно-инструментального обследования. Не всегда можно определить, что было первоначально - хроническое заболевание сердца или почек, поэтому деление заболеваний во многом условное. Пациенту может потребоваться консультация узких специалистов: эндокринолога, уролога. Алгоритм диагностики определяет нефролог, патологию подтверждают:
- Общий анализ мочи. В ОАМ отмечают кислую реакцию, высокий удельный вес из-за усиленной экскреции мочевины, повышенное содержание белка. Цвет урины насыщенный, темный. В осадке определяются лейкоциты, эритроциты, гиалиновые и зернистые цилиндры в небольшом количестве. Высокая плотность мочи - основной критерий, позволяющий дифференцировать застойную почку от почечной недостаточности. В дальнейшем по мере снижения СКФ удельный вес становится низким.
- Суточная протеинурия. При однократном выявлении микро- или макроальбуминурии возникает подозрение на нарушение почечной функции, окончательный вывод делают на основании повторного исследования. Анализ мочи на суточную протеинурию у пациента с ренальной гиперемией показывает содержание белка от 1-3 г/сут.
- Определение СКФ. Оценка скорости клубочковой фильтрации проводится у всех лиц с застойной недостаточностью и кардиоренальным синдромом. Для расчетов нефрологи используют специальные формулы Кокрофта-Голта, MDRD1, MDRD2 и пр. Стойкое снижение СКФ в течение 3 месяцев (менее 60 мл/минуту) свидетельствует о хроническом заболевании почек, а СКФ менее 90 мл/мин - о хронической ренальной дисфункции.
- Визуализационные методики. На сонограммах лоцируются увеличенные в размерах почки с нечеткой дифференцировкой паренхимы. Эти изменения в ряде наблюдений преходящие, по мере компенсации сердечной недостаточности картина может нормализоваться. МРТ и КТ-ангиография в диагностике сердечной почки более предпочтительна, чем УЗДГ, так как исследование показывает состояние даже мелких сосудов, особенности кровотока.
Дифференциальный диагноз проводят с гломерулонефритом, амилоидозом, инфарктом почки. Венозное полнокровие является противопоказанием к выполнению биопсии, поэтому нозологическую форму определяют с помощью лабораторных и инструментальных методов исследования. Если нет выраженных клинических проявлений со стороны сердца, но у пациента диагностирована застойная почка, показано дообследование для исключения латентных патологий: подострого бактериального эндокардита, системного васкулита и др.
Лечение застойной почки
Терапевтические мероприятия направлены на максимальную компенсацию застойной ХСН, уменьшение симптомокомплекса сердечной почки. По мере активации РААС прогрессирует патологический процесс с развитием фиброза в почках и сердце, поэтому важно раннее начало терапии. Пациента с ухудшением самочувствия и отрицательной динамикой клинико-лабораторных показателей госпитализируют в стационар.
Схему подбирают индивидуально с учетом рекомендаций кардиолога и нефролога после оценки результатов обследования. Выбор препаратов зависит от функционального класса сердечной недостаточности, степени поражения почек, сопутствующей патологии. Один из важных аспектов комплексного лечения - соблюдение диеты с максимальным ограничением поваренной соли менее 3 г и жидкости до 1,5 л в сутки в период активной диуретической терапии. Пациента ежедневно взвешивают для контроля скрытых отеков, считают количество выпитой воды и выделенной мочи, проводят динамическую тонометрию.
Консервативная терапия
К препаратам с доказанной эффективностью, снижающим уровень смертности и замедляющим прогресс застойной ХСН, относят ингибиторы АПФ/ БРА, антагонисты альдостерона, бета-блокаторы. По показаниям применяют комбинации нитратов и гидралазина, средства для стабилизации метаболизма миокарда и пр. Основные препараты действуют следующим образом:
- Ингибиторы АПФ и БРА. Клинические рекомендации по нефрологии для пациента с застойной сердечной недостаточностью относят блокаду РААС к мероприятиям первой линии, лежащим в основе кардио- и нефропротекции. Цель приема АПФ - выключение фермента, способствующего синтезу активного ангиотензина, который повышает давление. БРА также снижают АД, но работают с помощью устранения чувствительности рецепторов к ангиотензину.
- Диуретики. Для нормализации кровообращения не менее важно нейтрализовать минералокортикоидные рецепторы, для этого назначают антагонисты рецепторов альдостерона (калийсберегающие диуретики): спиронолактон, эплеренон. Их основное действие - вывод лишней жидкости и натрия при сохранении калия. Перед тем, как назначить то или иное средство, оценивают скорость клубочковой фильтрации. Фуросемид и торасемид применяют в качестве мочегонных средств при низкой СКФ.
- Бета-блокаторы. Лечение бета-блокаторами замедляет прогресс патологии, вызывает восстановление (ремоделирование) отделов сердца, улучшает функциональные возможности. На фоне приема препаратов уменьшается тахикардия, тормозится апоптоз и кардиотоксическое воздействие катехоламинов, опосредованно замедляется активность РААС. По показаниям бета-блокаторы могут использоваться в комбинированной терапии.
Хирургическое лечение
Хирургическое лечение в сочетании с медикаментозным преследует цель усилить насосную функцию миокарда. Застойная почка как осложнение ХСН может нивелироваться после оптимизации сердечного выброса. В случае наличия необратимых последствий с утратой функциональной способности прогрессирование ХБП можно существенно замедлить с помощью адекватной терапии. Операции при застойной ХСН и кардиоренальном синдроме включают:
- Ресинхронизацию. Ресинхронизирующая терапия помогает уменьшить функциональный класс ХСН. Искусственная синхронизация работы всех отделов сердца достигается путем имплантации кардиостимулятора. Основное показание - механическая асинергия желудочков и нарушение функции внутрижелудочковых структур.
- Прочие операции. При определении причины ХСН возможна коррекция дефекта с помощью оперативного лечения. При стенозе выполняют АКШ, но исследования не показали особых преимуществ операции в сравнении с медикаментозной терапией. Устранение митральной регургитации позволяет уменьшить клинические проявления у тщательно отобранных пациентов, отдаленный прогноз изучен недостаточно. Трансплантация сердца подходит для некоторых больных с терминальной стадией ХСН.
Экспериментальные способы: ультрафильтрация (УФ)
При рефрактерной (устойчивой) к терапии ХСН с прогрессированием уровня альбуминурии и снижением СКФ иногда применяют коррекцию водного гомеостаза путем выведения из крови безбелковой жидкости через естественные или искусственные фильтры. Дегидратация происходит дозированно, в этом заключается основное отличие от применения системных диуретиков. УФ осуществляется за счет разницы осмотического и гидростатического давления. Противоречивые данные клинических испытаний не позволяют широко рекомендовать УФ в клинической практике.
Существуют исследования, подтвердившие уменьшение массы тела за счет избавления от лишней жидкости в течение 48 часов после УФ при хронической СН. В другом исследовании оценивали состояние пациентов после проведения УФ и при назначении диуретиков без УФ. Получены данные, что количество осложнений (пневмония, бактериемия) больше в группе больных после ультрафильтрации. У испытуемых также было выявлено повышение креатинина сыворотки крови. Большинство нефрологов придерживается мнения, что УФ может назначаться для повышения эффективности диуретиков, но в составе комбинированного лечения.
Прогноз и профилактика
Исход при ХСН серьезный (неблагоприятный), застойная почка с прогрессированием ХПН утяжеляет прогноз. Чем выше функциональный класс сердечной недостаточности, тем больше вероятность летального исхода: при IV ФК летальность в течение 6 месяцев составляет 44%, при нетяжелой ХСН только 50% пациентов переживает 4-летний рубеж с момента установления диагноза. Внедрение современных методов лечения позволило уменьшить смертность при тяжелой СН на 35%.
Профилактика подразумевает приверженность к здоровому образу жизни. С превентивной целью даже здоровым людям следует регулярно контролировать уровень сахара и холестерина, артериальное давление, а при выявлении ХСН и нарушении почечной функции мониторировать уровень мочевины, креатинина, альбуминурии. Если врач назначил прием препаратов, необходимо четко следовать рекомендованной схеме, не менять группы и дозировки лекарств самостоятельно.
1. Поражение почек при сердечной недостаточности: от патофизиологии к лечению/ Шутов А.М.// Ремедиум-Приволжье 2015 - №1.
2. Болеет сердце - страдают почки: кардиоренальный синдром у больных с хронической сердечной недостаточностью/ Резник Е.В., Сторожаков Г.И., Гендлин Г.Е.// Лечебное дело - 2009 - №1.
3. Терапевтические стратегии лечения кардиоренального синдрома / Руденко Т.Е., Кутырина И.М., Швецов М.Ю., Шилов Е.М., Новикова М.С.// Лечащий врач - 2012 - №1.
Нефросклероз ( Сморщенная почка )
Нефросклероз — это патологическое состояние, вызванное гибелью нефронов, их замещением соединительной тканью с нарастанием почечной недостаточности. Проявляется полиурией, никтурией, гипертензией, отечностью, дискомфортом в пояснице, на поздних этапах — олигурией, гематурией, интоксикацией. Диагностируется с помощью лабораторных анализов, УЗИ, КТ, МСКТ почек, нефросцинтиграфии, ангиографии ренальных сосудов, урографии, биопсии. Для лечения применяют этиопатогенетическую терапию основного заболевания, антикоагулянты, антиагреганты, противоанемические, дезинтоксикационные, витаминно-минеральные средства, заместительную терапию, аллотрансплантацию почки.



Нефросклероз — вторичное клинико-анатомическое состояние, проявляющееся уплотнением, сморщиванием почек и снижением их функциональной состоятельности вследствие замещения паренхимы волокнами и межуточным веществом соединительной ткани. Сморщенная почка была впервые описана в 1914 году немецкими клиницистом Ф. Фольгардом и патологом К.Т. Фаром.
Обычно нефросклероз осложняет течение урологической и другой соматической патологии. В ХХ веке его ведущей причиной считался гломерулонефрит, в настоящее время — артериальная гипертензия и сахарный диабет (более 60% всех диагностированных случаев). Распространенность нефросклероза в европейских странах составляет 0,06%. При этом 10-20% больных нуждаются в проведении регулярного гемодиализа, а смертность от ХПН достигает 22%.

Причины нефросклероза
Сморщивание почки — полиэтиологический процесс, который осложняет различные сосудистые расстройства и урологические болезни. В зависимости от варианта нефросклероза специалисты в сфере урологии и нефрологии выделяют две группы причин, вызывающих первичное или вторичное замещение почечной паренхимы волокнистыми структурными элементами соединительной ткани. Первично сморщенная почка формируется на фоне поражения ренальных сосудов, обусловленного такими заболеваниями, как:
- Артериальная гипертензия. У больных с эссенциальной гипертонической болезнью и симптоматическими гипертензивными состояниями стойко спазмируются и сужаются почечные сосуды, нарушается питание паренхимы. Соединительнотканное уплотнение сосудистой стенки или гибель артериол, клубочковых капилляров завершается соответственно формированием медленно прогрессирующего артериосклеротического нефросклероза либо злокачественного артериолонекротического гломерулосклероза Фара.
- Атеросклероз ренальных артерий. Отложение на внутренней оболочке атеросклеротических бляшек делает сосудистую стенку менее эластичной, сужает просвет сосудов, питающих почечную паренхиму. Уменьшение тканевой перфузии провоцирует деструкцию нефронов и тканевую гипоксию, способствующую избыточному образованию соединительной ткани. Как следствие, в результате атеросклероза корковое вещество истончается, клетки мочевых канальцев атрофируются, из-за чего снижается функциональная состоятельность почки.
- Хроническое венозное полнокровие. На фоне застоя, вызванного нефроптозом, сужением или хроническим тромбозом ренальных вен, паренхиматозные сосуды паретически расширяются, приток насыщенной кислородом артериальной крови уменьшается, в тканях нарастает ишемия. Ситуация усугубляется уплотнением сосудистых стенок, дополнительно нарушающим тканевой метаболизм. В условиях гипоксии происходит частичное отмирание клеток, и на протяжении 10-15 лет возникает нефросклероз.
У некоторых пациентов ангиогенная деструкция почек возникает остро при частичной или полной тромбоэмболии ренальной артерии. Резкое нарушение кровообращения вызывает инфаркт почки — массовую гибель нефронов в результате острой ишемии. Впоследствии некротизированный участок постепенно замещается соединительной тканью, и развивается нефросклероз.
О вторично сморщенной почке говорят в тех случаях, когда пациент изначально страдает урологическим заболеванием, при которых почечная паренхима разрушается под влиянием инфекционных агентов, аутоиммунных комплексов, механических факторов (растяжения, травматизации конкрементами) и др. Основными причинами вторичного (нефрогенного) нефросклероза являются:
- Болезни почек. Склерозирование паренхимы может стать исходом пиелонефрита, туберкулеза почек, гломерулонефрита, мочекаменной болезни, поликистоза. Отдельную группу причин нефросклероза составляют вторичные нефропатии, осложнившее течение других патологических процессов — сахарного диабета, системной красной волчанки, злокачественных неоплазий, гестоза.
- Заболевания нижних мочевыводящих отделов. Нефросклероз может развиться на фоне гидронефроза, обусловленного обтурационным застоем мочи при склерозе шейки мочевого пузыря, формировании уретеро-вагинальных свищей, сдавливании опухолями малого таза. Атрофические процессы наблюдаются у 30-60% пациентов, страдающих пузырно-мочеточниковым рефлюксом.
Несмотря на разнообразие причин, вызывающих нефросклероз, механизм развития заболевания в целом является общим. Вначале под влиянием различных повреждающих факторов (гипоксии, воспалительных и дистрофических процессов, вызванных факторами патогенности микроорганизмов, аутоиммунными комплексами, прямыми травматическими воздействиями и др.) происходит деструкция клубочкового и канальцевого эпителия с выключение части нефронов из общего кровоснабжения.
Поскольку почечные клетки не способны к регенерации, после фагоцитирования разрушенных клеточных элементов начинается нефросклероз — поврежденный участок замещается соединительными волокнами, а сами почки уплотняются. В оставшихся клубочках усиливаются кровообращение и фильтрация, в результате чего увеличивается объем выделяемой мочи и уменьшается ее относительная плотность. На фоне нарушений кровотока повышается синтез ренина, регулирующего клубочковую фильтрацию, что способствует возникновению или усугублению артериальной гипертензии.
Благодаря высоким компенсаторным возможностям почечной ткани клинические признаки почечной недостаточности появляются только при выраженном нефросклерозе с потерей 70% нефронов обеих почек или 85% — одной. При сохранении 5% клеток и менее возникает функциональная несостоятельность органа, требующая проведения заместительной терапии.

Симптомы нефросклероза
Клиническая картина заболевания на ранней стадии характеризуется повышением количества суточной мочи (более 2 л), учащением актов мочеиспускания в ночное время (свыше 3-х раз за ночь), постоянными тянущими болями в области поясницы, увеличением артериального давления. По мере прогрессирования нефросклероза появляются отеки: сначала на лице, потом они распространяются равномерно по всему телу. Отечность наиболее выражена утром.
На поздней стадии симптоматика усугубляется: объем суточной мочи снижается до 0,5-0,8 л, в моче может появляться примесь крови, пациента беспокоит сухость во рту, постоянная жажда. Возникают и нарастают общие симптомы интоксикации: головная боль, тошнота и рвота, слабость, мышечные боли.
Серьезные нарушения процессов фильтрации и реабсорбции, возникающие при деструкции более 70-75% исходного числа нефронов, приводят к формированию хронической почечной недостаточности. Поскольку сморщенная почка перестает синтезировать эритропоэтин, необходимый для созревания эритроцитов в костном мозге, часто развивается железодефицитная анемия. У пациентов с нефросклерозом повышается риск нефрогенной артериальной гипертензии вследствие избыточной продукции ренина. При нарушении обмена витамина D возникает остеопороз с повышенной ломкостью костей и склонностью к образованию патологических переломов.
Пациентам с подозрением на нефросклероз назначают комплексное обследование, позволяющее определить особенности морфологической структуры почек, выявить признаки атрофии паренхимы, оценить функциональную состоятельность органа. Наиболее информативными лабораторными и инструментальными методами диагностики сморщенной почки считаются:
- Общий анализ мочи. Для нефросклероза показательно значительное уменьшение относительной плотности мочи (до 1,005-1,015 г/л). При нарастании признаков ХПН возможны эритроцитурия (до 2-3 эритроцитов в поле зрения), цилиндрурия, протеинурия (до 0,033 г/л).
- Общий анализ крови. У пациентов со сморщенной почкой снижается содержание гемоглобина и эритроцитов, отмечается умеренная тромбоцитопения, увеличение длительности кровотечения и времени свертываемости крови. Часто возникает небольшой лейкоцитоз.
- Биохимия крови. Оценка функциональной состоятельности по биохимическим показателям выявляет почечную недостаточность. При нефросклерозе может быть повышено содержание мочевой кислоты, креатинина, мочевины, магния, фосфора, натрия. Снижается уровень белка, калия.
- Сонография. Характерными эхографическими признаками нефросклероза служат уменьшение размеров пораженного органа, истончение паренхимы, атрофия коркового слоя, его нечеткая дифференциация с мозговым веществом. Зачастую по данным УЗИ почек выявляется нефрокальциноз.
- Ренгенологические методы. При обзорной и экскреторной урографии размеры почек, корковый слой уменьшены, в паренхиме определяются кальцификаты. Нарушение заполнения чашечно-лоханочной системы контрастным веществом может свидетельствовать о развитии ХПН.
- Ангиография. На ангиограммах почек артерии обычно сужены, деформированы. У части пациентов мелкий артериальный рисунок может отсутствовать (симптом «обгоревшего дерева»). Корковое вещество истончено. Типична неровность наружного контура почек.
- Динамическая нефросцинтиграфия. При сморщивании почка медленнее накапливает и выводит нефротропный радионуклид. Исследование дополняют статической нефросцинтиграфией, выявляющей дефекты паренхимы по неравномерному распределению радиофармпрепарата.
- Томография почек. На трехмерных моделях и послойных снимках, полученных в ходе КТ, МСКТ, выявляются истонченность коркового слоя, уменьшение размеров органа. Признаками нефросклероза являются сужение и деформация мелких артериальных сосудов.
- Пункционная биопсия почек. При гистологическом анализе биоптата почек отмечается значительное уменьшение количества нефронов, большое количество волокон соединительной ткани. В ходе исследования оценивается состояние артериол и капилляров.
Дифференциальная диагностика нефросклероза проводится с сахарным и несахарным диабетом, острой почечной недостаточностью, быстропрогрессирующим гломерулонефритом, гепаторенальным синдромом, гипохлоремической азотемией. При необходимости пациента, кроме врача-нефролога и уролога консультируют терапевт, кардиолог, фтизиатр, ревматолог, эндокринолог, онколог, онкогематолог.

Лечение нефросклероза
Консервативная терапия начальных стадий сморщивания почек направлена на коррекцию основного заболевания, спровоцировавшего склеротический процесс, и нарастающей почечной недостаточности. С учётом патологии, вызвавшей нефросклероз, пациенту назначают антибиотики, гипотензивные препараты, статины, глюкокортикостероиды, антигликемические, диуретические, нестероидные противовоспалительные и другие этиопатогенетические средства. Для купирования расстройств, вызванных функциональной почечной недостаточностью, могут применяться:
- Антикоагулянты и антиагреганты. За счет влияния на реологические свойства крови улучшают кровоток в ренальных артериолах, капиллярах и благодаря восстановлению тканевой перфузии замедляют нефросклероз. С осторожностью назначаются при нарастании ХПН.
- Витаминно-минеральные комплексы. Для коррекции изменений биохимического состава крови, вызванного нарушением фильтрации, используют препараты калия, кальция, витамин D, поливитаминные составы, бифосфонаты. Их прием улучшает метаболизм и предотвращает остеопороз.
- Противоанемические средства. При выявлении анемии назначают препараты эритропоэтина, стимулирующие образование эритроцитов, и железа, необходимого для синтеза гемоглобина. Уменьшение гемической гипоксии позволяет затормозить склеротические процессы в тканях почек.
- Дезинтоксикационная терапия. Чтобы ускорить выведение токсичных метаболитов, накапливающихся в организме при нефросклерозе, применяют энтеросорбенты, которые связывают продукты обмена в кишечнике. Для снижения уровня мочевины могут назначаться растительные средства на основе артишока.
Если сморщивание почки сочетается с ХПН III-IV стадии, показано проведение заместительной почечной терапии — перитонеального диализа, гемодиализа, гемодиафильтрации, гемофильтрации. Радикальным методом лечения, рекомендованным при нефросклерозе с уменьшением количества жизнеспособных нефронов до 5% и менее, является трансплантация почки после полостной или лапароскопической нефрэктомии.
При своевременном выявлении болезни прогноз относительно благоприятный, назначение адекватной терапии позволяет добиться длительного состояния компенсации нефросклероза. Со временем работа нефронов ухудшается, развивается хроническая почечная недостаточность: такие пациенты нуждаются в пересадке органа или регулярном гемодиализе.
Для профилактики нефросклероза необходимо соблюдать рекомендации специалиста по лечению нефрологических заболеваний (особенно воспалительного характера), контролировать уровень артериального давления, глюкозы крови, избегать переохлаждений, не злоупотреблять солью и мясной пищей. Важную роль в предупреждении развития сморщенной почки играет регулярное посещение семейного врача для раннего выявления и коррекции соматической патологии.
1. Патогенетические основы нефросклероза (Обзор литературы)/ Паунова С.С.// Нефрология и диализ. - 2005 - Т.7, № 2.
2. Формирование нефросклероза у детей/ Крутова А.С., Лучанинова В.Н., Полушин О.Г., Мельникова Е.А., Семешина О.В., Переломова О.В., Олексенко О.М.// Современные проблемы науки и образования. - 2016 - №4.
3. Функция почек при хроническом пиелонефрите, осложненном вторичным сморщиванием почки у детей: Автореферат диссертации/ Перевезенцева Ю.Б. - 2004.
Стеноз почечных артерий - симптомы и лечение
Что такое стеноз почечных артерий? Причины возникновения, диагностику и методы лечения разберем в статье доктора Илларионовой Ирины Николаевны, сосудистого хирурга со стажем в 7 лет.
Над статьей доктора Илларионовой Ирины Николаевны работали литературный редактор Вера Васина , научный редактор Вячеслав Подольский и шеф-редактор Маргарита Тихонова
Определение болезни. Причины заболевания
Стеноз почечной артерии — это патология, при которой сужается просвет и уменьшается кровоток в одной или обеих почечных артериях и их ветвях. Заболевание часто приводит к устойчивому повышению артериального давления.
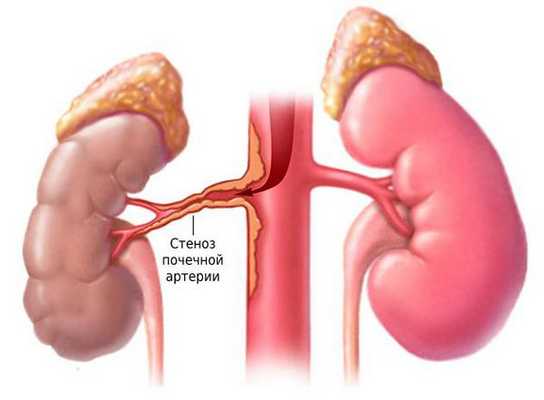
Причины заболевания
Примерно 90 % случаев стеноза почечной артерии вызваны атеросклерозом. Он может быть изолированным или поражать несколько сосудов. Чаще всего причиной атеросклеротического стеноза становятся бляшки, которые образуются на стенке аорты и разрастаются в просвет почечной артерии.
Менее чем в 10 % случаев стеноз возникает из-за фибромускулярной дисплазии — группы заболеваний, при которых поражаются стенки артериального сосуда. Причины патологии неясны, чаще ею страдают женщины молодого возраста [4] .
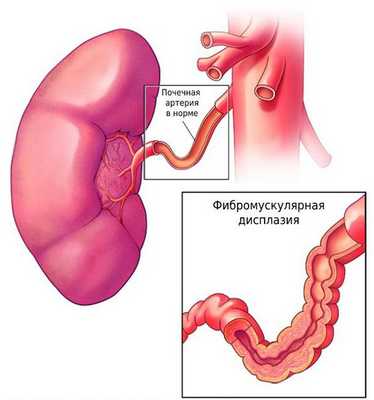
Другие причины, такие как системные васкулиты, частичное закрытие артерий тромбом и опухолевые заболевания, к стенозу почечной артерии приводят значительно реже.
Распространённость
Из-за старения населения атеросклеротический стеноз становится всё более распространён. Чаще всего встречается атеросклероз коронарных артерий, поражение почечных артерий находится на втором месте. Заболевание выявляется у 1-5 % больных гипертонией [1] [2] .
У пациентов с ишемической болезнью сердца, возникающей на фоне атеросклероза, почечные артерии поражены в 35-55 % случаев, при атеросклерозе артерий нижних конечностей — в 22-59 %. После 65 лет стеноз почечных артерий выявляется у 6,8 % пациентов: у 9,1 % мужчин и у 5,5 % женщин [3] .
Факторы риска
При обнаружении схожих симптомов проконсультируйтесь у врача. Не занимайтесь самолечением - это опасно для вашего здоровья!
Симптомы стеноза почечных артерий
Первое время стеноз почечной артерии протекает без выраженных симптомов. В дальнейшем болезнь проявляется в зависимости от её причины и возраста, в котором она началась.
Симптомы при фибромускулярной дисплазии
Фибромускулярной дисплазией преимущественно страдают женщины 30-50 лет. Болезнь чаще всего протекает со вторичной злокачественной гипертонией, то есть повышением артериального давления выше 180/120 и повреждением внутренних органов.
Симптомы при атеросклеротическом поражении почечной артерии
Заболевание зачастую развивается у пациентов старше 55 лет. Оно сопровождается тяжёлой артериальной гипертонией, устойчивой к лечению, и ухудшением работы почек.
В запущенной стадии при отёке лёгких появляется кашель с мокротой, окрашенной кровью, бледность и цианоз кожи, выраженная потливость. Пульс учащается, артериальное давление повышается. Могут появиться выраженные свистящие хрипы (сердечная астма) и признаки правожелудочковой недостаточности, например набухание вен шеи и отёки рук и ног.
При инфаркте почки возникает тупая боль в нижней части спины на поражённой стороне, повышается температура тела, появляется тошнота и/или рвота. В дальнейшем может развиться нефросклероз — сморщивание почки с нарушением её функции [5] .
Патогенез стеноза почечных артерий
При стенозе почечной артерии уменьшается кровоснабжение тканей почек и активируется ренин-ангиотензин-альдостероновая система (РААС) — гормональные факторы, регулирующие объём крови и кровяное давление. При этом почка длительное время продолжает стабильно работать.
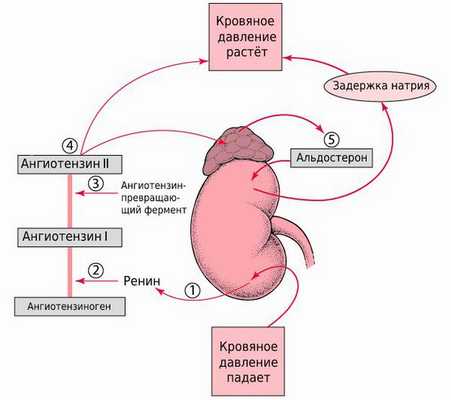
Активация ренин-ангиотензин-альдостероновой системы ускоряет развитие хронической почечной недостаточности.
При дальнейшем развитии стеноза резко снижается приток крови, что приводит к декомпенсации РААС. В результате уменьшается кровенаполнение клубочков, скорость клубочковой фильтрации и растёт уровень сывороточного креатинина — остаточного продукта, который образуется в мышцах при разрушении креатина. Он входит в цикл, снабжающий организм энергией для сокращения мышц. После интенсивной физической нагрузки креатинфосфат превращается в креатин, а затем — в креатинин, который фильтруется в почках и выделяется с мочой. Он почти полностью выводится почками, поэтому его уровень в крови показывает их функцию.
При последующем развитии стеноза почечной артерии:
- Сужаются сосуды и снижается содержание кислорода в органах и тканях.
- Развивается артериальная гипертензия.
- В сосудах разрастается соединительная ткань.
- На внутренней стенке почечной артерии образуются атеросклеротические бляшки.
- Почечная артерия может полностью закрыться.
Компенсацию сниженной функции почки, поддержание баланса натрия и воды берёт на себя противоположная почка. Если поражены обе почки, либо вторая почка отсутствует, то выделение натрия и воды из крови резко снижается и артериальная гипертензия становится объём-зависимой. Это означает, что задержка натрия и воды в организме приводит к повышению объёма циркулирующей крови и, соответственно, артериального давления [6] [7] .
Классификация и стадии развития стеноза почечных артерий
Стеноз почечной артерии относится к реноваскулярным, то есть почечно-сосудистым заболеваниям.
По причине развития выделяют:
- атеросклеротический стеноз — образование бляшек в стенках сосудов;
- врождённую фибромускулярную дисплазию — аномальное утолщение стенок артерий, не связанное с атеросклерозом или воспалением;
- стеноз, вызванный аутоиммунным заболеванием, например системным васкулитом;
- субтотальные тромботические окклюзии — закрытие просвета артерии тромбом;
- разрастание опухолей в почечную артерию.
Стеноз почечных артерий подразделяется на односторонний и двусторонний, гемодинамически значимый и незначимый.
При гемодинамически значимом стенозе артерия сужается более чем на 70 %, кровоток ускоряется.
Стеноз может поражать проксимальный отдел артерии, центральный и дистальный или охватывать всю артерию, а также распространяться на её ветви. Обычно развивается проксимальный стеноз почечной артерии.
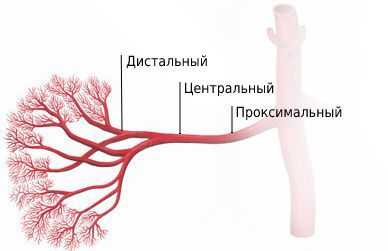
Стадии артериальной гипертензии при стенозе почечной артерии:
- стадия компенсации — давление в норме или умеренно повышено, снижается лекарствами, функция почки не ухудшена;
- стадия относительной компенсации — давление стабильно повышенное, но снижается лекарствами, почка немного уменьшена, её функция умеренно снижена;
- стадия декомпенсации — тяжёлая артериальная гипертензия, устойчивая к лечению, почка уменьшается, её функция значительно снижена;
- злокачественная артериальная гипертензия — устойчиво высокое давление, размеры почки выражено уменьшены, её функция угнетена.
Осложнения стеноза почечных артерий
К осложнениям стеноза почечной артерии относятся: прогрессирующая нефропатия, отёк лёгких, синдром Пикеринга и артериальная гипертензия.
Нефропатия
Основное осложнение стеноза почечной артерии — прогрессирующая нефропатия. При заболевании уменьшаются размеры и ухудшается работа почки, затем она полностью перестаёт выполнять свои функции.
Прогрессирующая почечная недостаточность приводит к сердечно-сосудистым осложнениям, таким как устойчивая сердечная недостаточность и внезапный отёк легких.
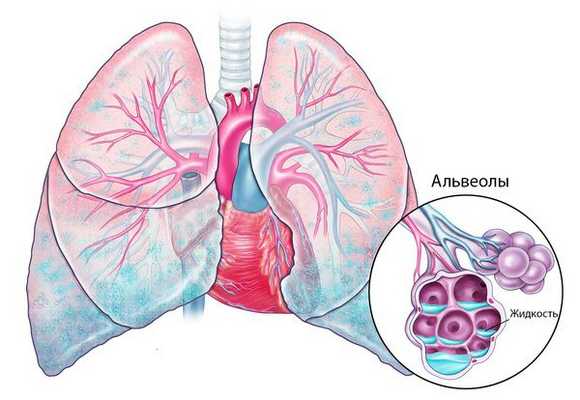
Отёк лёгких
Патогенез отёка лёгких недостаточно изучен. Предполагают три основных механизма его развития: задержка в организме натрия, развитие дисфункции сердца и повреждение барьера между воздухом в альвеолах и кровью.
При одностороннем стенозе почечных артерий функции повреждённой почки берёт на себя противоположная, увеличивая выделение натрия.
Пациенты с двухсторонним стенозом почечных артерий склонны к избыточному накоплению воды во внеклеточном пространстве с развитием отёка лёгких. Патология развивается из-за сниженного давления в почечных артериях, что приводит к росту уровня ангиотензина II, который, в свою очередь, вызывает рост артериального давления и задержку натрия.
Синдром Пикеринга
Впервые описан в 1998 году Томасом Пикерингом и его коллегами. Включает гипертонию, внезапный отёк лёгких и двусторонний стеноз почечной артерии.
Артериальная гипертензия
При стенозе почечной артерии часто наблюдается устойчивая к терапии артериальная гипертензия. Она приводит к дисфункции и выраженному увеличению объёма и массы левого желудочка. Возникающая диастолическая дисфункция (нарушение расслабления) способствует увеличению диастолического давления левого желудочка, давления в полости левого предсердия и лёгочных венах. Кроме диастолической дисфункции, при отёке лёгких снижается систолическая функция левого желудочка. Это приводит к тому, что уменьшается кровенаполнение почек, и в результате возникает порочный круг.
Диагностика стеноза почечных артерий
Ультразвуковое триплексное ангиосканирование — неинвазивный, безрадиационный и доступный метод диагностики, который может применяться при почечной недостаточности и аллергии на контрастное вещество. Позволяет оценить строение почечных артерий и движение крови по сосудам.
Недостатки метода: требует много времени, точность результатов сильно зависит от квалификации оператора, процедура технически сложна для пациентов с ожирением и метеоризом.
Компьютерная томографическая ангиография — отличный метод визуализации почечных артерий и окружающих структур. Позволяет быстро и с высокой точностью обнаружить стеноз почечной артерии.
Недостатки метода: использование йодированного контраста и ионизированного излучения. Кроме того, выраженный кальциноз почечной артерии может скрывать сужение просвета сосуда и затруднять оценку стеноза.
Магнитно-резонансная ангиография — неинвазивный метод, который позволяет получить качественные анатомические изображения почечных артерий и окружающих структур. Его точность в меньшей степени, чем ультразвукового триплексного ангиосканирования, зависит от оператора. Исследование высокочувствительно и специфично для обнаружения стеноза почечной артерии.
Недостатки метода: высокая цена; противопоказана пациентам с ферромагнитными имплантатами и нарушением функции почек со скоростью клубочковой фильтрации < 30 мл / мин / 1,73 м² ; не используется для оценки стеноза при установленном стенте.
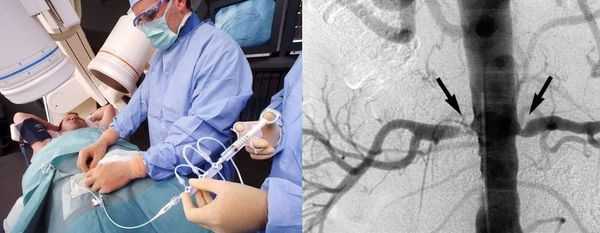
Катетерная ангиография почек — оптимальный метод диагностики стеноза почечной артерии. Позволяет измерить движение крови по сосудам и при необходимости восстановить проходимость артерии.
Недостатки метода: инвазивность, использование йодсодержащего контраста и ионизированного излучения, риски кровотечения, расслоения и повреждения сосудов, иногда требующие хирургического вмешательства.
Лабораторные исследования
При лабораторном обследовании можно выявить синдром почечной недостаточности — снижение скорости клубочковой фильтрации с умеренной азотемией (повышенным уровнем в крови азотистых продуктов обмена, выводимых почками).
Дифференциальную диагностику проводят с первичной артериальной гипертонией и другими вторичными гипертензиями [9] .
Лечение стеноза почечных артерий
Цель лечения — контролировать уровень артериального давления и сохранить функции почек. Оно включает медикаментозную терапию, хирургическую реконструкцию и восстановление проходимости артерий (реваскуляризацию) со стентированием или без него.
Медикаментозная терапия
Для лечения гипертензии, вызванной стенозом почечной артерии, применяют:
- ингибиторы ангиотензин-превращающего фермента (ИАПФ);
- блокаторы рецепторов ангиотензина (БРА);
- бета-адреноблокаторы и блокаторы кальциевых каналов [10] .
Если нет противопоказаний, то предпочтительны ИАПФ или БРА. Однако высокое давление при стенозе почечной артерии часто плохо снижается и приходится назначать несколько антигипертензивных средств. Дозировку и препараты врач подбирает индивидуально. Также пациентам может быть назначен аспирин и гиполипидемические препараты, чтобы замедлить развитие атеросклероза.
Образ жизни
Пациентам с атеросклеротическим стенозом почечной артерии важно отказаться от курения, контролировать вес и уровень сахара в крови.
Хирургические методы
Хирургическая реваскуляризация включает:
- аорторенальное и экстраанатомическое шунтирование — создание нового пути для притока крови, в обход заблокированной артерии;
- одностороннюю нефрэктомию — удаление почки;
- реконструкцию сосудов;
- почечную и трансаортальную эндартерэктомию — операции по очистке артерии от тромба .
Хирургическое вмешательство может быть показано при фибромускулярной дисплазии и аневризме. Однако из-за рисков и серьёзных осложнений, связанных с операцией, обычно при стенозе почечной артерии предпочтительнее чрескожная реваскуляризация, при которой катетер вводят в сосуд через прокол кожи [11] [12] [13] .
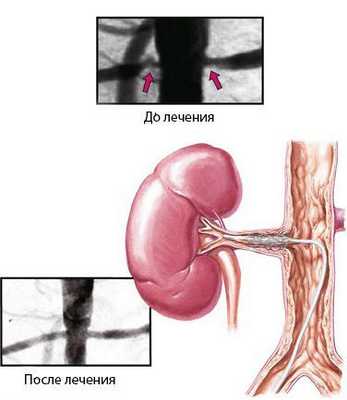
Прогноз. Профилактика
Эффективность лечения и прогноз зависят от коррекции факторов риска: избыточного веса, уровня холестерина и сахара в крови. Своевременная диагностика и приём лекарств, назначенных врачом, позволяют снизить риск развития почечных и сердечно-сосудистых осложнений. Вероятность, что они могут возникнуть без лечения, крайне высока, поэтому пациентам необходимо ежегодно проходить обследование.
При установке стента в первый год посещать доктора следует один раз в шесть месяцев, далее — один раз в год. Повторные стенозы артерии после почечной реваскуляризации в первый год встречаются в 2-8 % случаев, в течение пяти лет — от 15 до 60 %. При этом почечная функция постепенно снижается и может развиться ишемическая нефропатия [3] .
Читайте также:
- Этапы разработки лекарств от синтеза до регистрации
- Техника тенодеза бицепса при дегенеративном повреждении верхних отделов суставной губы плечевого сустава (SLAP)
- Мышечная гипертрофия. Быстрые и медленные мышечные волокна
- Цитология: методика получения мазка клеток в процессе митоза
- Причины, клиника, диагностика и лечение эпидурального абсцесса на фоне отита
