Зауербрух об операции Якобеуса. Оценка операции Якобеуса
Добавил пользователь Валентин П. Обновлено: 01.02.2026
БОАРИ ОПЕРАЦИЯ (A. Boari, итал. хирург) — пластическая операция для восстановления проходимости тазового отдела одного или обоих мочеточников. Свое название операция получила по решению Международного общества урологов.
Операция разработана в эксперименте Ван-Гуком (W- Van-Hook, 1893), Боари (1894). В клинике ее впервые выполнил Нюстрем (E. G. Nystrom, 1918), позднее применяли Оккерблад (N. Ockerblad, 1936), Колан (G. Caughlan, 1942), А. П. Фрумкин (1943).
Содержание
Показания
Плановую операцию производят при стриктуре или облитерации тазовых отделов мочеточников, образовавшихся гл. обр. после различных оперативных вмешательств (акушерские, гинекологические, урологические), а также при туберкулезе или ахалазии мочеточников. Показания к экстренному выполнению Б. о.— острая травма тазовых отделов мочеточников на значительном протяжении, когда исключается возможность наложения уретероуретеро- или уретероцистоанастомоза.
Противопоказания
Противопоказания к Б. о.: раковая инфильтрация тазовой клетчатки, сморщенный мочевой пузырь после интерстициального цистита.
Ранее проведенный курс лучевой терапии не является абсолютным противопоказанием к операции, хотя выполнение ее при этом связано со значительными техническими трудностями.
Техника операции
При подготовке к операции необходима тщательная санация мочевой системы в тех случаях, когда имеются мочевые свищи, особенно открывающиеся во влагалище.
Операцию производят под интратрахеальным наркозом с применением миорелаксантов (см.) и искусственной вентиляции легких. Наиболее удобным является разрез Пирогова (см. Пирогова разрез), который обеспечивает доступ к мочеточникам и мочевому пузырю. При двустороннем поражении мочеточников более благоприятные условия создает надлобковый дугообразный разрез. Однако применение внебрюшинного доступа может быть затруднено наличием спаечного процесса. В таких случаях применяется трансперитонеальный доступ, который облегчает мобилизацию мочеточников. Б. о. состоит из 4 основных этапов: 1) мобилизация мочеточника; 2) иссечение лоскута из мочевого пузыря; 3) формирование искусственного отдела мочеточника; 4) наложение мочеточниково-пузырного анастомоза. Выделяя мочеточники из окружающей плотной рубцовой ткани, нужно стремиться сохранить адвентициальную оболочку, чтобы избежать ишемии и некроза после операции. Мочеточники пересекают выше места облитерации, в пределах здоровых тканей, что важно для обеспечения достаточного кровоснабжения. Это способствует приживлению мочеточников и гарантирует хорошую проходимость и функцию анастомозов. В проксимальный конец мочеточника вводят на глубину 10—12 см полиэтиленовый катетер.
После выделения мочевого пузыря иссекают на его передне-боковой поверхности лоскут шириной 2—2,5 см, длиной 10—12 см. Основание лоскута должно быть примерно в 1/2 раза шире дистального конца и располагаться у дна пузыря, благодаря чему обеспечивается кровоснабжение его за счет ветвей верхней пузырной артерии. При двусторонней облитерации мочеточников одновременно выкраивают лоскуты: из свода пузыря в виде горизонтально расположенной буквы Н, либо два лоскута по вертикали, или один широкий лоскут, с к-рым соединяют оба мочеточника.
Лучшие условия питания лоскута создаются при продольном рассечении мочевого пузыря по средней линии. Затем обе половины рассеченной стенки отводят в стороны и мочеточники соединяют с ними одним из следующих способов:
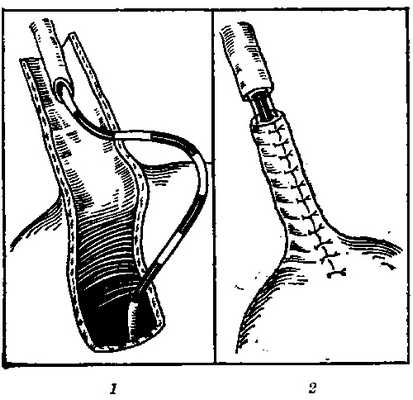
Операция восстановления мочеточника (на катетере) по Боари (некоторые способы): 1 — инвагинация мочеточника в трубку из стенки мочевого пузыря; 2 — конец мочеточника с трубкой, образованной из стенки мочевого пузыря, подготовлены к сшиванию конец в конец.
1. Инвагинационный метод — культю мочеточника погружают в пузырную трубку на глубину 1 — 1,5 см (рис., 1) и фиксируют швами к демукозированной его поверхности. При этом особое внимание обращают на то, чтобы слизистые оболочки были точно сопоставлены; в определенной степени это устраняет опасность образования стриктур анастомозов.
2. Анастомоз конец в конец: соединяют, как правило, косо срезанные концы пузырной трубки и мочеточников (рис., 2).
3. Имплантация культей мочеточников в подслизистый туннель на протяжении 1,5—2 см с последующим проведением их концов в просвет пузырной трубки.
Основными условиями, обеспечивающими успех операции, являются: хорошее кровоснабжение стебля, отсутствие натяжения в месте соединения мочеточника с пузырной трубкой и достаточный диаметр анастомоза.
Анастомоз накладывают с помощью узловатых кетгутовых швов. Затем закрывают дефект мочевого пузыря, предварительно выводя конец резинового дренажа наружу — у женщин по мочеиспускательному каналу, у мужчин — через дополнительный разрез на передней стенке мочевого пузыря; рядом с анастомозом устанавливают еще одну резиновую трубку. В нижний угол раны подводят пучок тонких резиновых дренажей. У больных с обильно развитой подкожной жировой клетчаткой рану дренируют через запирательное отверстие, а затем послойно ушивают до дренажа.
Формирование анастомозов осуществляют на предварительно введенном в просвет мочеточника катетере или трубке (шине). Лучшими являются полиэтиленовые трубки, т. к. они меньше инкрустируются мочевыми солями, но диаметр их не должен превышать № 12—14 по Шарьеру.
Трубки такого диаметра не угнетают развития эпителия и не вызывают рубцовых изменений в мочеточниках и в окружающей клетчатке.
Трубки из мочеточника удаляют обычно на 10-е сутки, т. к. более длительное их пребывание вызывает лимфоцитарную инфильтрацию, гипертрофию и фиброз стенки; пузырные дренажи — через 2 нед. При наличии нефростомы дренаж извлекают после установления проходимости мочеточниково-пузырного анастомоза.
Прогноз
Непосредственные результаты в большинстве случаев удовлетворительные. Критерием благополучного исхода Б. о. является свободный отток мочи из почечной лоханки в мочевой пузырь и ликвидация инфекции; такие исходы наблюдаются в 75—80% случаев. Свищи в области анастомозов наблюдают примерно в 8% случаев, преимущественно у больных, которые ранее подвергались лучевой терапии. Пузырно-мочеточниковый рефлюкс встречается примерно у 7% больных.
Летальность непосредственно после Б. о. составляет 2—3%. Основная причина смерти — перитонит. Основным осложнением в отдаленном периоде является стеноз анастомоза, развивающийся в 5—6% случаев и приводящий к гибели почечной ткани.
Библиография: Нан Д. В. Восстановительная хирургия мочеточников, М., 1973; Boari A. L’uret£ro-cysto-n£ostomie, Ann. Mai. Org. g6n.-urin., t. 17, p. 1059, 1141, 1899; Burns R. Reconstruction of the lower ureters by a tube made from bladder flaps, J. Urol. (Baltimore), v. 74, p. 348, 1955; С a u g h 1 a n G. V. Ureterovaginal fistula, repair of ureteral defect by use of bladder flap, ibid., v. 58, p. 428, 1947; Cukier J. Ь’орёгаШп de Boari, Acta urol. belg., t. 34, p. 15, 1966; N y s t r о m G. Beitrage zur Chirurgie der Ureteren, Nord. med. Ark., Bd 51, S. 109, 1918; Ockerb lad N. F. Reimplantation of ureter into bladder by flap method, J. Urol. (Baltimore), v. 57, p. 845, 1947.
Зауербрух об операции Якобеуса. Оценка операции Якобеуса
Подготовка к операции Якобеуса заключается прежде всего в постепенном доведении давления в плевральной полости до нуля, чтобы вскрытие ее не повлекло значительного изменения дыхания. Для этого увеличивают количество вводимого воздуха и частоту поддуваний, в течение 10—15 дней достигая выравнивания давления.
Если при этом больной испытывает тягостные ощущения или одышку, то операция откладывается до момента привыкания к большому коллапсу или вообще отменяется. Нужно, чтобы толщина слоя воздуха между грудной стенкой и легким была не менее 4 см. Если в плевральной полости имеется выпот, то стараются уменьшить его путем осторожных отсасываний с введением антибиотиков. При наличии других временных противопоказаний в предоперационном периоде пытаются ликвидировать их соответствующей терапией.
Для торакоскопии употребляются торакоскопы различной конструкции.
Торакоскоп с боковой оптикой создает видимость с углом зрения в 60°. Направление оптики отмечено на окуляре пуговкой. Недостатком этого то-ракоскопа является то, что при боковой оптике не видны предметы, расположенные впереди инструмента, искажается перспектива, т. е. отдаленные предметы кажутся слишком маленькими, а близко расположенные —слишком большими и, наконец, значительно искажается форма предмета. Преимуществом является возможность рассмотреть предметы, расположенные рядом с торакоскопом, а также возможность исследовать их со всех сторон при незначительном перемещении торакоскопа.
Торакоскоп с прямой оптикой позволяет видеть предметы в неискаженном виде, имеет угол зрения в 110°, но не дает возможности видеть предметы, расположенные рядом с торакоскопом. Обследование с помощью торакоскопа с прямой оптикой требует больших и неудобных его перемещений.
Инструмент, служащий для разрушения сращений, называется каутер. Он представляет собой изогнутый проводник, заканчивающийся на конце платиновой петлей. Каутер вводится вместе с футляром — тонкой трубкой, служащей проводником для каутера. Наконец, для прокалывания грудной стенки применяются специальные троакары, состоящие из стилета и канюли.
Подача тока для лампочки торакоскопа и для нагревания петли каутера осуществляется через обычный трансформатор, используемый для эндоскопии.
Стерилизация торакоскопов, каутеров и шнуров производится в парах формалина в закрытом сосуде или в спирте. Стилет, канюли и футляры стерилизуются кипячением. Торакоскопии производятся в затемненной операционной.
Развитие хирургии легочного туберкулеза продолжается с восьмидесятых годов прошлого до середины сороковых годов настоящего столетия.
К началу этого периода выявилась малая эффективность вскрытия туберкулезных каверн в легких [Серенвиль (De Cerenville), 1885; Рунеберг (J. Runeberg), 1887; Зонненбург (Е. Sonnenburg), 1891, и др.]. Наибольшим опытом в открытом лечении каверн обладал Тюфье (Т. Tuffier, 1899), который в 1897 г. на XII Международном медицинском конгрессе в Москве сообщил о 26 операциях с 13 летальными исходами.
Причины плохих результатов кавернотомии были многочисленны (Л. К. Богуш, 1955). Оперировали главным образом крайне тяжелых больных, у которых оздоровление каверны уже не могло изменить течения процесса. Во время операции возникали трудности с определением локализации каверны. Вмешательство часто осложнялось пневмотораксом и кровотечением. В послеоперационном периоде почти всегда образовывались стойкие бронхиальные свищи, нередко наблюдались бронхогенное обсеменение здоровых участков легкого и септическая инфекция раны грудной стенки.
Вследствие высокой послеоперационной летальности и частой неэффективности кавернотомию стали применять крайне редко [М. М. Дитерихс, 1926; Зауэрбрух (F. Sauerbruch), 1930]. Лишь в 1940 г. Н. Г. Стойко вновь вернулся к открытому лечению некоторых каверн нижней доли.
Значительно большее внимание привлекали хирургические методы уменьшения объема пораженного туберкулезом легкого. Они основывались на теоретических предположениях (К. К. Зейдлиц, 1842, и др.),. экспериментальных данных [Керзон (J. Carson), 1822] и многочисленных наблюдениях клиницистов о благоприятном влиянии эксудативного плеврита и спонтанного пневмоторакса на течение туберкулезного процесса.
В 1882 г. Форланини (С. Forlanini) опубликовал несколько работ, в которых предлагал лечить туберкулезные поражения одного легкого образованием искусственного пневмоторакса. Потен (М. Potain, 1888) применил этот способ при лечении больного со спонтанным пневмотораксом,, осложненным пневмоплевритом. В 1888 г. Форланини с успехом наложил пневмоторакс больному легочным туберкулезом и эксудативным плевритом, а в 1894 г. сообщил о своих клинических наблюдениях и технике операции.
В дальнейшем метод наложения искусственного пневмоторакса путем разреза межреберного промежутка изучали Мерфи (J. Murphy, 1898), Лемке (A. Lemke, 1899) и особенно Брауер (L. Brauer, 1906) с сотрудниками. Однако лишь разработка пункционного способа наложения пневмоторакса и введение в практику манометра [К. М. Сапежко, 1899; Заугман (Ch. Saugman), 1908], а также появление рентгенологического метода исследования сделали эту операцию практически безопасной и доступной не только хирургам, но и терапевтам и фтизиатрам. В 1914 г. А. Я. Штернберг уже считал, что искусственный пневмоторакс является «самым крупным завоеванием в борьбе с тяжелым туберкулезом легких, какое когда-либо знала медицина».
Постепенно лечение пневмотораксом целиком перешло в руки фтизиатров (А. Я. Штернберг, 1910; А. Н. Рубель, 1912; В. А. Равич-Щербо, 1927, и др.). Задача хирургов заключалась главным образом в коррекции пневмоторакса путем разрушения плевральных сращений.
В 1909 г. Ровзинг (Т. Bowsing) впервые произвел открытое пересечение сращений путем торакотомии. Больная погибла от септического плеврита. В 1911 г. 6 подобных операций были сделаны Зауэрбрухом (1930), но их исходы были плохими. Метод открытого пересечения сращений оказался в те годы неприемлемым вследствие кровотечений и частого развития эмпием.
В 1910—1913 гг. Якобеус (Н. Jacobeus, 1915) сконструировал торакоскоп и разработал операцию закрытого пережигания плевральных сращений. Первое время торакокаустика сопровождалась значительным количеством осложнений, главными из которых были кровотечения и повреждения легочной ткани. После детального морфологического изучения плевральных сращений, уточнения показаний к операции, улучшения инструментария и усовершенствования хирургической техники торакокаустика стала получать все большее распространение.
В СССР первую торакокаустику произвел М. П. Уманский в 1929 г. (по Н. В. Антелаве, 1952). С 1929 г. эту операцию стал широко применять К. Д. Есипов (1933). Для разработки, усовершенствования и пропаганды пережигания сращений особенно много сделал Н. Г. Стойко. За короткий срок торакокаустика была освоена десятками хирургов и фтизиатров нашей страны. Она стала самой распространенной операцией при туберкулезе легких, без которой искусственный пневмоторакс теряет половину своей ценности (Н. Г. Стойко, 1937).
Одновременно с первыми попытками лечения легочного туберкулеза наложением пневмоторакса объем пораженного легкого старались уменьшить путем резекции ребер. Этот метод представлялся особенно важным для больных с облитерированной плевральной полостью.
КОЛЛАПСОТЕРАПИЯ
Коллапсотерапия (лат. collapsus ослабевший, упавший + греч. therapeia лечение) — методы лечения туберкулеза путем достижения временного или постоянного спадения (уменьшения объема) пораженного легкого.
Впервые Коллапсотерапия в виде искусственного пневмоторакса была теоретически обоснована К. К. Зейдлицем (1842); искусственный пневмоторакс введен в практику в 1882 г. Форланини (G. Forlanini).
Лечебный эффект Коллапсотерапии заключается в том, что наступает рассасывание воспалительных туберкулезных инфильтратов и заживление каверны. Наиболее распространенными теориями механизма действия К. являются: функциональный покой пораженного легкого, лимфатический стаз, венозный застой в спавшемся легком, перегибы мелких бронхов, нейротрофические изменения в спавшейся легочной ткани. Один из этих факторов или все вместе стимулируют репаративные процессы в пораженном легком, приводящие в большом проценте случаев к излечению от активного туберкулеза легких.
Достигнуть спадения (коллапса) легкого позволяют следующие методы: введение воздуха в плевральную полость путем прокола иглой грудной стенки (см. Пневмоторакс искусственный); резекция задних отделов ребер над пораженным отделом легкого — экстраплевральная торакопластика (см.); отслоение париетальной плевры вместе с пораженным участком легкого и создание полости между грудной стенкой и отслоенной плеврой, в к-рую периодически вводится воздух,— экстраплевральный пневмоторакс; пересечение диафрагмального нерва (см. Френикотомия) или его алкоголизация в области шеи с целью создания паралича и подъема купола диафрагмы; повторные введения e брюшную полость воздуха через прокол иглой брюшной стенки с целью временного подъема купола диафрагмы (см. Пневмоперитонеум). Для каждого метода разработаны показания.
Из всех методов К. наибольшее значение приобрел искусственный пневмоторакс. До появления специфических противотуберкулезных химиопрепаратов он был основным методом лечения различных форм легочного туберкулеза. Его роль особенно возросла после разработки Якобеусом (H. Ch. Jacobaeus, 1913) метода закрытого пережигания плевральных сращений гальванокаутером. Л. К. Богуш (1945) широко применял гидравлическую препаровку плевральных сращений, вдвое увеличивающую эффективность операции Якобеуса.
При облитерации плевральной полости и невозможности наложения искусственного пневмоторакса у больных деструктивным туберкулезом легких широкое применение получили торакопластика и экстраплевральный пневмолиз (см.). Эти операции позволяют избирательно коллабировать пораженную часть легкого (селективная К.). Экстраплевральный пневмолиз применяется при ограниченных деструктивных процессах с небольшими кавернами в верхней доле легкого (верхний пневмолиз) или в VI сегменте (нижний пневмолиз). Л. К. Богуш (1950) усовершенствовал и упростил эту операцию, предложив подмышечный оперативный доступ и отслаивание париетальной плевры марлевым тупфером под контролем освещения лампочкой торакоскопа. Для стабилизации образованной экстраплевральной полости и удержания соответствующей части легкого в коллабированном состоянии в полость периодически вводят воздух (экстраплевральный пневмоторакс); созданную полость можно заполнить стерильным вазелиновым маслом — олеоторакс (см.).
Торакопластика с поднадкостничной резекцией пяти — семи верхних ребер применяется при фиброзно-кавернозном туберкулезе верхних долей легких. При поражении всего легкого производится тотальная торакопластика.
При кровотечении из каверны показания к наложению искусственного пневмоторакса, экстраплевральному пневмолизу или торакопластике могут быть срочными. Возможны двусторонний экстраплевральный пневмолиз, двусторонняя ограниченная торакопластика, а также сочетание пневмолиза на одной стороне с торакопластикой на другой.
С начала 50-х гг. 20 в. показания к К. резко сужены во всех случаях благодаря успехам химиотерапии туберкулеза и широкому применению резекции легких. Сохраняют значение пневмоперитонеум, который накладывают при инфильтративно-пневмоническом туберкулезе в фазе распада и обсеменения и при кровотечениях из каверн в нижней доле, а также торакопластика, к-рая по частоте применения занимает второе место после резекции легких среди методов хирургического лечения легочного туберкулеза.
Коллапсотерапия противопоказана при больших и гигантских кавернах, бронхостенозе, циррозе легкого, а также при выраженной дыхательной недостаточности (см.).
Библиография: Богуш Л. К. О гидравлической препаровке плевральных сращений, Пробл, туб., № 5, с. 29, 1949; Михайлов Ф. А. Искусственный пневмоторакс при туберкулезе легких, Свердловск, 1946; Многотомное руководство по хирургии, под ред. Б. В. Петровского, т. 5, с. 523, М.—Л., 1960; Стойко Н. Г. Хирургическое лечение легочного туберкулеза, М., 1949, библиогр.; Хрущева Т. Н. Экстраплевральный пневмоторакс и олеоторакс, М., 1952, библиогр.; Bier А., Вraun H. u. Kummell H. I. Chirurgische Operationslehre, Bd 3, T. 1, S. 381, Lpz., 1971, Bibliogr.; Malluche H. Die Pneumolyse, Lpz., 1957, Bibliogr.
Операция Якобеуса
Википедия
Статьи для врачей
- 12.02.2105 Восприятие марки настроено позитивно. Диктат потребителя
- 12.02.2105 Восприятие марки настроено позитивно. Диктат потребителя
- 12.02.2105 Восприятие марки настроено позитивно. Диктат потребителя
Статьи для пациентов
SPRINT: О целевом уровне артериального давления у пожилых
Антидепрессанты. Влияние на сон и когнитивные функции у пожилых
IDSA/ ATS. Рекомендации по лечению внутрибольничных пневмоний
Головная боль у взрослых. Виды головных болей.
Головная боль. Вопросы и ответы
Мигрень
Болезнь Альцгеймера и антидепрессанты
Артериальная гипертензия. Какое из имеющихся руководств лучше
Насыщенные жиры и риск сердечно-сосудистых заболеваний. Первые шаги революции?
Терпены
Терпены - группа природных ненасыщенных углеводородов, содержащихся гл. обр. в эфирных маслах (камфора, ментол и др.); применяются, напр., при изготовлении лекарственных средств и инсектицидов.
Тандлера схема
Тандлера схема (J. Tandler, 1869-1936, австрийский анатом) - схема расчета проекции долей и извилин большого мозга на кости черепа по наружным костным ориентирам.
Сустав локтевой
Сустав локтевой (a. cubiti, PNA, BNA, JNA) - сложный сустав, объединяющий плечелоктевой, плечелучевой и проксимальный лучелоктевой сустав, заключенные в одну суставную капсулу; в суставе локтевом возм.
Читайте также:
