Проблема лекарственно устойчивого туберкулеза
В настоящее время проблема лекарственной устойчивости возбудителя туберкулеза приобрела глобальное значение, во многом определяя распространение, клиническое течение и прогноз исходов заболевания. Важным аспектом является значительная эпидемиологическая опасность, которую представляют для окружающих больные, выделяющие мультирезистентные штаммы микобактерии туберкулеза. Устойчивость к рифампицину, первичная или приобретенная, значительно повышает вероятность обострений и рецидивов, а резистентность к рифампицину и изониазиду является прогностическим признаком неэффективности лечения, поэтому комбинированная устойчивость к этим двум препаратам расценивается как мультирезистентность микобактерий туберкулеза. Эффективность лечения этой категории больных значительно ниже, чем пациентов, выделяющих лекарственно-чувствительные штаммы микобактерии туберкулеза. Эпидемиологическое значение туберкулеза с лекарственной устойчивостью, особенно с мультирезистентностью, заключается, прежде всего, в том, что больные представляют собой наиболее опасный источник туберкулезной инфекции, в значительной мере определяя уровень инвалидности и смертности от туберкулеза.
С учетом вышесказанного изучение особенностей клинического течения, эффективности лечения лекарственно-устойчивого туберкулеза и разработка мер профилактики лекарственной устойчивости микобактерий туберкулеза к противотуберкулезным препаратам приобретают важное значение.
Целью исследования явился анализ результатов лечения больных туберкулезом, выделяющих штаммы микобактерий туберкулеза с лекарственной устойчивостью к противотуберкулезным препаратам за 2003 г. среди контингентов бактериовыделителей, состоящих на учете в противотуберкулезных учреждениях республики и среди вновь выявленных пациентов, находившихся на лечении в НИИ пульмонологии и фтизиатрии МЗ РБ, а также разработка методологии профилактики лекарственно-устойчивых форм туберкулеза.
В соответствии с поставленной целью была изучена эффективность диспансерного наблюдения контингентов бактериовыделителей за 2003 г. по показателям абациллирования и летальности от туберкулеза (по данным учетно-отчетных форм № 33).
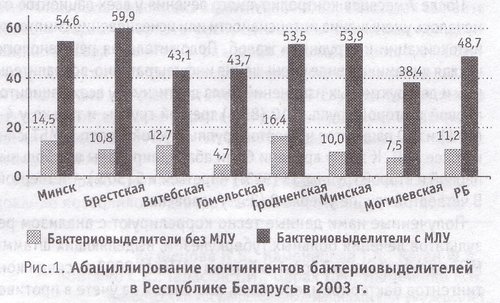
Как видно из рис. 1, частота абациллирования у бактериовыделителей с множественной лекарственной устойчивостью микобактерии туберкулеза к противотуберкулезным препаратам в Республике Беларусь почти в 4 раза ниже, чем у бактериовыделителей без множественной лекарственной устойчивости. Наиболее низкий показатель конверсии мокроты в Гомельской и Могилевской областях (4,7 и 7,5% соответственно); наиболее высокий - в г. Минске и Гродненской области (14,5 и 16,4% соответственно) несмотря на то, что эти показатели крайне низкие.
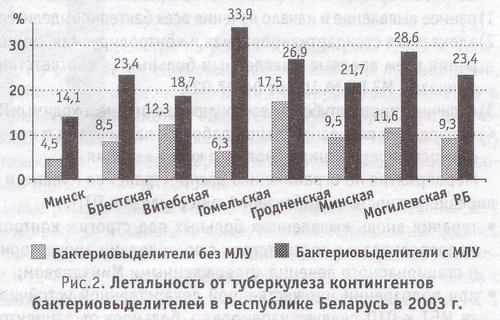
Как видно из рис. 2, летальность бактериовыделителей с множественной лекарственной устойчивостью микобактерий туберкулеза к противотуберкулезным препаратам из состоявших на диспансерном учете в 2003 г. в среднем по республике в 2,5 раза выше, чем бактериовыделителей без множественной лекарственной устойчивости. Наиболее неблагоприятная ситуация в Гомельской и Могилевской областях (33,9 и 28,6% соответственно), более благополучная - в г. Минске и Витебской области, где данные показатели составили 14,1 и 18,7% соответственно.
Параллельно на базе клиники НИИ пульмонологии и фтизиатрии МЗ РБ был проведен анализ результатов лечения 60 пациентов с впервые выявленным инфильтративным туберкулезом легких.
После получения результатов лекарственной чувствительности микобактерий туберкулеза к противотуберкулезным препаратам были выделены четыре группы. У 18 больных первой группы микобактерии туберкулеза были чувствительны к противотуберкулезным препаратам. У 20 пациентов второй группы была выявлена монорезистентность (устойчивость к изониазиду, рифампицину или стрептомицину). У 12 больных третьей группы отмечалась устойчивость микобактерий туберкулеза одновременно к двум и более препаратам (изониазиду - стрептомицину, рифампицину - стрептомицину, изониазиду - этамбутолу, изониазиду - стрептомицину - этамбутолу), т.е. полирезистентность. У 10 больных четвертой группы наблюдалась множественная лекарственная устойчивость (одновременная устойчивость к изониазиду и рифампицину с устойчивостью к другим противотуберкулезным препаратам или без таковой).
Полученные нами данные тесно коррелируют с анализом результатов лечения больныхтуберкулезом, выделяющих штаммы микобактерий туберкулеза с лекарственной устойчивостью к противотуберкулезным препаратам за 2003 г., среди контингентов бактериовыделителей, состоящих на учете в противотуберкулезных учреждениях республики.
Таким образом, наши данные свидетельствуют о том, что эффективность лечения больных туберкулезом с поли- и особенно множественной лекарственной устойчивостью микобактерий туберкулеза к противотуберкулезным препаратам очень низка по сравнению с таковой у лиц, выделяющих лекарственно-чувствительные и монорезистентные штаммы микобактерии.
В соответствии с поставленными задачами нами также были разработаны меры профилактики первичной и вторичной лекарственной устойчивости возбудителя туберкулеза.
Основные принципы профилактики лекарственной устойчивости:
- раннее выявление и начало лечения всех бактериовыделителей;
- адекватная стандартизированная и контролируемая химиотерапия всем впервые выявленным больным (в соответствии с приказом МЗ РБ № 106 от 04.07.02);
- наличие в противотуберкулезных учреждениях необходимых противотуберкулезных препаратов;
- проведение разъяснительной работы с пациентами о недопустимости прерывания основного курса лечения.
Мероприятия по ограничению распространения мульти- и полирезистентности микобактерии туберкулеза к противотуберкулезным препаратам:
Разработанные мероприятия позволят существенно снизить распространенность лекарственно-устойчивых форм туберкулеза и повысить эффективность его лечения, что даст экономию значительных финансовых средств. В целом это благоприятно отразится на показателях заболеваемости и смертности от туберкулеза в Республике Беларусь.
Скрягина Е. М., Борщевский В. В., Гуревич Г. Л., Астровко А. П., Суркова Л. К., Богомазова А. В.
НИИ пульмонологии и фтизиатрии МЗ РБ.
… увеличение групп риска детей и подростков по инфицированию и заболеванию туберкулезом служит неблагоприятным прогностическим фактором в отношении дальнейшего роста заболеваемости туберкулезом.
В настоящее время существует четкое определение понятия лекарственной устойчивости микобактерий туберкулеза.
Природно-устойчивые штаммы микобактерий туберкулеза – штаммы никогда ранее не подвергавшиеся воздействию противотуберкулезных препаратов, но по своей природе устойчивые к ним. Например, M. bovis природно-устойчивы к приразинамиду, M. africanum – к тиоацетазону.
Дикие мутанты лекарственно-устойчивых микобактерий туберкулеза – спонтанные мутанты, обнаруженные в диких штаммах с частотой, различной для каждого препарата.
Начальная (первичная) лекарственная устойчивость – наличие лекарственной устойчивости микобактерий туберкулеза к одному препарату и более у впервые зарегистрированных больных, ранее не принимавших противотуберкулезные препараты.
Приобретенная (вторичная) лекарственная устойчивость – устойчивость, развившаяся во время лечения у больных, имевших до начала лечения чувствительные микобактерии туберкулеза, ставшие устойчивыми в процессе лечения.
Монорезистентность – устойчивость к одному противотуберкулезному препарату.
Полирезистентность – устойчивость более чем к одному химиопрепарату (но не к рифампицину и изониазиду).
Множественная лекарственная устойчивость – устойчивость одновременно к рифампицину и изониазиду независимо от устойчивости к другим препаратам.
В настоящее время выделяют два варианта течения туберкулеза легких, характеризующихся обострениями клинической картины и исходов, а также требующие различных методических подходов к лечению. Это ( 1 ) лекарственно-чувствительный туберкулез легких, вызванный микобактериями туберкулеза, чувствительными ко всем противотуберкулезным препаратам и ( 2 ) лекарственно-устойчивый туберкулез легких, вызванный лекарственно-резистентными микобактериями туберкулеза к одному противотуберкулезному препарату и более. Особенно тяжело протекает лекарственно-устойчивый туберкулез у больных с множественной лекарственной устойчивостью микобактерий туберкулеза.
Определение лекарственной устойчивости микобактерий туберкулеза проводится по методам, утвержденным приказом Минздрава РФ № 109 от 21.03.03 .
Материалом исследования могут служить мокрота, промывные воды бронхов, бронхоальвеолярный лаваж, экссудат и другой патологический материал. С целью выявления лекарственной резистентности микобактерий туберкулеза используют метод абсолютных (критических) концентраций . Этот метод основан на добавлении в плотную питательную яичную среду Левенштейна-Йенсена определенных стандартных концентраций противотуберкулезных препаратов, которые принято называть предельными при расчете на мкг/мл. Недостатком этого метода является то, что результат определения устойчивости может быть получен через 2-3 месяца после взятия материала.
В крупных противотуберкулезных центрах, кроме метода абсолютных концентраций, используется метод определения лекарственной устойчивости в жидких средах с автоматизированной радиометрической и флуоресцентной системой учета роста микобактерий типа BACTEC , позволяющий сокращать сроки анализа до 2 недель.
Разрабатываются современные молекулярно-генетические методы диагностики резистентности микроорганизмов к лекарственным препаратам, которые из научно-исследовательских лабораторий переходят в арсенал практических методик. Особенно актуальным является применение методов генодиагностики для анализа резистентности у трудно культивируемых микроорганизмов, таких как Mycobacterium tuberculosis. Наиболее перспективным, быстрым и надежным методом определения лекарственной устойчивости микобактерий туберкулеза является метод биологических микрочипов , который идентифицируя мутацию сразу в нескольких генах, позволяет осуществлять своего рода генетическую паспортизацию полирезистентных штаммов микобактерий туберкулеза. Использование биологических микрочипов дало возможность однозначной идентификации этих и других мутаций, локализованных в различных клонах гроВ-гена. Метод биологических микрочипов был разработан академиком А.Д. Мизарбековым в Институте молекулярной биологии РАН им В.А. Энгельгардта. Преимуществом этого метода является возможность получения результата в первые 2-3 дня исследования, что позволяет правильно организовать лечение с первых дней выявления туберкулеза у больного.
ЛЕЧЕНИЕ ЛЕКАРСТВЕННО-УСТОЙЧИВОГО ТУБЕРКУЛЕЗА У ПОДРОСТКОВ
Лечение лекарственно-устойчивого туберкулеза вызывает определенные трудности вследствие (1) невозможности быстрого определения устойчивости микобактерий туберкулеза при использовании широко применяемых в настоящее время методик, а также (2) недостаточного количества резервных препаратов для больных с полирезистентностью микобактерий туберкулеза.
Принципы лечения лекарственно-устойчивого туберкулеза (В.И. Чуканов, 2001): ( 1 ) использование быстрых методов определения лекарственной чувствительности микобактерий туберкулеза; ( 2 ) использование в режиме химиотерапии основных противотуберкулезных препаратов, к которым сохранена чувствительность микобактерий туберкулеза; ( 3 ) введение в режим химиотерапии 2-3 резервных препарата, которые больной еще не получал; ( 4 ) соблюдение двухэтапного характера химиотерапии; ( 5 ) применение дифференцированных сроков проведения основного курса химиотерапии в зависимости от характера лекарственной резистентности микобактерий туберкулеза; ( 6 ) использование однократного (по возможности) приема суточной дозы противотуберкулезного препарата; ( 7 ) осуществление контролируемого приема всей суточной дозы противотуберкулезного препарата под непосредственным медицинским наблюдением; ( 8 ) проведение регулярного мониторинга эффективности химиотерапии по определению лекарственной резистентности один раз в месяц; ( 9 ) проведение современной коррекции режима химиотерапии после получения контрольных данных о лекарственной устойчивости микобактерий туберкулеза; ( 10 ) использование патогенетических методов лечения; ( 11 ) применение оперативных вмешательств по показаниям.
Важным является индивидуализированный режим химиотерапии с подбором препаратов для каждого больного в зависимости от данных устойчивости микобактерий туберкулеза.
Все сказанное в полной мере касается и организации лечения лекарственно-устойчивого туберкулеза у подростков. Лечение подростков, прежде всего, должно быть комплексным, с применением химиопрепаратов в условиях стационара, организацией полноценного питания, трудовой занятости больных, лечением сопутствующих заболеваний, применением патогенетических методов и др. При проведении химиотерапии выделяются две фазы лечения: (1) интенсивная фаза и (2) фаза продолжения лечения.
В период интенсивной фазы подросткам назначают 4-5 основных противотуберкулезных препаратов. По результатам контроля устойчивости (в фазу продолжения лечения) комбинацию препаратов меняют, назначают препараты, к которым чувствительность сохраняется. При полирезистентности и множественной лекарственной устойчивости , когда отмечается устойчивость к нескольким основным препаратам, назначаются резервные препараты (не менее двух).
В последние годы в практику лечения туберкулеза вошел препарат группы изоникотиновой кислоты – феназид , представляющий собой халатный комплекс двухвалентного железа и изониазида. Феназид оказался эффективным у больных туберкулезом с плохой переносимостью изониазида и наличием гипохромной анемии. Побочных реакций на ведение феназида у подростков не наблюдалось, а явления анемии исчезали через 1-2 месяца лечения. При лечении подростков с лекарственно-устойчивым туберкулезом используется также циклосерин . Его применение дает возможность повысить эффективность лечения у 63,1% больных с ранее неблагоприятной динамикой процесса. Кроме того, для лечения подростков используются искусственный пневмоторакс, пневмоперитонеум, хирургические вмешательства.
В целом процесс лечения лекарственно-устойчивого туберкулеза у подростков длителен. Интенсивная фаза составляет 3-4 месяца (используется 4-5 препаратов), фаза продолжения лечения – 8-9 месяцев (используется 3 препарата).
Заключение. Лечение лекарственно-устойчивого туберкулеза у подростков представляет большие трудности, однако правильно подобранные оптимальные схемы лечения с учетом чувствительности микобактерий туберкулеза и индивидуальный подход к больному дают возможность получить благоприятные исходы заболевания в большинстве случаев.

Туберкулез представляет серьезную угрозу здоровья населения во всем мире. В наши дни, как и в прошлые века, туберкулез остается ведущей причиной смерти среди всех инфекционных заболеваний. Примерно треть населения нашей планеты инфицирована микобактериями туберкулеза и подвержена опасности развития этого заболевания. Ежегодно в мире от туберкулеза умирает около 3 млн. человек, а каждый час – около 350 человек. В структуре социально значимых болезней ежегодно туберкулез занимает ведущее место.Россия входит в число 22 стран с высоким бременем туберкулеза и занимает 13 ранговое место по пораженности туберкулезом в мире. На прошедшем в Приморском краевом противотуберкулезном диспансере Дне Фтизиатра заведующий отделением МЛУ Валерий Иванишин озвучил актуальность проблемы и пути ее решения.
Коварный и устойчивый
В последние годы все большее внимание уделяется изучению устойчивости микобактерий туберкулеза к лекарственным противотуберкулезным препаратам. В 1999 году в официальную государственную статистику (О.Ф. №33) впервые включены сведения о множественной лекарственной устойчивости (МЛУ) микобактерий туберкулеза МБТ) к соответствующим препаратам.
- К множественной лекарственной устойчивости МБТ относят устойчивость к самым сильным противотуберкулезным препаратам- изониазиду и рифампицину, вне зависимости от наличия или отсутствия устойчивости к другим препаратам, -акцентировал Валерий Иванишин. - Больные, страдающие туберкулезом с лекарственно устойчивыми формами, наносят обществу существенный ущерб - как с позиции распространения туберкулеза с опасными для населения штаммами МБТ, так и с точки зрения опасности для самого пациента в связи с тем, что данные формы трудно поддаются лечению и чаще приводят к гибели больного.
Ключ к выздоровлению
До настоящего времени факторы и причины, способствующие увеличению лекарственной устойчивости возбудителя туберкулеза, особенно клинико-рентгенологической и микробиологической характеристик больных МЛУ туберкулезом легких остаются малоизученными. Установлено, что лекарственная устойчивость возбудителя развивается в результате одной или нескольких спонтанных мутаций в независимых генах микобактерий, которые, как правило, формируются под воздействием неадекватной лекарственной терапии.
Врач-фтизиатр не исключает, что появление, а точнее размножение лекарственно-устойчивых форм МБТ в процессе стандартной химиотерапии является следствием ослабленного иммунного надзора организма.
Ошибочно выбранный режим химиотерапии приводит к тому, что лекарственно устойчивый мутант, встречающийся в микобактериальной популяции, становится доминирующим у пациента, больного туберкулезом. Но даже при правильно назначенной противотуберкулезной терапии перерывы в лечении, временные отмены того или иного препарата, несоблюдение сроков химиотерапии способствуют формированию приобретенной устойчивости возбудителя.
- Ключом к выздоровлению является проведение длительного и полного контролируемого курса химиотерапии в стационаре, - подчеркивает Валерий Степанович. - Стационарный этап лечения является весьма важным, основополагающим для оказания лечебной помощи больным туберкулезом с МЛУ и достижения клинического излечения у них туберкулеза.
Вместе с тем, состояние многих туберкулезных стационаров находится на низком уровне. По данным Федеральной службы Роспотребнадзора, в 2007 году (более поздних сведений, к сожалению, не имеется) в капитальном ремонте в РФ нуждались 59,9% стационаров. Не соответствовали санитарным требованиям 61,8% помещений. Занижена площадь на 1 койку в 65,4% больничных учреждений РФ. Отсутствие канализации в 11,1% стационарах. Размещение посторонних служб в туберкулезных больничных помещениях было зарегистрировано в 5,6% учреждениях.
Неоптимистичная статистика
Кстати, по данным ВОЗ, за последние 14 лет показатели заболеваемости туберкулеза с МЛУ увеличились более чем в 2,5 – 3,5 раза. Это в определенной мере обусловлено как улучшением диагностики МЛУ МБТ к лекарственным препаратам, так и, главным образом, недостатками лечения.
Ежегодно лекарственная устойчивость МБТ развивается у каждого девятого больного туберкулезом в период диспансерного наблюдения и лечения.
Проведенные НИИ фтизиопульмонологии ММА им И.М. Сеченова специальные исследования показали, что туберкулез с МЛУ сокращает продолжительность жизни населения Российской Федерации в среднем на 1 год.
Среди всех состоящих на учете больных туберкулезом, больные с МЛУ составляют в РФ – 17,3 %, в Приморском крае – 33,0%. По сравнению с предыдущим годом доля этих больных увеличилась на 9,1%, и по состоянию на 01 декабря 2015 года на учете состоит 1181 больной туберкулезом с МЛУ МБТ+.
Работа на износ
Заведующий отделением МЛУ отметил, что по данным научных публикаций эффективность лечения в РФ значительно ниже, чем в большинстве государств той же Европы. Однако основными критериями излечения больных в большинстве стран является прекращение бактериовыделения МБТ методом микроскопии после краткосрочного интенсивного курса лечении, после которого наблюдение за больным прекращается. В РФ критерием клинического излечения больных туберкулезом с МЛУ является исчезновение всех признаков заболевания – клинических, рентгенологических и микробиологических. В преимущественном большинстве стран для этих целей, как правило, используются микробиологические методы без рентгенодиагностики.
С целью организации лечения больных туберкулезом с МЛУ в странах действуют разные законодательства.
Законодательная база стран для лечения больных туберкулезом с МЛУ
Обязательное лечение и изоляция
Эстония, Венгрия, Швейцария, Чехия, РФ, Норвегия
Обязательное лечение без изоляции
Обязательная изоляция больного без
принудительного лечения
Германия, Австралия, Великобритания, США,
Израиль, Нидерланды, ЮАР
Маркер состояния общества
Численность постоянного населения из года в год снижается как за счет естественной (67,3%), так и миграционной (32,7%) убыли. В основном миграционная убыль идет за счет экономически активного населения, но эмигрируют из региона и лица пенсионного возраста, так как на их пенсии не распространяются дальневосточные коэффициенты и северные надбавки.
- Туберкулез является не только производным уровня жизни населении, но и маркером состояния общества, - убежден Валерий Степанович. - Основными причинами напряженной эпидемиологической обстановки по туберкулезу с МЛУ в Приморском крае следует считать низкий уровень жизни населения, нестабильность в обществе, социальный стресс, основанный на утрате некоторыми группами населения мотивации к эффективной трудовой деятельности, А также большие миграционные процессы, рост числа социально дезадаптированных групп населения, наличие большого резервуара туберкулезной инфекции в пенитенциарных учреждениях, расположенных на территории Дальневосточного Федерального округа.
Существенное влияние на течение эпидемиологического процесса оказывает сокращение финансирования противотуберкулезных мероприятийсо снижением уровня организации противотуберкулезной помощи населению. Немаловажное значение в распространенности туберкулеза с МЛУ имеют состояние окружающей среды, географические и экологические факторы. Отрицательное влияние на течение эпидемиологического процесса туберкулеза с МЛУ оказали экономические кризисы, от которых зависит напряженность эпидемиологической обстановки как в Российской Федерации, так и в Приморском крае.
Болезнь среднего возраста
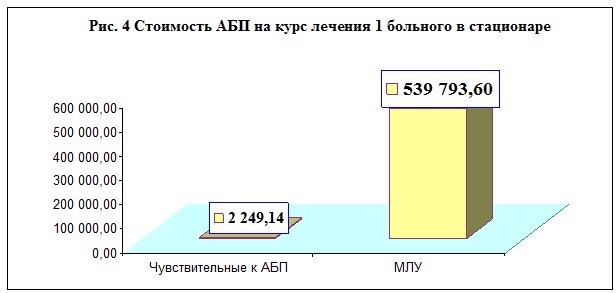
Стоимость медикаментов на лечение 1 больного с чувствительной формой туберкулеза составляет 25,46 руб. в день, на полный курс в 90 доз АБП – 2 249,14 руб., а больного туберкулезом с МЛУ – 1 325,26 руб. в день, и на полный курс стационарного лечения в 240 доз – 539 793,60 руб.(по ценам на 1 марта 2015 года).
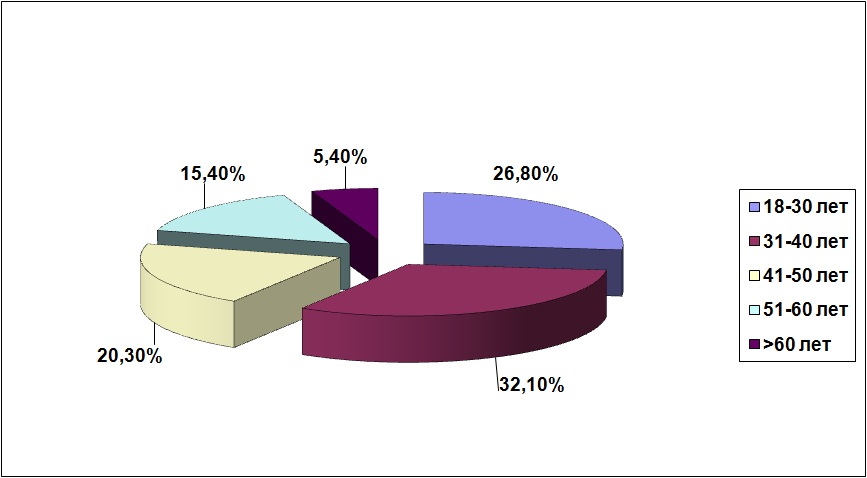
Наибольший процент (32,1%) больных туберкулезом МЛУ в Приморском крае составляет возрастная группа от 31 до 40 лет. Наименьший процент (5,4%) – люди старше 60 лет.
- Наши данные совпадают с отчетом Всемирной организации здравоохранения 2014 года, согласно которому возрастная группа от 31 до 40 лет больных МЛУ составляет 34%, старше 60 лет – 5%, - пояснил врач-фтизиатр. - Больные туберкулезом с МЛУ чаще всего страдают хроническим вирусным гепатитом С – 30,5%, хронической обструктивной болезнью легких (ХОБЛ) – 24,9%, сахарным диабетом – 13,1%. Данная сопутствующая патология характерна для молодого и среднего возраста, длительно злоупотребляющих курением, алкоголем и наркотиками. Больные сахарным диабетом относятся к группе высокой степени риска по туберкулезу.
Больные туберкулезом с МЛУ в стационаре получают лечение по 4 режиму химиотерапии (РХТ) по стандарту шестью противотуберкулезными препаратами: препаратом первого ряда – пиразинамид и препаратами второго (резервного ряда) каприомицин, циклосерин, левофлоксацин, протионамид, ПАСК. Стационарный этап лечения составляет 240 принятых доз АБП (240) дней.
Среди всех больных туберкулезом с МЛУ, получавших лечение по 4 РХТ наибольший процент занимает инфильтративный туберкулез – 77,2%, меньше всего 2,6% составляет очаговый туберкулез. Фиброзно-кавернозный – 6,6%. Эффективность лечения в стационаре высокая - абациллирование – 80,8% (по РФ – 80%), закрытие полостей распада – 62,1 (по РФ – 70%)
В 2014 году в отделении умерло 4 больных (в 2013г. – три, и в 2012г. – три). Основной причиной смерти больных туберкулезом с МЛУ является ВИЧ-инфекция – 80%, лица молодого возраста, до 30 лет. 20% больных старше 60 лет умерли от ишемической болезни сердца.
- После завершения интенсивной фазы лечения в стационаре больные выписываются на амбулаторное лечение, на фазу продолжения, это всего лишь половина больных – 52,3%, уточняет Валерий Иванишин. - На оперативное лечение переводятся пациенты, у которых не закрылись полости деструкции, это 19,6%. Самовольно уходят из отделения или выписываются за нарушение режима, тем самым прерывают лечение 28,1% (по РФ – 25% не привержены к лечению).
Основная задача – контроль над эпидситуацией
В Приморском крае сохраняется напряженная эпидемиологическая ситуация по туберкулезу. Основные статистические показатели превышают средний уровень по РФ в 1,5-2 раза. Ситуация усугубляется нарастанием туберкулеза с множественной лекарственной устойчивостью, формирующейся у больных как следствие неадекватного лечения.
Главной задачей сегодняшнего дня является установление контроля над развитием эпидемиологической ситуации по туберкулезу с МЛУ в Приморском крае. Реальныйнадзор над эпидобстановкой обусловлен следующими положениями:
- источником инфекции является в основном больной туберкулезом, которого можно достаточно легко вылечить;
- эффективное лечение заболевания в условиях стационара напрямую снижает распространение туберкулезной инфекции;
- при уменьшении числа источников инфекции эпидемиологическая ситуация улучшается;
- современные, эффективные препараты для лечения туберкулеза обеспечивают успешную терапию.
- Что нужно делать, чтобы не заболеть туберкулезом с МЛУ. Ответ очень простой – вести здоровый образ жизни, хорошо питаться и ежегодно проходить флюорографическое обследование, - заключил Валерий Иванишин.

Лекарственная устойчивость микобактерий туберкулеза – современные взгляды на проблему
Российская Федерация относится к числу стран с высоким уровнем заболеваемости туберкулезом, хотя с 2003 года стала отмечаться некоторая тенденция к стабилизации эпидемической ситуации. Наиболее неблагополучной по туберкулезу была в 1999 году территория Западной Сибири, где показатели заболеваемости занимали первое место среди всех субъектов России. Неуклонный рост показателей заболеваемости туберкулезом представляет значительную угрозу для общества.
Однако еще более серьезной для современной фтизиатрии является проблема лекарственной устойчивости (ЛУ) возбудителя туберкулеза, поскольку является одним из факторов, ограничивающих эффективность антибактериальной терапии. Лекарственная устойчивость — природная или приобретенная способность возбудителя заболевания сохранять жизнедеятельность при воздействии на него лекарственных препаратов.
Согласно классификации ВОЗ (1998), микобактерии туберкулеза (МБТ) могут быть:
- монорезистентные — устойчивые к одному противотуберкулезному препарату;
- полирезистентные — к двум и более противотуберкулезным препаратам (ПТП);
- множественно лекарственно резистентные — устойчивые как минимум к сочетанию изониазида и рифампицина, независимо от наличия или отсутствия устойчивости к другим ПТП.
Вопрос скрытой лекарственной устойчивости требует дальнейшего изучения. Достоверная идентификация этого вида лекарственной устойчивости возможна лишь при микробиологическом исследовании каверн, т.к. при бактериологическом исследовании мокроты у данных больных обнаруживают лекарственно-чувствительные МБТ. Последний вид лекарственной устойчивости, встречается довольно редко. В настоящее время, когда для лечения применяется много новых резервных препаратов, необходимо помнить о наличии перекрестной лекарственной устойчивости.
Появление первых антибиотико-резистентных штаммов микобактерий туберкулеза (МБТ) связывают с открытием в 1943 г. и широким применением стрептомицина как эффективного противотуберкулезного препарата. Уже первые системные данные о распространенности первичной лекарственной устойчивости к изониазиду и стрептомицину были получены в 50-е годы за рубежом при проведении эпидемиологических исследований. Были выделены страны с высоким до 9,4% (Япония и Индия) и низким — от 0,6 до 2,8% (США и Великобритания) уровнем лекарственной устойчивости к этим двум препаратам. При этом показатели устойчивости к стрептомицину были несколько выше устойчивости к изониазиду.
В России подобные исследования по изучению уровня лекарственной устойчивости к стрептомицину, ПАСК, препаратам группы ГИНК стали проводиться с середины 50-х годов Центральным НИИ туберкулеза. Полученные за шестилетний период (1956-1963 гг.) данные свидетельствовали об изменении за этот период структуры лекарственной устойчивости в сторону уменьшения штаммов МБТ, устойчивых к стрептомицину, и увеличения доли резистентности к препаратам группы ГИНК, а так же к 2 и 3 препаратам одновременно.
Открытие и внедрение в практику новых противотуберкулезных препаратов (в 50-х годах — препараты группы ГИНК, пиразинамид, циклосерин, этионамид, канамицин и каприомицин; в 60-х — рифампицин и этамбутол; в 80-х — препараты группы фторхинолонов), а так же использование схем химиотерапии, включающих одновременное применение 4-5 ПТП, позволяло хотя бы временно решать проблему лекарственной устойчивости. Возможно, поэтому до конца 80-х годов суммарные показатели лекарственной устойчивости в России сохранялись на относительно невысоком уровне, а ее колебания были незначительными.
Анализ данных лекарственной устойчивости к стрептомицину, изониазиду, рифампицину и этамбутолу (1991-2001 гг.), проводимый на Северо-Западе России, показал, что уровень устойчивости к последнему за этот период вырос более чем в 2 раза, хотя и продолжает оставаться ниже по сравнению с остальными препаратами. Уровень устойчивости к рифампицину лишь немногим уступает устойчивости изониазиду, а частая ассоциация лекарственной устойчивости этих двух препаратов делает рифампицин маркером множественной лекарственной устойчивости (МЛУ).
Являясь одним из основных препаратов, воздействующих на активно размножающуюся фракцию МБТ, рифампицин входит в состав всех схем химиотерапии, применяемых для лечения вновь выявленных больных активным туберкулезом, что делает особенно актуальной проблему мультирезистентности. Обсуждаются тревожные данные о вспышках мультирезистентного туберкулеза в тесных коллективах. С увеличением МЛУ связывают рост смертности от туберкулеза в мире. Наряду с этим имеются сведения о том, что больные, выделяющие микобактерии, устойчивые к изониазиду и рифампицину, являются менее заразными, чем другие пациенты.
Рост общей частоты лекарственной устойчивости, наблюдаемый при всех локализациях туберкулеза, сопровождается значительным утяжелением ее структуры за счет снижения монорезистентности и увеличения количества полирезистентных форм. Показатели лекарственной устойчивости МБТ распределены неравномерно по всей территории России и колеблются в достаточно широком диапазоне. Уже с конца 90-х годов отмечено отчетливое увеличение удельного веса показателя первичной лекарственной устойчивости от 18 до 61% по различным регионам России, показатели же вторичной лекарственной устойчивости практически повсеместно превышают 50-70, достигая в отдельных областях до 80-86%. Резистентность МБТ к основным препаратам более характерна для впервые выявленных больных с ограниченной распространенностью процесса. Развитие резистентности МБТ к сочетанию основных и резервных препаратов — для рецидивов и хронического течения туберкулеза легких.
Частота встречаемости МЛУ у вновь выявленных больных являются невысокой (2-10%), поэтому не может оказывать серьезного влияния на основные эпидемиологические показатели по туберкулезу. Большее эпидемиологическое значение имеет вторичная резистентность. Воздействие противотуберкулезных средств рано или поздно приводит к созданию популяции высокоустойчивых к лекарственному воздействию бактерий. Существует достаточно большая вероятность того, что массивное лекарственное воздействие не приводит к полной элиминации патогена из организма человека, а является дополнительным фактором его направленной эволюции.
Причины формирования лекарственной устойчивости различны. В индустриально развитых странах это может быть связано с врачебными ошибками при разработке схем лечения; в слаборазвитых — с недостатком финансирования и применением менее эффективных, более дешевых лекарственных препаратов. Группами риска по формированию лекарственно-устойчивого туберкулеза являются больные, нарушающие режим лечения и прерывающие основной курс лечения самовольно, либо по причине аллергических или токсических осложнений; злоупотребляющие алкоголем, наркотическими средствами; лица, контактирующие с больным туберкулезом, выделяющим лекарственно-устойчивые МБТ.
Лекарственная устойчивость формируется в результате одной или нескольких спонтанных мутаций в независимых генах МБТ, происходящих преимущественно при применении неадекватных схем химиотерапии. Эмпирическое назначение стандартной комбинации химиопрепаратов при наличии первичной лекарственной устойчивости, с последующей их заменой, а также прерывистые курсы терапии приводят к накоплению мутаций и являются основной причиной развития мультирезистентности.
Подобные мутации могут встречаться в микобактериальной популяции еще до контакта МБТ с противотуберкулезными препаратами. Частота возникновения спонтанных мутаций природных штаммов МБТ, влекущих за собой развитие лекарственной устойчивости к антибактериальным препаратам, вариабельна. В литературе описывается феномен кросс-резистентнтности — состояния, при котором наблюдается лекарственная устойчивость, генетически обусловленная к нескольким препаратам одновременно. Кросс-резистентность характерна для изониазида и этионамида, рифампицина и его производных, а также стрептомицина, канамицина, амикацина. Бурное развитие молекулярной генетики, наблюдаемое в последние годы, открыло возможности для изучения генов МБТ, контролирующих лекарственную устойчивость и механизмов ее развития. Наиболее полно изучены гены и механизмы формирования лекарственной устойчивости к препаратам первого ряда.
Устойчивость к изониазиду кодируется несколькими генами: kat G — осуществляет контроль клеточной каталазно-пероксидазной активности; inh A — контроль синтеза миколитических кислот; kas A — контроль протеиновых взаимодействий. Устойчивость к рифампицину связывают с единственным геном rpo B, контролирующим процесс транскрипции (синтеза РНК). Rps L и rrs — гены, кодирующие процессы трансляции и связанные с синтезом клеточного белка. Мутации в этих генах являются ключевыми при формировании устойчивости к стрептомицину и канамицину. Устойчивость к этамбутолу кодируется геном emb B, контролирующим процесс нормального построения клеточной стенки при конверсии глюкозы в моносахариды. Ген pcn A — отвечает за работу фермента энзимпиразимидазы, который осуществляет трансформацию пиразинамида в активный комплекс (пиразинодоновую кислоту).
Попадая в организм, препарат или его метаболиты вмешиваются в цикл работы микобактериальной клетки, нарушая ее нормальную жизнедеятельность. В результате приобретения клеткой генов лекарственной устойчивости метаболиты препарата становятся неактивными по отношению к своим мишеням, что и приводит к развитию картины лекарственно-устойчивого туберкулеза.
Влияние характера лекарственной резистентности на течение и исход заболевания является несомненным. Остро текущие формы туберкулеза легких в большинстве случаев развиваются на фоне множественной лекарственной устойчивости и сопровождаются большой распространенностью специфического и неспецифического воспаления в легочной ткани, отставанием темпов репарации очагов поражения и значительными нарушениями в иммунном статусе. Наличие резистентности к 1-2 препаратам практически не отражается на результатах лечения. Устойчивость к 3 и более препаратам, а особенно МЛУ, затрудняет процесс лечения и снижает его эффективность. Это выражается в замедлении темпов негативации мокроты, рассасывания инфильтративных и ликвидации деструктивных изменений, в связи с чем, наблюдается большая нуждаемость в хирургическом лечении.
Проблема повышения эффективности профилактических мероприятий, для предотвращения заражения лекарственно-устойчивым туберкулезом вызывает широкий интерес. Заболеваемость туберкулезом контактных лиц в семьях больных, выделяющих лекарственно-устойчивые штаммы МБТ, в 2 раза выше по сравнению с заболеваемостью контактов в семьях бактериовыделителей лекарственно-чувствительных МБТ.
Предпринимаются попытки совершенствования профилактических и лечебных мероприятий. Подтверждено совпадение спектра лекарственной устойчивости МБТ заболевших из контакта детей и взрослых с источником инфекции. Предпринимаются попытки разработки модели больного с лекарственно-устойчивым туберкулезом легких. Получен тренд линейности между возрастом и резистентностью. Дальнейшее изучение проблемы лекарственной устойчивости создает перспективные возможности для ограничения туберкулезной инфекции.
Читайте также:


