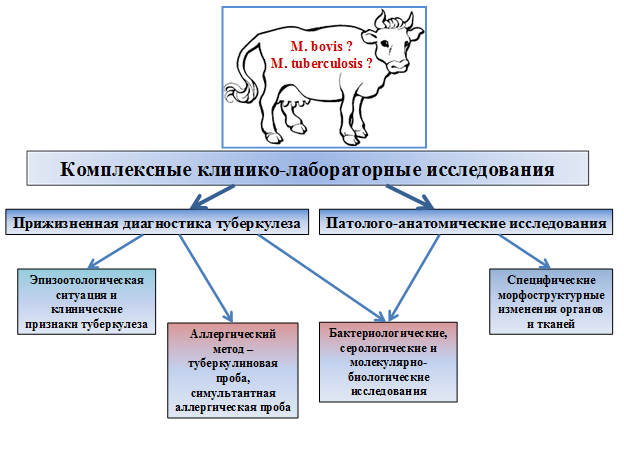
Взятие крови на туберкулез у крс
Рекомендации
по правилам взятия проб крови от крупного рогатого скота
Условия взятия крови и ее сохранность до начала лабораторных исследований имеют важное значение при получении достоверных результатов. Во многом эти результаты зависят от техники взятия крови и используемых при этой инструментов.
При венепункции прокол окружающих вену тканей и стенки вен делают в один прием.
На результаты лабораторных исследований могут влиять факторы, связанные с индивидуальными особенностями и физиологическим состоянием организма животного, такие как: возраст; эмоциональное состояние и психический стресс; климатические и метеорологические условия и др.
Брать кровь надо по возможности утром, до кормления животных.
Рекомендуется произвести дегельминтизацию животных за 2 недели до взятия крови.
В целях отсутствия получения ложно-положительных результатов исследований рекомендуют брать кровь не позднее, чем за три недели до отела и не ранее чем через 3 недели после отела.
На точность и правильность результатов также оказывает влияние техника взятия крови, используемые при этом инструменты (иглы, шприцы и др.), пробирки, в которые берется, а в последующем хранится и транспортируется кровь, а также условия хранения и подготовки пробы к анализу.
Традиционные и широко используемые в настоящее время способы взятия крови с помощью иглы и/или шприца оказываются основными источниками лабораторных ошибок, приводящих к низкому качеству результатов анализов. Кроме того, эти методы не могут быть стандартизованы и не обеспечивают безопасность персонала, берущего кровь.
При взятии проб венозной крови методом самотека с использованием иглы и обычных пробирок высока вероятность попадания крови животного на руки ветеринарного специалиста. В этом случае руки ветеринарного работника могут стать источником передачи и распространения возбудителей гемоконтактных инфекций другому животному путем контаминации кровью инъекционной ранки. Ветеринарный работник сам может заразиться от источника инфекции.
Использование медицинского шприца с иглой для взятия крови следует также избегать из-за его недостаточной безопасности для ветеринарного персонала и невозможности исключения гемолиза крови при переносе пробы под давлением в пробирку.
Взятие крови с использованием вакуум-содержащих систем:
Для взятия проб венозной крови наиболее предпочтительно использовать вакуум-содержащие системы. Этот способ имеет ряд преимуществ, основным из которых является то, что кровь попадает непосредственно в закрытую пробирку, предотвращающую любой контакт ветперсонала с кровью животного.
Речь идёт не только об упрощении процедуры взятия крови, что само по себе немаловажно, но и о значительном снижении процента преаналитических ошибок, увеличении безопасности процедуры, снижении риска заражения скота, сохранения уровня надоев после процедуры и отсутствия осложнений у животных после взятия крови.
Вакуум-содержащая система представляет собой закрытую двухкомпонентную систему - вакуумный шприц-контейнер и специальную иглу. Выделение сыворотки или соединение крови с антикоагулянтом происходит в том же объёме шприца, в который берётся кровь, то есть после взятия крови сам шприц является транспортной пробиркой с антикоагулянтом или сывороткой.
Под действием вакуума кровь втягивается через иглу вакуумной системы напрямую из вены в пробирку и сразу же смешивается с химическим реактивом. Тщательно дозированный объем вакуума обеспечивает точное соотношение кровь/реагент в пробирке.
На основе возможностей вакуум-содержащихх систем был разработан новый метод взятия крови у крупного рогатого скота из хвостовой вены:
- Кровь берут из v .с occygea (хвостовая вена).
- Для взятия крови животное не фиксируют.
- Хвост животного берут рукой в области средней трети и медленно поднимают вверх.
- Место взятия крови, область 2-5 хвостовых позвонков, дезинфицируют спиртом или 5% раствором йода.
- Кровь берут в средней трети тела 2-5 хвостовых позвонков, находящейся на линии, идущей вдоль хвоста и делящей его на 2 симметричные части.
- Иглу вводят под углом 90° до упора на глубину 5-10 мм.
| Неспецифическая реакция | Фактор, обуславливающий проявление неспецифической реакции | Особенности неспецифической реакции |
|---|---|---|
| Парааллергическая | Атипичные (нетуберкулезные) виды микобактерий и их ассоциации.
Mycobacterium tuberculosis (микобактерии туберкулеза человека). Mycobacterium avium (микобактерии туберкулеза птичьего) | Непостоянство реакции на туберкулин.
Сенсибилизация организма животного сохраняется от 1 до 3 месяцев после инфицирования [5]. Выявление наибольшего количества животных с выраженными реакциями на КАМ |
| Псевдоаллергическая | Наличие гельминтов (фасциол, дикроцелий, эхинококков). Актиномикоз. Микологические поражения легких. Гнойные или гнойно-некротические процессы во внутренних органах. Нарушения обмена веществ | В благополучных по туберкулезу стадах у отдельных животных регистрируется увеличение толщины кожной складки на месте введения туберкулина на 3–4 мм, признаки воспаления отсутствуют |
Лабораторные методы диагностики туберкулеза КРС
К лабораторным методам диагностики туберкулеза относятся бакте-риологическое исследование, серологическое исследование и молеку-лярно-биологическое исследование.
Бактериологическое исследование проводится с целью выделения возбудителя туберкулеза (рис. 4).
Отбор проб биоматериалов для бактериологического исследования производят как от животных с клиническими признаками туберкулеза, так и от животных, вызывающих подозрение на туберкулез. Исследуют молоко, мокроту, мочу. От павших и убитых животных для исследования отбирают пораженные участки органов на границе со здоровой тканью и измененные лимфатические уз-лы.
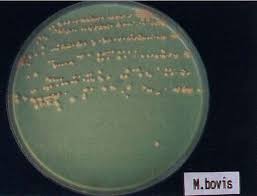
Рис. 4. Культура Mycobacterium bovis. Среда роста Гельберга [10]
При наличии характерных для туберкулеза изменений исследуются портальные, предлопаточные, надвыменные, поверхностные паховые лимфатические узлы и фрагменты внутренних органов – легких, печени, почек.
Бактериологическое исследование биоматериалов на туберкулез за-нимает срок до 3 месяцев. Заболевание животных туберкулезом считается установленным в случаях выделения микобактерий туберкулеза бычьего или человеческого из материала от убитых животных [3, 4, 8].
Серологическое исследование на туберкулез проводится в реакции связывания комплемента (РСК).
РСК применяется в двух вариантах:
1) для обнаружения в сыворотке больного животного специфических антител к возбудителю туберкулеза;
2) для выявления и идентификации в исследуемом материале антигена возбудителя туберкулеза.
Молекулярно-биологическое исследование на туберкулез.
Полимеразная цепная реакция (ПЦР) является одним из высокочувствительных и специфичных методов диагностики туберкулеза. Чувствительность метода ПЦР – от 10 до 100 микроорганизмов в пробе (чувствительность микроскопического метода – от 103 до 105 микроорганизмов). В основе метода лежит амплификация специфических участков ДНК возбудителя, которые содержатся в исследуемой пробе. В настоящее время в лабораторной практике применяются тест-системы как для выявления ДНК конкретного вида, так и для дифференцирования видов, входящих в Mycobacterium tuberculosis complex: микобактерий человеческого вида (M. tuberculosis), бычьего вида (M. bovis) и вакцинного штамма микобактерий бычьего вида (M. bovis BCG). Для проведения анализа используют следующие образцы биопроб от крупного рогатого скота: цельную кровь, молоко, фарингеальные смывы, мочу, фекалии, носовую слизь и биопсийные материалы, в том числе лимфатические узлы [3].
Молекулярно-биологическое исследование позволяет значительно ускорить раннюю диагностику туберкулеза, дифференцировать пара- и псевдоаллергические реакции на туберкулин, снизить количество подозреваемых в заражении туберкулезом и подвергаемых диагностическому убою животных [4, 5].
Патолого-анатомические исследования
Для убоя с диагностической целью отбирают животных по результатам вышеизложенных методов исследования.
Патолого-анатомические изменения в организме больного туберкулезом животного зависят как от его возраста, так и от стадии инфекционного процесса.
В начальных стадиях инфекционного процесса туберкулы имеют вид серых полупрозрачных узелков размером от булавочной головки до чечевичного зерна. Затем они становятся мутными, приобретают бело-желтый цвет, заполняются некротизированной сухой творожистой массой. В легких туберкулезные очаги поражения чаще выделяются над плеврой по тупому краю органа (рис. 5).
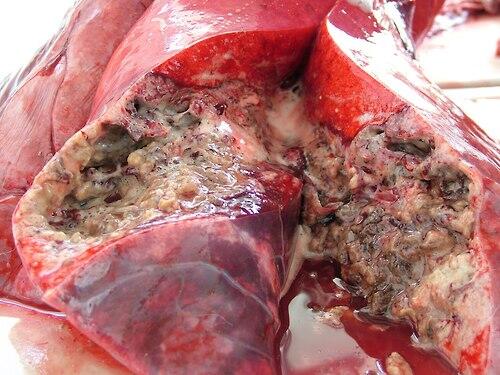
Рис. 5. Легкое крупного рогатого скота при туберкулезном поражении тканей [9]
Гистологические исследования проводят для дифференциации туберкулезных патолого-анатомических изменений от сходных изменений, наблюдаемых при других заболеваниях, например для дифференциации от гранулем паразитарного и микотического происхождения. В положительных случаях в гистологических препаратах, окрашенных по Цилю – Нильсену, находят гранулемы с некротизированным центром, окруженные зоной эпителоидных, отдельных гигантских лимфоидных клеток и соединительно-тканной капсулой.
Вместо заключения
Осуществление плановых профилактических диагностических иссле-дований на туберкулез способствует снижению риска инфицирования людей туберкулезом, ограничению распространения возбудителя из очагов инфекции, раннему выявлению неблагополучных по туберкулезу населенных пунктов.
Читайте также:
- Кто ввел термин туберкулез
- В понятие очага туберкулезной инфекции следует включить
- Почему больному туберкулезом противопоказаны физические нагрузки
- Чем опасен туберкулез презентация
- Что такое кубы при туберкулезе