Гепатит с вектор бест 0772

Новые наборы для экспресс-диагностики геморрагической лихорадки с почечным синдромом Ханта-IgМ-экспресс-БЕСТ и Ханта-IgG-экспресс-БЕСТ more
ID] => 2321 [TIMESTAMP_X] => 18.06.2019 09:49:14 [
TIMESTAMP_X] => 18.06.2019 09:49:14 [MODIFIED_BY] => 9321 [
MODIFIED_BY] => 9321 [DATE_CREATE] => 18.06.2019 09:49:14 [
DATE_CREATE] => 18.06.2019 09:49:14 [CREATED_BY] => 9321 [
CREATED_BY] => 9321 [IBLOCK_ID] => 17 [
IBLOCK_ID] => 17 [IBLOCK_SECTION_ID] => 2318 [
IBLOCK_SECTION_ID] => 2318 [ACTIVE] => Y [
ACTIVE] => Y [GLOBAL_ACTIVE] => Y [
GLOBAL_ACTIVE] => Y [SORT] => 600 [
SORT] => 600 [NAME] => Гепатит C [
NAME] => Гепатит C [PICTURE] => [
PICTURE] => [LEFT_MARGIN] => 9 [
LEFT_MARGIN] => 9 [RIGHT_MARGIN] => 10 [
RIGHT_MARGIN] => 10 [DEPTH_LEVEL] => 3 [
DEPTH_LEVEL] => 3 [DESCRIPTION] => [
DESCRIPTION] => [DESCRIPTION_TYPE] => text [
DESCRIPTION_TYPE] => text [SEARCHABLE_CONTENT] => ГЕПАТИТ C [
SEARCHABLE_CONTENT] => ГЕПАТИТ C [CODE] => [
SOCNET_GROUP_ID] => [LIST_PAGE_URL] => /prod/index.php [
LIST_PAGE_URL] => /prod/index.php [SECTION_PAGE_URL] => /prod/index.php?SECTION_ID=2321 [
SECTION_PAGE_URL] => /prod/index.php?SECTION_ID=2321 [IBLOCK_TYPE_ID] => products [
IBLOCK_TYPE_ID] => products [IBLOCK_CODE] => catalog [
IBLOCK_CODE] => catalog [IBLOCK_EXTERNAL_ID] => [
EXTERNAL_ID] => [IPROPERTY_VALUES] => Array ( ) [PATH] => Array ( [0] => Array ( [ID] => 2316 [
ID] => 2316 [CODE] => root_ifa [
CODE] => root_ifa [XML_ID] => [
EXTERNAL_ID] => [IBLOCK_ID] => 17 [
IBLOCK_ID] => 17 [IBLOCK_SECTION_ID] => [
IBLOCK_SECTION_ID] => [SORT] => 100 [
SORT] => 100 [NAME] => Иммуноферментная диагностика [
NAME] => Иммуноферментная диагностика [ACTIVE] => Y [
ACTIVE] => Y [DEPTH_LEVEL] => 1 [
DEPTH_LEVEL] => 1 [SECTION_PAGE_URL] => /prod/index.php?SECTION_ID=2316 [
SECTION_PAGE_URL] => /prod/index.php?SECTION_ID=2316 [IBLOCK_TYPE_ID] => products [
IBLOCK_TYPE_ID] => products [IBLOCK_CODE] => catalog [
IBLOCK_CODE] => catalog [IBLOCK_EXTERNAL_ID] => [
IBLOCK_EXTERNAL_ID] => [GLOBAL_ACTIVE] => Y [
GLOBAL_ACTIVE] => Y [IPROPERTY_VALUES] => Array ( ) ) [1] => Array ( [ID] => 2318 [
EXTERNAL_ID] => [IBLOCK_ID] => 17 [
IBLOCK_ID] => 17 [IBLOCK_SECTION_ID] => 2316 [
IBLOCK_SECTION_ID] => 2316 [SORT] => 300 [
SORT] => 300 [NAME] => Вирусные гепатиты [
NAME] => Вирусные гепатиты [ACTIVE] => Y [
ACTIVE] => Y [DEPTH_LEVEL] => 2 [
DEPTH_LEVEL] => 2 [SECTION_PAGE_URL] => /prod/index.php?SECTION_ID=2318 [
SECTION_PAGE_URL] => /prod/index.php?SECTION_ID=2318 [IBLOCK_TYPE_ID] => products [
IBLOCK_TYPE_ID] => products [IBLOCK_CODE] => catalog [
IBLOCK_CODE] => catalog [IBLOCK_EXTERNAL_ID] => [
IBLOCK_EXTERNAL_ID] => [GLOBAL_ACTIVE] => Y [
GLOBAL_ACTIVE] => Y [IPROPERTY_VALUES] => Array ( ) ) [2] => Array ( [ID] => 2321 [
EXTERNAL_ID] => [IBLOCK_ID] => 17 [
IBLOCK_ID] => 17 [IBLOCK_SECTION_ID] => 2318 [
IBLOCK_SECTION_ID] => 2318 [SORT] => 600 [
SORT] => 600 [NAME] => Гепатит C [
NAME] => Гепатит C [ACTIVE] => Y [
ACTIVE] => Y [DEPTH_LEVEL] => 3 [
DEPTH_LEVEL] => 3 [SECTION_PAGE_URL] => /prod/index.php?SECTION_ID=2321 [
SECTION_PAGE_URL] => /prod/index.php?SECTION_ID=2321 [IBLOCK_TYPE_ID] => products [
IBLOCK_TYPE_ID] => products [IBLOCK_CODE] => catalog [
IBLOCK_CODE] => catalog [IBLOCK_EXTERNAL_ID] => [
IBLOCK_EXTERNAL_ID] => [GLOBAL_ACTIVE] => Y [
GLOBAL_ACTIVE] => Y [IPROPERTY_VALUES] => Array ( ) ) ) ) [SECTIONS_COUNT] => 0 )
| № по каталогу | Наименование и краткое описание | Количество определений | ||||
|---|---|---|---|---|---|---|
| D-0760 |
Набор реагентов для иммуноферментного выявления иммуноглобулинов класса М к вирусу гепатита С. | 12x8 | ||||
| D-0770 | 24x8 | |||||
| D-0749 | 12х8 | |||||
| D-0771 | 2x96 | |||||
| D-0772 | 12x8 | |||||
| D-0773 | 24x8 | |||||
| D-0775 | 60x8 | |||||
| D-0774 | 6x4 | |||||
| D-0776 | 12x4 | |||||
| D-0777 | 12x8 | |||||
| D-0778 | 24x8 | |||||
| D-0779 | 12x8 | |||||
| D-0712 | 20 | |||||
| D-0738 | 24 флакона по 0,5 мл | |||||
| D-0740 | 6 образцов по 0,4 мл | |||||
| D-0741 |
| № по каталогу | Наименование и краткое описание | Количество определений |
|---|---|---|
| 24 флакона по 0,5 мл | ||
| 6 образцов по 0,4 мл | ||
| 24 образца по 0,5 мл |
D-0542
HBsAg-ИФА-БЕСТ (комплект 1/авто)
D-0543
HBsAg-ИФА-БЕСТ (комплект №2)
D-0544
HBsAg-ИФА-БЕСТ (комплект №3)
Набор реагентов для иммуноферментного выявления HBs-антигена вируса гепатита В.
Чувствительность: 0,01 МЕ/мл (нг/мл)
Срок годности: 12 месяцев
D-0546
Набор реагентов для иммуноферментного подтверждения присутствия HBs-антигена вируса гепатита В.
Чувствительность: 0,01 МЕ/мл (нг/мл)
Срок годности: 12 месяцев
D-0560
Вектогеп B-HBs-антиген-авто (комплект 1)
D-0549
Вектогеп B-HBs-антиген-авто (комплект 2/Чароит)
Набор реагентов для иммуноферментного выявления HBsAg для автоматических ИФА анализаторов.
D-0555
Вектогеп B-HBs-антиген (комплект 1)
D-0557
Вектогеп B-HBs-антиген (комплект 2)
D-0556
Вектогеп B-HBs-антиген (комплект 3)
D-0559
Вектогеп B-HBs-антиген (комплект 4)
Набор реагентов для иммуноферментного выявления HBsAg. Одностадийная постановка.
Чувствительность: 0,05/0,01 МЕ/мл
Срок годности: 24 месяцев
D-0558
Вектогеп В-HBs-антиген-подтверждающий тест (комплект 1)
D-0548
Вектогеп В-HBs-антиген-подтверждающий тест (комплект 2)
Набор реагентов для иммуноферментного подтверждения наличия HBsAg. Одностадийная постановка.
Чувствительность: 0,05/0,01 МЕ/мл
Срок годности: 24 месяцев
D-0582
Вектогеп B-HBs-антиген-2 (комплект 1/авто)
D-0583
Вектогеп B-HBs-антиген-2 (комплект 2)
D-0584
Вектогеп B-HBs-антиген-2 (комплект 3)
Набор реагентов для иммуноферментного выявления HBsAg. Двухстадийная постановка.
Чувствительность: 0,05 МЕ/мл (нг/мл)
Срок годности: 12 месяцев
D-0586
Вектогеп B-HBs-антиген-2-подтверждающий тест
Набор реагентов для иммуноферментного подтверждения выявления HBsAg.
Чувствительность: 0,05 МЕ/мл (нг/мл)
Срок годности: 12 месяцев
D-0545
Набор реагентов для иммуноферментного количественного определения HBs-антигена вируса гепатита В в сыворотке (плазме) крови
.
Чувствительность: 0,05 МЕ/мл (нг/мл)
Диапазон измерений: 0 — 10 МЕ/мл (нг/мг)
D-0562
Набор реагентов для иммуноферментного качественного и количественного определения антител к HBs-антигену вируса гепатита В в сыворотке (плазме) крови.
D-0564
Набор реагентов для иммуноферментного выявления иммуноглобулинов класса М к core-антигену вируса гепатита В.
D-0566
Набор реагентов для иммуноферментного выявления суммарных антител к core-антигену вируса гепатита В.
D-0574
Набор реагентов для иммуноферментного выявления иммуноглобулинов класса G к core-антигену вируса гепатита В в сыворотке (плазме) крови.
D-0576
Набор реагентов для иммуноферментного выявления E-антигена вируса гепатита В в сыворотке (плазме) крови.
D-0578
Набор реагентов для иммуноферментного выявления иммуноглобулинов класса G к HВe-антигену вируса гепатита В.
D-0538
D-0540
HBsAg-стандартная панель сывороток
Набор образцов сывороток крови, содержащих разные субтипы и мутантные формы HBsAg вируса гепатита В.
Аннотация научной статьи по клинической медицине, автор научной работы — Кудрявцева Е.Н., Корабельникова М.И., Красавченко К.С., Ястребова О.Н., Туманова О.Ю.
Проведено исследование по изучению диагностической значимости определения в ИФА core-антигена ВГС среди различных групп пациентов и лиц высокого риска инфицирования ВГС. Показано, что ни в одном случае у 363 пациентов, госпитализированных в отделения терапевтического и хирургического профиля крупного многопрофильного стационара, core-антиген ВГС обнаружить не удалось. Высказана точка зрения о нецелесообразности внедрения детекции core-антигена ВГС в систему скрининговых исследований пациентов, направляемых на госпитализацию в стационары неинфекционного профиля. Из 326 пациентов (код 120) у 4 (1,2%) доказано посредством определения РНК ВГС наличие гепатита С, единственным серологическим свидетельством которого был core-антиген ВГС . Обсуждается целесообразность проведения исследований по определению core-антигена ВГС среди лиц, обследуемых на наличие ВИЧ-инфекции по эпидемиологическим показаниям.
Похожие темы научных работ по клинической медицине , автор научной работы — Кудрявцева Е.Н., Корабельникова М.И., Красавченко К.С., Ястребова О.Н., Туманова О.Ю.
Diagnostic Importance of HCV Core-Antigen Detection
Research of the diagnostic importance of HCV core-antigen detection in immune-enzyme analysis among patients and high risk groups was carried out. It was revealed that HCV core-antigen was absent in all 363 patients from therapeutic and surgical branches of a large hospital. It was made an assumption that HCV core-antigen detection is unreasonable for screening in patients admitted to a noninfectious hospital. Hepatitis C was diagnosed in 4 (1.2%) from 326 patients (code 120) by means of HCV RNA detection. HCV core-antigen presence was the single serological marker of HCV-infection. The reasonability of HCV core-antigen detection among the persons examined for HIV-infection presence is discussed.
О диагностической значимости определения core-антигена вируса гепатита с
Е.Н. Кудрявцева1, М.И. Корабельникова1, К.С. Красавченко1, О.Н. Ястребова2, О.Ю. Туманова2, Е.И. Лебедева2, Л.Е. Кузина1, В.Я. Кицак1, А.С. Калашникова1, Т.А. Семененко3 (semenenko@gamaleya.org), С.Н. Кузин1, 3 (drkuzin@list.ru)
Проведено исследование по изучению диагностической значимости определения в ИФА core-антигена ВГС среди различных групп пациентов и лиц высокого риска инфицирования ВГС. Показано, что ни в одном случае у 363 пациентов, госпитализированных в отделения терапевтического и хирургического профиля крупного многопрофильного стационара, core-антиген ВГС обнаружить не удалось. Высказана точка зрения о нецелесообразности внедрения детекции core-антигена ВГС в систему скри-нинговых исследований пациентов, направляемых на госпитализацию в стационары неинфекционного профиля. Из 326 пациентов (код 120) у 4 (1,2%) доказано посредством определения РНК ВГС наличие гепатита С, единственным серологическим свидетельством которого был core-антиген ВГС. Обсуждается целесообразность проведения исследований по определению core-антигена ВГС среди лиц, обследуемых на наличие ВИЧ-инфекции по эпидемиологическим показаниям. Ключевые слова: core-антиген ВГС, иммуноферментные тест-системы, скрининг
Diagnostic Importance of HCV Core-Antigen Detection
Е.N. Kudryavceva1, M.I. ^rabernikova1, K.S. Кгavchenko1, О.N. Yastrebova2, О.Yu. Jumanova2, Е.I. Lebedeva2, L.E. Kuzina1, V.Ya. Kitsak1, A.S. Каlashnikova1, J.A. Semenenko3 (semenenko@gamaleya.org), S.N. Kuzin13 (drkuzin@list.ru)
Research of the diagnostic importance of HCV core-antigen detection in immune-enzyme analysis among patients and high risk groups was carried out. It was revealed that HCV core-antigen was absent in all 363 patients from therapeutic and surgical branches of a large hospital. It was made an assumption that HCV core-antigen detection is unreasonable for screening in patients admitted to a noninfectious hospital. Hepatitis C was diagnosed in 4 (1.2%) from 326 patients (code 120) by means of HCV RNA detection. HCV core-antigen presence was the single serological marker of HCV-infection. The reasonability of HCV core-antigen detection among the persons examined for HIV-infection presence is discussed. Key words: HCV core-antigen, immune-enzyme analysis, screening
при ГС существенна и во многом определяет передачу ВГС при гемотрансфузиях. Появившиеся значительно позднее закрытые диагностические системы, такие как ARCHITECT Anti-HCV (Abbott, США), Elecsys Anti-HCV (Roche, Швейцария) и другие, также можно отнести к тестам третьего поколения, поскольку в качестве иммуносорбента используется тот же набор антигенов, что и в ИФТС наиболее распространенной планшетной комплектации. Преимуществом закрытых диагностических систем является минимизация участия специалиста в процедуре исследования, что снижает вероятность ошибок, связанных с работой оператора. Вместе с тем хорошо известные недостатки, присущие ИФТС
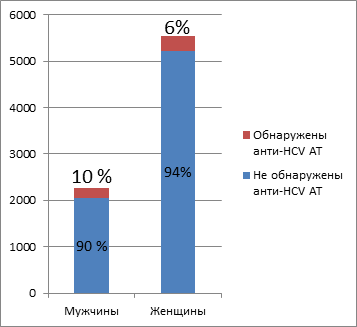
Появление в 1999 году ИФТС для определения core-антигена ВГС и активное изучение их диагностических возможностей привело к неоднозначным результатам. С одной стороны, K. Aoyagi et al. [6] и J. Peterson et al. [7] сообщили о выявлении core-антигена ВГС у пациентов с ОГС в среднем на 26 дней раньше, чем анти-ВГС. F. Komatsu и K. Takasaki [8] обнаружили прямую корреляцию между концентрацией РНК ВГС и core-антигена ВГС в крови пациентов с хроническими формами ГС, что может иметь значение в клинической практике. С другой стороны, как показали M. Krajden et al. [9], выявление в крови core-антигена ВГС не всегда можно расценивать как подтверждение активности инфекционного процесса. По данным этих авторов, примерно у 10% пациентов с РНК ВГС в крови core-антиген ВГС обнаружить не удалось.
Можно констатировать, что имеющийся опыт применения тест-систем для детекции core-антигена ВГС недостаточен для принятия решения о целесообразности их использования в системе эпидемиологического надзора за ГС или в клинической практике. Отсутствие опыта применения тест-систем для детекции core-антигена ВГС в России обусловливает целесообразность проведения соответствующих исследований.
Цель работы - определение диагностической значимости детекции core-антигена ВГС в ИФА при обследовании пациентов крупного многопрофильного стационара.
Материалы и методы
Положительные результаты серологических исследований на наличие соге-антигена ВГС подтверждали с помощью повторной постановки в ИФА на тех же тест-системах.
Результаты и обсуждение
Результаты первого цикла исследований по определению соге-антигена ВГС показали, что у пациентов, госпитализированных в плановом порядке в МОНИКИ, частота его обнаружения невелика (табл. 1).
Частота обнаружения мт-антигена ВГС у различных групп пациентов
Обследованные контингенты Кол-во Положительные результаты в ИФТС: Пациенты с core-антигеном ВГС в крови
ВГС Аг/Ат-ИФА-Бест Бест-анти-ВГС
Пациенты отделения хронического гемодиализа 145 16 11,0 16 11,0 -
Пациенты с онкологическими, аутоиммунными и эндокринологическими заболеваниями 112 3 2,8 2 1,9 1 (0,9%)
Пациенты с другими заболеваниями 106 0 - 0 - 0
Пациенты,код 120 186 75 40,3 58 31,2 17 (9,1%)
Таким образом, можно констатировать неоднозначность полученных результатов исследований (серологических, молекулярно-генетических, биохимических и клинических) образца сыворотки крови пациентки М. С одной стороны, зарегистрирован маркер, который, с нашей точки зрения, свидетельствует о развитии острой ВГС-инфекции, с другой стороны - никакими другими методами подтвердить ее наличие не удалось, при том что, как известно, гепатит С может протекать на фоне нормального уровня АлАт и при отсутствии в крови
РНК ВГС. Динамического обследования данной пациентки не удалось провести.
У пациентов с другими заболеваниями (отделения кардиологии, офтальмологии, ЛОР и др.) анти-ВГС и core-антиген ВГС не выявлены.
Обследованные контингенты Кол-во Выявлен core-антиген ВГС
Пациенты отделения хронического гемодиализа 47 2 (4,3%)
Пациенты различных отделений МОНИКИ (анти-ВГС+) 29 5 (17,2%)
Пациенты, код 120 140 7 (5,0%)
Среди пациентов отделения хронического гемодиализа соге-антиген ВГС выявлен у двух (4,3%) пациентов. У этих же пациентов также обнаружены анти-ВГС. По результатам исследований методом ПЦР у них обнаружена РНК ВГС в высокой концентрации: у одного пациента концентрация составила 1,29 х 107 (подтип ВГС 1Ь) и 1,32 х 106 (подтип ВГС 1а).
Таким образом, суммарно за два цикла серологических исследований из 192 пациентов отделения хронического гемодиализа ни у кого из них не был выявлен соге-антиген без сочетания с анти-ВГС.
Частота обнаружения соге-антигена ВГС у пациентов различных отделений МОНИКИ с анти-ВГС в крови, выявленными в результате скрининго-вых исследований, проводимых при госпитализации, составила 17,2% (5 из 29 пациентов). Во всех случаях у пациентов с сочетанием соге-антигена и антител к ВГС обнаружена РНК ВГС в высокой концентрации - от 9,46 х 105 до 2,27 х 106. У всех определен подтип ВГС 1Ь.
С нашей точки зрения, выявление в образце сыворотки крови только соге-антигена ВГС является основанием для более углубленного, возможно, динамического обследования пациента с использованием клинических и биохимических методов, что позволит с высокой степенью достоверности доказать наличие или отсутствие ВГС-инфекции.
Анализ результатов двух циклов исследований по определению диагностической значимости определения соге-антигена в ИФА среди различных групп пациентов крупного многопрофильного стационара показал, что у пациентов, госпитализированных в плановом порядке в различные отделения МОНИКИ, дополнительно к результатам скри-нингового исследования на наличие анти-ВГС соге-антиген ВГС обнаружить не удалось. Даже среди пациентов отделения хронического гемодиализа с пересадкой почки, где интенсивность эпидемического процесса гепатита С высока, о чем свидетельствуют результаты многочисленных исследований [10, 11], соге-антиген ВГС как единственный маркер ВГС-инфекции выявлен не был. Единственный эпизод с обнаружением соге-антигена ВГС у девочки с аутоиммунным тиреоидитом в отсутствие надежной системы верификации не дал оснований признать у нее наличие гепатита С в связи с отсутствием каких-либо других субъективных или объективных (клинических, биохимических, моле-кулярно-генетических) признаков заболевания.
1. Полученные результаты обосновывают точку зрения о нецелесообразности внедрения детекции соге-антигена ВГС в систему скрининговых исследований пациентов, направляемых на госпитализацию в стационары неинфекционного профиля.
2. Вместе с тем результаты серологического обследования специализированной группы пациентов (код 120) дают основания рекомендовать исследования на наличие соге-антигена
ВГС для этой группы. Таким образом, в рамках нашего исследования определен контингент, который в рамках действующей системы
эпидемиологического надзора за гепатитом С целесообразно обследовать на наличие core-антигена ВГС. ш
I. Colin C., Lanuar D., Touzet S. et al. Sensitivity and specificity of third-generation hepatitis C virus antibody detection assays: an analysis of the literature. J. Viral. Hepatitis. 2001; 8: 87 - 95.
Busch M. Closing the windows on viral transmission by blood transfusion. Blood safety in the new millennium, in: S.L. Stramer, ed. American Association of Blood Banks, Bethesda, Md.; 2001: 33 - 54.
Zachary P., Ullman M., Djeddi S. et al. Evaluation of three commercially available hepatitis C virus antibody detection assays under the conditions of a clinical virology laboratory. J. Clin. Virol. 2005; 34 (3): 207 - 210.
Кудрявцева Е.Н., Ястребова О.Н., Растегаева А.И. и др. О проблеме верификации результатов скрининговых исследований по определению антител к вирусу гепатита С. Альманах клинической медицины. 2011; 24: 53 - 59.
Кузина Л.Е., Ястребова О.Н., Садикова Н.В. и др. Сравнительная оценка результатов определения антител к вирусу гепатита С при использовании различных иммуноферментных тест-систем и подтверждающих тестов. Вопросы вирусологии. 2004; 6: 41 - 44.
Aoyagi K., Iida K., Ohue C., Matsunaga Y., Tanaka E., Kiyosawa K. et al. Performance of a conventional enzyme immunoassay for hepatitis C virus core antigen in the early phases of hepatitis C infection. Clin. Lab. 2001; 47: 119 - 127.
8. Komatsu F., Takasaki K. Determination of serum hepatitis С virus (HCV) core protein using a novel approach for quantitative evaluation of HCV viraemia in anti-HCV-positive patients. Liver. 1999; 19 (5): 375 - 380.
9. Krajden M., Shivji R., Gunadasa K. et al. Evaluation of the core antigen assay as a second-line supplemental test for diagnosis of active hepatitis C infection. J. Clin. Microbiol. 2004; 42 (9): 4054 - 4059.
10. Кудрявцева Е.Н., Мартынюк А.П., Лысенкова Н.В. и др. Маркеры вирусных инфекций у пациентов, находящихся в программе хронического гемодиализа. Сборник тезисов VII съезда Научного общества нефрологов России. Москва; 2010: 204 - 205.
II. Прокопенко Е.И., Ватазин А.В., Щербакова Е.О. Инфекционные осложнения после трансплантации почки. Москва; 2010: 296.
1. Colin C., Lanuar D., Touzet S. et al. Sensitivity and specificity of third-generation hepatitis C virus antibody detection assays: an analysis of the literature. J. Viral. Hepatitis. 2001; 8: 87 - 95.
2. Busch M. Closing the windows on viral transmission by blood transfusion. Blood safety in the new millennium, in: S.L. Stramer, ed. American Association of Blood Banks, Bethesda, Md.; 2001: 33 - 54.
3. Zachary R, Ullman M., Djeddi S et al. Evaluation of three commercially available hepatitis C virus antibody detection assays under the conditions of a clinical virology laboratory. J. Clin. Virol. 2005; 34 (3): 207 - 210.
4. Kudryavtseva E.N., Yastrebova O.N., Rastegayeva A.I. at al. About the problem of results verification of screening researches on determination of antibodies to hepatitis C. The Almanac of clinical medicine. 2011; 24: 53 - 59 (in Russian).
5. Cousina L.E., Yastrebova O.N., Sadikova N.V. et al. Comparative estimation of results of definition of antibodies to hepatitis C when using different ELISA test kits and confirmatory tests. Issues of Virology. 2004; 6: 41 - 44 (in Russian).
6. Aoyagi K., Iida K., Ohue C., Matsunaga Y., Tanaka E., Kiyosawa K. et al.: Performance of a conventional enzyme immunoassay for hepatitis C virus core antigen in the early phases of hepatitis C infection. Clin. Lab., 2001; 47: 119 - 127.
8. Komatsu F., Takasaki K. Determination of serum hepatitis C virus (HCV) core protein using a novel approach for quantitative evaluation of HCV viraemia in anti-HCV-positive patients. Liver. 1999; 19 (5): 375 - 380.
9. Krajden M., Shivji R., Gunadasa K. et al. Evaluation of the core antigen assay as a second-line supplemental test for diagnosis of active hepatitis C infection. J. Clin. Microbiol. 2004; 42 (9): 4054 - 4059.
10. Kudryavtseva E., Martynyuk A.R, Lysenkova N.V. et al. Markers of viral infections in patients in the program chronic hemodialysis. Abstracts of VII Congress of the scientific society of Nephrology Russia. Moscow; 2010: 204 - 205 (in Russian).
11. Rrokopenko E.I., Vatazin A.V., Shcherbakova E.O. Infectious complications after kidney transplantation. Moscow; 2010: 296 (in Russian).
О ситуации по полиомиелиту в мире (Пресс-релиз от 16.12.2013 г.
По данным ВОЗ, в 2013 году осложнилась эпидемиологическая ситуация в мире по заболеваемости полиомиелитом. Вспышки регистрируются в ряде стран, которые на протяжении многих лет были свободными от полиомиелита.
На текущий момент заболевания полиомиелитом регистрируются как в эндемичных странах (Афганистан, Нигерия, Пакистан), так и в странах, куда вирус полиомиелита был завезен (Сирийская Арабская Республика, Камерун, Кения, Сомали). В Израиле, а также на Западном берегу реки Иордан и секторе Газа случаи заражения людей не зарегистрированы, но обнаружена циркуляция вируса полиомиелита во внешней среде.
В связи со вспышкой на Ближнем Востоке в настоящее время в семи странах (Сирия, Израиль, Египет, Турция, Иордания, Палестина, Ливан) про-
водятся кампании по дополнительной иммунизации против полиомиелита, планируется привить 22 млн детей до пяти лет.
Постоянная миграция населения, тесные туристические связи увеличивают риск завоза полиомиелита в Европейский регион, в том числе в Российскую Федерацию.
ВОЗ рекомендует всем лицам, выезжающим в страны, неблагополучные по полиомиелиту, иметь полный курс прививок оральной полиомиелитной вакциной.
Читайте также:
- Запор у грудничка после прививки от гепатита в
- Вакцины свиней против цирковируса
- Медицинский журнал гепатит в
- Как снизить температуру у кота при вирусе
- Одна прививка от гепатита в и поездка на море