Идеальная среда для вирусов
Температурные границы и температурный оптимум размножения вирусов контролируется вирусным геномом, хотя в известной степени они зависят и от клеточной системы. Принято считать, что оптимальная температура для размножения большинства вирусов 36—37°С. Однако из этого правила имеются исключения. Например, для риновирусов температурный оптимум размножения равен 33—34°С. Герпесвирус 2 крупного рогатого скота максимально накапливается в первичной культуре клеток телят при 32°С. Вирус гриппа С, в отличие от вирусов гриппа А и В, лучше размножается при 32—33°С, хотя накапливается медленнее. Ряд альфавирусов накапливается в постоянной линии клеток комаров при 34,5°С в значительно большем титре, чем при оптимальной температуре, требующейся для размножения этих клеток.
В случаях, когда при высокой множественности заражения наблюдается торможение репродукции вируса за счет аутоинтерференции (феномен Магнуса), прибегают к удалению дефектных интерферирующих частиц (ДИЧ) или других ингибирующих субстанций. Применительно к безоболочечным вирусам хорошие результаты получают с помощью простой обработки вирусного инокулята фреоном или хлороформом.
При медленном накоплении вируса и невозможности обеспечения высокой множественности заражения вирус часто вносят в культуру одновременно с посевом клеток.
Иногда с целью повышения выхода применяют повторные сборы вируса путем смены среды в период выраженного накопления. Этот прием особенно эффективен при культивировании постоянных клеточных линий, хронически инфицированных вирусом (например ВЛ КРС) и экскретирующим его в культуральную среду. Кроме сохранения зрелого внеклеточного вируса, такая операция может способствовать его репродукции за счет уменьшения концентрации ингибиторов в культуре. Заметное влияние на репродукцию вирусов оказывает рН поддерживающей среды. Так, вирус бешенства гораздо интенсивнее размножался в культуре клеток КЭ при повышении рН поддерживающей среды от 7,4 до 8,2. Как показало изучение структуры вирусной популяции, при щелочном рН не происходит накопления ДИЧ и отсутствует аутоинтерференция.
Вирус Сендай не продуцировал инфекционных частиц в культурах клеточных линий. Обработка инфицированных клеток трипсином восстанавливала его биологическую активность благодаря расщеплению гликопротеина F (65 кД) на две субъединицы FI (51 кД) и F2 (15 кД). Для изоляции и культивирования парамиксовирусов человека весьма эффективной оказалась линия клеток NCI-H292 при использовании поддерживающих сред с добавлением трипсина (1,5 мкг/мл). Установлено, что вирус ньюкаcлской болезни содержит два предшественника гликопротеинов HNo и Fo, которые в результате протеолиза превращаются соответственно в гликопротеины HN и F С ними связана гемолитическая, гемагглютинирующая, нейраминидазная и инфекционная активность вируса. Существенные различия штаммов вируса ньюкаелской болезни по патогенности определяются структурными особенностями гликопротеинов наружной оболочки вириона, которые отличаются способностью активироваться протеолитическими ферментами. Наличие трипсина в поддерживающей среде стимулировало репродукцию вируса осповакцины. Протеолитический процессинг вирусных гликопротеинов зависит от природы вируса, а также от клеточных факторов культуральной системы. В наибольшей степени от протеолитической активизации зависит репродукция оболочечных вирусов, клетками-мишенями которых in vivo являются энтероциты. К таким вирусам прежде всего относятся ротавирусы млекопитающих и птиц, кишечные коронавирусы свиней и некоторые аденовирусы. Классическим примером протеолитической активации могут служить ротавирусы, выделение и культивирование которых стало возможным благодаря применению трипсина.
Обработка трипсином значительно способствует выделению и репродукции вируса трансмиссивного гастроэнтерита свиней, и обеспечивает размножение в культуре клеток Vero вируса эпизоотической диареи поросят. Вирус эпизоотической диареи свиней (ВЭДС) размножался в культуре клеток Vero только в присутствии трипсина (10 мкг/мл) в поддерживающей среде. ЦПЭ проявлялся образованием синцития. После ряда пассажей в клетках Vero в присутствии трипсина удалось адаптировать вирус к культурам клеток МА 104, СРК и ESK при добавлении трипсина. Попытка адаптировать вирус к шести типам первичных культур клеток эмбриона свиньи не увенчалась успехом. Использование этой, ставшей теперь рутинной, методики позволило размножить астровирус человека в первичной культуре клеток почки эмбриона человека и обезьян. После 11 пассажей вируса в культуре его размножение оставалось трипсинзависимым. Аналогичным образом удалось адаптировать астровирус крупного рогатого скота (штамм US2, серотипа 2) к размножению в культуре клеток новорожденного теленка. Вирус размножался в серийных пассажах только в присутствии трипсина. На ранних пассажах вирус накапливался в культу-ральной среде через семь суток, а в последующем — через трое. Количество инфицированных клеток в культуре было невысоким и не превышало 10—20%. Значение штамма, клеточного субстрата и протеолитической активации в репродукции вирусов можно проследить на примере ротавирусов птиц и кишечных аденовирусов человека. Ротавирус птиц с трудом культивируется в присутствии трипсина, вызывая ЦПЭ в культуре клеток печени и почек КЭ. После трех пассажей вирус терялся в культуре клеток печени, но полностью адаптировался к клеткам почек.
После шести пассажей вирус приобрел способность реплицироваться без обработки трипсином, а после 10 пассажей в почечных клетках — легко культивировался в печеночных клетках и фибробластах КЭ. Однако размножение ротавируса сопровождалось ЦПЭ только в культуре почечных клеток КЭ. Протеолитическая активация была необходима для выделения и репродукции в культуре клеток KB только некоторых серотипов кишечных аденовирусов человека. Добавление трипсина повышало выход инфекционного вируса гриппа С.
Имеются и другие сообщения о том, что обработка клеток трипсином благоприятно сказывается на размножении ряда вирусов.
Поскольку только часть прочитала мою полную публикацию и появились вопросы на которые уже есть вероятный ответ, я решил вставить сюда пару разделов своей статьи.
Был задан такой вопрос: как у коронавируса с температурой?
Ответ: ни в коем случае не низкие температуры. Разберемся в выживаемости в открытой среде типового коронавируса.
Меня в очередной раз обогнали. Только я начал копать в области средств защит статья уже вышла. В этом есть определенный плюс: мне требуется меньше работы.
Сюда я добавил то, о чем не было информации.Об остальном можете почитать в FAQ по защите органов дыхания и дезинфекции.
Я буду и далее отвечать на некоторые не отвеченные вопросы в виде мини публикаций на 10 тысяч слов. Все остальное моей в большой публикации на 100000 тысяч слов(с спойлерами)
Обо всем остальном о коронавирусе Личное исследование по поводу 2019-nCoV(более 80000 букв) .
семейство РНК-вирусов, включающее на январь 2020 года 40 видов вирусов, объединённых в 2 подсемейства.Они были названы из-за строения своей оболочки в виде короны.
Коронавирусы — вирусы с положительной цепью РНК (+РНК) по сравнению с другими РНК-вирусами имеют исключительно большой геном(от тысяч пар оснований) и используют сложную стратегию экспрессии генома.
Вирусные частицы(вирионы) сферической формы(с некоторыми признаками полиморфизма) диаметром 75—160 нм(размер 2019-nCoV от 60 до 140/
120 нанометров в диаметре).
Высота выступов разных коронавирусов в среднем составляет 12—24 нм(2019-nCoV 9 — 12).
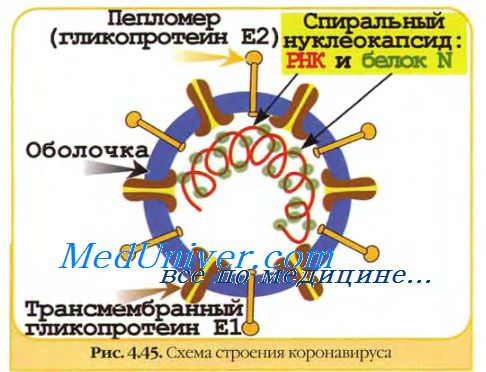
Коронавирусы имеют одно цепочечный геном РНК что кодирует 4–5 структурных белков, включая белок внешней оболочки (N), белок матрицы (M), белок малой оболочки (E), спайк (S) гликопротеин что обеспечивает связывание и проникновение клеток и
для некоторых бета-коронавирусов белок(гликопротеин)(HE), что некоторые оболочечные вирусы используют в качестве механизма вторжения.HEs помогает в прикреплении и разрушении определенных рецепторов сиаловой кислоты,
которые находятся на поверхности клетки-хозяина… 0 .
Они имеют полицистронную организацию генома и используют уникальный механизм транскрипции для генерации вложенного набора субгеномных (sg) мРНК.
Разные типы коронавирусов поражают людей, кошек, птиц, собак, крупный рогатый скот, свиней и зайцев, летучих мышей, верблюдов и других животных.
2019-nCoV: Царство:Riboviria, Тип:Incertae Sedis, Порядок:Nidovirales, Семья:Coronaviridae, Род:etacoronavirus, Подрод:Sarbecovirus
Подразделяются на 4 рода, которые называются альфа-коронавирус, бета-коронавирус, гамма-коронавирус и дельта-коронавирус 1 .
Полный геном 2019-nCoV, теперь хранится онлайн в GenBank: MN908947.3 .
HCoV-NL63 и HCoV-229E относятся к альфа-коронавирусам(120-160 нанометров), тогда как HCoV-OC43, HCoV-HKU1, SARS-CoV, MERS-CoV, 2019-nCoV относятся к бета-коронавирусам, 1 и 2
Многие из белков коронавируса, экспрессируемых в зараженной клетке, способствуют взаимодействию коронавируса с хозяином. Например, путем взаимодействия с клеткой-хозяином для создания оптимальной среды для репликации коронавируса,
путем изменения экспрессии гена-хозяина или противодействия противовирусной защите хозяина.
Многие из этих взаимодействий влияют на исход инфекции, в том числе на адаптацию и переход межвидового предела. Количество мутаций в рецепторсвязывающем домене белка SARS-CoV spike (S), для перехода межвидовой предел было незначительным. 1 . Li et al. 2005c (см. Главу 2). .
Химические вещества, подавляющих или задерживающих физико-химических процессов пептидазы не влияют на проникновение вируса.
Это указывает на то, что использование и проникновение рецептора SARS-CoV и MERS-CoV и, следовательно, 2019-nCoV не зависят от активности рецептора пептидазы.
Они зависят только от связывания с этими конкретными рецепторами-хозяевами. 1 .
Есть предположения, что среда формирующаяся через определенное время в масках способствует сохранению вирусов более длительное время.
Из-за этого есть определенный риск заразиться трогая маску и перенося вирус.
Вода, частое средство передачи вирусов, может способствовать их выживанию, но многие факторы окружающей среды будут оказывать неблагоприятное воздействие на популяцию вирусов.
Сохранение повязки мокрой может способствовать выживанию вируса.
Одно из таких исследований: Исследование выживания типичного вируса в водной среде
В отсутствие клеток-хозяев вирусные популяции в окружающей среде могут только уменьшаться или оставаться стабильными.
Оценка и анализ формы и интенсивности этого сокращения представляют основные цели исследований вирусной инактивации.
Более высокие температуры означают более быструю инактивацию вируса. При низких температурах выше нуля вирусы могут выживать в течение длительных периодов времени,
часто дольше, чем продолжительность исследования. Выживание в холодных условиях
При более высоких температурах вирусная популяция будет уменьшена на несколько порядков в течение нескольких дней.
Уменьшение популяции в более высоких температурах
Температура замерзания позволяет вирусам оставаться стабильными как минимум в течение пары месяцев, но в первые дни может наблюдаться первоначальное снижение. Выживание вирусов в температуре ниже нуля.
Солнечный свет — еще один важный фактор, вызывающий вирусную инактивацию под действием ультрафиолетового излучения.
Присутствие коренной микробной популяции оказывает негативное влияние на выживаемость вируса.
Наличие органического вещества в воде положительно влияет на выживаемость вируса.Другие факторы, ответственные за усиление вирусной инактивации,
включают присутствие дезинфицирующих средств.
Повышение температуры является основным фактором, влияющим на выживание вируса в окружающей среде, через денатурацию белка,
повреждение нуклеиновой кислоты или распад внешней оболочки вируса(капсида) Механизм инактивации
Активность солнечного света можно объяснить повреждением нуклеиновых кислот посредством образования димеров пиримидина или других продуктов,
могут быть задействованы и другие механизмы, такие как возбуждение активных веществ, присутствующих во внешней оболочки вирусов или в окружающей среде.
По поводу более конкретных данных: Было проведено пару исследований по эффективности масок, при чем большинство из них были полевыми исследованиями,
исследовали группы пациентов на эффективность мер.Ознакомьтесь с: 1 и 2
Были сделаны проспективное кластерно-рандомизированное исследования, в котором сравнивали хирургические маски, не проверенные маски P2 и отсутствие масок
в профилактике гриппоподобных заболеваний (ILI) в домашних хозяйствах.Было обнаружено, что приверженность использованию маски значительно снижает риск инфекции, связанной с ГПЗ,
но ,2 ,1 ,1 , экстремальный pH 1 ,1 , медь1 или аэрацию. Воздействие некоторых факторов, таких как жесткость воды, менее надежно доказано,1
Относительно большой размер 2019-nCoV (
Обнаружено минимальное снижение инфекционности через 21 день при 4 градусов цельсия. Нагрев до 56 °C инактивирует коронавирус быстро. 1 .
Основная масса распространения воздшно-капельным путем. До 100 миллионов геномов на мл находятся в выделениях из носоглотки.
В 32% случаев у пациентов в среднем через 3,2 дня после начала заболевания и в 68% на 14 день
Вирусная РНК обнаружена в образцах стула 97% пациентов через 2 недели после заболевания и у 42% анализов мочи.
Сильно подозревается фекально-оральная передача. 1 .
Представлены данные по SARS.Учитывая схожие особенности коронавирусов(отличия проявляются, например, в рецептор-связывающего домена(RBD)) можно достаточно достоверно прогнозировать ситуацию.
Учитывая основы теории представленной в предыдущем параграфе можно попытаться предсказать особенности по выживанию вируса вне организма.
В одной из научных статей поверхности окружающей среды были признаны вероятными факторами,
способствующими передаче внутрибольничных вирусных инфекций 1 .
Вопрос о том, играют ли поверхности больниц роль в распространении внутрибольничной вирусной инфекции, приобрел особую актуальность в связи недавними новостями.
Во время вспышки коронавируса SARS (SARS-CoV) были обнаружены нуклеиновые кислоты SARS-CoV на поверхностях и неодушевленных предметах
0 , 0
Есть вероятность, что поверхности могут быть источниками передачи вируса. Оценка риска, требует данных о инактивации вируса на поверхностях окружающей среды и данных о том,
как на инактивацию вируса влияют переменные среды, такие как температура воздуха (AT) и относительная влажность (RH) и другое.
Из-за того, что для изучения наиболее опасных коронавирусов нужен специально обученный персонал, работающий в лабораторных условиях уровня биобезопасности 3 (BSL-3),
есть большие проблемы при изучении этого вируса, и доступны только ограниченные данные о выживаемости коронавируса и реакции на стрессовые факторы окружающей среды.
Результаты показывают, что при депонировании большого количества суррогатов эти вирусы могут сохраняться в течение нескольких дней на поверхностях в окружающей среде AT и
в широком диапазоне уровней относительной влажности (от 20 до 60% относительной влажности), типичных для сред здравоохранения.
Коронавирус могут быть более устойчивыми к инактивации на поверхностях, чем ранее изученные коронавирусы человека. Сообщалось, что SARS-CoV выживал в течение 36 ч на нержавеющей стали
0 Однако условия AT и RH для предыдущего эксперимента не были представлены, что затрудняет сравнение.
Рабенау и соавтор 0 сообщили о гораздо более медленной инактивации SARS-CoV на поверхности полистирола
(снижение на 4 log 10 через 9 дней; условия AT и RH не сообщались),
что согласуется с некоторыми наблюдениями за TGEV и MHV
Выживаемость вируса была повышена за счет снижения AT. Аналогичные взаимосвязи между AT и инактивацией вируса наблюдались для вирусов с оболочкой в жидкостях и аэрозолях.
Данные по коронавирусу, полученные в этом исследовании, позволяют предположить, что, хотя показатели вирусной инактивации ниже при более низких АТ,
все же различны эффекты РЗ на выживаемость вирусов при каждом АТ.
При окружающих AT (около 20 °C) коронавирусы могут выживать в течение 2 дней, теряя при этом только 1–2 log 10 инфекционности, в зависимости от относительной влажности.
При уменьшении температуры выживаемость вируса поднимется. Вирус может выживать недели при температуре -1.
На основе данных по выживаемости можно предположить, что вирусы с оболочкой могут оставаться инфекционными на поверхностях достаточно долго,
чтобы люди могли с ними соприкоснуться, что создает риск заражения, которое приводит к инфекции и возможной передаче заболевания.
Взаимосвязь между инактивацией и относительной влажностью не является монотонной, была более высокая выживаемость или более высокий защитный эффект при низкой относительной влажности (20%)
и высокой относительной влажности (80%), чем при умеренной относительной влажности (50%). Были также доказательства взаимодействия между AT и RH. 0
Существует вопрос по поводу отопления в здании Neuromantix : 0 по поводу отопления в строении.
0 Результаты указывают что нужны дополнительные расчеты корреляции относительной влажности и разной температуры.
Подобрать в домашних условиях оптимальное соотношение температуры и влажности слишком сложно. Повышение температуры дает более стабильный результат в большинстве случаев.
Скорее всего отсутствуют практические исследования по повышению температуры в помещении как фактор уменьшения рисков.
Однако исходя из информации по температуре можете попробовать повысить температуру.Влажность можно выбирать по вкусу.
Однако полностью защититься подобным способом невозможно. 0 .
Чтобы обеспечить высокую скорость инактивации вируса надо обеспечить большую температуру чем 28-30 градусов.
Исходя из 1 и 1 SARS инактивировался ультрафиолетовым светом (УФ) при 254 нм,
термической обработкой при 65 ° С или более, щелочными (рН> 12) или кислотными (рН Итоги: вероятная живучесть вируса
Эффективность фильтрации отдельных фильтрующих респираторов для лица (FFR) и фильтрующих картриджей для твердых частиц N95 и P100, одобренных NIOSH,
была исследована против жизнеспособного вируса MS2, непатогенного бактериофага, аэрозольного из жидкой суспензии.Его размер (23-28 нанометров)
Испытания проводились в двух условиях циклического потока (минутные объемы 85 и 135 л / мин) и двух постоянных скоростях потока (85 и 270 л / мин).
Среднее проникновение жизнеспособного MS2 через FFR / картриджи N95 и P100 обычно составляло менее 2 и 0,03% соответственно при всех условиях потока.
Учитывая что минимальные образцы коронавирусов превышают размер MS2 минимум 40-60нм.
Можно констатировать приемлемый запас прочности для респираторов FFP2 и N95 при наличии хорошего лицевого уплотнения.
Респиратор с фильтром частиц N99(FFP3) фильтрует, по меньшей мере, 99% частиц в воздухе, но не устойчив к воздействию масла. 1
Со временем происходит деградация защитных возможностей респираторов.
Есть предположения, что среда формирующаяся через определенное время в масках способствует сохранению вирусов более длительное время.
Из-за этого есть определенный риск заразиться трогая маску и перенося вирус.
Для фильтрующих респираторов есть украинская научная статья. Указано значение деградации.
1
Количество бактерий на поверхности маски увеличивается с увеличением времени работы; значительная разница была обнаружена между 4–6-часовыми и 0-часовыми группами (р Часть ссылок
И еще 1000 ссылок, которые я еще не скоро добавлю.Часть ссылок смотрите сразу возле текста.
В зимний период, когда в воздухе витает множество инфекций, люди массово заболевают гриппом и другими вирусными заболеваниями, каждый думает о том, как снизить вероятность заражения.
В статье мы коснёмся только тех мер, которые помогут очистить воздух в помещении и препятствовать проникновению в него вирусов. Мы ничуть не умаляем важность укрепления иммунитета и своевременного лечения.
Идеальная среда для распространения вирусов – спёртый, сухой воздух. Для устранения вирусов нужно, чтобы помещение регулярно проветривалось, воздух в нём увлажнялся и очищался. Справиться с этой задачей поможет приточная вентиляция и мойка воздуха.
Исследования учёных из Колумбийского университета показали, что сухой воздух обеспечивает идеальную среду для распространения вирусов, в т.ч. вируса гриппа. Каждый раз, когда мы простужены и чихаем или кашляем, мы выпускаем туман частиц из носа и рта. Во влажном воздухе эти частицы могут оставаться относительно большими и падать на пол. Но в сухом воздухе они разбиваются на меньшие частицы — становятся настолько малыми, что могут оставаться на плаву часами или днями. В результате этого зимой мы дышим коктейлем из мертвых клеток, слизи и вирусов всех, кто недавно посещал комнату.
Изменяя кислотность или концентрацию соли в клочках слизи, влажный воздух может деформировать поверхность вируса, тем самым уничтожая оружие, которое позволяет ему атаковать наши клетки. В противоположность этому, вирусы в сухом воздухе могут плавать вокруг и оставаться активными часами — пока их не вдохнут или не проглотят, позволив осесть на клетках горла.
Исходя из этого, воздух в помещении нужно увлажнять. В отопительный сезон воздух сам по себе очень сухой из-за большой разницы температур на улице и дома. Оптимальный уровень влажности в помещении – 40-70%. Для достижения этого уровня мы рекомендуем использовать увлажнитель – мойку воздуха или воздухоочиститель. Такой прибор, в зависимости от его производительности, подходит и для квартиры, и для общественных помещений.
Учёные из клиники в Рочестере, штат Миннесота, подсчитали, что работа увлажнителя воздуха в школе в течение одного часа может убить порядка 30% всех вирусов, летающих в воздухе.
Мы не рекомендуем ультразвуковые увлажнители, поскольку они имеют ряд недостатков: оставляют белый налёт на мебели, продуцируют пар в помещении, часто переувлажняют, что приводит к возникновению плесени и грибка. Безопасность таких увлажнителей под вопросом, потому что принцип действия ультразвука до конца не изучен.
При проветривании помещений стандартным способом – через открытую форточку – частицы вирусов могут беспрепятственно проникать в помещение. Для того, чтобы избежать этого, мы рекомендуем установить проветриватель (аэрогивер) – приточный прибор, который подаёт свежий воздух, подогретый до комфортной температуры, и очищенный от мельчайших частиц вирусов и других вредных веществ.
Воздух перед тем, как попасть в помещение, проходит через несколько фильтров, улавливающих не только пыль, но и мельчайшие частицы, в т.ч. вирусов и бактерий. Работа приточного устройства стимулирует работу вытяжки, и загрязнённый воздух быстро покидает комнату. Это обеспечивает оптимальный микроклимат в помещении: воздух всегда свежий, чистый, комфортной температуры. При таком микроклимате, особенно в совокупности с увлажнением и очисткой воздуха, риск заразиться вирусным заболеванием крайне низок.
- Базовый фильтр задерживает пух, шерсть, крупную и среднюю пыль, плесень, пыльцу, способную вызывать поллиноз.
- HEPA фильтр (медицинский стандарт очистки воздуха) предназначен для защиты от мельчайшей пыли, аллергенов, бактерий, вирусов и других опасных микрочастиц.
- Адсорбционно-каталитический фильтр осуществляет очистку воздуха от выхлопных газов, промышленных выбросов.
Мойка воздуха Venta (пр-во Германия) - тихий энергосберегающий увлажнитель-очиститель воздуха. Благодаря концепции "ничего лишнего", стоимость моек Venta остаётся невысокой по сравнению с аналогами, а качество неизменно на высоком уровне. В наличии три бытовые модели разных цветов, подходящие как для небольших комнат, так и для залов до 75м 2 .
(с) Компания "Свежий Воздух". Копирование только с указанием URL.
- Главная
- ➫
- Как вентиляция поможет защититься от гриппа и других вирусных заболеваний?

Акции

Отзывы

FAQ


Глядя на все, что происходит вокруг этого вируса, у многих складывается мнение, что наука оказалась не готова к его появлению. Он выпрыгнул как черт из табакерки. В многочисленных телепередачах, в интернете звучат самые разные противоречивые мнения о его природе, опасности, распространении. Ваш комментарий?


Константин Северинов: Я бы не согласился с утверждением, что наука оказалась не готова. Эпидемия еще только набирала силу, а учеными уже был выявлен агент, который вызывает эту болезнь. На основании РНК вируса разработаны тесты для его выявления. Мы имеем дело с новым агентом, поэтому нужно время, чтобы его изучить, понять, как он взаимодействуют со своим хозяином, с человеком, как мы отвечаем на него. Для этого требуются серьезные исследования, многочисленные эксперименты. Наивно думать, что можно управиться за месяц. У нас есть пример - вирус СПИДА, который был выявлен в 1984 году. Понадобилось четыре года, чтобы появились первые лекарства. И только в начале этого века болезнь стала контролируемой.
В условиях пандемии, когда ей всего несколько месяцев, мы знаем о коронавирусе недостаточно. Во всем мире идет научный поиск, выдвигаются различные гипотезы, почти всегда неправильные, но постепенно появляется свет в конце туннеля. И это в науке нормальная ситуация. Есть уверенность, что только наука путем проб и ошибок сможет победить эпидемию или взять ее под контроль.
Как известно, за многие вирусы мы должны "благодарить" животных, в том числе и нынешний с большой вероятностью получен от летучих мышей. Но вот ученые из США заявили, что в появлении новых вирусов виноваты вовсе не животные, а сам человек, который нещадно эксплуатирует природу. Резко сокращается, а главное меняется ареал существования диких животных. Это может вызывать у них появление новых вирусов. А человек активно внедряется в природу, у него все больше контактов с фауной, а значит, растет вероятность передачи ему вирусов. Словом, что посеешь, то и пожнешь.
Константин Северинов: С этим утверждением трудно спорить. Вопрос в том, основан ли этот вывод на каких-то серьезных исследованиях или это общее соображение. Ведь давно известно, что многие вирусы переданы нам животными. Это происходило, уже когда древний человек их одомашнивал, когда стал заниматься охотой. Число его контактов с фауной из века в век росло, и вирусы передавались людям. Но принципиально важно, что эти болезни человека были локальными, не распространялись дальше небольшого региона, где жили заразившиеся. Там развивалась микроэпидемия, но потом она затухала. Сейчас картина принципиально иная. За какие-то сто лет мир кардинально изменился. Глобализация, гигантские перетоки людей, резкий рост числа контактов. Можно сказать, что вирусы сегодня получили почти идеальные условия для распространения.
Какой урок вынесет человечество из сложившейся в мире экстремальной ситуации? Как изменятся общество и экономика? И что делать науке? Как отвечать на такие страшные для всех нас вызовы? Есть мнение, что главная ее задача - уже сейчас готовиться к новым вирусам. Выявлять и оценивать их патогенность. И такой метод в портфеле науки, к счастью, уже есть - высокопроизводительное секвенирование. В чем суть этого "спасителя"?


Константин Северинов: Мы говорили о том, была ли готова наука к встрече с коронавирусом. Так вот он выявлен с помощью именно этой технологии. В чем ее суть? На исследование берется кровь человека, в ней изучаются последовательности ДНК или РНК. Ожидается, что они будут принадлежать только данному человеку. Но если он чем-то болен, могут попадаться и другие ДНК, "чужие". Высокопроизводительное секвенирование делает такой анализ очень быстро, что позволяет в краткие сроки выявлять неизвестные ДНК и делать предположения об агенте, вызвавшем заболевание.
Но можно ли было таким способом заранее выявить коронавирус COVID-19? Вообще искать неизвестные вирусы, чтобы подготовиться к встрече с ними? Предположим, вы выявили у человека какую-то неизвестную ДНК, но кому она принадлежит? Опасному вирусу или нет? Никто не скажет заранее. Поэтому надо вначале иметь много пациентов, страдающих каким-то заболеванием, а уже потом диагноз ассоциировать с неизвестной ДНК. По-другому вряд ли получится.
Но говорят, что существует около 300 тысяч вирусов, из них науке пока известен один процент. Среди этого вирусного океана предлагается искать аналоги уже известных вирусов и таким способом пытаться предсказывать новые возбудители. А высокопроизводительное секвенирование позволит во много раз ускорить этот перебор.
Константин Северинов: Не получится. Например, в геноме COVID-19 по последовательности ДНК невозможно заранее предсказать, что этот вирус будет опасным. Тем более что вызовет эпидемию. Можно вспомнить "испанку", которая унесла миллионы жизней. Когда сравнили тысячи последовательностей ДНК этого вируса и нашего гриппа, оказалось, что в них произошло всего 3-4 замены. Кто может заранее сказать, что именно эти 3-4 замены способны привести к миллионам жертв?
Ученые МГУ объявили, что намерены заняться поиском лекарств прямого действия, моделируя их на суперкомпьютере "Ломоносов". Но такие попытки делались давно, скажем, в 2003 году, когда люди стали умирать от атипичной пневмонии, но лекарство так и не появилось. Может, это невозможно в принципе?
Константин Северинов: Хотя суперкомпьютеры серьезно облегчают и ускоряют поиск, но все равно на разработку и внедрение в медицину новых препаратов нужно около десяти лет, многие миллиарды долларов и удача. Ведь суперкомпьютер ищет среди уже известных веществ, но это малая доля из существующих на планете. Многие лекарства растительного происхождения, их нашли случайно. Кстати, недавно ученый из Китая получила Нобелевскую премию за создание лекарства от малярии, которое она открыла во многом благодаря случаю. Так что удача здесь необходима, и даже суперкомпьютеру. А почему до сих пор не создано лекарство против атипичной пневмонии? Его никто особенно и не пытался создавать. Ведь болезнь появилась в 2003 году, а в 2004 году сама по себе исчезла. В такой ситуации никто на разработку миллиардов не даст.
Наш известный врач, который не сходит с экрана телевизора, неоднократно заявлял, что коронавирус COVID-19 не так опасен, что на самом деле мы всего в одной мутации от действительно страшной эпидемии, которая, как "испанка", унесет миллионы жизней. Речь о птичьем гриппе, летальность которого во много раз выше, чем у коронавируса. К счастью, пока этот вирус передается только от животного к человеку, поэтому широко не распространяется и не грозит эпидемиями. Но достаточно одной мутации, которая откроет возможность для передачи возбудителя от человека к человеку, и картина кардинально изменится. Неужели действительно мы в одном шаге от глобальной катастрофы?


Константин Северинов: Мягко говоря, эти слухи сильно преувеличены. Мир вирусов очень сложен. Здесь свои законы и отношения, жесточайшая конкуренция. Что такое эффективность вируса? С одной стороны - это летальность, с другой - скорость передачи от одного к другому. Эти два свойства совсем необязательно связаны между собой. Можно иметь высокую летальность, но плохо передаваться. Более того, как правило, если вирус эффективно убивает, он плохо передается. Этот врач говорит об одной "страшной" мутации или комбинации мутаций. Но никто не знает, какая должна быть эта комбинация, чтобы она повысила эффективность вируса. Вариантов множество. И, наконец, не понятно, почему этот "убийца", даже если он все же появится, должен победить в конкуренции с другими вирусами, менее летальными.
15 ведущих академий мира, в частности России, Франции, Германии, Великобритании, США, Японии, заявили о критической необходимости сотрудничества в борьбе с коронавирусом. Ученые подчеркнули, что в нынешней ситуации сохраняется неопределенность и многое еще предстоит сделать. В этот критический момент есть необходимость международного сотрудничества по нескольким направлениям. В частности, ученые должны быстро сообщать о развертывающейся эпидемиологии заболевания, включая способы передачи, инкубационный период и летальность, а также эффективность различных методов вмешательства, делиться информацией о происхождении вируса, генетике и мутациях, об исследованиях в области медицинских препаратов для борьбы с этим заболеванием. Человечество неоднократно подвергалось опасности инфекционных заболеваний и каждый раз преодолевало кризис. В заявлении говорится: "Нынешняя трагедия должна побудить нас резко активизировать наши усилия по профилактике инфекционных заболеваний и борьбе с ними, с тем чтобы усовершенствовать уровень готовности человечества и повысить устойчивость к бедствиям, связанным с инфекционными заболеваниями".
"Ломоносов" ищет лекарства от коронавируса
Сотрудники Вычислительного центра МГУ начали расчеты на суперкомпьютере "Ломоносов", которые помогут найти лекарство прямого действия от коронавируса. Воздействуя такими препаратами на белки-мишени коронавируса SARS-CoV-2, есть шанс победить инфекцию.


Сегодня во всем мире подбор молекул для будущих лекарств ведется с помощью суперкомпьютеров, что в разы ускоряет поиск. Ученые применяют уникальные методы моделирования молекул (докинг), предсказывающие наиболее эффективные варианты препаратов. Но даже для суперкомпьютеров это очень трудная задача. Скажем, ее пытаются решить для других коронавирусов этого же семейства с 2003 года, когда появились первые коронавирусы SARS-CoV. За это время многое стало понятно в функционировании этих вирусов и структуре их белков, но эффективные противовирусные препараты прямого действия для этого семейства вирусов так пока и не созданы. По мнению ученых, чтобы достичь успеха, необходимо сформировать непрерывный научный конвейер: поиск с помощью докинга в больших базах молекул, их дизайн и суперкомпьютерный докинг, экспериментальное тестирование активности, синтез новых молекул. Даже когда новые соединения перейдут на доклинические испытания на животных и далее на клинические испытания на людях, этот конвейер не должен останавливаться, так как из-за токсичности даже на последнем этапе клинических испытаний могут выявиться опасные побочные эффекты и новое соединение сойдет с дистанции.
Кстати, американские ученые, изучая структуру нового коронавируса, нашли его слабое место - белковые шипы. Дело в том, что при инфицировании такой шип на поверхности вируса SARS-CoV-2 прикрепляется к белку-рецептору на поверхности клеток человека - в частности, клеток легких. Примерно так ключ попадает в замочную скважину. Изучая особенности этих шипов и рецепторов человеческих клеток, ученые впервые обнаружили, что всего лишь несколько мутаций сделали шип более компактным, чем аналогичная структура у вируса SARS, который в 2002-2003 годах вызвал эпидемию атипичной пневмонии. Такие мутации помогли SARS-CoV-2 надежнее прикрепляться к рецепторами и быстрее распространяться. Зная свойства этих белков, позволяющие им устанавливать прочные связи с клетками человека, ученые рассчитывают найти способы блокировать вирус, не дать войти в контакт и распространять инфекцию.
Читайте также:


