Новые препараты для лечения гепатита в и дельта
Гепатит B+D

Инфицирование вирусами происходит при непосредственном контакте с биологическим материалом.
Основными путями заражения являются:
- гемотрансфузия;
- хирургические и микрохирургические вмешательства с использованием нестерильного инструмента;
- многократное применение шприцев разными людьми;
- незащищённый сексуальный контакт;
- общее использование средств личной гигиены: бритва, маникюрные принадлежности и пр.;
- вертикальное инфицирование при родах.
В большинстве случаев иммунитет человека подавляет действие вируса самостоятельно, но иногда инфекция переходит в хроническую стадию и тогда без лекарственной терапии уже не обойтись.

Опасным напарником вируса является гепатит D или дельта-вирус.
Данный тип микроорганизма имеет свои отличительные черты, которые выделяют его из основной линейки:
- крайне малый размер молекулы;
- он способен к размножению только в присутствии вируса типа B;
- трудно поддаётся лечению.
Заражение гепатитом D происходит либо одномоментно с получением вируса типа B, либо последовательно. От этого зависит дальнейшее течение заболевания и схема лечения.
Лечение совместной инфекции
Терапия хронического гепатита B заключается в комплексном медикаментозном воздействии на вирус.
Препараты, применяемые для лечения, различают по способу действия:
- стимуляторы собственного иммунитета;
- дополнительные защитные тела – интерфероны;
- противовирусные, аналоги нуклеозидов вирусного белка;
- гепатопротекторные средства.
Защитные функции организма повышают с помощью витаминов, а также препаратов, способных быстро выводить токсические продукты распада вирусов. Пегинтерфероны вводятся, чтобы помочь организму справиться с острой формой инфекции.

Гепатопротекторы восстанавливают поражённые участки печени и препятствуют проникновению вируса к здоровым клеткам. Наиболее точное воздействие наблюдается от использования в лечении нуклеозидных препаратов, которые способны встраиваться в молекулы ДНК вируса, разрушать его структуру и замедлять размножение.
Применение своевременной комплексной терапии имеет хорошие результаты в достижении ремиссии, которая способна сохраняться долгие годы, вплоть до конца жизни.
Лечение гепатита B осложняется, если к инфекции присоединяется дельта-вирус. Он способен за короткое время разрушать клетки печени, вызывая онкологию и цирроз. Проблема лечения гепатита D в том, что микроорганизм резистентен к противовирусным препаратам. Наиболее эффективное действие показывают препараты α-интерферона. Но и их активность направлена не против вируса, а в сторону повышения защиты организма.
Лучший способ справиться с размножением дельта-вируса – вовремя обнаружить и начать лечение гепатита B.
Прививка от гепатита B
Основным методом профилактики заражения вирусом гепатита B является вакцинация. Данная процедура общедоступна для любого гражданина, а люди с повышенным риском заражения (медицинские работники, контактирующие с кровью и пациенты, принимающие препараты крови) прививаются в обязательном порядке. Иммунитет к вирусу вырабатывается у 90% вакцинированных граждан и снижает показатель заболеваемости более чем в 30 раз.
Кроме того, прививка от гепатита B защищает и от дельта-вируса, так как он не существует без своего донора.
Инновации в лечении

Учёные по всему миру пытаются разгадать загадку такой устойчивости вируса к внешнему воздействию. С 2011 года ведётся разработка и испытание нового препарата, способного победить самое распространённое смертельно опасное заболевание планеты.
В настоящее время проводится завершающий этап испытаний препарата – наблюдение за пациентами, получавшими лечение, и его регистрация.
За это время были проведены:
- доклинические исследования, направленные на изучение безопасности приёма препарата и оценка возможных рисков (2011 год);
- подтверждение исследований по безопасности в первой клинической группе добровольцев (2012–2014 годы);
- доказательства эффективности препарата для лечения гепатита B (2013 год).
В исследованиях были задействованы 72 пациента из них 48, имеющие гепатит B и 24 ко-инфицированные дельта-вирусом.

Следующим этапом стал поиск оптимальной дозировки препарата и изучение последствий передозировки. А также оценивалось взаимодействие Мирклудекса с препаратами стандартной комплексной терапии вируса гепатита B. Завершение эксперимента в конце 2016 года показало высокую эффективность препарата в лечении и безопасность приёма даже у пациентов с тяжёлыми поражениями печени, которым не подходило стандартное медикаментозное воздействие. На тот момент в исследовании были задействованы 20 медицинских центров, изучающих заболевания печени в России и Германии. Экспериментальное лечение получили более 120 человек.
С начала 2017 года идёт завершающая стадия изучения препарата, называемая формальной. Эффективность лекарственного средства уже подтверждена клинически и идёт процесс регистрации торговой марки.
Завершение экспертизы и поступление средства в аптеки России планируется к концу 2018 года. Но некоторые источники озвучивают более поздние сроки.
Мирклудекс относится к пептидам, ингибиторам проникновения вируса в клетки печени. Средство предназначено для лечения хронического гепатита B, в том числе с присоединением к нему гепатита D. Пептидные цепи аминокислот связываются с рецепторами гепатоцитов, образуя защитную оболочку, препятствующую проникновению вируса внутрь. Такое действие исключает попадание дельта-вируса в благоприятную для размножения и прогрессирования среду. Эта инновация позволила остановить развитие гепатита D в организме.

Клинических данных о действии препарата не так много, так как он ещё не прошёл окончательные испытания. По данным на сентябрь 2016 года, среди пациентов контрольной группы, принимавших Мирклудекс, у 75% значительно снизилось количество дельта-вируса в составе крови, а у четверти из них микроорганизм полностью исчез. В группе, которая принимала препарат в совместной терапии с пегинтерфероном-2α, популяция вируса снизилась у всех пациентов, а у 71% инфекция исчезла вовсе.
Из этого следует, что новый препарат может стать отличным синергетиком интерферона в лечении дельта-гепатита.
Приблизительные данные по совместной терапии с нуклеозидными противовирусными средствами пока можно узнать из тематических форумов, но они не являются достоверным источником информации.
Пациент – мужчина, в анамнезе которого нелеченый хронический гепатит B с ко-инфекцией дельта-гепатита более 30 лет.
До лечения: ДНК HBV+, РНК HDV+, фиброз F4 (14 кПа), HbsAg+, АЛТ 50, АСТ 45, ГГТ 198.
Промежуточные результаты: ДНК HBV-, РНК HDV-, ГГТ 300
На конец терапии: ДНК HBV-, РНК HDV-, фиброз F4 (15 кПа), HbsAg+, АЛТ 18, АСТ 22, ГГТ 83.
В конце 70 недели, в этот период лекарственная терапия не проводилась: ДНК HBV+, РНК HDV-, фиброз F3 (11,8 кПа), HbsAg+.
Таким образом, видно, что препарат эффективен в применении уже на начальной стадии лечения. Помимо положительного действия на инфекцию, у пациента значительно улучшилось состояние печени и общее самочувствие.
Удалось добиться стойкой ремиссии в отношении гепатита D даже после отмены терапии. Также замечено, что вирус гепатита B активизировался после прекращения приёма препарата, и существует вероятность возвращения дельта-вируса.
Возможно, именно по этой причине в настоящий момент новая тестовая группа испытывает совместную терапию с нуклеозидными препаратами, эффективность действия которых в отношении вируса типа B давно изучена и доказана.
Профилактика гепатита
Пока общество ждёт выпуска нового препарата, нелишним будет вспомнить о профилактике вирусного гепатита.
К предупреждающим мерам относят:
- соблюдение правил чистоты: мытьё рук, влажная уборка, обработка фруктов и овощей дезсредствами, употребление только чистой питьевой воды;
- индивидуальное пользование предметами личной гигиены;
- исключение незащищённых половых контактов;
- контроль над применением медработниками, косметологами, стоматологами и другими специалистами одноразовых или стерильных приборов;
- вакцинация.
Радует, что современная наука и медицина не стоят на месте и, возможно, совсем скоро появятся новейшие препараты для терапии болезней, считающихся на сегодняшний день неизлечимыми.
Обмен знаниями, общение и поддержка людей с гепатитом
- Темы без ответов
- FAQ
- Поиск
- Правила
- Галерея
Гепатит D (Д, дельта) - всем новеньким сюда
![]()
Много вопросов задают в личку, особенно новички, им трудно разобраться в материале. Но другим наверное тоже было бы полезно еще раз пройтись по данным, поэтому решила немножно обобщить и сверстать что-то типа ЧАВО. Потом можно будет изменять, дополнять, обсуждать .
Наиболее часто задаваемые вопросы:
1. Какие анализы (маркеры)нужно сделать для определения гепатита Д?
Если уже выявлен гепатит В, то первым делом нужно сделать суммарные антитела к HDV . Если они есть - сделать антитела по классам: анти-HDV IgM и анти HDV IgG, и наличие RNA HDV. Последний маркер надо бы иметь в количественном выражении или хотя бы в полуколичественном.
Кроме этих маркеров необходимо сделать HBsAg количественно и DNA HBV количественно. Постараться найти возможность, чтобы сделать эти три маркера, касающиеся вирусной нагрузки, именно количественно !
Плюс обычная биохимия для определения активности процесса, бипсия печени или фиброскан для определения степени фиброза.
2. Как часто хроник с гепВ должен проверять наличие/отсутствие гепатита Д?
Угроза заражения всегда остается актуальной для хроника В. Поэтому желательно контролировать Д-маркеры после инвазивных процедур (лечение зубов, переливание крови, операции, иньекции, незащищенный секс с незнамо кем..) - проблизительно через 1,5 - 2 месяца после вышеназванного. А также при обострении хронического гепВ, ухудшении состояния. Если ничего такого не было - достаточно раз в 2 года - на всякий случай.
3. Надо ли определять генотипы вирусов?
Надо бы. очень желательно. Но в России только несколько лабов определяют генотип гепВ, дельту - нигде. Если бываете в европейских странах - не упустите момент и сделайте платно.
4. Зачем определять эти генотипы?
Иногда от генотипа зависит выбор тактики лечения.
Так, существует четыре генотипа вируса В (А, В, С, Д). Из них первые три хорошо поддаются лечению ИФН, генотип Д - плохо. С учетом остальных факторов иногда приходится отказываться от лечения пегами в пользу нуклеат/зидов (редко).
Генотипов вируса дельта восемь (по номерам называют) плюс есть подвиды. Наиболее "мягкий" - 2. Наиболее упорный - 1 генотип, он значительно хуже отвечает на лечение ИФН. Для сравнения - успех ИНФ-терапии достигает 45% в лечении генотипов 2, 4-8; 20-25% в лечении 3-го; лишь 8-12% у 1-го.
В России есть и 1 и 2.
4. Варианты развития заболевания?
Имеется ввиду именно суперинфекция - то есть заражение дельтой уже на фоне хрон. гепатита В.
Течение и прогноз зависит и от сочетания генотипов вирусов и от неизвестных пока факторов, определяющих взаимоотношения вирусов в конкретном организме.
Таких вариантов в основном 4:
а) оба вируса активны, оба с высокими цифрами нагрузки
б) оба малоактивны, даже могут временами уходить в минус. Иногда даже HBsAg не определяется
в) преобладает вирус В, дельта в небольших количествах, может уходить в минус, но в тканях печени он продолжает присутствовать
г) преобладает вирус дельта, подавляя вирус В, именно его влияние на печень определяет картину болезни. Вирус В может уходить в минус, но всегда есть HBsAg
Последний вариант наиболее типичен.
Разобравшись в этих деталях, можно выбрать наиболее оптимальный способ лечения. (термин "оптимальный" звучит весьма иронично, потому что лечение дельты крайне редко бывает успешным. но все-таки даже маленький шанс надо использовать)
![]()
Продолжение
5. Зачем нужно регулярно контролировать HBsAg количественно?
Так как для своего размножения дельта-вирус использует именно эту часть вируса В, существует корреляция между количеством HBsAg и количеством RNA HDV. Не вполне точная, но отчетливая. Поэтому новые рекомендации EASL (the European Association for the Study of the Liver)включают этот маркер в список необходимых при терапии дельта-гепатита. Тем более, что пока RNA HDV количественно выполняют лишь в немногих лабораториях и стоит он довольно дорого.
6. Обязательно ли делать биопсию печени?
Если лечиться по уму - биопсию надо делать обязательно, фиброскан ее не заменит. Во-первых, при дельта-гепатите ни биохимия, ни вирусная нагрузка не отражают уровень органических повреждений в печени. Анализы могут быть спокойными, вируса немного, а на биопсии - уже цирроз. Во-вторых, вирус Д может временами "пропадать", отсутствовать в крови, в ткани же печени он остается и продолжает свое черное дело. В биопсийном материале HDV Ag обнаруживается всегда.
6. Самое важное - как определить свои шансы на успех лечения?
Кое-что можно предвидеть заранее.
Критерии:
-генотипы вирусов - это уже понятно
-уровень вирусной нагрузки по дельте - не более 1,96 в 10*4 копии (проще сказать не более 20000 копий) и в также уровень HBsAg - не более 9000 ме. Если эти уровни выше указанных - шансы расцениваются как низкие.
-длительность заболевания - чем "свежее" дельта - тем легче ее вылечить
-возраст и пол пациента - молодые мужчины могут рассчитывать на более высокий процент успеха
![]()
![]()
![]()
8. Чем лечиться, если есть противопоказания к ИНФ-терапии?
Это случается. например, если есть аутоиммунное заболевание, тяжелое общее состояние, аллергия на ИФН или компоненты, тяжелое поражение щитовидной, хронический панкреатит и пр.
Раньше инфекционисты просто умывали руки. Но в протоколах 2012 г. появилась рекомендация вести в этих случаях гепатит-дельта как гепатитВ - то есть, если есть репликация вируса В, есть фиброз, есть признаки активности воспаления - использовать те же нуки в попытке придавить хотя бы один вирус и этим облегчить состояние печени. На практике - бараклюд или виреад пожизненно. или до появления нового лекарства. или до трансплантации печени.
9. Критерии успешного лечения
Элиминация вирусов В и Д (исчезновение их ДНК и РНК), и, в обязательном порядке! элиминация HBsAg. Пока антиген остается - сохраняется и опасность рецидива (возврата).
10. Когда надо останавливать терапию, как безуспешную?
Вопрос сложный. Дело в том, что небольшие колебания количества обоих вирусов часто наблюдаются на ПВТ пегами, и, до 52-56 недели это считается допустимым. Часто вирус В быстро уходит в минус, но РНК дельты и HBsAg остаются. Но их количество хотя и медленно, очень медленно, но снижаются. В этом случае, конечно, имеет смысл продолжать лечение.
Другое дело - вирусный прорыв, то возрастание количества вируса в разы на фоне ПВТ.
Пожалуй, при 1-м генотипе дельты такое встречается чаще всего. К сожалению.
(Ю.М. Алхазов описал подобный случай на русмедсерв, лечил мальчика 10 лет. До 56 недель все шло хорошо, нагрузки и трансаминазы снижались, вирус В упал аж до 50 копий - в другой лабе написали бы минус. HBsAg тоже снижался, и даже дельта опустилась до нескольких тысяч копий. Успех? Не тут то было - к 72 неделе количество РНК Д взлетело до сотен миллионов. Следом - именно следом за дельтой поползло вверх и количество HBsAg. ДНК В осталось на низком уровне. Лечение прервали, продолжать было бессмысленно.
Ю.М. сначала выложил этот печальный график, потом убрал его. Но я запомнила, потому что у меня было точно то же самое - также В ушел в минус, а дельта к концу лечения дала страшный взлет).
Запомните это! Количество ДНК В не может служить показателем успешного лечения дельта-гепатита, только количество РНК Д дает ясную картину. Вот поэтому без определения количества вируса дельты нельзя говорить о правильной тактике лечения.
11. Где можно сделать анализ РНК ГД количественно?
Пока только одна лаборатория в России выполняет этот анализ, в Санкт-Петербурге, при инфекционной больнице им. Боткина.
Анализ сдается в Больнице Боткина на ул. Миргородская, д. 3, стоит анализ 2800 рублей, вот телефоны 8(812)7177032, 8(812)7172715. Этот анализ принимают только в понедельник и вторник с 8.00 до 15.00, принимают его через неделю, т.е. неделю принимают и следующий раз через неделю. Готовится он 5 дней, но нужно договариваться кто заберет анализ, по телефону результат не сообщают и на эл. почту не высылают.(сообщила Таточка)
Клиники Германии, где определяют дельту количественно.
1. Klinik fur Gastroenterologie,
Hepatologie und Endokrinologie
Medizinische Hochschule Hannover
Carl-Neuberg-Str. 1
30623 Hannover
Fax: +49 0511 532-4896
тел. +49 0511-532-3779 K2 Ebene H
email: Gastro-Privatambulanzmh@hannover.de
2. Medizinische Fakultet der Universitet Heidelberg, Innere Medizin IV
Heidelberg, Germany, 69120
Клиники в Азии, где можно сделать РНК дельты количественно:
МОСКВА, 28 июл — РИА Новости, Альфия Еникеева. Ежегодно острые вирусные гепатиты уносят почти полтора миллиона жизней — больше, чем ВИЧ-инфекция, малярия и туберкулез. Во Всемирный день борьбы с гепатитом РИА Новости вместе с экспертами разбирается, чем опасна эта инфекция, и правда ли, что от нее теперь можно вылечиться.
Древняя болезнь

Их коллеги из Института изучения истории человечества Макса Планка в Йене полагают, что первое заражение человека произошло значительно позже — около семи тысяч лет назад. А британские ученые настаивают на еще более поздней датировке — от 4500 до 800 лет назад. При этом древнейшую вирусную ДНК гепатита В выделили из мумии XVI века, и она очень похожа на геном современного вируса, что само по себе странно. За пятьсот лет должны были произойти изменения.
Судя по многочисленным и противоречивым данным о происхождении вирусного гепатита, к согласию ученые придут не скоро. Пока ясно одно — несколько тысяч лет назад вирусный гепатит был столь же распространен, как и сегодня.
Как болеют россияне
"В России четыре-пять процентов взрослого населения болеют вирусным гепатитом В, два-пять процентов — гепатитом С. Это, конечно, не самые низкие показатели по миру, и в целом вирусный гепатит остается проблемой. Но что касается острого гепатита В, то мы тут на уровне передовых стран. И этого добились в последние 15-20 лет, когда появилась возможность привиться от этого заболевания", — рассказывает РИА Новости Галина Кожевникова, заведующая кафедрой инфекционных болезней медицинского института РУДН.
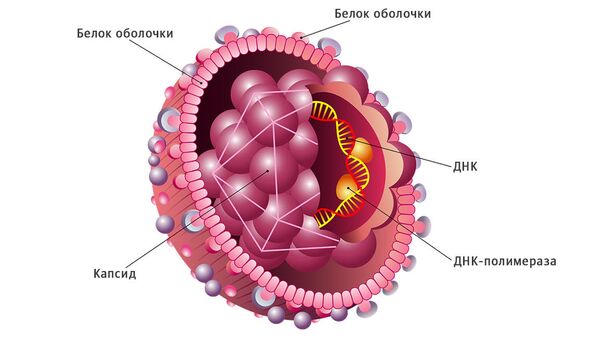
По словам Чавдара Павлова, профессора ПМГМУ имени И. М. Сеченова, в стране вирусный гепатит В уже стал управляемой инфекцией. Риск заражения при медицинских манипуляциях сведен к минимуму, вакцина, основанная на белке, а не на инфекционном материале, и хорошо переносимая людьми, внесена в Национальный календарь прививок и абсолютно бесплатна.
Два гепатита одним лекарством

Впрочем, по сообщениям Российского научного фонда, в ближайшие несколько лет на рынке могут появиться лекарства, способные полностью излечивать от вирусного гепатита В. Российские ученые первыми в мире разработали группу лекарственных препаратов, разрушающих вирус внутри клеток печени. Доклинические испытания на животных начнутся уже в следующем году.
Вероятно, это лекарство поможет и от гепатита дельта ( D ) — вируса-сателлита, которым заражаются инфицированные гепатитом В. Вирус-паразит кодирует всего один антиген (белок) и потому не может построить полноценную вирусную частичку — вирион. Для этого он использует белки оболочки вируса гепатита B.
Всего в мире около 15 миллионов человек инфицированы гепатитом дельта. Чавдар Павлов отмечает, что в России случаи коинфекции ( одновременного заражения вирусами гепатита В и дельта) и суперинфекции (инфицирования гепатитом D пациентов с хроническим гепатитом В) фиксируются в основном на Кавказе — в частности, в Дагестане.
Ласковый убийца обезврежен
Гепатит С — самый неприятный из всех вирусных гепатитов, так как острое течение болезни проходит практически бессимптомно. А при первых признаках недомогания — температура, тошнота, рвота, боли в мышцах — его можно спутать с обычным гриппом. Часто пациенты обращаются за медицинской помощью, когда болезнь уже запущена. Вирус гепатита С часто приводит к циррозу и раку печени, что в большинстве случаев заканчивается летальным исходом.

"Вакцины нет, ее сложно разработать. Вирус гепатита С ускользает от иммунологической защиты, внутри организма он меняет свои свойства. Те антитела, которые вырабатывала иммунная система три года назад, уже не действуют на новый, чуть измененный вирус. Но с гепатитом С очень хорошая история развития фармакологии. Сейчас мы совершенно точно можем говорить, что он излечим полностью. Разработаны и внедрены препараты так называемого прямого противовирусного действия. Они действуют на определенные структуры вируса, блокируют их и не позволяют ему размножаться", — резюмирует эксперт.
Специалисты предупреждают, что лучше свести риск заболевания этими опасными инфекциями к минимуму: вовремя вакцинироваться, предохраняться и с осторожностью относиться к пирсингу и татуировкам.
Среди примерно полумиллиарда лиц, инфицированных вирусом гепатита B, насчитывается около 25 млн инфицированных вирусом гепатита D. Дельта-вирус часто вызывает более тяжелые, быстро прогрессирующие поражения печени. Лечение дельта-вирусной инфекции остается нерешенной проблемой. Более 30 лет используются препараты интерферона. В настоящее время широкое распространение получил пегилированный интерферон альфа. Но применение препаратов интерферона не гарантирует излечения у большинства больных дельта-инфекцией, не обеспечивает стабильной элиминации вируса и дает множество побочных эффектов. Новые препараты с иным механизмом действия – аналоги нуклеотидов и препараты со специфическими механизмами действия мирклудекс B (myrcludex B), лонафарниб (lonafarnib), REP 2139 проходят клинические испытания. Перспективной представляется комбинированная терапия пегилированными интерферонами и аналогами нуклеотидов.
Среди примерно полумиллиарда лиц, инфицированных вирусом гепатита B, насчитывается около 25 млн инфицированных вирусом гепатита D. Дельта-вирус часто вызывает более тяжелые, быстро прогрессирующие поражения печени. Лечение дельта-вирусной инфекции остается нерешенной проблемой. Более 30 лет используются препараты интерферона. В настоящее время широкое распространение получил пегилированный интерферон альфа. Но применение препаратов интерферона не гарантирует излечения у большинства больных дельта-инфекцией, не обеспечивает стабильной элиминации вируса и дает множество побочных эффектов. Новые препараты с иным механизмом действия – аналоги нуклеотидов и препараты со специфическими механизмами действия мирклудекс B (myrcludex B), лонафарниб (lonafarnib), REP 2139 проходят клинические испытания. Перспективной представляется комбинированная терапия пегилированными интерферонами и аналогами нуклеотидов.
Лечение гепатита D
Согласно рекомендациям EASL 2017 г., терапией выбора у пациентов с коинфекцией HDV/HBV с хроническим гепатитом (ХГ) или компенсированным циррозом печени (ЦП) является пегилированный интерферон альфа (пегИФН-альфа) в течение 48 недель (уровень доказательности I, степень клинической рекомендации 1).
Больным с коинфекцией HDV/HBV с продолжающейся репликацией ДНК HBV необходимо назначать аналоги нуклеотидов (уровень доказательности II-2, степень клинической рекомендации 1).
При хорошей переносимости лечение пегИФН-альфа может быть продолжено до 48 недель независимо от ответа на него (уровень доказательности II-2, степень клинической рекомендации 2).
На сегодняшний день пегИФН-альфа – единственный доступный противовирусный препарат для лечения пациентов с хронической HDV-инфекцией с доказанной эффективностью. При использовании пегИФН-альфа вирусологический ответ на терапию достигается в 17–47% случаев [2].
По данным ряда исследований, у 25% пациентов концентрация РНК-HDV снижается на 24-й неделе применения пегИФН-альфа. Тем не менее поздние рецидивы после прекращения терапии отмечаются в 50% случаев, что позволяет подвергать сомнению возможность достижения устойчивого вирусологического ответа при коинфекции HDV/HBV. В связи с этим рекомендуется долгосрочное наблюдение за концентрацией РНК-HDV у всех получающих лечение пациентов – до тех пор, пока HBsAg определяется в сыворотке крови. Элиминация HBsAg возможна при длительном наблюдении примерно у 10% больных, находящихся на терапии пегИФН-альфа, что может служить маркером излечения HDV-инфекции [3, 4].
Были предприняты попытки повысить эффективность интерферонотерапии за счет увеличения ее длительности. Однако в настоящее время отсутствуют четкие доказательства, что подобная тактика подходит для большинства пациентов, хронически инфицированных HDV. При 96-недельной терапии пегИФН-альфа (монотерапия или в сочетании с тенофовиром) на 24-й неделе наблюдались рецидивы у 36,4% пациентов, ответивших на лечение [5].
Вероятность долгосрочного ответа на терапию пегИФН-альфа может быть оценена по уровням РНК-HDV и HBsAg на 12-й и 24-й неделе лечения. Преждевременное прекращение приема пегИФН-альфа не рекомендуется, если препарат переносится хорошо. Дело в том, что отрицательное прогностическое значение упомянутых маркеров невелико, а поздний ответ может возникнуть у больных с отсутствием раннего ответа на лечение. Предполагается, что терапия ИФН-альфа является фактором, приостанавливающим прогрессирование заболевания [6–9].
Ни аналоги нуклеотидов, ни рибавирин практически не влияют на уровень РНК-HDV у пациентов с HDV-инфекцией. Несмотря на то что HDV нередко доминирует, при естественном течении хронической HDV/HBV-инфекции можно наблюдать выраженные колебания концентрации обоих вирусов. Терапия аналогами нуклеотидов рекомендуется больным с уровнем ДНК-HBV выше 2000 МЕ/мл. Пациентам с декомпенсированным ЦП целесообразно назначать блокаторы репликации HBV, а не пегИФН-альфа. Такие больные должны пройти подготовку к трансплантации печени. Терапия аналогами нуклеотидов рекомендуется всем пациентам с декомпенсированным ЦП с определяемым уровнем ДНК-HBV [10, 11].
Современные рекомендации по применению интерферона альфа
Терапию ИФН-альфа могут получать только пациенты с компенсированным HDV-ассоциированным заболеванием печени. Единственным на сегодняшний день методом лечения декомпенсированного заболевания печени является трансплантация. ПегИФН-альфа – средство первого выбора при ХГ D. Годичный курс следует назначать всем больным, не получавшим ранее ИФН-альфа, а также тем, кто не ответил ранее на стандартную терапию ИФН-альфа. Сывороточные уровни РНК-HDV и HBsAg дают возможность клиницистам оценить ранний ответ, а также выявить больных с отсроченным вирусологическим ответом, которым может помочь длительная терапия [1, 2, 12].
Перспективы лечения хронического гепатита D
Эффективность терапии пегИФН-альфа как в монорежиме, так и в сочетании с аналогами нуклеотидов достаточно низкая, по окончании терапии часто возникают рецидивы. Поэтому крайне актуальна разработка новых видов терапии ХГ D.
В настоящее время клинические испытания проходят три класса новых лекарственных препаратов, влияющих на жизненный цикл HDV: ингибиторы его клеточного рецептора Na + -таурохолат ко-транспортного полипептида (NTCP), ингибиторы фарнезилтрансферазы (FTIs) и полимеры нуклеиновых кислот (NAPs).
Мирклудекс B: ингибитор проникновения вируса гепатита D в клетку
Впервые безопасность мирклудекса B для человека оценили A. Blank и соавт. В исследовании 36 здоровых добровольцев получали лекарственное средство либо внутривенно, либо подкожно в возрастающих дозах вплоть до 20 мг/сут. Использование препарата сопровождалось повышением уровня конъюгированных ЖК. Этот уровень на фоне длительного применения не достигал опасных для пациента значений. Концентрация мирклудекса B, необходимая для блокирования проникновения вирусов HBV/HDV через NTCP-рецептор, была приблизительно в 100 раз меньше, чем та, которая нарушала транспорт ЖК. Это указывало на возможность блокирования вирусов без избыточной нагрузки в отношении транспорта ЖК. Пациенты хорошо переносили лекарственное средство. Только в двух случаях отмечались серьезные побочные эффекты – повышение уровней липазы и амилазы. Данное исследование стало предварительным в отношении тестирования мирклудекса B у больных гепатитом B или D [17, 18].
Безопасность и эффективность мирклудекса B при ХГ D изучали в пилотном российском исследовании. 24 пациента были разделены на три группы поровну (рандомизация). Пациенты первой группы получали мирклудекс B 2 мг/сут в течение 24 недель после 48-недельной терапии пегИФН-альфа-2а, пациенты второй – мирклудекс B совместно с пегИФН-альфа-2а в течение 24 недель, затем монотерапию пегИФН-альфа-2a еще 24 недели. Пациентам третьей группы назначали только пегИФН-альфа-2a в течение 48 недель. Первой конечной точкой служил ответ HBsAg, определяемый как снижение сывороточной концентрации HBsAg не менее чем на 0,5 log IU/мл. Все пациенты были негативными по HBeAg, у троих имел место ЦП, девять больных ранее получали пегИФН-альфа-2a. Исходно средняя сывороточная концентрация РНК-HDV составила примерно 10 4 копий/мл, а средняя концентрация HBsAg около 10 4 IU/мл. Промежуточный анализ на 24-й неделе исследования у пациентов, получавших только мирклудекс B, показал нормализацию уровня аланинаминотрансферазы (АЛТ) в шести случаях и снижение уровня РНК-HDV более чем в 10 раз (1 log) – в четырех, с клиренсом 2. Однако уровень HBsAg оставался неизменным у всех больных. После прекращения лечения РНК-HDV вновь обнаруживалась у всех пациентов. У пятерых больных из тех, кто получал мирклудекс B вместе с пегИФН-альфа-2a, РНК-HDV стала негативной. ДНК-HBV также значимо снизилась только в этой группе. Побочными эффектами мирклудекса B были тромбоцитопения, лимфопения, эозинопения, нейтропения. Причем все изменения были незначительно выраженными, преходящими и не требовали изменения дозы препарата. Антитела к исследуемому препарату выявлены у шести пациентов, получавших комбинированное лечение с пегИФН-альфа-2a. Несмотря на то что это не влияло на эффективность лечения, ученые проанализировали значение данных антител. Во всех группах, в которых применяли мирклудекс B, уровень ЖК, конъюгированных с таурином и глицином, повышался [19].
Таким образом, мирклудекс B вызывает значительное снижение уровня РНК-HDV. Но этот эффект нестойкий, по окончании терапии не сохраняется. Результаты лечения были выше у больных, получавших одновременно мирклудекс B и пегИФН-альфа-2a. Монотерапия препаратом мирклудекс B при ХГ D малоэффективна. Уровни HBsAg не менялись при использовании мирклудекса B. Авторы предположили, что HBsAg может продуцироваться интегрированной в геном ДНК-HBV, отличной от cccDNA, и HBsAg снижается независимым от кинетики ДНК-HBV образом. Эффекты длительной монотерапии мирклудексом B или комбинированной терапии с пегИФН-альфа-2a и тенофовиром, а также использование более высоких доз должны быть изучены в дальнейших исследованиях [20].
Ингибитор сборки вируса лонафарниб и препарат REP 2139
Блокада процесса фарнезилирования с помощью FTI способствует накоплению промежуточных продуктов репликации HDV внутри гепатоцитов. Снижение концентрации сывороточной РНК-HDV происходит не за счет уменьшения количества инфицированных гепатоцитов, а в большей степени за счет снижения сборки частиц вируса HDV. Механизм, с помощью которого FTI уменьшает концентрацию сывороточной РНК-HDV, еще предстоит установить, а эффект внутриклеточного накопления частиц РНК остается малоизученным. Вопрос, может ли накопление репликативных интермедиатов HDV в печеночных клетках индуцировать цитотоксический эффект или усиливать иммуноопосредованное уничтожение клеток, остается нерешенным [23].
Лонафарниб, один из FTI, был изначально предложен как противораковое средство, поскольку фарнезилтрансфераза является важным клеточным ферментом, вовлеченным в некоторые клеточные функции, в том числе фарнезилирование ряда цитоплазматических белков семейства RAS, участвующих в росте, дифференцировке и выживании клеток, а также в Т-клеточной активации и выработке цитокинов [24, 25].
15 участников исследования LOWR HDV-1 (лонафарниб с добавлением ритонавира и без него для лечения HDV-инфекции) были разделены поровну на пять групп для определения оптимальной дозы препарата. Лонафарниб назначали в дозах 200 и 300 мг дважды в день или 100 мг трижды в день как в монорежиме, так и в сочетании с ритонавиром или пегИФН-альфа от восьми до 12 недель. Поскольку ритонавир является ингибитором цитохрома P450-3A4 – главного метаболизатора лонафарниба, предполагалось, что эта комбинация обеспечит максимальный внутрипеченочный уровень препарата. После четырех недель лечения HDV-виремия значительно уменьшилась независимо от схемы назначения лонафарниба – в монорежиме или в комбинации с другими препаратами. Это сочеталось со значительным снижением уровня АЛТ, однако отсутствовали изменения содержания HBsAg. Добавление ритонавира 100 мг к лонафарнибу 100 мг два раза в день вызывало более значительный антивирусный эффект и меньшее количество гастроинтестинальных побочных эффектов. Но в этой комбинации показатели HBsAg также не менялись. К концу лечения уровни сывороточных РНК-НDV и АЛТ возвращались к исходным параметрам у всех пациентов, за исключением двух. Пять пациентов, которые получали лонафарниб в дозах 200 и 300 мг дважды в день с пегИФН-альфа, прервали лечение в течение четырех недель из-за непереносимости [27].
Три других исследования под тем же акронимом (LOWR HDV-2, -3, -4) продолжаются, но предварительные результаты опубликованы в виде тезисов. В исследовании LOWR HDV-2, посвященном оценке наименьшей эффективной дозы лонафарниба в комбинированной терапии, 48 пациентов получали небольшие дозы препарата (75, 50 или 25 мг дважды в день) в комбинации с ритонавиром и пегИФН-альфа или без пегИФН-альфа. Тройной режим с лонафарнибом 25 или 50 мг, ритонавиром 100 мг дважды в день в комбинации с пегИФН-альфа 180 мкг показал лучший результат и переносимость [28].
В исследовании LOWR HDV-3 21 больной получал однократные ежедневные дозы лонафарниба (50, 75 или 100 мг) с ритонавиром 100 мг в течение 12 или 24 недель. Пациентам проводилась анти-HBV-терапия аналогами нуклеозидов до назначения лонафарниба. После 12 недель лечения средний log снижения концентрации РНК-HDV от исходного уровня колебался от 0,83 IU/мл (для лонафарниба 100 мг) до 1,6 IU/мл (для лонафарниба 50 мг). Комбинация ритонавира и лонафарниба у больных, получавших лечение в течение шести месяцев, была безопасной и эффективной в отношении снижения виремии HDV [29].
Увеличение дозы и достижение толерантности оценивали в исследовании LOWR HDV-4 с участием 15 пациентов. На старте терапии все больные получали лонафарниб в дозе 50 мг одновременно с ритонавиром 100 мг. Далее доза лонафарниба была увеличена до 75 мг, затем до 100 мг. Ритонавир назначали в дозе 100 мг дважды в день. В конце лечения снижение концентрации сывороточной РНК-HDV от исходного уровня составило 1,58 ± 1,38 log10 IU/мл. Уровни АЛТ нормализовались у 53% больных. Снижение РНК-HDV и нормализация уровня АЛТ не сохранялись после прекращения терапии. Кроме того, лонафарниб не оказывал существенного влияния на уровни HBsAg как до, так и после лечения. Возникновения резистентных мутаций не зафиксировано [30].
Значимость накопления рибонуклеопротеидного комплекса в гепатоцитах обусловливает перспективы длительного применения лонафарниба у больных ЦП. Более того, фарнезилтрансфераза является важным клеточным ферментом, что существенно для полного установления влияния его ингибирования на разнообразные внутриклеточные процессы.
REP 2139: полимер нуклеиновой кислоты
Фосфотионат фосфорилированных аналогов нуклеотидов (NAP) – это олигонуклеотиды с негативным зарядом и широкой ингибиторной активностью в отношении ряда вирусов (например, ВИЧ, вирус простого герпеса, вирус лимфоцитарного хориоменингита). Однако на модели НBV-инфекции на утках показано, что NAPs влияют как на проникновение вируса в клетку, так и на синтез и высвобождение HBsAg из гепатоцитов. Основываясь на этих результатах, безопасность и эффективность REP 2055 (Replicor) и REP 2139 (Replic) oценивали в первом, основанном на принципах доказательной медицины, исследовании у HBV-инфицированных HBeAg-позитивных больных. В обоих исследованиях на фоне монотерапии NAP наблюдалось уменьшение концентрации сывороточного HBsAg и ДНК-HBV с 2 до 7 и с 3 до 9 log соответственно, что сопровождалось появлением сывороточных анти-HBs (10–1712 мIU/мл). Из побочных эффектов лечения наблюдались лихорадка, головная боль и озноб [31–34].
Основываясь на значительном эффекте на сывороточный HBsAg, ученые изучили безопасность и эффективность REP 2139 в комбинации с пегИФН-альфа при ХГ D. В молдавском исследовании принимали участие 12 ранее не леченных больных в возрасте от 18 до 55 лет, позитивных по анти-HBeAg-антителам, а также по РНК-HDV с концентрацией сывороточного HBsAg свыше 1000 IU/мл и низким уровнем ДНК-HBV (от
Читайте также:


