Новый препарат от гепатита с нарлапревир
Содержание
Русское название
Латинское название вещества Нарлапревир
Брутто-формула
Фармакологическая группа вещества Нарлапревир
Нозологическая классификация (МКБ-10)
Характеристика вещества Нарлапревир
Фармакология
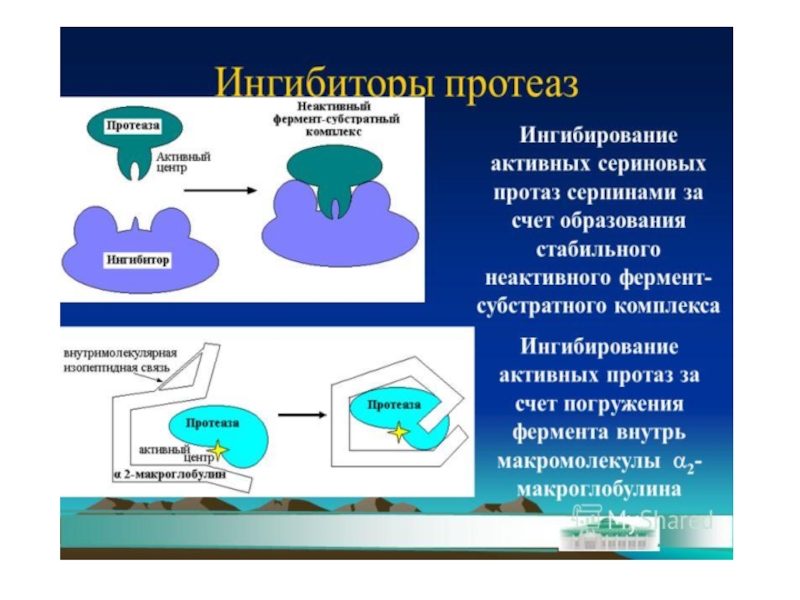
Нарлапревир является сильным пероральным ингибитором NS3 сериновой протеазы вируса гепатита С. Оказывает ингибирующее воздействие путем ковалентного, но обратимого связывания с сериновым активным центром протеазы вируса гепатита С посредством кетоамидной функциональной группы. Таким образом, нарлапревир ингибирует полипротеиновый процессинг вируса и предотвращает его репликацию в инфицированных клетках хозяина.
Противовирусная активность в клеточной культуре
Противовирусная активность нарлапревира изучалась в биохимическом анализе медленных ингибиторов протеазы и системы репликона вируса гепатита С, которая представляет собой хорошо изученную модель репликации вируса. Константа ингибирования (Ki) нарлапревира для NS3 протеазы генотипа lb составляет 7 нМ. Также нарлапревир проявляет активность в отношении генотипов 1а, 2а, 3а и 4 (Ki=0,7; 3; 7 и 16 нМ соответственно). В системе бицистронного репликона генотипа lb показатели нарлапревира IC50 и IC90 (концентрация, вызывающая 90% ингибирование) составляют 20 и 40 нМ соответственно. В системе же репликона генотипа la IC90 нарлапревира составляет 140 нМ. В присутствии 50% сыворотки крови человека IC50 нарлапревира в репликоне lb увеличивается до 720 нМ.
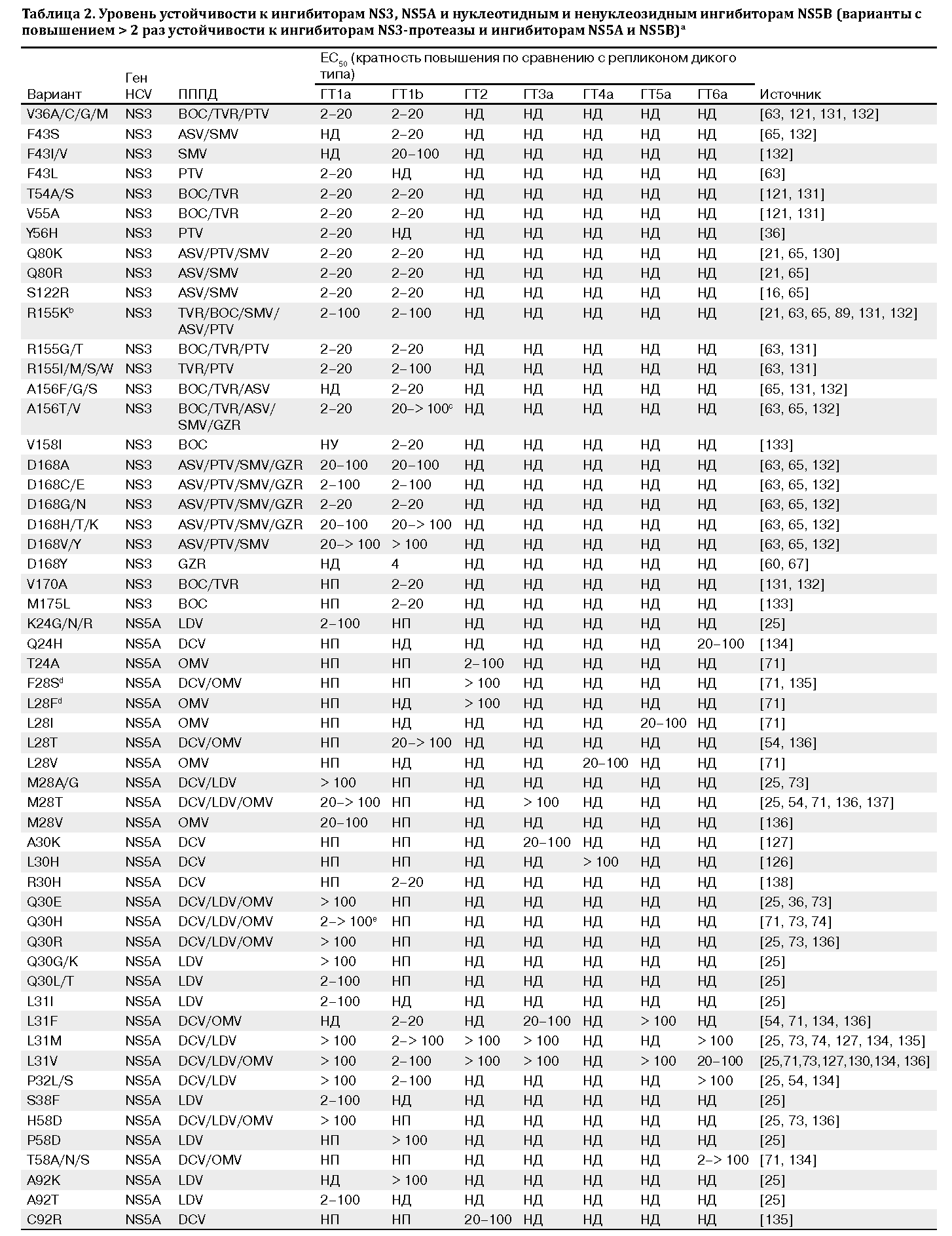
При проведении биохимических тестов и исследований репликона продемонстрирована перекрестная устойчивость к нарлапревиру при мутациях резистентности, возникших при применении других кетоамидных ингибиторов протеазы вируса гепатита С. Активность нарлапревира умеренно снижается при следующих основных мутациях вируса, ассоциированных с резистентностью к другим ингибиторам протеазы вируса гепатита С: V36M (Ki=12 нМ, IC50 для репликона = 430 нМ, IC90=940 нМ), V170A (Ki=30 нМ, IC50=300 нМ, IC90=900 нМ) и Т54А (Ki=40 нМ, IC50=400 нМ, IC90=700 нМ). Активность нарлапревира значительно снижается в отношении мутаций в локусах 155 (R155K) и 156 (A156S/T). Кратность увеличения резистентности при двойных мутациях приблизительно эквивалентна суммам показателей для отдельных мутаций (т.е. зависимость мультипликативная, а не аддитивная). Нарлапревир в полной мере активен в отношении мутации D168V.
После назначения нарлапревира внутрь после приема пищи в дозах 300–1500 мг один раз в сутки в комбинации с ритонавиром в дозе 100 мг один раз в сутки у здоровых лиц средние значения Тmах нарлапревира находились в диапазоне от 2,5 до 4,5 ч. Значения Сmах, Cmin и AUC , количественно отражающие концентрацию нарлапревира в организме, увеличивались пропорционально повышению дозы нарлапревира. Нарлапревир рекомендуется принимать с пищей, т.к. при назначении нарлапревира после приема пищи средние общие значения AUC и Сmах увеличивались в 1,8 и 2,8 раз относительно показателей, полученных в условиях натощак. При этом не выявлено явной задержки в достижении Тmах после приема пищи по сравнению с дозированием в условиях натощак.
Нарлапревир умеренно связывается с белками плазмы (от 86,5 до 91,4%) и характеризуется большим Vd , что предполагает экстенсивное распределение в тканях.
Нарлапревир экстенсивно метаболизируется путем окисления, редукции, расщепления и N-деалкилирования. Главным образом метаболизм нарлапревира и его основного метаболита обеспечивается изоферментом CYP3А 4 цитохрома Р450. Под действием изофермента CYP3A4 нарлапревир и его основной неактивный метаболит преобразуются в окисленные метаболиты. Таким образом, нарлапревир представляет собой субстрат изофермента CYP3A4 . Также нарлапревир проявляет слабые ингибирующие свойства в отношении изофермента CYP3A4 . При совместном применении нарлапревира с сильным ингибитором изофермента CYP3A4 ритонавиром наблюдается увеличение концентрации нарлапревира за счет оптимизации минимальных концентраций, что позволяет применять более удобный режим лечения — один раз в день.
Выведение нарлапревира изучалось в исследовании с радиоактивными изотопами, в котором здоровые добровольцы получали дозу 400 мг 14 С-нарлапревира внутрь в виде монотерапии или в комбинации с ритонавиром. Нарлапревир преимущественно экскретируется через кишечник (на 81,1%), почечный же клиренс вносит минимальный вклад (3,14%) в выведение нарлапревира. Применение ритонавира снижает клиренс и существенно повышает T1/2 нарлапревира.
Применение вещества Нарлапревир
Лечение хронического вирусного гепатита С, вызванного вирусом генотипа 1, у пациентов старше 18 лет с компенсированным поражением печени, в комбинации с ритонавиром, пэгинтерфероном альфа и рибавирином, ранее не получавших противовирусную терапию пэгинтерфероном альфа и рибавирином, или у которых предшествующее двухкомпонентное лечение пэгинтерфероном альфа и рибавирином было неэффективным.
Нарлапревир нельзя применять в качестве монотерапии.
Противопоказания
Повышенная чувствительность к нарлапревиру; тяжелая нейтропения (уровень нейтрофилов QT , требует тщательного контроля параметров ЭКГ . Назначение многократных терапевтических доз нарлапревира (300 мг/сут) в комбинации с ритонавиром (100 мг/сут) не приводит к значимому удлинению интервала QTс. При назначении нарлапревира в дозе 1500 мг, многократно превышающей терапевтическую, в комбинации с ритонавиром 100 мг 1 раз в день в течение 5 дней наблюдалось удлинение интервала QT .
Применение при беременности и кормлении грудью
Комбинация нарлапревира с ритонавиром, пэгинтерфероном альфа и рибавирином противопоказана при беременности и в период грудного вскармливания. Нарлапревир в исследованиях in vivo не продемонстрировал эмбрио- и фетотоксичность, однако отмечались признаки токсичности для организма матери.
Женщинам, получающим лечение нарлапревиром, ритонавиром, пэгинтерфероном альфа и рибавирином, а также женщинам-партнерам мужчин, получающих комбинацию этих препаратов, следует соблюдать особую осторожность для предупреждения беременности. Во время терапии женщины и мужчины детородного возраста должны использовать барьерный метод контрацепции (презерватив и/или диафрагма/шеечный колпачок).
Побочные действия вещества Нарлапревир
Ниже представлены нежелательные реакции, наблюдавшиеся в ходе лечения нарлапревиром в комбинации с ритонавиром, пэгинтерфероном альфа и рибавирином.
Для градации частоты побочных эффектов использовалась классификация ВОЗ : очень часто (>1 случая на 10 назначений); часто (>1 случая на 100 назначений) и нечасто ( ЖКТ : часто — тошнота, диарея; нечасто — боль в верхней части живота, сухость во рту, необычный кал, рвота, дискомфорт в животе, хейлит, гастроэзофагеальный рефлюкс, кровоточивость десен, анальный зуд, анальная трещина, прокталгия.
Со стороны печени и желчевыводящих путей: часто — гипербилирубинемия.
Со стороны кожи и подкожных тканей: часто — кожный зуд, алопеция, крапивница, сыпь (папулезная, макулярная); нечасто — ксеродерма, сухость кожных покровов, дерматит, экзема, гипергидроз, сыпь.
Со стороны скелетно-мышечной системы и соединительной ткани: часто — миалгия, артралгия; нечасто — боль в спине, боль в конечности.
Со стороны почек и мочевыводящих путей: нечасто — гемоглобинурия, протеинурия.
Со стороны половых органов и молочной железы: нечасто — бартолинит.
Общие расстройства и нарушения в месте введения: очень часто — астения; часто — гриппоподобное состояние, озноб, пирексия, утомляемость, боль; нечасто — гипертермия.
Лабораторные и инструментальные данные: очень часто — снижение уровня Hb; часто — снижение массы тела, повышение температуры тела, повышение активности ГГТ , снижение количества тромбоцитов; нечасто — снижение количества нейтрофилов, снижение количества лейкоцитов, повышение активности АСТ , повышение активности ЩФ в крови, повышение АД , повышение уровня триглицеридов в крови.
Взаимодействие
Нарлапревир является субстратом и слабым ингибитором изофермента CYP3A4 , кроме того, ритонавир, обязательный компонент терапии с применением нарлапревира, является сильным ингибитором изофермента CYP3A4 , поэтому при применении с лекарственными средствами, являющимися субстратами, ингибиторами и/или индукторами изофермента CYP3A4 , возможно изменение концентрации как нарлапревира и ритонавира, так и сопутствующих препаратов.
Было показано, что прием нарлапревира в терапевтических дозах в комбинации с ритонавиром не приводит к удлинению скорректированного интервала QT (QTcF). Однако в дозах, многократно превышающих терапевтическую, нарлапревир в комбинации с ритонавиром может удлинять интервал QTcF. Поэтому нарлапревир следует применять с осторожностью у пациентов, одновременно принимающих препараты, удлиняющие интервал QT .
Передозировка
Максимальная концентрация нарлапревира в плазме была определена при применении нарлапревира в дозе 1500 мг однократно в сутки в сочетании с ритонавиром в дозе 100 мг однократно в сутки на протяжении 5 дней. При этом явления токсичности не наблюдались. Данные по передозировке нарлапревира отсутствуют.
Следует осуществлять общие профилактические мероприятия и тщательный мониторинг жизненных функций организма. Если пациент находится в сознании, следует вызвать рвоту, возможно применение активированного угля внутрь.
Пути введения
Меры предосторожности вещества Нарлапревир
Во время всего периода лечения рекомендуется контролировать показатели общего и биохимического анализа крови, а также уровень вирусной нагрузки.
Отмена терапии. Комбинированное лечение рекомендуется полностью прекратить в следующих случаях:
- при развитии вирусологического прорыва (увеличение уровня РНК вируса гепатита С на ≥1 lg 10 выше низшего уровня или определяемый уровень РНК вируса гепатита С во время лечения после первоначального падения ниже предела обнаружения);
- при сывороточном уровне РНК вируса гепатита С >100 МЕ/мл на 12-й нед лечения, свидетельствующем о недостаточной эффективности лечения и малой вероятности достижения стойкого вирусологического ответа;
- при наступлении беременности пациентки, получающей лечение нарлапревиром, ритонавиром, пэгинтерфероном альфа и рибавирином;
- при развитии декомпенсированного заболевания печени (цирроз печени класса В или С по классификации Чайлд-Пью).
Коррекция дозы или приостановление терапии. Снижение дозы нарлапревира и/или ритонавира во время терапии не допускается. В случае отмены терапии нарлапревиром по причине развития нежелательных реакций или неадекватного вирусологического ответа возобновление терапии нарлапревиром не допускается.
В случае развития нежелательных реакций, потенциально связанных с пэгинтерфероном альфа или рибавирином, и требующих коррекции дозы или приостановки терапии любым из этих лекарственных препаратов, необходимо руководствоваться указаниями, изложенными в инструкциях по применению соответствующего лекарственного препарата.
Снижение Hb ниже нормы отмечалось на 8–12 нед лечения у большей доли пациентов, получавших нарлапревир и ритонавир в комбинации с пэгинтерфероном альфа и рибавирином, в сравнении с пациентами, получавшими только пэгинтерферон альфа и рибавирин. В начале терапии нарлапревиром и ритонавиром в комбинации с пэгинтерфероном альфа и рибавирином чаще отмечалось снижение абсолютного числа лейкоцитов ниже нормы по сравнению с пациентами, получавшими только пэгинтерферон альфа и рибавирин. Однако после 4-й нед группы лечения по этому показателю не различались.
Влияние на способность к управлению транспортными средствами, механизмами. В настоящее время не были выявлены какие-либо эффекты нарлапревира, влияющие на способность управлять транспортными средствами и механизмами. Специальных исследований влияния нарлапревира на способность управлять транспортными средствами и механизмами не проводилось.
Из-за возможности появления утомляемости или сонливости на фоне комбинированной терапии нарлапревиром, ритонавиром, пэгинтерфероном альфа и рибавирином не рекомендуется управлять автомобилем и/или сложной техникой.

История появления и производитель
Проводились широкомасштабные клинические испытания нарлапревира, в том числе и на базе научно-исследовательского центра компании Шеринг Плау, которые подтвердили его высокий профиль безопасности и эффективности.

В странах Европы и США нарлапревир не зарегистрирован FDA, так как расценивается как устаревшая действующая субстанция. Он применяется только как составляющая комбинированной схемы лечения с включением интерферона. Эффективность нарлапревира как составляющей безинтерфероновой схемы терапии не изучена и не доказана.
Состав и форма выпуска
Как действует Нарлапревир
Нарлапревир в умеренной степени связывается с плазматическими белками. В печеночной ткани подвергается различным метаболическим превращениям. Выводится в виде метаболитов активных и неактивных преимущественно с содержимым кишечника и, в меньшей степени, с мочой.
Показания к применению
Нарлапревир показан пациентам с хроническим гепатитом С, у которых заболевание вызвано вирусом 1 генотипа. Его применение целесообразно:

Комбинацию определенных действующих веществ для конкретного пациента подбирает лечащий доктор.
Противопоказания
Нарлапевир не применяется как средство монотерапии, только в комбинации с другими лекарственными средствами.
Способ приема и дозировка
Нарлапревир – это только один из компонентов комплексной терапии. Обязательно сочетать это действующей вещество с другими противовирусными препаратами, а именно с ритонавиром, интерфероном и рибавирином.
Длительность терапии нарлапревиром такая же, как и других противовирусных средств в комбинированном лечении, варьируется от 24 до 48 недель.

Побочные действия
Все возможные побочные эффекты можно условно разделить на 3 группы:
- регистрирующиеся у 1 из каждых 10 пациентов (очень частые);
- отмечающиеся у 1 из каждых 100 пациентов (частые);
- регистрирующиеся менее, чем у 1 из 100 пациентов (редкие).
Среди очень частых возможных побочных эффектов пациенты отмечали астенический синдром (постоянная слабость и усталость, продолжительный упадок сил). При лабораторном обследовании наблюдалось снижение гемоглобина среди мужчин и женщин в одинаковой степени.
Среди не так часто встречающихся побочных реакций описаны:
- снижение аппетита на протяжении длительного времени;
- разлитая головная боль;
- сухой кашель;
- тошнота и эпизоды рвоты, боль в животе разлитого характера;
- кожный зуд в сочетании с различными видами сыпи;
- умеренной интенсивности болевые ощущения в поперечнополосатых мышцах и крупных суставах;
- температура около 37°С;
- анемия и лейкопения в общем анализе крови.
У ограниченного количества пациентов отмечались такие редкие побочные эффекты, как:
- фарингит и обострение герпесвирусной инфекции;
- снижение гормонсинтезирующей функции щитовидной железы;
- инверсия сна, кошмарные сновидения;
- повышение артериального давления и увеличение частоты пульса;
- боли в области прямой кишки и трещины слизистой анального прохода;
- болевые ощущения в поясничной области;
- нарушения выделительной функции почек;
- повышение функциональных проб печени.

Большинство пациентов отмечали, что побочные эффекты редко имели продолжительных характер и становились причиной для отмены противовирусной терапии.
Передозировка
В современной медицинской литературе не описаны случаи передозировки нарлапревира даже при приеме на протяжении 48 недель. Развитие передозировки этого лекарственного вещества возможно только при сознательном приеме большого количества таблеток (более 10-15 штук).
Взаимодействие с другими медикаментами
Оценить возможность лекарственного взаимодействия именно нарлапревира сложно, так как уже указывалось, что это составляющая комплекса противовирусного лечения, а не монотерапия. В большинстве фармакологических справочников указано, что такая комбинация не удлиняет интервал QT, то есть безопасна для пациентов с сердечно-сосудистой патологией.
Стоимость препарата
Особенности хранения
Минздрав уже дважды менял модель лекобеспечения больных ВИЧ, вирусными гепатитами и включенным в 2016 году в ту же госпрограмму туберкулезом: сначала закупку профильной номенклатуры вел федеральный центр, потом ее поручили регионам, затем какую‑то часть госзаказа взялся обслуживать Минздрав, делегировавший регионам право докупать необходимые пациентам препараты за свой счет. В 2017 году Минздрав совокупно выделил на закупочную кампанию более 17 млрд рублей.

Стоит заметить, что, в отличие от ВИЧ, требующего пожизненного приема АРВ‑препаратов, вирусный гепатит С (ВГС) уже в 2011 году научились излечивать, а к 2013‑му на глобальном рынке появились средства с терапевтической эффективностью до 100%.
Впрочем, мировая лекарственная эволюция, которой так долго ждали профильные пациенты, на объеме финансирования и структуре целевых госзакупок в России никак не сказалась: с момента централизации 2017 года выделяемая Минздравом на лечение ВГС сумма только сокращалась – от максимума, едва превысившего в 2018 году 1 млрд рублей, до 760 млн, заложенных в госбюджет на закупки 2019 года.
Такую динамику опрошенные Vademecum представители врачебного сообщества и участники рынка лекарственного госзаказа не смогли объяснить ничем, кроме общего для отрасли дефицита финансирования. И лишь один из наших собеседников на условиях анонимности высказался чуть более конкретно: лечение ВГС, в отличие, например, от онкологических и сердечно‑сосудистых заболеваний или даже ВИЧ, не входит в число приоритетных задач государства, а потому ни количественных, ни качественных прорывов на этом нозологическом направлении ждать не стоит.
Как же тогда быть с подписанной РФ в 2016 году Стратегией ВОЗ по элиминации (изгнанию, выдворению) вирусных гепатитов, предполагающей к 2030 году глобальное снижение заболеваемости на 90% и смертности на 65%? Похоже, никак. Что красноречиво подтверждает разительное отличие применяемых сегодня в России схем лечения от рекомендаций ВОЗ.
С 2013 года в большинстве развитых стран при лечении ВГС по возможности отказываются от схем, содержащих пегилированный интерферон: эффективность длительного, 24‑недельного, курса редко превышает 60%, препараты плохо переносятся пациентами. Российский вариант клинических рекомендаций по лечению ВГС, тем не менее, предлагает современные безинтерфероновые протоколы лишь в последних рядах терапии.
Зато сегмент пегинтерферонов, хоть и сужается в объеме закупок Минздрава, иллюстрирует собой все сбывшиеся надежды регуляторов – на импортозамещение и локализацию, на конкуренцию и снижение начальной цены аукционов.

Объемы розничных продаж пегинтерферонов неумолимо сокращаются. Если в 2016 году, по данным DSM Group, аптеки реализовали ПегИнтрона на 28 млн рублей, то в 2018‑м распродажи остатков снятого с производства и потерявшего в шесть раз в цене (до 1,6 тысячи рублей за упаковку) препарата принесли лишь 823 тысячи. Более популярный Пегасис подешевел не так резко (до 6,5 тысячи рублей за упаковку), но тоже не удержал прежнего уровня розничных продаж, упавших в два с лишним раза – с 69,9 млн рублей до 27,7 млн.
С 2010 года на мировом рынке стали появляться препараты прямого противовирусного действия (ПППД), первое поколение которых, правда, все еще требовало совместного применения пегинтерферона. Проникновение ПППД в Россию запаздывало, что вынуждало регуляторов вплоть до 2017 года при планировании закупок отдавать предпочтение интерфероновым схемам.
Первый в РФ ПППД – Совриад (симепревир) – зарегистрировала в 2013 году Janssen. Но лишь спустя три года, в 2016‑м, да еще и с оговоркой, что препарат может закупаться только по решению медицинской комиссии, симепревир был включен в перечень ЖНВЛП. В 2018 году оригинатор прекратил продвижение Совриада в связи с появлением на рынке новых, более эффективных препаратов от ВГС.
И регулятор, надо заметить, это стремление Janssen в последние два года поддерживал: в 2017‑м Минздрав приобрел 860 упаковок симепревира на 143,48 млн рублей, в 2018‑м – 1 200 упаковок на 171 млн рублей.
На 2019 год Минздрав запланировал закупку симепревира в заметно меньших объемах – всего на 53,45 млн рублей, заменив его, следуя курсом импортозамещения, Арлансой (нарлапревир) – отечественным препаратом с зарубежными корнями.

Несмотря на поздний лонч, нарлапревиру пообещали и оказали поддержку: включили в перечень ЖНВЛП. В 2018 году объем закупки Арлансы регионами превысил 248 млн рублей, в 2019‑м совокупный госзаказ вырастет за счет подключения Минздрава, запланировавшего приобретение нарлапревира на сумму 139,06 млн.
На момент регистрации в России первых поколений ПППД рекомендации ВОЗ уже содержали безинтерфероновые схемы терапии с эффективностью до 100%. Пионером этой линейки в РФ стал включенный в перечень ЖВНЛП на 2018 год в качестве средства для лечения ВГС первого типа комплексный препарат Викейра Пак (дасабувир; омбитасвир+паритапревир+ритонавир) от AbbVie.

До включения в перечень ЖНВЛП Совальди обходился закупающим его регионам в среднем по 187,9 тысячи рублей за упаковку. И тем не менее в 2018 году на долю софосбувира пришлось 15% от общего объема госзакупок – 800,92 млн рублей. Включение в ЖНВЛП заставило Gilead снизить предельную цену препарата до 126 тысяч рублей.
В открытых источниках информации о попытках кого‑либо из российских производителей получить у оригинатора лицензию на софосбувир нет. В Минздраве тематический запрос Vademecum оставили без ответа.
Этим протоколом ВОЗ в 2018 году воспользовалась Челябинская область, отказавшаяся от интерферонов в пользу приобретения даклатасвира и софосбувира. Регион закупил Даклинзу на 13 млн рублей, уступив по объему заказа только Москве и Минздраву, и законтрактовал одну из самых крупных партий Совальди – на 41,74 млн.
Тем временем Gilead уже готовится презентовать на рынке новые комбинации: Харвони (софосбувир+ледипасвир) для лечения первого генотипа ВГС и пангенотипичную Эпклусу (софосбувир+велпатасвир). Препараты, как следует из реестра КИ, завершили национальные клинические испытания в 2017 и 2018 годах соответственно. Заявки на регистрацию в Минздрав уже поданы, комбинации станут в РФ коммерчески доступны в 2019 году, заявили Vademecum в штаб‑квартире Gilead.
Несмотря на глобальную востребованность софосбувира и лончи дорогостоящих новинок, в целом продажи препаратов для терапии ВГС у Gilead падают. В 2018 году выручка компании от реализации Совальди, Epclusa, Harvoni сократилась в 2,5 раза – до $3,7 млрд. В Gilead нисходящий тренд объясняют снизившейся из‑за уступок средней ценой препаратов, излечением пациентов и усилением позиций конкурентов, в первую очередь AbbVie и MSD.
В России продукты этих компаний – Мавирет (глекапревир+пибрентасвир) от AbbVie для лечения всех генотипов ВГС и Зепатир (гразопревир+элбасвир) от MSD для терапии наиболее часто встречающихся 1 и 4 генотипов – зарегистрированы в апреле и сентябре 2018 года соответственно.
Зепатир от MSD появился на отечественном коммерческом рынке только в начале 2019 года, однако тут же был заявлен в региональных тендерах – препарат по 190 тысяч рублей за упаковку приобрела поликлиника №9 Владивостока, а в феврале‑марте аукционы на закупку комбинации гразопревир+элбасвир объявили администрация Орловской области и Ставропольская краевая инфекционная больница. Как сообщили Vademecum в MSD, компания сейчас изучает возможность подачи заявки на включение Зепатира в перечень ЖНВЛП.
Сложно сконструированная модель госпрограммы по лекарственному обеспечению пациентов с ВИЧ, вирусными гепатитами и туберкулезом, ставит больных с ВГС в уязвимое положение. Государственная стратегия по противодействию распространения ВИЧ утверждена и по возможности реализуется. Глобальная стратегия ВОЗ по вирусным гепатитам Россией подписана, но эта виза, как уже было замечено выше, пока не получила сущностного сопровождения.
Указывающие на это обстоятельство пациентские организации, в частности, отмечают, что включенный с таким трудом в перечень ЖНВЛП софосбувир в плане‑графике закупок Минздрава на 2019 год так и не появился, а применяемый в одной с ним схеме, но дешевый даклатасвир ведомство решило приобретать.
В ответ на новый запрос Vademecum в Минздраве еще раз пояснили: объем выделяемых бюджетом средств рассчитан только на пациентов с ВГС и коинфекцией ВИЧ.
Если выделить аудиторию больных ВГС и поставить задачу вылечить всех, то денег на это может потребоваться даже больше, чем тратится сейчас на ВИЧ, считает Алексей Михайлов, но оговаривается: сводные по стране эпидемические данные по вирусным гепатитам пока не сформированы.
В данной статье можно ознакомиться с инструкцией по применению лекарственного препарата Нарлапревир. Представлены отзывы посетителей сайта - потребителей данного лекарства, а также мнения врачей специалистов по использованию Нарлапревира в своей практике. Большая просьба активнее добавлять свои отзывы о препарате: помогло или не помогло лекарство избавиться от заболевания, какие наблюдались осложнения и побочные эффекты, возможно не заявленные производителем в аннотации. Аналоги Нарлапревира при наличии имеющихся структурных аналогов. Использование для лечения хронического вирусного гепатита C у взрослых, детей, а также при беременности и кормлении грудью. Состав препарата.
Нарлапревир - это сильный пероральный ингибитор NS3 сериновой протеазы вируса гепатита C. Оказывает ингибирующее воздействие путем ковалентного, но обратимого связывания с сериновым активным центром протеазы вируса гепатита C посредством кетоамидной функциональной группы. Тем самым прием Нарлапревира ингибирует полипротеиновый процессинг вируса и предотвращает его репликацию в инфицированных клетках хозяина.
Состав
Нарлапревир + вспомогательные вещества.
Фармакокинетика
Фармакокинетика Нарлапревира не описана. Известно, что серьёзным недостатком нарлапревира является быстрое падение концентрации препарата в крови, вынуждающее применять его совместно с фармакокинетическим усилителем ритонавиром, обладающим гепатотоксичностью и плохим профилем межлекарственного взаимодействия.
Показания
- хронический вирусный гепатита C, вызванный вирусом генотипа 1, у пациентов старше 18 лет с компенсированным поражением печени, в комбинации с ритонавиром, пэгинтерфероном альфа и рибавирином, ранее не получавших противовирусную терапию пэгинтерфероном альфа и рибавирином, или у которых предшествующее двухкомпонентное лечение пэгинтерфероном альфа и рибавирином было неэффективным.
Формы выпуска
Таблетки, покрытые оболочкой 100 мг.
Инструкция по применению и режим дозирования
Таблетки Нарлапревир принимают внутрь, 200 мг 1 раз в день.
Нельзя использовать в качестве монотерапии. Следует применять в составе комбинированной терапии с другими противовирусными препаратами (ритонавиром, пэгинтерфероном альфа и рибавирином).
Побочное действие
- фарингит;
- герпесвирусная инфекция;
- анемия, лейкопения, нейтропения, лимфопения, тромбоцитопения;
- аллергические реакции;
- гипотиреоз (состояние, обусловленное длительным, стойким недостатком гормонов щитовидной железы);
- снижение аппетита;
- гиперурикемия (состояние, при котором уровень мочевой кислоты в крови превышает предельные показатели);
- гипертриглицеридемия;
- расстройство сна, бессонница;
- снижение интереса;
- головная боль, головокружение;
- дисгевзия (расстройство вкуса);
- сонливость.
Противопоказания
- генотипы вируса, отличные от субтипа 1b;
- беременность или период кормления грудью;
- детский возраст до 18 лет;
- тяжелая нейтропения;
- печеночная недостаточность;
- предшествующее лечение хронического гепатита C ингибиторами протеазы вируса гепатита C;
- дефицит лактазы, непереносимость лактозы, глюкозо-галактозная мальабсорбция;
- гиперчувствительность к компонентам препарата;
- соответствующие противопоказания к применению ритонавира, пэгинтерферона альфа и рибавирина, так как Нарлапревир следует применять только в комбинации с этими препаратами.
Применение при беременности и кормлении грудью
Противопоказано применение Нарлапревира при беременности и в период лактации (грудного вскармливания).
Применение у детей
Противопоказан в детском и подростковом возрасте до 18 лет.
Применение у пожилых пациентов
Пациентам пожилого возраста снижение дозы не требуется.
Особые указания
Запрещено применять Нарлапревир в качестве монотерапии.
Лечение должно проводиться под тщательным мониторингом врача, обладающего достаточным опытом терапии хронического гепатита C.
Лекарственное взаимодействие
Так как таблетки Нарлапревир применяются в комбинации с ритонавиром, пэгинтерфероном альфа и рибавирином, следует учитывать возможные межлекарственные взаимодействия сопутствующей терапии с каждым из компонентов терапии.
При применении с лекарственными препаратами, являющимися субстратами, ингибиторами и/или индукторами изофермента CYP3A4, возможно изменение концентрации как действующего вещества нарлапревира и ритонавира, так и сопутствующих препаратов.
Аналоги лекарственного препарата Нарлапревир
Структурные аналоги по действующему веществу:
Аналоги препарата Нарлапревир по фармакологической группе (противовирусные, за исключением ВИЧ, средства):
- Авонекс;
- Актавирон;
- Актипол;
- Альфаферон;
- Амизон;
- Амиксин;
- Арбидол;
- Арланса;
- Ацикловир;
- Бараклюд;
- Бонафтон;
- Валацикловир;
- Вальцит;
- Виворакс;
- Виразол;
- Виролекс;
- Виферон;
- Генферон;
- Гервиракс;
- Герпевир;
- Герперакс;
- Герпинат;
- Гроприносин;
- Даклатасвир;
- Даклинза;
- Девирс;
- Зовиракс;
- Изопринозин;
- Ингавирин;
- Инозин пранобекс;
- Интераль;
- Интерферон;
- Инфагель;
- Кагоцел;
- Лавомакс;
- Лакринат;
- Лизавир;
- Медовир;
- Минакер;
- Моликсан;
- Невирпин;
- Неовир;
- Номидес;
- Оксолин;
- Осельтамивир;
- Полудан;
- Провирсан;
- Реленза;
- Ремантадин;
- Рибавирин;
- СинноВекс;
- Совриад;
- Софосбувир;
- Суправиран;
- Тамифлю;
- Телбивудин;
- Тилаксин;
- Триворин;
- Фавирокс;
- Фамацивир;
- Фенистил Пенцивир;
- Ферровир;
- Цивалган;
- Цикловакс;
- Цикловир;
- Цитивир;
- Экставиа;
- Элгравир;
- Энтекавир;
- Эразабан.
Отзыв врача инфекциониста
Препарат Нарлапревир из моих пациентов с хроническим вирусным гепатитом C получал только один человек. Это была комплексная терапия четырьмя препаратами. Поэтому про переносимость конкретно Нарлапревира сложно что-то сказать. Со слов пациента, его беспокоили периодические головные боли, неприятные ощущения в животе, почти всегда мучила бессонница. Иногда он отмечал ухудшение аппетита и замечал, что вкус некоторых продуктов был не таким, как ранее, до начала лечения. В выписке из стационара имеются данные об изменении некоторых лабораторных показателей крови, а именно снижение уровня гемоглобина, количества эритроцитов и общего числа лейкоцитов.
Читайте также:


