Острые кишечные инфекции герпес вирусом
Герпес-вирусные инфекции (от греч. herpes — ползучий) — группа инфекционных заболеваний, вызываемых представителями семейства герпес-вирусов (Herpesviridae). Антигенных серотипов, выделенных от человека, восемь: вирус простого герпеса 1-го и 2-го типов, вирус ветряной оспы — опоясывающего герпеса или вирус герпеса человека 3-го типа, вирус герпеса человека 4-го типа — вирус Эпштейна–Барр (ВЭБ) — вызывает инфекционный мононуклеоз; вирус герпеса человека 5-го типа — цитомегаловирус (ЦМВ), вирус герпеса человека 6-го, 7-го типов — вызывают внезапную экзантему и синдром хронической усталости, вирус герпеса человека 8-го типа ассоциирован с саркомой Капоши [1]. Все герпес-вирусы являются ДНК-содержащими и сходны по морфологии, типу нуклеиновой кислоты, способу репродукции в ядрах инфицированных клеток.
В РФ сохраняется высокий уровень детской инфекционной заболеваемости [2]. Отмечается возрастание роли инфекций, вызванных вирусами цитомегалии, ВЭБ, герпеса 1-го, 2-го, герпеса 6-го и 8-го типов. Среди детской популяции герпетическая инфекция широко распространена. Так, 70–90% детей 3-летнего возраста имеют достаточно высокий титр вируснейтрализующих антител к вирусу простого герпеса 1-го типа [3]. Эти инфекции у детей часто принимают хроническое течение вследствие персистенции возбудителя и формирования необратимых изменений в органах и системах.
За последние пять лет увеличилось число детей в возрасте до одного года, умерших от генерализованных вирусных инфекций [4]. Велика роль герпес-вирусных инфекций, особенно цитомегаловирусной, в формировании перинатальной патологии и младенческой смертности. Риск развития внутриутробной инфекции зависит от характера взаимоотношений между организмом беременной женщины и микроорганизмом (первичное заражение во время беременности или реактивация ранее приобретенной инфекции).
Проблема врожденной инфекционной патологии является приоритетной для России [5].
Иммуногенез герпес-вирусной инфекции. Длительное нахождение герпес-вируса в организме человека становится возможным благодаря сложной стратегии противоборства и ускользания от иммунной системы хозяина. В достижении этого состояния можно выделить три пути стратегии возбудителя:
Вирус простого герпеса. В инфицированных клетках вирус простого герпеса образует внутриядерные включения и гигантские клетки, оказывает выраженное цитопатическое действие, проявляющееся округлением и образованием многоядерных клеток. Вирус является слабым индуктором интерферона, в связи с чем инактивация вирусной ДНК внутри клеток не наступает и он сохраняется внутри клеток длительное время, периодически вызывая рецидивы заболевания.
ЦМВ. Сущность проблемы ЦМВ-инфекции в том, что последняя относится к так называемым оппортунистическим инфекциям, клинические проявления которых возможно в условиях первичного или вторичного иммунодефицита.
ЦМВ поражает разнообразные клетки, чаще всего лейкоциты (лимфоциты, моноциты), эпителиальные клетки (дыхательных путей, слюнных желез, почек). С клеток крови ЦМВ с большим постоянством переходит на эндотелий, тропизм к которому у него весьма выражен. Поврежденные эндотелиальные клетки постоянно обнаруживаются в токе крови при активной/реактивированной ЦМВ-инфекции. Повреждение эндотелия сосудов имеет собственное патогенетическое значение в формировании органных поражений, так как вызывает ишемию или кровоизлияния в различные ткани [6].
В раннем неонатальном периоде (0–7 дней) у детей с ЦМВ-инфекцией наблюдались симптомы интоксикации, серый колорит кожи, выраженная мышечная гипотония, большая первоначальная потеря массы тела, синдром рвоты или срыгиваний, признаки угнетения ЦНС. В позднем неонатальном периоде (от 7 дней до одного мессяца) анализ клинических проявлений острой ЦМВ-инфекции выявляет поражение многих органов и систем. Так, у всех детей обнаруживаются гипоксически-ишемическая энцефалопатия с трансформацией синдрома угнетения в синдром гипервозбудимости, проявления анемии, патологическая гипербилирубинемия, увеличение печени и селезенки.
ВЭБ относится к подсемейству бета-герпес-вирусов. Вирусный геном заключен в нуклеокапсид, который покрыт гликопротеидным тегументом gp350, являющимся фактором рецепторного взаимодействия [7]. Проникновение вируса в В-лифоциты осуществляется через рецептор этих клеток CD21-рецептор к C3d-компоненту комплемента. ВЭБ-инфекция широко распространена среди людей, причем первичное инфицирование, как правило, происходит в антенатальном или детском возрасте, но манифестация ВЭБ-инфекции в виде отчетливых клинических проявлений инфекционного мононуклеоза в большинстве случаев происходит в школьном возрасте при различного рода иммунопатологических реакциях. Манифестация инфекции в виде инфекционного мононуклеоза может осложняться поражением печени, слизистой оболочки желудка, ткани почек, лимфоидного аппарата.
Особый характер взаимодействия микро- и макроорганизма при хронических персистирующих инфекциях обусловливают трудности лабораторной диагностики. Обнаружение возбудителя не может быть единственным критерием подтверждения диагноза. Необходима комплексная оценка клинических и лабораторных данных для постановки диагноза.
Цель исследования. Определить клинические особенности течения персистирующих герпес-вирусных инфекций у детей и оценить значимость комплекса лабораторных исследований, в том числе показателей общей иммунологической реактивности у больных при персистирующем у них инфекционном процессе.
Материал и методы исследований. Под наблюдением находилось 63 пациента в возрасте от одного месяца до 7 лет, из них детей до одного года было 25, от одного года до трех лет — 22 и старше трех лет — 15 больных. Среди обследованных детей преобладали пациенты первых двух лет жизни — 47 детей (74,6%) и старше двух лет было 15 больных (25,4%).
Результаты. В клинической диагностике персистирующих инфекций у детей следует отводить первостепенное значение неблагополучию акушерского анамнеза матерей больных детей.
Беременность и роды были осложненными у большинства матерей наблюдаемых детей, чаще всего у них отмечались гестозы и угроза выкидыша, рождение недоношенных, в родах гипоксия плода, преждевременная отслойка плаценты, кесарево сечение и др. У 32 женщин из 63 (50,7%) были различные соматические заболевания (хронический пиелонефрит, кольпит, анемия, аутоиммунный тиреоидит и др.). При обследовании беременных женщин было выявлено как моноинфицирование (у 30 из 63–47,6%), так и сочетания инфекций (у 16 из 63–25,4%). Наиболее часто обнаруживались герпес-вирусы и цитомегаловирусы (суммарно у 27 женщин из 63–43%) и реже другие возбудители — хламидии, микоплазмы (у 11 беременных — 17,4%). Высокая частота вышеуказанных осложнений свидетельствует о несомненной роли инфекции как отягощающего фактора в течение гестационного периода и родов.
Заподозрить внутриутробную или персистирующую инфекцию у детей можно было по высокой степени поражения у детей различных органов и систем: ЦНС (71,4%), органов дыхания (88,8%), желудочно-кишечного тракта (95,2%), поражению глаз (31,7%), лимфатического аппарата (15,9%).
В процессе наблюдения за детьми в недалеком прошлом все дети обследовались на состояние микробиоценоза кишечника.
У всех детей обнаруживались нарушения как в основных компонентах биоценоза, так и в составе условно-патогенной флоры. Следует отметить, что у всех пациентов проводилась коррекция микробиоценоза повторными курсами пре- и пробиотиков, однако восстановления микрофлоры до нормобиоценоза не наблюдалось ни у одного пациента. Следовательно, без выявления и адекватного лечения основного заболевания не удается курировать дисбиотические нарушения в организме ребенка.
Закономерен вопрос о правильности выбора комплекса диагностики внутриутробной и персистирующей инфекции у детей. В зависимости от возраста пользуются разными методами диагностики. Важное значение отводится сбору семейного анамнеза. Диагностика внутриутробных инфекций у детей должна опираться на клинические проявления как общего характера, так и на типоспецифические ее признаки, а также основываться на анализе комплекса лабораторных методов обследования [8].
При оценке клинических анализов крови у наблюдаемых детей обращали на себя внимание значительные отклонения в различных показателях гемограммы: выраженная анемизация (у 31,7% пациентов), нейтропения (у 19%), лимфоцитоз (у 27%), лейкопения с лимфоцитопенией (36,5%), ускорение СОЭ (у 27%), что в совокупности свидетельствовало о наличии воспалительного процесса в организме с выраженным снижением иммунореактивности у детей.
При скрининговом серологическом обследовании методом ИФА на внутриутробные инфекции у детей наиболее часто выявлялись положительные титры типоспецифических антител класса IgM и/или IgG к герпес-вирусам. Диагностические титры антител класса IgM и IgG определялись к ЦМВ (у 9 детей), к HV 1-го, 2-го типа (у 9 детей). Антитела к антигенам ВЭБ обнаруживались у 20 детей, из них у 10 детей были антитела класса IgG к раннему антигену ВЭБ и антитела класса IgM к капсидному антигену ВЭБ, что свидетельствовало об активной фазе ВЭБ-инфекции. Остальные 10 пациентов имели антитела класса IgG к нуклеарному (ядерному) антигену ВЭБ, что расценивалось как поздняя стадия инфекции.
У детей при персистирующем течении с реактивацией инфекции, которое чаще возникало после провоцирующих воздействий (ротавирусные диареи, ОРВИ, профилактические прививки) ПЦР-тесты при исследовании биосубстратов: кровь, осадок мочи, секрет из зева давали положительные результаты с последующим нарастанием титра типоспецифических антител по данным ИФА.
Совокупность проведенных исследований позволила выделить у обследованных больных следующие формы инфекций: моноинфекции были у 21 пациента — 31,8% (ЦМВ — у 5 детей, HV 1-го, 2-го типа — у 6 детей и ВЭБ — у 10), у 42 детей из 63 (68,2%) обнаруживались микст-инфекции. У 23 детей была ассоциация ЦМВ с герпес-вирусами (у 9 детей с HV 1-го, 2-го типа, у 3 детей — с HV 6-го типа и у 11 детей — с C. albicans и хламидиями). Микст-формы герпеса 1-го, 2-го типа были выявлены у 9 больных, у них были ассоциации с микоплазмами и хламидиями. Ассоциации ВЭБ были обнаружены у 10 детей (5 больных имели ассоциацию с ЦМВ, пациента — с HV 6-го типа и 2 больных — с Yersinia pseudotuberculosis).
Из 63 больных у 21 (33,3%) с моноинфекцией течение заболевания расценивалось как латентное (с ЦМВ-инфекцией у 5 и HV 1-го, 2-го типа у 6) и как персистирующее (у 10 детей с ВЭБ-инфекцией). У 14 детей из 42 с микст-инфицированием (у 1/3) было персистирующее течение инфекционного процесса (у 3 детей с ЦМВ-инфекцией в ассоциации с HV 6-го типа и у 11 детей с ЦМВ-инфекцией в ассоциации с C. albicans и хламидиями). У 28 детей из 43 (у 2/3) наблюдалось персистирующее течение с реактивацией инфекции (у 9 детей с ЦМВ-инфекцией в ассоциации с HV 1-го, 2-го типа; у 9 детей с HV 1-го, 2-го типа в ассоциации с хламидиями или микоплазмами и у 10 детей с ВЭБ инфекцией в ассоциации с ЦМВ, HV 6-го типа и ВЭБ в ассоциации с Y. pseudotuberculosis).
Коэффициент фагоцитарной защиты у детей с моноинфицированием и микст-формами герпесвирусной инфекции оказался достоверно сниженным по сравнению со средневозрастной нормой для здоровых детей (0,634 ± 0,05 усл. ед. и 0,540 ± 0,03 усл. ед. соответственно при норме 0,946 ± 0,03, Р1–2 и Р2–3 0,05). Недостаточность защиты клеточно-фагоцитарного звена иммунитета играет важную роль в патогенезе герпес-вирусных инфекций, что должно учитываться в лечении этих заболеваний.
Отклонение величины показателя ИЛМП имело противоположную направленность, она оказывалась достоверно повышенной как при моноинфекции, так и при микст-формах герпес-вирусных инфекций по сравнению с контролем (Р1–3 и Р2–3 0,05. Увеличение показателя ИЛМП у детей с герпес-вирусной инфекцией еще раз подтверждает лимфотропность вирусных антигенов.
ЛИИ оказался достоверно повышенным у больных с микст-формами герпес-вирусной инфекции по сравнению со средневозрастной нормой в контроле (Р2–3 0,05), они имели лишь тенденцию к повышению. Однако при оценке индивидуальных показателей ЛИИ у детей с моноинфицированием герпес-вирусами выявились существенные особенности. У 13 детей из 21 (61,9%) ЛИИ был ниже возрастной нормы, что отражало фазу положительной анергии к совершенно определенному антигену. Это свидетельствует, что организм защищен сейчас только от специфических антигенов, однако он остается уязвимым в отношении других патогенов, то есть низкий индекс интоксикации отнюдь не указывает на полное благополучие организма.
Полученные результаты исследований подтверждают выраженность иммунного дисбаланса как в клеточно-фагоцитарном звене иммунитета, так и в гуморальном, а также свидетельствуют о значимости эндогенной интоксикации у больных с микст-формами герпес-вирусной инфекции и уязвимости иммунной защиты у детей и при моноинфицировании.
Клинический пример. Андрей С., 2 года 5 мес., поступил в стационар с жалобами на высокую температуру — 39 °С, однократную рвоту, сниженный аппетит и жидкий стул 5 раз в сутки. Болен в течение двух недель ОРВИ, получил амбулаторно симптоматическое лечение. К концу второй недели ухудшилось состояние, рецидив лихорадки — 39 °C и дисфункция кишечника. Направлен на госпитализацию.
Анамнез жизни. От первой беременности, протекала с угрозой выкидыша, нефропатией, преэклампсией в родах. Во время беременности перенесла ОPВИ с лимфаденитом. Обследование на пренатальные инфекции, обнаруживались антитела класса IgG к антигенам ЦМВ и вирусу герпеса 1-го, 2-го типа. Лечение не проводилось. Роды в срок, масса при рождении 3500 г, длина 51 см. К груди приложен сразу, сосал активно, грудное вскармливание до года, прикормы вводились в 5 и 6 месяцев. Адаптация к пище нормальная. В массе прибавки достаточные, в 2 г. 5 мес — масса 14 кг 810 г, рост 93 см.
Состояние здоровья в течение первого года жизни неблагополучное. Длительно держалась желтуха, в возрасте 3 недель: общий билирубин — 315,1 мкмоль/л, непрямой — 297,3 мкмоль/л, прямой — 17,8 мкмоль/л. Одновременно с желтухой был неустойчивый стул. В 1-месячном возрасте неврологом установлен диагноз перинатального поражения ЦНС, гипоксическо-ишемического генеза, гипертензионный синдром.
К возрасту 6 мес были обнаружены изменения в гемограмме: гемоглобин — 112 г/л, эритроциты — 4,2 × 10 12 /л, лейкоциты — 7,8 × 10 9 /л, сегментоядерные нейтрофилы — 12%, лимфоциты — 67%, моноциты — 12%, эозинофилы — 8%, базофилы — 1%, СОЭ — 3 мм/час. В повторных анализах крови во 2-м полугодии продолжала выявляться нейтропения. Консультирован гематологом, установлен диагноз доброкачественной нейтропении детского возраста. В 10 мес в анализе крови выявлена анемия (гемоглобин — 107 г/л, эритроциты — 3,81 × 10 12 /л, цветовой показатель — 0,84, тромбоциты — 280 × 10 9 /л, сегментоядерные нейтрофилы — 11%, лимфоциты — 76%, моноциты — 90%, эозинофилы — 3%, базофилы — 1%). Гематологом назначено лечение Сорбифером дурулесом, курс 1 месяц.
Осмотрен ортопедом: отмечено ограниченное отведение бедер. В один год на УЗИ органов брюшной полости определялся перегиб в области шейки желчного пузыря, холестаз. Осмотр генетика: диагностирована недифференцированная дисплазия соединительной ткани с поражением костно-мышечной системы. В 1 г. 5 мес перенес острый энтероколит неуточненной этиологии, госпитализировался в стационар на 10 дней, получал лечение метронидазолом и Энтеролом. В течение 1,5 лет переносит частые ОРВИ с повышением температуры до 38,8 °С в течение 3–4 дней и катаральными явлениями.
Объективные данные. При последней госпитализации отмечались явления назофарингита в течение 5 дней, лихорадка до 39 °С 2 дня, кожные покровы без сыпи. При осмотре — гиперемия зева и увеличение подчелюстных, передних и заднешейных лимфоузлов, стул учащенный до 3 раз в сутки, с 5 дня лечения — оформленный. ЛОР-врачом диагностирован хронический тонзиллит и аденоидит, в фазе обострения.
Обследование. В мазке из зева — высев гемолитического стрептококка. Посевы на патогенную кишечную флору отрицательные. ИФА на ротавирус — отрицательный. Реакция непрямой гемагглютинации (РНГА) с кишечными диагностикумами — отрицательные.
Гемограмма при поступлении: гемоглобин 104 г/л, эритроциты — 3,7 × 10 12 /л, цветовой показатель — 0,85, лейкоциты — 6,4 × 10 9 /л, палочкоядерные нейтрофилы — 4%, сегментоядерные — 72%, лимфоциты — 18%, моноциты — 4%, эозинофилы — 2%, СОЭ — 4 мм/час.
Гемограмма в динамике: гемоглобин — 109 г/л, эритроциты — 3,4 × 10 12 /л, лейкоциты — 7,8 × 10 9 /л, палочкоядерные нейтрофилы — 19%, сегментоядерные — 42%, лимфоциты — 28% (широкоплазменные лимфоциты), моноциты — 8%, плазматические клетки — 1%, эозинофилы — 2%, СОЭ — 13 мм/час. В дальнейшем — красная кровь оставалась без динамики, число лейкоцитов не изменялось, нарастал лимфоцитоз до 43% (широкоплазменные формы), моноцитов до 12%, СОЭ повысилась до 20 мм/час.
Анализ мочи без отклонений от нормы (пятикратно). В биохимическом анализе крови — умеренная гипоальбуминемия, печеночные пробы — в норме. ИФА на специфические антитела к антигенам ЦМВ класса IgM — отрицательный, класса IgG — положительный. Маркеры ДНК-ЦМВ в осадке мочи и в секрете из зева методом ПЦР не найдены. ИФА на специфические антитела к хламидийному антигену (Chlamydia pneumoniae) — положительный в титре 1:80. Маркеры ДНК Ch. pneumoniae в мазке из носоглотки методом ПЦР — положительный. ИФА с микоплазменным антигеном — IgM и IgG — отрицательные, с герпес-вирусами 1-го, 2-го типа — IgM и IgG отрицательные. ИФА на специфические антитела к антигенам ВЭБ: IgM к капсидному антигену — отрицательный, IgG к раннему антигену — положительный и IgG к ядерному антигену (IgGNA) — положительный (> 0,5 ед.). Совокупность данного анализа была индикатором активной фазы мононуклеозной инфекции.
После проведенного обследования ребенку была назначена адекватная комплексная терапия (Cумамед, Ликопид с последующим переходом на Виферон, витамины А, Е, Пиридоксин, пробиотики — курс Примадофилуса). Наблюдение за ним продолжается.
Выводы
- В пользу диагностики персистирующих инфекций у детей свидетельствует отягощенный акушерско-гинекологический и соматический анамнез, а также инфекционный фактор беременных женщин.
- Заподозрить внутриутробное инфицирование у детей раннего возраста можно по высокой степени поражения различных органов и систем: ЦНС, органов дыхания, пищеварения, лимфатического аппарата.
- Диагностика внутриутробных инфекций должна базироваться на клинических проявлениях болезни и основываться на комплексе лабораторных и иммунологических методов исследования с их оценкой в динамике (в 1 мес, 3 мес, 6 мес и в 1 год жизни).
- Правильность выбора комплекса клинических и лабораторных тестов (ИФА в динамике, ПЦР-тесты с различными биосубстратами) приводит к своевременной диагностике внутриутробных инфекций и позволяет выявить моноинфицирование или микст-формы при их длительной персистенции.
- Для суждения о состоянии общей иммунологической реактивности детей с персистирующими герпесвирусными инфекциями может использоваться оценка интегральных показателей (КФЗ и ИЛМП): чем меньше величина КФЗ, тем больше выражен риск прорыва защитного барьера на пути инфекции.
- Наиболее неблагоприятное персистирующее течение имеют микст-формы герпесвирусной инфекции (ЦМВ, герпес, ВЭБ) или их сочетания с внутриклеточными возбудителями.
Литература
Ф. Н. Рябчук, кандидат медицинских наук, доцент
З. И. Пирогова, кандидат медицинских наук, доцент
СПбМАПО, Санкт-Петербург
С неприятными проявлениями герпеса знакомы очень многие. Это неудивительно, ведь по данным ВОЗ более 78% населения планеты инфицированы самыми распространенными типами вируса: 67% заражены вирусом простого герпеса 1 типа, и еще 11% – вирусом простого герпеса 2 типа.
Что же такое герпес, из-за чего он бывает, чем опасен, и как его нужно лечить? Имея знания о болезни, можно минимизировать риск ее обострения, а главное – избежать осложнений.

Рисунок 1 - Герпес на губах
Герпес – это вирус
Источник заболевания – так называемые герпесвирусы. Это ДНК-содержащие микроорганизмы, являющиеся возбудителями разного рода инфекций.
Первичное попадание вируса в организм обычно происходит через слизистые оболочки (хотя не исключается попадание и через поврежденную кожу). Преодолев тканевые барьеры, вредоносные микроорганизмы попадают в кровь и лимфу и разносятся по всему организму. Они способны проникать в клетки внутренних органов и нервных окончаний. Особенность и опасность герпеса в том, что он генетически внедряется в ядро нервных клеток, после чего остается в организме навсегда.
Многие люди даже не догадываются, что являются носителями вируса, поскольку патология в большинстве случаев протекает бессимптомно, ничем себя не проявляя (это называется латентным состоянием).
Рисунок 2 - Простой герпес
Симптомы герпеса разных типов
Существует несколько типов вируса герпеса – они отличаются по своим проявлениям. Чаще всего в медицинской практике встречаются такие диагнозы, как ВПГ-1 и ВПГ-2 – это сокращенное название вирусов простого герпеса 1 и 2 типов.
Внешне заболевание проявляется в виде высыпаний. Они представляют собой один или целое скопления пузырьков с жидким содержимым. На вопрос, может ли быть температура при герпесе, ответ положительный: многие больные жалуются на повышение температуры, головные боли и общую слабость.
В среде медиков есть и другое название патологии: увидев в своей медкарте такой диагноз, как оральный или лабиальный герпес, знайте, что речь идет о вирусе простого герпеса первого типа.
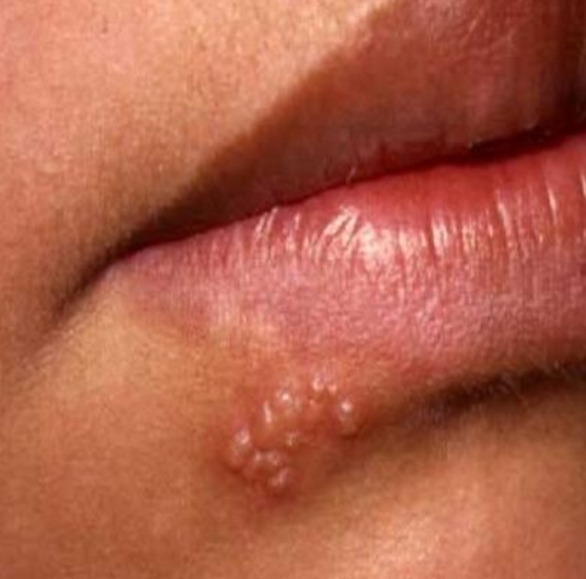
Рисунок 3 - Герпес на губе обычно сильно чешется
Второй тип простого герпеса сопровождается развитием генитальных (половых) инфекций. Заболевание в большинстве случаев протекает бессимптомно или, как и при лабиальном герпесе, сопровождается появлением пузырьков (язвочек), но только в области наружных половых органов. Другие признаки ВПГ-2 – температура, ломота в теле, усталость, увеличение лимфатических узлов на гениталиях. Чаще всего болезнь передается половым путем, но инфицирование может произойти и от человека с лабиальным герпесом.
Вирус 3 типа, он же вирус герпеса Зостер, – виновник ветряной оспы. Чтобы заразиться, достаточно вступить в разговор с больным человеком (передача происходит воздушно-капельным путем). Переболев ветрянкой, человек на всю жизнь остается носителем этого вируса. В случае рецидива возникает риск развития опоясывающего лишая.
Для данного заболевания характерно появление по всему телу зудящих высыпаний, а также повышенная температура.
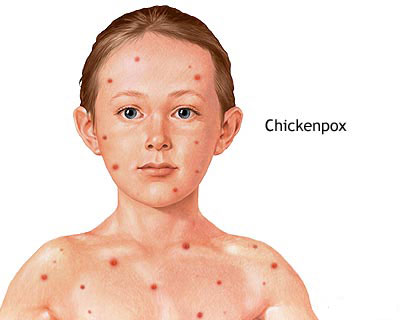
Рисунок 4 - Ветреная оспа
Герпес 4 типа вызывает такое серьезное инфекционное заболевание, как мононуклеоз. Эта болезнь сопровождается увеличением лимфатических узлов и повышенной температурой, больной жалуется на боль в горле и общую слабость. Поражаются также печень и селезенка.
Герпес 5 типа провоцирует развитие цитомегаловируса. Заболевание проявляется по-разному, в зависимости от того, какой орган поражен. Насморк, нарушения в работе желудочно-кишечного тракта, воспалительные заболевания половых органов – все это может быть признаком патологии.
Помимо вышеописанных, различают также герпес 6, 7 и 8 типов. Сейчас ученые занимаются изучением этих вирусов.
Герпес – из-за чего он появляется?
Риск подхватить инфекцию возникает с самого раннего возраста, ведь вокруг маленького ребенка находится огромное количество взрослых, большая часть которых являются носителями герпеса. Заражение может произойти и в утробе инфицированной матери.
Итак, от чего может возникнуть герпес на губах? Дети (и взрослые) часто заражаются при поцелуях, а также вследствие использования одной посуды. Если рядом находится человек с герпесом, который кашляет или чихает, высок риск инфицирования воздушно-капельным путем. Кроме того, вирус передается половым путем (в первую очередь это касается ВПГ-2). В группу риска также входят люди, которым переливают кровь.
- заболевания – эндокринные, вирусные и бактериальные;
- переохлаждение;
- стрессы;
- истощение организма;
- переутомление;
- травмы;
- нарушения обмена веществ.
У женщин еще одним провоцирующим фактором является менструация.
Есть ли профилактика от герпеса?
Чтобы противостоять вирусу, нужен крепкий иммунитет. Поэтому тем, кто страдает от частой простуды на губах, нужно уделить внимание своей иммунной системе. Позаботьтесь о здоровом, сбалансированном питании, не забывайте о спортивных занятиях, соблюдайте нормальный график дня (в первую очередь обеспечьте себе полноценный сон) и постарайтесь избавиться от вредных привычек (курение и т.п.).
Важно соблюдать элементарные правила гигиены, включая регулярное мытье рук. Рекомендуется использовать индивидуальные средства гигиены. В период инфекционных эпидемий по возможности желательно избегать пребывания в людных местах.
Для снижения риска генитального герпеса следует пользоваться презервативами.
Как узнать о наличии вируса?
Уже при первичном осмотре пациента врач может определить наличие герпеса (зачастую за врачебной помощью обращаются люди, у которых есть визуальные проявления болезни). Но для того, чтобы подтвердить диагноз и определить степень развития инфекции, назначаются лабораторные исследования.
Анализы важны в момент планирования беременности, поскольку вирус опасен для плода. Обязательными являются анализы и для пациентов, готовящихся к трансплантации.
Рисунок 5 - Диагностика герпеса
Как развивается простой герпес?
- Все начинается с зуда и/или пощипывания в том месте, где развивается герпес – как мы уже выяснили, чаще всего это область носогубного треугольника. Кожа краснеет и начинает чесаться.
- Далее начинается стадия воспаления. На пораженном участке появляется отечность и возникает маленький болезненный прыщик – волдырь, содержащий прозрачную жидкость. Со временем эта жидкость мутнеет. Маленький прыщик (прыщики) постепенно увеличивается в размерах.
- Через 3–5 дней после начала болезни волдыри лопаются. Из них течет жидкость, в которой находится несчетное количество вирусных частиц. В этот период контакты с больным человеком нужно прекратить, поскольку весьма велик риск заражения. На месте высыпаний образуются язвы с гнойной коркой (струпы). При повреждении струпа открывается кровотечение.
Естественный вопрос каждого пациента, за сколько дней проходит герпес? Обычно на это уходит около 10 дней. Если на протяжении этого времени симптомы не исчезли, нужно показаться врачу, поскольку герпес может сигнализировать о наличии других заболеваний.

Возможные осложнения
Вирус не ограничивается поверхностными тканями – он легко проникает и во внутренние. Главные мишени герпеса – слизистые оболочки, кожный покров, глаза (конъюнктивиты также могут быть следствием герпеса), а также центральная нервная система и мозг. Пострадать от вируса могут лимфатические узлы и внутренние органы. По вине болезнетворного микроорганизма может нарушиться работа печени, легких, кишечника и почек.
Следствием герпеса могут быть стоматиты, бесплодие, выкидыш, врожденные уродства у детей, энцефалит, воспаления в суставах, простатит, доброкачественные и злокачественные опухоли. Ученые, опираясь на исследования, связывают с герпесом развитие рассеянного склероза и болезни Альцгеймера.
Помощь какого врача может понадобиться при герпесе?
Как лечить герпес?
Полностью уничтожить вирус, проникший в организм, невозможно. Но подавить его деятельность настолько, чтобы он не беспокоил, вполне реально. В современной медицине для этого используют комплексный подход. Лучший результат дает комбинированная терапия, которая подразумевает применение противовирусных препаратов (они выпускаются в виде лекарств для внутреннего приема и в виде наружных средств), а также средств, укрепляющих иммунитет. В некоторых случаях дополнительно пациенту назначают местные анальгетики и физиотерапевтические процедуры.
Многие интересуются, можно ли герпес прижигать спиртом? Увы, такой метод не действует на вирус, а только повреждает слизистые оболочки, поэтому лучше использовать специальные мази.
Какие обычно назначают средства от герпеса на губах? В таблице приведен список наиболее распространенных лекарственных препаратов при терапии вируса.
Название, лекарственная форма
Выпускается в виде таблеток, крема, глазных мазей, инъекционных растворов.
Недорогой противовирусный препарат, останавливающий размножение вируса. Адресуется взрослым и детям старше 3 лет. Не рекомендуется принимать при беременности.

Рисунок 7 - Противовирусная мазь
Выпускается в виде таблеток 500 мг.
Один из лучших препаратов от герпеса. От Ацикловира отличается способом доставки действующего компонента. Подавляет активность вируса и уменьшает симптомы. При приеме препарата уменьшается риск заражения при контактах с другими людьми.
Рисунок 8 - Лечение герпеса за 3 дня
Фамцикловир (он же Famvir)
Выпускается в виде таблеток 125, 250 и 500 мг.
Так же, как Ацикловир и Валтрекс, блокирует размножение вируса. Помогает при терапии простого вируса и вируса, вызывающего ветряную оспу. Фамцикловир эффективен против вирусов, устойчивых к Ацикловиру.
Рисунок 9 - Фамцикловир
Выпускается в виде раствора для внутривенных инъекций, а также в форме геля и суппозиториев (свечей).
Противовирусный, противовоспалительный и иммуномодулирующий препарат растительного происхождения. Повышает устойчивость организма к инфекциям, оказывает жаропонижающее действие.
Докозанол (он же Эразабан)
Выпускается в виде крема для наружного применения.
Оказывает противовирусное действие. Предназначен для применения у взрослых и детей от 12 лет. Беременным назначают с осторожностью.
Выпускается в виде капель.
Противовирусное средство системного назначения. Предназначается для лечения простого герпеса у детей и взрослых. Используется в педиатрической практике (в том числе у детей до 1 года).
Выпускается в виде сиропа.
Эффективен при лечении простого герпеса, а также при терапии и профилактике гриппа. Используется в педиатрической практике (в том числе у детей до 1 года).
Представленный перечень препаратов далеко не полный – врач в зависимости от особенностей конкретного пациента может порекомендовать и другие средства. Например, в некоторых случаях не обойтись без антибиотиков (если есть риск заражения другими инфекциями).
Читайте также:


