Ретровирусы вирус иммунодефицита человека
Ретровирус – это семейство вирусов, в которых генетический материал состоит из РНК. Микроорганизмы содержат обратную транскриптазу.
Ретровирусы – это микроскопические организмы, способные вызывать некоторые виды онкологических заболеваний, различные вирусные инфекции. Причем патологии могут возникать не только у людей, но и у животных. У людей ретровирусы вызывают ВИЧ-инфекцию (СПИД).
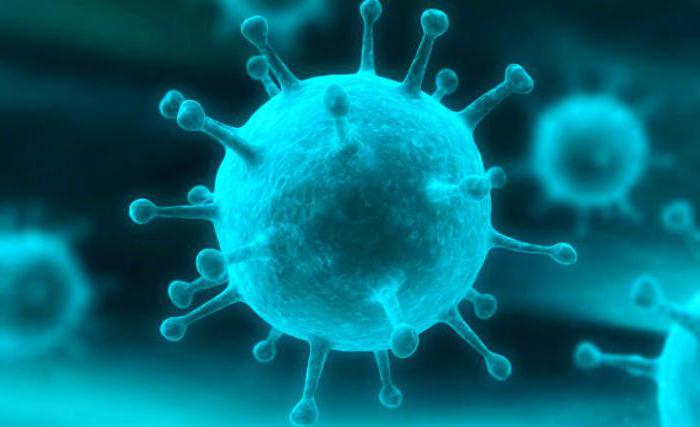
Особенности вируса
Ретровирусы – это уникальные организмы. Они способны размножаться, транскрибируясь в ДНК. Они попадают в кровь, начинается процесс транскрипции. После ее завершения вирусный геном получает полный доступ к ДНК клетки хозяина и начинает воспроизводить все происходящие с ней процессы. В дочерних клетках вирусная ДНК создает РНК копии. Этот процесс может продолжаться длительное время, но, в конце концов, копии покидают дочерние клетки и покрываются белковой оболочкой. В результате этого ретровирусы вызывают изменение нормального процесса репликации, происходящего в клетках, при котором задействуется РНК. Этот процесс обращается вспять. Сами же инфицированные клетки длительное время сохраняются в организме. В некоторых случаях изменяемые клетки разрушаются, как это происходит при ВИЧ-инфекции, а иногда превращаются в раковые.
К ретровирусам относится семейство вирусов Retroviridae. Они склонны к мутациям, из-за чего быстро приобретают устойчивость к противовирусным препаратам. Из-за этой особенности бороться с ретровирусной инфекцией сложно.
Некоторые люди считают, что ретровирус – это простой вирус, напоминающий грипп, но это не так. Данная разновидность опасна и с ней практически невозможно бороться. Чтобы оказать противодействие, необходимо разрабатывать особые схемы терапии с использованием противовирусных препаратов. Чтобы не заразиться ретровирусной инфекцией, проще проводить профилактические мероприятия в виде плановых прививок.
Несмотря на то, что ретровирусы способны вызывать опасные для жизни заболевания, их легко побороть обычным мылом и водой: для дезактивации достаточно мыть руки с мылом. Для предотвращения распространения применяют барьерные меры профилактики, в числе которых резиновые перчатки, маски для лица, некоторые марки презервативов.
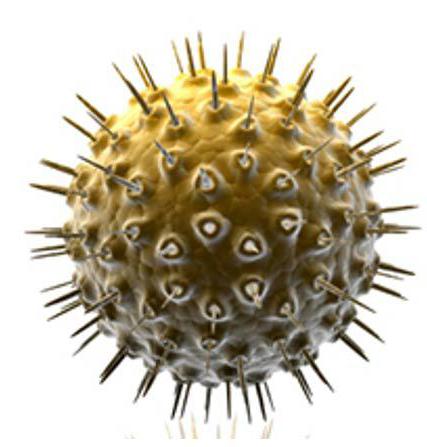
Классификация ретровирусов
Первые примеры ретровируса и его воздействия на живой организм были описаны более ста лет назад. С тех пор интерес к микроорганизму сильно вырос. Сейчас ретровирусы подразделяются на следующие виды:
- Семейство онкогенных вирусов. Эта разновидность способствует развитию сарком и лейкемии в организме человека и животных. Одним из самых важных представителей этого типа недуга является T-лимфотропный вирус человека.
- Семейство лентивирусов. Ярким представителем группы является ВИЧ.
- Семейство спумавирусов. Этот вид не связан ни с какими патологиями, но способен вызывать изменения на клеточном уровне.
По мере изучения морфологии вируса были выявлены самые разные типы организмов, которые разделили на несколько групп:
- Безоболочечные организмы.
- Оболочечные виды с ацентрическим расположением нуклеокапсидом.
- Оболочечные виды, у которых нуклеокапсид располагается центрально.
- Вирусы крупного размера с минимальным количеством шипов.
РНК вируса имеет несколько рамок считывания информации, соответственно, кодировать она будет только определенные группы структурных белков: группы Gag, CA, MA и NC.

Патологии, вызываемые РНК-вирусами
Существует ряд патологий, которые вызываются РНК-содержащими вирусами. К ним относятся:
- Грипп.
- Краснуха.
- Корь.
- Вирусный энтерит.
- Паротит.
- Энтеровирусные инфекции.
- ВИЧ.
- Т-лимфотропная инфекция человека типа 1.
- Т-лимфотропная инфекция человека типа 2.
РНК-вирусы могут спровоцировать развитие сарком и лейкемий.
Острый ретровирусный синдром при ВИЧ
Среди всех существующих патологий, вызванных РНК-содержащими микроорганизмами, самым распространенным является острый ретровирусный синдром. Это первичное инфицирование вирусом иммунодефицита человека, продолжающееся до полугода после заражения.
После заражения ВИЧ обычно проходит от нескольких недель до нескольких месяцев. В это время нет никаких клинических проявлений инфекции. Этот бессимптомный период называют инкубационным. В некоторых случаях он может длиться до года.
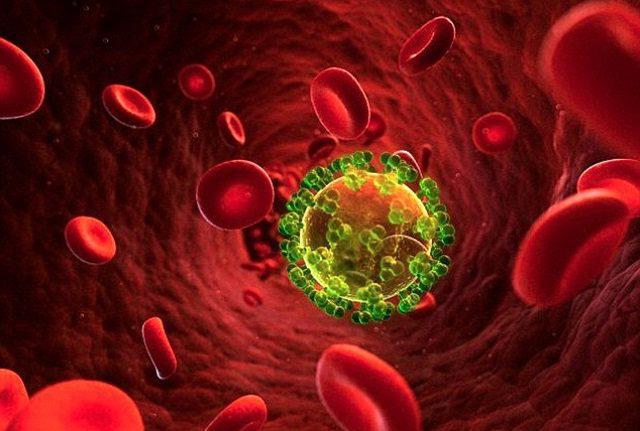
Симптомы ретровируса проявляются постепенно, начиная с поражения верхних дыхательных путей, как при гриппе, хотя намного чаще у больных начало патологии протекает как мононуклеоз:
- появляется стоматит, фарингит с поражением лимфоузлов;
- повышается температура тела;
- снижается аппетит, пациент начинает терять вес;
- тошнота, нарушение стула;
- размеры селезенки и печени увеличиваются;
- на коже появляется сыпь;
- развивается асептический менингит, нарушается психическое состояние пациента, появляются невриты.
Диагностика синдрома
Острая фаза патологии длится около десяти дней. Чтобы установить, что у пациента имеется вирусная патология, необходимо сдать кровь на анализ: в плазме выявляют РНК ВИЧ. Затем проводится подтверждение острой фазы ретровирусного синдрома. Для этого сдает повторный анализ. Если через три недели в крови обнаружат антитела к ВИЧ, а в общем анализе лейкопению и лимфопению, то можно предположить острую фазу.
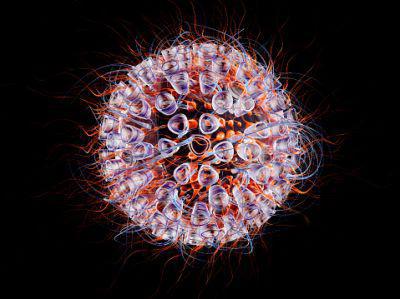
Если в эту фазу не будет обнаружено заболевание и не назначено лечение, симптомы ретровируса могут затихнуть на несколько лет. Единственным клиническим проявлением может стать увеличение лимфоузлов.
Если диагностика проведена вовремя, а лечение ретровируса назначено верно, то пациенты могут прожить с патологией более двадцати лет.
Лечение
Существует множество самых различных мнений о начальном лечении, но все они сводятся к тому, что терапию следует начинать сразу же после установки диагноза, не дожидаясь клинических проявлений и осложнений.
Зная, от чего погибает ретровирус, врач может правильно подобрать схему лечения и назначить противовирусные препараты. Обычно подбирается два антиретровирусных средства, прием которых ведется под лабораторным контролем сыворотки крови.
Чаще всего назначают:
- препараты, относящиеся к группе нуклеозидов обратной транскриптазы;
- средства из группы протеазы;
- препараты, относящиеся к ненуклеозидным ингибиторам транскриптазы.
Огромную роль в лечение ретровирусной инфекции имеет терапия вторичных патологий. С этой целью врач назначает полное обследование, в ходе которого определяют, какими недугами страдает больной. После выявления хронических заболеваний подбирается терапия, направленная на избавление от болезней или на достижение стойкой ремиссии.
В качестве дополнительного лечения обязательно проводится витаминотерапия, физиолечение, иммунотерапия, коррекция питания.
После лечения пациенту придется всю жизнь наблюдаться у врача, вести здоровый образ жизни, соблюдать строгие рекомендации. В противном случае ретровирус может вновь активироваться.
Т-лимфотропные вирусы человека
Т-лимфотропные патологии делятся на два типа: тип 1 и тип 2. Каждый из них представлен определенными недугами, вызываемыми РНК-вирусами.
К первому типу Т-лимфотропной инфекции относят Т-клеточный лейкоз, лимфому и спастический парапарез тропического типа. В эпидемиологических районах, где наблюдается высокий уровень заражения Т-лимфотропным вирусом, диагностируются дерматиты, пневмонии, артриты.
Т-лимфотропная инфекция второго типа вызывает Т-клеточную лимфому и некоторые виды лейкозов. В редких случаях микроорганизм способен привести к развитию волосатоклеточного лейкоза.
В заключение
Любую инфекцию проще предупредить, чем лечить, и особенно заражение РНК-вирусами. Чтобы быть здоровым, следует соблюдать правила личной гигиены, мыть руки с мылом. Защититься от патологии поможет хороший иммунитет и здоровый образ жизни.
Для профилактики ретровирусных инфекций следует взять за привычку мыть руки каждый раз, зайдя в дом с улицы, перед каждым приемом пищи. В обязательном порядке применяют барьерные средства - презервативы, резиновые перчатки, маски. Эти простые правила помогут снизить до минимума риск заражения ретровирусной инфекцией.
Вирус гепатита G.
Гепатит G вызывается РНК - содержащим вирусом из группы флавивирусов. Вирус передается парентерально, способен вызывать острые и хронические гепатиты. Описано несколько генотипов HGV. У этого вируса обнаружено два структурных оболочечных белка - Е1 и Е2 и пять неструктурных белков. Маркеры гепатита G распространены среди населения даже чаще, чем - вируса гепатита С, особенно при трансплантации почки, у наркоманов, больных гемофилией, при гемодиализе и наиболее часто - у носителей вируса гепатита С.
Как метод лабораторной диагностики чаще используют ПЦР - определение РНК вируса (при остром гепатите G в первые шесть месяцев можно определить только вРНК), антитела к оболочечному белку Е2 выявляют не ранее 5 - 6 месяцев с момента инфицирования.
Острый гепатит G переходит в хронический реже, чем гепатит С. С хроническими гепатитами G связана персистенция вируса, возникновение циррозов печени. Гепатит G к настоящему времени изучен еще недостаточно.
Современные представления о вирусных гепатитах изменяются быстро, список вирусов расширяется. К новым гепатотропным вирусам, действие которых уточняется, следует отнести TTV (ДНК- вирусы нового семейства Circinoviridae) и SEN- вирусы.
TTV- вирус- спутник, сопутствующий известным вирусным парентеральным гепатитам. Это- вирус - оппортунист, активирующийся при иммунодефицитах (в т.ч. ВИЧ- инфекции). SEN- вирусы- это ДНК -вирусы, близкие к семейству TTV, связаны с переливаниями крови, реплицируются в гепатоцитах, чаще встречаются у больных с парентеральными вирусными гепатитами В и С, генетически высоко изменчивы.
Вирус иммунодефицита человека (ВИЧ или HIV) относится к семейству ретровирусов, подсемейству лентивирусов (медленных вирусов). Геном ретровирусов уникален - он представлен двумя идентичными молекулами позитивной РНК, т.е. это РНК - вирусы с диплоидным геномом. Свое название ретровирусы получили за отличительные особенности репродукции (РНК à ДНК à иРНК à геномная РНК). Особенности репродукции связаны с функциями фермента обратной транскриптазы (ревертазы или РНК - зависимой ДНК - полимеразы), обладающей тремя видами активности - обратной транскриптазы, РНК - азы и ДНК - полимеразы.
Семейство Retroviridae включает три подсемейства.
1. Lentivirinae - возбудители медленных вирусных инфекций, в т.ч. ВИЧ.
2. Oncovirinae - онкогенные вирусы, с которыми связано превращение клеток в опухолевые. Раньше не знали, как РНК - вирусы могут встраиваться в геном клетки и способствовать опухолевому росту (не были известна возможность обратной транскрипции у вирусов), что тормозило научную разработку вирусологии опухолевого роста.
3. Spumavirinae - “пенящие” вирусы, название которых связано с характерным “вспененным” видом инфицированных ими клеточных культур как результатом интенсивного симпластообразования.
Первыми открытыми в конце 70- х годов ретровирусами были HTLV-1 и HTLV-2 (от “human T- lymphotropic virus) - возбудители Т - клеточных лейкозов и лимфом. Наиболее известны обладающие лимфотропным и цитопатическим действием вирусы ВИЧ-1 (HIV-1 в английском варианте) и ВИЧ-2, вирус иммунодефицита обезьян (ВИО или SIV), к которому по ряду свойств ближе (чем к ВИЧ-1) ВИЧ-2. К настоящему времени имеется информация уже о нескольких сотнях ретровирусов, интегрированных с геномом человека и практически очень мало об их роли в патологии.
История изучения и происхождения ВИЧ.
Синдром приобретенного иммунодефицита (СПИД) впервые выделен как самостоятельное заболевание в США в 1981г. Возбудитель (ВИЧ-1) был описан почти одновременно в 1983г. французом Л.Монтанье и американцем Р.Галло. Эпидемиология нового вида патологии поражала своей необычностью. Почти 100% больных были мужчинами в возрасте 25-49 лет, 94% - гомо- или бисексуалами, отмечалась высокая летальность. У больных были выявлены дефекты клеточного иммунитета, развитие пневмоцистозной пневмонии, кандидоза и саркомы Капоши у них было расценено как оппортунистические заболевания. СПИД окрестили болезнью четырех “H”- по первым буквам английских вариантов слов гомосексуалы, гемофилия, гаитяне и героин. В 1986г. был идентифицирован еще один вирус - ВИЧ-2.
Окончательного ответа на вопрос о месте, времени и условиях возникновения ВИЧ нет. Ретроспективные исследования показали циркуляцию этого вируса по крайней мере с конца 50-х - начала 60-х годов. Прародительницей ВИЧ считают тропическую Африку, где широко распространен ВИО (близкородственный ВИЧ-2) среди обезьян. Первые известные серологические находки ВИЧ отмечены в Африке, здесь же - наибольшая интенсивность передачи ВИЧ наиболее естественным гетеросексуальным путем. Однако эпидемическое распространение ВИЧ - инфекция получила с конца 70-х - начала 80-х годов. В 1987г. выявлен первый случай в России, в настоящее время счет идет на десятки тысяч инфицированных в год. В мире регистрируют десятки миллионов инфицированных ВИЧ в год, ежегодно число вновь инфицированных увеличивается, т.е. налицо пандемия ВИЧ - инфекции.
Структура вириона ВИЧ.
ВИЧ имеет сферическую форму и размеры 100-120 нм в диаметре. Наружная оболочка образована двойным липидным слоем с гликопротеиновыми “шипами”, состоящими из трансмембранного белка gp41 (пронизывает липидный слой) и наружного белка gp120. Эти оболочечные белки кодируются геном env и участвуют в прикреплении вириона к мембранам клеток хозяина. С внутренней стороны липидной оболочки находится матричный каркас, образованный белком р17. Он окружает внутреннюю структуру вириона - нуклеокапсид или сердцевину (англ. - core). Собственная оболочка сердцевины образована “коровским” белком р24. Внутри нуклеокапсида находится геном вируса в виде двух цепочек, связанных белками р7 и р9, полимеразный комплекс ревертазы, протеаза, интеграза (эндонуклеаза), затравочная т - РНК. Наиболее распространен ВИЧ-1, который в зависимости от строения гена env имеет субтипы. Субтипы A-H составляют доминирующую группу M (major), наиболее распространены субтипы С и Е.
Жизненный цикл ВИЧ.
Инфекционный процесс при заражении ВИЧ носит последовательный фазовый характер и начинается с проникновения вируса через слизистую оболочку половых путей или с непосредственного поступления в кровоток. Проникнув в организм, вирус в первую очередь атакует клетки, имеющие специфичный для него рецептор CD4. Этот рецептор имеют в большом количестве Т - хелперы, в меньшем - макрофаги и моноциты, нейроны, клетки нейроглии и некоторые другие клетки (см. лекции по общей иммунологии). Вирус распознает CD4 - рецепторы с помощью своего белка gp120. Процесс инфицирования клетки вирусом осуществляется в два этапа : прикрепления и слияния. Прикрепленный через белок gp120 к рецептору CD4 клетки - мишени вирус белком оболочки gp41 сливается с мембраной клетки. Белок gp41 обеспечивает не только слияние вирусной и клеточной мембран, но и слияние мембран клеток с образованием синцития (многоядерных клеток), обреченного на гибель. Нуклеокапсид, освобожденный от суперкапсида при слиянии мембран, попадает в цитоплазму. На пути к ядру освобождается геномная РНК и ассоциированные с ней компоненты сердцевины. Обратная транскриптаза синтезирует на вирионной РНК минус - цепь ДНК, РНК-аза разрушает вирионную РНК, а вирусная ДНК - полимераза синтезирует на минус - цепи плюс - цепь ДНК.
Двунитевая ДНК транспортируется в ядро клетки, где приобретает кольцевую форму и интегрируется под действием эндонуклеазы (интегразы) с ядром клетки, превращаясь в ДНК - провирус.Последующие этапы жизненного цикла ВИЧ - латентная фаза, фаза активации транскрипции с ДНК- провируса и последующая трансляция белков вируса, наработка компонентов вируса и формирование новых вирионов, их выход из клетки, сопровождающийся цитопатическим эффектом для клетки - мишени.
ДНК - провирус может длительно находиться в неактивном состоянии (персистентное инфицирование). В этот период вирус можно выявить только с помощью ПЦР. Активация транскрипции особым ядерным фактором в результате действия иммунокомпетентных клеток или микробных антигенов приводит к продуктивной фазе - активному размножению ВИЧ. Факторы экспрессии генов ВИЧ - специфические антигены (прежде всего - герпес - вирусы), неспецифические митогены (фитогемагглютинин), цитокины (фактор некроза опухолей, интерфероны, гамма - интерферон), бактериальные иммуномодуляторы (фосфолипиды сальмонелл), глюкокортикостероиды.
Антигенные свойства ВИЧ.
Функция обратной транскриптазы не подвергается контролю, что обусловливает высокую частоту генетических ошибок при репликации и мутации структурных белков вируса. С учетом частоты изменчивости ни один ВИЧ не производит при репликации вирион, в точности соответствующий родительскому. Высокая генетическая изменчивость реализуется в вариабельности антигенных и биологических свойств ВИЧ. Высокой изменчивостью характеризуется продукт гена env - оболочечный белок gp120, особенно петлеобразный V3 - домен (из 35 аминокислот), к которому образуется до 90-95% всех вируснейтрализующих антител.
ВИЧ-1 и ВИЧ-2 имеют существенные отличия в строении, гомология первичной структуры геномов составляет только около 42%, перекрестного иммунитета между этими вирусами нет. Антигенными свойствами обладают все основные структурные элементы вириона, прежде всего - белки. Исключительная генетическая и антигенная изменчивость позволяет вирусу выживать в инфицированном организме.
Наряду с генетическими особенностями, ВИЧ-1 имеет фенотипические различия по ряду свойств - эффективности репликации, характеру цитопатического действия и способности образовывать синцитий (этот признак связан с вирулентностью), преимущественному тропизму к клеткам - моноцитотропные изоляты (начальные этапы болезни) и лимфотропные изоляты (разгар болезни).
Рецептором для ВИЧ является дифференцировочный антиген CD4, имеющий гомологичные участки с иммуноглобулинами и белком gp120 ВИЧ. Расположенный на мембранах Т- хелперов и Т- индукторов, рецептор CD4 в комплексе с белками HLA II класса выполняет функцию распознавания антигенов. Фиксация вируса через gp120 ВИЧ-1 (или gp105 ВИЧ-2) с мембранным рецептором CD4 блокирует основную функцию этих иммунокомпетентных клеток - восприятие сигналов от антиген- представляющих клеток. Последующая репликация вируса ведет к гибели этих клеток и выпадению их функций, т.е. к развитию иммунодефицита. Чем активнее CD4+ клетки, тем активнее процесс репродукции вируса. ВИЧ угнетает преимущественно Т- хелперы -1 (связанные с многими цитокинами клеточного иммунитета), что способствует развитию вирусных инфекций и опухолей.
Сродство вирусного gp120 (gp105 в случае ВИЧ-2) к этому рецептору определяет высокую избирательность поражения клеток. В патологический процесс вовлекаются в первую очередь и в наибольшей степени CD4+ лимфоциты, моноциты крови и макрофаги тканей, дендритные клетки крови, лимфоузлов, селезенки, кожи, альвеолярные и интерстициальные макрофаги легких, микроглия и другие клетки нервной системы, имеющие CD4+ рецепторы. Поражаются также В- и 0- лимфоциты, ретикулярные клетки, эпителиальные клетки кишечника. Большое значение в распространении ВИЧ и длительному сохранению в организме придают клеткам Лангерганса.
В патогенезе ВИЧ - инфекции большое значение имеют механизмы иммунного повреждения. Наличие сходных участков в структуре белков gp120, HLA класса II и CD4 - рецепторов определяет перекрестное реагирование антител к ВИЧ с этими структурами с рядом патологических эффектов (блокада кооперации CD4+ лимфоцитов и HLA класса II, неадекватная стимуляция CD4+ клеток и др.).
Поражение иммунной системы при ВИЧ - инфекции носит системный характер, проявляясь глубокой супрессией Т- и В- звеньев иммунитета. Происходят изменения гиперчувствительности немедленного и замедленного типа, гуморального иммунитета и факторов неспецифической защиты. Наряду с дефицитом CD4+ лимфоцитов в динамике болезни нарастает функциональная недостаточность CD8+ лимфоцитов, NK клеток, нейтрофилов. Нарушение иммунного статуса проявляется рядом синдромов - инфекционным, аллергическим, аутоиммунным, лимфопролиферативным.
Манифестный синдром приобретенного иммунодефицита (СПИД) проявляется в трех основных клинических формах: нейроСПИД, онкоСПИД, инфектоСПИД (оппортунистические инфекции). Это зависит от путей внедрения ВИЧ, его преимущественного тропизма к CD4 Т- лимфоцитам или макрофагам, наличия кофакторов (цитомегаловирус, вирус Эпштейна- Барр), дозы инфекта, иммунного статуса организма и др.
В динамике ВИЧ- инфекции можно выделить следующие основные стадии: заражение, латентный период, появление лабораторных признаков инфекции, первичная клиника острой вирусной (ретровирусной) инфекции (эта стадия может отсутствовать), клинический СПИД (иммунодефицит плюс индикаторные болезни). Особое значение имеет выявление лабораторных признаков ВИЧ- инфекции.
Можно выделить три типа инкубации:
- вирусологическую ( от инфицирования до определения в крови вируса или его антигенов) - в среднем 2 - 4 недели;
- серологическую (от заражения до сероконверсии - появления положительных серологических результатов) - в среднем 8 - 12 недель;
- СПИД - инкубацию (равно или более 10 лет). Безусловный иммунологический критерий СПИДа - снижение CD4+ лимфоцитов до 200 клеток в микролитре.
Лабораторная диагностика ВИЧ - инфекции методически базируется на ИФА, иммуноблоте и ПЦР. Основными ее направлениями являются:
- выявление антител к ВИЧ;
- выявление ВИЧ или его антигенов;
- определение изменений в иммунном статусе.
Для выявления антител применяют ИФА с различными тест - системами (лизатными, рекомбинантными, пептидными антигенами ВИЧ-1 и ВИЧ-2). Основная проблема - ложноположительные результаты (перекрестная реактивность gp120, CD4+ рецепторов, белков HLA II класса и др.). Поэтому исследования в ИФА проводят как правило с использованием параллельно нескольких различных тест - систем.
Иммуноблот чаще применяют как подтверждающий тест для выявления антител к отдельным белкам ВИЧ. Антитела к основным внутренним белкам (р17, р24) обнаруживают у 70% инфицированных и примерно у половины больных СПИДом. В иммуноблоте чаще всего выявляются антитела к gp41 (до 85%) и gp160 (до 100%).
В ранние сроки используют выявление в ИФА антигена р24. Наиболее чувствительным методом выявления ВИЧ является ПЦР - диагностика.
Основным клинико - лабораторным показателем диагностики СПИДа у ВИЧ - инфицированных является определение количества CD4+ лимфоцитов. Уровень ниже 200 клеток/мкл является основным критерием СПИДа.
Лечение является одним из наиболее актуальных и до настоящего времени не решенных проблем ВИЧ - инфекции. Теоретически наиболее оправдано применение препаратов, ингибирующих обратную транскрипцию - зидовудин, азидотимидин, диданозин, ставудин и др. Вакцины против ВИЧ находятся в стадии разработки. С учетом высокой изменчивости вируса это очень сложная задача.
Одна интересная черта ретровирусов заключается в том, что мы можем понять их эволюцию и эволюцию нашей клеточной защиты. Вирус иммунодефицита человека пришел к нам от приматов. Самый распространенный тип ВИЧ называется ВИЧ-1. Он составляет примерно 60 миллионов человеческих заражений ВИЧ. Это практически единичный случай, когда вирус шимпанзе поразил человека и стал распространяться среди человеческого населения. Мы знаем, что направление заражения именно такое — от шимпанзе к человеку, — потому что у шимпанзе существует больше типов этого вируса, чем у людей.
Существует еще один тип ВИЧ, названный ВИЧ-2, который пришел к нам от африканских обезьян, а именно дымчатого мангобея. И снова разновидностей этого вируса у мангобеев намного больше, чем у человека. Это говорит нам о том, что перенос вируса происходит от обезьяны к человеку. ВИЧ-2 вызывает похожую болезнь, что и ВИЧ-1, у примерно 20–30% людей. Однако у большинства людей не наблюдаются никакие значимые симптомы после заражения ВИЧ-2. Поэтому один из важных вопросов ВИЧ-биологии заключается в поиске отличий между тем вирусом, который заразил 60 миллионов человек, и тем, что не инфицировал даже приблизительно такое число.
У приматов есть похожие вирусы. Более того, большинство африканских приматов имеют вирус, который родственен нашему ВИЧ-1. Обычно мы называем эти вирусы в соответствии с видом, в котором мы их нашли. Вирус шимпанзе называется ВИО (SIV) — вирус иммунодефицита обезьян (simian immunodefiency virus). В таком случае, бывает ли у шимпанзе СПИД? Это не до конца понятно. Не все шимпанзе заражены. Существуют определенные территории, где проживают зараженные шимпанзе. Но так как они не живут жизнью людей, не ведут утонченный образ жизни, а, наоборот, проживают более трудную жизнь, то умирают намного раньше, за ними становится очень сложно следить и выяснять, есть ли у них это заболевание.
Из-за этого долгое время мы думали, что они не страдают никакими болезнями, потому что у них нет такого сильного иммунодефицита, как у людей. Но в последнее время мы стали думать, что они тоже имеют эту болезнь, возможно, в менее суровой форме. Так как они не живут долго, им не приходится страдать от тех симптомов, которые переживает человек.
Таким образом, до конца не известно, что происходит с ретровирусной инфекцией в организме обезьян. У африканских обезьян вирус практически не вызывает никаких заболеваний, поэтому кажется, что имеет место адаптация как носителя, так и самого вируса по такому принципу, что обезьяна может быть инфицирована, но не страдать от болезней. Они могут заразиться в достаточно раннем возрасте, поэтому могут иметь вирус в своем теле, но при этом не ощущать значимых последствий для своей жизни.
Среди других видов ретровирусы тщательно изучались у мышей. Это делалось в основном потому, что ретровирусная инфекция у мышей способна вызывать рак. Мышь заражается ретровирусом, который обычно называют гамма-ретровирус. Оказывается, что эта ретровирусная инфекция вызывает у мышей рак. Люди, изучавшие рак в 1950–1960-х годах, то есть в самом начале подобных исследований, выращивали мышь до тех пор, пока она не становилась очень уязвимой к этой болезни, а потом пытались выяснить, почему у этих мышей развивается рак. Оказалось, что они получали рак, потому что были инфицированы ретровирусом. Эти ретровирусы переносили гены (онкогены), которые вызывали рак. Таким образом, все первичные исследования ретровирусов были направлены на понимание того, как работает рак и что его вызывает.
Когда появился ВИЧ и стал вызывать иммунодефицит, это стало первым случаем, когда такой тип вируса вызвал такую болезнь. До этого мы знали о ретровирусах только из исследований гамма-ретровирусов, вызывающих рак. Ретровирусы — это такие типы вирусов, которые можно рассматривать как вирусы, путешествующие налегке. Так, например, ВИЧ имеет всего девять генов, а другие ретровирусы вообще три. Так что они действительно путешествуют налегке по сравнению с вирусом герпеса, например, который имеет около двухсот генов. Я считаю, что эти вирусы — МО (modus operandi), их стратегия — путешествовать налегке и быть тихими. Их цель при поражении клетки — не активировать ее и не причинить много ущерба. Я думаю, что изначально они не вызывают сильных болезней, но в длительной перспективе эта инфекция может вызвать болезни вроде рака у мышей. Хотя, возможно, они не вызовут рак у диких мышей. Это происходит только тогда, когда мы пробиваем защиту мыши.
Итак, ретровирусы — это относительно милосердные вирусы, я считаю, потому что они не управляют вашим телом, как делают другие вирусы. Главное их отличие в том, что они превращают РНК в ДНК и интегрируют ДНК в хроматин. Это и есть уникальная черта ретровирусов. Некоторые другие вирусы поступают так же, но только в качестве дополнения. Ретровирусы целиком зависят от этого процесса интеграции. Если клетка не может от них избавиться, она должна умереть для избавления себя от вирусной инфекции.
Ретровирусы внедряют свой геном в хроматин хозяина. Стоит этим генам попасть внутрь хроматина — они останутся там навсегда. Клетка в целом относится к ним как к клеточным генам, так что они считываются, производят РНК, а позже эта РНК направляется в цитоплазму. Вирус производит протеин, клетка производит вирусный протеин, новые вирусы формируются, и они готовы двигаться дальше, заражать новые клетки. Так ретровирусы стали отличным инструментом для изучения клеточной биологии, и это потому, что они простые. Некоторые из них имеют всего три гена. Даже сложный ретровирус вроде ВИЧ имеет всего девять генов. Поэтому очень легко взять их, разделить на части и изучать, какая часть за что отвечает.
В поле генной терапии существует трюк, когда берут ретровирус, вынимают из него ретровирусные гены и вставляют те гены, которые нужны. Потом можно сформировать ретровирусные частицы. Этот трюк можно использовать для развития ретровирусного вектора. Работает это так: можно взять ретровирусный геном, который обычно шифрует все ретровирусные гены, избавиться от них и поставить на их место предпочтительный ген, например терапевтический ген или ген, который можно просто измерять, — мы обычно используем ЗФБ (GFP), который заставляет клетки зеленеть. Если вы это сделаете, вы сможете производить ретровирусные частицы, которые будут только заражать клетку и производить белок. В ретровирусе не окажется ретровирусных генов, так что он сможет производить только терапевтические гены или ЗФБ. И это прекрасный инструмент для изучения клеточной биологии.
Например, можно изменить клетку и посмотреть, продолжает ли вирус оказывать на нее свое влияние, или можно, наоборот, изменить вирус и проверить, может ли он теперь инфицировать клетку. Это будет называться генетическим подходом. Можно выяснить роль различных частей вируса в попадании в клеточное ядро, в попадании в клетку, в пересечении цитоплазмы.
Читайте также:


