Суточная доза риамиловир при лечении гриппа
В состав данного средства, вне зависимости от формы выпуска входит одноименное действующее вещество, за счёт которого и происходит развитие клинического эффекта.

Его массовая доля отличается в зависимости от формы выпуска, так в мази Ацикловир действующего вещества содержится 50 грамм, глазная мазь содержит 30 грамм, крем 50 грамм, в таблетках может содержаться от 200 или 400 мг, а в лиофилизате 250, 500 мг или 1000 мг.
Состав вспомогательных веществ будет зависеть от вида лекарственной формы. Их массовая доля не влияет на развитие каких-либо эффектов для организма, лишь в редких случаях может вызывать аллергическую реакцию.
Форма выпуска
Существует достаточно большое количество лекарственных форм, в которых представлен Ацикловир. Среди них следует отметить, мази, крема, лиофилизаты и таблетированные формы.
Фармакологический эффект

Ацикловир способен формировать противовирусное действие. Это достигается за счёт угнетения репликационных процессов в клетках вируса. Воздействует он преимущенно на герпесные типы.
Содержащаяся в вирусных клетках тимидинкиназа фосфорилирует Ацикловир в монофосфатную форму, а под воздействием других форм идёт разложение до дифосфата.
Именно в подобном виде происходит внедрение Ацикловир в генетический материал вируса, что вызывает прекращение ее удлинения. Подавляется также и ДНК—полимераза, и репликация вируса в последствии тормозится.
За счёт этого уменьшается выраженность кожных высыпаний, а также тормозится формирование новых. Кроме того, в незначительной степени следует ожидать развития иммуностимулирующего действия.
Фармакокинетика
В зависимости от формы выпуска:
- При пероральном приеме всасывание Ацикловир происходит быстро. Максимальную концентрацию можно зафиксировать спустя 1,5-2 часа. При попадании в кровь происходит связывание с белком плазмы крови. Именно в подобном связанном состоянии идёт транспортировка Ацикловир в клетки печени. Именно в них происходит метаболизм до активных метаболитов.
- После развития клинического эффекта идёт выведение через мочевыводящую систему посредством канальцевой секреции. Лишь единичные количества Ацикловир выводятся через кишечник.
- При попадании в организм Ацикловир проходит через все гисто-гематические барьеры. Особенно это важно при локализации возбудителя в нервной системе или переходе в организм плода. При приеме Ацикловир пациентам с опоясывающим герпесом, следует учитывать, что в клетках спинного мозга концентрация препарата будет уменьшена на 50%.
- Период полувыведения достигает в среднем трёх часов, если имеются нарушения функций почек, он достигает 20 часов.
- Местное использование Ацикловир предусматривает отсутствие всасывания при отсутствии повреждений на кожных покровах, если же повреждения имеются, Ацикловир может всасываться в незначительном количестве.
- Глазная мазь при нанесении на слизистую оболочку не всасывается, так как в крови действующего вещества не обнаруживают.
Показания к применению
Выбор показаний к применению может во многом быть связан с лекарственной формой:
![]()
Так, лиофилизаты или таблетки Ацикловир могут использоваться в качестве лечебной и профилактической цели предупреждения или предотвращения инфекционных процессов в различной клинической форме, которые вызваны вирусом герпеса. Среди основных патологий может быть генитальный герпес, формы простого герпеса и ветряной оспы. Применяться Ацикловир может у людей с нормальным иммунным статусом или же на фоне его снижения, вызванного инфицирование вируса иммунодефицита человека. Ацикловир применяется у пациентов, после трансплантации органов.- Форма геля или мази применяется с целью комбинированного лечения вирусных инфекций, которые спровоцированы герпесом. Среди них проявления опоясывающего лишая, ветряной оспы, генитальной формы герпеса вируса простого герпеса.
- Глазная мазь помогает справиться с герпетическим кератитом. Но, перед нанесением мази проводится тщательная очистка полости глаза.
Правила применения
Среди основных правил применения выделяют:
- Выбор показаний осуществляется только после предварительной консультации врача.
- Курс выбирается в индивидуальном порядке, в зависимости от степени тяжести и состояния иммунитета.
- Предварительно следует предупредить индивидуальную гиперчувствительность и развитие аллергических проявлений.
- Перед нанесением местной формы требуется провести гигиенические процедуры, направленные на очистку кожных покровов.
- В случае нарушения работы почек изменяют дозировку с учетом индивидуальных особенностей.
- При появлении побочных эффектов требуется отменить препарат.
Можно ли применять Ацикловир при гриппе или простуде?

Поскольку простуда и грипп имеют вирусное происхождение и многие пациенты предпочитают применять средство с лечебной целью при вышеописанных патологиях, следует учитывать, что назначение вышеописанного препарата нецелесообразно.
Это связано с тем, что Ацикловир способен воздействовать лишь на один тип вируса.
Именно поэтому, в случае гриппа и простуды он не приведёт к ускорению выздоровления.
Назначению с профилактической целью эффективно в том случае, если требуется повышение общих иммунных сил.
Ацикловир при ОРВИ
Назначение при ОРВИ будет эффективно только с профилактической целью. Начало лечения во время клинических проявлений не вызовет положительного эффекта.
Именно поэтому средство можно использовать людям, со сниженным иммунитетом для предотвращения развития острых респираторных вирусных инфекций.
Противопоказания
Перед тем, как начать приём Ацикловир, требуется внимательно ознакомиться с наличием противопоказаний.
Среди основных выделяют:
- Наличие индивидуальной гиперчувствителтности, вне зависимости от того, развивается она на основной или любой из вспомогательных компонентов.
- Развитие гиперчувствительности на Валацикловир.
- Таблетированная форма запрещена к применению пациентам, до двухлетнего возраста.
- Системные формы нельзя применять кормящим женщинам.
Особые меры осторожности следует соблюдать:
- Использование системной формы для беременных женщин, у которых выражена неврологическая симптоматика.
- Применение таблеток или лиофилизата пациентам, с нарушениями работы почек, а также сочетании с цитостатическими средствами.
- Местная лекарственная форма применяется под строгим наблюдением беременным и кормящим женщинам.
Инструкция по применению
Приём Ацикловир следует проводить после употребления пищи, таблетку следует запить небольшим количеством воды.
Суточная доза Ацикловир будет составлять 1000 мг, которые, как правило делят на 5 приемов.
Дозировка зависит от заболевания:
![]()
При ВИЧ инфекции дозировка должна быть увеличена вдвое. Средний курс терапии составляет 10 суток.- С целью профилактики назначается употребление 400 мг дважды в сутки.
- Неосложненный генитальный герпес предусматривает также употребление 1000 мг вещества при пятикратном режиме в течение 10 суток. Рецидивирующий герпес лечится 5 дневным курсом с аналогичной дозировкой.
- В случае опоясывающего герпеса необходимо употреблять 800 мг пятикратно, курс лечения может длиться от 5 до 10 дней.
- При ветряной оспе доза Ацикловир составляет 3200 мг ежесуточно длительностью в 5 дней.

Дозировка следующая:
- Простой герпес требует введения 5-10 мг на килограмм массы тела трехкратно в течение недели.
- Для гениального герпеса вводится 5 мг на один килограмм при трехкратном введении на протяжении 5 дней.
- Энцефалит, который вызывается подобным возбудителем предусматривает введение 10 мг трехкратно в течение 10 дней.
- Для опоясывающего герпеса дозировка остаётся прежней, но длительность терапии составляет неделю.
Глазную мазь наносят в небольшом объеме, длиной не более одного сантиметра при помощи чистого пальца или специальной лопатки. Мазь следует закладывать пятикратно в сутки. Длительность терапии строго индивидуальна, так как требуется продолжать лечение в течение 3 суток после клиники выздоровления.
Побочные эффекты
Проявление побочных эффектов будет во многом зависеть от формы выпуска, которая применяется пациентом.
На фоне употребления таблеток развиваются:
- Аллергические проявления с кожной сыпью, зудом и отеком слизистых.
- Нарушения пищеварительной функции с формированием рвоты, диареи, тошноты и болей в животе.
- Неврологические проявления с головными болями, головокружениями, галлюцинациями различного характера.
- Поражения кровеносной системы с лейкопенией, лимфоцитопенией, нарушениями в биохимических показателях ферментов печения с возрастанием билирубин или трансаминаз.
При использовании лиофилизата может возникать:
- Поражение пищеварительной системы с тошнотой, рвотой и диспепсическими проявлениями.
- Высокий риск того, что проявится острая почечная недостаточность, особенно на фоне существующих патологий в мочевыводящей системе.
- Энцефалопатическая клиника с головокружением, галлюцинациями, нарушениями сознания, повышениями сонливости или психозами с судорожным синдромом.
- Аллергические реакции с преимущественно отечным синдромом.
Местная форма побочных эффектов от применения инъекционной формы выражается развитием флебитов в зоне введения.
Использование местной формы менее опасно, так как среди побочных эффектов могут проявляться:
- Эритемы.
- Зудящие элементы.
- Шелушение и сухость кожных покровов.
- Жжение.
При применении глазной мази развиваются:
- Блефариты.
- Конъюнктивиты.
- Кератиты.
- Местные жжения или отеки.
Передозировка
Развитие передозировки может быть вызвано несоблюдением правил приема, которые изложены в инструкции к Ацикловир, а также повышении индивидуальной чувствительности или неправильном использовании различных лекарственных форм.
Среди проявлений передозировки:
![]()
Нарушение функции мочевыводящих путей с недостаточностью почек, вплоть до острой недостаточности.- Поражение нервной системы с судорожным синдромом, потерями сознания, летаргическими состояниями, а также коматозными поражениями.
- При незначительной передозировке формируется головная боль, поражение пищеварительной системы с диареей, болью в животе, тошнотой, рвотой, диспепсическими проявлениями.
Лекарственное взаимодействие
Перед приемом Ацикловир требуется внимательно изучить влияние препарата на организм при сочетании с другими средствами.
Среди них следует отметить:
- Сочетание Ацикловир с иммуностимуляторами, в результате чего происходит развитие усиления эффектов.
- Пробенецид и Ацикловир формируют уменьшенную канальцевую секрецию последнего препарата, это вызывает увеличенное содержание вещества, уменьшая выведение.
- Микофенолат мофетил вызывает одновременное повышение концентрации двух препаратов.
- Нефротоксические препараты вызывают патологическое влияние Ацикловир на почки, повышая риск острой почечной недостаточности.
- Ацикловир в лиофилизате вызывает развитие щелочной реакции организма.
- Особое внимание следует уделять сочетанию Зиновудина у лиц с ВИЧ-инфекцией, это не приводит к побочным реакциям, а также симптомам передозировки.
Особые указания
Среди них выделяют:
- Ацикловир следует ограничить к употреблению при нарушениях функционального или органического характера в мочевыводящей системе.
- Проведение лечения одновременно с нефротоксическими препаратами, а также при патологиях почек требует регулярного контроля за лабораторными анализами. Требуется внимательно проводить инъекционное введение, запрещается введение с быстрой скоростью, а также использование при дегидратации. До периода полувыведения требуется контролировать креатинин и мочевину.
- Если герпес проявляется на губах рекомендовано для ускорения выздоровления сочетать Ацикловир в различных формах выпуска, например таблетки и мазь.
- Местные формы Ацикловир наносятся с особой осторожностью при нарушении целостности кожных покровов на слизистых оболочках. Особенно это касается использования Ацикловир при генитальных поражениях.
- Генитальный герпес предусматривает ограничение половых контактов с применением презерватива или полное исключение половой жизни на период лечения Ацикловир. Также Ацикловир применяют для профилактики заболевания полового партнера.
- Ацикловир при ветряной оспе чаще всего назначается пациентам, у которых диагностировано иммунодефицитное состояние, что предусматривает развитие осложнений.
Аналоги
Среди аналогичных средств выделяют:
- Валтрекс. Аналог Ацикловира, который в качестве основного действующего вещества включает валацикловир. Это обеспечивает использование препарата при сформированной лекарственной устойчивости. Механизм его действия, а также список показаний и противопоказаний у них сходен. Поскольку цена его в разы выше, возникают существенные ограничения к применению. Но, его назначение является обязательным у лиц с иммунодефицитом, в тех случаях, когда Ацикловир неэффективен.
- Зовиракс. Подобные лекарства имеют не только идентичный состав, но и схожий эффект с побочными проявлениями и клиникой передозировки.
- Виворакс. Аналог в виде таблеток, который содержит 200 мг действующего вещества. Он обладает схожим клиническим эффектом и показаниями к использованию. В результате низкого процента накопления в клетках возникает необходимость в длительном курсе терапии.



Купить препарат можно по средней цене в пределах 80-210 рублей.
Условия хранения
Хранить препарат нужно в температурных условиях не превышающих 25 градусов.
Условия продажи
Инъекционную и таблетированную форму можно приобретать при условии наличия рецепта, местная находится в свободной продаже.
Противовирусные препараты — соединения природного или синтетического происхождения, применяющиеся для лечения и профилактики вирусных инфекций. Действие многих из них избирательно направлено на различные стадии развития вирусной инфекции и жизненного цик
Противовирусные препараты — соединения природного или синтетического происхождения, применяющиеся для лечения и профилактики вирусных инфекций. Действие многих из них избирательно направлено на различные стадии развития вирусной инфекции и жизненного цикла вирусов.
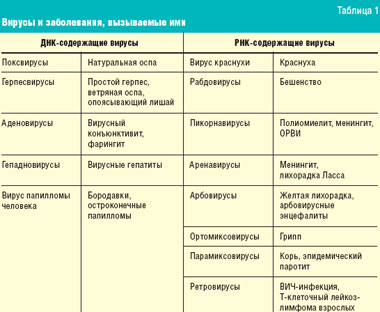
В настоящее время известно более 500 вирусов, возбудителей заболеваний человека. Вирусы содержат одно- или двухцепочечную рибонуклеиновую кислоту (РНК) или дезоксирибонуклеиновую кислоту (ДНК), заключенную в белковую оболочку — капсид. У некоторых из них есть и внешняя оболочка из липопротеидов. Многие вирусы содержат ферменты или гены, обеспечивающие репродукцию в клетке-хозяине. В отличие от бактерий у вирусов нет собственного обмена веществ: они используют метаболические пути клетки-хозяина.
РНК-содержащие вирусы или синтезируют матричную РНК (мРНК), или сама РНК выполняет функцию мРНК. На ней синтезируются вирусные белки, в том числе РНК-полимераза, при участии которой образуется мРНК вируса. Транскрипция генома некоторых РНК-содержащих вирусов осуществляется в ядре клетки-хозяина. Под действием обратной транскриптазы ретровирусов на основе вирусной РНК синтезируется комплементарная ей ДНК (провирус), которая встраивается в геном клетки-хозяина. В дальнейшем при транскрипции образуется как клеточная РНК, так и мРНК вируса, на которой синтезируются вирусные белки для сборки новых вирусов. Вирусы и заболевания, которые ими вызываются, отражены в табл. 1.
На стадии заражения вирус адсорбируется на клеточной мембране и проникает в клетку. В этот период применяются препараты, нарушающие этот процесс: растворимые ложные рецепторы, антитела к мембранным рецепторам, ингибиторы слияния вируса с клеточной мембраной.
На следующем этапе начинается внутриклеточный синтез вирусных компонентов. На этом этапе эффективны ингибиторы вирусных ДНК-полимераз, РНК-полимераз, обратной транскриптазы, геликазы, праймазы, интегразы. На трансляцию вирусных белков действуют интерфероны (ИФН), антисмысловые олигонуклеотиды, рибозимы и ингибиторы регуляторных белков. На протеолитическое расщепление воздействуют ингибиторы протазы.
ИФН и ингибиторы структурных белков активно воздействует на сборку вируса.
Заключительный этап репликационного цикла включает выход дочерних вирионов из клетки и гибель инфицированной клетки-хозяина. На этом этапе эффективны ингибиторы нейраминидазы, противовирусные антитела и цитотоксические лимфоциты.
Существуют различные классификации противовирусных средств. В данной статье представлена классификация по воздействию на тот или иной вирус (табл. 2).

Рассмотрим противогриппозные и противогерпетические препараты.
Классификация противовирусных препаратов, разрешенных к применению на территории России.
- руппа противогриппозных препаратов:
– Амантадин;
– Арбидол;
– Осельтамивир;
— Римантадин. - Препараты, действующие на герпесвирусы:
– Алпизарин;
– Ацикловир;
– Бонафтон;
– Валацикловир;
– Ганцикловир;
– Глицирризиновая кислота;
– Идоксуридин;
– Пенцикловир;
– Риодоксол;
– Теброфен;
– Тромантадин;
– Фамцикловир;
– Флореналь. - Антиретровирусные препараты:
– Абакавир;
– Ампренавир;
– Атазанавир;
– Диданозин;
– Залцитабин;
– Зидовудин;
– Индинавира сульфат;
– Ламивудин;
– Нелфинавир;
– Ритонавир;
– Саквинавир;
– Ставудин;
– Фосфазид;
– Эфавиренз. - Другие противовирусные препараты:
– Инозин пранобекс;
– Интерферон альфа;
– Интерферон альфа-2;
– Интерферон альфа-2b;
– Интерферон бета-1а;
– Интерферон бета-1b;
– Йодантипирин;
– Рибавирин;
– Тетраоксо-тетрагидронафталин (Оксолин);
– Тилорон;
– Флакозид.
Арбидол — производное индолкарбоновой кислоты. Механизм действия препарата складывается из подавления репродукции вируса гриппа, влияния на синтез ИФН, повышения количества Т-лимфоцитов и функциональной активности макрофагов, а также антиоксидантного эффекта.
Препарат проникает в неизмененном виде как в незараженные, так и в зараженные клетки и определяется в ядерной и цитоплазматической фракциях. Арбидол ингибирует процесс слияния липидной вирусной оболочки с мембранами эндосом (при рН 7,4), приводящий к высвобождению вирусного генома и началу транскрипции. В отличие от амантадина и римантадина, Арбидол ингибирует освобождение самого нуклеокапсида от наружных белков, нейраминидазы и липидной оболочки. Таким образом, Арбидол действует на ранних стадиях вирусной репродукции.
У препарата отсутствует штаммовая специфичность (в культурах клеток он подавляет репродукцию вируса гриппа А на 80%, вируса гриппа В — на 60% и вируса гриппа С — на 20%, а также воздействует и на вирус птичьего гриппа, однако слабее, чем на репродукцию человеческих штаммов вируса гриппа).
Синтез ИФН нарастает, начиная с приема 1 таблетки до 3 таблеток. Однако дальнейшего увеличения уровня ИФН при приеме Арбидола не наблюдается. Быстрое нарастание синтеза ИФН может оказывать профилактическое действие при приеме препарата до начала заболевания гриппом.
Арбидол оказывает иммуномодулирующее действие, приводя к повышению общего количества Т-лимфоцитов и Т-хелперов. Причем нормализация данных показателей наблюдалась у пациентов с исходно сниженным числом CD3- и CD4-клеток, а у лиц с нормальным функционированием клеточного звена иммунитета практически отсутствовали изменения количества Т-лимфоцитов и Т-хелперов. При этом применение Арбидола не ведет к существенному снижению абсолютного числа Т-супрессорных лимфоцитов — таким образом, стимулирующая активность препарата не связана с угнетением функции супрессорных клеток. Арбидол увеличивает общее число макрофагов с поглощенными бактериями и фагоцитарное число. Предполагается, что активирующими стимулами для фагоцитарных клеток явились цитокины и, в частности, ИФН, продукция которого усиливается под воздействием препарата. Увеличивается также содержание натуральных киллеров — NK-клеток, что позволяет характеризовать препарат как индуктор активности естественных киллеров.
Препарат быстро всасывается из желудочно-кишечного тракта (ЖКТ). Т1/2 составляет 16–21 ч. Экскретируется в неизмененном виде с калом (38,9%) и мочой (0,12%). В течение первых суток выводится 90% введенной дозы.
Лекарственные взаимодействия Арбидола с другими лекарственными препаратами в литературе не описаны.
Практически единственными побочными эффектами препарата являются аллергические реакции. Препарат разрешен к применению с 2-летнего возраста.
Арбидол обладает достаточно широким спектром противовирусного действия и используется для профилактики и лечения гриппа типов А и В, в том числе осложненного бронхитом и пневмонией; острых респираторных заболеваний (ОРВИ); хронического бронхита, пневмонии, рецидивирующей герпетической инфекции; в послеоперационном периоде — для нормализации иммунного статуса и профилактики осложнений.
Амантадин и римантадин — производные адамантана. Оба препарата даже в малых дозах подавляют репродукцию вируса А. Их противовирусная активность обусловлена двумя механизмами.
Во-вторых, они могут действовать и на этапе сборки вируса, по-видимому, за счет изменения процессинга гемагглютинина. Этот механизм возможен у некоторых штаммов вирусов.
Среди диких штаммов устойчивость к препаратам возникает редко, однако от больных, принимающих их, получают устойчивые штаммы. Чувствительность и устойчивость вирусов к амантадину и римантадину перекрестная.
Оба препарата хорошо всасываются при приеме внутрь, имеют большой объем распределения. Большая часть амантадина выводится с мочой в неизмененном виде. Период полувыведения (Т1/2) у молодых людей составляет 12–18 ч, у пожилых возрастает почти вдвое, а при почечной недостаточности увеличивается еще больше. Поэтому дозу препарата необходимо уменьшать даже при незначительном изменении функции почек. Римантадин активно метаболизируется в печени, Т1/2 в среднем составляет 24–36 ч, 60–90% препарата выводится с мочой в виде метаболитов.
При приеме обоих препаратов наиболее часто отмечают незначительные дозозависимые нарушения со стороны ЖКТ (тошнота, снижение аппетита) и центральной нервной системы (ЦНС) (раздражительность, бессонница, нарушение концентрации внимания). При приеме высоких доз амантадина возможно значительное нейротоксическое действие: спутанность сознания, галлюцинации, эпилептические припадки, кома (эти эффекты могут усиливаться при одновременном приеме Н1-блокаторов, М-холиноблокаторов, психотропных средств и этанола). Безопасность применения во время беременности не установлена. Разрешено применение с 7-летнего возраста.
Препараты применяются для профилактики и лечения гриппа А. Их прием во время эпидемий гриппа позволяет избежать инфекции в 70–90% случаев. У лиц с неосложненным гриппом А лечение препаратами в течение 5 дней в возрастных дозировках, начатое на ранней стадии заболевания, на 1–2 сут уменьшает длительность лихорадки и общих симптомов, ускоряет выздоровление и иногда сокращает период выделения вируса.
Осельтамивир является неактивным предшественником, который в организме превращается в активный метаболит — осельтамивира карбоксилат. Он является переходным аналогом сиаловой кислоты и избирательным ингибитором нейраминидазы вирусов гриппа А и В. Кроме того, он подавляет штаммы вируса гриппа А, устойчивые к препаратам — производным адамантана.
Нейраминидаза вируса гриппа отщепляет концевые остатки сиаловых кислот и, таким образом, разрушает рецепторы, находящиеся на поверхности клеток и новых вирусов, т. е. способствует выходу вируса из клетки по окончании репродукции. Активный метаболит осельтамивира вызывает изменения в активном центре нейраминидазы и подавляет ее активность. Происходит агрегация вирусов на поверхности клетки и замедляется их распространение.
Устойчивые штаммы вируса гриппа А обнаруживают у 1–2% больных, принимающих препарат. Устойчивых штаммов вируса гриппа В на сегодняшний день не обнаружено.
При приеме внутрь препарат хорошо всасывается. Прием пищи не влияет на его биодоступность, но снижает риск побочного действия на ЖКТ. Препарат подвергается ферментативному гидролизу в ЖКТ и печени с образованием активного метаболита. Объем распределения препарата приближается к объему жидкости в организме. Т1/2 осельтамивира и его активного метаболита составляет 1–3 и 6–10 ч соответственно. Оба соединения выводятся главным образом почками в неизмененном виде.
При приеме внутрь возможны незначительные неприятные ощущения в животе и тошнота, которые уменьшаются при приеме препарата во время еды. Желудочно-кишечные расстройства обычно проходят через 1–2 сут, даже если больной продолжает прием препарата. Клинически значимых взаимодействий осельтамивира с другими препаратами не выявлено. Препарат применяют у детей старше 1 года.
Осельтамивир применяют для лечения и профилактики гриппа. Профилактический прием осельтамивира в период эпидемий снижает заболеваемость как среди вакцинированных противогриппозной вакциной, так и среди невакцинированных. При лечении гриппа этим препаратом выздоровление наступает на 1–2 сут раньше, а количество бактериальных осложнений снижается на 40–50%.
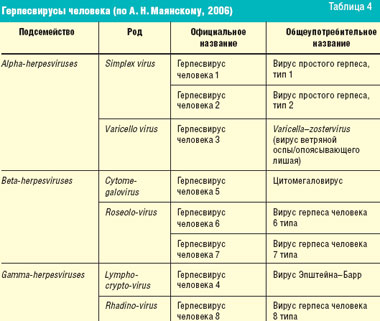
Прежде чем перейти к обсуждению противогерпетических средств, необходимо вспомнить различные вирусы герпеса и заболевания, вызываемые ими (табл. 4). К сожалению, в арсенале современных противовирусных средств нет препаратов, действующих на все вирусы герпеса одновременно (табл. 5).
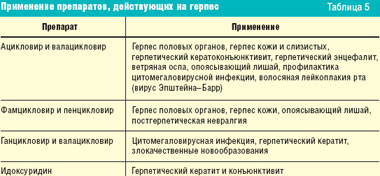
Вирус простого герпеса типа 1 вызывает поражение кожи, рта, пищевода и головного мозга, вирус простого герпеса типа 2 — поражение наружных половых органов, прямой кишки, кожи и мозговых оболочек. Первым из допущенных к применению противогерпетических препаратов был видарабин (1977). Однако ввиду высокой токсичности его применяли для лечения заболеваний, вызванных вирусом простого герпеса и Varicella–zostervirus, лишь по жизненным показаниям. С 1982 г. для лечения больных с менее тяжелым течением заболевания стали применять ацикловир.
Ацикловир — ациклический аналог гуанозина, а валацикловир — L-валиновый эфир ацикловира. Ацикловир подавляет синтез вирусной ДНК после фосфорилирования вирусной тимидинкиназой внутри зараженных клеток. Образующийся в клетке ацикловиртрифосфат встраивается в синтезируемую в клетке-хозяине цепь ДНК, что приводит к прекращению роста вирусной цепи ДНК. Молекула ДНК, в состав которой входит ацикловир, связывается с ДНК-полимеразой, необратимо инактивируя ее.
Устойчивость вируса может возникнуть в результате снижения активности вирусной тимидинкиназы и изменения вирусной ДНК-полимеразы. Изменение активности ферментов возникает в результате мутаций.
Биодоступность ацикловира при приеме внутрь составляет всего 10–30% и уменьшается с увеличением дозы. В отличие от ацикловира, биодоступность валацикловира при приеме внутрь достигает 70%. Препарат быстро и почти полностью превращается в ацикловир. Ацикловир проникает во многие биологические жидкости, в том числе в содержимое везикул при ветряной оспе, спинно-мозговую жидкость, накапливается в молоке, околоплодных водах и плаценте. Концентрация его во влагалищном содержимом колеблется в широких пределах. Сывороточная концентрация препарата у матери и новорожденного примерно одинаковы. Через кожу препарат практически не всасывается. Т1/2 ацикловира составляет в среднем у взрослых 2,5 ч, у новорожденных — 4 ч, у больных с почечной недостаточностью может увеличиваться до 20 ч. Препарат практически полностью выводится почками в неизмененном виде. При беременности фармакокинетика препаратов не меняется.
Как правило, ацикловир переносится хорошо. При применении мази на основе полиэтиленгликоля возможно раздражение слизистой половых органов и чувство жжения. При приеме внутрь препарат изредка вызывает головную боль, головокружение, сыпь и диарею. Еще реже отмечаются почечная недостаточность и нейротоксическое действие. Побочные эффекты валацикловира сходны с таковыми у ацикловира — тошнота, диарея, головная боль; высокие дозы могут вызвать спутанность сознания, галлюцинации, поражения почек и — очень редко — тромбоцитопению. При внутривенном введении больших доз ацикловира могут развиться почечная недостаточность и поражения ЦНС.
Фамцикловир сам неактивный, но при первом прохождении через печень быстро превращается в пенцикловир. Пенцикловир — это ациклический аналог гуанозина. Механизм действия препарата сходен с механизмом действия ацикловира. Как и ацикловир, пенцикловир действует главным образом на вирусы простого герпеса и Varicella–zostervirus. Устойчивость к пенциклавиру в клинике встречается редко.
В отличие от пенцикловира, биодоступность которого при приме внутрь составляет лишь 5%, фамцикловир хорошо всасывается. При приеме фамцикловира биодоступность пенцикловира возрастает до 65–77%. Прием пищи совместно с препаратом замедляет всасывание последнего, но в целом биодоступность не снижается. Объем распределения пенцикловира в 2 раза превышает объем жидкости в организме, Т1/21/2 увеличивается до 9,9 ч. Препарат легко удаляется при гемодиализе.
Переносится ацикловир хорошо, но иногда возможно возникновение головной боли, тошноты, диареи, крапивницы, а у пожилых людей — галлюцинаций и спутанности сознания. Препараты для местного применения могут вызвать контактный дерматит и изъязвления.
Безопасность препарата во время беременности, а также взаимодействие его с другими лекарственными средствами не установлена.
Ганцикловир — это ациклический аналог гуанозина. Механизм действия препарата сходен с механизмом действия ацикловира. Активен в отношении всех герпесвирусов, но наиболее эффективен в отношении цитомегаловируса.
Биодоступность ганцикловира при приме внутрь во время еды составляет 6–9% и несколько меньше при приеме натощак. Валганцикловир хорошо всасывается и быстро гидролизуется до ганцикловира, биодоступность которого возрастает до 61%. При приеме валганцикловира во время еды биодоступность ганцикловира повышается еще на 25%. При нормальной функции почек Т1/2 составляет 2–4 ч. Более 90% препарата выводится почками в неизмененном виде. При почечной недостаточности Т1/2 увеличивается до 28–40 ч.
Основной дозалимитирующий побочный эффект ганцикловира — угнетение кроветворения (нейтропения, тромбоцитопения). У 5–15% больных отмечают поражения ЦНС разной степени тяжести (от головной боли до судорог и комы). При внутривенном введении возможны флебиты, азотемия, анемия, сыпи, лихорадка, изменение биохимических показателей печени, тошнота, рвота, эозинофилия.
У лабораторных животных препарат оказывал тератогенное и эмбриотоксическое действие, необратимо нарушал репродуктивную функцию. Цитостатические препараты усиливают побочное действие ганцикловира на костный мозг.
Идоксуридин — йодсодержащий аналог тимидина. Механизм противовирусного действия до конца не изучен. Известно, что фосфорилированные производные препарата встраиваются в вирусную и клеточную ДНК, но ингибируют репликацию только вирусной ДНК. При этом ДНК становится более хрупкой, легко разрушается, при ее транскрипции чаще возникают ошибки. Устойчивые штаммы выделяют от больных герпетическим кератитом, получавших идоксуридин. Препарат разрешен лишь для местного применения. При его использовании возможны боль, зуд, воспаление и отек в области глаз, аллергические реакции.
Успехи антимикробной терапии ХХ столетия привели к почти полному контролю над бактериальными инфекциями. Задачей инфекционистов и фармакологов ХХI века является обеспечение контроля над вирусной инфекцией. Помимо высокой эффективности новые противовирусные препараты должны обладать хорошей переносимостью. В настоящее время разрабатываются новые средства с принципиально новыми механизмами действия. Перспективными могут оказаться средства для подавления патологических иммунных реакций и иммунотерапия моноклональными антителами и вакцинами.
Н. М. Киселева, кандидат медицинских наук, доцент
Л. Г. Кузьменко, доктор медицинских наук, профессор
РГМУ, Москва
Читайте также:





