Антисинтетазный синдром при дерматомиозите
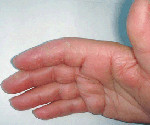
Антисинтетазный синдром – это особый тип течения дерматомиозита, характеризующийся острым началом, интерстициальным легочным фиброзом, резистентностью к стандартной глюкокортикостероидной терапии. Клиническая картина складывается из лихорадки, признаков фиброзирующего альвеолита (кашля, одышки), феномена Рейно (бледности и цианоза пальцев кистей). Иногда возникают мышечная слабость, артралгии. Диагноз подтверждается определением в крови антисинтетазных антител, гистологическими исследованиями биоптатов легких и мышц. Терапия проводится с помощью мощных иммуносупрессивных и антифибротических препаратов, пульс-терапии ГКС. Хирургическое лечение заключается в пересадке легких.
МКБ-10
- Причины
- Патогенез
- Классификация
- Симптомы
- Осложнения
- Диагностика
- Лечение антисинтетазного синдрома
- Прогноз и профилактика
- Цены на лечение
Общие сведения
Антисинтетазный синдром (АСС) является не самостоятельным заболеванием, а подтипом дерматомиозита – хронической диффузной болезни соединительной ткани из группы воспалительных миопатий. Для дерматомиозита специфично преобладание симптомов поражения скелетных мышц и кожных покровов. Отличительная особенность АСС – преимущественное вовлечение в патологический процесс легочной ткани. АСС наблюдается при мерно в 20-30% случаев дерматомиозита и может возникнуть в любом возрасте. Пики заболеваемости приходятся на 10-15 лет, 45-54 года и 75-84 года. Дерматомиозитом чаще страдают женщины, в то время как АСС встречается одинаково у обоих полов.

Причины
Точная причина АСС не установлена. Предполагается этиологическая роль инфекционных возбудителей – вирусных (вируса Коксаки, герпеса, пикорнавируса), бактериальных (риккетсий), паразитарных (токсоплазм, трихинелл). Рассматривается вероятность генетической предрасположенности к дерматомиозиту и АСС. В ходе генетических исследований у многих пациентов были обнаружены определенные антигены гистосовместимости. В частности, АСС обычно ассоциирован с HLA B8, DR3, B14. Описанные случаи заболеваемости среди монозиготных близнецов и близких родственников подтверждают наследственный характер дерматомиозита и АСС. К провоцирующим факторам относят вакцинацию, длительное применение некоторых лекарственных средств (антибиотиков, инсулина), чрезмерную физическую нагрузку. Самым значимым из них считается продолжительная инсоляция.
Патогенез
Основным звеном патогенеза является гиперактивация клеточного и гуморального иммунитета. У предрасположенных лиц под действием различных триггеров вырабатываются миозит-специфические и миозит-ассоциированные антитела. При АСС наиболее изучены антитела к гистидил-тРНК-синтетазе. В результате реакций иммунной аутоагрессии происходит клеточная инфильтрация скелетных мышц, их воспаление с последующей атрофией.
Образующиеся иммунные комплексы оседают на эндотелии сосудов мелкого калибра, вызывая нарушение микроциркуляции. В легочной ткани наблюдается накопление лимфоцитов, пролиферация мезенхимальных клеток с избыточным выделением коллагена, что приводит к патологическому разрастанию экстрацелюллярного матрикса и уплотнению паренхимы легких (фиброзу).
Классификация
По степени вовлечения мышц при антисинтетазном синдроме различают амиопатический и гипомиопатический варианты. Встречаются перекрестные формы с системной склеродермией, криоглобулинемическим васкулитом. По типу поражения легких выделяют следующие формы АСС:
- Быстропрогрессирующая. Самая неблагоприятная форма. Типичны стремительное развитие дыхательной недостаточности, высокая частота летальных исходов.
- Медленно прогрессирующая. Манифестирует постепенно в виде небольшой одышки и непродуктивного кашля.
- Субклиническая. Отличается практически полным отсутствием респираторных симптомов при наличии рентгенологических изменений в легких.
Симптомы
Чаще всего антисинтетазный синдром дебютирует в весеннее время, для него характерно острое начало и течение. Появляется лихорадка (от субфебрильных цифр до 39°С), незначительные боли в мелких суставах кистей, упорный сухой кашель. Затрудняется дыхание по типу смешанной одышки: сначала при выполнении физических нагрузок, затем в спокойном состоянии. Дыхательная дисфункция может быть вызвана как фиброзирующим альвеолитом, так и функциональной неполноценностью дыхательной мускулатуры (диафрагмы, межреберных мышц).
Пациентов беспокоит мышечная слабость, которая особенно выраженно ощущается при ходьбе по лестнице, подъеме со стула, выполнении бытовых действий (расчесывании волос, одевании, умывании). Это связано с более сильным воспалительным процессом в проксимальных мышцах верхних и нижних конечностей. Иногда из-за слабости мышц глотки, гортани, верхней трети пищевода возникают осиплость голоса, дисфагия. Суставной синдром протекает в виде симметричных незначительных болей в лучезапястных суставах и мелких суставах кистей, быстро проходящих в процессе лечения.
Осложнения
Большинство осложнений антисинтетазного синдрома развивается вследствие фиброзирующего альвеолита и сосудистых патологий. Быстропрогрессирующий фиброз легких у 70% пациентов приводит к дыхательной недостаточности, требующей экстренного медицинского вмешательства. При перифокальном отеке легочных сосудов повышается давление в малом круге кровообращения (легочная гипертензия). Длительный вазоспазм при феномене Рейно опасен ишемическими васкулопатиями (некрозом, сухой гангреной пальцев рук). Функциональная несостоятельность мышечного аппарата глотки и пищевода может осложниться аспирационной пневмонией. К редким неблагоприятным последствиям АСС относится острая почечная недостаточность, причиной которой является высвобождение большого количества миоглобина из мышц при массивном воспалении.
Диагностика
Пациентов с антисинтетазным синдромом ведут ревматологи и пульмонологи. При физикальном обследовании, в частности, пальпации мышц, пациент ощущает боль. В случае дыхательной недостаточной обращают на себя внимание цианоз губ, активное участие при дыхании вспомогательной мускулатуры, симптом барабанных палочек (колбовидное утолщение концевых фаланг пальцев). Дополнительное обследование включает:
Антисинтетазный синдром следует, прежде всего, дифференцировать с диффузными болезнями соединительной ткани, заболеваниями суставов (системная склеродермия, ревматоидный артрит). Также, вследствие сходства клинической картины АСС с системными васкулитами, сопровождающимися поражением легких, необходимо проводить дифференциальную диагностику с узелковым полиартериитом, синдромом Чержда-Стросса, гранулематозом Вегенера. Кожные высыпания требуют дифференцировки с дерматологическими патологиями, такими как экзема, псориаз, атопический дерматит. При быстропрогрессирующем легочном фиброзе обязательно исключение тромбоэмболии легочной артерии, пневмонии бактериальной или вирусной этиологии.
Лечение антисинтетазного синдрома
Все пациенты подлежат госпитализации в отделение клинической ревматологии, а при тяжелой дыхательной недостаточности – в палату интенсивной терапии для подключения к аппарату искусственной вентиляции легких. Этиотропной терапии не существует. Основная роль отводится патогенетическому лечению. Различают следующие направления лекарственной терапии АСС:
- Противовоспалительная. С целью купирования воспаления назначаются лекарственные средства (ЛС) с мощным иммуносупрессивным действием (микофенолата мофетил, циклофосфамид, метотрексат) в комбинации с пульс-терапией глюкокортикостероидами (преднизолон, метилпреднизолон). При их неэффективности прибегают к генно-инженерным биологическим препаратам – моноклональным антителам (инфликсимаб, ритуксимаб), блокаторам стимуляции Т-лимфоцитов (этанерцепт, абатацепт).
- Антифибозная. Традиционно для подавления процессов фиброза в легких используются гамма-интерферон, D-пеницилламин и колхицин. Перспективными современными антифибротическими лекарствами считаются пирфединон - ингибитор фибротических цитокинов и иматиниба месилат – специфический ингибитор тирозинкиназы.
- Вазоактивная. Для улучшения кровообращения в области периферических сосудов и предупреждения ишемических осложнений синдрома Рейно применяются ЛС, улучшающие микроциркуляцию – блокаторы медленных кальциевых каналов (амлодипин, нифедипин) и ксантинола никотинат. При агрессивном течении синдрома Рейно данные ЛС меняют на аналоги простагландина Е1 (алпростадил).
При резистентности к фармакотерапии проводятся экстракорпоральные процедуры (плазмаферез), удаляющие из плазмы крови циркулирующие антитела. При генерализованном фиброзном процессе в легких, вызывающем выраженную дыхательную недостаточность, а также безуспешности всех предыдущих методов лечения выполняется жизнеспасающая операция - трансплантация легких.
Прогноз и профилактика
АСС является тяжелой патологией. Прогноз главным образом определяется степенью легочного фиброза. При быстропрогрессирующей форме смерть наступает в 60-70% случаев от легочной недостаточности. Медленно прогрессирующий вариант протекает более доброкачественно. Частота летального исхода составляет 25-30%. Благоприятный прогноз наблюдается у больных с субклиническим вариантом. При своевременной диагностике и адекватном лечении смертность у таких пациентов практически не отличается от общей популяции. Так как этиологический фактор антисинтетазного синдрома остается неизвестным, эффективных профилактических мер в настоящее время не существует.
Рубрика МКБ-10: M35.8
Содержание
- 1 Определение и общие сведения
- 2 Этиология и патогенез
- 3 Клинические проявления
- 4 Другие уточненные системные поражения соединительной ткани: Диагностика
- 5 Дифференциальный диагноз
- 6 Другие уточненные системные поражения соединительной ткани: Лечение
- 7 Профилактика
- 8 Прочее
- 9 Источники (ссылки)
- 10 Дополнительная литература (рекомендуемая)
- 11 Действующие вещества
Антисинтетазный синдром
Антисинтетазный синдром представляет собой клинически гетерогенную форму идиопатической воспалительной миопатии, характеризующуюся наличием миозита, артралгий, феномена Рейно, руки "механика", интерстициального заболевания легких, а также присутствием в сыворотке крови аутоантител к аминоацил-тРНК-синтетазе (anti-ARS).
Распространенность и ежегодный уровень заболеваемости не известны. Антисинтетазный синдром относится к группе полимиозитов и дерматомиозитов, их общая распространенность оценивается приблизительно как 1/4,650. Примерно четверть из этих пациентов могут иметь антисинтетазный синдром, обеспечивая гипотетически оценку распространенности в 1 / 25,000 - 1/33000. Заболевание поражает женщин в два раза чаще, чем у мужчин.
Точные механизмы, приводящие к возникновению антисинтетазного синдрома не известны. Вирусные инфекции, как полагают, способствуют формированию антисинтетазных антител. Гены HLA-DRB1*0301, DQA1*0501 и DQB1*0201 являются факторами риска развития заболевания.
Возраст начала сильно варьирует (диапазон от 19 до 82) со средним значением 50 лет. Интерстициальное заболевание легких является одним из клинических признаков синдрома, респираторные симптомы (одышка, кашель, дисфагия) встречаются у 40-60% больных в начале заболевания. Дыхательная недостаточность может быть острой или развиваться постепенно. У некоторых пациентов развивается явно выраженный миозит, в то время как у других может наблюдаться гипо- или даже амиопатическая формы заболевания. В начале болезни, у 20-70% пациентов наблюдается мышечная слабость проксимальных и осевых мышц, у многие проявляется миалгия и ригидность мышц, напоминая клиническую картину полимиозита или дерматомиозита. Другие основные клинические признаки антисинтетазного синдрома: повышенная температура тела, потеря аппетита, потеря веса, как правило, симметричный артрит, артралгия, тендовагинит, синдром Рейно, гелиотропная сыпь, нарушения моторики дистального отдела пищевода и рука "механика" (растрескивание и шелушение кожи боковых и дистальных отделов рук). Редко сообщалось о появлении Shawl- и V - признаков (эритема на спине и плечах или на передней поверхности шеи и грудной клетки в форме буквы - V) и околоногтевой эритемы. Легочная артериальная гипертензия отмечаласьу некоторых пациентов, как серьезное осложнение течения синдрома.
Пациенты в основном являются положительными по одному из семи антисинтетазных аутоантител: анти-Jo-1 является наиболее распространенными из них (70% случаев). Диагноз основывается на клинических признаках и подтверждается положительным серологическим анализом на присутствие антисинтетазных антител (анти-Jo-1, анти-PL-12, анти-PL-7, анти-OJ, анти-KS). Интерстициальное заболевание легких диагностируется с помощью компьютерной томографии легких. Уровень креатинфосфаткиназы часто значительно повышен. Отсутствие миозита или интерстициальной болезни легких не исключает диагноз антисинтетазного синдрома. Диагноз также нельзя исключать у пациентов с интерстициальной болезнью легких и/или воспалительной миопатией при наличии антисинтетазных аутоантител.
Дифференциальный диагноз включает другие воспалительные миопатии и идиопатическую изолированную интерстициальную болезнь легких, также как и обычную интерстициальную пневмонию. Участие суставов может также имитировать или даже пересекаться с ревматоидным артритом.
Кортикостероиды (преднизолон) внутрь и иммунодепрессанты являются основой лечения. Нет единого мнения по схемам лечения при антисинтетазном синдроме. В зависимости от тяжести и симптоматики, схемы лекарственной терапии может включать в себя азатиоприн, метотрексат, циклофосфамид, циклоспорин, такролимус, микофенола мофетил или ритуксимаб. Дерматологические симптомы эффективно купируются с помощью гидроксихлорохина. У больных с сочетанной интерстициальной болезнью легких, реакция на иммуносупрессивную терапию, как правило, положительная.
Прогноз неблагоприятный в тяжелых случаях, иногда заболевание имеет летальный исход. В других случаях, может быть достигнута стабилизация или улучшение состояния. Прогрессирование интерстициальной болезни легких является основным отрицательным прогностическим фактором. Антисинтетазный синдром является хроническим заболеванием, требующим длительного лечения.
Синдром эозинофилии—миалгии
Этиология и патогенез
Во всех случаях развитию заболевания предшествует прием триптофана, содержащего токсичные примеси.
Клинические проявления
Первое описание синдрома эозинофилии—миалгии относится к концу 80-х гг., когда была отмечена вспышка заболевания, проявлявшегося миалгией и выраженной эозинофилией. Синдром эозинофилии—миалгии — системное заболевание. Поражение легких наблюдается у 50—60% больных, рентгенологические изменения в легких — у 15—25%. Основные симптомы — кашель, одышка, свистящее дыхание, миалгия, повышенная утомляемость, слабость мышц, артралгия, отеки, восходящая полинейропатия.
Диагностика
Число эозинофилов в крови превышает 1000 мкл –1 . При поражении легких наблюдается гипоксемия. Рентгенография и КТ грудной клетки выявляют сетчатое или сетчато-узелковое поражение и плевральный выпот. Во время физической нагрузки значительно снижается диффузионная способность легких и уменьшается легочный кровоток. При исследовании функции внешнего дыхания иногда определяются рестриктивные нарушения. В биоптатах пораженных органов обнаруживается инфильтрация тканей и мелких сосудов лимфоцитами, моноцитами и эозинофилами.
Диагноз ставят, если в анамнезе есть указания на миалгию, одышку и эозинофилию после приема триптофана.
Несмотря на то что в США триптофан снят с производства в 1990 г., это заболевание все же встречается. Прогноз благоприятный. У части больных прекращение приема триптофана и назначение кортикостероидов быстро приводит к улучшению, у других симптомы сохраняются дольше.

Открытие новых аутоантигенных систем, связанных с идиопатическими воспалительными миопатиями (миозитами) у взрослых и детей, имеет серьезные последствия для диагностики и лечения этой группы заболеваний в отношении широкого спектра медицинских специальностей. Традиционно аутоантитела, обнаруженные у пациентов с миозитом, описываются как аутоантитела, специфичные для миозита (МСА), или аутоантитела, ассоциированные с миозитом (МАА), в зависимости от их распространенности при других состояниях. Однако некоторые МСА более тесно связаны с внемышечными проявлениями, такими как заболевания кожи и легких, чем с самим миозитом. Каждое МСА связано с отличительной формой заболевания или фенотипа, что имеет последствия для диагностики и более персонализированного подхода к терапии. Знание функции и локализация аутоантигенных мишеней для МСА обеспечило ключевое понимание потенциальных иммунопатогенных механизмов миозита. В частности, данные свидетельствуют о том, что изменение экспрессии аутоантигена, связанного с миозитом, с помощью определенных воздействий или онкогенеза окружающей среды может быть поворотным событием, связывающим генерацию аутоантител с развитием болезни.
МСА и их клинические ассоциации Хотя было показано, что при регенерации мышечных волокон активируются определенные антигены, отдельный индивидуум будет генерировать только один тип МСА (то есть, для одного аутоантигена), что позволяет точно определить клинические фенотипы, связанные с каждым отдельным МСА. Ключевыми клиническими особенностями пациентов с миозитом являются болезни кожи, мышц и легких и озлокачествление; хотя спектр заболевания очень гетерогенен, используя аутоантитела можно идентифицировать подмножества пациентов с относительно однородными клиническими признаками.
Антисинтетазный синдром
АСС является наиболее распространенным фенотипом, связанным с миозитом, наблюдаемым у взрослых и хорошо описан в литературе.
Наиболее распространенное анти-АРС-антитело (АТ к маиноацил-тРНК-синтетазе) распознает Jo1 (гистидил-тРНК-синтетаза) и впервые было идентифицировано в 1980 году. Хотя аутоантитела против Jo1 часто считаются классическими к полимиозиту, у пациентов с АСС может развиться кожная сыпь, типичная для дерматомиозита. Кроме того, АСС имеет свою собственную гистологическую картину при биопсии мышц, которая наиболее часто подходит для диагностики дерматомиозита в соответствии с гистологическими критериями европейского нейромышечного центра.
Иммуноопосредованная некротизирующая миопатия
ИОНМ является подтипом миозита, который жестко связан с антителами к частицам распознавания сигналов (signal recognition particle (SRP)) и к 3-гидрокси-3-метилглутарил-CoA-редуктазе (3-hydroxy-3-methylglutaryl CoA reductase (HMGCR)). Характерно, что в образцах биопсии мышц отмечался миофибрильный некроз с минимальными или отсутствующими воспалительными инфильтратами. Пациенты с ИОНМ обычно имеют очень высокий уровень креатинкиназы, часто имеют выраженную мышечную слабость и могут быть устойчивыми к традиционной иммуносупрессивной терапии. В дополнение к вышеуказанным особенностям, аутоантитела против SRP были связаны с тяжелой болезнью мышц; в одном исследовании также была обнаружена возможная связь с участием сердечной мышцы, хотя этот вывод не был подтвержден в последующих исследованиях. Дисфагия и интерстициальное поражение легких также были зарегистрированы у пациентов с анти-SRP аутоантителами.
Анти-HMGCR аутоантитела связаны с ИОНМ и с использованием статинов, хотя, только 40–60% пациентов с этими аутоантителами имеют историю использования статинов. Анти-HMGCR аутоантитела не присутствуют, однако, у пациентов со связанной со статинами миалгией, а также у пациентов с мягкими повышениями уровней креатинкиназы, и, по-видимому, специфичны для ИОНМ. Сообщается, что пациенты с анти-HMGCR-аутоантителами хорошо реагируют на лечение, но пациенты, использующие статины, которые были моложе при начале заболевания, могут быть резистентны к терапии.
Исследование 2017 года, в котором были стратифицированы пациенты с аутоантителами против HMGCR в группы по возрасту начала заболевания (4–52 года, 53–61 год и 61–84 года), показало, что более молодые пациенты с аутоантителами против HMGCR имели более тяжелое заболевание и худший прогноз, чем те, кто был старше во время начала заболевания, но эти характеристики болезни не были независимо связаны с историей использования статинов.
Связанный с раком миозит
Повышенный риск развития рака у пациентов с миозитом, особенно с дерматомиозитом недавнего начала, признавался многие годы. Связанный с раком миозит обычно определяется как развитие злокачественности в течение 3 лет после постановки диагноза миозита. Миозит ассоциируется со злокачественными новообразованиями у взрослых, но не при начале в детском возрасте. Связь между дерматомиозитом и злокачественными новообразованиями особенно сильна у пациентов с антителами к транскрипции промежуточного фактора 1γ (transcription intermediary factor 1γ (TIF1γ), также известного как TRIM33) или белка ядерной матрицы 2 (nuclear matrix protein 2 (NXP2), также известного как MORC3). Действительно, более 50% взрослых пациентов с аутоантителами против TIF1γ будут иметь ассоциированный рак. Озлокачествление чаще встречается у лиц с анти-TIF1γ и анти-TIF1α-аутоантителами, чем у пациентов только с аутоантителами против TIF1γ. Антиантитела против NXP2 обнаруживаются у 15% пациентов с ювенильным дерматомиозитом, и эти антитела также были связаны с злокачественными новообразованиями у взрослых пациентов с дерматомиозитом. Увеличение распространенности злокачественных новообразований у взрослых пациентов с аутоантителами против NXP2 делает эту ассоциацию заслуживающей внимания проблемой.
Хотя было показано, что аутоантигены миозита, включая белки TIF1, активируются при определенных раках, соответствующие МСА не были идентифицированы в когортах рака, что свидетельствует о том, что их присутствие специфично для миозита.
Дерматомиозит
Источник:
McHugh N. J., Tansley S. L. Autoantibodies in myositis //Nature Reviews Rheumatology. – 2018. – Т. 14. – №. 5. – С. 290.
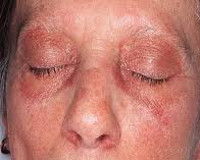
Гелиотропная сыпь при дерматомиозите проявляется в 75% случаев от общего числа пациентов с таким диагнозом. При заболевании двигательная функция мускулатуры нарушается. Важно вовремя заметить заболевание и начать лечение.

Особенности и причины
Заболевание нельзя назвать распространенным. Подтверждение диагноза наблюдается в среднем у 5 человек на один миллион. Специфика болезни встречается у пожилых людей, пересекших 50-летний рубеж, или у детей, не достигших пятнадцатилетнего возраста.
- Какие факторы провоцируют появление миозита
- Межреберный миозит: лечение недуга
Вредоносные микроорганизмы могут долго просуществовать в теле человека, пока не появится провоцирующий механизм. В его роли может выступать:
- Острые инфекционные заболевания.
- Частые стрессовые ситуации.
- Аллергическая реакция.
- Вакцинация.
- Солнечный удар или перегрев организма.
- Переохлаждение.
Чаще болезни подвержены женщины, мужчины болеют дерматомиозитом почти в два раза реже. Не стоит упускать факт, что болезнь имеет генетическую предрасположенность. Причины становятся лишь пусковым механизмом, вследствие которого начинается процесс поражения мускулатуры.
Симптомы заболевания

Начало заболевания не прогрессирующее, симптомы дерматомиозита проявляются постепенно. Слабость в мышцах ног и рук неуклонно растет, в некоторых случаях мышечная слабость проявляет себя в течение 5 лет в качестве редких, неназойливых болевых синдромов. Больные жалуются на следующие проявления симптомов:
- болевой синдром в мышцах,
- слабость в конечностях,
- повышение температуры тела, лихорадочное состояние,
- кожные сыпи, в том числе гелиотропный вид сыпи,
- ходьба по лестнице, подъем с кровати сопровождаются трудностями в виде болевых ощущений и дискомфорта,
- отечность мышц, локализованная очагом поражения,
- синдром Рейно.
В редких случаях симптоматика набирает резкие обороты. В течение 2-4 недель организм человека выдает полную клиническую картину болезни.
Дерматомиозит, как и многие аутоиммунные заболевания, протекает в трех формах:
- Острая, для которой характерен пик проявления симптомов. В этот период в организме больного может происходить распад мышечной ткани, который вызывает интоксикацию организма. Мускулатура подвергается обездвиживанию, существует риск поражения сердечно-сосудистой системы вплоть до летального исхода. Острое течение болезни развивается стремительно, для проявления осложнений достаточно 2-3 месяца.
- Подострая , с наблюдением снижения активности развития поражения. Проявляется после удачного на первый взгляд лечения дерматомиозита. Однако, по прошествии некоторого времени, болезнь рецидивирует, поражая внутренние органы. Симптомы развиваются достаточно медленно, проявление полной клинической картины может занять от года до двух лет.
- Хроническая, развивается, когда болезнь приобретает частый или постоянный характер, но имеющей более благоприятный вариант течения болезни. Поражение происходит лишь на небольшом участке мышц, что не мешает человеку вести обычный образ жизни. Если наблюдается кальциноз, существует огромный риск обездвиживания конечностей.
Помимо форм течения дерматомиозита, патологический процесс имеет три основных периода, которые отличаются степенью активности заболевания:
- Продромальный период. Он считается первой и начальной ступенью, во время которой наблюдаются признаки: отеки век, лихорадка.
- Манифестный период. Кожные проявления дерматомиозита в это время особо выражены.
- Дистрофический или кахектический период, во время которого проявляются осложнения. Третий период наступает вследствие бездействия на начальных стадиях болезни.
Когда отсутствует кожная сыпь, это говорит о полимиозите. Лечение полиомиозита отличается от терапии дерматомиозита только отсутствием методов, направленных на избавление кожи от покраснения и зуда. В остальном, симптоматика, диагностика и лечение этих болезней схожи. Дерматомиозит может поражать области, подверженные инфекционным заболеваниям:
- слизистая глаза, что ведет за собой конъюктивит,
- ротовая полость, вызывая стоматит,
- глотка, с вытекающим фарингитом.
При возникновении дерматомиозита самостоятельно, его классифицируют как первичную форму. Вторичный дерматомиозит развивается на фоне опухолевых процессов. Опухоль и поражение мышц имеют прямую связь друг с другом.
Болезнь развивается у взрослых и детей. Воспалительный процесс мышц в детском возрасте называется , ювенильный дерматомиозит. Заболевание может протекать с васкулитами – опухолями, склонными к рецидиву. От ювенильного дерматомиозита страдают одинаковое число мальчиков и девочек.
На начальных стадиях дерматомиозита, симптомы могут быть неярко выражены, эта стадия дает больше шансов на быстрое восстановление мышечной активности.
Поражение кожи при дерматомиозите
Поражение кожи является основным признаком заболевания. На кожных покровах возникают высыпания разного рода:
Пятна могут быть разного рода, проявляться в виде красных точек. Над суставами кистей рук, они покрываются чешуйками и вызывают зуд. Раздражение кожных покровов приводит к расширению сосудов, появляются предпосылки варикоза.
Эритема на открытых частях тела встречается у 40% больных. Затрагивание патологическим процессом мышцы лица, лишают человека возможности проявления эмоций. Мимика становится заторможенной. Не обойтись без помощи невропатолога, который займется лечением с учетом степени поражения лицевых мышц.
Подобная симптоматика – явный признак нарушения работы организма, в частности иммунитета человека.
Поражение мышц при дерматомиозите
Для дерматомиозита характерна слабость мышц шеи. Поражение проксимальных отделов мускулатуры затрудняют больному стереотипные телодвижения, становится трудно вставать, одеваться или совершать акты гигиены. При запущенном течении полиомиозита человеку сложно держать голову самостоятельно. Возникают трудности в передвижении, пациент не может долго держать предметы средней тяжести.

В некоторых случаях, болезнь повреждает мышцы пищеварительного тракта: глотки, гортани, пищевода. Это приводит к нарушению речи, внезапным и беспричинным приступам кашля. Глотание даже мягкой пищи вызывает болезненные ощущения.
Миозит затрагивает следующие отделы:
- Дистальные мышцы конечностей. Патология отзывается отечностью, болевым синдромом, в запущенных случаях развивается атрофия.
- Межреберные мышцы.
- Когда страдает диафрагма, легкие перестают полностью расправляться, что приводит к пневмонии.
- Область глаз поражается крайне редко.
Около 50% больных дерматомиозитом или миозитом отмечают проявление различных симптомов нарушения работы желудочно-кишечного тракта:
- кишечная непроходимость,
- запор,
- понос,
- в редких случаях наблюдается анорексия, полное отсутствие аппетита.
Когда дерматомиозит затрагивает мышцы, это становится первым звоночком, говорящем о возможности перехода патологического процесса на внутренние органы, в частности на сердце. Могут появиться следующие болезни сердца:
- Перикардит, при котором серозная оболочка вокруг сердца попадает под воспалительный процесс.
- Миокардит, характерный воспалением сердечной мышцы.
- Эндокардит. Внутренняя оболочка сердца воспаляется.
- Перебои в работе сердечно-сосудистой системы, одышка, отеки, нарушенное сердцебиение.
Данные симптомы служат основным показателем при постановке правильного диагноза.
Суставной синдром при дерматомиозите
Суставной синдром при сильном дерматомиозите встречается не часто, однако имеет место быть. Деформация суставной сумки может возникнуть вследствие отсутствия лечения или факторов, осложняющих течение болезни. В остальных случаях область поражения приходится только на мелкие суставы:
- кисти,
- лучезапястные сочленения,
- голеностопные,
- плечевые,
- локтевые,
- коленные.
При суставном синдроме возможно покраснение кожных покровов, боль и отек, локализованные очагом поражения. В редких случаях наблюдается отложение кальцификатов. При сильном поражении, наблюдается развитие анкилоза – невозможность движения суставов.
Если не предпринять лечебные меры, вскоре наступит ограничение подвижности.
Прогноз и профилактика
В большинстве случаев наблюдается положительная динамика после прохождения курса лечения. Реабилитационные мероприятия предполагают постепенную адаптацию к физической нагрузке, лечебная гимнастика обязательна.
При отсутствии грамотного лечения осложнений не избежать. Заболевание со временем будет только прогрессировать, мышцы станут слабее, что неизбежно приводит к инвалидному креслу. В крайне запущенных случаях возможен летальный исход.
- Природа заболевания фибромиозита
- Перечень симптомов при шейном миозите
- Курс терапии при миозите грудной клетки
Остановка патологического процесса происходит за счет длительного приема глюкокортикоидных гормонов, они эффективно справляются с поставленной задачей, но провоцируют развитие диабета и снижение массы кости. Человек набирает лишний вес и страдает повышением артериального давления. Избежать подобных осложнений можно придерживаясь диеты, ограничивающей углеводы, но при этом, обогащенной кальцием и витамином D.
Общие профилактические меры дерматомиозита включают:
- своевременное лечение инфекционных заболеваний,
- адекватное распределение нагрузок,
- избегание попадания прямых солнечных лучей,
- сокращение стрессовых ситуаций.
Своевременное обращение к врачу и грамотная постановка лечебных процедур – гарант возможности восстановления функциональности мышц и суставов. Пренебрежение мер профилактики и игнорирование симптомов, наоборот, приводит к плачевным последствиям.
Читайте также:


