Артрит энцефалит коз противоэпизоотические мероприятия
Артрит-энцефалит коз (англ. — Caprine arthritis/encephalitis; лейкоэн-цефаломиелит-артрит коз, АЭК) — медленно прогрессирующая болезнь коз, характеризующаяся развитием демиелинизирующего энцефалита, прогрессирующего артирита, интерстициальной пневмонии и гибелью животных.
Историческая справка, распространение, степень опасности и ущерб.АЭК как лейкоэнце-фалит впервые был описан в 1974 г., в ранних сообщениях болезнь была представлена как мэди, или прогрессирующая пневмония коз, по аналогии с болезнью овец, но в последующие годы возбудитель был охарактеризован подробнее. АЭК обнаружен во многих странах, в частности европейских. На территории России болезнь официально не зарегистрирована. Предполагается, что широта распространения и степень инфицирования высокие.
Возбудитель болезни. Возбудитель АЭК — ДНК-РНК-содержащий медленный вирус (Lentivirus) семейства Retroviridae, диаметром Ю0. 120нм, со свойствами, характерными для ретровирусов, в частности вируса вис-ны-мэди овец (содержит РНК-зависимую ДНК-полимеразу). Структурные белки вируса АЭК также очень похожи на белки вируса висна-мэди овец. Однако установлено, что вирусы АЭК и висна-мэди различаются по критерию гомологичности нуклеотидных последовательностей генома и являются двумя различными представителями семейства ретровирусов.
Возбудитель выращивают в некоторых культурах тканей (в частности, синовиальной ткани) коз и овец. Размножение вируса происходит параллельно с образованием синцитиев, но литического ЦПД не наблюдают. Патогенный спектр ограничивается козами.
Эпизоотология. Сведения об эпизоотологии АЭК неполные. Серологические исследования свидетельствуют о широком распространении инфекции. Болезнь поражает козлят в возрасте 1. 5 мес. Эпизоотологичес-
360кие наблюдения позволяют предположить, что козлята заражаются внутриутробно или сразу же после рождения. Клинически болезнь проявляется только у 20 % всех инфицированных животных, у остальных протекает преимущественно бессимптомно. Естественная передача вируса АЭК происходит с молоком инфицированных матерей. Вероятно, возбудитель может переноситься с другими секретами или трансплацентарно.
Вирус АЭК обнаружен в молоке и молозиве инфицированных коз. В экспериментальных условиях вирусом могут быть инфицированы ягнята, у которых он вызывает артриты и продукцию вирусспецифических антител.
Патогенез.После интрацеребрального, интраартикулярного или интраперитонеального заражения развиваются разного рода изменения. Через 1 нед появляются первые воспалительные повреждения в головном мозге, суставах и легких, которые сохраняются в течение 8. 21 мес независимо от возраста животных. В лейкоцитах периферической крови жизнеспособный вирус обнаруживается начиная со 2-й недели после заражения в течение всей жизни животного.
Течение и клиническое проявление.Заболевание наблюдается у козлят в возрасте 1. 5мес. В целом заболевание характеризуется неврологическими изменениями с лейкоэнцефалитом, интерстициальной пневмонией и артритом.
Клинические симптомы развиваются очень медленно. Заболевание проявляется атаксией, гиперестезией, иногда лихорадкой, прогрессирующими парезами конечностей, перерастающими в параличи. Процесс чаще начинается с задних конечностей и распространяется на передние. Кроме того, отмечают хромоту вследствие развития артрита и одышку. У заболевших животных свалявшаяся шерсть, они отстают в росте. Аппетит не нарушен. Иногда наступает атрофия мускулатуры на парализованной конечности. Присоединяются явления пневмонии. Животные больше не могут стоять и погибают в положении лежа.
У взрослых коз чаще развивается артрит, особенно на карпальных суставах, в то время как у 2. 4-месячных козлят болезнь проявляется прежде всего лейкоэнцефаломиелитами. Течение АЭК — несколько недель, исход летальный.
Картина крови, как правило, без изменений, иногда может наблюдаться лимфопения. В цереброспинальной жидкости отмечают плеоци-тоз, в основном за счет мононуклеарных клеток, и увеличение содержания белка.
Патологоанатомические признаки.Патологоанатомические изменения локализуются в центральной нервной системе, суставах и легких.
Гистологически доминирует демиелинезирующий энцефалит с очаговыми скоплениями лимфоцитов и макрофагов в малом мозге. Вместе с тем наблюдаются очаговые некрозы. Изменения выражены в белом веществе головного и спинного мозга и мозжечка. Наиболее выраженные поражения чаще обнаруживают в шейных и грудных отделах спинного мозга. Микроскопически они характеризуются образованием плотных пери-васкулярных муфт из мононуклеарных клеток, формированием лимфоци-тарных инфильтратов, пролиферацией глии и выраженной первичной демиелинизацией. В тяжелых случаях участки нервных клеток замещаются глиальными рубцами.
Поражения суставов характеризуются артритами с синовиальной гиперплазией. При прогрессировании болезни нарастают дегенеративные
361изменения, такие, как фиброз, некроз и минерализация синовиальных оболочек, появляются периартикулярные коллагенозные структуры.
В легких отмечают диффузную интерстициальную пневмонию, как при мэди.
Диагностика и дифференциальная диагностика.Диагноз устанавливают на основании клинико-эпизоотологических данных и результатов патоло-гогистологических, вирусологических (культивирование возбудителя на культурах тканей и типизация в РДП, ИФА) и серологических (РИД, ИФА, РН) исследований.
При дифференциальной диагностике необходимо исключить инфекционные болезни: висна-мэди, скрепи, листериоз, по-лиоэнцефаломаляцию, токсоплазмоз, болезнь Борна; другие заболевания мышечной и скелетной систем (недостаток витамина Е, септические артриты и травмы, недостаток меди).
Иммунитет, специфическая профилактика.После заражения у инфицированных животных образуются сывороточные антитела, которые, однако, защиты не создают. Средства специфической профилактики АЭК не разработаны.
Профилактика.Проводят комплекс профилактических, ветеринарно-санитарных мероприятий, таких же, как при других медленных инфекциях овец и коз.
Лечение.Неэффективно.
Меры борьбы.Меры борьбы сводятся к проведению в неблагополучном хозяйстве ветеринарно-санитарных мероприятий, выявлению и выбраковке больных и серопозитивных животных.
Применяют метод изолированного выращивания козлят путем разделения матерей и козлят сразу же после окота; скармливание молозива только после прогревания в течение 60 мин при 56 °С или скармливание молока свободных от вируса коз или пастеризованного молока коз или коров.
Проводят серологический контроль выращенных таким образом коз на наличие антител к вирусу АЭК в РДП или РИД с 6-месячным интервалом и удаление всех серопозитивных животных.
При получении двух отрицательных результатов с 6-месячным интервалом животные считаются свободными от АЭК-вируса. Хозяйство считается оздоровленным, если в нем не выявлено ни одного положительно реагирующего животного.
Контрольные вопросы и задания.1. Охарактеризуйте основные клинические признаки симтомокомплекса мэди и аденоматоза у овец. 2. В чем заключаются основные паталого-анатомические различия при мэди и аденоматозе овец? 3. Какой основной метод лабораторной диагностики висна-мэди? 4. Чем заканчиваются заболевания овец медленными вирусными инфекциями?
ЧУМА СВИНЕЙ
Чума свиней (лат. — Pestis suum; англ. — Swine fever, Hog cholera; классическая чума свиней) — высококонтагиозная болезнь, характеризующаяся при остром течении лихорадкой, септицемией и геморрагическим диатезом, а при подостром или хроническом течении — крупозной пневмонией и крупозно-дифтеритическим воспалением слизистой оболочки толстого отдела кишечника (см. цв. вклейку).
Историческая справка, распространение, степень опасности и ущерб.Болезнь впервые описана в Северной Америке в 1833 г. В 60-х годах XIX в. она распространилась в большин-
362стве стран Европы, и до 50-х годов XX в. ее регистрировали во многих странах мира. В Россию вирус чумы занесен в 1893 г. из Западной Европы. Вирусную природу болезни установили в 1903 г. американские исследователи Швейниц и Дорсет. В 1908 г. впервые была предложена противочумная гипериммунная сыворотка, с 1936—1939 гг. началось производство вакцин (США, СССР и другие страны).
В настоящее время болезнь встречается более чем в 60 странах на всех континентах (за исключением США, Канады, Австралии, Скандинавских стран). Более других от этой инфекции страдают страны Европы, Азии, Южной и Центральной Америки, где хорошо развито свиноводство. В России в конце XX в. в результате проведения систематических про-тивоэпизоотических мероприятий с применением вакцин ареал распространения заболевания сократился, болезнь отмечается в виде энзоотических вспышек, число неблагополучных пунктов снизилось до единичных. За последние годы чума свиней интенсивно изучалась, предложены вакцины, разработаны средства и методы диагностики, однако предпринимаемые попытки полностью ликвидировать болезнь успеха пока не имеют.
За рубежом считается аксиомой, что страны, в которых продолжается вакцинация свиней против классической чумы свиней, да еще и живыми вакцинами, нельзя считать полностью свободными от возбудителя этой болезни.
Классическая чума свиней (КЧС) относится к списку А особо опасных инфекций и наносит большой экономический ущерб свиноводству как в развивающихся, так и в развитых странах с хорошо организованным ветеринарно-санитарным надзором.
Возбудитель болезни.Возбудитель чумы свиней — довольно мелкий (40. 60нм) РНК-содержащий вирус из рода Pestivirus , семейства Flaviviridae. По степени вирулентности различают А-, В- и С-варианты вируса. В вариант А входят вирулентные эпизоотические штаммы, вызывающие у свиней всех возрастов остро протекающую болезнь. Вирусы варианта В вирулентны только для поросят и вызывают атипичную или хроническую чуму. К варианту С относится американский слабовирулентный штамм. По антигенной структуре вирус однороден и не имеет ни серологических, ни иммунологических вариантов, но обладает антигенным родством с вирусом диареи крупного рогатого скота. В организме инфицированных или вакцинированных живыми вирус-вакцинами свиней вырабатываются специфические антитела.
Вирус патогенен только для домашних свиней и диких кабанов. Животные других видов, в том числе лабораторные, а также человек нечувствительны к заражению. В организме свиней вирус пантропен — накапливается во всех органах и тканях, но преимущественно в лимфатических узлах, костном мозге, селезенке, печени, слизистой оболочке кишечника и эндотелии кровеносных сосудов. Вирус размножается в гомологичных (свиньи) и гетерологичных (крупный рогатый скот, овцы, козы) первичных культурах клеток без ЦПД.
По устойчивости к химическим дезинфицирующим средствам вирус чумы относится к устойчивым (вторая группа). В свинарниках не теряет вирулентности до 1 года, в замороженном мясе — более 4 лет, в свежеох-лажденном мясе —45. 71 день, в солонине — более бмес, в копченостях — 3 мес. Прогревание мясных продуктов при 44 °С инактивирует вирус через 4 ч. В навозе и трупах возбудитель погибает через 3. 5 дней, в почве —через 1. 2 нед. Вирус неустойчив к высоким температурам, при кипячении погибает моментально, при 60 "С — за 10 мин, быстро инакти-вируется под действием ультрафиолетового облучения. Для дезинфекции наиболее эффективны растворы: гидроксида натрия 4%-ный, формалина 2%-ный, хлорной извести 3%-ный, хлорида йода 5%-ный, пероксида водорода 4%-ный, йодеза 1%-ный, виркона С 1: 350 и др.
Эпизоотология.Важнейшие эпизоотологические данные о чуме представлены на рисунке 5.5.
В благополучные хозяйства возбудитель заносится чаще с необеззара-женными пищевыми и боенскими отходами, с транспортом и с животны-
363 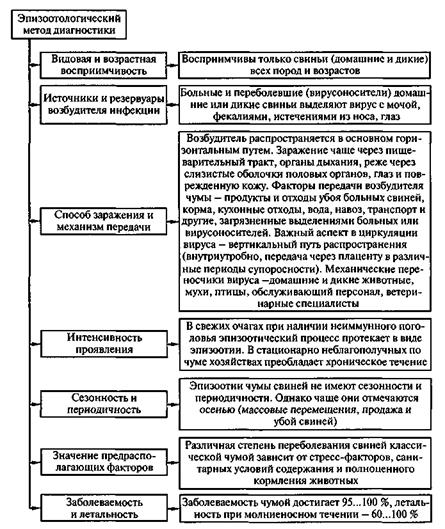
Рис. 5.5. Эпизоотологическая характеристика классической чумы свиней
ми-вирусоносителями. Возможен занос вируса с грубыми и сочными кормами, загрязненными выделениями больных диких свиней, а также комарами.
Природная очаговость болезни связана с территориями обитания инфицированных диких кабанов. Слабовирулентные вирусы варианта В вызывают атипичную форму, отличающуюся по клиническим признакам и сопровождающуюся низкой летальностью.
Патогенез.Вирус, попав в организм свиньи, репродуцируется в лимфоидно-ретикуляр-ной ткани входных ворот (миндалины и носоглотка). Через 16. 24ч он проникает в регионарные лимфатические узлы, репродуцируется и накапливается преимущественно в органах, богатых лимфоидно-ретикулярными клетками (селезенка, лимфатические узлы, костный мозг, печень и эндотелий кровеносных сосудов), вызывая дистрофические и некротические изменения. В результате этого повышается проницаемость стенок сосудов, что приводит к возникновению кровоизлияний, отеков и воспалительных процессов в различ-
364ных тканях и органах, а в селезенке — к инфарктам. Вирусемия сопровождается лихорадкой, нарушением обмена веществ. В результате поражения кроветворных органов развиваются анемия и лейкопения, сильное угнетение опсоно-фагоцитарной реакции и резкое снижение бактерицидности сыворотки крови. Размножаясь в клетках иммунной системы и вызывая их разрушение, вирус заметно снижает иммунные силы организма, что способствует активизации условно-патогенных микроорганизмов, следствием чего становятся пневмония и крупозно-дифтеритический колит. Воспалительные процессы в мозговой ткани обусловливают появление в ней инфильтратов, что клинически проявляется нервными явлениями (депрессия, возбуждение, припадки). При остром течении смерть наступает в результате морфологических поражений всех систем организма, особенно органов кроветворения и кровообращения.
Течение и клиническое проявление.Инкубационный период в зависимости от вирулентности вируса, дозы, метода заражения и резистентности животного длится 3. 9 дней, реже 12. 20 дней.
Болезнь может протекать сверхостро, остро, под остро и хронически.
Сверхострое течение наблюдают в основном в популяции неиммунных свиней и у молодняка. Отмечают повышение температурь: тела (41. 42 °С), угнетенное состояние. У больных отсутствует аппетит, возникают рвота, жажда, учащаются сердцебиение и дыхание, на коже появляются ярко-красные пятна. Животные погибают через 1. 2 дня.
Острое течение чаще регистрируют в начале эпизоотии. Основные признаки: лихорадка постоянного типа до 40,5. 41 °С, угнетение, отказ от корма. Развивается гнойный конъюнктивит, появляются рвота, запор, а затем диарея (фекалии иногда с примесью крови). Мочеиспускание затруднено. Одновременно с этим общее число лейкоцитов снижается с 8,5. 9,0тыс/мкл [(8,5. 9) 10 9 /л] до 2,5. 3,0тыс/мкл [(2,5. 3) 10 9 /л], увеличивается доля эозинофильных и базофильных гранулоцитов, число тромбоцитов уменьшается со 180. 300тыс/мкл (в норме) до ЮОтыс/мкл. Животные передвигаются с трудом, спина сгорблена, отмечаются парезы задних конечностей. Супоросные свиньи абортируют, часто возникает сли-зисто-гнойный ринит, а у отдельных животных — носовое кровотечение. На коже внутренней поверхностей бедер, живота, шеи и основания ушных раковин появляются пустулы, заполненные желтоватым экссудатом, а позже — точечные кровоизлияния, которые в дальнейшем сливаются и образуют темно-багровые пятна, не исчезающие при надавливании. В результате сердечной недостаточности кожа пятачка, ушных раковин, живота и конечностей приобретает синюшную окраску. Перед гибелью температура понижается до 35. 36 °С. Животные погибают в состоянии комы на 7. 10-й день.
Подострое течение длится до 3 нед и проявляется преимущественно поражением органов дыхания (грудная форма) или пищеварения (кишечная форма). Продолжительность болезни увеличивается до 10. 20 дней. У животных наблюдают затрудненное дыхание, кашель, слизисто-гнойное истечение из носа. При поражении желудочно-кишечного тракта запоры сменяются диареей со зловонным запахом и примесью слизи, а иногда крови. Свиньи худеют, ослабевают, передвигаются с трудом, и болезнь заканчивается гибелью, реже переходит в хроническое течение.
Хроническое течение продолжается до 2 мес и более. Клинические признаки могут сильно варьироваться в зависимости от осложнений секун-дарной инфекцией. Наблюдаются периодические диареи, лихорадка непостоянного типа, кашель. Животные имеют изнуренный и истощенный вид, на кожных покровах области живота, шеи и особенно ушных раковин и хвоста появляются экзематозные, иногда кровоточащие струпья грязного цвета, вследствие чего возможны случаи некроза ушей и хвоста.
365Свиньи приобретают вид заморышей, полностью не выздоравливают и остаются вирусоносителями. При подостром и хроническом течении летальность достигает 30. 60 %.
В последнее время под влиянием различных причин болезнь часто протекает атипично (более продолжительный инкубационный период, субклиническое переболевание взрослого свинопоголовья, а у поросят и подсвинков — развитие нервного синдрома без явного геморрагического диатеза).
Атипичная форма обычно проявляется у поросят-сосунов и отъемы-шей, имевших колостральный иммунитет или зараженных слабовирулентным вирусом варианта В. Для нее характерно подострое и хроническое течение продолжительностью 2. 3 нед и более. Болезнь характеризуется анорексией, конъюнктивитом, внутрикожными кровоизлияниями, гипертермией. Одни животные выздоравливают, а у других болезнь осложняется вторичной бактериальной инфекцией, заканчивающейся гибелью либо превращением в заморышей.
Обладая тератогенными свойствами, вирус, попавший в организм свиноматок в период 60. 70 дней супоросности, более чем у 30 % из них вызывает гибель плодов. У свиноматок, инфицированных на 94. 101-й день супоросности, гибели плодов не наблюдается. Аналогичными свойствами обладают и вакцинные вирусы, которые могут проникать в плоды свиноматок 60. 70 дней супоросности, репродуцироваться в них, вследствие чего после рождения поросята становятся толерантными к вирусу, их иммунная система не обеспечивает образование иммунитета после вакцинации. Эти поросята остаются восприимчивыми к полевым вирусам, и в случае его циркуляции возникают новые вспышки чумы.
Общие признаки классической чумы свиней при различных течениях болезни приведены в таблице 5.7.
[youtube.player]Артрит-энцефалит коз (англ. - Caprine arthritis/encephalitis, или CAE) является вирусным заболеванием, распространенным во многих странах мира. Многочисленные опыты подтверждают, что именно международная торговля является основным фактором распространения инфекции между различными регионами. Кроме того, CAE - это медленная инфекция, для которой характерно отсутствие сезонности и периодичности эпизоотии, географической принадлежности. Учитывая эпизоотологические особенности CAE, можно предположить вероятность большей распространенности этой болезни в зарубежных странах, чем это показывают данные МЭБ.
Чаще всего вирус встречается в районах интенсивного козоводства - Европе, Австралии, США. Только у 1-2% инфицированных животных болезнь влияет на ЦНС, в то же время у 30-40% коз определяют поражение суставов. Наибольшей группой риска являются козлята в возрасте 1-5 месяцев. Для нашей страны болезнь является экзотической и неизученной. По клиническим признакам вирус CAE похож на синдром Висна-Мэди у овец. В ранних сообщениях он был описан как Висна-Мэди: по аналогии с аденоматозом овец, артрит-энцефалит коз проявляется атаксией, гиперестезия, иногда лихорадкой, прогрессивными парезами конечностей, в свою очередь перерастают в паралич. Процесс чаще начинается с задних конечностей и распространяется на передние.
Передача вируса в стаде легко происходит путем выпаивания инфицированного молока козлятам - это основной способ распространения инфекции. Даже однократное введение CAEV-загрязненного молока или молозива козленку хватает для возникновения инфекции. У взрослых коз инфекция распространяется путем вдыхания респираторных секретов. Этот путь заражения требует длительного прямого контакта между животными. Аналогично было показано наличие CAEV в сперме инфицированных козлов, но половой путь инфицирования не подтверждался. Широкому распространению инфекции также способствует симптомокомплекс поражения ЦНС, суставов, легких. Картина крови обычно без изменений, иногда может наблюдаться лимфопения. В цереброспинальной жидкости отмечается плеоцитоз, в основном через мононуклеарные клетки и увеличение количества белка. Течение болезни - несколько недель, результат - летальный.

Фото 1. Клинические признаки САЭ у козы (увеличение путового сустава)
Клинические признаки проявляются у примерно 20% коз, инфицированных CAE вирусом (фото 1). Самым распространенным проявлением является артрит, который прежде всего наблюдается у взрослых коз, но может проявиться и у молодняка. У пораженных вирусом коз шерсть может поредеть, на более поздних стадиях заболевания наблюдается потеря веса и хроническое истощение.

Фото 2. Козленок в возрасте 2 месяца инфицированный вирусом (клинические признаки болезни не проявляются)
Патологоанатомические признаки
Патологоанатомические изменения локализуются в центральной нервной системе, суставах и легких. Наиболее выраженные поражения чаще выявляются в шейных и грудных участках спинного мозга. В суставах выявляется гиперплазия синовиальных клеток. В случае прогрессирования болезни нарастают дегенеративные изменения, такие как фиброз, некроз и минерализация синовиальных оболочек. В легких - интерстициальная пневмония, гиперплазия лимфоидной ткани.
Диагностика
Диагноз устанавливают на основании клинико-эпизоотологических данных и результатов патолого-гистологических, вирусологических (культивирование возбудителя на культурах тканей и типизация в РДП, ИФА) и серологических (РИД, ИФА, РН) исследований. На дифференциальной диагностике следует исключить инфекционные болезни: Висна-Мэди, скрепи, листериоз, полиоенцефаломаляцию, токсоплазмоз, болезнь Борна; другие заболевания мышечной и скелетной систем (недостаток витамина Е и меди, септические артриты и травмы).
Профилактика
После заражения у инфицированных животных образуются сывороточные антитела, которые не создают защиты. Средства специфической профилактики не разработаны. Меры борьбы сводятся к проведению в неблагополучном хозяйстве ветеринарно-санитарных мероприятий, выявления и выбраковка больных и серопозитивных животных. Несколько недавних исследований в Польше показали, что распространенность CAE среди поголовья коз колеблется от 4,2 до 80%, но в большинстве стад было около 30-40%. В одном из товарных польских хозяйств вообще все взрослые животные были больными.
Для сравнения - в Норвегии распространенность внутри стад колеблется от 11,5 до 97,3%. Исследование, проведенное в стадах молочных коз в Калифорнии, показало, что носителями вируса являются от 38,3 до 80,1%. Очевидно, распространенность внутри стада увеличивается пропорционально сроку, прошедшее с момента инфицирования. Поскольку вирус передается преимущественно через инфицированное молоко, эффективными мерами оздоровления стада является отлучение козлят сразу после рождения и выращивания их в строгой изоляции, скармливая молозиво здоровых коз или пастеризованное молоко, скармливание молозива только после прогрева в течение 60 мин при температуре +56 ° С. Проводят серологический контроль выращенных таким образом коз на наличие антител к вирусу САЭ в РДП или ИФА с 6-месячным интервалом. Хозяйство считается оздоровленным, если в нем не обнаружено ни одного положительного на вирус животного.
[youtube.player]Г.Д. СИДЕЛЬНИКОВ, Д.В. КОЛБАСОВ, А.Ю. ЧИЧИКИН, И.Ю. ВОЛКОВА, А.В. РЖАВИН
ВНИИВВиМ
Артрит-энцефалит коз (АЭК) - медленно протекающее вирусное заболевание, характеризующееся развитием демиелинизирующего энцефалита, прогрессирующего артрита, интерстициальной пневмонии, реже - маститов, оканчивающееся летально [3,4].
Болезнь распространена повсеместно, но чаще встречается в районах с интенсивным козоводством. Симптомокомплекс поражения трех систем органов (центральной нервной системы, суставов, легких) у коз описан во многих странах [2, 9], в том числе и в России [1]. При этом только у 1 -2 % инфицированных животных поражается центральная нервная система (в основном молодняка) и до 30 - 40 % (впоследствии) - суставы.
Существующие в настоящее время программы искоренения артрита-энцефалита коз за рубежом включают комплекс взаимосвязанных звеньев [7, 8, 10]: серологическое обследование импортируемых и продаваемых в другие хозяйства внутри страны коз, выявление скрытых вирусоносителей с использованием ПЦР-анализа, а также карантинирование и оздоровление неблагополучных по инфекции хозяйств. До появления молекулярно-биологических методов диагностики артрита-энцефалита коз основным инструментом для обнаружения больных животных было серологическое обследование восприимчивого поголовья такими способами, как реакция диффузионной преципитации в агаровом геле и иммуноферментный анализ в различных модификациях [5, 6].
В программах по контролю АЭК наряду с выявлением всех серопозитивных животных особое значение имеет обнаружение вирусоносителей - наиболее опасных источников инфекции. Создание и совершенствование высокочувствительных молекулярно-генетических методов значительно облегчают осуществление программ по искоренению болезни.
Цель наших исследований - разработать и провести мероприятия по оздоровлению хозяйства от артрита-энцефалита коз с применением ПЦР- анализа как сигнального метода диагностики.
Материалы и методы. Диагностические исследования провели в одном из козоводческих хозяйств Тверской области, а лабораторные - на базе ВНИИВВиМ, используя образцы крови от клинически больных и подозреваемых в заражении животных. Во время транспортировки пробы крови стабилизировали ЭДТА (Трилон-В). Кровь брали 4 раза: первый в марте 2003 г. у подозреваемых и клинически больных животных (п=7), а также у основных производителей (п=3); второй -в мае 2005 г. у всех особей, полученных от ранее исследованных производителей (п=104); третий - в июне 2006 г. (п=25); четвертый - в январе 2007 г. (п=25).
Провирусную ДНК в образцах крови животных выявляли ПЦР-анализом.
Последний обладает наиболее высокой чувствительностью и специфичностью, кроме этого в отечественной практике отсутствуют средства серологической диагностики. При проведении ПЦР-анализа препараты нуклеиновых кислот, выделенные из крови животных, гибридизировали праймерами, комплементарными последовательностям gag-гена вируса АЭК, фланкирующими ампликоны размером 392 и 173 п.о. соответственно. Пробы ДНК амплифицировали в 25 мкл реакционной смеси, содержащей: 20 pmoles каждого праймера; 200 мкМ смеси dNTP; 25 mM Tris HCI, рН 8,8; 60 mM KCI; 2,5 mM MgCI2; 7,5 мМ EDTA; 0,5% Tween 20; 0,01% желатины и 2 ед. Tag-полимеразы. Режим амплификации на термоцикле "Touchdown" фирмы Hybaid был следующим: денатурация 94 °С - 30 с, отжиг прай-меров 55 °С - 30 с, элонгация цепи 72 °С -30 с (35 циклов), финальная элонгация 72 °С - 3 мин. Результаты амплификации учитывали с помощью электрофореза в 2,0 %-ном агарозном геле.
Результаты исследований. В 1992 г. у коз, завезенных из госплемзавода "Никоновский" Раменского района Московской области, отметили первые признаки болезни - развитие хронических артритов, чаще карпальных суставов, хромоту, маститы с последующей индурацией вымени, агалактию. Различные схемы терапии животных ожидаемого эффекта не принесли. Коз выбраковывали в начальной стадии развития парезов конечностей и кахексии. Случаев выздоровления не зафиксировали. К моменту проведения работы (весна 2003 г.) в стаде насчитывалось: 60 дойных коз зааненской породы, 23 козы в возрасте 1 год, 1 козел англонубийской породы и 3 зааненской породы.
По результатам эпизоотологического анализа и клинического обследования животных поставили предварительный диагноз - артрит-энцефалит коз, а молекулярно-генетическими исследованиями проб крови методом ПЦР-анализа подтвердили его.
При выборочном анализе образцов (п=10) в марте 2003 г. провирусную ДНК выявили в крови 2 основных производителей и 1 взрослой козы. Массовое повторное исследование в мае 2005 г. показало, что уровень инфицированности поголовья составил 8,7 % (9 положительных проб из 104 исследованных).
Установив факт циркуляции возбудителя в хозяйстве, провели комплекс мероприятий, включающий карантинные и ветеринарно-санитарные меры. Были приостановлены хозяйственно-экономические связи с партнерами (купля - продажа животных, кормов, молока и сыра), оборудованы дезбарьерами въездные пути в хозяйство и помещения. Положительно реагирующих коз с клинической формой болезни немедленно изолировали из стада с последующим их убоем на специально оборудованной площадке. Туши выбракованных животных уничтожали сжиганием. Особей, в крови которых обнаруживали провирусную ДНК ВАЭК, в последующем также убивали. Исключение составляли лишь особо ценные в племенном отношении козематки, которых выбраковывали по мере получения от них последнего приплода.
Для предотвращения передачи возбудителя козлят, полученных от положительно реагирующих на ВАЭК маток, отнимали немедленно после рождения (до момента облизывания их и первого акта сосания) и в дальнейшем им выпаивали только обеззараженное козье молозиво, а также пастеризованное коровье молоко. Молозиво обеззараживали при 56 °С в течение 60 мин. Посуду регулярно автоклавировали при 120 °С в течение 30 мин.
Животноводческие помещения и производственные цеха дезинфицировали 3%-ным горячим раствором NaOH с последующей побелкой площадей, а кормушки и инвентарь на выгульных двориках и летних кормовых площадках - 3%-ным раствором формальдегида.
В животноводческих помещениях, кормоцехе, цехе готовой продукции и складах провели дератизацию, используя препарат аратам-к.
По результатам определения вирусоно-сительства среди коз (ПЦР-анализ) мы отслеживали движение инфицированных животных внутри стада (учитывая источники его пополнения), изучали гениалогическое древо козлов-производителей, коз маточного поголовья и их потомства. На основании этих данных выявили прямую наследственную связь всех АЭК-позитивных животных.
По мере проведения селективной (результаты ПЦР-анализа) выбраковки инфицированных особей контролировали "чистоту" получаемого приплода. В январе 2007 г. из 25 проб крови молодняка от положительно реагирующих родителей только 1 была положительной. Причиной этого послужило несоблюдение методики экстренного отъема новорожденных козлят от маток в момент их рождения.
Заключение. Результаты по оздоровлению хозяйства от артрита-энцефалита коз по рекомендуемой нами схеме позволяют считать ее эффективной при условии планомерного и полномасштабного выполнения этих мероприятий. При исходном уровне инфицированности поголовья коз в 2005 г. 8,7 % к 2007 г. процент положительно реагирующих животных был сведен до минимума, с полным отсутствием инцидентности болезни.
1. И.Ю. Волкова и др. //Ветеринария. 2007. № 1.
2. Caprine Arthritis/Encephalitis in Bosnia and Herzegovina. //OIE. FAO. HandiSTATUS , 20.04.2005.
3. Cork L.C. et al. // J. Infec. Dis. 1974, 129.
4. Crawford T.B. et al. // Science. 1980, 207.
5. Cutlip R. С et al.// Am. J. Vet. Res. 1977, 3.
6. Houwers D. J. et al. // Vet. Microbiol. 1982, 7.
7. Krieg A. et al.// Schweiz. Arch. Tierheilkd. 1990, 132.
8. Kuhn N. // Faculty of Veterinary Medicine, University of Bern, Bern, Switzerland. 1998.
9. Misako Konishi et al. //J. Vet. Med. Sci. 2004, 66(8). 10. Peterhans E. et al. // Vet. Res. 2004, 35.
[youtube.player]Читайте также:


