Атрофия мышц от преднизолона
Здравствуйте. Извините если что-то сделала не по правилам.
У меня была острая почечная недостаточность.Я принимала преднизолон полтора месяца в дозировке 6 таблеток в день (мой вес 45 кг). По окончании курса было резкое снижение преднизолона по таблетке в день. Закончила принимать в конце февраля этого года. Сейчас очень мучают постоянные отеки нижних век по утрам вплоть до обеда. Скажите пожалуйста, возможно ли избавиться от этого? Я так понимаю что произошло побочное действие - задержка натрия и воды в организме. Это лечится. Сил больше нет. Смотреть на себя не хочется! И второе побочное действие - атрофия тазобедренных мышц? Можно ли восстановить мышцы?
С уважением,
Елена.
Если бы вас догнали на вершине Эвереста и начали засовывать в рот преднизолон- был бы топик и была бы тема.
Но вас спасали от острой почечной недостаточности и на фоне преднизолона явления кушингоидизации с прибавкой массы тела и пр- законная плата за жизненно необходимое вмешательство
За время лечения вы не стали моложе и почки не стали лучше, но после отмены преднизолона может быть
Все что кгодно, кроме задержки жидкости из -за альдостерона или ренина
Надпочечники могли перестать работать- да, но выделять больше альдостерона никак не могли, ренин мог стать побоьше из - за поражения почек и вытащить за собой альдостерон- но никак не преднизолон
Во время приема преднизолона могло несколько увеличиться содержание жира в орбите - это да, но тут уж время и снижение потребления соли
Но ключевое и главное- почки сами по себе вполне очень даже водно - солевым обменом занимаются и дай им Бог выйти бес функциональных потерь
Приём белкового коктейля бессмысленная лишняя белковая нагрузка.
Чтобы мышцы выросли их надо тренировать, они восстановятся. Белковый коктейль + интенсивные тренировки - путь для бодибилдеров, которые идут на это ради спортивного результата и денег, жертвуя здоровьем.
Я сама зимой пару месяцев тренировок по болезни пропустила, так восстанавливалась месяца три - только тогда вернулась выносливость и заодно объём мышц, хотя я и не гонюсь за последним, просто велосипедист-любитель.
Мы тратим куда больше времени на рассеивание ваших ошибочных представлений , чем на дело
Но придется начать с азов : внутривенный преднизолон напрловину разрушаетмя после первого прохождения через печень, и роковая цифра 20 мг , столь тревожащая вас не имеет ни малейшего отношения к венному пз- но к принятому через рот и не менее 3-х месяцев
50 же мг венного пз - меньше чем ничто в долгосрочном плане , да и набрать то их трудно- в ампуле 30 мг
Ваш текст заставляет прежде всего думать о стрессорном расстройстве и нарушении цикла как следствии именно стресса и сверхценных идеях, вами сейчас владеющих
Смысл ведра ненужных анализов неясен, а нужные фсг и пролактин с ттг так и не приведены, равно как и непонятна линия планируемой беременности . Вы не замужем и вам 35 лет( поздий репродуктивный период начался) когда вы планируете приступить к реализации проблем с деторождением?
И , уж простите, прошлая история- болезни и пр
До преднизолона:
ЛГ - 6.45 (норма 1.9 - 12.5)
ФСГ - 7.01 (норма 2.5 - 10.2)
Эстрадиол - 299 (норма 40-606)
Пролактин - 194 (норма 56-619)
Прогестерон - 4.4 (норма 0.48 - 4.4)
После преднизолона спустя 1.5 месяца:
От 07.03.12.
ЛГ - 4.65 (норма 1.9 - 12.5)
ФСГ - 6.48 (норма 2.5 - 10.2)
Эстрадиол - 146 (норма 40-606)
Пролактин - 114 (норма 56-619)
Прогестерон - 0.639 (норма 0.48 - 4.4)
От 07.04.2012. Сдавала в другой лаборатории, поэтому показатели нормы другие:
ЛГ - 5.68 (норма 1.68-15)
ФСГ - 8.42 (норма 1.37 - 9.90) ( ФСГ повысился)
Эстрадиол - 39.9 (норма 20-160)
Пролактин - 13.4 (норма 1.9-29.2)
Прогестерон - 0.39 (норма 0.20 - 1.13)
Принимаю дюфастон с 16 по 25 день цикла. Сейчас 4 месяц приема.
Результаты узи малого таза:
В овуляторную фазу - узи без паталогии, все в норме. В яичниках мелкие фолликулы. Размеры матки и яичников в норме. Единственное толщина эндометрия очень низкая ( 2-3 мм, не соответствует фазе цикла). На 21-23 день (на дюфастоне) толщина эндометрия немного повышается 7-8 мм). УЗИ без паталогии. Овуляция есть.
Беспокоит, что как я поняла при отмене дюфастона месячных не будет. Эндометрий слишком маленький, не нарастает. Прогестерон очень снизился.
- Свежие записи
- Архив
- Друзья
- Личное дело
- Избранное
Т. М. Уэлш: Полимиозит
А. Общие сведения
1. Полимиозит - воспалительное аутоиммунное заболевание мышц, проявляющееся слабостью и утомляемостью. Течение вариабельно, наблюдаются обострения и ремиссии, которые могут возникать под влиянием терапии или спонтанно. К неблагоприятным прогностическим признакам относятся наличие онкологического заболевания, вовлечение сердечной мышцы, пожилой возраст, позднее начало лечения. При полимиозите страдают и внутренние органы. Часто возникает интерстициальное поражение легких.
2. Клиническая картина вариабельна, однако наиболее характерна слабость проксимальных мышц. При наблюдающемся иногда остром течении за несколько недель может развиться полная обездвиженность. В части случаев отмечается подострое течение, при котором слабость нарастает в течение нескольких месяцев. Лицевые мышцы обычно не страдают, а мышечные атрофии развиваются лишь на поздней стадии. При поражении глоточной мускулатуры появляется дисфагия, но речь обычно остается нормальной. Часто вовлекаются задние шейные мышцы. Иногда появляются эритематозные высыпания на тыле кистей, проксимальных фалангах пальцев, в области коленных и локтевых суставов, а также характерный периорбитальный отек с эритемой. У некоторых развивается склеродактилия. Полимиозит с кожными проявлениями называют дерматомиозитом (лечение такое же, как при полимиозите). Сердце поражается в 30% случаев. При остром начале может возникать миоглобинурия.
Б. Диагностика
1. Активность мышечных ферментов ( КФК , аминотрансфераз, фруктозодифосфатальдолазы) обычно повышена, хотя иногда бывает нормальной.
2. СОЭ не коррелирует с активностью заболевания.
3. На ЭМГ выявляются неспецифические изменения, характерные для первичного поражения мышц (короткие низкоамплитудные полифазные потенциалы действия двигательных единиц). Однако нередко регистрируются также положительные острые волны, потенциалы фибрилляций и повторные высокочастотные разряды.
4. При биопсии мышц в 85-90% случаев обнаруживают воспалительные инфильтраты и некроз мышечных волокон. Часто для того, чтобы подтвердить диагноз, приходится проводить повторную биопсию.
5. Дифференциальный диагноз обычно несложен, но требует применения вышеуказанных методов (включая биопсию). Полимиозит дифференцируют с пароксизмальной миоглобинурией, трихинеллезом, ревматической полимиалгией, врожденными миопатиями, тиреотоксической или другими эндокринными миопатиями, диабетической амиотрофией.
6. Связь со злокачественными новообразованиями. Полимиозит традиционно считался спутником скрыто протекающих онкологических заболеваний, однако последние исследования показывают, что это далеко не всегда так. Тем не менее частота злокачественных новообразований у больных с истинным полимиозитом (который следует отличать от мышечных атрофий при раковой кахексии) достигает 20%; она выше при дерматомиозите и при денервационных изменениях на ЭМГ .
1. Кортикостероиды
а. Кортикостероиды, несомненно, оказывают благоприятное действие при полимиозите, хотя контролируемые испытания не проводились. Кортикостероиды не уменьшают смертность, но способствуют более быстрому наступлению ремиссии и уменьшают выраженность осложнений. Часто их сочетают с метотрексатом или азатиоприном.
б. Особенно хороший эффект кортикостероиды оказывают в ранней стадии острого полимиозита; напротив, при хроническом полимиозите и мышечных атрофиях эффект может отсутствовать. Если при хроническом полимиозите лечение не приводит к улучшению в течение двух месяцев, переходят на иные средства (см. гл. 16, п. VII.В.2).
1) Начальная доза преднизолона обычно составляет 60-100 мг (ежедневно однократно утром). После улучшения дозу снижают до 40 мг и лечение проводят еще несколько месяцев.
2) Чтобы избежать рецидива, дозу снижают медленно - на 5-10 мг каждые 3-7 сут. По мере того как суточная доза уменьшается, эти 5-10 мг становятся все больше в процентном отношении, и поэтому интервалы между снижениями дозы должны увеличиваться. После того как доза станет равной двум третям от первоначальной, дальнейшее снижение прекращают на несколько месяцев. Через 6-12 мес большинство больных переводят на поддерживающую дозу (15-20 мг преднизолона однократно утром). При стабильной ремиссии можно перейти на прием через день (по 30-40 мг). При обострении приходится возвращаться к высоким дозам. Об эффективности лечения и о развитии рецидива можно судить по активности мышечных ферментов.
3) Попытку отменить кортикостероиды следует предпринять через 24 мес лечения, поскольку к этому времени активность заболевания часто снижается. В большинстве случаев достигается устойчивая 8-летняя ремиссия.
4) При активном полимиозите низкие дозы кортикостероидов не позволяют добиться ремиссии.
г. Стероидная миопатия, возникающая у больных с хроническим полимиозитом, осложняет лечение. Ее следует заподозрить при нарастании мышечной слабости, если нет увеличения активности мышечных ферментов и ухудшения на ЭМГ . Морфологическим признаком стероидной миопатии является преимущественная атрофия волокон 2 типа. Однако для подтверждения диагноза биопсии обычно не требуется - достаточно клинического улучшения при снижении дозы кортикостероидов. Дозу обычно снижают до поддерживающей под контролем активности мышечных ферментов. Если она повышается, а слабость нарастает, вновь переходят к высоким дозам. Стероидная миопатия чаще развивается у женщин, поэтому им по возможности назначают более низкие дозы.
д. Наблюдение. Активность мышечных ферментов ( АсАТ , КФК , фруктозодифосфатальдолазы и др.) обычно достаточно хорошо отражает активность патологического процесса, однако иногда активность всех или почти всех ферментов остается нормальной даже при обострении. С другой стороны, активность ферментов может снижаться за несколько недель до клинического улучшения и повышаться перед обострением.
2. Иммуносупрессивная терапия
а. Показания: хронический прогрессирующий полимиозит, неэффективность или непереносимость кортикостероидов.
б. Иммунодепрессанты применяют в сочетании с кортикостероидами (для уменьшения дозы последних) или самостоятельно.
1) Метотрексат
а) Дозы. При неэффективности кортикостероидов добавление метотрексата приводит к улучшению в 75% случаев. Препарат вводят в/ в течение 20-60 мин. При нормальной функции печени и почек начинают с 0,4 мг/кг, затем в течение 2-3 нед дозу увеличивают до 0,8 мг/кг.
б) Частота введения. Вначале препарат вводят еженедельно. При положительном эффекте переходят на введение через две, а затем через три недели. После достижения максимального улучшения препарат вводят один раз в месяц в течение 10-24 мес. По мере стихания активности дозу кортикостероидов снижают.
в) Побочные эффекты метотрексата проявляются стоматитом и другими расстройствами ЖКТ , которые обычно проходят при уменьшении дозы. Возможны поражение печени и лейкопения; в тяжелых случаях препарат приходится отменять.
2) Азатиоприн применяют внутрь в дозе 1,5-2 мг/кг самостоятельно или в сочетании с преднизолоном. При добавлении азатиоприна к преднизолону эффект может долго не наступать. Препарат назначают также на длительный срок при неэффективности или непереносимости преднизона. Дозу постепенно увеличивают, пока в крови не снизится количество лейкоцитов, после чего лечение продолжают в этой же дозе вплоть до достижения ремиссии. Основные побочные эффекты: угнетение кроветворения, анорексия, тошнота, рвота, желтуха.
3. Другие лечебные мероприятия
а. В острой стадии необходим постельный режим.
б. Добившись улучшения, сразу же начинают ЛФК , прежде всего упражнения на объем движений.
в. При длительной слабости используют корсеты и другие ортопедические приспособления.

Весь контент iLive проверяется медицинскими экспертами, чтобы обеспечить максимально возможную точность и соответствие фактам.
У нас есть строгие правила по выбору источников информации и мы ссылаемся только на авторитетные сайты, академические исследовательские институты и, по возможности, доказанные медицинские исследования. Обратите внимание, что цифры в скобках ([1], [2] и т. д.) являются интерактивными ссылками на такие исследования.
Если вы считаете, что какой-либо из наших материалов является неточным, устаревшим или иным образом сомнительным, выберите его и нажмите Ctrl + Enter.
Лечение воспалительных миопатий
Лечение и дерматомиозита, и полимиозита обычно начинают с кортикостероидов. Начальная доза преднизолона, назначаемого внутрь, варьирует от 30 до 100 мг/сут, однако предпочтительным считается более агрессивный подход, поскольку чем выше суммарная доза, тем более значительным будет клинический эффект в первые несколько месяцев лечения. Кроме того, чем раньше начато лечение, тем лучше может быть его результат. При позднем начале лечения его эффективность снижается. Суточную дозу преднизолона (80-100 мг, или 1 мг/кг) обычно принимают однократно утром ежедневно на протяжении 4-6 недель, пока не станет увеличиваться сила мышц и/или не начнет снижаться уровень КФК. Хотя сообщалось о том, что падение уровня КФК обычно предшествует увеличению мышечной силы, мы наблюдали ряд больных, у которых снижение активности КФК происходило через некоторое время после уменьшения мышечной слабости. Таким образом, при определении дозы кортикостероида можно ориентироваться на оба показателя, однако более надежным считается клиническая реакция, а не изменение того или иного лабораторного показателя.
При благоприятной реакции и отсутствии нежелательных побочных эффектов дозу преднизолона можно постепенно снижать на 20 мг каждые 3-4 недели, пока не будет достигнута (обычно через 4-6 месяцев) поддерживающая доза: 15-20 мг ежедневно или 30 мг через день. Последующее снижение дозы производят очень медленно - на 2,5 мг (при ежедневном приеме) или 5 мг (при приеме через день) каждые 4-6 недель при условии сохранения или усиления терапевтического эффекта. Для сохранения эффекта часто необходим прием поддерживающей дозы преднизолона 2 .
Циклоспорин, тормозящий активацию Т-клеток интерлейкином-2 или другие реакции, активирующие Т-клетки, действует, связываясь со специфическим иммунофилином и может вызывать нефротоксическое и гепатотоксическое действие, а также артериальную гипертензию. В нескольких исследованиях, проведенных на небольших группах больных с дерматомиозитом и полимиозитом, отмечен положительный эффект циклоспорина, однако высокая стоимость препарата и его потенциальные побочные действия ограничивают его применение. Лечение начинают с дозы 6 мг/кг/сут, в последующем ее снижают до 4 мг/кг/сут, чтобы снизить риск нефротоксического действия. Контроль концентрации препарата в сыворотке может сделать его применение более безопасным. Рекомендуемый уровень препарата в сыворотке - от 100 до 150 мкг/мл.
Теоретически плазмаферез может оказывать положительный эффект при воспалительных миопатиях, особенно при дерматомиозите, поскольку способен снижать уровень циркулирующих иммунных комплексов и иммуноглобулинов. Однако в двойном слепом плацебо-контролируемом исследовании у 39 больных с полимиозитом и дерматомиозитом, резистентных ккортикостероидам, не удалось показать эффективность плазмафереза.
Наиболее важная особенность, отличающая миозит с включениями от дерматомиозита и полимиозита, - низкая эффективность иммуносупрессивной терапии. В случаях полимиозита, резистентных к кортикостероицам, повторная биопсия часто выявляет морфологические признаки миозита с включениями. Тем не менее небольшой процент больных с миозитом с включениями положительно реагирует на кортикостероиды. Поэтому во всех случаях рекомендуется пробное 3-месячное лечение преднизолоном внутрь. В отсутствие эффекта показано назначение в/в иммуноглобулина. При двойном слепом плацебо-контролируемом исследовании у 19 больных с миозитом с включениями «функционально значимое улучшение отмечено в 6 (28%) случаях. Однако в лучшем случае эффект был умеренным, тем не менее исследование на небольшом числе больных могло не выявить в достаточной степени положительный эффект в/в иммуноглобулина при миозите с включениями. Необходимы дальнейшие исследования патогенеза этого заболевания и поиски его эффективного лечения.

[1], [2], [3], [4], [5], [6], [7], [8], [9], [10], [11], [12]
1. Основным препаратом для лечения полимиозита и дерматомиозита является преднизолон, применяемый в высоких дозах. Рекомендуемые дозы — 1,0—1,5 мг/кг/суг. за один прием, до завтрака, в течение 3—4 недель. Общая доза не должна превышать 100 мг. Применяется преднизолон до тех пор, пока не будет заметно несомненное улучшение мышечной силы. Тяжелым больным назначают высокие дозы метилпреднизолона внутривенно (250 мг 2 раза в сутки в течение 3-5 дней; вводить медленно в течение 2 часов, под контролем ЭКГ и уровня калия в крови). Затем дозу постепенно уменьшают в течение 10 недель на 1 мг/кг через день.
Если при этом не наступает ухудшение состояния, то далее дозу уменьшают на 5-10 мг каждые 3—4 недели, пока не будет подобрана минимальная доза препарата, контролирующая симптомы. Если мышечная слабость нарастает, не следует больше уменьшать дозу препарата. Показателем эффективности лечения служит нарастание мышечной силы в течение 3 месяцев. Некоторым больным может потребоваться лечение преднизолоном не менее года, а иногда и более. Хорошее самочувствие пациента и уменьшение уровня мышечных ферментов в крови без нарастания мышечной силы не являются основными критериями эффективности.
Если через 3 месяца после начала лечения преднизолоном нет положительной динамики мышечной силы, следует постепенно отменять препарат и начинать лечение другим иммуносупрессантом.
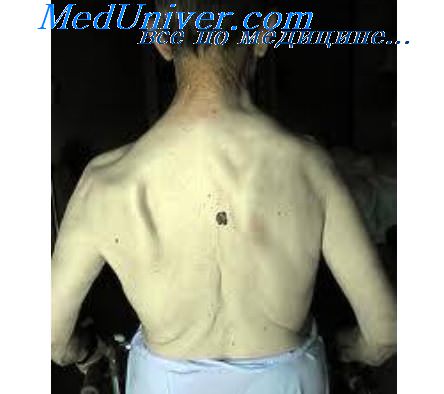
Крайне важно подробно проинформировать больного о возможных побочных эффектах длительного лечения преднизолоном для того, чтобы предотвратить их появление или бороться с ними. Пациентам следует ограничивать прием жидкости и поваренной соли. Для профилактики прибавки массы тела также необходимо ограничивать употребление углеводов, особенно сахара. Очень внимательно нужно следить за уровнем калия в крови, и при его недостатке необходима заместительная терапия. Следует контролировать уровень артериального давления, т. к. существует риск развития артериальной гипертензии. Наиболее опасными осложнениями лечения являются асептический некроз головки бедра, остеопороз и переломы костей.
Профилактика остеопороза заключается в дополнительном приеме глюконата или карбоната кальция (500—1000 мг/сут.) и кальцитриола (рокальтрола) (0,2—0,5 мкг/сут.). Кроме того, необходимы активные и пассивные физические нагрузки. Следует контролировать уровень кальция в крови. Нередко у больных отмечается метеоризм и прибавка массы тела. Для профилактики пептических язв желудка и двенадцатиперстной кишки рекомендуется принимать антациды и блокаторы гистаминовых рецепторов II типа. Периодически больные должны осматриваться окулистом для ранней диагностики катаракты и глаукомы. Среди других побочных эффектов отмечаются угревая сыпь, гирсутизм, лунообразное лицо, бессонница, головокружение, головные боли, изменения личности, плохое заживление ран, присоединение инфекции и сахарный диабет.
Применение преднизолона может привести к развитию стероидной миопатии — нарастанию мышечной слабости при нормальном уровне креатинкиназы. Дифференциальная диагностика прогрессирования полимиозита и развития стероидной миопатии представляет сложную задачу. Решение, касающееся увеличения или, наоборот, снижения дозы преднизолона, принимается только после внимательного изучения истории болезни пациента — динамики изменений мышечной силы, уровней креатинкиназы в крови и изменений режима приема препаратов за последние месяцы.
2. Азатиоприн назначается в тех случаях, когда стероиды не рекомендованы из-за наличия серьезных осложнений; когда неэффективны высокие дозы преднизолона или при быстром прогрессировании заболевания с развитием дыхательной недостаточности. Эффект от лечения азатиоприном может наступить только через 3—6 месяцев. Азатиоприн используется в сочетании с преднизолоном, при этом последний назначается в более низких дозах, чем при монотерапии. Это уменьшает вероятность развития побочных эффектов преднизолона. Азатиоприн назначается в дозе 2 мг/кг/сут. (до 3 мг/кг/сут.) в течение 4—6 месяцев. Начальная доза составляет около 50 мг/сут. Затем дозу постепенно наращивают.
Суточную дозу препарата следует делить на 2—3 приема и принимать во время еды.
К дозозависимым побочным эффектам относятся тошнота, рвота, сыпь и панкреатит. Дозозависимые побочные эффекты — угнетение функции костного мозга и гепатотоксический эффект. Больным, принимающим азатиоприн, еженедельно в течение первого месяца и затем один раз в месяц назначают клинический анализ крови и определение функциональных проб печени. Среди других побочных эффектов следует упомянуть анорексию, выпадение волос, вероятное онкогенное воздействие и тератогенный эффект. Строго противопоказан одновременный прием аллопуринола. Азатиоприн не применяется у детей.
3. Метотрексат в дозе 0,5—0,8 мг/кг/неделю внутримышечно рекомендован в тех случаях, когда азатиоприн неэффективен.
Аннотация научной статьи по клинической медицине, автор научной работы — Грознова Ольга Сергеевна, Шаховская Марина Сергеевна, Артемьева Светлана Брониславовна, Тренева Надежда Ивановна
Приводится статистический анализ проспективного исследования, проведенного в отделе патологии сердечно-сосудистой системы Московского НИИ педиатрии и детской хирургии в 1994-2011 г., в которое были включены 342 больных прогрессирующей мышечной дистрофией Дюшенна/Беккера . Установлено, что преднизолонотерапия в низких дозах дробным курсом у данной категории больных дает положительный эффект в виде увеличения продолжительности самостоятельной ходьбы.
Похожие темы научных работ по клинической медицине , автор научной работы — Грознова Ольга Сергеевна, Шаховская Марина Сергеевна, Артемьева Светлана Брониславовна, Тренева Надежда Ивановна
Efficiency of prednisolone therapy in patients with Duchenne/Becker progressive muscular dystrophy
The paper gives a statistical analysis of a prospective study conducted at the Department of Cardiovascular System Pathology, Moscow Research Institute of Pediatrics and Pediatric Surgery, in 1994 to 2011, which has enrolled 342 patients with Duchenne/Becker progressive muscular dystrophy . Split-course therapy with low-dose prednisolone in this category of patients has been found to exert a positive effect as longer walk unaided.
Эффективность терапии преднизолоном у больных прогрессирующей мышечной дистрофией Дюшенна/Беккера
О.С. Грознова, Н.И. Шаховская, С.Б. Артемьева, М.С. Тренева
Efficiency of prednisolone therapy in patients with Duchenne/Becker progressive muscular dystrophy
O.S. Groznova, N.I. Shakhovskaya, S.B. Artemyeva, M.S. Treneva
Московский НИИ педиатрии и детской хирургии; Московская областная психоневрологическая больница для детей с поражением ЦНС с нарушением психики
Приводится статистический анализ проспективного исследования, проведенного в отделе патологии сердечно-сосудистой системы Московского НИИ педиатрии и детской хирургии в 1994—2011 г., в которое были включены 342 больных прогрессирующей мышечной дистрофией Дюшенна/Беккера. Установлено, что преднизолонотерапия в низких дозах дробным курсом у данной категории больных дает положительный эффект в виде увеличения продолжительности самостоятельной ходьбы.
Ключевые слова: дети, прогрессирующая мышечная дистрофия Дюшенна/Беккера, кардиомиопатия, преднизолон, лечение.
The paper gives a statistical analysis of a prospective study conducted at the Department of Cardiovascular System Pathology, Moscow Research Institute of Pediatrics and Pediatric Surgery, in 1994 to 2011, which has enrolled 342 patients with Duchenne/Becker progressive muscular dystrophy. Split-course therapy with low-dose prednisolone in this category of patients has been found to exert a positive effect as longer walk unaided.
Key words: children, Duchenne/Becker progressive muscular dystrophy, cardiomyopathy, prednisolone, treatment.
Прогрессирующая мышечная дистрофия Дюшенна/Беккера — генетически детерминированное заболевание, основным клиническим проявлением которого служит нарастающая мышечная слабость. Это наиболее часто встречающаяся форма миодис-трофии у детей. Болезнь дебютирует в раннем детском возрасте. Потеря способности к самостоятельной ходьбе чаще всего происходит к 8—10 годам.
Интерес исследователей к кортикостероидной терапии больных прогрессирующей мышечной дистрофии Дюшенна/Беккера появился в 70-х годах прошлого века, когда были проведены первые клинические испытания эффективности преднизолона
Ros Vestn Perinatol Pediat 2011; 3:46-48
Адрес для корреспонденции: Грознова Ольга Сергеевна — к.м.н., ст.н.с. отделения патологии сердечно-сосудистой системы МНИИ педиатрии и детской хирургии
Тренева Марина Сергеевна — к.м.н., ст.н.с. отделения аллергологии и клинической иммунологии того же института 125412 Москва, ул. Талдомская, д. 2
Шаховская Надежда Ивановна — к.м.н. зам. гл. врача по лечебной работе Московской областной психоневрологической больницы для детей с поражением ЦНС с нарушением психики
Артемьева Светлана Брониславовна — к.м.н. зав. вторым психоневрологическим отделением той же больницы 127486 Москва, ул. Ивана Сусанина, д. 1
для коррекции мышечных расстройств у этих пациентов. Первоначально использовались высокие дозы преднизолона — до 5 мг/кг в сутки [1]. Эффект в виде увеличения мышечной силы был кратковременным и нестабильным, а побочные эффекты кортикосте-роидов значительно выражены. Практически сразу было предложено уменьшить дозу до 1,5—2 мг/кг в сутки, что привело к улучшению результатов лечения и пролонгированию эффекта [2]. В дальнейшем доза преднизолона претерпела дальнейшее снижение вплоть до 0,65 мг/кг и даже 0,35 мг/кг в сутки, при этом положительный эффект действия на мышечную силу сохранялся [3]. В настоящее время применение преднизолона у больных прогрессирующей мышечной дистрофией Дюшенна/Беккера рекомендуется большинством неврологов для коррекции мышечной слабости, однако этот вопрос, а также дозы и схема приема препарата остаются открытыми [4].
В 80-х годах ХХ века было обращено внимание на поражение сердечно-сосудистой системы у больных прогрессирующей мышечной дистрофией Дюшенна/Беккера. Это произошло после того, как на первое место в структуре смертности пациентов вышли кардиальные причины. В дальнейшем было доказано первичное поражение сердечной мышцы вследствие отсутствия белка дистрофина,
Грознова О.С. и соает. Эффективность терапии преднизолоном у больных прогрессирующей мышечной дистрофией.
приводящее к развитию кардиомиопатии у этих больных.
Среди схем с низкими дозами преднизолона наибольшее распространение получили схемы с дробным приемом (через день и т. п.). В основном рассматриваются дозы от 0,5 до 0,75 мг на 1 кг массы тела в сутки. Низкие дозы позволяют достичь более пролонгированного эффекта и избежать осложнений кортикостероидной терапии. В идеале необходимо для каждого пациента подбирать индивидуальную схему и дозу препарата, титруя ее по уровню активности ферментов цитолиза — креатинкиназы, ала-нинаминотрансферазы и аспартатаминотрансферазы (их активность должна снижаться при назначении препарата). Однако на практике в настоящее время добиться реализации такого подбора терапии весьма сложно.
характеристика детей и методы исследования
В проспективное исследование, проведенное в отделе патологии сердечно-сосудистой системы Московского НИИ педиатрии и детской хирургии в течение 17 лет (1994—2011), включены 342 больных прогрессирующей мышечной дистрофией Дюшен-на/Беккера. Критериями включения в исследование были: типичные клинические признаки мышечной дистрофии Дюшенна/Беккера, первично-мышечный характер поражения по результатам накожной и/или игольчатой электромиографии и повышение активности цитолитических ферментов крови (креа-тинкиназы, аланинамино-и аспартатаминотрансфе-разы).
Больные, у которых проводилась ДНК-диагностика и выявлена мутация гена дистрофина (n=68), составили анализируемую выборку детей с генетически подтвержденным диагнозом прогрессирующей мышечной дистрофии Дюшенна/Беккера. Длительность катамнести-ческого наблюдения составила от 5 до 17 лет. К 2011 г в анализируемой выборке 16 больных умерли, 38 — живы, но утратили способность к самостоятельной ходьбе, 14 — живы и способны к самостоятельной ходьбе.
Возраст наступления летального исхода в группе с преднизолонотерапией составил 21,10±2,13 года, в группе без лечения преднизолоном — 18,83±1,17 года. Сопоставление возрастов наступления смерти методом непараметрической статистики (Манна—Уитни и-тест) показало отсутствие достоверных различий (р=0,057). Однако полученные цифры позволяют предположить, что при большем объеме выборки различия могут быть достоверными.
Статистический анализ № 2 проводился среди самостоятельно ходящих детей 6—9 лет. Из анализируемой выборки были отобраны следующие группы: 1-я группа — 32 больных в возрасте от 6 до 9 лет, не утративших способность к самостоятельной ходьбе, получавших лечение кортикостероидами (пред-низолон в таблетках) в течение 24 мес. Преднизолон назначался по двум различным схемам: 17 больных принимали его в дозе 0,55 мг на 1 кг массы тела в сутки через день (3 мес — прием препарата, 3 мес — перерыв и так в течение 24 мес); 15 больных — в дозе 0,75 мг на 1 кг массы тела в сутки (каждое 1, 3, 5, 7, 9-е число месяца в течение 24 мес).
Во 2-ю группу вошли 14 самостоятельно ходящих больных в возрасте 6—9 лет, которые лечения корте-костероидами не получали.
Среди больных 1-й группы (п=32) к окончанию срока лечения ходили самостоятельно 26 детей, утратили способность к ходьбе 6 пациентов. Среди больных 2-й группы (п=14) на момент окончания срока наблюдения (24 мес) ходили самостоятельно 5 больных, утратили способность к ходьбе 9 больных.
Дети 1-й группы, получавшие в течение 2 лет терапию преднизолоном, к моменту прекращения лечения сохраняли самостоятельную способность ходить достоверно дольше, чем дети такого же возра-
ста 2-й группы без терапии преднизолоном (соответственно 0=0,81 С1 95% 0,68 . 0,95 и 02=0,36 С1 95% 0,11 . 0,61).
Статистический анализ № 3 проводился для изучения возраста потери способности к самостоятельной ходьбе (в группах живых и умерших). В группе живых к настоящему моменту детей, получавших преднизо-лон (п=16), возраст прекращения самостоятельной ходьбы составил 11, 11, 11, 12, 11, 11, 12, 11, 11, 12, 11, 9, 11, 10, 10, 11 лет. В группе не получавших предни-золон (п=22) возраст прекращения самостоятельной ходьбы составил 10, 8, 8, 8, 10, 8, 8, 9, 9, 8, 8, 9, 9, 9, 7, 7, 9, 7, 9, 10, 8, 8 лет.
Оценен возраст прекращения самостоятельной ходьбы у живых и умерших больных (п=54), которые были разделены на две группы: 1-я группа (п=28) никогда не получала лечение преднизолоном, 2-я группа (п=26) получала когда-либо терапию преднизолоном по какой-либо схеме. Выявлены достоверные различия (р=0,00000001386) возраста прекращения самостоятельной ходьбы, который в 1-й группе с преднизолонотерапией составил 10,46±1,07 года (среднее значение и страндартное отклонение по выборке) и был достоверно больше, чем во 2-й группе больных, — 8,39±0,96 года.
Статистический анализ № 4 оценивал частоту развития кардиомиопатии у больных в анализируемой выборке. Среди умерших больных относительная частота развития кардиомиопатии с сердечной недостаточностью как причина летального исхода составила: в группе умерших, получавших лечение преднизо-лоном (по какой-либо схеме в течение жизни), 0,40; в группе умерших, не получавших преднизолоноте-рапию, 0,67. Доверительные интервалы указанных
частот не были определены в связи с отсутствием условий для их подсчета вследствие малого объема этой выборки.
Среди больных, потерявших способность к самостоятельной ходьбе, относительная частота развития кардиомиопатии в группе получавших преднизолон составила 0,75 (0,54. 0,96), в группе не получавших преднизолонотерапию — 0,27 (0,09. 0,46). Тем самым достоверно чаще кардиомиопатия была выявлена в группе больных, получавших лечение преднизо-лоном. Пытаясь объяснить результаты проведенного анализа, мы сопоставили их с данными статистических анализов № 2 и № 3, где доказано, что больные с преднизолонотерапией достоверно дольше сохраняют способность к ходьбе. По нашему предположению, именно длительно персистирующая физическая нагрузка в виде самостоятельной ходьбы создает предпосылки для клинических проявлений кардио-миопатии у данной категории больных.
Возраст прекращения самостоятельной ходьбы умерших больных, получавших лечение преднизоло-ном, был достоверно больше по сравнению с не получавшими данный вид лечения детьми. Терапия пред-низолоном достоверно способствовала сохранению способности самостоятельной ходьбы на протяжении более длительного времени.
Таким образом, преднизолонотерапия в низких дозах дробным курсом у больных прогрессирующей мышечной дистрофией Дюшенна/Беккера дает положительный эффект в виде увеличения продолжительности периода самостоятельной ходьбы.
Читайте также:


