Бпвп при ревматоидном артрите расшифровка

Весь контент iLive проверяется медицинскими экспертами, чтобы обеспечить максимально возможную точность и соответствие фактам.
У нас есть строгие правила по выбору источников информации и мы ссылаемся только на авторитетные сайты, академические исследовательские институты и, по возможности, доказанные медицинские исследования. Обратите внимание, что цифры в скобках ([1], [2] и т. д.) являются интерактивными ссылками на такие исследования.
Если вы считаете, что какой-либо из наших материалов является неточным, устаревшим или иным образом сомнительным, выберите его и нажмите Ctrl + Enter.
Лечение ревматоидного артрита проводит ревматолог, поскольку функциональное состояние больных, находящихся под наблюдением врача, лучше, а применение современных методов фармакотерапии ревматоидного артрита требует специальных знаний. Необходимо информировать пациентов о характере заболевания, побочных эффектах применяемых лекарственных средств. При появлении соответствующих симптомов пациент должен немедленно прекратить приём препарата и обратиться к врачу.
При выборе лечения необходимо учитывать факторы риска неблагоприятного прогноза и продолжительность периода между появлением симптомов и началом приёма БПВП.
К факторам неблагоприятного прогноза, обусловливающим необходимость проведения более активного лечения, относят следующие:
- Серопозигивность по РФ и анти-ЦЦЛ антителам в дебюте болезни.
- Высокую воспалительную активность.
- Вовлечение в патологический процесс многих суставов.
- Развитие внесуставных проявлений.
- Увеличение СОЭ и уровня СРБ.
- Обнаружение определённых аллелей HLA DR (0101, 0401, 0404/0408, 1402).
- Обнаружение эрозий в суставах в дебюте болезни.
- Молодой или пожилой возраст начала болезни.
- Плохие социально-экономические условия жизни.
При продолжительности заболевания более 6 месяцев лечение должно быть более активным. При выявлении факторов риска неблагоприятного прогноза притри том выбора считают метотрексат (начальная доза 7,5 мг/нед) с быстрым (в течение примерно 3 мес) увеличением дозы до 20 25 мг/нед.
Эффективность лечения ревматоидного артрита оценивают, используя стандартизованные индексы, такие, как критерии улучшения Американской коллегии ревматологов, динамику индекса DAS28 (каждые 3 мес. рекомендации Европейской антиревматической лиги), функциональную способность пациента (HAQ) (каждые 6 мес), прогрессирование деструкции суставов по данным рентгенографии с с использованием методов Шарпа или Ларсена (каждый год).
В настоящее время эффективным считают лечение ревматоидного артрита, позволяющее достичь клинического улучшения не менее чем уровня ACR70 или ремиссии.
Дли того чтобы оценить улучшение по критериям Американской коллегии ревматологов, необходимо учесть следующее.
Количество болезненных суставов (выраженность синовита определяют путём подсчета количества болезненных и количества болезненных и припухших суставов).
АCR20, ACR50, ACR70 указывают на 20, 50 и 70% улучшение перечисленных, по крайней мере, пяти из семи показателей (улучшение первых двух считают обязательным).
Характеристика ремиссии при ревматоидном артрите
По критериям Американской коллегии ревматологов (клиническая ремиссия: сохранение пяти из шести следующих признаков в течение не менее 2 мес).
- Утренняя скованность менее 15 мин.
- Нет недомогания.
- Нет болей в суставах.
- Нет болей в суставах при движении.
- Нет припухлости суставов.
- СОЭ менее 50 мм/ч у женщин и 1000/мм3.
Хотя спленэктомия приводит к быстрой (в течение нескольких часов) коррекции гематолологических нарушений, в настоящее время её рекомендуют проводить только у пациентов, резистентных к стандартной терапии. Это связано с тем, что у четверти больных наблюдают рецидивирование гранулоцитопении, а у 26-60% пациентов рецидивирование инфекционных осложнений.
Проводить гемотрансфузию не рекомендуют за исключением случаев очень тяжелой анемии, ассоциированной с кардиоваскулярным риском. Эффективность эпоэтина бета (эритропоэтина) не доказана. Его рекомендуют применять только перед хирургическими операциями (при необходимости).
Лечение амилоидоза
Есть данные об определённой клинической эффективности циклофосфамида, хлорамбуцила, ГК и особенно инфликсимаба.
Лечение инфекционных осложнений
Для РА характерно увеличение риска развития инфекционных осложнений с локализацией в костях, суставах, дыхательной системе и мягких тканях. Кроме того, многие препараты, применяемые для лечения заболевания (НПВП, БПВП и особенно ГК), могут увеличивать риск развития инфекционных осложнений. Это диктует необходимость тщательного мониторинга и активного раннего лечения инфекционных осложнений.
Факторами риска развития инфекций при РА считают:
- пожилой возраст;
- внесуставные проявления;
- лейкопению;
- коморбидиые заболевания, включая хронические заболевания лёгких и сахарный диабет;
- лечение ГК.
Пациенты С РА очень подвержены развитию септического артрита. К особенностям септического артрита при РА можно отнести поражение нескольких суставов и типичное течение у больных , получающих глюкокортикостероиды.
Лечение кардиоваскулярных осложнений у пациентов с РА (включая недифференцированный артрит) выше риск развития кардиоваскулярных заболеваний (острого ИМ, инсульта), поэтому они должны пройти обследование для оценки риска возникновения данной патологии.
Лечение остеопороза
Остеопороз частое осложнение РА. Остеопороз может быть связан как с воспалительной активностью самого заболевания и нарушением физической активности, так и с лечением, в первую очередь ГК. Профилактику остеопороза необходимо проводить у следующих категорий пациентов:
- получающих ГК;
- с нетравматическими переломами костей скелета в анамнезе;
- старше 65 лет.
У пациентов, имеющих факторы риска развития остеопороза и получающих ГК, ежегодно необходимо проводить определение МПК.
Основными препаратами для профилактики и лечения остеопороза, в том числе глюкокортикоидного, считают бисфосфонаты. При непереносимости бисфосфонатов можно применять стронция ранелаг. Кальцитонин (по 200 ME/сут) показан при выраженных болях, связанных с компрессионными переломами позвонков Всем пациентам назначают комбинированную терапию препаратами кальция (по 1.5 мг/сут) и холекальциферола (витамина Д) (по 800 МЕ/сут).
Хирургическое лечение ревматоидного артрита
Хирургическое лечение ревматоидного артрита считают основным методом коррекции функциональных нарушений на поздней стадии болезни. Применение на ранней стадии РА в подавляющем большинстве случаев нецелесообразно ввиду широких возможностей лекарственной терапии. В развернутой стадии болезни необходимость применения хирургического лечения определяют индивидуально при установлении показаний.
- Сдавление нерва вследствие синовита или теносиновита.
- Угрожающий или совершившийся разрыв сухожилия.
- Атланто-аксиальный подвывих, сопровождающийся появлением неврологи ческой симптоматики.
- Деформации, затрудняющие выполнение простейших повседневных действий.
- Тяжёлые анкилозы или дислокации нижней челюсти.
- Возникновение бурситов, нарушающих работоспособность пациента, а также ревматических узелков, имеющих тенденцию к изъязвлению.
Относительные показания к операции.
- Резистентные к лекарственной терапии синовиты, теносиновиты или бурситы.
- Выраженные боли в суставах.
- Значительное ограничение движении в суставе.
- Тяжёлая деформация суставов.
Эндопротезирование - основной метод лечения при деформациях тазобедренного и коленного суставов, а также суставов пальцев кисти. Применяют также синовэктомию (в последнее время проводят преимущественно в мелких суставах) и теносиновэктомию. Артроскопическая синовэктомия получает всё большее распространение, однако и отдаленные результаты ещё не изучены. Выполняют резекции костей, артропластику (применяют в основном на суставах стол) Артродез может быть методом выбора при тяжелой деформации голеностопного первого плюснефалангового и лучезапястного суставов.
Что должен знать пациент о лечении ревматоидного артрита?
Ревматоидный артрит - аутоиммунное заболевание. Дли него характерно развитие эрозивного артрита и системное поражение внутренних органов. Симптомы обычно бывают стойкими и в отсутствие лечении неуклонно прогрессируют.
Медикаментозную терапию считают основным методом лечения РА. Это единственный способ, позволяющий затормозить развитие воспалительного процесса и сохранить подвижность в суставах. Другие методы лечения: физиотерапия, диета, ЛФК имеют вспомогательное значение и не способны оказать существенное влияние на течение болезни.
В основе лечения РА лежит применение БПВП. К ним относят большое число разнообразных по химической структуре и фармакологическим свойствам лекарственных средств, таких как метотрексат, лефлуномид, сульфасалазин и т.д. Их объединяет способность в большей или меньшей степени и за счёт различных механизмов подавлять воспаление и (или) патологическую активацию иммунной системы. Новым методом лечения РА считают применение так называемых биологических агентов. Биологические агенты (не путать с биологически активными добавками) - это белковые молекулы, избирательно воздействующие на отдельные вещества или группы клеток, участвующие в процессе хронического воспаления. К биологическим препаратам относят инфликсимаб, ритуксимаб, адалимумаб.
Ревматоидный артрит лечение обычно начинают с назначения метотрексата или лефлуномида. Биологические агенты (инфликсимаб, адалимумаб и ритуксимаб), как правило, добавляют к этим препаратам при недостаточной эффективности ионотерапии. Быстрый противовоспалительный эффект могут давать ГК. НПВП представляют собой важный компонент лечения РА, поскольку могут уменьшить боль и скованность в суставах. Наиболее часто применяют диклофенак, нимесулид, мелоксикам, кетопрофен, целекоксиб.
Ревматоидный артрит лечение лекарствами может давать очень хорошие результаты, но требует тщательного контроля. Контроль должен проводить квалифицированный специалист-ревматолог и сам пациент. Пациенту необходимо посещать врача не реже чем 1 раз в 3 мес в начале лечения. Помимо осмотра, назначают анализы крови, ежегодно проводят рентгенологическое исследование суставов для оценки течения заболевания. Следует помнить об ограничениях, связанных с лечением на фоне терапии метотрексатом и лефлуномидом не
Примерные сроки нетрудоспособности
Временная нетрудоспособность может наступать при РА с умеренной и высокой активностью и сохраняться на период развития клинического эффекта от медикаментозного лечения. Пациенты теряют трудоспособность и выходят на инвалидность из-на нарушения функций суставов в течение первых 5 лет болезни в 50% случаен. При длительности болезни более 15 лет инвалидами групп I и II признают 80% пациентов.
Раннее активное лечение ревматоидного артрита, включающее применение биологических агентов, позволяет существенно сократить сроки временной нетрудоспособности и количество инвалидизированных пациентов.

[33], [34], [35], [36], [37]
Прогноз
И конце XX в. в среднем около половины пациентов теряли трудоспособность в течение первых 10 лет, к 15-му году болезни примерно 80% пациентов становились инвалидами групп I и II. У больных РА наблюдали уменьшение продолжительности жизни по сравнению с общей популяцией на 5-10 лет. Самыми распространёнными причинами смерти были кардиоваскулярные заболевания (инсульт, острый инфаркт миокарда), возникновение которых связывают с интенсивным развитием атеросклероза и склонностью к тромбозам вследствие хронического иммунного воспаления. Нередко наблюдали летальные исходы по причине вторичного амилоидоза. сопутствующих инфекций (пневмонии, нагноения мягких тканей и др.).
Современное активное лечение, особенно н ранней стадии ревматоидного артрита, позволяет существенно улучшить результаты по сохранению трудоспособности, достичь клинической ремиссии у 40-50% пациентов, довести ожидаемую продолжительность жизни до популяционного уровня.

[38], [39], [40], [41], [42], [43], [44]
Комбинированная терапия БПВП
Применяют 3 основных варианта комбинированной терапии.
• Начинать лечение с монотерапии с последующим назначением одного или нескольких БПВП (в течение 8—12 нед) при сохранении активности процесса (step-up).
• Начинать лечение с комбинированной терапии с последующим переводом на монотерапию (через 3—12 мес) при подавлении активности процесса (step-down).
• Проведение комбинированной терапии в течение всего периода болезни.
Преимущества комбинированной терапии над монотерапией или определённой стратегии комбинированной терапии не доказаны.
• На ранних стадиях РА комбинированная терапия (в качестве одного из её компонентов обязательно применяется метотрексат) эффективнее монотерапии любым БПВП, но чаще развиваются побочные эффекты.
• Необходим более тщательный мониторинг токсических реакций, чем при проведении монотерапии.
• Считают, что у пациентов с тяжёлым течением РА лечение следует начинать с комбинированной терапии, а у пациентов с умеренной активностью - с монотерапии с последующим переводом на комбинированную терапию при недостаточной эффективности лечения.
Ведение пациентов с ревматоидным артритом на фоне беременности и кормления грудью
Анемии
Синдром фелти
Контролируемых исследований не проводилось.
• Основные ЛС — соли золота парентерально, при неэффективности - метотрексат; тактика применения такая же, как и при других формах РА.
• Монотерапия ГК (>30 мг/сут) приводит только к временной коррекции гранулоцитопении, которая рецидивирует после снижение дозы ГК.
• У пациентов с агранулоцитозом показано применение пульс-терапии ГК по обычной схеме.
• Увеличение числа гранулоцитов до 2,0x109/л и улучшение 2 из следующих параметров:
♦ Снижение частоты инфекционных осложнений (по крайней мере на 50%).
♦ Снижение частоты кожных язв (по крайней мере на 50%).
♦ Снижение частоты приступов лихорадки (по крайней мере на 50%).
• Увеличение числа гранулоцитов до 1,0-2,0х109/л и улучшение 2 из следующих параметров:
♦ Снижение частоты инфекционных осложнений на 25%.
♦ Снижение частоты кожных язв (по крайней мере на 25%).
♦ Снижение частоты приступов лихорадки (по крайней мере на 25%).
Лечение внесуставных (системных) проявлений ревматоидного артрита
Контролируемых исследований не проводилось.
Рекомендации по лечению экстраартикулярных проявлений РА:
• Перикардит или плеврит — ГК( 1 мг/кг) + БПВП.
• Интерстициальное заболевание лёгких — ГК (1 — 1,5 мг/кг) + циклоспорин А или циклофосфамид; избегать назначения метотрексата.
• Изолированный дигитальный артериит — симптоматическая сосудистая терапия.
• Системный ревматоидный васкулит - интермиттирующая пульс-терапия циклофосфамидом (5 мг/кг/сут) и метилпреднизолоном (1 г/сут) каждые 2 нед в течение 6 нед, с последующим удлинением интервала между введениями; поддерживающая терапия — азатиоприн; при наличии криоглобулинемии и тяжёлых проявлений васкулита целесообразно проведение плазмафереза.
• Кожный васкулит — метотрексат или азатиоприн.
Рекомендации по лечению пациентов с ревматоидным артритом
По современным стандартам лечение РА должно основываться на следующих основных принципах:
1. Основная цель — достижение полной (или хотя бы частичной) ремиссии.
2. Для достижения этой цели:
• лечение БПВП должно начинаться как можно раньше;
• лечение должно быть максимально активным с изменением (при необходимости) схемы лечения в течение 2 — 6 мес;
• при выборе терапии необходимо учитывать:
♦ факторы риска неблагоприятного прогноза, к которым относятся высокие титры РФ,
увеличение СОЭ и СРБ, быстрое развитие деструкции в суставах
♦ продолжительность периода между появлением симптомов и началом терапии БПВП: если он более 6 мес, терапия должна быть более активной;
• при наличии факторов риска средством выбора является метотрексат (начальная доза 7,5 мг/нед) с быстрым (в течение примерно 3 мес) увеличением дозы до 20-25 мг/нед;
• эффективность терапии следует оценивать с использованием стандартизованных клинических и рентгенологических критериев (см. Приложение).
Лечение ревматоидного артрита в стадии необратимых структурных повреждений (end-stage) суставов
Цели терапии • уменьшение боли • предохранение развития необратимых изменений в непоражённых суставах • поддержание функции суставов.
Глава 13. Базисные противовоспалительные препараты
НПВП и преднизолон не являются основными лекарствами для большинства болезней суставов (за исключением НПВП при болезни Бехтерева и гормонов для ревматической полимиалгии). Их нельзя использовать для постоянного и непрерывного лечения этих болезней.
Все базисные противовоспалительные препараты (БПВП) делятся на синтетические, которые синтезируются в химических лабораториях, и генно-инженерные биологические препараты (они же просто биологические), которые создаются при помощи современных клеточных технологий.
Что относят к синтетическим базисным противовоспалительным препаратам:
• Метотрексат. Современную ревматологию невозможно представить без метотрексата, это одно из самых важных лекарств для лечения ревматоидного артрита и некоторых разновидностей псориатического артрита.
Существует масса страшилок о том, что метотрексат – это онкологический препарат, который используют при химиотерапии, и что применение этого лекарства у людей без онкологии якобы приводит к плохим последствиям. Конечно, это раздутый миф.
В настоящее время десятки миллионов людей принимают метотрексат в связи с болезнями суставов. Его безопасность и эффективность не подвергаются сомнению. Не слушайте страшилки!
Онкологи же используют метотрексат в режиме капельниц с дозировками в десятки и даже сотни раз больше ревматологических, и, конечно, переносимость подобного лечения существенно отличается!
Метотрексат существует в разных формах, например в виде таблеток, которые пациенты должны принимать всего один раз в неделю, иногда для улучшения переносимости дозировка может быть разбита на 2 или даже 3 приема с интервалом в 12 часов (в таких ситуациях метотрексат принимается как бы 1,5 дня в неделю). Также сейчас можно купить метотрексат в виде подкожных или внутримышечных инъекций, подкожные инъекции предпочтительнее таблеток при высоких дозах метотрексата (выше 20 мг в неделю), поскольку не только лучше усваиваются организмом, но и в целом легче переносятся, хотя улучшение переносимости можно отметить не у всех пациентов!
Не пугайтесь и не удивляйтесь назначениям врача. Сейчас в ревматологии используют более высокие дозы метотрексата, чем 10 лет назад. Причем это относится и к началу лечения (старт происходит с 10 мг или даже 15 мг в неделю), и к целевым дозировкам препарата (20–30 мг в неделю).
Для улучшения переносимости метотрексата врачи почти всегда параллельно назначают фолиевую кислоту, которую нужно принимать ежедневно по 1–5 мг в сутки (иногда врачи рекомендуют не принимать фолиевую кислоту в день использования метотрексата), что позволяет уменьшить тошноту, дискомфорт в животе, ослабить влияние метотрексата на печень. К сожалению, приблизительно 20–30 % людей не могут продолжать прием этого препарата в связи с не очень хорошей переносимостью, и тогда требуется поиск альтернативного препарата.
• Лефлуномид (Арава, Элафра, Лефлайд). Этот препарат, как правило, представляет собой альтернативу метотрексату при плохой переносимости последнего. Назначают лефлуномид принимать каждый день в таблетках по 10–20 мг. Иногда для ускорения наступления эффекта врач может порекомендовать использовать нагрузочную дозировку – три дня по 100 мг, с последующим переходом на 20 мг в сутки. Как правило, лефлуномид переносится хорошо, из наиболее распространенных нежелательных эффектов следует выделить поносы и подъемы АД.
• Тофацитиниб (Яквинус). В настоящее время это самый новый синтетический препарат для лечения ревматоидного артрита. Как правило, тофацитиниб назначают при неэффективности или непереносимости метотрексата или биологических препаратов. Принимать его следует два раза в сутки по 5 мг, при необходимости дозировка может быть увеличена до 20 мг/сутки. В целом переносимость у препарата хорошая, однако на фоне его приема, так же как и при приеме метотрексата или лефлуномида, необходимо регулярно (раз в 4–8 недель) сдавать общий анализ крови и показатели ферментов печени (АСТ, АЛТ). К сожалению, тофацитиниб по своей стоимости существенно превосходит все остальные синтетические базисные противовоспалительные препараты.
При беременности ведущими ревматологическими организациями мира (России, США, Европы и Великобритании) разрешены для постоянного приема гидроксихлорохин и сульфасалазин. Метотрексат, лефлуномид и тофацитиниб нельзя использовать в течение всей беременности и во время кормления грудью!
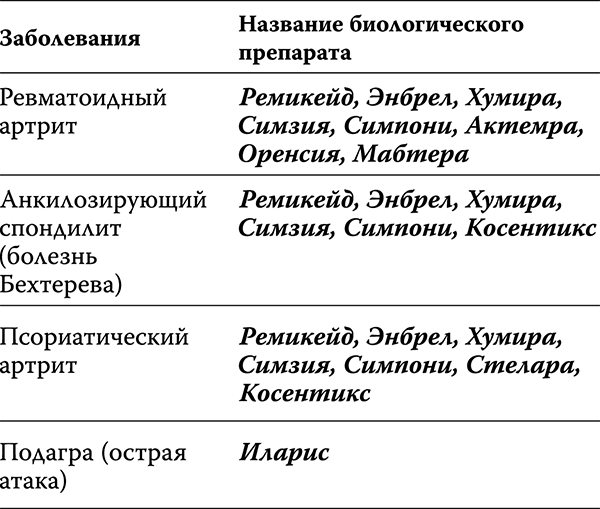
Биологические базисные противовоспалительные препараты – это быстрорастущая группа современных препаратов для борьбы с целым рядом ревматических заболеваний. Что нужно знать об этих лекарствах? Данные вещества представляют собой крупные белковые структуры, которые получают в процессе сложного и длительного производства. Именно в связи с необычно трудной технологией получения эти лекарства стоят так дорого. В настоящее время для лечения воспалительных болезней суставов используют следующие препараты (см. таблицу ниже).

Несмотря на свою хорошую эффективность и переносимость, биологические препараты имеют ряд возможных нежелательных эффектов. В первую очередь это касается увеличения риска инфекционных осложнений (в особенности в первые 6 месяцев лечения!), вот почему всем пациентам, которые находятся на биологической терапии, врачи настоятельно рекомендуют ежегодно вакцинироваться против гриппа (вне зависимости от сезона или эпидемии!), раз в пять лет – против пневмококковой инфекции (это возбудитель тяжелого воспаления легких), а также против гепатита В (если пациент им никогда не болел ранее и не вакцинировался). Также очень важно перед стартом биологической терапии исключить спящую туберкулезную инфекцию, для этого необходимо сделать рентген легких (а иногда и КТ легких!) и один из трех методов дополнительной диагностики на туберкулез: проба Манту, или диаскин-тест (эти исследования представляют собой кожные пробы), или квантиферон-туберкулезный тест (анализ крови).
Кроме диагностики туберкулеза нужно сдать анализы крови на ВИЧ, гепатит В, гепатит С, сифилис. Лечение биологическими лекарствами, как и синтетическими базисными противовоспалительными препаратами, длится годы, при этом в некоторых случаях врачи могут сочетать биологический и синтетический препарат, но никогда не назначают два биологических лекарства одновременно, так как это может привести к серьезным осложнениям в организме в виде угнетения иммунитета!
Возможность продолжения использования биологических лекарств во время беременности или кормления грудью мало изучена, однако в начале 2016 г. появились новые международные рекомендации по этому вопросу. Некоторые из биологических препаратов уже имеют неплохой мировой опыт безопасного применения при беременности, все зависит от конкретного препарата и срока беременности, поэтому для более точной информации проконсультируйтесь со своим лечащим врачом.

Начало 21 века прошло под знаком стремительного развития фармакологии, иммунологии и молекулярной биологии, что отразилось на принципах терапии многих аутоиммунных заболеваний. К аутоиммунным болезням относится и ревматоидный артрит, лечение которого всегда считалось одной из наиболее актуальных проблем научной медицины. Как изменились взгляды на фармакотерапию РА за последние 10 лет, какие новые препараты появились в распоряжении ревматологов? Обзору прогрессивных методов лечения РА мы посвящаем этот материал.
Современное лечение ревматоидного артрита: общие принципы
ГИБП целенаправленно воздействуют на молекулярные мишени, участвующие в аутоиммунном воспалении. Иными словами, современные методы лечения направлены на глубинные молекулярные механизмы иммунных реакций, которые лежат в основе патогенеза РА. Блокируя определенные звенья иммунного ответа, ГИБП останавливают лавину патологических изменений в пораженных суставах, купируют воспаление и препятствуют прогрессированию болезни. А теперь поговорим обо всем этом подробнее.
Ниже мы рассмотрим основные группы биологических препаратов для лечения ревматоидного артрита и раскроем тезисы, озвученные в небольшом вступлении.
1. Блокаторы ФНО-α
Ингибиторы фактора некроза опухоли являются теми лекарственными средствами, с которых началось современное лечение ревматоидного артрита. ФНО-α – это белок из семейства цитокинов, участвующий в миграции лимфоцитов и стимулирующий синтез медиаторов воспаления. Блокируя ФНО-α, мы можем остановить каскад аутоиммунного воспаления на одной из ранних стадий – выделение медиаторов воспаления (цитокины) клетками иммунной системы.
Одним из первых препаратов таргетной терапии ревматоидного артрита был Ремикейд (МНН Инфликсимаб). Применяется инфликсимаб, как правило, в комбинации с метотрексатом (препарат из группы БПВП), назначается при тяжелых и среднетяжелых формах РА и считается препаратом 1-й линии антицитокиновой терапии. Это значит, что если лечение преднизолоном ревматоидного артрита (и/или другими БПВП) недостаточно эффективно, доктора включают в схемы терапии инфликсимаб. Если же инфликсимаб на дает желаемого результата, ревматологи могут принять решение о переводе пациента на ингибиторы ФНО-α нового поколения (пример – этанерцепт, или Энбрел).
2. Блокаторы CD20 рецепторов В-лимфоцитов
Ранее считалось, что в патогенезе РА главную роль играют цитотоксические Т-лимфоциты, однако исследования, проведенные в начале 21 века, показали, что и значение В-звена иммунитета тоже достаточно велико. В клинических испытаниях, посвященных изучению роли ингибитора CD20 (ритуксимаб, или Мабтера) в схемах химиотерапии неходжкинских лимфом, был обнаружен позитивный ответ у пациентов с лейкозом, страдающих одновременно и ревматоидным артритом. Дальнейшее изучение свойств ингибитора CD20 подтвердило огромный потенциал лекарства при РА.
Масштабные клинические испытания (REFLEX и DANCER) препарата ритуксимаб доказали, что он достоверно замедляет прогрессирование РА, позволяет достичь стойкого ответа по критериям ACR, купирует болевой синдром, улучшает функциональное состояние суставов и повышает качество жизни. Отзывы пациентов, которые уже получают лечение этим уникальным лекарством (Мабтера разрешен в РФ с 2006 года), являются лишним доказательством его высокой эффективности.
3. Блокаторы CD80 и CD86 рецепторов Т-лимфоцитов
Активация Т-лимфоцитов – важнейшее звено патогенеза РА. Происходит эта активация при участии специфических рецепторов CD80 и CD86, расположенных на поверхности Т-лимфоцитов. Заблокировав эти клеточные маркеры, мы препятствуем активации Т-лимфоцитов цитокинами и тем самым останавливаем каскад патологических изменений в суставах. На эту мишень (CD80 и CD86) нацелено действие препарата абатацепт (Орсения), еще одного инновационного средства из группы ГИБП для лечения ревматоидного артрита. Как правило, абатацепт назначается в качестве второй линии терапии, то есть при отсутствии желаемого терапевтического отклика на ФНО-α.
4. Блокатор JAK-киназ Т-лимфоцитов
Наконец, мы добрались до наиболее прогрессивной группы таргетных препаратов – блокатор JAK-киназ тофацитиниб (Яквинус). Чтобы не слишком усложнять и без того непростой для понимания материал, скажем, что JAK-киназы – это сигнальные мембранные белки, влияющие на активность клеточного звена иммунитета. Взаимодействие с этими белками различных цитокинов (интерферон-гамма, интерлейкины) приводит к активации Т-лимфоцитов, что, как вы уже понимаете, ведет к обострению аутоиммунного воспаления в суставах. Блокировка JAK-киназ, напротив, останавливает аутоиммунные реакции и улучшает состояние пациента с РА.
Перед нами поистине новое слово в лечении РА, наиболее инновационная группа лекарств. Масштабные клинические испытания (ORAL Scan) завершены только в конце 2013 года. Клинические эксперименты, в которых участвовало более 5000 пациентов с РА, доказали отличный профиль безопасности тофацитиниба и высокую эффективность при тяжелых формах ревматоидного артрита. Еще одним достоинством препарата является таблетированная форма выпуска, что делает длительное лечение тофацитинибом максимально комфортным и избавляет человека от необходимости регулярных инъекций лекарственных средств.
На примере четырех групп антицитокиновых препаратов мы познакомились с основными направлениями современной фармакотерапии ревматоидного артрита. Читатель, который смог дочитать этот материал до конца, должен понимать две вещи. Во-первых, эти препараты назначаются при тяжелой и среднетяжелой форме РА, лечить легкую форму столь мощными (и дорогостоящими) средствами нецелесообразно.
Во-вторых, при всей эффективности эти лекарства не являются панацеей, именно поэтому ученые продолжают искать новые мишени для фармакотерапии. Терапевтический отклик на определенный ГИБП достигается примерно у 70 % пациентов с тяжелым РА, а оставшимся 30 % приходится искать другой препарат таргетной терапии. Это означает, что при лечении РА одним из ключевых факторов остается опыт лечащего ревматолога и его умение выбрать из множества возможностей оптимальный, наиболее эффективный лекарственный препарат!
Читайте также:


