Чрескостный остеосинтез при лечении остеомиелита
Блестящие исходы дает внеочаговый чрескостный остеосинтез на сегментах конечностей, не имеющих больших мышечных массивов, особенно на голени. Использование его при переломах бедренной кости, особенно в верхней трети и у тучных людей, связано с резко увеличивающейся опасностью нагноения в тканях вокруг спиц и возникновением спицевых остеомиелитов. Если же спицы аппарата должны быть проведены через заведомо инфицированные участки кости или через активно гноящиеся мягкие ткани, то это неизбежно приводит к резкому обострению уже существующего в кости воспалительного процесса или его распространению на кость из мягких тканей.
Это обычно вынуждает к снятию аппарата и переходу к другому методу лечения — как правило, к иммобилизации гипсовой повязкой. Такие смены методов лечения обычно происходят в условиях усугубления гнойного процесса и отягощения состояния больного. Все это указывает на преимущества способов лечения гнойных процессов у этой категории больных, при которых удается сохранить погружной металлический фиксатор до полной консолидации перелома.
Иллюстрацией тяжелых последствий торопливой и непродуманной смены методов лечения служит следующее наблюдение, которое также является примером задержанного нагноения (нагноение в средние сроки).
Больному С., 24 лет, в травматологическом отделении одной из московских больниц был произведен интрамедуллярный остеосинтез по поводу закрытого перелома правой бедренной кости в средней трети. Через 12 дней после операции швы сняты, констатировано первичное заживление раны, и больной выписан для амбулаторного лечения. Вскоре после выписки появились выделения из раны. Около месяца лечился амбулаторно, а затем в связи с обострением процесса повторно был госпитализирован в то же отделение.
В связи с развившимся нагноительным процессом (рост в посеве отделяемого из раны золотистого гемолитического стафилококка) больной повторно оперирован: удален интрамедуллярный штифт и наложена тазобедренная (кокситная) гипсовая повязка, еще через месяц гипсовая повязка снята и наложен аппарат Илизарова из 4 колец. Уже спустя 2 нед после наложения данного аппарата начали гноиться ткани вокруг каждого из проколов спиц. Общее состояние больного ухудшилось и он был переведен в ЦИТО в отделение раневой инфекции.
При поступлении в ЦИТО общее состояние больного тяжелое. Аппетит резко снижен, не спит из-за болей, покровы и слизистые бледны. Пульс 128 в минуту. Температура 39°С. По наружнопередней поверхности средней и верхней трети бедра — рана больших размеров с грязно-серым некротическим налетом. Несколько меньшего размера (9x5 см), но с таким же налетом — рана в области ягодицы, где производили разрез для извлечения гвоздя.
Из обеих ран — обильное гнойное отделяемое с зеленоватым оттенком и неприятным запахом. Конечность фиксирована аппаратом Илизарова. Верхние кольца аппарата интимно предлежат к коже, а доступ к спицам резко затруднен. Из каждой кожной ранки (их 8), через которые проходят спицы, при надавливании на кожу изнутри выделяется гной. Признаков воспалительной реакции со стороны окружающей ранки кожи нет.
Посевы гноя дают рост ассоциации микробов из стафилококка, синегнойной палочки и клебсиеллы.
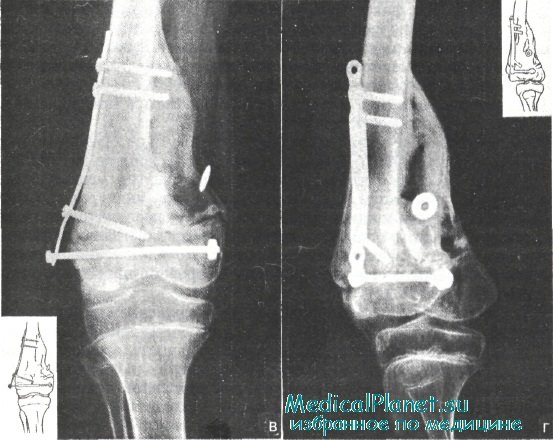
Начата активная трансфузионная терапия, проведены повторные переливания крови и кровезаменителей, белковых препаратов, низкомолекулярных декстранов. Компрессионно-дистракционный аппарат сняли и наложили мостовидную тазобедренную (кокситную) гипсовую повязку. Раны при перевязках тщательно промывали перекисью водорода и другими антисептическими растворами и вводили в них протеолитический фермент.
Последний вводили шприцем также в каждую ранку в местах проведения спиц, из которых продолжалось обильное гноетечение. При введении раствора в одну из них он обычно вытекал через несколько других, а также через основную рану на бедре. Проводили общую антибиотикотерапию — внутримышечно вводили гентамицин по 80 мг 2 раза в день, карбенициллин по 500 мг 3 раза в день.
Через 3 нед после поступления больного, когда общее состояние его улучшилось, основные показатели гомеостаза нормализовались, а раны стали очищаться от некротических налетов, предпринято первое оперативное вмешательство. Операция заключалась в радикальной хирургической обработке костного очага с удалением нескольких мелких секвестров и широкой резекции стенок костной полости (секвестрнекрэктомия), рассечении нескольких гнойных карманов в мягких тканях и тщательном удалении из них патологических грануляций. Во время операции было установлено, что идет процесс консолидации перелома с образованием костной перемычки между внутреннезадними стенками костных фрагментов.
После окончания хирургических, манипуляций рана имела вид корытообразного углубления с костным дном. После промывания, обработки ультразвуком и заполнения препаратом КФ рана дренирована двумя парами дренажных трубок и послойно ушита наглухо. Наложена тазобедренная (кокситная) гипсовая повязка.
В послеоперационном периоде проводили постоянное промывание раны через дренажи, продолжали общую антибиотикотерапию. Рана на ягодице выполнялась грануляциями, эпителизировалась по краям. Однако постепенно послеоперационная рана нагнаивалась, швы прорезались и развился рецидив процесса вследствие нагноения в резко измененных мягких тканях бедра. Из закрывшихся ранок мягких тканей в местах проведения спиц снова начал выделяться гной.
Основным возбудителем в ране оставалась синегнойная палочка. Общее состояние больного периодически улучшалось, затем вновь ухудшалось — он терял аппетит, нарушался сон. Обострение гнойного процесса в ране усиливало также боли, которые уменьшались после курсов лечения иглоукалыванием. Из общеукрепляющих средств больной получал внутрь элеутерококк. Снова начался длительный период терапевтических воздействий (внутривенные переливания крови и кровезаменителей, вливание витаминов, белковых растворов и т. д.), частых перевязок с промыванием раны, тщательного и кропотливого ухода за больным. Общее его состояние и местное течение процесса периодически настолько ухудшалось, что стоял вопрос об ампутации бедра.
Через 1,5 мес после первой операции в ЦИТО больного оперировали повторно. Рану вновь рассекли так, что в кожный разрез были включены две небольшие активно функционирующие ранки в местах проведения спиц. Обращало на себя внимание плохое состояние мягких тканей бедра — мышцы были рубцово изменены и неподатливы, кожа малоподвижна. Кость только на ограниченном участке не покрыта надкостницей и грануляциями и здесь ее резецировали. Проведены обычная обработка раны и тампонирование ее по Микуличу и наложена тазобедренная гипсовая повязка. Рана медленно выполнялась грануляциями и долго активно гноилась.
Постепенно общее состояние больного улучшилось, а рана уменьшилась и эпителизировалась по краям. Все же сформировался свищ по наружной поверхности бедра. Для его ликвидации была предпринята третья операция — иссечение свища; послеоперационную рану вели открыто по Микуличу, и она зажила вторичным натяжением. Перелом сросся, но костная мозоль слабая, в связи с чем больному изготовили ортопедический аппарат с опорой на седалищный бугор. Конечность укорочена за счет бедра на 5 см, активные движения в коленном суставе возможны в пределах 25 градусов. Проведена лечебная гимнастика для коленного сустава.
Таким образом, для ликвидации раневого гнойного процесса после интрамедуллярного остеосинтеза, предпринятого по поводу закрытого перелома бедренной кости с резким его отягощением, после удаления интрамедуллярного фиксатора и наложения компрессионно-дистракционного аппарата потребовалось более 2 лет лечения в стационаре. Существовала реальная угроза для ноги больного и даже для его жизни. Сохраненная нога укорочена, движения в коленном суставе через год после последней операции значительно ограничены.
Показания к удалению металлического фиксатора при возникновении гнойного раневого осложнения, конечно, есть. К ним следует отнести такое течение заболевания, при котором бурно развивающаяся картина воспалительного процесса связана со скоплением гнойного отделяемого в костномозговом канале и сам фиксатор мешает оттоку гноя. Другим показанием к удалению фиксатора является ситуация, когда фиксатор не выполняет своей роли — интрамедуллярный штифт значительно меньшего диаметра, чем костномозговой канал трубчатой кости; шурупы не фиксируют пластину; металлический фиксатор поломан (он превращается в бесполезное и вредное инородное тело и подлежит удалению).
При эндопротезировании крупных суставов инфекционные осложнения развиваются в 1,5-
20 % случаев от общего числа всех операций по замене суставов различных локализаций.
При эндопротезировании крупных суставов инфекционные осложнения развиваются в 1,5-20 % случаев от общего числа всех операций по замене суставов различных локализаций. Они протекают злокачественно, с трудом поддаются лечению и требуют от специалистов мобилизации всех возможных способов лечения с целью сохранения эндопротеза К сожалению, до настоящего времени нет единой патогенетически
обоснованной тактики реабилитации этой категории больных. При этом все хирурги независимо от используемых методов лечения едины во мнении о большой сложности восстановительного лечения, что обусловлено спецификой патологии. Летальность при нагноениях в области эндопротезов составляет до 2,5 %, а в
группе пожилых больных достигает 8 %.
Хронический остеомиелит относится, как правило, к поздним послеоперационным осложнениям атегории больных.
Остеомиелит после эндопротезирования сочетает в себе взаимоотягощающие проблемы:
первая – это больше общехирургическая гнойная инфекция костей и мягких тканей, вторая –ортопедическая, обусловленная наличием сложного дефекта кости.
Сложность лечения хронического остеомиели-
та обусловлена следующими факторами: снижением реактивности организма пациента вследствие хронической интоксикации; предшествующими операциями и многократной антибактериальной терапией; толерантностью микрофлоры к большинству применяемых антибактериальных препаратов; сложностью создания необходимой
терапевтической концентрации антибиотиков в зоне гнойного поражения из-за нарушения кровоснабжения области имплантата; вынужденной высокой травматичностью оперативного вмешательства из-за локализации и распространенности гнойного процесса; сложностью обеспечения фиксации конечности после удаления имплантата;невозможностью заместить образующийся дефект костной ткани, восстановить целостность и опоро-
способность конечности.
В связи с этим материальные затраты на лечение больных остеомиелитом после эндопротезирования во много раз превосходят стоимость первичного протезирования и требуют от врача и пациента больших физических и моральных затрат в течение длительного времени.
Всем пациентам применена методика чрескостного остеосинтеза после удаления имплан-
тата и секвестрнекрэктомии.
Показаниями к открытому чрескостному ос-
теосинтезу служили:
1. Длительно функционирующие свищи с гнойным отделяемым с периодическими обострениями хронического остеомиелита и рентгенологическими признаками прогрессирования гнойно-некротического процесса в костной ткани.
2. Длительно-функционирующие свищи с гнойным отделяемым, несмотря на проводимую антибактериальную терапию и паллиативные хирургические вмешательства с рентгенологическими признаками прогрессирования гнойно-некротического процесса в костной ткани.
3. Нестабильность эндопротеза, сочетающаяся с хроническим гнойным процессом в области имплантата.
В послеоперационном периоде все больные получали медикаментозное лечение.
РЕЗУЛЬТАТЫ И ИХ ОБСУЖДЕНИЕ
При выполнении остеосинтеза были поставлены следующие задачи:стойкая ликвидация хронического гной-
ного процесса с устранением местных и общих проявлений заболевания;восстановление целостности кости и опо-
роспособности конечности;обеспечение функциональной возможности пациента к активному передвижению.
Всем пациентам применена методика чрескостного остеосинтеза после удаления имплантата и секвестрнекрэктомии.
При изучении отдаленных результатов выявлено 98,5 % положительных исходов лечения,что проявлялось в стойкой ремиссии воспалительного процесса.
Оперативный (открытый) остеосинтез при хроническом остеомиелите после эндопротезирования имеет свои особенности после удаление имплантата (при некрэктомии, дренировании,непосредственном выполнении самого чрескостного остеосинтеза).
Многолетний опыт эндопротезирования показал, что существует ряд факторов,влияющих на частоту гнойных осложнений: местные (тяжесть предшествующей травмы, травматичность предшествующего оперативного лече-
ния, в том числе, ревизионное эндопротезирование, характер консервативного лечения, в том числе внутрисуставное введение анаболических гормонов, степень патологических изменений сустава, костей, окружающих мягких тканей и кожных покровов, наличие в анамнезе воспалительных и гнойно-воспалительных заболеваний оперируемого сустава и смежных сегментов); общие(пожилой возраст, избыточный вес, наличие со-
путствующих соматических заболеваний, их стадия и степень компенсации (особенно эндокринные и аутоиммунные), состояние реактивности организма); интраоперационные (качество имплантата, некорректный подбор имплантата, травматичность операции в целом и введение компонентов эндопротеза в частности, кровопотеря , длительность операции (более 3 часов); послеоперационные (несоответствие между степенью функциональных нагрузок и физиологическими возможностями костной ткани (резорбция, нестабильность), несоблюдение температурного режима (переохлождение, перегревание);организационные.
Пациенты, настроившиеся на улучшение качества жизни после операции эндопротезирования и получившие в результате ее тяжелое гнойное осложнение с глубокой и необратимой инвалидизацией, в большинстве своем находятся в состоянии депрессии с утратой веры в излечение.
Анализируя имеющийся материал, мы пришли к следующим выводам:
1. Хронический остеомиелит после эндопротезирования является тяжелым заболеванием, требующим сложного, длительного и дорогостоящего лечения.
2. Чрескостный остеосинтез в лечении больных хроническим остеомиелитом после эндопротезирования на сегодня является методом выбора.
3. Для снижения количества хронического остеомиелита после эндопротезирования необходимо использовать все возможные профилактические мероприятия: организационные, материально–технические, медицинские, кадровые и другие,что возможно преимущественно в специализированных стационарах.

Весь контент iLive проверяется медицинскими экспертами, чтобы обеспечить максимально возможную точность и соответствие фактам.
У нас есть строгие правила по выбору источников информации и мы ссылаемся только на авторитетные сайты, академические исследовательские институты и, по возможности, доказанные медицинские исследования. Обратите внимание, что цифры в скобках ([1], [2] и т. д.) являются интерактивными ссылками на такие исследования.
Если вы считаете, что какой-либо из наших материалов является неточным, устаревшим или иным образом сомнительным, выберите его и нажмите Ctrl + Enter.
Остеосинтез представляет собой операцию, при которой хирург восстанавливает целостность кости (соединяет отломки). Существует два вида подобной операции: погружной и наружный чрескостный остиесинтез.
При наружном остиосинтезе соединение происходит с помощью специальных аппаратов, при погружном – для удержания отломков костей используют различные фиксаторы (винты, штифты, гвозди).
Целью данного хирургического метода является обеспечение неподвижности отломков костей до их полного сращения.
Чрескостный остеосинтез по Илизарову
В 1950 году Гавриил Абрамович Илизаров изобрел компрессионно-дистракционный аппарат, состоящий из стержней, колец и спиц и предназначенный для фиксации отломков костей.
4 стержня соединенные 2 кольцами, в которые туго натянуты перекрещенные спицы, не только надежно фиксируют кости, но и управляют сложным биологическим процессом развития костной ткани – сжатием и растяжением (компрессия и дистракция).
Аппарат Илизарова позволяет сохранить в некоторой степени работоспособность мышц и подвижность смежных суставов, что в целом обеспечивает скорейшее сращение отломков кости.
Чрескостный остиосинтез может проводиться при переломах голени, большеберцовой кости, но чаще всего его проводят при закрытых оскольчатых переломах (особенно при множественных осколках).
Чрескостный компрессионно-дистракционный остеосинтез
После того, как в хирургии стали использовать внеочаговый компрессионно-дистракционный остиосинтез, у медиков появилась возможность успешно лечить множественные переломы без вмешательства непосредственно в область перелома.
Преимуществами данного метода являются низкая травматичность, возможность сохранить подвижность в суставах и открытый доступ к пораженным участкам, что позволяет ухаживать за кожей.
Чрескостный остиосинтез с помощью внешних фиксирующих аппаратов требует организованной работы всего персонала, хорошей технической базы, а также определенных знаний и опыта медработников (младшего, среднего персонала и врачей).
Подготовку аппаратов осуществляет техник по металлу, который делает индивидуальную подгонку, проводит ремонт и т.п.
Закрытый чрескостный остеосинтез
Чрескостный остиосинтез по способу разделяют, как упоминалось, на наружный (компрессионно-дистракционный) и погружной. В свою очередь, погружной остиосинтез может быть открытым или закрытым, при котором после сопоставления всех отломков, в мозговой канал сломанной кости, через небольшой разрез вводят полый металлический стержень. Введение стержня проводится при помощи проводника (которые после удаляется), операция ведется под контролем рентгена.

[1], [2], [3], [4], [5], [6], [7]
Билокальный чрескостный остеосинтез
Билокальный остиосинтез был разработан для лечения ложного сустава. Основной проблемой данного ортопедического заболевания было то, что консервативное лечение не приводило к желаемому эффекту, а после хирургического в подавляющем большинстве случаев случаются рецидивы.
Билокальный остиосинтез назначается при болтающихся ложных суставах, при укорочении более 1,5см и истонченных фрагментах.
Ложным суставом называют патологическую подвижность в каком-либо участке скелета, чаще всего, патология встречается в области голени. Лечение предполагает два этапа – билокальный чрескостный оситиосинтез и костно-пластическая операция.
При билокальном остиосинтезе происходит удаление ложного сустава и одновременное удлинение и косметическое утолщение конечности. Удлинение конечности проводится после искусственного перелома кости (остеотомии), путем разрыва эпифизраной зоны.
Несмотря на положительные результаты, риск повторного развития патологии остается высоким, а полный курс лечения занимает около 2 лет.
Чрескостный остиисинтез показывает положительные результаты при лечении ложных суставов и патологиях длинных трубчатых костей, также этот метод показан при остеомиелите (на фоне лечения не возникает обострение заболевания).
При помощи аппарата устраняется как ложный сустав, так и деформация кости (при необходимости).
При атрофических ложных суставах открытый метод сращения кости является малоэффективным, в этом случае рекомендуется обнажение отломков костей и создание встречно-боковой компрессии спицами.
После того, как кость срослась, хирурги проводят удлинение при помощи аппаратов и остеотомии.
Как и любого другого метода, остеосинтез имеет недостатки, среди которых можно выделить возможность повреждения крупных сосудов, нервных стволов, кожных покровов, воспалительные процессы вокруг спиц, косметические дефекты, неудобство.
Для наложения аппарата требуется довольно много времени, кроме этого, необходима определенная подготовка хирурга, также наблюдаются трудности при замене спиц.
Специалисты рекомендуют данный метод при открытых переломах, которые сопровождаются существенным размозжением тканей, а также при травмах или неправильно сросшихся переломах.

[8], [9], [10]
Особенности лечения травматического остеомиелита длинных костей у больных после применения различных видов остеосинтеза
На основе анализа лечения 187 больных с травматическим остеомиелитом выявлены особенности поражения в зависимости от вида остеосинтеза. Индивидуальные особенности являлись информационной базой, на основе анализа которой и вырабатывалась и осуществлялась лечебная (хирургическая и консервативная) тактика лечения.
На основі аналізу лікування 187 хворих з травматичним остеомієлітом виявлені особливості ураження залежно від остеосинтезу. Індивідуальні особливості були інформаційною базою, на основі аналізу якої і вироблялася і здійснювалася лікувальна (хірургічна і консер-вативна) тактика лікування.
On the basis of the analysis of treatment of 187 patients with a traumatic osteomyelitis are revealed features of defeat depending on an osteosynthesis kind. Specific features were information base on the basis of which analysis it was developed and carried out medical (surgical and conservative) treatment tactics.
травматический остеомиелит, лечение
травматичний остеомієліт, лікування
traumatic osteomyelitis, treatment
Проблема лечения травматического остеомиелита после применения различных видов остеосинтеза становится актуальной в последнее время. Бурное развитие травматологии, широкое внедрение новых методик ведет к развитию гнойно-некротических осложнений в высоком проценте случаев. Определение тактики лечения в этих случаях является не однозначным, общепринятым и носит ярко выраженный индивидуальный характер в каждом конкретном клиническом случае.
Целью является выработка оптимальной тактики лечения на основе систематизация особенностей развития гнойно-некротических осложнений при определенных видах остеосинтеза, группировка по основным признакам Задачами исследования является определения характерных особенностей характера воспалительных поражений у пострадавших после различных видов остеосинтеза, определение факторов выработки объема санирующей и пластической составляющих, консервативной терапии.
Материал и методы
Под нашим наблюдением находилось 187 больных с травматическим остеомиелитом, находящихся на лечении в отделении костно-гнойной хирургии Донецкой областной травматологической больницы, у которых ранее применялись различные виды остеосинтеза переломов. Пострадавшие были обследованы. Выявленный характер поражения, индивидуальные особенности являлись информационной базой, на основе анализа которой и вырабатывалась и осуществлялась лечебная (хирургическая и консервативная) тактика лечения.
Результаты и обсуждение
Остеосинтез – один из основных способов оптимизации репаративного процесса при переломах костей. Основными общепринятыми свойствами его должны быть устойчивая фиксация сопоставленных отломков, что делает возможным раннюю нагрузку на конечность. Широкое скелетирование отломков при проведении остеосинтеза ведет к нарушению их питания, травматизация мягких тканей создает условия для развития гнойной инфекции. При этом инфицирование области перелома может происходить не только экзогенно, но при наличии нарушений иммунитета – и экзогенно, из кишечника (транслокация). Все виды остеосинтеза имеют свои свойства и характеристики, показания к применению. Именно они и обуславливают особенности травматического остеомиелита после различных видов остеосинтеза. Общепринятой классификацией, наиболее удобной для характеристики посттравматического остеомиелита, является анатомическая классификация Cierny-Mader (рис.1).
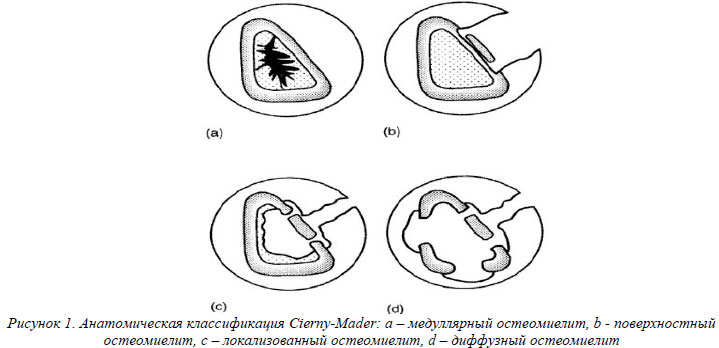
Хирургическим подходом в лечении травматического остеомиелита является радикальная санация, пластика дефектов и восстановление сегмента как органа опоры. В тоже время мы считаем, что при выборе объемов вмешательства в каждом конкретном случае большую роль имеет не только степень поражения кости гнойным процессом, но и перспектива восстановления функции конечности (выраженность репаративных процессов и риск повторного перелома). Предложенная нами характеристика посттравматического остеомиелита базируется на анатомических принципах – степени (распространенности) воспалительного процесса в кости и выраженности репаративных процессов при переломе кости (есть сращение или его нет), риск наступления рефрактур (рис.2).
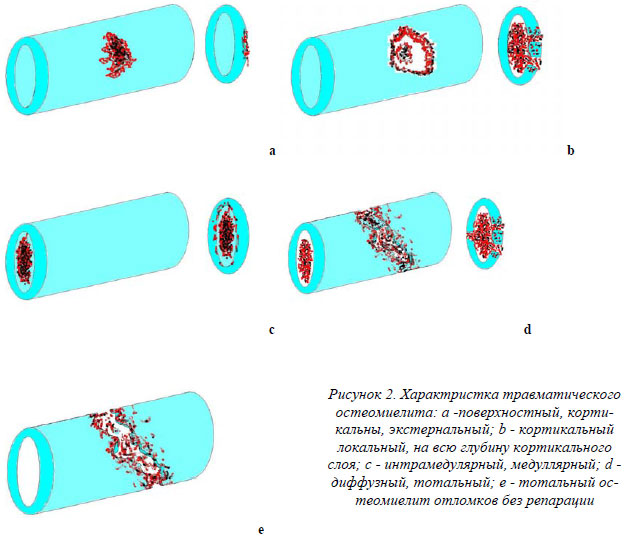
Предложенная характеристика лежит в основе выработки тактики хирургического лечения. Для упрощения и более удобного использования в практике были выделены следующие градации процессов. Степень поражения костной ткани травматическим остеомиелитом делилась на 3 группы: менее 1/3 диаметра, от 1\3 диаметра до 1\2 диаметра и более 1\2 диаметра. Степень репаративной регенерации костной ткани упрощенно делили на отсутствие сращения (ложный сустав) и сращение отломков (восстановление кости). Различные комбинации этих характеристик поражения и выработка хирургической тактики в упрощенном виде представлены в таблице.
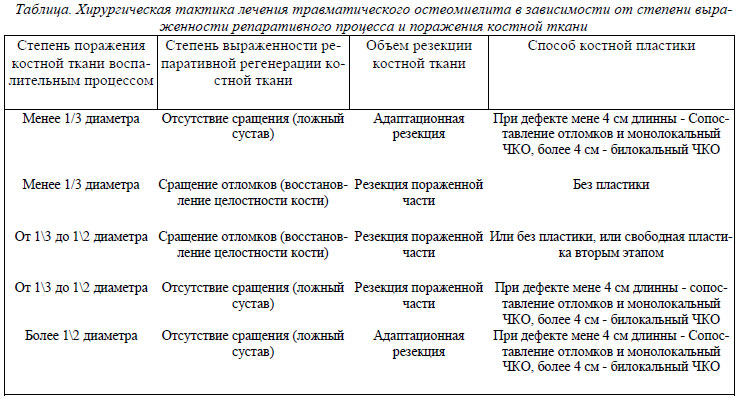
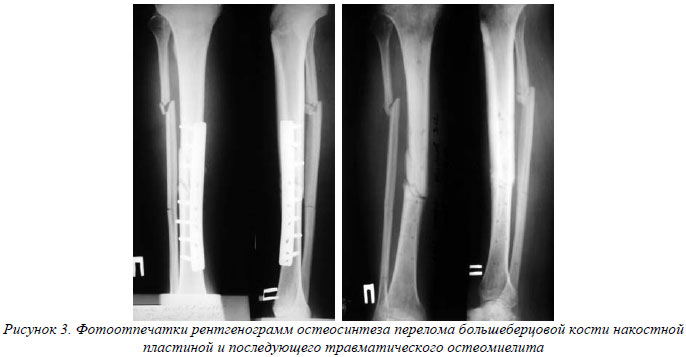
После накостного остеосинтеза воспалительный процесс в кости вызван широким скелетированием, давлением на кость пластины, контактом не всегда однородных металлов пластины и шурупа часто развивается медуллярный остеомиелит вдоль шурупов, зачастую присоединяется и диффузный (рис.3).
Малотравматичным, с редкими осложнениями, является блокируемый остеосинтез - БИОС. Однако выполнение всех технологических требований подразумевает использование специального оборудования и нередко трудно выполнимо в ургентных условиях. Проведение блокируемого интрамедуллярного остеосинтеза после накостного остеосинтеза или внеочаговго чрескостного остеосинтеза (ВЧКО) и развития ложных суставов подразумевает в подавляющем большинстве случаев широкое скелетирование костных отломков, что резко повышает риск развития травматического остеомиелита.
После БИОС остеомиелит зачастую носит характер медуллярного, в области стояния шурупов – локального. При открытом остеосинтезе возможно поражение концов отломков (рис.4).
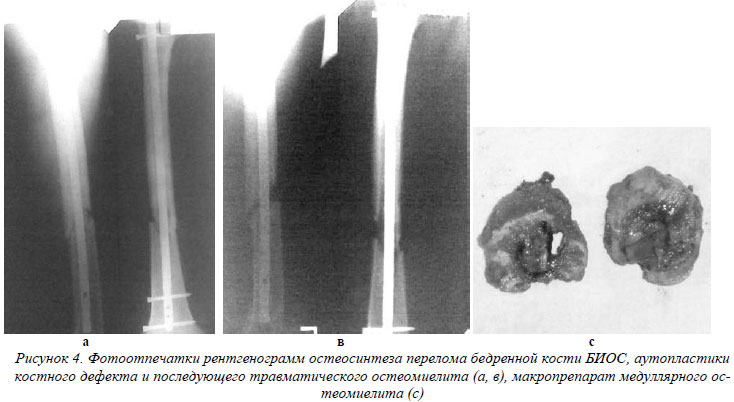
В 2 случаях остеомиелит развился после аутопластики и в 2 случаях после пластики аллографтом тутопластом. В 1 случае остеомиелит диагностирован после того, как свободно лежащий отломок фиксировался шурупом, еще в одном – серкляжной проволокой.
Эти данные дают нам основание говорить о том, что пластика костных дефектов, фиксация костных отломков дополнительными методами при проведении БИОС является достаточно опасной и с высокой долей вероятности может привести к септическому поражению костной ткани. Менее опасным является проведение закрытого штифтования. Остеомиелит после ВЧКО характеризуется локальным (спицевым остеомиелитом), реже остеомиелит концов отломков.
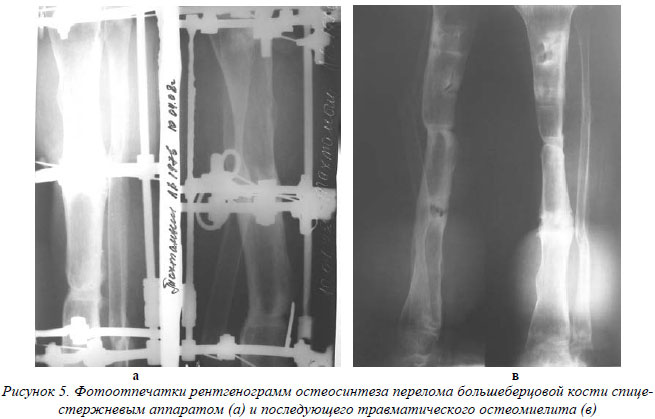
Следует отметить, что помимо вида остеосинтеза характер остеомиелитического процесса был обусловлен и видом перелома (тяжесть повреждения костной и мягких тканей, всего сегмента), а также сочетанными повреждениями и сопутствующими заболеваниями. При одинаковых условиях наиболее травматичным видом остеосинтеза, вызывающим тяжелые формы остеомиелита, является накостный. Самой щадящей является внеочаговая фиксация, в случаях открытых переломов с массивным поражением тканей, тяжелым общим состоянием и при сочетанных повреждениях предпочтительным мы считаем использование спице-стержневых аппаратов.
Направления противовоспалительной терапии и обеспечение репаратиных потребностей осуществлялось следующим образом:
- предшествующая мультимодальная анестезия (спинномозговая анестезия (СМА) Маркаин или проводниковая анестезия, династата (40 мг) с целью премедикации и обезболивания в ближайшем прослеоперационном периоде (через 12 часов);
- антибактериальная терапия в соответствии с выявленной чувситвительностью флоры (сульбактимные антибиотики сульперазон, уназин; фторхинолоны);
- эндотелиопротекторы (пентоксифилин, ГЭКи рефортан, стабизол);
- обеспечение пластических и энергетических потребностей (аминокислоты инфезол, раствор глюкозы, СаД3Никомед форте, поливитамины нейробион, берлитион);
- улучшение реологии, профилактика микротромбозов (цибор, целебрекс);
- детоксикация, десенсибилизация;
- иммуномодуляция (лавомакс).
Выводы
- Наиболее существенными факторами, определяющими объем резекции, а затем и выбор способа костной пластики, является степень поражения костной ткани воспалительным процессом (классификация Cierny-Mader), а так же степень выраженности репаративного процесса.
- Основой комплексной консервативной терапии явилось понимание травматического остеомиелита как синдрома системного воспалительного процесса.
- Использование предложенных подходов позволило достичь положительных результатов у 157 (87,9%) больных с травматическим остеомиелитом.
- Гарячий Є. В. Лікування хронічного травматичного остеомієліту з корекцією тіреоїдного статусу: Дис. . канд. мед. наук. – К., 2000. – 19 с.
- Никитин Г. Д., Рак А. В., Линник С. А. Хирургическое лечение остеомиелита. – СПб, 2000. – 287 с.
- Cierny G 3rd, Mader JT. Adult chronic osteomyelitis. Orthopedics.1984; 7:1557 -64.
- Зайцев А. Б. Реконструктивно-восстановительное лечение больных стеомиелитом голени \\ Автореферат диссертации на соискание ученой степени доктора медицинских наук. Нижний Новгород – 2009, 32 С.
- Urbaán F., Benkő I., Sánta S., Fekete K. Effects of antibiotics useful in osteomyelitis on the granulocyte-macrophag progenitor cells // 6-th European Trauma Congress (Abstracts). – May 16–19, 2004. – Р. 92.
- Schmidt H. Komplikationsmanagement der chronischen Knocheninfektion. – 17 Workshop "Good Clinical Practice" "Septische Chirurgie", 16–17 Dezember 2005, Langenbeck-Virchow-Haus, Berlin und der Aesculap Akademie. – Р. 10.
Читайте также:


