Цитомегаловирусная инфекция диагностика клиника лечение
Инкубационный период при приобретенной ЦМВ-инфекции неизвестен, так как начальные симптомы ее, как правило, отсутствуют. Клиническая манифестация возникает после какого-либо ослабляющего воздействия на организм человека. Общепринятой клинической классификации ЦМВ-инфекции не существует. Ниже приводится классификация, предложенная сотрудниками клиники инфекционных болезней Военно-медицинской академии (Ю.В. Лабзин, А.П. Казанцев, Н.Н. Попова). Выделяют следующие клинические формы
ЦМВ-инфекции
А. Приобретенная цитомегалия:
1. Латентная (локализованная);
2. Острая мононуклеозная,
3. Генерализованная цитомегалия.
Б Врожденная цитомегалия
Острая и хроническая формы.
В Цитомегалия у ВИЧ-инфицированных и других лиц с ослабленным иммунитетом
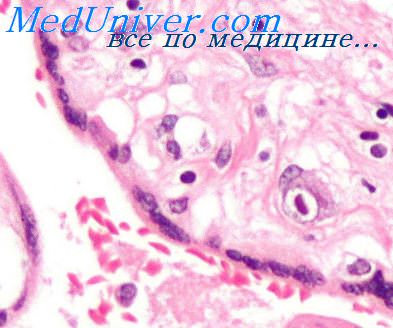
Латентная форма приобретенной ЦМВ-инфекции характеризуется только наличием специфических антител. Каких-либо симптомов болезни при ней не наблюдается. По некоторым данным, у здоровых лиц (доноров) антитела обнаруживали почти у 2/3 обследованных.
Острая форма ЦМВ-инфекции проявляется повышением температуры и симптомами интоксикации. По течению она более всего напоминает инфекционный мононуклеоз, но при ней отсутствуют тонзиллит и лимфаденопатия, как это имеет место при мононуклеозе. В периферической крови - относительный лимфоцитоз с атипичными мононуклеарами (более 10%), чаще нормоцитоз и умеренная лейкопения. Монотест и гетерофильные антиэритроцитарные антитела не определяются. В ряде случаев течение болезни напоминает грипп или вирусный гепатит. Длительность острой формы болезни от 2 до 6 недель, после чего сохраняются постинфекционная астения и вегетосо-судистая дистония. Могут быть осложнения: пневмония (интерстициальная или сегментарная), плеврит, миокардит, артрит, энцефалит, синдром Гийена-Барре.
Генерализованная форма встречается редко и наблюдается у лиц с ослабленным иммунологическим фоном Клинически проявляется лихорадкой, симптомами интоксикации, увеличением печени, лимфаденопатией, вяло текущей пневмонией (в мокроте обнаруживают клетки, характерные для цитомегалии).
Врожденная цитомегаловирусная инфекция характеризуется клиникой, зависящей от сроков инфицирования плода. Она неотличима от других инфекций (краснуха, токсоплазмоз, корь и др.), поражающих плод внутриутробно
У больных СПИДом цитомегаловирусная инфекция протекает тяжело и является частым спутником его терминальной стадии, приводяк гибели больного. При трансплантации органов (почек, сердца, печени, костного мозга и других органов) она возникает через 1-4 мес после операции; протекает тяжело в виде пневмонии, гепатита, поражения глаз, сепсиса. Может быть причиной дисфункции трансплантанта.
Клинически ЦМВ-инфекцию диагностировать невозможно Диагноз устанавливается лабораторно при цитоскопии слюны, мочи, биопсииного материала, в которых находят цитомегалические клетки С помощью ПЦР возможно обнаружение специфической вирусной ДНК Используются серореакции (ИФА, РИА, РИФ, иммуноблотинг)для поиска специфических антител различных классов. При острых формах ЦМВ-инфекции образуются IgM, при обострениях латентной - одновременно IgM и IgG. При стихании клинических проявлений продуцируются только IgG.
Лечение цитомегаловирусной инфекции представляет трудную задачу. Эффективных этиотроп-ных препаратов пока не существует. Применение интерферона, ацик-ловира, виразола, видарабина не дает заметных результатов. Ганцик-ловир оказывает некоторое положительное действие при ретинитах, но не замедляет развития поражений легких, печени и др Обнадеживает назначение фоскарнета, цимевена. Для превентивного лечения внутриутробной ЦМВ-инфекции рекомендуется введение нормального человеческого иммуноглобулина (по 6-12 мл внутримышечно с интервалами 2-3 недели в течение первых трех месяцев беременности). Проводят патогенетическое и симптоматическое лечение. Прогноз при латентной форме благоприятный, при генерализованной и врожденной формах болезни - серьезный.
Единственный источник инфекции - человек. Вирус присутствует в слюне, грудном молоке, моче, испражнениях, сперме, секретах из уретры, влагалища, шейки матки, а также в крови и спинномозговой жидкости. Инфицированность женщин детородного возраста составляет от 60 до 80% обследованных.
Передача инфекции возможна различными путями: воздушно-капельным, контактным (при поцелуях, половым), при использовании нестерильных шприцев, биологических жидкостей, тканей и органов при трансплантациях. У беременных женщин, инфицированных цитомегаловирусом, передача инфекции плоду происходит трансплацентарно и во время родов
Специфическая профилактика отсутствует. Проводится обследование доноров и беременных женщин на наличие антител к вирусу ЦМВ. Наиболее эффективной мерой могло бы стать обследование женщин до зачатия Мероприятия в очаге инфекции не проводятся.
Цитомегалия – это инфекционное заболевание вирусного генеза, передающееся половым, трансплацентарным, бытовым, гемотрансфузионным путем. Симптоматически протекает в форме упорной простуды. Отмечается слабость, недомогание, головные и суставные боли, насморк, увеличение и воспаление слюнных желез, обильное слюноотделение. Часто протекает бессимптомно. Опасна цитомегалия беременных: она может вызывать самопроизвольный выкидыш, врожденные пороки развития, внутриутробную гибель плода, врожденную цитомегалию. Диагностика осуществляется лабораторными методами (ИФА, ПЦР). Лечение включает противовирусную и симптоматическую терапию.
МКБ-10
Общие сведения
Другие названия цитомегалии, встречающиеся в медицинских источниках, - цитомегаловирусная инфекция (ЦМВ), инклюзионная цитомегалия, вирусная болезнь слюнных желез, болезнь с включениями. Цитомегалия является широко распространенной инфекцией, и многие люди, являясь носителями цитомегаловируса, даже не подозревают об этом. Наличие антител к цитомегаловирусу выявляется у 10—15% населения в подростковом возрасте и у 50% взрослых людей. По некоторым источникам, носительство цитомегаловируса определяется у 80% женщин детородного периода. В первую очередь это относится к бессимптомному и малосимптомному течению цитомегаловирусной инфекции.

Причины
- воздушно-капельным: при чихании, кашле, разговоре, поцелуях и т.д.;
- половым путем: при сексуальных контактах через сперму, влагалищную и шеечную слизь;
- гемотрансфузионным: при переливании крови, лейкоцитарной массы, иногда - при пересадке органов и тканей;
- трансплацентарным: во время беременности от матери плоду.
Нередко цитомегаловирус находится в организме многие годы и может ни разу не проявить себя и не нанести вреда человеку. Проявление скрытой инфекции происходит, как правило, при ослаблении иммунитета. Угрожающую по своим последствиям опасность цитомегаловирус представляет у лиц со сниженным иммунитетом (ВИЧ-инфицированных, перенесших трансплантацию костного мозга или внутренних органов, принимающих иммунодепрессанты), при врожденной форме цитомегалии, у беременных.
Патогенез
Попадая в кровь, цитомегаловирус вызывает выраженную иммунную реакцию, проявляющуюся в выработке защитных белковых антител – иммуноглобулинов М и G (IgM и IgG) и противовирусной клеточной реакцией - образованием лимфоцитов CD 4 и CD 8. Угнетение клеточного иммунитета при ВИЧ-инфекции приводит к активному развитию цитомегаловируса и вызываемой им инфекции.
Даже при бессимптомном течении инфекции носитель цитомегаловируса является потенциально заразным для неинфицированных лиц. Исключение составляет внутриутробный путь передачи цитомегаловируса от беременной женщины плоду, который происходит в основном при активном течении процесса, и лишь в 5% случаев вызывает врожденную цитомегалию, в остальных же носит бессимптомный характер.
Симптомы цитомегалии
В 95% случаев внутриутробное инфицирование плода цитомегаловирусом не вызывает развития заболевания, а протекает бессимптомно. Врожденная цитомегаловирусная инфекция развивается у новорожденных, матери которых перенесли первичную цитомегалию. Врожденная цитомегалия может проявляться у новорожденных в различных формах:
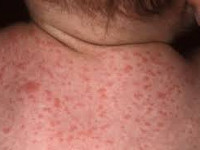
- петехиальная сыпь – мелкие кожные кровоизлияния - встречается у 60-80% новорожденных;
- недоношенность и задержка внутриутробного развития плода - встречается у 30% новорожденных;
- желтуха;
- хориоретинит – острый воспалительный процесс в сетчатке глаза, часто вызывающий снижение и полную потерю зрения.
Летальность при внутриутробном инфицировании цитомегаловирусом достигает 20-30%. Из выживших детей большая часть имеет отставание в умственном развитии или инвалидность по слуху и зрению.
При инфицировании цитомегаловирусом в процессе родов (при прохождении плода по родовым путям) или в послеродовом периоде (при бытовом контакте с инфицированной матерью или грудном вскармливании) в большинстве случаев развивается бессимптомное течение цитомегаловирусной инфекции. Однако у недоношенных младенцев цитомегаловирус может вызывать затяжную пневмонию, к которой часто присоединяется сопутствующая бактериальная инфекция. Часто при поражении цитомегаловирусом у детей отмечается замедление в физическом развитии, увеличение лимфоузлов, гепатит, сыпь.
У лиц, вышедших из периода новорожденности и имеющих нормальный иммунитет, цитомегаловирус может вызывать развитие мононуклеозоподобного синдрома. Течение мононуклеазоподобного синдрома по клинике не отличается от инфекционного мононуклеоза, вызываемого другой разновидностью герпесвируса – вирусом Эбштейна-Барр. Течение мононуклеозоподобного синдрома напоминает упорную простудную инфекцию. При этом отмечается:
- длительная (до 1 месяца и более) лихорадка с высокой температурой тела и ознобами;
- ломота в суставах и мышцах, головная боль;
- выраженные слабость, недомогание, утомляемость;
- боли в горле;
- увеличение лимфоузлов и слюнных желез;
- кожные высыпания, напоминающие сыпь при краснухе (обычно встречается при лечении ампициллином).
В отдельных случаях мононуклеозоподобный синдром сопровождается развитием гепатита – желтухой и повышением в крови печеночных ферментов. Еще реже (до 6% случаев) осложнением мононуклеозоподобного синдрома служит пневмония. Однако у лиц с нормальной иммунной реактивностью она протекает без клинических проявлений, выявляясь лишь при проведении рентгенографии легких.
Длительность течения мононуклеозоподобного синдрома составляет от 9 до 60 дней. Затем обычно наступает полное выздоровление, хотя на протяжении нескольких месяцев могут сохраняться остаточные явления в виде недомогания, слабости, увеличенных лимфоузлов. В редких случаях активизация цитомегаловируса вызывает рецидивы инфекции с лихорадкой, потливостью, приливами и недомоганием.
Ослабление иммунитета наблюдается у лиц, страдающих синдромом врожденного и приобретенного (СПИД) иммунодефицита, а также у пациентов, перенесших пересадку внутренних органов и тканей: сердца, легкого, почки, печени, костного мозга. После пересадки органов пациенты вынуждены постоянно принимать иммунодепрессанты, ведущие к выраженному подавлению иммунных реакций, что вызывает активность цитомегаловируса в организме.
У пациентов, перенесших трансплантацию органов, цитомегаловирус вызывает поражение донорских тканей и органов (гепатит – при пересадке печени, пневмонию при пересадке легкого и т. д.). После трансплантации костного мозга у 15-20% пациентов цитомегаловирус может привести к развитию пневмонии с высокой летальностью (84-88%). Наибольшую опасность представляет ситуация, когда инфицированный цитомегаловирусом донорский материал пересажен неинфицированному реципиенту.
Цитомегаловирус поражает практически всех ВИЧ-инфицированных. В начале заболевания отмечаются недомогание, суставные и мышечные боли, лихорадка, ночная потливость. В дальнейшем к этим признакам могут присоединяться поражения цитомегаловирусом легких (пневмония), печени (гепатит), мозга (энцефалит), сетчатки глаза (ретинит), язвенные поражения и желудочно-кишечные кровотечения.
У мужчин цитомегаловирусом могут поражаться яички, простата, у женщин – шейка матки, внутренний слой матки, влагалище, яичники. Осложнениями цитомегаловирусной инфекции у ВИЧ-инфицированных могут стать внутренние кровотечения из пораженных органов, потеря зрения. Множественное поражение органов цитомегаловирусом может привести к их дисфункции и гибели пациента.
Диагностика
С целью диагностики цитомегаловирусной инфекции проводится лабораторное обследование. Постановка диагноза цитомегаловирусной инфекции основана на выделении цитомегаловируса в клиническом материале или при четырехкратном повышении титра антител.
- ИФА-диагностика. Включает определение в крови специфических антител к цитомегаловирусу - иммуноглобулинов М и G. Наличие иммуноглобулинов М может свидетельствовать о первичном заражении цитомегаловирусом либо о реактивации хронической ЦМВИ. Определение высоких титров IgМ у беременных может угрожать инфицированию плода. Повышение IgМ выявляется в крови спустя 4-7 недель после заражения цитомегаловирусом и наблюдается на протяжении 16-20 недель. Повышение иммуноглобулинов G развивается в период затухания активности цитомегаловирусной инфекции. Их наличие в крови говорит о присутствии цитомегаловируса в организме, но не отражает активности инфекционного процесса.
- ПЦР-диагностика. Для определения ДНК цитомегаловируса в клетках крови и слизистых (в материалах соскобов из уретры и цервикального канала, в мокроте, слюне и т. д.) используется метод ПЦР-диагностики (полимеразной цепной реакции). Особенно информативно проведение количественной ПЦР, дающей представление об активности цитомегаловируса и вызываемого им инфекционного процесса.
В зависимости от того, какой орган поражен цитомегаловирусной инфекцией, пациент нуждается в консультации гинеколога, андролога, гастроэнтеролога или других специалистов. Дополнительно по показаниям проводится УЗИ органов брюшной полости, кольпоскопия, гастроскопия, МРТ головного мозга и другие обследования.
Лечение цитомегаловирусной инфекции
Неосложненные формы мононуклеазоподобного синдрома не требует специфической терапии. Обычно проводятся мероприятия, идентичные лечению обычного простудного заболевания. Для снятия симптомов интоксикации, вызываемой цитомегаловирусом, рекомендуется пить достаточное количество жидкости.
Лечение цитомегаловирусной инфекции у лиц, входящих в группу риска, проводится противовирусным препаратом ганцикловиром. В случаях тяжелого течения цитомегалии ганцикловир вводится внутривенно, т. к. таблетированные формы препарата обладают лишь профилактическим эффектом в отношении цитомегаловируса. Поскольку ганцикловир обладает выраженными побочными эффектами (вызывает угнетение кроветворения - анемию, нейтропению, тромбоцитопению, кожные реакции, желудочно-кишечные расстройства, повышение температуры и ознобы и др.), его применение ограничено у беременных, детей и у людей, страдающих почечной недостаточностью (только по жизненным показаниям), он не используется у пациентов без нарушения иммунитета.
Для лечения цитомегаловируса у ВИЧ-инфицированных наиболее эффективен препарат фоскарнет, также обладающий рядом побочных эффектов. Фоскарнет может вызывать нарушение электролитного обмена (снижение в плазме крови магния и калия), изъязвление половых органов, нарушение мочеиспускания, тошноту, поражение почек. Данные побочные реакции требуют осторожного применения и своевременной корректировки дозы препарата.
Прогноз
Особую опасность цитомегаловирус представляет при беременности, так как может провоцировать выкидыш, мертворождение или вызывать тяжелые врожденные уродства у ребенка. Поэтому цитомегаловирус, наряду с герпесом, токсоплазмозом и краснухой, относится к числу тех инфекций, обследоваться на которые женщины должны профилактически, еще на этапе планирования беременности.
Профилактика
Особенно остро вопрос профилактики цитомегаловирусной инфекции стоит у лиц, входящих в группу риска. Наиболее подвержены инфицированию цитомегаловирусом и развитию заболевания ВИЧ-инфицированные (особенно больные СПИДом), пациенты после трансплантации органов и лица с иммунодефицитом иного генеза.
Неспецифические методы профилактики (например, соблюдение личной гигиены) неэффективны в отношении цитомегаловируса, так как заражение им возможно даже воздушно-капельным путем. Специфическая профилактика цитомегаловирусной инфекции проводится ганцикловиром, ацикловиром, фоскарнетом среди пациентов, входящих в группы риска. Также для исключения возможности инфицирования цитомегаловирусом реципиентов при пересадке органов и тканей необходим тщательный подбор доноров и контроль донорского материала на наличие цитомегаловирусной инфекции.
[youtube.player]ЦИТОМЕГАЛОВИРУСНАЯ ИНФЕКЦИЯ
Цитомегаловирусная инфекция - это острая или хроническая антрапонозная вирусная инфекция, характеризующаяся многообразием клинической картины с различной степенью выраженности от латентных форм, до клинической манифестации на фоне снижения иммунной защиты, часто протекает под маской других заболеваний.
Возбудитель принадлежит к семейству Herpesviridae (ВГЧ 5 – вирус герпеса человека 5 типа), подсемейству β, роду Cytomegalovirus. У возбудителя есть некоторые составляющие, обуславливающие клиническую картину, они будут представлены в причинно-следственной последовательности:
- Возбудитель ДНК-содержащий, он встраивает свой геном в геном клетки макроорганизма, что вызывает её изменения – инфицированная клетка увеличивается в размерах и становится цитомегальной клеткой, которая продуцирует вирус цитомегалии, и репликация этого вируса нарушает синтетические процессы и энергетический обмен в заражённых клетках.
- Этот вирус имеет тропность к нейронам и нейроглии, но также и к другим тканям: эпителиальные клетки слюнных желёз, почечных канальцев и других тканей, эндотелий сосудов, лейкоциты (лимфоциты, макрофаги,нейтрофилы), мегакариоциты, фибробласты; Такая расширенная тропность объясняет полиморфность клиники и развитие иммунодепрессии, поэтому стоит на втором месте от СПИДа по развитию ИДС (иммунодефицитного состояния); Также, тропность к клеткам формирует основание для развития аутоимунных заболеваний (системная красная волчанка, гломерулонефрит, аутоиммунные гепатиты, рассеянный склероз и др.)
- Сильное повреждающее действие ЦМВИ оказывает на Т и В-клетки (именно это объясняет иммунодепрессию), вызывая Т-клеточный иммунодефицит, поликлональную активацию В-лимфоцитов, нарушение функционирования макрофагов и выработки интерферонов с цитокинами.
- Особенности этого возбудителя заключаются в низкой цитопатогенности и вирулентности.
- Как и все герпесвирусы, цитомегалия вызывает длительную персистенцию и латентное течение при достаточном иммунном ответе, и реактивироваться вызывая генерализацию при ослаблении иммунитета.
- В отличии от других герпес-вирусов, этот имеет более длительную репликацию, что не позволяет сформироваться иммунитету; Иными словами информация об этом вирусе для клеток иммунной системы формируется слишком длительно.
Устойчивость
неустойчив во внешней среде и на него губительно действуют высокие температуры (при 56⁰С гибнет в течении 10-20 минут), замораживание, высушивание, действие стандартных дезинфектантов.
Восприимчивость и распространённость
Восприимчивость и распространенность повсеместная, но в странах с низким социально-экономическим уровнем отмечается тенденция заражения детского населения, а в странах более развитых эта цифра сведена к минимуму. Но чем старше человек, тем больше вероятность его заражения и, достигая 50 летнего возраста количество инфицированных достигает 99%.
Причины заражения
Источник – больной или вирусоноситель. Пути передачи инфекции: контактный и контактно-бытовой, воздушно-капельный, фекально-оральный, парентеральный (гемотрансфузионный), половой, вертикальный (трансплацентарный).
Симптомы цитомегаловирусной инфекции
Инкубационный период практически не определяется, т.к зависит от возраста инфицированного и от состояния его иммунной системы, но принято считать от 2-12 недель. В этот период происходит проникновение возбудителя в организм через слизистые или повреждённую кожу с последующим заражением лейкоцитов и размножением в них, в дальнейшем наступает вирусемия (как только концентрация возбудителя достигает предельного уровня, наступает период клинических проявлений). Период клинических проявлений начинается на фоне ослабленного иммунитета и характеризуется гематогенной диссеминацией в различные органы, в противном случае наступает длительная персистенция с последующей активацией при иммунодепрессии. Клинические проявления зависят от формы инфекции (первичное заражение, реинфекция, реактивация латентного вируса), но на первый план выступает симптомы интоксикации, лихорадки и полиорганных поражений (мононуклеозоподобный синдром, поражение лёгких, почек, ЦНС, печени и других ораганов). Т.к инфицироваться может любой орган, то ниже будут описаны наиболее часто встречающиеся случаи:
Особенность течения врождённой ЦМВИ будет зависеть от сроков гестации, т.к на ранних сроках это может привести к выкидышу или тяжёлым порокам развития, так в первые 28 недель беременности, ребёнок рождается с множественными пороками развития и задержкой внутриутробного развития , и на этом фоне возникают микст-инфекции с дальнейшим летальным исходом. Также при внутриутробном заражении, обмен веществ приобретает катаболическую направленность и поэтому часто регистрируется метаболический синдром.
У большей части детей поражается ЦНС и возникают энцефалиты и менингоэнцефалиты, возникают продуктивно-некротические изменения в веществе головного мозга, в результате чего развиваются кисты и кальцинаты. У новорожденных клиника полиморфна: нарушение сознания от возбужджения до сопорозного состояния, мышечная гипо- или гипертония, угнетение или отсутствие рефлексов характерных для новорожденных, судороги, менингиальные знаки и др. Также из-за тропности к нервной ткани, отмечают нейросенсорную глухоту с двухсторонним снижением слуха и нарушением восприятия речи, также страдает и зрительный анализатор.
С первых дней жизни появляется желтуха, которая связана с ЦМВ-гепатитом в результате которого происходит усиленный гемолиз эритроцитов, а в последующем быстро развивается холестатический синдром; Поражение печение помимо желтушности кожных покровов и эктеричности склер, будет сопровождаться болями в правой подвздошной области, а при дополнительной диагностике будет отмечаться гепатоспленомегалия, изменение цвета мочи и кала, отмечается гипербилирубинемия за счёт прямой фракции билирубина (т.к функция печени нарушается, то нарушается и конъюгация билирубина, не происходит его тансформации и он остаётся токсичным), увеличивается активность трансаминаз/щелочной фосфотазы (ЩФ)/холестирина.
Эти желтухи нужно дифференцировать с затянувшейся физиологической желтухой новорожденных, конъюгационной желтухой и гемолитической болезни новорожденных.
При поражении ЦМВ лёгких, появляются одышка, диспноэ, тахипноэ, апноэ, и при рентгенологическом обследовании – двусторонние интерстициальные инфильтраты и эмфизема, все эти признаки говорят о интерстициальной пневмонии.
При поражении почек развивается гломерулонефрит или нефрит, проявляющийся положительным симптомом Пастернацкого, цитомегалическими клетками в моче, а также цилиндрами, эритрацитами, лейкоцитами, а в крови увеличен остаточный азот и мочевина.
При поражении ЖКТ, возникают симптомы гастроэнтерита: тошнота, рвота, жидкий стул, метеоризм, изъязвления толстого отдела кишечника приводит к возникновению патологических примесей в стуле и дальнейшим развитием перитонита; Также возможно развитие панкреатита; Все вышеперечисленные формы возникают при остром начале, а при хроническом течении отмечаются стёртые малоинформативные признаки: субфебрилитет, плохая прибавка в массе, отставание в психомоторном развитии, генерализованная лимфоаденопатия, гепатоспленомегалия и другие проявления описанные выше с преобладанием какоего-либо признака.
Диагностика цитомегаловирусной инфекции
- Серологический метод направлен на обнаружение специфических антител в крови, но результаты нельзя считать стандартными как при других инфекционных заболеваниях, так при обнаружении специфических IgG невозможно точно сказать, есть ли заражение, т.к эти антитела передаются от матери ребёнку трансплацентарно. Опровергнуть или подтвердить заражение можно только путём определения степени авидности (прочность связывания антитела и антигена) и чем она меньше тем недавнее произошло заражение (если менее 30%). Если в крови определяются только IgM, без IgG, говорит об острой инфекции. При исследовании крови на наличие специфических антител, используют парные сыворотки с интервалом 14-21 суток.
- Вирусологический метод заключается в обнаружении возбудителя в биологических материалах с помощью культурального метода и молекулярного, последний метод наиболее информативен и позволяет установить наличие инфицирования в ранние сроки. Но наличие возбудителя в слюне ещё не говорит о активном заражении, а вот обнаружение возбудителя в крови/ ликворе/ моче /амниотической жидкости – диагностически неблагоприятные показатели.
Лечение цитомегаловирусной инфекции
Особого режима и диеты при заболевании ЦМВИ не требуется, а вот этиотропная терапия включает в себя ряд медикаментозных препаратов: ганцикловир, валганцикловир, фоскарнет натрия, цидовир. Считатеся, что интерфероновый ряд и иммунокорректоры не эффективны, но в повседневной практике этого утверждать нельзя.
При обнаружении возбудителя в крови беременной, назначают неоцитотек (иммуноглобулин человека антицитомегаловирусный), этот препарат назначают и новорожденным но в других концентрациях.
При врождённой ЦМВИ, помимо неоцитотека, назначают пентаглобин. Длительность терапии зависит от доминирующей клиники, так при поражении ЦНС длительность лечения может превышать 6 недель.
Реабилитация заключается в контроле участковыми педиатрами или терапевтами. Для детей первых лет жизни эти осмотры осуществляются в 1,3,6 и 12 месяцев, а потом 1 раз в пол года, а дополнительные осмотры специалистов – по показаниям. Параллельно с осмотрами, проводят и контроль лабораторных данных: ОАК, мочи, маркёры ЦМВИ методом ИФА и ПЦР, моча и слюна ЦМК, иммунограмма, и остальные лабораторные анализы – по показаниям. В реабилитационную терапию входит охранительный режим, сбалансированное витаминизированное питание, обогащённое витаминами и микроэлементами.
Осложнения цитомегаловирусной инфекции
Осложнения также многообразны, как и клиника. Со стороны ЖКТ: гепатит, эзофагит, язвы, панкреатит, может привести к формируванию сахарного диабета 2 типа. Со стороны органов зрения – ретинит, который может привести к полной потери зрения. При поражении надпочечников может сформироваться надпочечниковая недостаточность. Которая проявляется стойкой гипотонией, гиперпигментацией кожи, анорексия, психоневрологические нарушения и т.д (в зависимости от того, какой слой поражён в наибольшей степени). При поражении слухового нерва, возникает сенсорноневральная глухота, возникающая у 60% больных активными формами. При поражении сердца возникает миокардит и/или дилатационная кардипатия. Это только часть возможных осложнений, и невозможно предугадать, какой орган будет поражён в той или иной степени, и какая клиника будет доминирующая.
Профилактика цитомегаловирусной инфекции
Вакцина против ЦМВИ не прошли лицензирования в отношении безопасности, поэтому основное значение имеет неспецифическая профилактика, которая заключается только в соблюдении личной гигиены и санитарно-профилактического режима при контакте с больным манифестной формой. Так для профилактики реактивации ЦМВИ у реципиентов трансплантантов, используют цитотек, ганцикловир, фоскарнет и ванцикловир.
[youtube.player]Цитомегаловирус (ЦМВ) или вирус герпеса 5 типа, – ДНК-содержащий вирус Cytomegalovirus hominis семейства Herpesviridae подсемейства Betaherpesvirinae. Цитомегаловирусная инфекция (ЦМВИ) человека – хроническая антропонозная болезнь вирусной этиологии, характеризующаяся многообразием форм патологического процесса и клинических проявлений – от латентной инфекции до клинически выраженного генерализованного заболевания. Заболевание ЦМВИ классифицируют в зависимости от сроков и механизмов заражения (врожденная и приобретенная инфекция, пренатальная, интранатальная и постнатальная), степени активности вируса (латентная, персистирующая и реактивированная инфекция), первичного или повторного заражения (острая инфекция, реактивация вируса и реинфекция).
Отличительными особенностями инфекции являются возможность ЦМВ персистировать во многих органах и способность его к инфицированию практически всех клеток организма человека, что предопределяет многообразие клинических проявлений, как при врожденной, так и приобретенной формах инфекции. ЦМВ рассматривается в качестве основного возбудителя внутриутробной инфекции, имеющей самые различные исходы: от инфицирования без реализации инфекции, формирования пороков развития и заболевания новорожденных до гибели плода и мертворождения.
ЦМВИ – типичный антропоноз. Источником инфекции является больной человек либо вирусоноситель. Пути передачи: вертикальный, половой, воздушнокапельный, фекально-оральный, артифициальный (парентеральный). Факторами передачи являются кровь, цервикальный и вагинальный секреты, сперма, женское молоко. Вирус выделяется с мочой, фекалиями, слюной, мокротой, в меньшей степени – со слезной жидкостью. Заражение может происходить также при переливании крови, трансплантации органов и тканей. Цитомегалия — широко распространенная инфекция, среди взрослого населения РФ у 73–98% обнаружены АТ-ЦМВ.
ЦМВИ относится к оппортунистическим инфекциям, особую опасность представляет для больных с иммунодефицитами различной природы. Иммуносупрессия приводит к реактивации латентной инфекции и развитию манифестных вариантов болезни с поражением различных органов и систем, способных привести к летальному исходу. Манифестная ЦМВИ занимает одно из первых мест в структуре оппортунистических заболеваний у ВИЧ-инфицированных пациентов. Данная патология встречается у 20–40% больных СПИДом, не получающих антиретровирусной терапии. Клинически выраженная ЦМВИ — одно из серьезных инфекционных осложнений при трансплантации органов, инфекция обостряет процессы, приводящие к реакции отторжения трансплантата.
При персистенции ЦМВ в организме человека выделяют две стадии, которые сменяют друг друга – продуктивную (с репликацией вируса) и латентную. Выход вируса из латентной стадии означает реактивацию, что может быть предопределено снижением иммунорезистентности либо появлением иных факторов, способствующих его репродукции. Выявление прямых маркеров репликации вируса (виремия, ДНК или АГ) свидетельствует о наличии инфекции.
При первичном заражении на 5–7 день вырабатываются АТ IgM, через 10–14 дней – низкоавидные АТ IgG, затем постепенно авидность этих АТ увеличивается, они становятся высокоавидными. АТ IgM исчезают через один месяц, низкоавидные АТ IgG – через 1–3 месяца, высокоавидные АТ IgG циркулируют в крови носителя пожизненно. При первичном инфицировании в стадии “серологического окна”, до начала синтеза АТ, происходит активная репликация вируса, в этот период единственным маркером инфекции является ДНК вируса в крови. При реактивации возможно появление АТ IgM и/или IgA, а также низкоавидных АТ IgG; в пик реактивации выявляются ДНК либо АГ ЦМВ в плазме крови.
Решающим условием антенатальной ЦМВИ является виремия у матери вследствие первичного или повторного заражением вирусом или его реактивации. ЦМВ способен преодолевать плацентарный барьер и поражать плод в различные сроки беременности, вызывая врожденную инфекцию. По данным различных авторов, активная форма ЦМВИ выявляется у женщин с отягощенным акушерским анамнезом в 35–60% случаев. Входными воротами для вируса в антенатальном и интранатальном периодах течения беременности могут быть плацента и плодные оболочки, в неонатальном периоде и позже – дыхательные пути и пищеварительный тракт, возможно заражение и через кровь.
ЦМВ обладает преимущественно нейротропным, эпителиотропным, гепатотропным и кардиотропным действием на плод. Его воздействие может быть и опосредованным, приводящим к различным нарушениям в плаценте: расстройству маточно- плацентарного кровообращения, отклонению в эволюционном формировании плаценты. Клиническим эквивалентом этих расстройств могут быть сокращение продолжительности беременности и преждевременное родоразрешение, рождение детей с симптомами перенесенной гипоксии или признаками внутриутробной гипотрофии, общая задержка внутриутробного развития.
Наибольшее значение для развития ранних перинатальных поражений плода имеет гематогенный путь инфицирования. Кроме того, для интранатальных и более поздних поражений характерными являются вертикальный и контактный пути передачи ЦМВ, нередки также случаи смешанного инфицирования. Острая ЦМВИ может протекать в виде генерализованной формы с присоединением вторичных инфекций и иметь летальный исход уже в первые недели жизни ребенка. При инфицировании плода во время реактивации латентной ЦМВИ чаще имеют место поздние проявления инфекции в виде нарушений зрения, слуха, задержки психического развития, двигательных нарушений. При отсутствии выраженных иммунологических нарушений острая ЦМВИ переходит в латентную с пожизненным присутствием вируса в организме человека. Развитие иммуносупрессии, в частности связанной с ВИЧ-инфекцией, ведет к возобновлению репликации ЦМВ, появлению вируса в крови и манифестации заболевания. Летальность больных ВИЧ-инфекцией, страдающих ЦМВИ, составляет 25–27%.
Клинический диагноз ЦМВ-инфекции требует обязательного лабораторного подтверждения. Выявление в крови пациента АТ-ЦМВ IgМ и/или IgG недостаточно ни для установления факта активной репликации ЦМВ, ни для подтверждения манифестной формы заболевания.
Показания к обследованию
- Женщины, планирующие беременность;
- женщины с отягощенным акушерским анамнезом (перинатальные потери, рождение ребенка с врожденными пороками развития);
- беременные женщины (в первую очередь имеющие УЗИ-признаки внутриутробной инфекции, лимфоаденопатии, лихорадку, гепатит и гепатоспленомегалию неясного генеза);
- беременные женщины с иммунодефицитом, в т. ч. с ВИЧ-инфекцией;
- матери, родившие ребенка с признаками внутриутробной инфекцией или врожденными пороками развития;
- дети, имеющие симптоматику врожденной инфекции, пороки развития или рожденные женщинами из группы риска по внутриутробной передаче ЦМВ;
- пациенты (в первую очередь новорожденные) с сепсисом, гепатитами, менингоэнцефалитом, пневмонией, поражением ЖКТ;
- пациенты с наличием иммунодефицита с клинической картиной органных или генерализованных поражений.
- Врожденная ЦМВИ – краснуха, токсоплазмоз, неонатальный герпес, сифилис, бактериальная инфекция, гемолитическая болезнь новорожденных, родовая травма, наследственные синдромы;
- мононуклеозоподобное заболевание – инфекции, вызываемые вирусом Эпштейна-Барр, герпес-вирусами 6 и 7 типов, острая ВИЧ-инфекция, стрептококковый тонзиллит, дебют острого лейкоза;
- заболевание органов дыхания у детей раннего возраста – коклюш, бактериальный трахеит или трахеобронхит, РС-вирусной инфекция, герпетический трахеобронхит;
- у больных с иммунодефицитом – пневмоцистная пневмония, туберкулез, токсоплазмоз, микоплазменная пневмония, грибковые и герпетические инфекции, бактериальный сепсис, лимфопролиферативные заболевания, ВИЧ-энцефалит, нейросифилис, прогрессирующая многоочаговая лейкоэнцефалопатия;
- полинейропатия и полирадикулопатия – полирадикулопатия, вызванная герпесвирусами 2 и 6 типов, синдром Гийена-Барре, токсическая полинейропатия, связанная с приемом лекарственных средств, алкоголя, наркотических психотропных веществ.
Этиологическая лабораторная диагностика включает микроскопические исследования, выявление возбудителя в культуре клеток, обнаружение АГ или ДНК, определение АТ IgM, IgА, IgG, авидности АТ IgG.
Материал для исследования
- Кровь (сыворотка, плазма), лейкоциты крови, моча, слюна, СМЖ – культуральные исследования, выявление ДНК;
- пуповинная кровь, амниотическая жидкость – выявление ДНК;
- слюна, моча – выявление АГ;
- сыворотка/плазма крови – определение АТ.
Для обнаружения АГ вируса в слюне и моче используют метод РИФ, по количеству светящихся клеток можно приблизительно оценить интенсивность выделения вируса. В связи с персистенцией ЦМВ обнаружение АГ не указывает на активность инфекционного процесса, для ее оценки требуются дополнительные исследования – выявление отдельных АГ вируса (р55, рр65 и др.).
При проведении микроскопического исследования (световая микроскопия) основными морфологическими признаками ЦМВИ являются гигантские клетки с внутриядерными включениями (цитомегалы). Их можно обнаружить в эпителии почечных канальцев, желчных протоках, выводных протоках слюнных желез, поджелудочной железы, ткани легких, клетках глии, нейронах, эндотелиоцитах. Наличие таких клеток указывает на репродукцию вируса, однако они обнаруживаются не во всех случаях активной инфекции. Диагностическая чувствительность метода не превышает 50%.
Определение специфических АТ к вирусу помогает в распознавании заражения человека ЦМВ, но ввиду длительного периода нарастания титра АТ от момента инфицирования, последующего долгого сохранения их в крови, трансплацентарного перехода АТ IgG от матери к плоду (выявляются у ребенка до 1,5 лет) диагностическая ценность исследования ограничена. При наблюдении в динамике (2–4 недели) повышение титра АТ IgG в 4 раза указывает на активную ЦМВИ. Однако необходимость длительного периода наблюдения (до 4 недель) и возможность сохранения повышенного титра АТ на протяжении ряда лет лимитирует использование такого подхода к диагностике.
Дополнительным исследованием при поражении мозга, вызванного ЦМВ, может быть параллельное обнаружение АТ IgG в периферической крови и СМЖ методом ИФА с последующим расчетом их соотношения. Значение соотношения позволяет выявить интратекальную продукцию АТ и соответственно вовлечение в инфекционный процесс ЦНС.
Иммуноблот позволяет детектировать АТ IgM и IgG к отдельным белкам ЦМВ, подтвердить специфичность исследования, следить в динамике за появлением и исчезновением отдельных белков, что имеет высокое диагностическое и прогностическое значение. Наличие АТ к отдельным АГ вируса подтверждает формирование иммунного ответа к ЦМВ.
Показания к применению различных лабораторных исследований и интерпретация их результатов у разных категорий обследуемых
Диагностика первичного заражения, в т. ч. в период беременности, возможна только у пациентов, в крови которых отсутствуют АТ-ЦМВ. Независимо от клинических вариантов заболевания, при первичной ЦМВИ выявляются прямые (присутствие вируса, его ДНК или АГ) и косвенные (АТ-ЦМВ) лабораторные маркеры активной репликации ЦМВ. При обследовании больных при подозрении на активную ЦМВИ и манифестную форму заболевания (ЦМВ-болезнь) необходимо количественное определение содержания ДНК ЦМВ в крови. Определение ДНК ЦМВ в ликворе, плевральной жидкости, БАЛЖ, биоптатах бронхов, биоптатов органов выполняют при наличии соответствующей органной патологии.
Выявление прямых маркеров репликации вируса (виремия, ДНК или АГ) свидетельствует о наличии инфекции. Выявление ДНК ЦМВ или АГ вируса в крови беременной женщины – основной маркер высокого риска заражения плода и развития врожденной ЦМВИ.
Отсутствие АТ-ЦМВ IgM, IgА и IgG означает отсутствие ЦМВ в организме. Однако у лиц с выраженным иммунодефицитом при активной репликации ЦМВ продукция специфических АТ может быть снижена до неопределяемого уровня.
Выявление АТ-ЦМВ разных классов позволяет определить фазы инфекционного процесса (репликативная или латентная). АТ IgM чаще оценивают как маркер первичной герпес-вирусной инфекции. При выявлении АТ IgM для подтверждения инфицирования ЦМВ рекомендуются дополнительные исследования: определение АТ IgА или авидности АТ IgG, выявление АТ к отдельным белкам с использованием иммуноблота; повторное обследование женщины или ребенка через 2 недели. Выявление АТ IgА и(или) низкоавидных АТ IgG подтверждает наличие инфекции. При повторном выявлении АТ IgM и отсутствии IgА и(или) низкоавидных IgG результат выявления АТ IgM считают ложноположительным.
Выявление АТ IgM и IgG к предранним белкам-антигенам и низкоавидных АТ IgG свидетельствует о первичном инфекционном процессе.
Обнаружение только АТ IgG не позволяет охарактеризовать период заболевания. При наличии иммуносупрессии классического (4-х кратного) увеличения АТ IgG во время рецидива не наблюдают.
Установление факта инфицирования плода осуществляется на основании обнаружения ДНК ЦМВ. Выбор биологического материала определяется с учетом срока гестации, обусловливающего возможность проведения того или иного метода инвазивной пренатальной диагностики: амниотическая жидкость – 16–23 недели, пуповинная кровь – 20–24 недели. Косвенным подтверждением факта инфицирования плода является обнаружение АТ IgM и/или АТ IgА в пуповинной крови (проведение исследования возможно с 22 недели беременности).
Лабораторная диагностика врожденной ЦМВИ основана на обнаружении ЦМВ, его ДНК или АГ в различном биологическом материале (периферическая кровь, моча, слюна, смывы и мазки от ротоглотки, СМЖ) и выявлении в сыворотке или плазме крови АТ IgМ и IgА в течение первых 7 дней после рождения. Проведение исследования в более поздние сроки не позволяет дифференцировать врожденную и приобретенную инфекцию. Выявление ДНК ЦМВ или АГ вируса в крови, моче, соскобах со слизистой ротовой полости через 4–6 недель жизни ребенка при отсутствии вируса в первые 2 недели говорит об интранатальном или раннем постанатальном заражении. Подтверждением манифестной ЦМВИ у детей первых месяцев жизни является наличие ДНК ЦМВ в крови.
При сомнительных результатах дополнительную диагностическую информацию может дать выявление АТ IgМ к отдельным белкам-антигенам вируса методом иммуноблота. Отсутствие АТ-ЦМВ у детей с врожденной ЦМВИ может быть связано с развитием иммунологической толерантности к АГ вируса цитомегалии (инфицирование ЦМВ не сопровождается эффективным синтезом АТ-ЦМВ).
Выявление АТ IgG в сыворотке крови новорожденного без сопоставления с уровнем АТ в крови матери не является диагностически значимым вследствие возможности их трансплацентарного переноса из материнского организма. Только при динамическом (с интервалом в 14–21 день) сравнении уровня АТ IgG новорожденного ребенка с уровнем АТ IgG в крови матери можно судить об их природе. Если титры АТ IgG у ребенка при рождении равны материнским, а при повторном исследовании через 3–4 недели снижаются приблизительно в 1,5–2 раза, то АТ, выявленные у ребенка, являются материнскими.
Скрининг беременных женщин – выявление АТ IgМ и низкоавидных АТ IgG. Для исключения реактивации целесообразно определение АТ IgА и низкоавидных АТ IgG.
Обследование больных с наличием иммунодефицита при подозрении на активную ЦМВИ и манифестную форму заболевания (ЦМВ-болезнь) включает гистологическое исследование биопсийных материалов для выявление цитомегалов (окраска гематоксилином и эозином), обнаружение ДНК ЦМВ в ликворе, плевральной жидкости, БАЛ, биоптатах бронхов, биоптатов внутренних органов при наличии соответствующей органной патологии; выявление АГ ЦМВ в крови, определение концентрации ДНК ЦМВ в крови методом ПЦР. В диагностике ЦМВИ у ВИЧинфицированных наиболее информативно наличие в крови ДНК ЦМВ в высокой концентрации (в плазме крови >10000 копий/мл, в лейкоцитах > 1000 копий/ 105 лейкоцитов).
Продолжая использовать наш сайт, вы даете согласие на обработку файлов cookie, пользовательских данных (сведения о местоположении; тип и версия ОС; тип и версия Браузера; тип устройства и разрешение его экрана; источник откуда пришел на сайт пользователь; с какого сайта или по какой рекламе; язык ОС и Браузера; какие страницы открывает и на какие кнопки нажимает пользователь; ip-адрес) в целях функционирования сайта, проведения ретаргетинга и проведения статистических исследований и обзоров. Если вы не хотите, чтобы ваши данные обрабатывались, покиньте сайт.
Copyright ФБУН Центральный НИИ Эпидемиологии Роспотребнадзора, 1998 - 2020

! Продолжая использовать наш сайт, вы даете согласие на обработку файлов cookie, пользовательских данных (сведения о местоположении; тип и версия ОС; тип и версия Браузера; тип устройства и разрешение его экрана; источник откуда пришел на сайт пользователь; с какого сайта или по какой рекламе; язык ОС и Браузера; какие страницы открывает и на какие кнопки нажимает пользователь; ip-адрес) в целях функционирования сайта, проведения ретаргетинга и проведения статистических исследований и обзоров. Если вы не хотите, чтобы ваши данные обрабатывались, покиньте сайт.
[youtube.player]Читайте также:


