Дисбактериоз кишечника пособие для врачей
Что понимают под дисбактериозом? Какие методы диагностики являются современными и достоверными? Какие лекарственные препараты применяются при дисбактериозе? Вкишечнике человека находится свыше 500 различных видов микробов, общее количество которых
Вкишечнике человека находится свыше 500 различных видов микробов, общее количество которых достигает 10 14 , что на порядок выше общей численности клеточного состава человеческого организма. Количество микроорганизмов увеличивается в дистальном направлении, и в толстой кишке в 1 г кала содержится 10 11 бактерий, что составляет 30% сухого остатка кишечного содержимого.
В тощей кишке здоровых людей находится до 10 5 бактерий в 1 мл кишечного содержимого. Основную массу этих бактерий составляют стрептококки, стафилококки, молочнокислые палочки, другие грамположительные аэробные бактерии и грибы. В дистальном отделе подвздошной кишки количество микробов увеличивается до 10 7 –10 8 , в первую очередь за счет энтерококков, кишечной палочки, бактероидов и анаэробных бактерий. Недавно нами было установлено, что концентрация пристеночной микрофлоры тощей кишки на 6 порядков выше, чем в ее полости, и составляет 10 11 кл/мл. Около 50% биомассы пристеночной микрофлоры составляют актиномицеты, примерно 25% — аэробные кокки (стафилококки, стрептококки, энтерококки и коринеформные бактерии), от 20 до 30% приходится на бифидобактерии и лактобациллы.
Количество анаэробов (пептострептококки, бактероиды, клостридии, пропионобактерии) составляет около 10% в тонкой и до 20% в толстой кишке. На долю энтеробактерий приходится 1% от суммарной микрофлоры слизистой оболочки.
До 90-95% микробов в толстой кишке составляют анаэробы (бифидобактерии и бактероиды), и только 5-10% всех бактерий приходится на строгую аэробную и факультативную флору (молочнокислые и кишечные палочки, энтерококки, стафилококки, грибы, протей).
Кишечные палочки, энтерококки, бифидобактерии и ацидофильные палочки обладают выраженными антагонистическими свойствами. В условиях нормально функционирующего кишечника они способны подавлять рост несвойственных нормальной микрофлоре микроорганизмов.
Площадь внутренней поверхности кишечника составляет около 200 м 2 . Она надежно защищена от проникновения пищевых антигенов, микробов и вирусов. Важную роль в организации этой защиты играет иммунная система организма. Около 85% лимфатической ткани человека сосредоточено в стенке кишечника, где продуцируется секреторный IgA. Кишечная микрофлора стимулирует иммунную защиту. Кишечные антигены и токсины кишечных микробов значительно увеличивают секрецию IgA в просвет кишки.
Расщепление непереваренных пищевых веществ в толстой кишке осуществляется ферментами бактерий, при этом образуются разнообразные амины, фенолы, органические кислоты и другие соединения. Токсические продукты микробного метаболизма (кадаверин, гистамин и другие амины) выводятся с мочой и в норме не оказывают влияния на организм. При утилизации микробами неперевариваемых углеводов (клетчатки) образуются короткоцепочечные жирные кислоты. Они обеспечивают клетки кишки энергоносителями и, следовательно, улучшают трофику слизистой оболочки. При дефиците клетчатки может нарушаться проницаемость кишечного барьера вследствие дефицита короткоцепочечных жирных кислот. В результате кишечные микробы могут проникать в кровь.
Под влиянием микробных ферментов в дистальных отделах подвздошной кишки происходит деконъюгация желчных кислот и преобразование первичных желчных кислот во вторичные. В физиологических условиях от 80 до 95% желчных кислот реабсорбируется, остальные выделяются с фекалиями в виде бактериальных метаболитов. Последние способствуют нормальному формированию каловых масс: тормозят всасывание воды и тем самым препятствуют излишней дегидратации кала.
В понятие дисбактериоза кишечника входит избыточное микробное обсеменение тонкой кишки и изменение микробного состава толстой кишки. Нарушение микробиоценоза происходит в той или иной степени у большинства больных с патологией кишечника и других органов пищеварения. Следовательно, дисбактериоз является бактериологическим понятием. Он может рассматриваться как одно из проявлений или осложнение заболевания, но не самостоятельная нозологическая форма.
Крайней степенью дисбактериоза кишечника является появление бактерий желудочно-кишечного тракта в крови (бактериемия) или даже развитие сепсиса.
Состав микрофлоры кишечника нарушается при болезнях кишечника и других органов пищеварения, лечении антибиотиками и иммунодепрессантами, воздействиях вредных факторов внешней среды.
Клинические проявления дисбактериоза зависят от локализации дисбиотических изменений.
При дисбактериозе тонкой кишки численность одних микробов в слизистой оболочке тонкой кишки увеличена, а других уменьшена. Отмечается увеличение Eubacterium (в 30 раз), α-стрептококков (в 25 раз), энтерококков (в 10 раз), кандид (в 15 раз), появление бактерий рода Acinetobacter и вирусов герпеса. Уменьшается от 2 до 30 раз количество большинства анаэробов, актиномицетов, клебсиелл и других микроорганизмов, являющихся естественными обитателями кишечника.
Причиной дисбактериоза могут быть: а) избыточное поступление микроорганизмов в тонкую кишку при ахилии и нарушении функции илеоцекального клапана; б) благоприятные условия для развития патологических микроорганизмов в случаях нарушения кишечного пищеварения и всасывания, развития иммунодефицита и нарушений проходимости кишечника.
Повышенная пролиферация микробов в тонкой кишке приводит к преждевременной деконъюгации желчных кислот и потере их с калом. Избыток желчных кислот усиливает моторику толстой кишки и вызывает диарею и стеаторею, а дефицит желчных кислот приводит к нарушению всасывания жирорастворимых витаминов и развитию желчнокаменной болезни.
Бактериальные токсины и метаболиты, например фенолы и биогенные амины, могут связывать витамин В12.
Некоторые микроорганизмы обладают цитотоксическим действием и повреждают эпителий тонкой кишки. Это ведет к уменьшению высоты ворсинок и углублению крипт. При электронной микроскопии выявляется дегенерация микроворсинок, митохондрий и эндоплазматической сети.
Состав микрофлоры толстой кишки может меняться под влиянием различных факторов и неблагоприятных воздействий, ослабляющих защитные механизмы организма (экстремальные климатогеографические условия, загрязнение биосферы промышленными отходами и различными химическими веществами, инфекционные заболевания, болезни органов пищеварения, неполноценное питание, ионизирующая радиация).
В развитии дисбактериоза толстой кишки большую роль играют ятрогенные факторы: применение антибиотиков и сульфаниламидов, иммунодепрессантов, стероидных гормонов, рентгенотерапия, хирургические вмешательства. Антибактериальные препараты значительно подавляют не только патогенную микробную флору, но и рост нормальной микрофлоры в толстой кишке. В результате размножаются микробы, попавшие извне, или эндогенные виды, устойчивые к лекарственным препаратам (стафилококки, протей, дрожжевые грибы, энтерококки, синегнойная палочка).
Клинические проявления чрезмерного роста микроорганизмов в тонкой кишке могут полностью отсутствовать, выступать в качестве одного из патогенетических факторов хронической рецидивирующей диареи, а при некоторых болезнях, например, дивертикулезе тонкой кишки, частичной кишечной непроходимости или после хирургических операций на желудке и кишечнике, приводить к тяжелой диарее, стеаторее и В 12 -дефицитной анемии.
Особенностей клинического течения заболевания у больных с различными вариантами дисбактериоза толстой кишки, по данным бактериологических анализов кала, в большинстве случаев установить не удается. Можно отметить, что больные хроническими заболеваниями кишечника чаще инфицируются острыми кишечными инфекциями по сравнению со здоровыми. Вероятно, это связано со снижением у них антагонистических свойств нормальной микрофлоры кишечника и, прежде всего, частым отсутствием бифидобактерий.
Особенно большую опасность представляет псевдомембранозный колит, развивающийся у некоторых больных, длительно лечившихся антибиотиками широкого спектра действия. Этот тяжелый вариант дисбактериоза вызывается токсинами, выделяемыми синегнойной палочкой Clostridium difficile, которая размножается в кишечнике при угнетении нормальной микробной флоры.
Очень редко наблюдается молниеносное течение псевдомембранозного колита, напоминающее холеру. Обезвоживание развивается в течение нескольких часов и заканчивается летальным исходом.
Таким образом, оценка клинической значимости дисбиотических изменений должна основываться прежде всего на клинических проявлениях, а не только на результатах исследования микрофлоры кала.
Диагностика дисбактериоза представляет собой сложную и трудоемкую задачу. Для диагностики дисбактериоза тонкой кишки применяют посев сока тонкой кишки, полученного с помощью стерильного зонда. Дисбактериоз толстой кишки выявляют с помощью бактериологических исследований кала.
Микробная флора образует большое количество газов, в том числе водорода. Это явление используют для диагностики дисбактериоза. Концентрация водорода в выдыхаемом воздухе натощак находится в прямой зависимости от выраженности бактериального обсеменения тонкой кишки. У больных с заболеваниями кишечника, протекающими с хронической рецидивирующей диареей и бактериальным обсеменением тонкой кишки, концентрация водорода в выдыхаемом воздухе значительно превышает 15 ppm.
Для диагностики дисбактериоза применяют также нагрузку лактулозой. В норме лактулоза не расщепляется в тонкой кишке и метаболизируется микробной флорой толстой кишки. В результате количество водорода в выдыхаемом воздухе повышается (рис. 1).
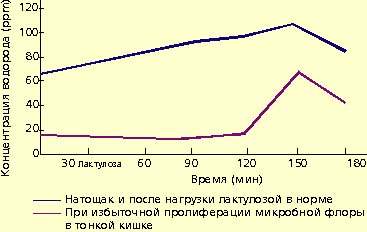 |
| Рисунок 1. Концентрация водорода в выдыхаемом воздухе |
Наиболее частыми бактериологическими признаками дисбактериоза толстой кишки являются отсутствие основных бактериальных симбионтов — бифидобактерий и уменьшение количества молочнокислых палочек. Увеличивается количество кишечных палочек, энтерококков, клостридий, стафилококков, дрожжеподобных грибов и протея. У отдельных бактериальных симбионтов появляются патологические формы. К ним относятся гемолизирующая флора, кишечные палочки со слабо выраженными ферментативными свойствами, энтеропатогенные кишечные палочки и т. д.
Углубленное изучение микробиоценоза показало, что традиционные методы не позволяют получить истинную информацию о состоянии микрофлоры кишечника. Из 500 известных видов микробов в целях диагностики обычно изучаются лишь 10-20 микроорганизмов. Важно, в каком отделе — в тощей, подвздошной или толстой кишках — исследуется микробный состав. Поэтому перспективы разработки клинических проблем дисбактериоза в настоящее время связывают с применением химических методов дифференциации микроорганизмов, позволяющих получить универсальную информацию о состоянии микробиоценоза. Наиболее широко для этих целей используются газовая хроматография (ГХ) и газовая хроматография в сочетании с масс-спектрометрией (ГХ-МС). Этот метод позволяет получить уникальную информацию о составе мономерных химических компонентов микробной клетки и метаболитов. Маркеры такого рода могут быть определены и использованы для детектирования микроорганизмов. Главным преимуществом и принципиальным отличием этого метода от бактериологических является возможность количественного определения более 170 таксонов клинически значимых микроорганизмов в различных средах организма. При этом результаты исследования могут быть получены в течение нескольких часов.
Проведенные нами исследования микробиоценоза в крови и биоптатов слизистой оболочки тонкой и толстой кишок у больных с синдромом раздраженного кишечника позволили обнаружить отклонения от нормы до 30-кратного увеличения или уменьшения многих компонентов. Существует возможность оценки изменений микрофлоры кишечника на основании данных анализа крови методом ГХ-МС-микробных маркеров.
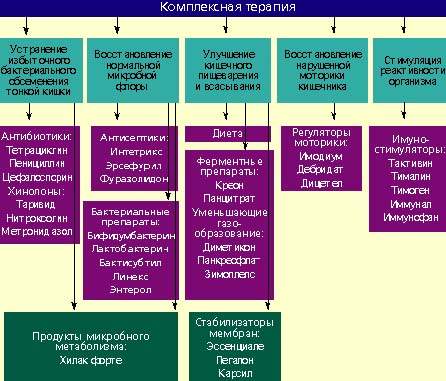 |
Лечение дисбактериоза должно быть комплексным (схема) и включать в себя следующие мероприятия:
- устранение избыточного бактериального обсеменения тонкой кишки;
- восстановление нормальной микробной флоры толстой кишки;
- улучшение кишечного пищеварения и всасывания;
- восстановление нарушенной моторики кишечника;
- стимулирование реактивности организма.
Антибактериальные препараты необходимы в первую очередь для подавления избыточного роста микробной флоры в тонкой кишке. Наиболее широко применяются антибиотики из группы тетрациклинов, пенициллинов, цефалоспорины, хинолоны (таривид, нитроксолин) и метронидазол.
Однако антибиотики широкого спектра действия в значительной степени нарушают эубиоз в толстой кишке. Поэтому они должны применяться только при заболеваниях, сопровождающихся нарушениями всасывания и моторики кишечника, при которых, как правило, отмечается выраженный рост микробной флоры в просвете тонкой кишки.
Антибиотики назначают внутрь в обычных дозах в течение 7–10 дней.
При заболеваниях, сопровождающихся дисбактериозом толстой кишки, лечение лучше проводить препаратами, которые оказывают минимальное влияние на симбионтную микробную флору и подавляют рост протея, стафилококков, дрожжевых грибов и других агрессивных штаммов микробов. К ним относятся антисептики: интетрикс, эрсефурил, нитроксолин, фуразолидон и др.
При тяжелых формах стафилококкового дисбактериоза применяют антибиотики: таривид, палин, метронидазол (трихопол), а также бисептол-480, невиграмон.
Антибактериальные препараты назначают в течение 10–14 дней. В случае появления в кале или кишечном соке грибов показано применение нистатина или леворина.
У всех больных с диареей, ассоциированной с антибиотиками, протекающей с интоксикацией и лейкоцитозом, возникновение острой диареи следует связывать с Cl. difficile.
В этом случае срочно делают посев кала на Cl. difficile и назначают ванкомицин по 125 мг внутрь 4 раза в сутки; при необходимости доза может быть увеличена до 500 мг 4 раза в день. Лечение продолжают в течение 7-10 суток. Эффективен также метронидазол в дозе 500 мг внутрь 2 раза в сутки, бацитрацин по 25 000 МЕ внутрь 4 раза в сутки. Бацитрацин почти не всасывается, в связи с чем в толстой кишке можно создать более высокую концентрацию препарата. При обезвоживании применяют адекватную инфузионную терапию для коррекции водно-электролитного баланса. Для связывания токсина Cl. difficile используют холестирамин (квестран).
Живые культуры нормальной микробной флоры выживают в кишечнике человека от 1 до 10% от общей дозы и способны в какой-то мере выполнять физиологическую функцию нормальной микробной флоры. Бактериальные препараты можно назначать без предварительной антибактериальной терапии или после нее. Применяют бифидумбактерин, бификол, лактобактерин, бактисубтил, линекс, энтерол и др. Курс лечения длится 1-2 месяца.
Возможен еще один способ устранения дисбактериоза — воздействие на патогенную микробную флору продуктами метаболизма нормальных микроорганизмов. К таким препаратам относится хилак форте. Он создан 50 лет назад и до настоящего времени применяется для лечения больных с патологией кишечника. Хилак форте представляет собой стерильный концентрат продуктов обмена веществ нормальной микрофлоры кишечника: молочной кислоты, лактозы, аминокислот и жирных кислот. Эти вещества способствуют восстановлению в кишечнике биологической среды, необходимой для существования нормальной микрофлоры, и подавляют рост патогенных бактерий. Возможно, продукты метаболизма улучшают трофику и функцию эпителиоцитов и колоноцитов. 1 мл препарата соответствует биосинтетическим активным веществам 100 млрд. нормальных микроорганизмов. Хилак форте назначают по 40–60 капель 3 раза в день на срок до 4 недель в сочетании с препаратами антибактериального действия или после их применения.
Совсем недавно появились сообщения о возможности лечения острой диареи, ассоциированной с антибактериальной терапией и Cl. difficile, большими дозами пре- и пробиотиков.
У больных с нарушением полостного пищеварения применяют креон, панцитрат и другие панкреатические ферменты. С целью улучшения функции всасывания назначают эссенциале, легалон или карсил, т. к. они стабилизируют мембраны кишечного эпителия. Пропульсивную функцию кишечника улучшают имодиум (лоперамид) и тримебутин (дебридат).
Для повышения реактивности организма ослабленным больным целесообразно применять тактивин, тималин, тимоген, иммунал, иммунофан и другие иммуностимулирующие средства. Курс лечения должен составлять в среднем 4 недели. Одновременно назначаются витамины.
Первичная профилактика дисбактериоза представляет очень сложную задачу. Ее решение связано с общими профилактическими проблемами: улучшением экологии, рациональным питанием, улучшением благосостояния и прочими многочисленными факторами внешней и внутренней среды.
Вторичная профилактика предполагает рациональное применение антибиотиков и других медикаментов, нарушающих эубиоз, своевременное и оптимальное лечение болезней органов пищеварения, сопровождающихся нарушением микробиоценоза.
Похожие темы научных работ по ветеринарным наукам , автор научной работы — Яковенко Э. П.
Кафедра гастроэнтерологии ФУВ РГМУ
Микрофлора пищеварительного тракта
Микрофлора желудочно-кишечного тракта (ЖКТ) представляет собой сложную экологическую систему, ведущая роль которой состоит в защите организма от колонизации патогенных и условно патогенных бактерий. Кишечная микрофлора подразделяется на облигатную (синонимы: главная, резидентная, индигенная, аутохтон-ная), факультативную (сапрофитная и условно патогенная) и транзиторную (случайная).
В состав облигатной микрофлоры входят анаэробы (бифидобактерии, пропионо-бактерии, пептострептококки) и аэробы (лактобактерии, энтерококки, кишечные палочки).
Факультативная микрофлора представлена сапрофитами: бактероиды, пептококки, стафилококки, стрептококки, аэробные и анаэробные бациллы, дрожжевые грибы. К условно патогенным энтеробактериям относятся клебсиеллы, протеи, цитробак-теры, энтеробактеры и др.
Основная масса бактерий фиксирована к специфическим рецепторам эпителиоци-тов слизистой оболочки ЖКТ (пристеночная или мукозная микрофлора), образуя микроколонии, покрытые биопленкой. Незначительная часть нормальной кишечной микрофлоры находится внутри просвета кишки. В слизистой оболочке тонкой кишки имеются рецепторы для адгезии только аэробной флоры, а в толстой кишке преобладают рецепторы для фиксации анаэробов.
В двенадцатиперстной, тощей и начальных отделах подвздошной кишки общее число бактерий составляет 103—104 клеток в 1 г кишечного содержимого. Важно отметить, что в данном биотопе практически отсутствуют облигатно анаэробные бактерии, а также представители семейства энтеробактерий (в первую очередь, кишечная палочка). В тонкой кишке микроорганизмы локализуются преимущественно пристеночно. В дистальных отделах тонкой кишки концентрация микроорганизмов возрастает до 105—109 клеток в 1 г, и к биоценозу присоединяются облигатные анаэробы (бактероиды, бифидобактерии и др.).
Толстая кишка является основным местом обитания нормальной кишечной флоры. В данном биотопе обнаруживаются бактероиды в количестве 1010—1012 клеток в
1 г, бифидобактерии (108—1010), энтерококки и клостридии (107—108), лактобациллы (106—109), кишечные палочки (106—108), стрептококки и кандиды (104—105), стафилококки (102—104) и ряд других бактерий.
Стабильность состава кишечной микрофлоры у здорового человека поддерживается с участием ряда механизмов. К ведущим факторам макроорганизма, лимитирующим бактериальный рост в тонкой кишке, относятся секреция соляной кислоты и кишечная моторика. На состав кишечной микрофлоры определенное влияние оказывают целостность слизистой оболочки кишечника, секреция слизи, пищеварительных ферментов, иммуноглобулинов (особенно секреторного IgА), объем десквамированного кишечного эпителия, а также компоненты пищи. К факторам бак-------------------Лечебное дело 3.2004
терий, поддерживающим их нормальный состав в кишке, относятся: конкуренция за использование питательных веществ, изменение внутрипросветного уровня рН, продукция токсичных метаболитов, энзимов, антибиотиков типа “колицинов”, утилизация кислорода аэробами.
Нормальные кишечные бактерии не проникают во внутреннюю среду организма благодаря барьерной функции слизистых оболочек ЖКТ. Кишечная цитопротекция включает преэпителиальный, эпителиальный и постэпителиальный защитные слизистые барьеры.
Основными компонентами преэпители-ального защитного барьера являются слизь; иммуноглобулины А1 и А2, связанные с гликопротеинами слизи; гликокаликс с его нормальными реологическими параметрами, обеспечивающими резистентность эпителия к бактериальным и химическим агентам; ряд низкомолекулярных кишечных метаболитов, обеспечивающих колонизационную резистентность слизистой оболочки к условно патогенным и патогенным микроорганизмам.
Эпителиальный защитный барьер включает апикальные клеточные мембраны и тесные межклеточные соединения, блокирующие пассаж макромолекул в клетку и препятствующие их межклеточному проникновению.
В состав постэпителиального барьера входит кровоток, обеспечивающий фагоцитоз, гуморальные иммунные реакции и другие механизмы защиты, а также функционирование преэпителиального и эпителиального барьеров. Большую защитную роль выполняет кишечная лимфатическая система, включающая внутриэпителиальные Т-лим-фоциты, пейеровы бляшки и собственную пластинку слизистой оболочки кишки, а также ряд регуляторных субстанций (про-стагландины, энкефалины, факторы роста, секретин и др.), которые усиливают защитные функции слизистого барьера.
Функции микрофлоры ЖКТ
Нормальная кишечная микрофлора выполняет ряд важных функций в организме человека. Она является антагонистичной по отношению к патогенной и условно патогенной микрофлоре, что предупреждает развитие острых кишечных инфекций.
Кишечная микрофлора синтезирует витамины (Вр В2, Вб, К, фолиевую, никотиновую кислоту и др.); способствует активации иммунных реакций, создавая иммунологическую резистентность.
Кишечные бактерии участвуют в процессах пищеварения, в первую очередь в гидролизе клетчатки. Компоненты пищи расщепляются широким спектром бактериальных полисахаридаз, гликозидаз, протеаз и пептидаз до олигомеров глюкозы и аминокислот. Последние, в свою очередь, ферментируются до короткоцепочечных жирных кислот, водорода, углекислого газа и других продуктов. Конечные продукты гидролиза оказывают различное действие на функцию толстой кишки: стимулируют моторику, способствуют задержке жидкости в просвете кишки. Органические кислоты, всасываясь в толстой кишке, увеличивают энергетический потенциал макроорганизма. Бактериальная продукция Б-лак-тата может приводить к накоплению в крови Б-молочной кислоты, вызывающей развитие состояния, похожего на алкогольную интоксикацию. Продукты микробного гидролиза белка — аммиак, амины, индол, скатол — усиливают эндогенную интоксикацию.
Микрофлора разрушает пищеварительные ферменты, различные стеролы и стероиды, включая холестерин, деконъюги-рованные желчные кислоты, андрогены и эстрогены. Учитывая, что эти вещества включаются в энтерогепатическую циркуляцию, разрушение их микрофлорой приводит к уменьшению в крови уровней андрогенов и эстрогенов и повышению уровня холестерина.
Понятие дисбактериоза кишечника
Причины нарушения кишечного биоценоза разнообразны. Основными из них являются болезни ЖКТ, неполноценные диеты, перенесенные острые кишечные инфекции, лекарства (включая антибиотики), которые нарушают иммунный статус кишки и ее моторику.
Термин “дисбактериоз кишечника” (ДБК) включает:
1) изменение количественного и качественного состава микрофлоры в различных биотопах (тонкая и толстая кишка);
2) появление факультативных (условно патогенных) штаммов, не входящих в состав резидентной микрофлоры: Proteus, Morganella, Klebsiella, Enterobacter, Citrobacter, Hafnia, E. coli (с ферментативной недостаточностью или гемолизирующими свойствами), Pseudomonas и др.
Следует отметить, что ДБК (синонимы: избыточный бактериальный рост в кишечнике, дисбиоз кишечника и др.) не является самостоятельным заболеванием, но сопровождается развитием ряда симптомов и синдромов, которые вносят свою лепту в клиническую картину болезней органов пищеварения и других органов.
Клинические проявления и патогенез
Клинические проявления ДБК включают местные (кишечные) симптомы и синдромы, а также системные нарушения, обусловленные транслокацией кишечной микрофлоры и ее токсинов во внутреннюю среду макроорганизма, нарушением процессов всасывания, иммунологическими нарушениями и др.
Формирование кишечных проявлений ДБК обусловлено тремя механизмами.
Первый из них связан с продукцией органических кислот, которые повышают ос-молярность кишечного содержимого и сни-
приводит к задержке жидкости в просвете кишки. Клинические симптомы: боли в животе, метеоризм, осмотическая диарея, которая уменьшается или купируется после 24—48 ч голодания, потеря массы тела.
Второй фактор — бактериальная деконъюгация желчных кислот, гидроксилирование жирных кислот, с которыми связана стимуляция интестинальной секреции воды и электролитов, а также химические повреждения слизистой оболочки. Клинические проявления: секреторная диарея, которая не купируется после 24-часового голодания, воспаление и эрозии слизистой оболочки. Оба вышеуказанных механизма приводят к снижению содержания и активности внутрипросветных и пристеночных ферментов за счет падения внутрикишеч-ного уровня рН, разрушения ферментов бактериями, снижения их концентрации в результате разведения кишечного содержимого и структурных нарушений щеточной каймы энтероцитов. Клинически данные нарушения проявляются развитием диса-харидазной (лактазной) недостаточности, а также бродильной и/или гнилостной диспепсии.
Третий механизм связан с моторными расстройствами кишечника, основными из которых являются: гипермоторная диски-незия с наличием поносов; гипомоторная дискинезия с наличием безболевых запоров; гипомоторная дискинезия с эпизодами интестинальной псевдообструкции (интенсивные боли в животе, тошнота, рвота, метеоризм); спастическая дискинезия толстой кишки с развитием запоров с бобовидным калом и болями в животе. Кроме того, наличие условно патогенной микрофлоры в тонкой и толстой кишке может приводить к развитию воспалительных процессов.
К факторам риска системных поражений при ДБК, приводящим к повреждению кишечного барьера и транслокации кишеч-
жают внутрипросветный уровень рН, что
ной микрофлоры, относятся: присутствие условно патогенных микроорганизмов и их токсинов; прием нестероидных противовоспалительных препаратов, глюкокортикостероидов, цитостатиков, нарушающих основные механизмы преэпителиальной и иммунологической защиты; нарушение кровотока (абдоминальная ишемия, портальная гипертензия); нарушения целостности эпителия слизистой оболочки кишечника и др.
В патологический процесс при транслокации кишечных бактерий могут вовлекаться лимфатические узлы (мезадениты), мочевыводящая система (бактериурия, пиелонефрит, мочекаменная болезнь), печень и билиарная система, в которых могут формироваться неалкогольный стеатоз, стеато-гепатит и даже цирроз печени, неспецифический реактивный гепатит, внутрипече-ночный холестаз, печеночно-клеточная дисфункция, воспалительные процессы внепеченочного билиарного тракта.
Большое значение придается циркуля -ции в крови и накоплению в тканях бактериальных токсинов с активацией гуморальных иммунных реакций и формированием перекрестной иммунологической реактивности, что приводит к развитию полиарт-ралгий, реактивных артритов (реже), миал-гий, аллергических дерматозов, пищевой псевдоаллергии.
Определенная роль в формировании клиники ДБК отводится развитию полиги-повитаминозов и нарушениям обмена мак-ро- и микроэлементов.
Диагностика ДБК основывается на результатах клинических исследований и микробиологического анализа кишечного содержимого. Для установления этиологии ДБК необходимо обследование ЖКТ, в том числе эндоскопическое (по показаниям — с биопсией слизистой оболочки тонкой и толстой кишки), рентгенологическое — в первую очередь, для изучения характера
моторных нарушений ЖКТ. Определенное значение имеет исследование копрограм-мы после предварительной пищевой нагрузки, по результатам которой определяется тип диспепсии, а также выявляются косвенные признаки дисбактериоза толстой кишки (наличие перевариваемой клетчатки, йодофильной микрофлоры, внеклеточного крахмала).
Наиболее частыми бактериологическими признаками ДБК являются снижение или отсутствие основных бактериальных симбионтов — бифидобактерий и молочнокислых палочек, энтерококков, стафилококков, дрожжеподобных грибов, появление условно патогенных штаммов.
Одно из направлений в диагностике ДБК — исследование содержания в выдыхаемом воздухе различных метаболитов, которые продуцируются с участием кишечных бактерий, например дыхательный тест с С14-холеглицином, Б-ксилозой или лак-тулозой. Кроме того, в настоящее время внедряются в практику химические методы, позволяющие определять виды аэробных и анаэробных бактерий и грибов в различных биологических средах с использованием газовой хроматографии и масс-спект-рометрии.
Терапия больных с ДБК включает лечение основного заболевания (этиологическое лечение) и восстановление нормального состава кишечных бактерий.
Одной из главных задач является создание условий для роста и функционирования нормальной микрофлоры. Для этого назначается диета с учетом типа диспепсии, моторных нарушений кишечника и основного заболевания. При бродильной диспепсии на 7—10 дней необходимо ограничить овощи, фрукты, растительную клетчатку (особенно бобовые), молоко. При гнилостной диспепсии на период обострения рекомендуется питание с преобла-
данием овощей и фруктов, подвергнутых кулинарной обработке.
Пробиотики и пребиотики
В комплекс лечения ДБК обязательно входят пробиотики — биологические препараты, содержащие нормальные кишечные бактерии, и пребиотики — не перевариваемые ферментами пищевые ингредиенты или продукты жизнедеятельности нормальной микрофлоры, которые стимулируют ее рост и функциональную активность. Пробиотики и пребиотики оказывают прямой антагонистический эффект в отношении условно патогенных бактерий, стимулируют иммунные реакции, увеличивая титр антител, макрофагальную активность, количество Т-киллеров, продукцию интерферонов, концентрацию ^А, повышают колонизационную резистентность слизистой оболочки, способствуют регенерации кишечного эпителия и нормализации функций слизистой оболочки кишечника.
Пробиотики включают препараты, содержащие:
• аэробные бактерии (колибактерин, лак-тобактерин и др.);
• анаэробную флору (бифидумбактерин, пробифор и др.);
• их комбинации (бифиформ, бификол, линекс, примадофилус и др.).
Препараты, содержащие бифидобактерии, предпочтительно использовать при нарушениях микробного состава толстой кишки, а аэробные штаммы — тонкой кишки. Комбинированные препараты имеют преимущество при восстановлении микробного биоценоза всех отделов кишечника. Любой пробиотик назначается, как правило, 2 раза в день в течение 2 нед со строгим соблюдением прилагаемой инструкции по его приему.
К пребиотикам относятся лактулоза, пищевые волокна и, вероятно, хилак форте. Лактулоза назначается преимущественно
больным с запорами по 15—30 мл 1 раз в сутки, а хилак форте — при поносах по 30—40 капель 3 раза в день в течение 2—4 нед. Пребиотики целесообразно использовать одновременно с пробиотиками.
В ряде случаев перед назначением пробиотиков требуется прием антибактериальных средств (кишечных антисептиков).
Показания для проведения деконтаминации кишечника:
• наличие избыточного бактериального роста в тонкой кишке;
• выявление условно патогенной микрофлоры в посевах кишечного содержимого;
• транслокация кишечных бактерий во внутреннюю среду;
• отсутствие эффекта от предшествующей терапии пробиотиками.
Подход к назначению антибактериальных средств в основном эмпирический. Необходимо учитывать, что при избыточном бактериальном росте в тонкой кишке и при транслокации бактерий за пределы кишечника приоритетными являются всасывающиеся в ЖКТ, а при нарушении микрофлоры толстой кишки — невсасывающиеся препараты.
Нитрофураны обладают широким спектром действия в отношении грамположи-тельных кокков, а также грамотрицатель-ных микроорганизмов, в том числе патогенных. Используются в основном невса-сывающийся нифуроксазид по 200 мг 4 раза в сутки и всасывающийся фуразолидон по 100 мг 3—4 раза в сутки.
Сульфаниламиды оказывают антибактериальное действие на многие грамположи-тельные и грамотрицательные микроорганизмы, включая и патогенные. Назначаются комбинированные всасывающиеся (сульфаметоксазол/триметоприм по 960 мг
2 раза в сутки) и невсасывающиеся препа-
раты (фталазол или сульгин по 0,5—1,0 г 4 раза в сутки).
Фторхинолоны эффективны в отношении большинства грамотрицательных микроорганизмов, исключая анаэробы. Используются ципрофлоксацин по 250—500 мг 2 раза в сутки и пефлоксацин по 400 мг 2 раза в сутки.
Метронидазол обладает активностью против анаэробов (в частности, бактероидов) и некоторых других микроорганизмов, а также простейших: лямблий, амеб, трихомонад. Используется в дозе 250 мг 3—4 раза в сутки.
Интетрикс — кишечный антисептик широкого спектра действия. Оказывает про-тивомикробное, противогрибковое и про-тивопротозойное действие. Эффективен в отношении большинства грамположитель-ных и грамотрицательных патогенных кишечных бактерий, тогда как нормальная кишечная микрофлора к нему не чувствительна. Назначается по 2 капсулы 3 раза в день во время еды.
В ряде случаев используются биологические “антибактериальные” препараты: бактерии или дрожжевые клетки, обладающие антагонизмом в отношении патологической кишечной флоры, а также бактериофаги. С этой целью возможно назначение бактисубтила, энтерола (2—4 капсулы в сутки) или соответствующих бактериофагов (15 мл в сутки и более).
Антибиотики для деконтаминации кишечника используются редко, преимущественно при патологии тонкой кишки или при транслокации кишечных бактерий с развитием воспалительных процессов в других органах. В основном это тетрацик-лины (тетрациклина гидрохлорид по 250 мг 4 раза в день, доксициклин по
100 мг 2 раза в день), аминогликозиды (канамицин, неомицин, мономицин по 250—500 мг 3—4 раза в день) и левомицетин (по 500 мг 3—4 раза в день).
Все антибактериальные средства назначаются внутрь, продолжительность курса — 5—7 дней. Возможно проведение 2—3 курсов антибактериальной терапии с последующим назначением пробиотиков. Одновременно назначаются кишечные адсорбенты (буферные антациды, белая глина и др.), ферменты, нормализующие моторику кишечника препараты, витамины группы В.
Профилактика ДБК определяется рациональным питанием, ранним выявлением и адекватным лечением болезней человека вообще и заболеваний ЖКТ в частности.
Грачева Н.М., Ющук Н.Д., Чупринина Р.П. и др. Дисбактериозы кишечника, причины возникновения, диагностика, применение бактерийных биологических препаратов: Пособие для врачей и студентов. М., 1999. 44 с.
Григорьев П.Я., Яковенко А.В. Клиническая гастроэнтерология. М., 1998. 647 с.
Григорьев П.Я., Яковенко Э.П. Нарушение нормального состава кишечной микрофлоры, клиническое значение и вопросы терапии. Метод. пособие. М., 2000. 15 с.
Приказ МЗ РФ от 9 июня 2003 г. № 231 “Об утверждении отраслевого стандарта. Протокол ведения больных. Дисбактериоз кишечника” // Проблемы стандартизации в здравоохранении. 2003. № 9. С. 18—91.
Читайте также:


