Глубокая инфекция эндопротеза коленного сустава
Для продолжительности срока использования и функциональной характеристики суставов-имплантатов важны разные аспекты – из какого материала сделаны поверхности соприкасающихся искусственных компонентов, состояние костной ткани, активность пациента, его рост, вес, возраст, перенесенные операции на костях, хронические заболевания. Гнойно-воспалительные процессы возникают из-за внедрения микробов во время хирургической операции. Они могут попасть в рану аэрогенным путем (из воздуха), контактным (руками хирурга, инструментами), гематогенным (из очагов хронической инфекции).
- Материалы и продолжительность срока службы.
Одной из причин возникновения параинфекции является непереносимость компонентов искусственного сочленения. Организм иногда бурно реагирует на чужеродный агент. Перед операцией надо выявить персональную реакцию на конструкцию протеза, на все его компоненты. Чтобы увеличить прочность искусственных суставов, используемые материалы должны соответствовать самым высоким стандартам медицины. Неизбежный износ, возникающий в результате трения и истирания, должен быть как можно более низким. Кроме того, совместимость с телом и хорошее срастание коленного сустава с окружающими его костями должны быть максимально оптимальными, чтобы не было малейшего травмирования окружающей ткани. В этом случае вероятность инфицирования сводится к минимуму. Новая технология VERILAST (ВЕРИЛАСТ) объединяет два инновационных материала в уникальную пару трения: OXINIUM и высокосшитый полимерный материал. Результаты лабораторных исследований подтверждают, что эта комбинация является ключом к уменьшению износа при эндопротезировании и минимизирует риск инфицирования.
Традиционный полиэтилен был с 1968 года надежным компонентом, обеспечивающим легкое скольжение материалов друг по другу. Однако, наряду со своей высокой биосовместимостью, у этого материала есть недостаток, который и явился основной причиной для его ревизии: износ и - результирующая от этого - реакция тканей вплоть до асептического ослабления. Однако, с помощью новой технологии, которая дает возможность получить высокую степень сшивания полимеров посредством облучения, теперь создается стабильная сетчатая структура. Новая технология VERILAST считается устойчивой к окислению и демонстрирует улучшенную износостойкость.
Риск послеоперационных осложнений особенно высок у лиц, страдающих определенными болезнями. Рассмотрим некоторые из них.
Ожирение - наличие патологического ожирения можно рассматривать в качестве фактора риска при эндопротезировании коленного сустава. В рамках метаболического синдрома оно может нести ответственность за более частое возникновение диабета типа II. Менископатии и возникающие дегенеративные заболевания коленного сустава в качестве прямых последствий ожирения, часто являются показаниями для имплантации протеза коленного сустава, что, в свою очередь, приводит к увеличению доли пациентов с ожирением с протезами коленного сустава.
Сахарный диабет несет ответственность за нарушение процесса заживления ран; в качестве причин этого рассматриваются такие факторы, как замедленный синтез коллагена, оказание отрицательного влияния на фагоцитоз и замедленное прорастание капилляров в рубцовую ткань. Диабет же, в свою очередь, способствует возникновению раневых осложнений. Проксимальная мышечная слабость и диабетическая периферическая полинейропатия, в результате которых увеличивается частота возникновения и персистенция поражений кожи (таких, как например, нейротрофическая язва) приводят к увеличению риска возникновения инфицирования. Кроме того, у диабетиков увеличивается вероятность возникновения окклюзии периферических артерий. Таким образом, сахарный диабет следует рассматривать как фактор риска развития инфекции при выполнении имплантации протеза. Предоперационное оптимальное регулирование сахара в крови может свести к минимуму существующий риск. По данным некоторых исследований пациенты с диабетом имеют более плохое общее качество жизни после развития инфекции протеза коленного сустава по сравнению с контрольной группой пациентов, нестрадающих диабетом.
- Окклюзионное заболевание периферических артерий.
Болезнь также может способствовать нарушению процесса заживления ран, прежде всего, вследствие снижения перфузии в области раны. Поэтому, до проведения операции необходимо уточнить состояние периферических сосудов пациента и провести при необходимости ряд специальных обследований.
По данным некоторых исследований, при наличии у пациентов - в качестве предыдущего заболевания - хронического полиартрита, следует ожидать не только более частого возникновения инфекций, но и более плохих клинических результатов. У пациентов с хроническим полиартритом по сравнению с группой пациентов, не страдающих полиартритом, наблюдалось значительно меньшее количество случаев сохранения протезов и, в свою очередь, ампутации были чаще. Кроме того, число смертельных исходов было выше у пациентов, страдающих ревматизмом. Однако эти различия не были значительными
У многих пациентов является ослабленной защита организма в результате приема различных иммунодепрессантов. Примерно 10% пациентов во время имплантации протеза коленного протеза приходилось регулярно принимать кортикостероиды. В результате, риск инфицирования у пациентов с артрозом значительно увеличивается, а некоторые авторы утверждают, что риск инфицирования даже утраивается. Кроме того, ревматики имеют более низкое качество костей, что может привести к проблемам фиксации эндопротеза, особенно в субхондральной области, что, в свою очередь, приводит к ревизиям и, следовательно, к повышенному риску инфицирования. Кстати, и длительная антибиотикотерапия перед операцией порой может спровоцировать появление инфекции, так как появляются резистентные формы возбудителей, и борьба с инфекцией в дальнейшей становится малоэффективной.
- Деформации верхних конечностей.
Деформации и дефекты верхних конечностей могут приводить к проблемам при послеоперационной мобилизации. Средний возраст этих пациентов при первичной имплантации протеза в среднем на 10 лет меньше, в результате чего протез должен оставаться функциональным в течение более длительного периода времени и, следовательно, вероятность возникновения поздних осложнений (таких как асептическое ослабление или инфекция протеза) является, соответственно, более высокой
- Предыдущие операции на колене.
Дополнительными факторами риска развития инфекции протеза является наличие у пациентов предыдущих инвазивных оперативных вмешательств на колене. Хирургические вмешательства или внутрисуставные пункции на соответствующем колене до проведения первичной операции по имплантации протеза коленного сустава приводят к меньшему количеству случаев сохранения первичного протеза и к большей частоте случаев ревизионного протезирования или выполнения артродезов, а также к более высокой смертности. Количество ранее выполненных оперативных вмешательств не играли никакой роли для клинических результатов.
- Нарушение предписания лечащего специалиста.
Реабилитационный период чрезвычайно важен для качественного восстановления. Необходимо тщательно соблюдать все рекомендации врача, добросовестно принимать лекарства, помнить о важности ЛФК, о щадящем режиме. Надо быть особо терпеливым и ответственным на этом не менее важном для сустава этапе.
- Халатное отношение к выбору клиники и врача.
Операции по эндопротезированию доведены до совершенства и изучены до малейших нюансов. Но эти знания есть только у опытных практикующих врачей, работающих в специализированных ортопедических центрах. Надо внимательно отнестись к выбору клиники, желательно предварительно посетить ее, услышать отзывы больных и поговорить с врачами, которым вы хотите довериться.
Длительная операция способствует появлению инфекции, так, ее продолжительность более 3-х часов значительно увеличивает риск заражения тканей из-за их контакта с окружающей нестерильной средой. Периоперационный риск инфицирования может быть снижен путем предоперационной оптимизации некоторых из вышеуказанных факторов риска. Это включает в себя, как целенаправленное снижение веса пациентов, так и достижение в долгосрочной перспективе оптимальных показателей уровня глюкозы в крови у пациентов с диагностированным сахарным диабетом. Пациенты с хроническим полиартритом до начала лечения должны быть проинформированы о возможности получения более плохих конечных результатов.
У пациентов с ранней инфекцией более часто достигалось сохранение первичного протеза и относительно более часто было успешное использование ревизионных протезов.
Напротив, при поздних инфекциях было выполнено больше артродезов и при этом было зафиксировано больше случаев смертельного исхода. Частота случаев ампутации была примерно одинаковой в обеих группах. Представленные различия являются незначительными.
Прогноз при парапротезной инфекции достаточно благоприятный, но сохранить функциональность сустава иногда не получается, поэтому инфекционные риски, имеющие место при эндопротезировании, являются большой проблемой в медицине и для социума. Необходимо тщательно подойти к профилактике осложнений эндопротезирования. Она будет заключаться в определенных действиях до госпитализации, во время самого вмешательства и в реабилитационном периоде. Поэтому чрезвычайно важно найти специализированную клинику и опытного квалифицированного врача. Большое значение играет положительный настрой самого пациента и желание активно участвовать в процессе выздоровления. Особенно важна подготовка пациента перед операцией, а затем его настойчивость и добросовестность на этапе восстановлениявосстановления.



Поиск
Метод двухэтапной ревизии при глубокой парапротезной инфекции эндопротеза коленного сустава
Д.В. РИМАШЕВСКИЙ 2 , Е.Т. КУРМАНГАЛИЕВ 2 , И.Ф. АХТЯМОВ 1 , А.А. БЕЛОКОБЫЛОВ 3 , А.Е. АЛИ 3,4 , А.А. АЛИБЕКОВ 3,5
1 Республиканская клиническая больница МЗ РТ, 420064, г. Казань, Оренбургский тракт, д. 135
2 Карагандинский областной центр травматологии и ортопедии им. проф. Х.Ж. Макажанова, 100019, Республика Казахстан, г. Караганда, пр. Сакена Сейфуллина, д. 13
3 НИИТО (НАУЧНО-ИССЛЕДОВАТЕЛЬСКИЙ ИНСТИТУТ ТРАВМАТОЛОГИИ И ОРТОПЕДИИ) Республики Казахстан, 010000, Республика Казахстан, г. Астана, ул. Абылай хана, д. 15а
4 Городская клиническая больница № 4, 050039, Республика Казахстан, г. Алматы, ул. Папанина, д. 220
5 Областная клиническая больница, 090000, Республика Казахстан, г. Уральск, ул. Н. Савичева, д. 85
Римашевский Денис Владимирович — консультант, тел. +7-909-943-06-18, e-mail: [email protected] 2
Курмангалиев Еркин-Дауир Толеувич — заместитель главного врача, тел. +7-701-426-22-10, e-mail: [email protected] 2
Ахтямов Ильдар Фуатович—доктор медицинских наук, профессор, заведующий кафедрой травматологии, ортопедии и хирургии экстремальных состояний КГМУ, главный научный сотрудник научного отдела РКБ МЗ РТ, тел. +7-905-315-01-50, e-mail: [email protected] 1
Белокобылов Алексей Александрович — заведующий отделением эндопротезирования суставов, тел.+7 (7172) 54-77-17 2
Али Адил Ермаханович — соискатель НИИТО Республики Казахстан, врач травматолог-ортопед ГКБ № 4, тел. +7 (727) 300-36-04, e-mail: [email protected] 3,4
Алибеков Асылбек Алибекович — соискатель НИИТО Республики Казахстан, ортопед-травматолог Уральской областной больницы, тел. +7 (7112) 26-62-71, e-mail: [email protected] 3,5
Цель исследования — внедрение в клиническую практику модульного спейсера коленного сустава на первом этапе лечения инфекционных осложнений артропластики.
Ретроспективно проведена оценка результатов 16 случаев двухэтапной ревизии эндопротезирования коленного сустава, выполненной авторами по поводу перипротезной инфекции с 2011 по 2013 гг. В основе метода лежит использование модульного спейсера из костного цемента с антибиотиками. Конструктивной особенностью его является наличие бедренного и разъемного большеберцового компонента, состоящего из интрамедуллярного армированного стержня и вкладыша. Применение спейсера позволило провести эффективную локальную антибиотикотерапию. Эрадикация инфекции с возможностью установки ревизионного эндопротеза была достигнута в 87,5% случаев (14 из 16). Ни в одном случае не выявлено прогрессирующего разрушения кости.
Авторы делают вывод, что во время первого этапа ревизии необходимо устанавливать спейсеры как в каналы бедренной, так и большой берцовой костей, стабилизировать бедренный спейсер, а спейсер-вкладыш — без дополнительного цементирования.
Ключевые слова: парапротезная инфекция, ревизионное эндопротезирование, спейсер.
D.V. RIMASHEVSKIY 2 , E.T. KURMANGALIYEV 2 , I.F. AKHTIAMOV 1 , H.Z. MAKAZHANOV 3 , A.A. BELOKOBYLOV 3 , A.E. ALI 3,4 , A.A. ALIBEKOV 3,5
1 Republican Clinical Hospital of the Ministry of Healthcare of the Republic of Tatarstan, 138 Orenburgskiy Trakt, Kazan, Russian Federation, 420064
2 Karaganda region Center for Traumatology and Orthopedics named after Prof. Kh.Zh. Makazhanov, 13 Saken Seifullin Prospekt, Karaganda, Republic of Kazakhstan, 100019
3 Scientific-Research Institute for Traumatology and Orthopedics of Kazakhstan Republic, 15а Abylai khan St., Astana, Republic of Kazakhstan, 010000
4 City Clinical Hospital № 4, 220 Papanin St., Almaty, Republic of Kazakhstan, 050039
5 Oblast Clinical Hospital, 85 Savichev St., Uralsk, Republic of Kazakhstan, 090000
Karaganda method of two staged revision of deep periprostetic knee infection
Rimashevskiy D.V. — consultant, tel. +7-909-943-06-18, e-mail: [email protected] 2
Kurmangaliyev E.T. — Vice Chief Doctor, tel. +7-701-426-22-10, e-mail: [email protected] 2
Akhtyamov I.F. — D. Med. Sc., Professor, Head of the Department oа Traumatology, Orthopedics and Urgent Surgery of Kazan State Medical University, Chief Researcher of Scientific Department of Republican Clinical Hospital, tel. +7-905-315-01-50, e-mail: [email protected] 1
Belokobylov A.A. — Head of the Department of Replacement Arthroplasty, tel. +7 (7172) 54-77-17 2
Ali A.E. — applicant of Scientific-Research Institute for Traumatology and Orthopedics, traumatologist – orthopedist of City Clinical Hospital № 4, tel. +7 (727) 300-36-04, e-mail: [email protected] 3,4
Alibekov A.A. — applicant of Scientific-Research Institute for Traumatology and Orthopedics, traumatologist – orthopedist of Oblast Clinical Hospital, tel. +7 (7112) 26-62-71, e-mail: [email protected] 3,5
The aim of work is to implement into clinical practice the modular spacer at the first stage of treating the infectious complications of knee arthroplasty.
16 cases of two-stage revision of septic total knee prosthesis, performed by the authors in 2011 — 2013, were retrospectively evaluated. The key element of the method was the use of a modular bone cement spacer loaded with antibiotics. Its constructive features were: presence of intramedullary, femoral and tibial (insert-like) components; tibial component stabilization by protruding part of tibial intramedullary spacer; press-fit femoral spacer implantation. Modular spacer allowed to perform effective local antibiotic therapy. Infection was eradicated in 87.5% of cases (14 out of 16). In none of the cases, bone deficit progression was seen.
The authors conclude that during the first stage of knee revision, the intramedullary canal spacers should be implanted in both femur and tibia. Femoral spacer and insert-like spacer should be stabilized without cementing.
Key words: periprosthetic infection, revision joint replacement, spacer.
Эндопротезирование коленного сустава — эффективная и выполняемая практически во всех крупных специализированных стационарах операция. Вместе с ростом числа первичных операций, увеличивается число осложнений, в том числе и инфекционных. Глубокая перипротезная инфекция (ППИ) на сегодняшний день является самой проблемной причиной ревизий даже в странах с длительной историей эндопротезирования [1]. Стоимость лечения ППИ и ревизионного эндопротезирования несопоставимо выше первичной операции, что становится серьезной социальной проблемой [1]. Для пациентов с патологией коленного сустава характерны ряд особенностей: пожилой возраст, излишний вес, сопутствующие соматические заболевания и т.п., что повышает риск развития инфекционных осложнений. Подобное положение дел предопределяет настороженность в отношении развития инфекций после эндопротезирования суставов и требует ответственно подходить к профилактике развития инфекции.
В основе борьбы с ППИ лежат ранняя диагностика и лечение. Для лечения тяжелейшего из осложнений эндопротезирования традиционно применяют ряд вариантов, наиболее приемлемым из них является попытка сохранения первичного протеза. Несомненным условием при этом является не более чем 3–4-х недельный срок после его установки, отсутствие свища и подозрений на полирезистентные штаммы микроорганизмов. Как правило, успех возможен лишь при отсутствии факторов риска высокой резистентности флоры, таких как: недавний прием антибиотиков, женский пол, сахарный диабет, возраст старше 65 лет, недавняя госпитализация и перенесенная инфекция мягких тканей, ВИЧ [2]. Во всех остальных случаях отдается предпочтение хорошо зарекомендовавшим себя двухэтапным ревизиям [2,3]. Подобная ревизионная артропластика предусматривает на первом этапе использование локальной антибиотикотерапии в виде установки временного эндопротеза (спейсера) из костного цемента с антибиотиком. Костный цемент имеет свойство освобождать во времени со своей поверхности часть антимикробного препарата, создавая повышенную его концентрацию в окружающих тканях. В ортопедической практике используются как преформированные (фабричные), либо кустарно изготовленные в ходе операции спейсеры.
Цели исследования— внедрение в клиническую практику модульного спейсера коленного сустава на первом этапе лечения инфекционных осложнений артропластики.
Предъявляемые требования: спейсер должен иметь высокую антибактериальную эффективность, быть простым в изготовлении для любого хирурга, владеющего техникой первичного эндопротезирования, безопасным для пораженной костной ткани, сохранять опороспособность пациента между первым и вторым этапами ревизии, не ограничивать движения в суставе и, что важно – быть дешевым.
Материалы и методы
Исследования и внедрение разработки проводилось на базе ряда клиник Республики Казахстан и в первую очередь в Карагандинском областном центре травматологии и ортопедии им. проф. Х.Ж. Макажанова в сотрудничестве с кафедрой травматологии, ортопедии и хирургии экстремальных состояний Казанского государственного медицинского университета. Методическое руководство осуществлялось со стороны НИИ травматологии и ортопедии г. Астана. Ретроспективно был проведен анализ результатов 16 случаев двухэтапной ревизии глубокой инфекции после тотального эндопротезирования коленного сустава (ТЭКС), выполненной с ноября 2011 по июнь 2013 года.
Данные по пациентам представлены в таблице 1.
Таблица 1.
Пациенты с ППИ
| Мужчины | Женщины | Всего | |
| Стафилококк | 1 | 3 | 4 |
| Нестафилококковая флора | 1 | 2 | 3 |
| Неустановленная флора | 2 | 7 | 9 |
| Возраст, лет | 56 (42-74) | 61 (34-73) | 60 |
| Срок после первичной операции, мес. | 37 (6-62) | 12 (2-12) | 18 |
| Неудачная двухэтапная ревизия в анамнезе | 1 | 1 | 2 |
Мы исключили из исследования пациентов с дефектами типа T3 и F3 по классификации Engh [7], а также с не состоятельностью коллатеральных связок, собственной связки надколенника, которым были установлены неартикулирующие варианты спейсеров.
В основе метода лежит использование авторской разработки новой модели модульного спейсера коленного сустава. Бедренный сегмент состоит из интамедуллярного стержня, изготовленного из армированного костного цемента и стандартного металлического феморального компонента первичного эндопротеза. Тибиальный компонент в виде фигурной пластины из костного цемента имеет посадочную площадку для опоры на интрамедуллярном стержне большой берцовой кости. Схема спейсера приведена на рисунке 1.
Рисунок 1.
Установка спейсера в интрамедуллярный канал

Рисунок 2.
Установка бедренного компонента на пленку

Рисунок 3.
Установка внутрисуставного спейсера

Рисунок 4.
Схема установки спейсера и рентгенография, выполненная после имплантации спейсера коленного сустава

Результаты и обсуждение
Все пациенты были активизированы в первые сутки после операции. Ходьба разрешалась со второго дня с полной, либо дозированной нагрузкой на ногу. Пациенты на вторые-третьи сутки отмечали практически полное исчезновение болевого синдрома.
Целью первого этапа ревизионного эндопротезирования коленного сустава было купирование инфекционного процесса. Локальная антибиотикотерапия (использование спейсера из костного цемента с Ванкомицином) в обязательном порядке сочеталась с системной терапией. Верификация купирования инфекции заключалась в комплексной оценке клинического состояния пациента, локальных проявлений, кратных анализах крови и пункционного биоптата из области коленного сустава. У 14 пациентов эрадикация инфекции была подтверждена клинически и лабораторно и микробиологически. У 2 пациентов имелись клинические и лабораторные признаки рецидива инфекции в коленном суставе.
Второй этап ревизии выполняли на сроках от 3 до 9 месяцев. На момент госпитализации, до выполнения второго этапа ревизии, все пациенты ходили с полной нагрузкой на оперированную ногу. 6 из 8 работающих пациентов вернулись к труду между этапами ревизии. У всех пациентов на момент ревизии объем движений в коленном суставе превышал 90 градусов.
Таким образом, нам удалось элиминировать инфекцию у 14 из 16 пациентов. При этом оба пациента с рецидивом нарушили предписание врача на амбулаторном этапе, прекратив антибиотикотерапию вскоре после выписки из стационара. Следует признать, что разработанный вариант спейсера обладает существенным недостатком, поскольку сопряжена с установкой удаленного бедренного компонента, поверхность которого может служить основой для формирования микробной биопленки. Однако именно наличие металлического бедренного компонента позволило нам отказаться от его дополнительного цементирования, а пациентам давать возможность нагрузки на оперированную ногу.
Выводы
Предложенная методика проведения первого этапа двухэтапной ревизии инфицированных эндопротезов коленного сустава позволяет с высокой степенью вероятности добиться эрадикации инфекции. Она проста в исполнении, не требует дорогостоящих расходных материалов и позволяет пациентам в период между первым и вторым этапами ревизии сохранять приемлемое качество жизни.
1. Bozic K.J., Kurtz S.M., Lau E., Ong K. et al. The epidemiology of revision total knee arthroplasty in the United States //Clin. Orthop. Relat. Res. — 2010, Jan. — № 468 (1). —P. 45-51.
2. Parvizi J., Adeli B., Zmistowski B., Restrepo C. et al. Management of Periprosthetic Joint Infection: The Current Knowledge: AAOS Exhibit Selection //J. Bone Joint Surg. Am. —2012. —№ 94 (14). —P. 1041-9.
3. Schnettler R., Steinau H.U. Septic bone and joint surgery // Thieme Medical Pub.—2010.
4. Scuderi G.R., Tria A.J., Knee Arthroplasty Handbook. Techniques in Total Knee and Revision Arthroplasty. —2006, Springer Science+Business Media, Inc. ISBN-10: 0-387-30730-3, ISBN-13: 978-0387-307305:120-132.
5. Kaya I., Sungur I., Yimazi M.,Pehlivanoglu F., Kartyafiar K., Sengos A. Comparison of the efficiency of different antibiotic irrigation solutions in decontamination of allografts contaminated with Staphylococcus aureus // Acta Orthop. Traumatol. Turc.—2013.— № 47(4).—P. 281-285.
6. Amin T.J., Lamping J.W., Hendricks K.J, McIff T.E. Increasing the Elution of Vancomycin from High-Dose Antibiotic-Loaded Bone Cement: A Novel Preparation Technique// J. Bone Joint Surg. Am. —2012, Nov. 07.—№ 94 (21).—P. 1946-1951.
7. Osmon D.S., Berbari E.F., Berendt A.R., Lew D. et al. Diagnosis and Management of Prosthetic Joint Infection: Clinical Practice Guidelines by the Infectious Diseases Society of America //Clinical Infectious Diseases.— 2013. —56 (1).—P. 1-25.
1. Bozic K.J., Kurtz S.M., Lau E., Ong K. et al. The epidemiology of revision total knee arthroplasty in the United States. Clin. Orthop. Relat. Res., 2010, Jan., no. 468 (1), pp. 45-51.
2. Parvizi J., Adeli B., Zmistowski B., Restrepo C. et al. Management of Periprosthetic Joint Infection: The Current Knowledge: AAOS Exhibit Selection. J. Bone Joint Surg. Am., 2012, no. 94 (14), pp. 1041-9.
3. Schnettler R., Steinau H.U. Septic bone and joint surgery. Thieme Medical Pub., 2010.
4. Scuderi G.R., Tria A.J., Knee Arthroplasty Handbook. Techniques in Total Knee and Revision Arthroplasty. 2006, Springer Science+Business Media, Inc. ISBN-10: 0-387-30730-3, ISBN-13: 978-0387-307305:120-132.
5. Kaya I., Sungur I., Yimazi M.,Pehlivanoglu F., Kartyafiar K., Sengos A. Comparison of the efficiency of different antibiotic irrigation solutions in decontamination of allografts contaminated with Staphylococcus aureus. Acta Orthop. Traumatol. Turc., 2013, no. 47(4), pp. 281-285.
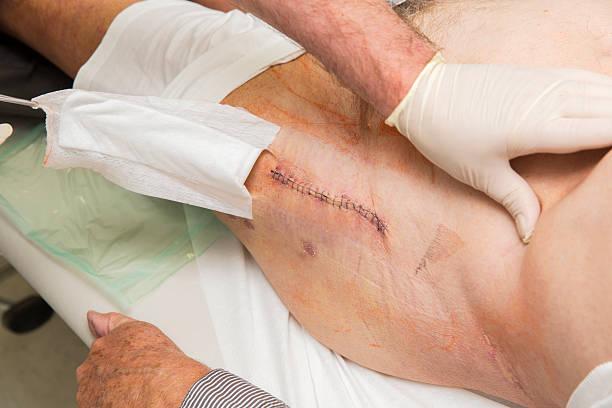
Гной в послеоперационной ране говорит о развитии инфекционных осложнений. В ортопедии и травматологии они тяжело поддаются лечению и приводят к инвалидизации пациентов. Парапротезные инфекции обусловливают увеличение срока пребывания в стационаре и требуют затрат на борьбу с ними.

Выделения из ТБС.
Инфекции после эндопротезирования бывают поверхностными или глубокими, острыми или хроническими, развиваться в раннем или позднем послеоперационном периоде. Воспалительный процесс может затрагивать только мягкие ткани нижней конечности или распространяться на прооперированный сустав.
Если после эндопротезирования у вас появился гной в шраме, повысилась температура и возникли боли в ноге – немедленно идите к врачу. Тот осмотрит вас, назначит нужные исследования и выяснит, насколько тяжелое у вас состояние. Вам придется лечь в стационар и пройти курс лечения.
Актуальность проблемы
По разным данным, частота развития ранней парапротезной инфекции после первичной замены крупных суставов составляет 0,3-0,5%, после ревизионной – 9%. Воспалительные процессы выявляют в течение первых трех недель после хирургического вмешательства.
Если говорить о частоте развития поздних инфекционных осложнений, то чаще всего они возникают в первые два года после эндопротезирования (1,63% пациентов). Реже (у 0,59% прооперированных) глубокие парапротезные инфекции развиваются в последующие 8 лет после операции.
Частота инфекционных осложнений на протяжении нескольких десятилетий остается неизменной. Однако заметно увеличилось общее количество артропластик, выросло и общее число осложнений. Поэтому становится все более актуальной их профилактика, ранняя диагностика и лечение.
Факт! Как показали научные исследования, риск развития инфекционных осложнений зависит от вида эндопротеза. Выяснилось, что в общей сумме имплантация отечественных моделей приводит к воспалению чаще (3-10% случаев), чем установка импортных (0,3-4,8%).
Что такое инфекция в области хирургического вмешательства
ИОХВ – это острое или хроническое воспаление, развивающееся в месте разреза или в области, которая подвергалась ятрогенному воздействию в ходе хирургического вмешательства. В 67% случаев инфекция затрагивает только зону операционного разреза, в 33% – распространяется на имплантированный сустав.
Факторы развития ИОХВ:
- длительность операции более 3 часов;
- технические трудности во время хирургического вмешательства;
- интраоперационная кровопотеря более 1 литра;
- нестабильность установленного эндопротеза;
- использование дополнительных синтетических и биологических материалов в ходе операции;
- наличие тяжелых хронических заболеваний.

Воспалительные процессы, которые не распространяются на прооперированный сустав, можно победить без ревизионного эндопротезирования. Если же инфекция затрагивает костную ткань, компоненты эндопротеза, остатки суставной капсулы или другие части коленного или тазобедренного сустава – лечить ее будет крайне тяжело. В этом случае больному скорее всего потребуется повторное эндопротезирование.
Существует ряд факторов, которые отягощают состояние пациента, замедляют выздоровление и ухудшают прогноз: снижение иммунитета, перенесенные операции, частое лечение антибиотиками. Стойкость обнаруженной микрофлоры к антибактериальным средствам, плохое кровообращение в области сустава, массивные гнойные очаги тоже осложняют терапию.
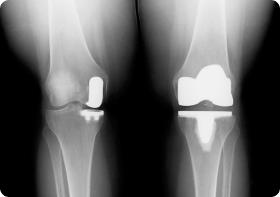
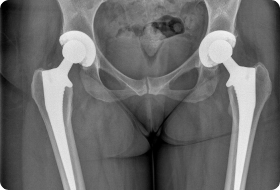
Виды парапротезной инфекции
В ортопедии и травматологии используют несколько классификаций ИОХВ. Систематизация и отнесение инфекции к конкретному виду помогает врачам оценить тяжесть состояния пациента. Классификация Coventry-Fitzgerald-Tsukayama самая распространенная.
Таблица 1. Типы глубокой парапротезной инфекции по Coventry-Fitzgerald-Tsukayama.
| Тип | Время развития | Тактика лечения | |
| I | Острая послеоперационная | 1-й месяц | Ревизия послеоперационной раны, удаление некротизированных тканей, при необходимости – замена некоторых частей эндопротеза при сохранении его основных компонентов. |
| II | Поздняя хроническая | От 1 месяца до 1 года | Обязательное ревизионное эндопротезирование. |
| III | Острая гематогенная | После 1 года | Вполне оправданной является попытка сохранить установленный протез. |
| IV | Положительные интраоперационные культуры | Бессимптомная бактериальная колонизация поверхности импланта | Консервативное лечение, заключающееся в парентеральной антибиотикотерапии на протяжении 6 недель. |
В классификации, созданной Новосибирским НИИТО, ИОХВ делят на ранние острые, поздние острые и хронические. Первые развиваются на протяжении трех месяцев после эндопротезирования, вторые – на 3-12 месяце, третьи – после 1 года. Инфекционные осложнения могут протекать в латентной, свищевой, флегмоноподобной или атипичной форме.
По распространенности инфекции бывают эпифасциальными (поверхностными) и субфасциальными (глубокими). Могут сопровождаться тотальной, бедренной или тибиальной нестабильностью.
Поверхностные и глубокие инфекции
Возникают в первый месяц после эндопротезирования. Характеризуются развитием воспаления в мягких тканях нижней конечности. Сам бедренный или коленный сустав остается интактным, то есть не вовлекается в патологический процесс. Причиной осложнения чаще всего является занесение в рану патогенных микроорганизмов во время хирургического вмешательства или в послеоперационном периоде.
- некроз кожных покровов;
- лигатурные свищи;
- расхождение краев раны;
- подкожная гематома.
- некроз парапротезных тканей;
- глубокие свищи;
- инфицированная субфасциальная гематома.
Факт! Незначительная болезненность, локальная припухлость, покраснение и гипертермия кожи в области шрама обычно указывают на поверхностную инфекцию, которая поддается лечению. Появление лихорадки, спонтанное расхождение швов и сильные боли в ноге позволяют заподозрить воспаление глубоких тканей. В этом случае прогноз менее благоприятный.
Инфекции протезированного сустава
При патологии воспаление распространяется на полости и оболочки прооперированного сустава, остатки синовиальной оболочки, кости в месте фиксации эндопротеза и прилегающие мягкие ткани. Причиной осложнения является колонизация поверхностей сустава патогенной микрофлорой. Бактерии могут попадать из внешней среды или заноситься гематогенным путем.
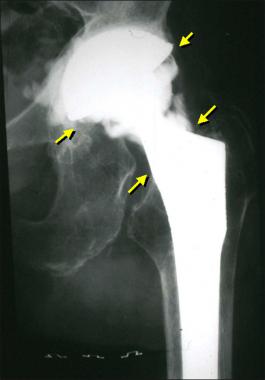
Так выглядит инфекция на рентгене.
Инфекции протезированного сустава самое грозное осложнение среди всех ИОХВ. Они не поддаются консервативной терапии, поэтому лечить их приходится хирургическим путем. Врачи заменяют эндопротез, однако иногда им все же удается сохранить его.
Существует три метода лечения инфекций протезированного сустава: ревизия раны без удаления импланта, ревизионное одноэтапное и двухэтапное эндопротезировение. Выбор методики зависит от состояния пациента, время манифестации инфекции, стабильности компонентов протеза и характера патогенной микрофлоры.
Методы диагностики ИОХВ
На наличие инфекционного процесса в области послеоперационной раны указывают гнойные выделения, боль, припухлость и локальное повышение температуры. Все эти симптомы появляются как при глубоких, так и при поверхностных инфекциях.
Рентгенологические исследования
Большую роль в дифференциальной диагностике свищевых форм инфекции играет рентгенофистулография. С ее помощью можно определить размер, форму и расположение свищей, выявить гнойные затеки и их связь с очагами костной деструкции. Это позволяет отличить поверхностные ИОХВ от глубоких.
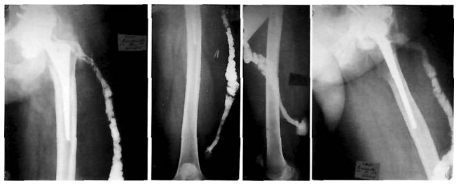
Фото: Рентгенофистулография, свищ в нижней трети бедра.
Для диагностики инфекции протезированного сустава чаще всего используют рентгенографию. Метод на дает 100% верных результатов, однако позволяет заподозрить патологию. На наличие парапротезной инфекции указывает внезапное появление периостальной реакции и остеолиза. Если эти признаки возникают внезапно, вскоре после успешно проведенной операции, – есть повод заподозрить неладное.
Любопытно! МРТ, УЗИ и радиоизотопное сканирование в диагностических целях используют редко из-за их низкой информативности. К примеру, установленный эндопротез создает помехи при магнитно-резонансной томографии, что делает изображение размытым и нечетким.
Лабораторные анализы
Сдача анализов помогает выявить острые и хронические воспалительные процессы в организме. Повышение показателей не является достоверным признаком ИОХВ. Для постановки диагноза нужно учитывать наличие определенных клинических симптомом, данных рентгенографии и других методов исследования.
Клинически значимые лабораторные показатели:
- Количество лейкоцитов. Имеет значение в диагностике острой парапротезной инфекции. Ярким признаком воспаления является повышение общего количества лейкоцитов и нейтрофилов, сдвиг лейкоцитарной формулы влево.
- СОЭ. Является неспецифическим показателем. Нормальная скорость оседания эритроцитов говорит об отсутствии воспалительных процессов, повышенная – об их наличии.
- С-реактивный белок. СРБ является белком острой фазы воспаления и высокочувствительным маркером ИОХВ для людей, которым выполнили эндопротезирование. При диагностике парапротезных инфекций нужно обращать внимание именно на этот показатель.


Микробиологические исследования
Бактериоскопическое и бактериологическое исследования позволяют выявить и идентифицировать возбудителя инфекции, а также определить его чувствительность к антибиотикам. Количественные исследования дают возможность установить число микробных тел в гнойном отделяемом.
Для исследования могут использоваться такие материалы:
- отделяемое из раны;
- образцы ткани;
- жидкость из суставной полости;
- протезный материал.
При имплант-ассоциированной инфекции выявить бактерии в биологических жидкостях и тканях практически невозможно. Патогенные микроорганизмы обнаруживают на самих поверхностях эндопротезов. Они покрывают импланты в виде адгезивной пленки.
Факт! Кроме бактериологического исследования для диагностики могут использовать ПЦР – полимеразную цепную реакцию. Метод имеет высокую чувствительность, но низкую специфичность. Из-за этого он нередко дает ложноположительные результаты.
Лечение
Прежде чем решить, как бороться с инфекцией, врачи тщательно обследуют пациента. Лишь установив диагноз и определив чувствительность патогенной микрофлоры к антибиотикам, они принимают окончательное решение.
Таблица 2. Методы лечения парапротезных инфекций:
| Метод | Показания | Результаты |
| Санация раны с сохранением эндопротеза | Проводится в том случае, когда ИОХВ возникла в первые 3 месяца после операции. Сохранить эндопротез можно лишь при отсутствии гнойных затеков и тяжелых сопутствующих заболеваний. При этом имплант должен быть стабильным, а микрофлора – высокочувствительной к антибиотикам. | Является наименее травматичным методом лечения. По разным данным, эффективность хирургической санации составляет 18-83%. |
| Ревизионное (повторное) эндопротезирование | Одномоментная или двухмоментная замена импланта выполняется в том случае, когда сохранить сустав не представляется возможным. Подобная ситуация наблюдается при нестабильности компонентов эндопротеза, позднем развитии инфекции, низкой чувствительности микрофлоры к антибиотикам, наличии тяжелых соматических заболеваний. | Позволяет полностью справиться с проблемой в 73-94% случаев. К сожалению, в ходе лечения больному приходится полностью менять установленный эндопротез. |
| Артродез с чрезкостным остеосинтезом | Глубокая рецидивирующая парапротезная инфекция, нечувствительная к антибиотикам микрофлора, наличие тяжелой сопутствующей патологии. | В 85% случаев позволяет устранить воспалительный процесс и восстановить опороспособность нижней конечности. |
| Экзартикуляция в тазобедренном суставе | Хроническое рецидивирующее воспаление, угрожающее жизни больного, или полная потеря функции нижней конечности. | Человек безвозвратно теряет ногу. Отсекают ее на уровне тазобедренного сустава. |
Имплант-сохраняющая тактика
Ее главная цель – устранение инфекционного процесса при одновременном сохранении эндопротеза. Больному проводят хирургическую обработку раны, в ходе которой удаляют гной и некротизированные ткани. При вовлечении в патологический процесс самого сустава выполняют артроскопический дебридмент. Больному назначают массивную антибактериальную терапию.
Любопытно! Научные исследования доказали эффективность безоперационного лечения ранних глубоких инфекций. Как выяснилось, комбинация антибиотиков и ферментных препаратов помогает ликвидировать воспаление за 5-7 дней.
Ревизионные операции
Выполняются в тех случаях, когда врачам не удается сохранить сустав. Хирурги полностью удаляют эндопротез, а на его место ставят новый. Риск повторного развития инфекции после ревизионного эндопротезирования выше, чем после первичного.
Читайте также:


