Грамотрицательные бактерии возбудители раневых инфекций
ЛЕКЦИЯ № 19. Грамотрицательные бактерии – возбудители гнойно-воспалительных заболеваний
1. Гемофильная палочка
Семейство Pasterellaceae, род Haemophilus, вид H. influenza.
Это мелкие или средних размеров прямые палочки, неспоробразующие, неподвижные, грамотрицательные, аэробы. В организме образуют капсулу.
Для культивирования требуются питательные среды, содержащие кровь (кровяной агар) или ее препараты (шоколадный агар).
В окружающей среде микроорганизмы быстро погибают от действия температуры выше 55 °C, солнечных лучей, высушивания, дезинфицирующих растворов.
Биохимическая активность выражена слабо. Расщепляют в основном углеводы до кислоты (без образования газа). По способности образовывать индол, продуцировать уреазу и орнитиндекарбоксилазу гемофилы инфлюэнцы делятся на шесть биоваров.
1) соматический белковый О-антиген;
2) капсульный полисахаридный К-антиген;
По строению капсульного К-антигена вид делится на пять сероваров (обозначаемых a, b, c, d, e). Серовар b – наиболее частый возбудитель менингитов.
2) капсульный полисахарид, обладающий антифагоцитарной активностью.
Экзотоксин не продуцирует.
Гемофильная палочка может входить в состав нормальной микрофлоры слизистой ротоглотки и верхних дыхательных путей, поэтому инфекция может возникать как эндогенная.
При экзогенном инфицировании вызывает инфекции лор-органов и органов дыхания (отиты, пневмонии), менингит. Путь передачи воздушно-капельный. Источником инфекции являются больной или бактерионоситель (антропонозная инфекция).
Чаще всего заболевание развивается как вторичная инфекция при снижении общей резистентности организма, обусловленной основным заболеванием.
Бактериальные менингиты, вызванные гемофильной палочкой, возникают чаще всего у детей от 6 месяцев до 3 лет. Это связано с тем, что у детей в возрасте до 3 месяцев обнаруживаются сывороточные антитела, переданные им от матери, но впоследствии исчезающие, и только к 3–5 годам вновь появляются бактерицидные комплементзависимые антитела к капсульному полисахариду возбудителя.
1) бактериологическое исследование – основной метод; материал – мокрота, спинномозговая жидкость, кровь; среда – кровяной агар. Необходимо дифференцировать от сходных микроорганизмов этого же рода – представителей нормальной микрофлоры носоглотки и ротовой полости;
2) экспресс-метод – иммуноиндикация с помощью реакции иммунофлюоресценции со специфической сывороткой типа b (используют при диагностике менингитов).
Этиотропная терапия проводится антибиотиками с учетом чувствительности возбудителя.
Специфическая профилактика: химическая вакцина.
2. Синегнойная палочка
Относится к семейству Pseudomonadaceae, роду Pseudomonas, виду P. aerugenosa.
Род Pseudomonas, кроме синегнойной палочки, включает в себя еще более 20 видов, многие из которых также могут вызывать заболевание у человека.
Это прямые или слегка изогнутые палочки средних размеров, подвижные (лофотрихи или монотрихи), грамотрицательные, облигатные аэробы. Спор не образуют, имеют тонкую слизистую капсулу.
Синегнойная палочка нетребовательна к питательным средам, хорошо растет на искусственных питательных средах. На мясопептонном бульоне дает рост в виде помутнения с сероватой пленкой на поверхности. На плотных питательных средах формируются крупные полупрозрачные колонии флюоресцирующего зеленоватого цвета. При этом в толщу среды диффундируют синевато-зеленые водорастворимые пигменты – пиоцианин или флюоресцеин. Способность псевдомонад образовывать пигменты – наиболее характерный дифференциально-диагностический признак.
Культура синегнойной палочки при культивировании на питательных средах имеет кисловато-сладкий ароматный запах (специфический запах жасмина).
Устойчива во внешней среде. Обладает естественной устойчивостью к антибиотикам.
1) низкая сахаролитическая активность, расщепляет глюкозу до кислоты;
2) высокая протеолитическая активность, разлагает некоторые аминокислоты;
3) редуцирует нитриты до газообразного азота;
4) разжижает желатин.
Метаболизм только окислительный.
1) соматический О-антиген, группоспецифический, по его строению делится на серогруппы;
2) жгутиковый Н-антиген;
3) М-антиген внеклеточной слизи.
1) в организме может образовывать капсулоподобное вещество, имеющее защитные свойства;
2) выделяет термолабильный экзотоксин А, обладающий цитотоксическим и дермонекротическим действием;
3) выделяет эндотоксин;
4) некоторые штаммы продуцируют гемолизины и лейкоцидин;
5) имеет ферменты агрессии, такие как плазмокоагулаза, протеазы, антиэластазы.
Синегнойная палочка может обитать в кишечнике человека, обнаруживается на коже и слизистых оболочках.
Чаще всего синегнойная инфекция является внутрибольничной. Источник – больной (или бактерионоситель). Может вызывать различные заболевания. Особенно часто выделяется при гнойно-воспалительных осложнениях ожоговых ран.
Иммунитет после перенесенной инфекции обусловлен гуморальными и клеточными механизмами.
Диагностика: бактериологическое исследование; материал определяется клиническими проявлениями заболевания.
1) антибиотики (цефалоспорины, аминогликозиды);
2) синегнойный бактериофаг;
3) синегнойная иммунная плазма;
4) убитая лечебная стафило-протейно-синегнойная вакцина.
Род Klebsiella включает в себя несколько патогенных для человека видов. Наиболее значимы K. pneumoniae, K. ozaenae, K. rhinoscleromatis.
Это грамотрицательные палочки средней величины, не образующие спор. Факультативные анаэробы. В препаратах располагаются поодиночке, попарно или короткими цепочками. Не имеют жгутиков, неподвижны. Спор не образуют.
Это истинно-капсульные бактерии: образуют капсулу в организме и на питательных средах. Капсула имеет полисахаридную структуру.
Нетребовательны к питательным средам. На плотных питательных средах образуют характерные куполообразные мутные слизистые колонии. При росте на мясопептонном бульоне вызывают равномерное помутнение, иногда со слизистой пленкой на поверхности.
Клебсиеллы устойчивы к факторам внешней среды, благодаря капсуле длительно сохраняются в воде, на предметах, в помещениях.
Обладают выраженной сахаролитической активностью, ферментируют углеводы с образованием кислоты и газа. По биохимическим свойствам род делится на шесть видов. Для дифференциации используют следующие тесты:
1) ферментацию глюкозы;
2) ферментацию лактозы;
3) образование уреазы;
4) утилизацию цитрата.
1) соматический О-антиген – группоспецифический;
2) капсульный К-антиген.
К-антигены является общими с антигенами эшерихий и сальмонелл.
1) обладают выраженными адгезивными свойствами;
2) главный фактор – капсула, защищающая микроорганизмы от фагоцитоза;
3) имеют К-антиген, подавляющий фагоцитоз;
4) выделяют эндотоксин.
Клебсиеллы нередко обнаруживаются на коже и слизистых оболочках, в связи с чем возможно развитие эндогенной инфекции. Но экзогенное заражение встречается чаще. Источниками инфекции могут быть больной, бактерионоситель, объекты внешней среды. Пути передачи – воздушно-капельный, контактно-бытовой.
K. pneumoniae может вызывать у человека пневмонию, поражение суставов, мозговых оболочек, мочеполовых органов, гнойные послеоперационные осложнения, сепсис.
K. ozaenae поражает слизистую оболочку верхних дыхательных путей и придаточных пазух носа, вызывая их атрофию.
K. rhinoscleromatis поражает слизистую оболочку носа, трахею, бронхи, глотку, гортань.
Постинфекционный иммунитет нестойкий.
1) бактериологическое исследование; материал – отделяемое пораженных слизистых оболочек;
1) антибиотики, фторхинолоны с учетом чувствительности возбудителя;
2) убитая лечебная вакцина Солко-Уровак (для лечения урогенитальных инфекций);
3) вакцина ВП-4 (для лечения инфекций дыхательных путей).
Специфическая профилактика: вакцина IRS19.
Род Proteus. Возбудителем гнойно-воспалительных заболеваний является вид P. mirabilis.
Это полиморфные грамотрицательные палочки с закругленными концами, факультативные анаэробы. Капсулообразование отсутствует. Имеют перитрихиально расположенные жгутики.
Н-формы этих бактерий отличаются высокой подвижностью, хотя встречаются и неподвижные (О-формы).
Нетребовательны к питательным средам. На мясопептонном агаре Н-форма протея дает характерный ползучий рост в виде нежной вуали голубовато-дымчатого цвета (феномен роения), затягивающий всю поверхность сплошным налетом без образования отдельных колоний. В жидкой питательной среде дает рост в виде диффузного помутнения. При культивировании характерен гнилостный запах.
О-формы образуют крупные с ровными краями колонии. Некоторые штаммы вызывают гемолиз эритроцитов в кровяных средах.
В окружающей среде устойчивы, могут сохранять жизнеспособность в слабых растворах дезинфектантов. Широко распространены в природе. Являются обитателями кишечника человека и животных.
1) ферментируют глюкозу до кислоты;
2) не разлагают маннит и лактозу;
3) продуцируют сероводород;
4) разжижают желатин, расщепляют мочевину с образованием аммиака;
5) обладают протеолитической и пептолитической активностью.
1) соматический О-антиген – группоспецифический;
2) жгутиковый Н-антиген – вариантспецифический.
По Н-антигену протеи делят на 110 сероваров. Внутри вида различают фаговары, бактерициновары, бактериоциногеновары.
1) адгезины – пили;
3) патогенные амины – индол, скатол;
4) ферменты агрессии – протеазы.
Протеи в небольших количествах могут обнаруживаться в кишечнике здорового человека, поэтому протейная инфекции может развиваться как эндогенная.
Основным местом их обитания являются объекты внешней среды, гниющие продукты, сточные воды, почва. Источниками инфекции для человека могут быть больной и бактерионоситель.
Бактерии участвуют в развитии гнойно-воспалительных заболеваний мочевыводящих путей, быстро распространяются по ожоговой поверхности, давая характерный гнилостный запах.
Постинфекционный иммунитет нестойкий.
Диагностика: основной метод – бактериологическое исследование; материал определяется локализацией очага поражения. Посев по методу Шушкевича в каплю конденсированной влаги свежескошенного мясопептонного агара; характерен рост в виде вуали по всей поверхности среды.
1) антибиотики, нитрофураны, фторхинолоны;
2) протейный или колипротейный бактериофаг;
3) убитая лечебная стафило-протейно-синегнойная вакцина.
[youtube.player]Особенности патогенеза раневой инфекции в большой степени зависят от вида возбудителей и их свойств. Поэтому знание микробиологической характеристики современной раневой инфекции является обязательным. Здесь можно выделить ряд общих моментов.
1. Отличительной особенностью раневой инфекции является полиморфизм возбудителей. Помимо влияния организма, судьба микрофлоры ран зависит от характера взаимодействия ассоциантов между собой.
Для возбудителей раневой инфекции наиболее важными типами взаимоотношений являются синергизм и антагонизм.
Синергизм характеризуется усилением физиологических функций у членов микробной ассоциации. Ярким примером синергизма является возможность существования анаэробов при доступе воздуха благодаря выделяемым аэробами ферментов каталазы и супероксиддисмутазы, защищающими клетки от токсического действия кислорода. В свою очередь, анаэробы продуцируют бета-лактамазу и особые вещества, повышающие в тысячи раз устойчивость аэробов к антибиотикам и бактерицидному действию человеческих лейкоцитов. Для хирургов важно, что часто раневая инфекция возникает и поддерживается, если присутствует каждый из участников ассоциации. Поэтому подавление даже одного из них может предотвратить или ликвидировать инфекционное
осложнение.
При антагонистических взаимоотношениях происходит борьба за кислород, питательные вещества и место обитания. Особенно мощными антагонистическими свойствами обладают нормальные обитатели человеческого тела: E.coli, Str.faecalis, молочнокислые бактерии, актиномицеты, микрофлора кожи, носоглотки и др. Длительное неоправданное применение антибиотиков (особенно энтеральное), нарушение функции верхних отделов желудочно-кишечного тракта (из-за отсутствия энтерального питания, длительной ИВЛ) блокируют защитное действие этих антагонистов патогенной флоры.
2. Условно-патогенные возбудители раневой инфекции обладают высокой степенью избирательности - тропностью 0по отношению к различным тканям. Механизм избирательности обеспечивается с помощью специфических структур микробных поверхностей, называющихся адгезинами, и особых молекулярных образований на поверхности клеток-мишеней (рецепторов). Так адгезины грамположительных кокков
обладают сродством к гепарину, альбумину, к рецепторам эритроцитов, лейкоцитов, лимфоцитов, тромбоцитов, эпителиальных клеток полости рта и верхних дыхательных путей, а грамотрицательные бактерии отличаются высокой тропностью к слизистой желудочно-кишечного тракта (E. coli) и к мочевыводящим путям (E.coli, Ps.aeruginosa), к эпителию дыхательного тракта (Ps.aeruginosa). Вещества, входящие в состав микробных рецепторов клеток организма, стимулируют одни виды микробов и препятствует образованию колоний других. От наличия адгезинов на поверхности бактериальной клетки зависит вирулентность возбудителей. Количественные и качественные характеристики адгезинов определяются условиями среды обитания и, в частности, метаболическим состоянием тканей. В свою очередь, повреждение создает благоприятную концентрацию на клеточных мембранах описанных выше микробных рецепторов, которые одновременно формируют трудно преодолимый для фагоцитов и антибиотиков барьер из скоплений тромбоцитов и фибрина. По-видимому, этот же механизм играет определенную роль в закономерной смене одних возбудителей в ране на другие, когда измененный метаболизм создает условия для адгезии микробов, обладающих тропностью к другим тканям. В результате, бактерии локализуются в особых (в т.ч. поврежденных) тканях, а не повсюду, причем именно там в первую очередь развивается болезнь. Знание этого является одним из ключевых моментов для планирования мероприятий по борьбе с раневой инфекцией.
3. Отличительной чертой раневой инфекции является закономерная смена возбудителей в течение раневого процесса.
В первые сутки после ранения, как правило, высевается грамположительная микрофлора - стафилококки, стрептококки, микрококки, дифтероиды, а также спорообразующие бактерии родов Bacillus и Clostridium. Начиная с третьих суток пребывания раненого в стационаре, увеличивается доля грамотрицательных микроорганизмов. Преобладание последних наблюдается с 7-9 суток. Это главным образом относится к синегнойной палочке, протею и кишечной палочке. Важной причиной смены микробов в ране является способность некоторых возбудителей выделять антибиотики, подавляющие грамположительную флору (пиоцианин синегнойной палочки), т.е. антагонизм микробов.
4. Большинство раневых инфекционных осложнений являются смешанными - аэробно-анаэробными. Поэтому для успешной диагностики и лечения раневой инфекции необходимо знание особенностей анаэробов. Они излагаются в главе об анаэробных формах раневой инфекции. Ведущим представителем грамположительной микрофлоры является стафилококк (St.aureus, St.epidermidis), доля которого среди представителей аэробной флоры свежих ран и острых гнойных процессов составляет 70-85%. Это экзо-эндотоксический микроб. Важнейшими факторами патогенности стафилококков являются:
- выделение альфа-токсина, самого сильного стафилококкового токсина, избирательно поражающего клеточные мембраны и обладающего выраженной кардиотоксичностью;
- наличие фермента гиалуронидазы, расщепляющей основное вещество соединительной ткани - гиалуроновую кислоту. Фермент повышает проницаемость капилляров, усиливает адсорбционную способность эндотелия и тем самым увеличивает отек, развивающийся в результате ранения;
- развитие отека связано также со свертыванием плазмы под действием коагулазы. Последнее свойство ведет к возникновению инфицированных микротромбов в мелких сосудах, что усиливает ишемию тканей, способствует развитию некроза и служит основой образования депо возбудителей, как в тканях, окружающих рану, так и в общей системе микроциркуляции;
- антикоагулазы стафилококка (фибринолизин) тормозят свертывание и ускоряют фибринолиз. Коагуляция плазмы и фибринолиз протекают последовательно. Поэтому стафилококковая инфекция склонна к абсцедированию.
Важнейшим свойством стафилококка является быстрое возникновение антибиотикоустойчивых форм, обусловленное селекцией резистентных штаммов и способностью вырабатывать бета-лактамазу, разрушающую пенициллины и ряд других антибиотиков. В настоящее время 70-80% стафилококков устойчивы одновременно к 4-5 препаратам.
Грамотрицательная флора представлена главным образом синегнойной палочкой (Pseudomonas aeruginosa), протеем (Proteus vulgaris и mirabilis) и кишечной палочкой (Escherichia coli). Колонизация, размножение и патогенное воздействие этой флоры - достоверное свидетельство снижения резистентности организма травмой и предыдущим
инфекционным процессом.
Синегнойная палочка обладает выраженной протеолитической активностью. Ее экзотоксин А (наиболее токсичный из всех продуктов синегнойной палочки) резко подавляет синтез белка в клетках. Эндотоксин поражает сосуды микроциркуляции, усиливает отек, вызывает диапедезные кровоизлияния. Результат ее жизнедеятельности – лизис эпителия и пересаженных лоскутов, подрытость краев раны, замедление и прекращение репаративных процессов, тяжелейшие поражения внутренних органов (гепатоцеллюлярный некроз, геморрагические поражения в легких, тубулярный некроз почечной ткани). Синегнойная палочка, являясь антагонистом грамположительной микрофлоры, при ее подавлении сама беспрепятсвенно размножается, т.к. нечувствительна к большинству применяемых в клинике антибиотиков. Патогенность кишечной палочки при раневой инфекции определяется наличием эндотоксина, действие которого мало отличается от интоксикации, вызванной эндотоксином другого происхождения. Это прежде всего сосудистый яд, вызывающий расстройство микроциркуляции. Под его воздействием повышается проницаемость биологических мембран, в частности лизосомальных мембран, что может стать причиной дегенеративных изменений в клетках вплоть до ферментативного аутолиза. Присутствие в ране протея может придавать инфекционному процессу анаэробный характер. Все перечисленные возбудители раневой инфекции вырабатывают токсические вещества, избирательно повреждающие лейкоциты, подавляющие фагоцитоз, что может приводить к срыву механизмов противомикробной защиты.
Таким образом, на определенной стадии развития возбудителей их патогенные свойства, суммируясь с патогенетическими факторами раневого процесса, формируют качественно новый процесс - раневую инфекцию. Для нее характерно усугубление микротромбэмболизма, усиление отека под воздействием стафилококка; нарушения в системе протеолиза и, как следствие, возникновение очагов вторичного некроза (особенно при анаэробных формах инфекции и синегнойной палочке); усиление общих нарушений (кровообращения, легочных, печеночных и т.д.) под воздействием экзо- и эндотоксинов. Из описанных особенностей патогенеза и этиологии раневой инфекции следует, что развивающиеся патологические изменения в организме в ранние сроки после ранения в большей степени зависят от влияния первичного очага повреждения, то есть, биологического состояния тканей, окружающих рану. Именно в этот период решается вопрос - возникнут ли условия для развития только микрофлоры раны или инфекционный процесс разовьется по полной программе.
Последнее изменение этой страницы: 2017-01-18; Нарушение авторского права страницы
[youtube.player]Мир бактерий удивительно разнообразен и очень богат. Они встречаются везде: в воздухе, почве, на коже человека, на его слизистых. При определенных обстоятельствах бактерии становятся опасными для человека, вызывая серьезные заболевания. Некоторые из них легко поддаются лечению антибиотиками или даже обычными антисептиками, от других избавиться намного сложнее. Поэтому при постановке диагноза, а также при назначении лечения выделяют грамположительные и грамотрицательные бактерии. Такой метод деления микроорганизмов был предложен еще в XIX веке, но используется до сих пор.
Мир бактерий
Царство микроорганизмов настолько разнообразно и сложно устроено, что даже современная наука еще не изучила его полностью. Есть такие бактерии, которые выживают при высоких температурах и не погибают даже при длительном кипячении, другие же гибнут при малейшем изменении температуры или состава внешней среды, например после добавления обычного сахара. Некоторые микроорганизмы прекрасно себя чувствуют в горячих источниках, в кислоте, питаются метаном или другими химическими веществами.
Бактерии - это самые древние организмы и очень широко распространены в мире. Они встречаются везде: на дне океана, в воздухе, в почве - даже на большой глубине, в организме живых существ. Причем, наукой доказано, что клеток бактерий внутри человека в 10 раз больше, чем собственных. Некоторые микроорганизмы просто живут рядом с другими живыми существами, другие же активно с ними взаимодействуют. Они могут приносить пользу или вызывать различные заболевания. Причем полезных бактерий в десятки раз больше, чем патогенных.
Многие микроорганизмы приносят пользу. Например, те, которые обитают в кишечнике человека, участвуют в пищеварении и защищают его от инфекций. Это лактобактерии и бифидобактерии. В полости рта человека обитает около 40 млн видов бактерий, но всего 5 % из них патогенные. Есть микроорганизмы, которые участвуют в разложении отходов. Но, несмотря на то что полезных бактерий все же больше, патогенные их виды приносят много вреда, так как вызывают опасные болезни. До сих пор много человек во всем мире умирает от туберкулеза, холеры, столбняка, брюшного тифа, ботулизма и других инфекций. Поэтому очень важно научиться правильно взаимодействовать с миром бактерий.
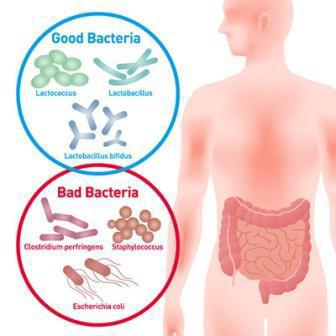
Метод Грама
Человек давно ищет пути лечения инфекционных заболеваний. После того как было обнаружено существование патогенных бактерий, ученые стараются их классифицировать, чтобы выяснить, как с ними бороться. Лучший способ был предложен в 1884 году врачом Гансом Кристианом Грамом. Он довольно простой, но информативный и используется до сих пор. По этому методу различаются грамположительные и грамотрицательные бактерии.
Доктор Грам использовал при изучении микроорганизмов фиолетовый краситель и заметил, что некоторые из них поддаются окрашиванию, другие же - нет. Он выяснил, что связано это с особенностями клеточных стенок бактерий. Так как эти микроорганизмы состоят из одной, реже двух клеток, для них очень важно иметь прочную оболочку. Поэтому клеточные стенки у них имеют сложное строение. Они защищают внутреннюю среду от проникновения жидкостей. Сложнее всего строение у грамотрицательных бактерий. Они устойчивы к проникновению слюны, желудочного сока и других жидкостей.
Суть метода Грама в том, что исследуемую среду обрабатывают анилиновым красителем, фиксируют йодом, а затем смывают спиртом. При этом грамотрицательные бактерии обесцвечиваются, а грамположительные приобретают синюю окраску. После повторной обработки красным красителем отрицательные виды могут окраситься в розовый цвет, причем погибшие микроорганизмы окрашиваются ярче.

Применение метода в медицине
Метод Грама по разделению микроорганизмов на грамположительные и грамотрицательные бактерии способствовал совершенствованию микробиологических исследований. Он помогает выявлять устойчивость патогенных видов к лекарственным препаратам, разрабатывать новые антибиотики для борьбы с ними. Ведь прочная клеточная стенка грамотрицательных бактерий делает их нечувствительными к обычным антибактериальным препаратам. А оболочка грамположительных микроорганизмов, хоть и очень толстая, но проницаема для жидкостей и антибиотиков.
Грамположительные и грамотрицательные бактерии
Метод Грама позволил разделить все микроорганизмы на две большие группы. Их особенности и характеристики помогают выбрать более подходящее лечение инфекционных заболеваний. Грамположительные бактерии, которые быстро окрашиваются в синий цвет анилиновым красителем, образуют споры, экзотоксины, поэтому довольно опасны для здоровья. Но их оболочка проницаема для антибактериальных препаратов.
Как и грамположительные, грамотрицательные бактерии - возбудители серьезных заболеваний. Они не образуют спор, и во многих случаях являются условно патогенными. Но при определенных условиях начинают выделять эндотоксины и являются причиной тяжелого воспаления и интоксикации. Из-за сложного строения клеточной стенки они почти нечувствительны к антибиотикам.
В организме человека содержатся оба вида эти микроорганизмов. Правильное соотношение грамположительных и грамотрицательных бактерий поддерживает нормальную микрофлору влагалища, кишечника, полости рта. Это помогает защищать организм от инфекций.
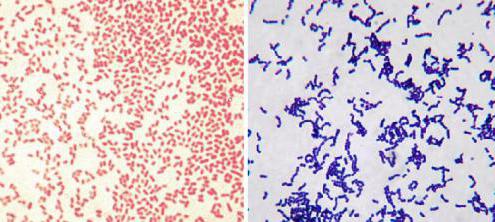
Грамположительная флора
Большинство бактерий, которые поддаются окрашиванию фиолетовым красителем, то есть имеют проницаемую клеточную стенку, опасны для человека. К ним относятся стрептококки, стафилококки, листерии, бациллы, клостридии, микобактерии, актиномицеты. Особенно опасен золотистый стафилококк, который поражает ослабленный организм и без лечения быстро приводит к смерти больного. Но к ним относятся также полезные молочнокислые лактобактерии.
Грамположительные микроорганизмы поражают дыхательные пути, сердечную мышцу, головной мозг, кожу. Они провоцируют гнойную инфекцию в ранах, заражение крови.
Заболевания, которые они вызывают
Именно грамположительные бактерии являются причиной таких распространенных инфекционных болезней, как:
- тонзиллит, фарингит;
- синусит, отит;
- ревматизм;
- заражение крови;
- пневмония;
- воспаление мозга;
- сибирская язва;
- пищевые токсикоинфекции;
- ботулизм;
- дифтерия;
- столбняк;
- газовая гангрена.

Грамотрицательные бактерии
Список их довольно большой, но среди них много таких, которые не приносят никакого вреда человеку. К ним относятся в основном условно патогенные микроорганизмы. В обычных условиях они обитают в организме человека, не причиняя ему вреда. Самыми распространенными являются следующие грамотрицательные бактерии. Виды их разнообразны:
- протеобактерии;
- псевдомонады;
- хламидии;
- менингококки;
- бруцеллы;
- спирохеты;
- гонококки;
- хеликобактерии.
Микроорганизмы, не окрашивающиеся в фиолетовый цвет, являются устойчивыми также к любым антителам и антибактериальным препаратам. Поэтому заболевания, вызываемые ими, очень сложно лечить.
Какие заболевания вызывают
При определенных условиях грамотрицательные бактерии становятся причиной серьезных болезней. Связано это с тем, что сложная оболочка этих микроорганизмов при разрушении выделяет много токсинов, которые, разносясь по кровотоку человека, вызывают сильнейшую интоксикацию. Получается, что патогенны не сами бактерии, а особенности их клеточной оболочки - липополисахаридный слой, который вызывает иммунную реакцию организма. Они приводит к развитию воспаления. Но если у человека иммунитет в порядке, он легко справляется с такими микроорганизмами, и инфекция ему не страшна.
К грамотрицательным бактериям относятся микроорганизмы, вызывающие гонорею, сифилис, менингит и респираторные заболевания. Особенно распространены такие бактерии, котрые вызывают поражение дыхательных и мочевыделительных путей, желудочно-кишечного тракта. К грамотрицательным относятся такие известные возбудители инфекций, как протей, эшерихия, энтеробактерии, сальмонеллы. Они вызывают сальмонеллез, менингит, брюшной тиф, дизентерию. Кроме того, именно такие устойчивые микроорганизмы являются причиной тяжелых внутрибольничных инфекций. Ведь они могут выжить даже после серьезной дезинфекции.
Использование этих знаний при лечении болезней
При диагностике заболевания для определения более эффективного лечения обязательно применяется метод Грама для определения того, какие микроорганизмы вызвали болезнь: грамположительные или грамотрицательные бактерии. Антибиотики назначаются в зависимости от этого. Ведь неправильно выбранное лечение может только усугубить ситуацию.
Для определения возбудителя исследуется мокрота, выделения из носа или влагалища, анализ кала, синовиальной или плевральной жидкости. Эти образцы подвергаются обследованию по методу Грама.
Сложнее всего вылечить заболевания, вызываемые грамотрицательными бактериями. В основном на них воздействуют сочетанием двух антибиотиков или же препараты нового поколения. Эфективными против них могут быть "Ампициллин" или "Амоксициллин", "Хлорамфеникол", "Стрептомицин", а также группа цефалоспоринов. Они могут справиться с внешней мембраной таких бактерий.
Знания о строении стенки бактерий позволило улучшить эффективность лечения инфекционных заболеваний.
[youtube.player]
За последние годы во многих странах мира отмечается значительное увеличение числа заболеваний, вызываемых грамотрицательными бактериями: эшерихиями, синегнойной палочкой, протеем, клебсиеллой, цитробактером, серрацией и др. Эти заболевания в значительной степени являются суперинфекциями или же имеют внутри больничное или послеоперационное происхождение, а их распространение тесно связано с широким применением антибиотиков и других ХТП.
Случаи суперинфекций, вызываемые различными грамотрицательными бактериями (особенно синегнойной палочкой и протеем), участились во многих больницах и в настоящее время занимают второе место после стафилококковых суперинфекции, представляя серьезную проблему.
Многие грамотрицательные бактерии, особенно синегнойная палочка и протей, ранее рассматривались если не как истинные сапрофиты, то как микроорганизмы, лишь в очень редких случаях вызывающие воспалительные, преимущественно местные, заболевания. В настоящее время повсеместно отмечаются вызываемые ими общие и гнойные инфекции, нередко септического характера, тяжело протекающие и слабо поддающиеся лечению.
Одной из основных причин распространения этих заболеваний является бесконтрольное и часто нерациональное применение антибиотиков и других лекарственных средств. Поэтому синегнойная палочка и другие антибиотикоустойчивые бактерии стали частыми возбудителями суперинфекций у больных, получающих ХТП. Ранее послеоперационные инфекции вызывались преимущественно стрептококком, а после появления пенициллина, уже в 50-х годах, в их этиологии стал преобладать стафилококк. Однако широкое применение новых противостафилококковых препаратов привело к значительному увеличению числа случаев, инфекций, вызываемых устойчивой к их действию синегнойной палочкой, реже другими грамотрицательными бактериями.
Увеличение количества подобных заболеваний связано и с широким применением различных иммунодепрессивных препаратов (кортикостероидных гормонов, цитостатиков и др.), а также лучевой терапии, снижающей устойчивость организма больных. В связи с увеличением числа хирургических вмешательств, особенно тяжелых (пересадка органов, операции на сердце и др.), а также различных инструментальных лечебных и диагностических процедур (катетеризация, внутривенные капельные вливаний, зондирование и др.) увеличилось количество входных ворот для условно-патогенных микроорганизмов. Синегнойные и некоторые другие инфекции особенно часто наблюдаются у больных сахарным диабетом, лейкемией, лейкозом и злокачественным и опухолями. После пересадки почек или других органов, сопровождающейся применением иммунодепрессантов, наблюдаются частые случаи синегнойной инфекции, а пневмония, вызываемая этими бактериями, нередка в палатах интенсивной терапии. Не редкими в настоящее время стали и септические заболевания, особенно бактериемии, вызываемые грамотрицательными бактериями. Синегнойный сепсис в 90 % случаев оканчивается смертью больного (M. Courwith, 1974, и др.).
Вызываемые синегнойной палочкой инфекции наиболее часто осложняют различные хирургические, особенно урологические заболевания, при которых они уже значительно превышают количество стафилококковых осложнений. Протей наиболее часто выделяют при заболеваниях мочевых органов и пищевого канала. Все это связано с тем, что основным местом обитания обеих бактерий являются кишки (А. Б. Черномордик, 1958, V. Sutter и V. Hust, 1966). Отсюда они легко проникают в мочевые пути, чему способствуют урологические манипуляции, в частности катетеризация (особенно постоянные катетеры), а также могут попадать в другие органы.
Инфекции, вызываемые грамотрицательными возбудителями, чаще всего наблюдаются у детей, лиц пожилого возраста и особенно часто у лиц, страдающих другими тяжелыми заболеваниями, что объясняется снижением сопротивляемости организма. Многие из этих бактерий, особенно синегнойная палочка, могут размножаться в присутствии ряда распространенных. ХТП (бензилпенициллина, стрептомицина, тетрациклина гидрохлорида, левомицетина, производных нитрофурана и др.), что способствует возникновению вспышек инфекции. Образование этими возбудителями токсинов усугубляет течение заболеваний.
Некоторые грамотрицательные бактерии способны размножаться даже при низкой температуре (в условиях холодильника), что увеличивает возможность массивного загрязнения ими различных сохраняемых при низкой температуре лекарственных растворов, а также консервированной крови. Известно немало случаев синегнойной и протейной инфекции, связанных с введением больным инфицированных этими бактериями растворов пенициллина, изотонического раствора натрия хлорида, различных глазных капель, раствора фурацилина и т, п. Особенно опасно введение таких загрязненных растворов в субарахноидальное пространство, серозные полости или в кровь. Описаны случаи загрязнения синегнойной палочкой стерильной воды, в которой промывали шприцы для инъекций и иглы, а также изотонического раствора натрия хлорида, предназначенного для внутривенного введения. Известны случаи обнаружения этой палочки в моющих и дезинфекционных растворах, находившихся в перевязочных и операционных, особенно в растворе фурацилина.
Многие грамотрицательные бактерии, в частности синегнойная палочка, некоторые штаммы эшерихий, характеризуются значительной антагонистической активностью в отношении кокков и других бактерий. Это также может иметь известное значение в распространении вызываемых ими инфекций, способствуя быстрейшему размножению антагонистически действующих возбудителей.
Наблюдались случаи стимулирования антибиотиками размножения грамотрицательных бактерий. Отмечено, что после исчезновения из гнойных ран патогенных кокков могут возникать тяжелые септицемии, вызываемые синегнойной палочкой, протеем и другими грамотрицательными бактериями. Возможность стимулирования развития синегнойной палочки пенициллином показал L. Garrod (1951), который отметил их появление в моче лечившихся этим антибиотиком больных. Многие исследователи наблюдали размножение различных грамотрицательных бактерий в организме больных, особенно в кишках, в результате применения тетрациклинов, левомицетина, эритромицина и других антибиотиков.
В доантибиотическое время синегнойную палочку обнаруживали у больных довольно редко. Поэтому ее изучение, как правило, проводили самое большее на нескольких десятках штаммов. В настоящее время обычными стали исследования 200—300 и более ее штаммов, а иногда 1500 и более. Так, I. Rivera и соавт., изучали 179 штаммов синегнойной палочки и 1123 штамма протея, а I. Zahorodnacky (1974) — 1574 штамма синегнойной палочки, вы-деленные за 1968—1972 гг. в одной из больниц в г. Пильзене.
Большинство грамотрицательных бактерий, как и патогенный стафилококк, характеризуются высокой устойчивостью ко многим ХТП. У протея, серраций и синегнойной палочки это является врожденной видовой особенностью, а у эшерихий и некоторых других бактерий чаще наблюдается как приобретенное свойство.
Высокая, обычно множественная, лекарственная устойчивость этих возбудителей объясняет случаи слабой эффективности лечения вызываемых ими инфекций, поэтому нередко характеризующихся длительным тяжелым течением и высокой смертностью. Если для лечения современной антибиотикоустойчивой стафилококковой инфекций имеется значительное число активнодействующих препаратов даже на ее антибиотикоустойчивые культуры, то в отношении грамотрицательных бактерий таких препаратов меньше и их ассортимент ограничен.
[youtube.player]Читайте также:


