Хирургическое лечение параколостомической грыжи

Что нужно о ней знать
Одним из наиболее частых осложнений после операции по формированию стомы является параколостомическая грыжа, иногда сопровождаемая постоянной болью. Чаще всего она встречается у людей с колостомой, примерно у 30% из числа прооперированных.
Симптоматика грыжи варьируется от ощущения легкого физического дискомфорта из-за боли при растяжении тканей, до нарушения проходимости стомы из-за сдавливания, что может привести к серьёзным, а порой и к угрожающим жизни осложнениям. В серьезных случаях, выпячивание или видимая опухоль, которую трудно скрыть под одеждой, может причинять стомированным сильные муки, не говоря уже об эстетической стороне дела.
Илона Френч
Откуда же она берется?
Параколостомическая грыжа - это значительное выпячивание кишечника через мышцы брюшнины рядом с местом наложения колостомы. Имеется ряд факторов, влияющих на появление паталогии.
Внутрибрюшное давление создается при чихании или кашле или при поднятии груза. К другим причинам относятся наличие инфекции, ожирение, неправильное выбранное месторасположение стомы или технические погрешности при операции (слишком большое отверстие в брюшной стенке).
Принимаем меры
Как предотвратить появление параколостомической грыжи? Ответить на вопрос нелегко, но есть пара советов, которые могут помочь.
Вы, возможно, думаете, что упражнения по укреплению мышц живота могут снизить шансы развития грыжи или помочь тем, у кого она уже есть. Эти упражнения делать не рекомендовано. Мышцы стомированного человека по существу ослаблены, поэтому определенные виды спортивной тренировки, типа упражнений по приседанию, могут только способствовать образованию грыжи или ухудшить положение дел.
Но это не означает, что стомированные люди и те, у кого имеется грыжа, должны бездейственно сидеть дома. Наоборот, для поддержания нормального веса целесообразно вести активный образ жизни.
Большинство стомированных согласятся, что постоянное ношение фиксирующего пояса будет наилучшим решением для поддержания грыжи предотвращения ее дальнейшего роста.
Для каждого вида деятельности можно подобрать свой тип пояса. Чтобы не ошибиться в выборе, учитывайте:
•Брюшной обхват на линии расположения стомы
•Предпочтительную ширину пояса, что б закрыть стому
•Размер дренажного мешка
•Расположение колостомы (справа, слева)
•Материал, из которого изготовлен пояс
Диагностика и лечение
Во время визита к стома-терапевту, стомированные проходят полное диагностическое обследование.
Несмотря на то, что операция по удалению грыжи рекомендована - кроме случаев, когда она не рекомендуется по медицинским показаниям здоровья больного - при определенных мероприятиях на какое-то время можно уменьшить проявление клинических проявлений, избежав оперативного вмешательства.
Фиксирующий пояс (бандаж), который можно приобрести в большинстве магазинов медтехники, поддерживает область вокруг стомы, уменьшает выпирание и помогает поддерживать крепление дренажного мешка на стоме. Кроме ношения пояса, пациентам рекомендуется расслабиться и, лежа на спине, делать легкий массаж грыжи, попытавшись снизить ее выпячивание.
Согласно Джулии Вильямс, преподавателю медсестринского дела по уходу за пациентами, перенесшими операцию на кишечнике, Универсистет госпиталя St.Mark, Лондон, большинство хирургов неохотно берутся за операции по удалению параколостомических грыж, потому что в 50% случаев такое вмешательство приводит к летальному исходу, особенно при репарации с использованием местных тканей.
Вильямс обнаружила, что при грыже у пациентов возникают трудности во время крепления аксессуаров на перистомальную поверхность, работа стомы становится весьма непредсказуемой. При росте грыжи, вздутие в области колостомы становится заметнее, эвакуация содержимого кишечника сопровождается то диареей, то протекает очень вяло (испражнения сухие, мелкими шариками), что так же осложняет крепление мешка. У некоторых стомированных пациентов при росте грыжи наблюдается появление болей. Так же людям становится тяжелее подобрать одежду, часто приходится брать большие размеры, что б скрыть недостаток.
Иногда операции по коррекции грыжи не избежать.
Выбор способа устранения грыжи зависит от индивидуального случая пациента до самого хирурга. Чаще всего делают перемещение колостомы и накладывают сетку. Как упоминалось раньше, при удалении грыжи напрямую часто возникают рецидивы ее образования из-за наличия давления внутренних органов на ослабленные стенки мышц живота.
Терапевты разрабатывают методы по устранению образования грыж и их рецидивов. Возможно, в будущем данная проблема будет решена.
До настоящего времени эффективность внедрения сеток при первой операции и снижение риска образования грыж после этого пока не была доказана.
Так почему же наиболее предпочтительным является хирургическое удаление грыжи, если известно, что она может заново появится? Когда грыжа и сопутствующее вздутие тканей начинает мешать необходимому креплению дренажной системы, становится слишком большой и сопровождается выраженным болевым синдромом, операция неизбежна.
Так же при росте грыжи кожа начинает сильно растягиваться и истончаться и может лопнуть. Не говоря уже об экстренных ситуациях, когда операцию невозможно отложить даже на время.
Параколостомическая грыжа - осложнение, сопутствующее операции по формированию колостомы. Однако с грыжей можно жить, определенными способами снизив клиническое проявление симптомов и ее рост, грыжу можно удалить хирургическим путем или, следуя советам врачей и медсестер, избежать ее возникновения после операции. При реализации новых методик борьбы с возникновением параколостомических грыж в медицинской практике, не все так плохо, как кажется!
Реферат. Представлены результаты исследования причин, влияющих на развитие параколостомических осложнений после брюшно-промежностной экстирпации прямой кишки по поводу рака у больных, находившихся на лечении с 2005 по 2012 г. Установлено, что на развитие параколостомических осложнений оказывает влияние возраст больных, наличие сопутствующих заболеваний, выраженность анемии, ожирения. Выделение факторов риска и групп пациентов с повышенной степенью риска развития осложнений позволяет дифференцированно подходить к их профилактике.
Ключевые слова: параколостомические осложнения, аллопластический материал, колостома, рак прямой кишки.
В последние десятилетия отмечается неуклонный рост заболеваемости колоректальным раком в России [1]. В структуре смертности от онкологических заболеваний в большинстве развитых стран, в том числе в России, колоректальный рак занимает второе место [2]. Ведущим методом лечения этой патологии является хирургический. При локализации опухоли в нижнеампулярном отделе основным оперативным вмешательством остается брюшно-промежностная экстирпация органа с формированием постоянной колостомы [1, 3]. Параколостомические грыжи живота являются одними из самых распространенных хирургических осложнений и встречаются у 25—40% оперированных пациентов.
Несмотря на появление новых способов наложения колостомы для профилактики возникновения грыж, эти осложнения до сих пор остаются в ряду самых важных проблем колоректальной хирургии.
Основная доля (до 50%) летальных исходов при данном заболевании приходится на лиц старческого возраста. Наличие у таких больных сопутствующих заболеваний, а также возрастная астенизация являются основными прогностическими факторами возникновения параколостомических осложнений, что неблагоприятно влияет на исход хирургического вмешательства.
Цель настоящего исследования — поиск оптимального способа наложения концевой колостомы у больных колоректальным раком после брюшно-промежностной экстирпации прямой кишки.
Материал и методы
• гистологически подтвержденный рак нижнеам-пулярного отдела прямой кишки; возраст > 45 лет;
• возможность проведения планового оперативного вмешательства с предоперационной лучевой терапией;
• сопутствующие заболевания (хронический об-структивный бронхит, эмфизема легких, сахарный диабет, ожирение).
На основании данных предоперационного обследования с помощью модифицированной британской шкалы для колоректальных операций (Cr—POSSUM) [4] для каждого пациента был рассчитан показатель прогнозируемой послеоперационной летальности и послеоперационных осложнений. Данная шкала учитывает влияние 6 физиологических (возраст, наличие сердечной недостаточности, систологическое артериальное давление, частота сердечных сокращений, уровень гемоглобина и уровень мочевины плазмы крови) и 6 хирургических (объем операции, наличие инфекционных процессов в брюшной полости, стадия колоректального рака, срочность хирургического вмешательства) параметров на течение периоперационного периода. Осложнения были разделены на хирургические и нехирургические. Хирургическими считали несостоятельность колостомических швов, кровотечение, нагноение в параколостомической области, эвентарция, пролапс стомы. К нехирургическим относили развитие органных дисфункций.
Из 151 больного мужчин было 64 (42,38%), женщин — 87 (57,61%).
Для выявления зависимости частоты послеоперационных осложнений от возраста все оперированные больные были разделены на следующие группы (табл. 1).

У 111 (73,51%) пациентов на момент постановки диагноза колоректального рака имели место сопутствующие заболевания (табл. 2). Из них 21 (13,90%) пациент ранее не получал патогенетической обоснованной терапии, в дооперационном периоде им проводилась корригирующая медикаментозная терапия. Из 19 (12,58%) больных, поступивших в стационар с анемией различной степени выраженности, 9 (5,96%) в предоперационном периоде потребовалось ге-мотрансфузия. Противоязвенную терапию с учетом эндоскопических признаков у 3 (1,9%) пациентов проводили в дооперационном периоде.

Из 151 больного 144 (95,36%) получили предоперационную лучевую терапию (из них 32 больных — дистанционную гамма-терапию в разовой дозе 2 Гр до суммарной очаговой дозы 38—42 Гр и 112 пациентов — среднефракционную дистанционную гамма-терапию в разовой дозе 5 Гр до суммарной очаговой дозы 25 Гр. У остальных пациентов имелись противопоказания для проведения лучевой терапии: наличие распадающейся опухоли, кровотечение из опухоли и острая кишечная непроходимость.
У 80 (52,98%) больных была II стадия опухолевого процесса (T3-4N0-3M0), у 47 (31,12%) — III стадия (T1-4N1-3M0). Больных с I стадией (T1-2N0M0) было 18 (11,9%) человек, с IV стадией (T1-4N0-3M1) — 6 (3,97%).
По морфологическому строению опухоли преобладала аденокарцинома различной степени дифференцирования у 120 (79,47%) больных. Недифференцированный рак выявлен у 29 (19,2%) больных. Меланома прямой кишки — у 2 (1,3%) пациентов.
Нами выполнено 44 (29,13%) комбинированных операций (табл. 3).

В соответствии с применявшимися в клинике методами формирования концевой колостомы за анализируемый 7-летний период, который в целом отражает поиски путей оптимизации способов создания и профилактики осложнений искусственного заднего прохода, нами были выделены 2 группы больных, правомерность сравнения которых была подтверждена их сопоставлением по целому ряду наиболее важных параметров.
В 1-ю группу (контрольную) включен 101 больной, которым после брюшно-промежностной экстирпации прямой кишки накладывали колостому классическим способом по общепринятой методике, которая заключается в послойном подшивании выводимой кишки к передней брюшной стенке.
Во 2-ю группу (основной ) включено 50 пациентов, которым на конечном этапе операции была сформирована колостома с использованием аллопластиче-ского материала.
Результаты и их обсуждение
Ранние послеоперационные осложнения в области концевой колостомы у больных контрольной группы наблюдались в 19 (18,81%) случаях (табл. 4).

Как видно из табл. 4, в контрольной группе наиболее грозными осложнениями явились заворот тонкой кишки вокруг выведенной стомы (1 пациент), ретракция стомы (2 пациента), некроз стенки выведенной кишки (2 пациента) и перфорация стенки кишки (1 пациент). Все эти осложнении потребовали повторного оперативного лечения, летальных исходов не было.
В основной группе в ранние сроки общее количество параколостомических осложнений составило 7 (14%), они не были связаны с предложенной методикой наложения колостомы.
При изучении отдаленных результатов контрольной группы было отмечено возникновение 14 (13,86%) осложнений в области колостомы у 101 оперированного больного, прослеженные в сроки от 3 мес до 5 лет после радикального вмешательства. Как видно из табл. 5, наибольший удельный вес в структуре осложнений после выписки имели следующие: параколостомические грыжи —7 (6,9%), выпадение кишки (пролапс) — 4 (3,9%). В основной группе поздних осложнений не наблюдали.

В основной группе в раннем послеоперационном периоде гнойно-воспалительные параколостоми-ческие осложнения имели место у 3 (6%) больных, причем в двух случаях они не имели связь с алло-пластическим материалом, процесс локализовался в пределах подкожно-жировой клетчатки. У одного пациента потребовалось пункция серомы под УЗИ-контролем. Все эти осложнения были связаны на этапе освоения методики. При контрольных обследованиях в отдаленные сроки специфических параколостоми-ческих осложнении не отмечено.
Применение разработанного способа колосто-мии привело не только к существенному улучшению непосредственных результатов лечения, но и достоверному сокращению числа ранних и поздних параколостомических осложнений по сравнению с традиционными методами. Это создает реальные предпосылки для полноценной реабилитации радикально оперированных больных раком прямой кишки с сопутствующими заболеваниями и избыточной массой тела.
Все вышеизложенное дает основание считать разработанную методику и технику формирования постоянной колостомы методом выбора при выполнении радикальных хирургических вмешательств по поводу рака нижнеампулярного отдела прямой кишки.
1. Давыдов,М.И.,АксельЕ.М. // Вестник РОНЦ им. Н.Н. Бло-хина РАМН.— 2011. — Т. 22, № 3. — С. 85.
2. Статистика злокачественных новообразований в России и странах СНГ в 2005 г. / под ред. М.И. Давыдова, Е.М. Аксель // Вестник онкологического научного центра им. Н.Н. Блохина РАМН. — 2007. — Т. 18, № 2 (прил. 1).
Парастомальная грыжа
Парастомальные (колостомические) грыжи встречаются достаточно часто. По данным различных авторов, они наблюдаются в 4-10% случаев наложения стом. Основные причины образования парастомальных грыж - неправильное расположение стомы, технические ошибки и инфицирование раны в области выведения стомы. Предрасполагающие факторы - чрезмерное развитие или же отсутствие подкожной жировой клетчатки. В качестве основных профилактических мероприятий формирования данного вида грыж служат трансректальное расположение плоской стомы и правильный расчёт размеров разреза фасциальных слоев передней брюшной стенки.
Хирургическое лечение парастомальных грыж обычно проводят только в 10-20% клинических наблюдений. Низкая хирургическая активность обусловлена эффективностью применения консервативных мероприятий, которые заключаются в ношении специального бандажа. К показаниям для хирургического вмешательства относят большой размер грыжевого мешка, ущемление грыжевого содержимого, рецидивирующую частичную кишечную непроходимость, стеноз и пролапс стомы, косметический дискомфорт.
Для закрытия парастомальных грыж применяют первичный фасциальный шов в сочетании или без его укрепления синтетическим эксплантатом и перемещение стомы в другой отдел передней брюшной стенки.
Послеоперационная вентральная грыжа
К началу XXI века значительно изменилась эпидемиология грыж. Возросшее число хирургических операций привело к резкому увеличению числа пациентов с послеоперационными вентральными грыжами. Основная причина их формирования заключается в расхождении мышечно-апоневротических слоев передней брюшной стенки в области хирургического доступа. Кроме того, причиной формирования послеоперационных вентральных грыж может стать нарушение иннервации мышечно-апоневротических структур передней брюшной стенки после выполненного хирургического вмешательства. При этом развивается паралитическая релаксация мышц с последующей их атрофией и нарушением каркасной функции передней брюшной стенки.
В первые месяцы формирования грыжи грыжевые ворота обычно имеют эластическую консистенцию. Затем прогрессирующий рубцовый фиброз приводит к образованию тяжей и перемычек. Грыжевые ворота становятся грубыми и ригидными, нередко формируются множественные камеры, развивается дегенерация образующих их мышечных структур. Размеры грыжевых ворот послеоперационных вентральных грыж вариабельны, нередко диагностируют их множественный характер, а грыжевой мешок имеет выраженную васкуляризацию. Содержимым грыжевого мешка послеоперационной вентральной грыжи могут быть любые органы брюшной полости. В результате развития спаечного процесса грыжевое содержимое обычно на большом протяжении сращено со стенками грыжевого мешка, что существенно усложняет проведение хирургической операции. Диагностика послеоперационных грыж не представляет трудностей.
Не существует единой общепринятой классификации вентральных грыж. При проведении плановых оперативных вмешательств и определении способа пластики передней брюшной стенки у больных с вентральными грыжами всё большее распространение и популярность получает SWR-классификация, которую разработали J.P. Chevrel и A.M. Rath (1999). Эта классификация учитывает три параметра вентральной грыжи, проста и удобна в практическом применении (табл. 68-2).
Хирургическое лечение при послеоперационных вентральных грыжах
Лечение этой категории пациентов представляет особые трудности. В среднем у 10-15% пациентов, оперированных по поводу вентральных грыж, возникают рецидивы заболевания, а после операций по поводу рецидивных грыж частота нового рецидива увеличивается ещё в 2-3 раза. Послеоперационные грыжи любых размеров лучше всего оперировать под общим обезболиванием с интубационным наркозом. У пожилых пациентов и больных с выраженной сопутствующей соматической патологией метод выбора - применение перидуральной анестезии.
Обработка краёв грыжевых ворот
Грыжевые ворота при послеоперационных вентральных грыжах обычно имеют неправильную форму и нередко разделяются между собой рубцовыми тканями на отдельные фрагменты. Во время хирургического вмешательства в обязательном порядке показано разделение всех рубцовых перегородок с экономным иссечением их краёв, в результате чего грыжевые ворота приобретают овальную форму. Снаружи края грыжевых ворот очищают от жировой клетчатки, а со стороны брюшной полости отделяют от подпаянных органов на протяжении 4-6 см во все стороны. При проведении грыжесечения нередко возникает необходимость устранить последствия спаечного процесса и в брюшной полости. В случаях выявления деформированных и рубцово-изменённых петель тонкой кишки и участков большого сальника последние иногда приходится даже резецировать. Это связано с тем, что спайки нередко становятся причиной болевого абдоминального синдрома и рецидивирующих приступов острой спаечной кишечной непроходимости.
Пластика передней брюшной стенки
Выбор способа пластики передней брюшной стенки при послеоперационных вентральных грыжах определяется величиной и локализацией грыжевых ворот, состоянием тканей передней брюшной стенки, а также объёмом грыжевого образования и степенью снижения объёма брюшной полости. Простое восстановление анатомических соотношений передней брюшной стенки с последующим её ушиванием показано только в ранние сроки после первичного хирургического вмешательства и только лишь при малых размерах грыжевых ворот. В таких случаях при хорошей адаптации мышечно-апоневротических краёв раны без натяжения наиболее часто применяется аутопластика с формированием дупликатуры листков апоневроза в области грыжевых ворот.
Эксплантат выкраивают по форме раны. Его размеры должны перекрывать образовавшийся шов во всех направлениях не менее чем на 4-5 см. Эксплантат укладывают на апоневроз поверх сшитых краёв и фиксируют по периметру к передней стенке влагалища прямых мышц живота. Фиксацию можно выполнять как отдельными узловыми, так и непрерывными швами. Оперативное вмешательство завершают активным дренированием раны с расположением перфорированных дренажей вдоль краёв эксплантата. Дренажи выводят на кожу через контрапертуры в нижнем углу раны и герметично фиксируют к коже. Для достижения полной герметичности раны необходимо ушить подкожную клетчатку и наложить продольный косметический шов на кожу.
В образовавшееся предбрюшинное пространство помещают синтетическую сетку, выкроенную по размерам грыжевых ворот. Сначала эксплантат по периметру подшивают U-образными сквозными швами к апоневрозу и мышцам без завязывания швов. Затем края апоневроза сшивают край в край без образования дупликатуры. После ушивания апоневроза завязывают ранее наложенные U-образные швы.
После выделения грыжевого мешка и вправления грыжевого содержимого в брюшную полость стенки грыжевого мешка сшивают. Затем края грыжевых ворот тщательно освобождают от жировой клетчатки для надёжной фиксации синтетического трансплантата. Для этого апоневроз острым путём освобождают на ширину до 5-6 см, а сосуды, перфорирующие передний листок влагалища прямых мышц живота, тщательно коагулируют или лигируют. Эксплантат выкраивают таким образом, чтобы его размер во всех направлениях превышал дефект апоневроза на 5 см. После выкраивания сетки, её укладывают на апоневроз и без натяжения фиксируют к нему по всему периметру грыжевых ворот непрерывным швом. Затем вторым рядом швов края эксплантата подшивают к апоневрозу.
После завершения фиксации эксплантата рану санируют раствором антисептика с последующей установкой активных дренажей. Операцию завершают ушиванием кожи без натяжения, в связи с этим иссечение избытка кожи рекомендуется выполнять только перед ушиванием операционной раны.
Пластика методом разделения анатомических компонентов
При длительно существующих медиальных послеоперационных грыжах развивается контрактура наружных косых и значительное расхождение прямых мышц живота. При этом объём брюшной полости уменьшается, а внутренние органы перемещаются в грыжевой мешок, который достигает гигантских размеров. Целью хирургического вмешательства при подобных грыжах служит не только закрытие дефекта передней брюшной стенки, но-и увеличение объёма брюшной полости до размеров, при которых репозиция вышедших внутренних органов не приведёт к значительному повышению внутрибрюшного давления.
Увеличение объёма брюшной полости достигается разделением анатомических компонентов брюшной стенки по методике, предложенной Ramirez. При этом виде пластики первоначально мобилизуют грыжевой мешок и передние листки влагалищ прямых мышц живота до спигелиевых линий с обеих сторон. Затем на уровне перехода наружных косых мышц живота в их сухожилия они пересекаются на всём протяжении от рёберной дуги до уровня подвздошной кости. Далее отделяют наружные косые мышцы от внутренних косых мышц живота в латеральном направлении. После проведения мобилизации передняя брюшная стенка становится более растяжимой, и влагалище прямой мышцы на уровне пупочного кольца свободно смещается на 8-10 см в медиальном направлении. Наружная косая мышца остаётся в состоянии контрактуры. В результате этого приёма грыжевые ворота значительно уменьшаются, а объём брюшной полости увеличивается. При этом полностью сохраняется кровоснабжение и иннервация прямых мышц живота; они сближаются между собой и восстанавливают свою функцию.
Раневую поверхность тщательно промывают, производят окончательный гемостаз и дренируют подкожную клетчатку двумя дренажами для активной аспирации. Кожные лоскуты подтягивают медиально и фиксируют как к краям эксплантата, так и по средней линии. Избыток кожи иссекают с последующим наложением швов.
Лапароскопические операции при послеоперационных грыжах
Первые лапароскопические операции по поводу послеоперационных грыж были выполнены в 1991 г. Показания к ним - грыжи, которые сложно закрыть местными тканями, или же есть необходимость симультанного вмешательства на органах брюшной полости.
Положение пациента на операционном столе и операционной бригады зависит от локализации грыжи, при этом оперирующему хирургу необходимо располагаться на противоположной грыже стороне, а зона грыжи должна находиться выше других отделов брюшной полости. Первый троакар вводят в брюшную полость максимально далеко от грыжевых ворот, где наименее вероятен спаечный процесс. После выполнения диагностической лапароскопии вводят дополнительные троакары, разделяют внутрибрюшные спайки, отделяют грыжевое содержимое от стенок грыжевого мешка, определяют расположение грыжевых ворот и их размеры.
Выбор способа пластики передней брюшной стенки у пациентов с вентральными грыжами
При выборе методики расположения эксплантата необходимо учитывать тот факт, что при надапоневротическом его расположении послеоперационный период достаточно часто осложняется формированием серомы послеоперационной раны, а предбрюшинное расположение эксплантата сопровождается техническими трудностями его фиксации. В связи с этим наиболее рационально располагать эксплантат в позадимышечном пространстве на задней стенке влагалища прямой мышцы передней брюшной стенки.
Основное и обязательное условие выполнения пластики передней брюшной стенки при грыжевых образованиях больших размеров (W3-W4) и снижении объёма брюшной полости - наличие в лечебном учреждении анестезиологической и реанимационной службы с соответствующим оснащением и подготовкой.
Эндоскопические методики выполнения оперативных вмешательств используются у пациентов с небольшими размерами вентральных грыж (W1), симультанных оперативных вмешательствах при отсутствии выраженного спаечного процесса в брюшной полости.
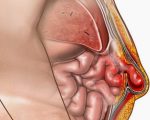
Параколостомическая грыжа (ПКГ) — это выпячивание органов живота, покрытых брюшиной, через патологически сформированные отверстия в области кишечной стомы. Заболевание проявляется периодической или постоянной болью, косметическим дефектом, затруднениями при пользовании калоприемником. Для диагностики ПКГ проводится физикальное обследование пациента, с целью уточнения диагноза назначается рентгенография пассажа бария и УЗИ. В большинстве случаев показана хирургическая коррекция грыжи с последующим закрытием колостомы или сетчатой аллопластикой. Небольшие бессимптомные грыжевые выпячивания подлежат консервативному лечению.
МКБ-10
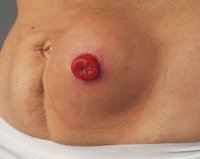
- Причины
- Патогенез
- Классификация
- Симптомы параколостомической грыжи
- Осложнения
- Диагностика
- Лечение параколостомической грыжи
- Консервативная терапия
- Хирургическое лечение
- Прогноз и профилактика
- Цены на лечение
Общие сведения
Параколостомические (парастомальные) грыжи — наиболее распространенное осложнение после вмешательств по выведению колостомы. Анатомическая особенность ПКГ заключается в том, что одной из стенок грыжевого мешка является стенка выведенной кишки. В зависимости от техники хирургического вмешательства патологические образования встречаются у 10-60% пациентов. Грыжи, связанные с наложением колостомы, развиваются в 3 раза чаще, чем после илеостомы. Осложнение в основном возникает у людей старше 75 лет, а также страдающих сопутствующим сахарным диабетом или онкологическими болезнями.

Причины
Основным этиологическим фактором формирования грыж признаны гнойно-воспалительные процессы в параколостомической области. Воспаление нарушает процессы заживления раны, способствует формированию спаек в брюшной полости. Образование грыжевого выпячивания невозможно без наличия факторов риска, которые подразделяются на 3 группы:
- Предрасполагающие. Включают конституциональные особенности человека: недостаточность мышечного каркаса передней брюшной стенки, истощение или ожирение, синдром слабости соединительной ткани. Риск появления параколостомической грыжи повышается у многократно рожавших женщин, которые имеют перерастянутые мышцы живота.
- Производящие. К ним относят упорные запоры, затрудненное мочеиспускание, приступы мучительного кашля. Эти факторы способствуют внезапному повышению внутрибрюшного давления с дальнейшим выпячиванием органов через параколостомическое отверстие. Такая же ситуация возникает при поднятии тяжестей.
- Особенности формирования стомы. При выведении кишки через косые мышцы живота частота осложнения превышает 20%, тогда как при проведении через прямую мышцу — до 3%. Вероятность параколостомической грыжи возрастает при формировании слишком большого отверстия в апоневрозе либо при прочной фиксации брюшины к стенке живота.
Патогенез
Таким образом, сальник и петли тонкой кишки не могут свободно перемещаться по левому боковому каналу живота, как это происходит в норме. При повышении внутрибрюшного давления брюшные органы выходят в сформировавшийся карман. Чаще всего грыжевые ворота образуются около латеральной полуокружности колостомы. Грыжевой мешок постепенно увеличивается, его содержимым могут быть петли толстой и тонкой кишки, большой сальник.
Классификация
По диаметру образования грыжи подразделяют на небольшие (до 10 см), большие (10-20 см), гигантские (более 20 см). По отношению к колостоме выпячивания бывают локализованы с одной стороны от выведенной кишки либо имеют кольцевое расположение вокруг стомы. На основе анатомических особенностей строения грыжевого мешка английский хирург Х.Б. Делвин в 1983 году предложил выделять 4 типа параколостомических грыж:
- Интерстициальная. Грыжевой мешок локализован между мышцами передней стенки живота. Такие грыжи характеризуются асимметричным увеличением колостомы и цианозом кожи вокруг нее.
- Подкожная. Выпячивание проходит вблизи стенки толстого кишечника и располагается на уровне подкожной клетчатки. Мышечные слои брюшной стенки в процесс не вовлекаются.
- Интрастомальная. При данном осложнении подвижные органы живота проникают в выходное отверстие выведенной кишки, но не выпячиваются наружу через колостому.
- Чрезстомальная. Самый редкий тип параколостомической грыжи, когда органы брюшной полости выходят непосредственно через колостому.
Симптомы параколостомической грыжи
По характеру течения грыжи бывают бессимптомными либо сопровождающимися клиническими проявлениями. Бессимптомное или малосимптомное течение характерно для образований небольшого размера, которые не нарушают пассаж каловых масс по кишечнику. Ведущим симптомом параколостомических выпячиваний большого диаметра является боль. Сначала болевые приступы беспокоят при смене положения тела, наклонах, а затем принимают постоянный характер.
Пациенты жалуются на наличие выпячивания в параколостомической зоне, которое болит при надавливании или трении одеждой. В начале грыжа самостоятельно вправляется в брюшную полость, исчезает в положении лежа. В дальнейшем произвольное или ручное вправление органов становится невозможным. Характерно постепенное увеличение образования в размерах. Кожа над грыжей имеет обычный цвет и температуру.
Патогномоничное проявление параколостомической грыжи — нарушение ритма испражнения кишечника. У больных с колостомой со временем устанавливается регулярная порционная дефекация 2-3 раза в день. При развитии грыжевого выпячивания частота выделения кала возрастает до 10-20 раз в сутки, усиливается выделение газов. Частые дефекации сменяются продолжительными запорами.
При нарушениях стула возникают трудности в использовании калоприемника, а при больших выпячиваниях это становится практически невозможным. Такие проблемы оказывают серьезное психологическое давление на человека: пациент с параколостомической грыжей становится раздражительным, тревожным. Больные избегают контактов с друзьями и семьей, что еще более усугубляет невротические реакции.
Осложнения
При длительном существовании параколостомической грыжи наблюдается рубцовое сужение выходного отверстия кишки, что сопровождается тяжелой толстокишечной непроходимостью. Частая травматизация выпячивания провоцирует воспаление в грыжевом мешке, которое заканчивается формированием спаек между кишечными петлями. Реже наступает выпадение петли кишечника через колостому из-за возрастания внутрибрюшного давления.
Опасным осложнением параколостомической грыжи является ущемление органов в грыжевых воротах, которое вызывает ишемию и некроз участка кишечника. В результате формируется флегмона, которая постепенно распространяется по всей полости брюшины с развитием гнойного или калового перитонита. Состояние относят к прогностически неблагоприятным, у ослабленных больных оно нередко заканчивается смертью.
Диагностика
Для постановки диагноза параколостомической грыжи опытному хирургу достаточно произвести физикальный осмотр пациента в горизонтальном и вертикальном положении. Врач обращает внимание на размеры и форму выпячивания, возможность его самостоятельного вправления. Производится пальцевое исследование грыжевых ворот. Чтобы уточнить диагноз, назначают инструментальные методы:
- Рентгенологическое исследование.Рентгенография пассажа бария по кишечнику в динамике проводится для визуализации содержимого грыжевого мешка, установления анатомических взаимоотношений петель тонкой кишки. На рентгенограммах удается обнаружить признаки спаечного процесса.
- Сонография.УЗИ параколостомической грыжи — быстрый и неинвазивный способ визуализации органов, которые находятся внутри грыжевого мешка. Методика помогает выявить осложнения — наличие воспалительного процесса и экссудата, спайки между петлями кишечника.
Лечение параколостомической грыжи
Избежать оперативного лечения возможно при маленьких параколостомических грыжах, которые никак клинически не проявляются. Пациентам подбирают соответствующий калоприемник и детально объясняют особенности его использования. Рекомендуется ограничение физической активности, специальную диету для профилактики запоров. Больные подлежат регулярному диспансерному наблюдению у хирурга.
Абсолютными показаниями к операции служит наличие большой или гигантской параколостомической грыжи, клинических проявлений или осложнений. Хирурги определяют тактику оперативного вмешательства с учетом общего состояния больного и тяжести основного заболевания, по поводу которого накладывалась стома:
- Закрытие временной колостомы. Во время реконструктивной операции ликвидируется кишечная стома и восстанавливается анатомическая целостность кишечника. Вмешательство обеспечивает хорошие отдаленные результаты, возвращает больных к полноценной жизни.
- Реконструктивная операция. Зачастую в абдоминальной хирургии прибегают к герниопластике параколостомической грыжи с применением сетчатого протеза, поскольку такая операция имеет минимальный риск рецидива. Реже проводят иссечение грыжевого мешка и реконструкцию колостомы без пластики.
Прогноз и профилактика
Современные хирургические методики позволяют устранить негативные проявления параколостомической грыжи и значительно снижают вероятность рецидива. Сочетание оперативных и реабилитационных мероприятий улучшает качество жизни больных, поэтому прогноз благоприятный. Вызывают опасение ПКГ, развивающиеся на фоне опухолевого процесса, которые трудно поддаются лечению. Профилактика заключается в ликвидации производящих факторов риска.
Читайте также:


