Интенсивная терапия при энцефалите
Лечение энцефалитов включает патогенетическую, этиотропную, симптоматическую терапию, а также восстановительные мероприятия.
Основные направления патогенетической терапии таковы:
• дегидратация и борьба с отёком и набуханием мозга (10-20% раствор маннитола по 1-1,5 г/кг внутривенно, фуросемид 20-40 мг внутривенно или внутримышечно, 30% глицерол 1 - 1 ,5 г/кг внутрь, ацетазоламид);
• десенсибилизация (клемастин, хлоропирамин, мебгидролин, дифенгидрамин);
• гормональная терапия (преднизолон в дозе до 10 мг/кг В сутки по методу пульс-терапии 3-5 дней, дексаме:газон - 1 6 мг/сут по 4 мг через 6 ч внутривенно или внутримышечно) , оказывающая противовоспалительное, десенсибилизирующее, дегидратирующее действие, а также защищающая кору надпочечников от функционального истощения;
• улучшение микроциркуляции (внутривенное капельное введение изотонического раствора декстрана [мол. масса 30 000-40 000]);
• антигипоксанты (этилметилгидроксипиридина сукцинат и др.);
• поддержание гомеостаза и водно-электролитного баланса (парентеральное и энтеральное питание, калия хлорид, декстроза, декстран [ср. мол. масса 50 000- 70 000], декстран [мол. масса 30 000-40 000], натрия гидрокарбонат) ;
• ангиопротекторы: гексобендин + этамиван + этофиллин, винпоцетин, пентоксифиллин и др.;
• устранение сердечно-сосудистых расстройств (камфора, сульфокамфорная кислота + прокаин, сердечные гликозиды, поляризующая смесь, вазопрессорные препараты, глюкокортикоиды);
• нормализация дыхания (поддержание проходимостидыхательных путей, оксигенотерапия, гипербарическая оксигенация, при бульбарных нарушениях - интубация или трахеостомия, ИВЛ);
• восстановление метаболизма мозга (витамины, полипептиды коры головного мозга скота, гамма-аминомасляная кислота, пирацетам и др.);
• противовоспалительная терапия (салицилаты, ибупрофен и др.).
Специфических методов лечения вирусных энцефалитов пока не существует. При меняют противовирусные препараты - нуклеазы, задерживающие размножение вируса.
В качестве противовирусной терапии назначают интерферон альфа-2, в тяжёлых случаях в сочетании с рибавирином (10 мг/кг в сут в течение 14 дней) . При РНКи ДНК-вирусных энцефалитах эффективно применение тилорона. Используют глюкокортикоиды (метилпреднизолон) по методу пульс-терапии внутривенно до 10 мг/кг В течение 3 сут. Альтернативно при выраженном отёке головного мозга можно первые 3 сут применять дексаметазон (0,5-1 мг/кг в сут на 3-4 приёма внутривенно). При нарушениях сознания и судорогах - маннитол, противосудорожные средства. обязателен перевод на ИВЛ, при судорожном статусе назначают барбитураты, натрия оксибат, диазепам. В тяжёлых случаях можно использовать трансфузии внутривенных иммуноглобулинов. Необходима интенсивная поддерживающая терапия, поскольку у большинства больных происходит полное или почти полное восстановление.
Симптоматическая терапия включает следующие составляющие.
• Антиконвульсантная терапия. Для купирования эпилептического статуса применяют диазепам в дозе 5-10 мг внутривенно на растворе декстрозы, 1 -2% раствор гексобарбитала внутривенно, 1% раствор тиопентала натрия внутривенно, ингаляционный наркоз, фенобарбитал, примидон.
• Антипиретическая терапия. Для снижения температуры используют литические смеси, 2 мл 50% раствора метамизола натрия, дроперидол, местную гипотермию, ибупрофен.
• Терапия делириозного синдрома. Применяют литические смеси, хлорпромазин, дроперидол. Целесообразно назначать магния сульфат, ацетазоламид. Для нормализации сознания применяют биостимуляторы, метаболические препараты (холина альфосцерат), для нормализации психики - транквилизаторы, антидепрессанты.
• Нормализация сна. Применяют бензодиазепины (нитразепам) и другие снотворные средства.
Восстановительное лечение включает несколько компонентов.
• Лечение паркинсонизма. Применяют холинолитики, препараты леводопы (леводопа + бенсеразид), миорелаксанты (толперизон, тизанидин) , препараты, воздействующие на метаболизм мозга. Стереотаксические операции показаны при нарастании ригидности и безуспешности лекарственной терапии.
• Лечение гиперкинезов. Назначают метаболические препараты, α -адреноблокаторы, нейролептики (галоперидол, хлорпромазин), транквилизаторы. Стереотаксические операции показаны при тяжёлых гиперкинезах, не поддающихся медикаментозной терапии.
• Лечение кожевниковской эпилепсии. Применяют препараты, улучшающие метаболизм мозга, антиконвульсанты (вальпроевая кислота, карбамазепин), транквилизаторы (хлордиазепоксид, мепробамат, тетраметилтетраазобициклооктандион) , нейролептики (хлорпромазин). При прогрессирующих формах возможно оперативное лечение.
• Лечение парезов. Назначают препараты, улучшающие метаболизм в мозге и мышечной ткани (трифосаденин, полипептиды коры головного мозга скота, глутаминовая кислота, витамины группы В, витамин Е), энергокорректоры (карнитин и его аналоги, идебенон), препараты, улучшающие нервно-мышечную проводимость (бендазол, галантамин, неостигмина метилсульфат, амбенония хлорид, ипидакрин) . Большое значение в восстановлении двигательных функций имеют лечебная физкультура и массаж, физиотерапия.
• Лечение нейроэндокринных расстройств. Применяют метаболические препараты, десенсибилизирующие средства, транквилизаторы, нейролептики.

Весь контент iLive проверяется медицинскими экспертами, чтобы обеспечить максимально возможную точность и соответствие фактам.
У нас есть строгие правила по выбору источников информации и мы ссылаемся только на авторитетные сайты, академические исследовательские институты и, по возможности, доказанные медицинские исследования. Обратите внимание, что цифры в скобках ([1], [2] и т. д.) являются интерактивными ссылками на такие исследования.
Если вы считаете, что какой-либо из наших материалов является неточным, устаревшим или иным образом сомнительным, выберите его и нажмите Ctrl + Enter.
Лечение энцефалитов включает патогенетическую, этиотропную, симптоматическую терапию, а также восстановительные мероприятия.

[1], [2], [3], [4], [5], [6], [7], [8], [9], [10], [11], [12]
Патогенетическое лечение энцефалитов
Основные направления патогенетической терапии таковы:
- дегидратация и борьба с отёком и набуханием мозга (10-20% раствор маннитола по 1-1,5 г/кг внутривенно, фуросемид 20-40 мг внутривенно или внутримышечно, 30% глицерол 1-1,5 г/кг внутрь, ацетазоламид);
- десенсибилизация (клемастин, хлоропирамин, мебгидролин, дифенгидрамин);
- гормональная терапия (преднизолон в дозе до 10 мг/кг в сутки по методу пульс-терапии 3-5 дней, дексаметазон - 16 мг/сут по 4 мг через 6 ч внутривенно или внутримышечно), оказывающая противовоспалительное, десенсибилизирующее, дегидратирующее действие, а также защищающая кору надпочечников от функционального истощения;
- улучшение микроциркуляции (внутривенное капельное введение изотонического раствора декстрана [мол. масса 30 000-40 000]);
- антигипоксанты (этилметилгидроксипиридина сукцинат и др.);
- поддержание гомеостаза и водно-электролитного баланса (парентеральное и энтеральное питание, калия хлорид, декстроза, декстран [ср. мол. масса 50 000-70 000], декстран [мол. масса 30 000-40 000], натрия гидрокарбонат);
- ангиопротекторы: гексобендин + этамиван + этофиллин, винпоцетин, пентоксифиллин и др.;
- устранение сердечно-сосудистых расстройств (камфора, сульфокамфорная кислота + прокаин, сердечные гликозиды, поляризующая смесь, вазопрессорные препараты, глюкокортикоиды);
- нормализация дыхания (поддержание проходимости дыхательных путей, оксигенотерапия, гипербарическая оксигенация, при бульбарных нарушениях - интубация или трахеостомия, ИВЛ);
- восстановление метаболизма мозга (витамины, полипептиды коры головного мозга скота, гамма-аминомасляная кислота, пирацетам и др.);
- противовоспалительная терапия (салицилаты, ибупрофен и др.).
В настоящее время эту форму называют диффузный склероз Шильдера.
Этиотропное лечение энцефалитов
Специфических методов лечения вирусных энцефалитов пока не существует. Применяют противовирусные препараты - нуклеазы, задерживающие размножение вируса.
В качестве противовирусной терапии назначают интерферон альфа-2, в тяжёлых случаях в сочетании с рибавирином (10 мг/кг в сут в течение 14 дней). При РНК-и ДНК-вирусных энцефалитах эффективно применение тилорона. Используют глюкокортикоиды (метилпреднизолон) по методу пульс-терапии внутривенно до 10 мг/кг в течение 3 сут. Альтернативно при выраженном отёке головного мозга можно первые 3 сут применять дексаметазон (0,5-1 мг/кг в сут на 3-4 приёма внутривенно). При нарушениях сознания и судорогах - маннитол, противосудорожные средства. Обязателен перевод на ИВЛ, при судорожном статусе назначают барбитураты, натрия оксибат, диазепам. В тяжёлых случаях можно использовать трансфузии внутривенных иммуноглобулинов. Необходима интенсивная поддерживающая терапия, поскольку у большинства больных происходит полное или почти полное восстановление.

[13], [14], [15], [16], [17], [18]
Симптоматическое лечение энцефалитов
Симптоматическая терапия включает следующие составляющие.
- Антиконвульсантная терапия. Для купирования эпилептического статуса применяют диазепам в дозе 5-10 мг внутривенно на растворе декстрозы, 1-2% раствор гексобарбитала внутривенно, 1% раствор тиопентала натрия внутривенно, ингаляционный наркоз, фенобарбитал, примидон.
- Антипиретическая терапия. Для снижения температуры используют литические смеси, 2 мл 50% раствора метамизола натрия, дроперидол, местную гипотермию, ибупрофен.
- Терапия делириозного синдрома. Применяют литические смеси, хлорпромазин, дроперидол. Целесообразно назначать магния сульфат, ацетазоламид. Для нормализации сознания применяют биостимуляторы, метаболические препараты (холина альфосцерат), для нормализации психики - транквилизаторы, антидепрессанты.
- Нормализация сна. Применяют бензодиазепины (нитразепам) и другие снотворные средства.
Восстановительное лечение энцефалитов
Восстановительное лечение включает несколько компонентов.
- Лечение паркинсонизма. Применяют холинолитики, препараты леводопы (леводопа + бенсеразид), миорелаксанты (толперизон, тизанидин), препараты, воздействующие на метаболизм мозга. Стереотаксические операции показаны при нарастании ригидности и безуспешности лекарственной терапии.
- Лечение гиперкинезов. Назначают метаболические препараты, а-адреноблокаторы, нейролептики (галоперидол, хлорпромазин), транквилизаторы. Стереотаксические операции показаны при тяжёлых гиперкинезах, не поддающихся медикаментозной терапии.
- Лечение кожевниковской эпилепсии. Применяют препараты, улучшающие метаболизм мозга, антиконвульсанты (вальпроевая кислота, карбамазепин), транквилизаторы (хлордиазепоксид, мепробамат, тетраметилтетраазобициклооктандион), нейролептики (хлорпромазин). При прогрессирующих формах возможно оперативное лечение.
- Лечение парезов. Назначают препараты, улучшающие метаболизм в мозге и мышечной ткани (трифосаденин, полипептиды коры головного мозга скота, глутаминовая кислота, витамины группы В, витамин Е), энергокорректоры (карнитин и его аналоги, идебенон), препараты, улучшающие нервно-мышечную проводимость (бендазол, галантамин, неостигмина метилсульфат, амбенония хлорид, ипидакрин). Большое значение в восстановлении двигательных функций имеют лечебная физкультура и массаж, физиотерапия.
- Лечение нейроэндокринных расстройств. Применяют метаболические препараты, десенсибилизирующие средства, транквилизаторы, нейролептики.
Энцефалит – воспалительное поражение головного мозга, связанное с инфекцией, аутоиммунным или опухолевым поражением нервной ткани. Заболевание протекает остро или хронически, что зависит от особенностей организма человека и причины развития патологии. Симптомы включают в себя интоксикационные явления, а также очаговую неврологическую симптоматику, связанную с поражением конкретных участков центральной нервной системы.
При появлении признаков болезни необходимо сразу же обращаться за медицинской помощью в лечебное учреждение. Патология способна быстро прогрессировать при отсутствии лечения и приводить к тяжелым последствиям, вплоть до летального исхода.
Общая информация

Воспалительный процесс при патологии у взрослых и детей может быть связан с различными группами причин. Для облегчения диагностики и назначения терапии, доктора выделяют следующие категории факторов, запускающих воспаление:
- инфекционные агенты – вирус клещевого энцефалита, менингококковая инфекция, грибковые микроорганизмы и др.;
- аутоиммунные реакции, которые часто развиваются после перенесенных инфекций, например, ветряной оспы (характерный признак аутоиммунитета – демиелинизация нервных волокон);
- паранеопластические процессы, связанные с наличием в организме злокачественного новообразования.
Распространенность воспалительных заболеваний ЦНС вне зависимости от их причины широка. Особенно актуален вопрос инфекционного поражения головного мозга при клещевом вирусном энцефалите. В эндемических по переносчикам возбудителей районах, встречаемость патологии может достигать нескольких случаев на тысячу людей.
Доктора выделяют следующих переносчиков энцефалита при его инфекционной причинной обусловленности:
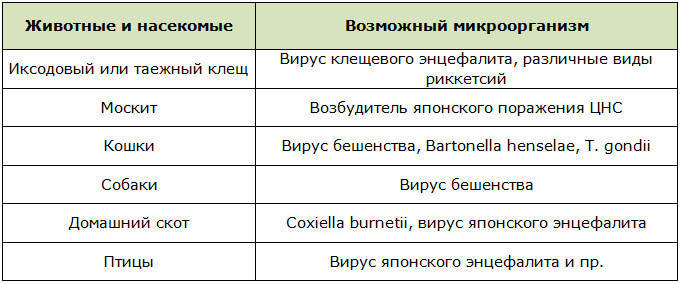
При возникновении вирусного поражения, связанного с вирусами герпеса, полиовирусом, вирусом кори, краснухи и Эпштейна-Барр, важнейшим источником инфекции является больной или вирусоноситель. В этом случае ответ на вопрос – передается ли заболевание от человека к человеку – положительный, так как резервуаром возбудителя является только пациент.
Виды заболевания
Постановка точного диагноза подразумевает определение разновидности болезни, так как это влияет на прогноз для пациента и методы терапии. Выделяют несколько классификаций, основанных на характере патологии, степени тяжести и темпу развития клинических проявлений.
Определение вида энцефалита по причине развития подразумевает деление всех случаев заболевания на две большие группы:
- Первичные – связанные с непосредственным поражением нервной ткани головного мозга инфекционным агентом. Наиболее часто встречается заболеваемость клещевым, японским и герпетическим энцефалитом. В эту группу относят эпидемический энцефалит Экономо, причины которого не до конца ясны, однако, имеются признаки инфекционного характера болезни.
- Вторичные поражения более разнообразны. Их возникновение обычно связано с перенесенными вирусными болезнями, проведенной вакцинацией без учета противопоказаний к ней, бактериальными, грибковыми и паразитарными инфекциями.
По характеру течения выделяют сверхострую, острую, подострую, хроническую и рецидивирующую форму. В зависимости от тяжести клинических проявлений, все случаи заболевания бывают средней, тяжелой и крайне тяжелой степени тяжести.
В клинической практике используются дополнительные виды классификаций: по морфологическим изменениям, по распространенности на структуры центральной нервной системы и по преимущественной локализации поражения. Все они помогают врачу подобрать для больного индивидуальную и эффективную терапию.
Клинические проявления
Острый энцефалит встречается чаще хронической формы. Симптоматика при этом зависит от конкретного возбудителя и характера течения заболевания.
Клещевой вирусный энцефалит
Возбудитель клещевого энцефалита широко распространен в средней полосе России – от Урала до Дальнего востока. Заражение происходит в результате укуса иксодового клеща. Возможно инфицирование при употреблении свежего молока. Продолжительность инкубационного периода колеблется от одного до 30 дней, в зависимости от состояния организма.
Первые признаки энцефалита развиваются остро – повышение температуры тела до высоких значений (39-40°С), общая слабость, общемозговые проявления в виде сильной головной боли и рвоты. При тяжелом течении инфекции возможны нарушения сознания и расстройства психической сферы: бред, галлюцинации, изменения настроения и пр. В отсутствии лечения, патология быстро прогрессирует, приводя к необратимому поражению головного мозга с развитием стойкого неврологического дефицита в виде параличей, парезов, нарушений чувствительности и изменении психической и когнитивной сферы.
Японский энцефалит и его проявления
Основной переносчик – обычные москиты. При заражении инкубационный период длится одну-две недели.
Болезнь начинается с резкого появления лихорадки до 40°С, многократной рвоты, не приносящей облегчения и головной боли. Характерный признак – выраженность интоксикационных проявлений в виде герпетической сыпи на кожном покрове, тахи- или брадикардии, сухости кожного покрова и слизистых оболочек. В зависимости от преимущественной локализации патологического очага у больного выявляют неврологические симптомы в виде нарушений чувствительности, движений, зрения и др.
Болезнь протекает тяжело в связи с постепенным нарастанием симптомов в первую неделю инфекции. Большая часть больных умирает в начальную стадию, что связано с тяжелым поражением головного мозга и возникновением осложнений со стороны дыхательной и сердечно-сосудистой системы.
Поражение герпес-вирусами
Герпетический энцефалит – осложнение инфекции, вызванной вирусом простого герпеса. Подобное состояние может возникнуть у новорожденных детей и людей с выраженным иммунодефицитом.
Болезнь начинается остро с подъема температуры и появления менингиальных симптомов, в связи с первичным поражением мозговых оболочек. Больные отмечают рвоту, сильную головную боль. У большого числа пациентов возникают эпилептические припадки, связанные с раздражением участков головного мозга. Характерно появление очаговых симптомов поражения ЦНС: нарушения зрения, слуха, координации движения, способности человека к вниманию и других когнитивных навыков.
Герпес-связанное заболевание протекает тяжело даже на фоне противовирусной терапии. Всемирная организация здравоохранения отмечает высокий уровень летальности от данного вида патологии по сравнению с другими вирусными поражениями головного мозга.
Диагностические мероприятия

Правильная диагностика энцефалита основывается на комплексном подходе к обследованию. Диагностические мероприятия проводятся по следующему алгоритму:
В процессе обследования лечащий врач проводит дифференциальную диагностику со следующими состояниями: геморрагический инсульт, опухолевое поражение головного мозга, токсическая энцефалопатия, менингит и др. При необходимости проводится консультация со смежными специалистами.
Подходы к терапии
Любой пациент с подозрениями на болезнь или с выявленным заболеванием, должен быть госпитализирован в лечебное учреждение в связи с высоким риском развития тяжелых осложнений, в том числе, летального исхода. Терапия носит комплексный характер и имеет следующие цели:
- борьба с возбудителем;
- устранение интоксикационных явлений;
- восстановление нарушенных функций.
Помимо проведения лечебных мероприятий, организуется постоянное наблюдение за жизненно важными функциями организма (уровень артериального давления, пульс, частота дыхания) и неврологическим статусом.
Из методов немедикаментозной терапии больному назначают постельный режим и приподнятое положение головного конца кровати. Последняя рекомендация позволяет предупредить отек головного мозга за счет облегчения оттока венозной крови из сосудов черепа.
Этиотропная терапия – ключевая часть лечения энцефалита. Используемые лекарственные средства зависят от конкретного возбудителя заболевания:
- При вирусном клещевом энцефалите, пациенту показано введение противоклещевого иммуноглобулина в количестве 0,1 мл на килограмм массы тела. Введение продолжают в течение 5 дней до признаков улучшения состояния человека. Общая курсовая доза лекарства не должна быть меньше 70 мл. В случаях тяжелого течения, курсовую дозу увеличивают. Помимо этого, при выраженной очаговой симптоматике назначается Рибавирин в дозировке 10 мг/кг в сутки.
- Выявление герпетической патологии служит показанием к внутривенному введению Ацикловира на протяжении одной-двух недель. Дозировка рассчитывается на вес пациента – по 10-12 мг на килограмм.
- Лечение цитомегаловирусной инфекции требует внутривенного применения Ганцикловира в дозе 5 мг/кг дважды в сутки. Общая продолжительность терапии от 2 до 3 недель. Дополнительно используется Цитотект 100 Ед на килограмм массы тела по одной дозе каждые два дня до полного исчезновения клинических признаков патологии.
- Для терапии поражения, вызванного японским комариным возбудителем, используют гипериммунную сыворотку людей, которые ранее переболели данными болезнями.
- При бактериальных поражениях терапия осуществляется с помощью антибиотиков, выбираемых в зависимости от выявленного вида микроорганизмов.
Выбор конкретного средства для этиотропной терапии должен осуществляться после идентификации конкретного возбудителя.
Патогенетические методы терапии направлены на прерывание механизмов прогрессирования болезни и развития ее последствий. С этой целью используют ряд подходов.
Для снижения риска развития отека головного мозга применяют дегидратационное лечение, основанное на применении диуретика Маннитола или Фуросемида. Препараты вводят внутривенно дважды в сутки на протяжении 2-4 дней. Помимо этого, противоотечным действием обладают глюкокортикостероиды, например, Дексаметазон. Доза препарата рассчитывается на массу тела больного. Средняя продолжительность приема – 1 неделя.
Предупреждение сенсибилизации организма возможно при использовании Хлоропирамина. Медикамент используют в таблетированном виде в дозировке от 1 до 2 мг на кг массы тела в сутки. Лечение продолжают в течение одной недели.
Интоксикационные явления приводят к ухудшению микроциркуляции во внутренних органах. Для коррекции нарушения используют внутривенное капельное вливание препаратов декстрана. Помимо этого, большое внимание уделяют устранению расстройств работы сердечно-сосудистой и дыхательной системы.
Развитие клинических проявлений приводит к выраженному дискомфорту пациента, а некоторые симптомы, например, лихорадка, могут стать причиной тяжелых последствий. В связи с этим, всем больным назначается симптоматическая терапия:
- жаропонижающие препараты (Парацетамол, литическая смесь);
- устранение судорожного синдрома возможно при использовании Диазепама, Фенобарбитала или Гексенала;
- при признаках делирия и бреда используют Аминазин, Дроперидол и другие антипсихотики.
Выбор конкретной тактики лечения в зависимости от конкретной формы болезни, имеющихся у пациента показаний и противопоказаний всегда производит только лечащий врач. Самолечение невозможно.
Возможности профилактики

Предупредить развитие болезни возможно при некоторых ее клинических формах. Профилактика заболевания может быть специфической и не специфической.
Специфическая защита связана с постановкой прививки от энцефалита. Подобная профилактика разработана в отношении клещевой формы патологии. Вакцинация против клещевого энцефалита проводится как в детском, так и во взрослом возрасте при наличии показаний. Постановка прививки требуется при планировании посещения эндемичных районов или работе на их территории. Вакцинация проводится по следующей схеме: вторая прививка проводится через один месяц после первой, а третья через один год. Подобное введение вакцины обеспечивает формирование иммунной защиты уже после второй прививки, что позволяет человеку избежать возникновения клещевого энцефалита. Ревакцинация проводится один раз в год. В отношении поражений мозга другой инфекционной природы, специфическая профилактика не разработана.
Неспецифическое предупреждение инфекции основывается на следовании рекомендациям докторов:
- Избегать людей, имеющих признаки инфекционной патологии, особенно при наличии признаков иммунодефицита.
- При наличии герпеса, цитомегаловирусной инфекции и других болезней инфекционной природы, необходимо своевременно обращаться за медицинской помощью и не отказываться от назначенного врачом лечения.
- Необходимо исключить факторы, приводящие к иммунодефицитным состояниям: недосыпание, хронический стресс, декомпенсированные болезни внутренних органов, чрезмерные физические нагрузки.
- При возникновении симптомов инфекционного поражения организма на фоне использования иммуносупрессивных препаратов (цитостатики, глюкокортикоиды) необходимо проконсультироваться с врачом по поводу отказа от подобной терапии.
Очень важно, при появлении любых признаков заболевания сразу обращаться за профессиональной помощью, так как энцефалит способен быстро прогрессировать, приводя к осложнениям. Особенно актуально это в отношении детей, у которых болезнь может привести к гибели на фоне отсутствия лечения в течение нескольких суток.
Прогноз для пациента
Важный вопрос для каждого больного человека – лечиться ли энцефалит? При своевременном начале лечения с использованием этиотропных и дезинтоксикационных средств, эффективность терапии высока. Как правило, симптомы болезни и изменения в головном мозге носят обратимый характер и полностью проходят в течение 2-3 недель. Остаточные проявления наблюдаются редко, так как структуры ЦНС сохраняют свою целостность.
При позднем обращении в медицинское учреждение и отсутствии комплексной терапии, болезнь может прогрессировать быстро, особенно в детском возрасте. В этом случае наблюдаются структурные изменения головного мозга с высоким риском развития отека, его дислокации в сторону большого затылочного отверстия и смертью пациента. После лечения у больного может оставаться неврологический дефицит в виде парезов, нарушений работы органов чувств, в том числе, кожной чувствительности, изменения в психической сфере.

Злокачественный нейролептический синдром (ЗНС) является редким, но крайне опасным осложнением нейролептической терапии, протекающим с центральной гипертермией, кататонической симптоматикой с мышечным гипертонусом, нарушением сознания и комплексом соматовегетативных расстройств. Течение ЗНС сопровождается изменениями основных параметров гомеостаза и функции жизненно важных органов и систем организма и может приводить к летальному исходу. Летальность при ЗНС по данным различных публикаций составляет от 5,5 до 10% [5, 9, 13, 29, 34, 37, 43], а частота развития от 2 до 0,01% от всех больных, получающих нейролептики [14, 22, 39, 43]. Наиболее часто ЗНС развивается при проведении нейролептической терапии у больных шизофренией или шизоаффективным расстройством. В мировой литературе описаны случаи развития осложнения у больных аффективными расстройствами, деменцией и органическими психозами [34]. Развитие ЗНС может отмечаться при назначении нейролептиков различных химических групп, вне зависимости от их дозировок. Наиболее часто развитие осложнения отмечено при назначении традиционного антипсихотика – галоперидола [5, 21, 34, 39, 43]. Имеются описания развития ЗНС и при применении атипичных антипсихотиков – клозапина, рисперидона, кветиапина и оланзапина [34, 35, 43], а также на фоне одномоментной отмены психотропных средств [5].
Этиология и патогенез ЗНС остаются до настоящего времени до конца не изученными. Большинство исследователей объясняют развитие ЗНС блокадой дофаминовых рецепторов в базальных ганглиях и гипоталамусе, а не прямым токсическим действием нейролептиков [13, 29]. У больных ЗНС отмечается подавление дофаминегрической и повышение адренегрической и серотонинергической активности [40]. Ряд исследователей рассматривает ЗНС как проявление острой нейролептической энцефалопатии [1]. При этом на ЭЭГ выявляются признаки метаболической энцефалопатии с генерализованным торможением электрической активности головного мозга [14, 43]. Результаты проведенных клинико-патогенетических исследований установили, что в патогенезе ЗНС и фебрильной шизофрении важную роль играют иммунологические нарушения и повышение проницаемости гематоэнцефалического барьера, с нейросенсибилизацией организма и последующим аутоиммунным поражением ЦНС, преимущественно гипоталамуса и висцеральных органов [9, 10]. Доказательством этого является высокая гуморальная сенсибилизация к различным аутоантигенам головного мозга с выявлением антител к лобной доли,зрительному бугру и максимальным количеством (до 66%) к гипоталамусу [9]. Причиной летального исхода являются нарастающие нарушения гомеостаза и, в первую очередь, водно-электролитного баланса и гемодинамики, явления отека мозга.
Анализ патоморфологических изменения у больных ЗНС с летальным исходом в мировой литературе не представлен. Обнаруженные патоморфологические изменения головного мозга при фебрильной (гипертоксической) шизофрении, а ряд исследователей рассматривают ЗНС как вызванную нейролептиками (drug-induced) форму летальной кататонии, не укладываются в какую-либо определенную нозологическую форму и могут быть отнесены к токсико-дистрофическому процессу в сочетании с генерализованными дисциркуляторными нарушениями. В таламо-гипофизарной области мозга у этих больных выявляются следующие изменения:
1) острое набухание, вакуализация, ишемия и гибель нервных клеток;
2) вздутие и набухание миелиновых оболочек ганглиоцитарных волокон;
3) гипертрофия и дистрофические изменения микроглиоцитов [7].
Факторами риска развития ЗНС является наличие у больных резидуальной церебральной органической недостаточности (перенесенные антенатальные и перинатальные вредности, черепномозговая травма, инфекции и интоксикации) [5, 9]. Предполагается, что физическое истощение и дегидратация, возникающие на фоне психомоторного возбуждения, могут приводить к повышению чувствительности к нейролептикам и способствовать развитию ЗНС [21, 43]. К факторам риска ЗНС относится также и наличие кататонических расстройств [43].
Диагностика ЗНС основывается на выявлении основных симптомов осложнения: центральной гипертермии, кататонической симптоматики с развитием ступора и мышечной ригидности, нарушения сознания, а также характерных изменений лабораторных показателей (умеренный лейкоцитоз без палочкоядерного сдвига, лейкопения и ускорение СОЭ, резкая активность КФК в плазме крови).
Наиболее ранним признаком развития ЗНС у больных шизофренией и шизоаффективным психозом, важным для диагностики осложнения, является появление экстрапирамидной симптоматики с одновременным обострением психоза и развитием кататонических расстройств в виде ступора с явлениями негативизма и каталепсии [5, 43] В связи с этим некоторые исследователи рассматривают ЗНС как нейролептический вариант злокачественной или фебрильной кататонии, относя их к заболеваниям одного спектра [3, 31, 30]. Это подтверждается как общностью клинических проявлений фебрильной шизофрении и ЗНС [7, 8, 41], так и сходностью биохимических и иммунологических нарушений [9], а также общими принципами терапии. Они включают отмену нейролептиков, назначение транквилизаторов, проведение инфузионной терапии и ЭСТ [5, 9, 14, 19, 36, 43, 45]. Эффективность агониста дофаминовых рецепторов бромокриптина и миорелаксанта дантролена при ЗНС не подтверждены доказательными исследованиями [6, 37, 38]. Имеются данные об эффективности плазмафереза и гемосорбции [3, 5]. Прогноз течения ЗНС зависит от того, насколько быстро отменяется нейролептическая терапия и назначается интенсивная инфузионная терапия, корригирующая гомеостаз. При своевременной отмене нейролептиков, адекватности проведения инфузионной терапии, дифференцированного применения методов ЭСТ удается в течение первых 3–7 дней добиться терапевтического эффекта у большинства больных [5], в соответствии с рекомендациями DSM-5 ЗНС необходимо дифференцировать с такими заболеваниями как вирусный энцефалит, объемные, сосудистые и аутоиммунные поражения ЦНС, а также с состояниями связанными с употреблением других лекарственных средств (амфетамины, фенциклидин, ингибиторы моноами-ноксидазы, серотонинергические антидепрессанты и рядом других препаратов).
В 2007 году были впервые описаны серии случаев, аутоиммунного NMDA рецепторного энцефалита, протекающего с психотическими симптомами и кататонией, вегетативными нарушениями и гипертермией, и риском развития летального исхода [16]. Симптоматика этого заболевания схожа с ЗНС и фебрильной кататонией и вызывает трудности дифференциальной диагностики [15, 23]. Заболевание вызывается антителами к NR1 и NR2-субединицами глутаматного NMDA-рецептора. Первоначально анти-NMDA рецепторный энцефалит был описан у молодых женщин с тератомами яичников [16]. В последующем вне связи с опухолевым процессом у лиц обоего пола и разных возрастов [26]. Диагностика анти-NMDA рецепторного энцефалита основывается на выявлении в плазме крови и спинномозговой жидкости аутоантител к NR1 и NR2-субъединицами глутаматного NMDA рецептора [17, 18, 20]. В последние годы случаи аутоимунного энцефалита были выявлены у больных психиатрических стационаров с первоначальными диагнозами шизофрения, шизоаффективное расстройство, нарколепсия и большое депрессивное расстройство [42, 46]. Лечение заболевания предусматривает проведение иммунотерапии с назначением иммуноглобулина и метилпреднизолона. Препаратами второй линии, которые используют при отсутствии эффекта, является ритуксимаб в сочетании с циклофосфамидом. Для купирования психомоторного возбуждения могут использоваться транквилизаторы, атипичные антипсихотики или хлопромазин [25, 44]. Имеется положительный опыт применения ЭСТ [12, 24, 27, 29, 32] и плазмафереза [11, 33].
Больная Ш., 1988 года рождения, поступила на лечение в клиническую психиатрическую больницу №4 им. П.Б.Ганнушкина 18.06.2015 г. с диагнозом острое полиморфное психотическое расcтройство.
Неврологический статус: лицо симметричное, зрачки D=S, фотореакция сохранена. Отмечается повышение сухожильных рефлексов. Мышечный тонус не повышен. Менингеальных знаков нет, очаговая неврологическая симптоматика отсутствует.
Данные лабораторного обследования. Исследование общего клинического и биохимического анализов крови и мочи значимых патологических изменений не выявили, RW, ВИЧ, HBSAg, HCV –отрицательные, BD, BL – не выявлены. РПГА – столбняк – 0,77, дифтерия – 0,17. ЭКГ – синусовый ритм, ЧСС 55–62 в минуну. Нормальная ЭОС.
Заключение: явления отека головного мозга на фоне интоксикационного синдрома. Рекомендовано проведение КТ головного мозга, МРТ с контрастом, перевод в стационар с реанимационным отделением. В 19:50 в сопровождении реанимационной бригады больная переведена в ПСО ГКБ им. С.П.Боткина для продолжения лечения и проведения обследования.
При поступлении состояние было расценено как тяжелое. Сохранялась заторможенность с элементами оглушения, не реагировала на обращенную речь, слабо реагировала на болевые раздражители. Отмечалось повышение тонуса в мышцах конечностей и шеи. Заторможенность, которая периодически сменялось возбуждением, ограниченным пределами постели, с повторением отдельных слов по типу речевых стереотипий. В соматическом статусе отмечались бледность кожных покровов, тахикардия до 110 уд. в мин., гипертермия. С целью дифференциальной диагностики демиелинизирующего заболевания и энцефалита проведена люмбальная пункция – цитоз 40 в 3мл, белок 0,33, лимфоциты 37, нейтрофилы 3. Антитела к вирусу Эпштейн-барра, вирус герпеса, микобактерии туберкулеза и к treponema pallidum в ликворе не обнаружены.
После осмотра инфекциониста диагноз вирусного энцефалита был снят. На МРТ головного мозга с контрастированием от 21.07.2015 г. выявлялась зона острого отека в семиовальных центрах справа, которое следует дифференцировать с острым нарушением мозгового кровообращения по ишемическому типу, опухолевым, димиелинизирующим и аутоиммунным заболеванием. Полученные результаты иммунотипирования лимфоцитов ликвора лимфопролиферативное заболевание не подтвердили. В отделении реанимации проводилась инфузионная терапия до 2 л. в сутки под контролем диуреза, дезинтоксикационная терапия, антибактериальная терапия (цефритиаксон, амоксициклин). С 24.07.2015 в схему лечения добавлен дексаметазон 12 мг/сут в/в капельно. Несмотря на проводимую терапию состояние больной оставалось тяжелым отмечалось повышение температуры тела до 40º С, падение артериального давления.
Заключение консилиума врачей от 29.07.2015. Состояние больной тяжелое, сохраняется фебрильная лихорадка и кататоническая симптоматика. Наиболее вероятным представляется наличие у больной фебрильной шизофрении. Выявленные на МРТ-исследовании изменения, учитывая их несоответствие клинической симптоматики, по всей видимости, является случайной находкой и могут быть последствием перенесенного ранее нарушения мозгового кровообращения.
29.07.2015 г. произошла остановка дыхания и сердечной деятельности. Начатые реанимационные мероприятия к восстановлению дыхания и сердечной деятельности не привели. В 22 ч. 15 мин констатирована биологическая смерть.
На вскрытии. Аутоиммунный энцефалит с преимущественным поражением подкорковых структур головного мозга: гиппокампа, таламуса, гипоталамуса. Периваскулярные лимфоплазмоцитарные инфильтраты с выходом иммунокомпетентных клеток в вещество подкорковых структур головного мозга; периваскуллярный и перицеллюлярный отек; дистрофия ганглиоцитов с частичным цитозом и реактивным глиозомом с формированием глиомезодермальных очагов. Причина смерти: смерть больной (первичная причина) наступила от аутоиммунного энцефалита, осложнившимся отеком головного мозга с дислокацией его ствола в большое затылочное отверстие (непосредственная причина смерти).
Тщательное соматическое, лабораторное и инструментальное обследование, в том числе исследование спинномозговой жидкости и МРТ головного мозга с контрастированием, установить причину, которая бы могла лежать в основе развития тяжелого психического и соматического состояния больной не смогло.
Смерь больной наступила на фоне гипертермии и нарастающих явлениях отека мозга, несмотря на отмену нейролептиков, проведение интенсивной терапии и назначения дексаметазона. Данные патологоанатомического исследования выявили у больной проявление аутоиммунного энцефалита с поражением подкорковых структур мозга, что явилось основанием для расхождения диагноза. В то же время у больной не проводились исследования крови и спинномозговой жидкости на выявление аутоантител к NMDA-рецепторам на основании которых диагностируется аутоиммунный энцефалит. Кроме того результаты патоморфологического исследования не противоречат диагнозу ЗНС, поскольку в проведенных клинико-патогенетических исследованиях была доказана важная роль аутоиммунной патологии с преимущественным поражением гипоталамуса в патогенезе развития фебрильных приступов шизофрении [9].
Известно, что нейролептики соединяясь с белками плазмы крови приобретают свойства гаптенов к которым начинают образовываться антитела, блокирующие их антипсихотическое действие [3]. Они же при определенных условиях, по всей видимости, способны спровоцировать развитие аутоиммунного процесса и вызвать развитие ЗНС. Следует отметить, что алгоритм диагностики ЗНС до последнего времени не предполагал исследование крови и спинномозговой жидкости на наличие аутоантител к NMDA-рецепторам. При этом в мировой литературе имеются описания случаев, когда первоначально выставленный диагноз ЗНС пересматривался после обнаружения в крови и ликворе аутоантител к NMDA-рецепторам [23]. Можно предположить, что ранняя диагностика ЗНС с отменой нейролептиков, назначения адекватной инфузионной терапии и проведение ЭСТ позволило бы предотвратить летальный исход. Однако особенностью данного случая явилось то, еще до момента манифестации психоза у больной выявлялись изменения на МРТ мозга в виде участка глиоза, что непозволяло полностью исключить наличие текущего органического заболевания ЦНС и поставить диагноз эндогенного заболевания – шизофрении или шизоаффективного психоза опираясь на структуру психопатологических расстройств.
Литературные сслыки можно просмотреть в оригинале
Читайте также:


