Как принимать преднизолон при красной волчанке
- 19174
- 14,9
- 4
- 4
![]()
Ольга Георгинова
![]()
Антон Чугунов![]()
Андрей Панов
- Аутоиммунитет
- Иммунология
- Фармакология
Системная красная волчанка — это мультифакторное заболевание, развивающееся на основе генетического несовершенства иммунной системы и характеризующееся выработкой широкого спектра аутоантител к компонентам клеточного ядра. Молекулярно-генетические основы болезни изучены довольно плохо, в связи с чем специфического лечения до сих пор не создано, а в основе проводимой в клинике патогенетической терапии лежат иммунодепрессанты — глюкокортикостероиды и цитостатики. И вот, после более чем 50 лет попыток разработать специфическое лечение волчанки, произошел сдвиг: Управление по контролю за качеством пищевых продуктов и лекарств США официально утвердило в качестве лекарства от волчанки препарат Бенлиста (Benlysta) на основе моноклональных антител, специфически блокирующих B-лимфоцит-стимулирующий белок (BLyS).
Системная красная волчанка (СКВ) — одно из самых распространённых аутоиммуных заболеваний, в основе которого лежит генетически обусловленное комплексное нарушение иммунорегуляторных механизмов. При заболевании происходит образование широкого спектра аутоантител к различным компонентам ядра клеток и формирование иммунных комплексов. Развивающееся в различных органах и тканях иммунное воспаление приводит к обширным поражениям микроциркуляторного кровяного русла и системной дезорганизации соединительной ткани [1], [2].
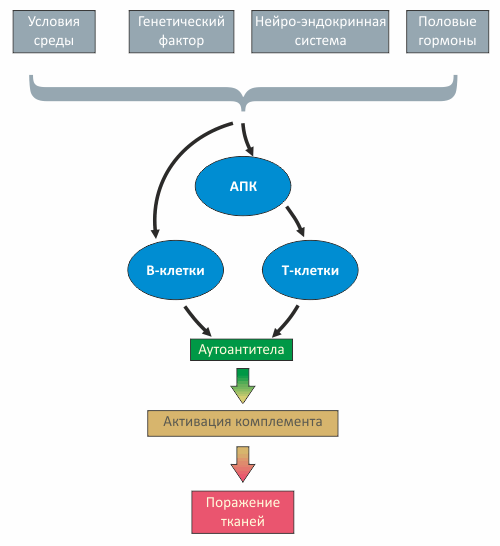
Рисунок 1. Патогенез СКВ
Волчанка во многом связана с нарушениями на уровне пролиферации различных клонов В-клеток, активируемых многочисленными антигенами, в роли которых могут выступать медицинские препараты, бактериальная или вирусная ДНК и даже фосфолипиды мембраны митохондрий. Взаимодействие антигенов с лейкоцитами связано либо с поглощением антигенов антиген-презентирующими клетками (АПК), либо с взаимодействием антигена с антителом на поверхности В-клетки.
В результате поочередной активации то T-, то B-клеток увеличивается продукция антител (в том числе, аутоантител), наступает гипергаммаглобулинемия, образуются иммунные комплексы, чрезмерно и неконтролируемо дифференцируются Т-хелперы. Разнообразные дефекты иммунорегуляции, свойственные СКВ, связаны также с гиперпродукцией цитокинов Th2-типа (IL-2, IL-6, IL-4, IL-10 IL-12).
Одним из ключевых моментов в нарушении иммунной регуляции при СКВ является затрудненное расщепление (клиренс) иммунных комплексов, — возможно, вследствие их недостаточного фагоцитоза, связанного, в частности, с уменьшением экспрессии CR1-рецепторов комплемента на фагоцитах и с функциональными рецепторными дефектами.
Распространённость СКВ колеблется в пределах 4–250 случаев на 100 000 населения; пик заболеваемости приходится на возраст 15–25 лет при соотношении заболевших женщин к мужчинам 18:1. Наиболее часто заболевание развивается у женщин репродуктивного возраста с увеличением риска обострения во время беременности, в послеродовом периоде, а также после инсоляции и вакцинации.
СКВ часто становится причиной инвалидности. В развитых странах в среднем через 3,5 года после постановки диагноза 40% больных СКВ полностью прекращают работать, — в основном, в связи с нейрокогнитивными дисфункциями и повышенной утомляемостью. К потере трудоспособности чаще всего приводят дискоидная волчанка и волчаночный нефрит.
Клинические проявления СКВ чрезвычайно разнообразны: поражение кожи, суставов, мышц, слизистых оболочек, лёгких, сердца, нервной системы и т.д. У одного пациента можно наблюдать различные, сменяющие друг друга варианты течения и активности заболевания; у большинства больных периоды обострения заболевания чередуются с ремиссией. Более чем у половины больных есть признаки поражения почек, сопровождающиеся ухудшением реологических свойств крови [4].
Поскольку молекулярные и генетические механизмы, лежащие в основе заболевания, до сих пор как следует не изучены, специфического лечения волчанки до недавнего времени не существовало. Базисная терапия основана на приёме противовоспалительных препаратов, действие которых направлено на подавление иммунокомплексного воспаления, как в период обострения, так и во время ремиссии. Основными препаратами для лечения СКВ являются:
- глюкокортикоиды (преднизолон, метилпреднизолон);
- цитостатические препараты (циклофосфамид, азатиоприн, метотрексат, мофетила микофенолат, циклоспорин).
Для лечения СКВ применяют также препарат моноклональных антител, селективно действующий на CD20 + В-лимфоциты, — ритуксимаб, зарегистрированный FDA для лечения неходжкинской лимфомы. Впрочем, высокая цена этого препарата не позволила ему получить широкого применения при лечении СКВ в нашей стране.
Исследователи, желая специфически блокировать BLyS, сделали ставку на человеческое моноклональное антитело, разработанное совместно с английской биотехнологической фирмой Cambridge Antibody Technology, и названное белимумаб (belimumab). В начале марта 2011 года американское Управление по контролю за качеством пищевых продуктов и лекарственных препаратов (FDA) впервые за 56 лет одобрило препарат, предназначенный для специфического лечения системной красной волчанки. Эти препаратом стал Бенлиста — коммерческое название антитела белимумаба, производством которого уже занимается компания GlaxoSmithKline. До того FDA одобряла для терапии СКВ гидроксихлорохин — лекарство от малярии; было это в 1956 году.
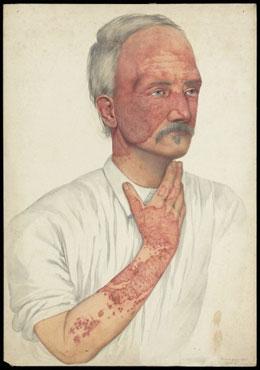
Рисунок 2. Человек, больной системной красной волчанкой (акварель 1902 года кисти Мэйбл Грин). Свое название заболевание получило ещё в средневековье, когда людям казалось, что характерная волчаночная сыпь на переносице напоминает волчьи укусы.
Целенаправленная терапия
Следующие на очереди
Учебная медицинская литература, онлайн-библиотека для учащихся в ВУЗах и для медицинских работников
Системная красная волчанка (СКВ) — системное полисиндромное воспалительное заболевание соединительной ткани, развиваюшееся преимущественно у девушек и молодых женщин на фоне генетически обусловленного дефекта иммунорегуляторных процессов, приводящего к неконтролируемой продукции антител к собственным клеткам и их компонентам.
Лечебная программа при СКВ.
- Режим.
- Диета.
- Лечение гормональными иммунодепрессантами.
- Лечение негормональными иммунодепрессантами.
- Иммунотерапия.
- Интенсивная терапия.
- Лечение аминохинолиновыми соединениями.
- Применение НПВС.
- Лечение антикоагулянтами и антиагрегантами.
- Эфферентная терапия.
- Лечение люпус-нефрита.
- Диспансеризация.
1. Режим
Режим больного СКВ зависит от характера течения, степени активности заболевания, выраженности системных проявлений. Лечение в фазе обострения проводится в стационаре, при тяжелом течении (особенно при развитии диффузного миокардита, эндокардита; люпус-нефрита), высокой активности процесса рекомендуется постельный режим; в случае диффузного миокардита — строгий постельный режим до улучшения состояния, показателей гемодинамики и ликвидации недостаточности кровообращения.
При хроническом течении СКВ и минимальной активности процесса лечение проводится амбулаторно.
2. Лечебное питание
В питании больного следует предусмотреть достаточное количество витамина С, витаминов группы В, ненасыщенных жирных кислот. При развитии недостаточности кровообращения, поражении почек необходимо ограничить потребление поваренной соли, жидкости.
3. Лечение гормональными иммунодепрессантами
Этиологическое лечение СКВ в настоящее время невозможно. Патогенетическая терапия является ведущей и направлена на подавление иммунокомплексной патологии.
Гормональные иммунодепрессанты — глюкокортикоиды — являются лекарствами первого ряда при СКВ.
В. А. Насонова указывает, что обоснована необходимость применения длительной терапии глюкокортикоидами, позволяющей сохранить или продлить жизнь многим больным, значительно улучшить прогноз этого заболевания — от безнадежного до вполне удовлетворительного. Следует учесть, что неадекватное прерывистое лечение глюкокортикоидами сопровождается развитием синдрома отмены с последующими еще более тяжелыми обострениями.
Адекватное лечение глюкокортикоидами в подавляющих дозах, длительное применение их в поддерживающих дозах дает возможность добиться длительной ремиссии. Эффект глюкокортикоидов обусловлен их способностью подавлять иммунокомплексный воспалительный процесс и аутоиммунные реакции.
Абсолютным показанием к назначению глюкокортикоидов является острая, подострая форма СКВ и обострение хронической СКВ. Из всех глюкокортикоидных препаратов наибольшее значение имеет преднизалон, обладающий достаточно высоким терапевтическим эффектом и вызывающий сравнительно нетяжелые побочные реакции при многолетнем приеме. Лучшей переносимостью и хорошим терапевтическим эффектом обладает метилпреднизолон (урбазон). Он значительно реже, чем другие глюкокортикоиды, вызывает поражение ЖКТ (стероидные эрозии и язвы).
Согласно данным В. А. Насоновой, лечение СКВ преднизолоном проводится следующим образом. Доза препарата зависит от остроты течения и активности процесса.
При остром течении с самого начала заболевания, а при подостром и хроническом течении при II и III ст. активности патологического процесса назначаются глюкокортикоиды.
Преднизолон в подавляющей дозе 40-50 мг в сутки назначают при остром и подостром течении (III ст. активности), а при нефротическом синдроме или менингоэнцефалите — в дозе 60 мг в сутки и более.
При подостром течении II ст. активности, а также при хроническом течении II-III ст. активности подавляющая доза может быть меньше 30-40 мг, при I ст. активности — 15-20 мг в сутки. Продолжительность приема преднизолона в подавляющей дозе определяется степенью выраженности клинико-лабораторных признаков (обычно не менее 3 месяцев, а при необходимости — до 6 месяцев и более). В случаях длительной терапии большими дозами глюкокортикоидов можно применять следующую альтернирующую методику приема этих препаратов. При снижении клиниколабораторных признаков активности до II ст. (обязательно исчезновение полиартрита, полисерозита, миокардита) суточную дозу преднизолона можно давать следующим образом: 20 мг утром между 8 и 9 ч после завтрака, два приема по 10 мг в дневные часы (в 12 и 14 ч) после легкого обеда. Достигнув эффекта, дозу преднизолона снижают постепенно: сначала дневную (в 14 ч), затем назначаемую в полдень (в 12 ч), затем утреннюю (после 8 ч утра) (табл. 12).
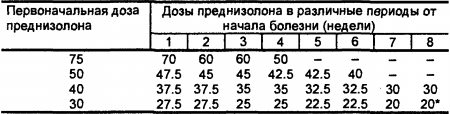
Табл. 12. Примерная схема снижения доз преднизолона (в мг) при достижении терапевтического эффекта. * Далее очень медленно — по 2.5 мг через 1-3 месяца (по показателям общего состояния больного и лабораторных исследований).
Чрезвычайно важен подбор поддерживающей дозы преднизолона, т.е. той наименьшей дозы, которая позволяет поддерживать клинико-лабораторную ремиссию. Преднизолон в поддерживающей дозе 5-10 мг в сутки назначается годами. Для уменьшения побочных явлений преднизолона (кушингоидный синдром, атрофия мышц, артериальная гипертензия, гипокалиемия, остеопороз коры надпочечников) при длительной терапии принимаются удвоенные поддерживающие дозы через день.
Критериями эффективности лечения преднизолоном являются: уменьшение активности патологического процесса, устранение или значительное уменьшение выраженности висцеральных проявлений, особенно со стороны почек, стабилизация течения заболевания.
Величина поддерживающей дозы глюкокортикоидов является одним из критериев глубины клинико-лабораторной ремиссии:
чем меньше поддерживающая доза, тем надежнее ремиссия. Величина поддерживающей дозы 15-20 мг может указывать на активность процесса и на необходимость увеличения дозы, а также, возможно, на целесообразность применения цитостатиков.
Причины неэффективности глюкокортикоидноЙ терапии: нерегулярность приема, неадекватная доза, позднее начало лечения, тяжелая степень иммунокомплексной органной патологии.
При отсутствии преднизолона можно применять триамцинолон, дексаметазон, исходя из паритета : 1 таблетка этих препаратов равна 1 таб летке преднизолона.
О побочных системных действиях глюкокортикоидной терапии см. гл. “Лечение ревматоидного артрита”.
4. Лечение негормональными иммунодепрессантами
Негормональные иммунодепрессанты обладают противовоспалительным эффектом, способностью подавлять иммунокомплексный противовоспалительный процесс и аутоантителообразование.
Показания к назначению цитостатиков:
- высокая активность процесса и быстропрогрессирующее течение;
- активный нефротический и нефритический синдромы;
- генерализованный васкулит (поражение легких, ЦНС, язвенное поражение кожи);
- недостаточная эффективность глюкокортикоидноЙ терапии;
- необходимость быстро уменьшить подавляющую дозу преднизолона из-за плохой переносимости и выраженности побочных действий (подростковый и климактерический возраст больных, значительная и быстрая прибавка в массе тела, тяжелая артериальная гипертензия, стероидный сахарный диабет, психоз, выраженный остеопороз с признаками спондилопатии, аваскулярные некрозы костей);
- необходимость уменьшить поддерживающую дозу преднизолона, если она превышает 15-20 мг в сутки;
- глюкокортикостероидная зависимость.
Наиболее часто применяют азатиоприн (имуран) и циклофосфамид в дозе 1-3 мг на 1 кг массы тела, т.е. от 100 до 200 мг в сутки в сочетании с 30 мг преднизолона. Указанные дозы назначают в течение 2-2.5 месяца (обычно в стационаре), а затем переходят на поддерживающие дозы 50-100 мг в сутки в течение многих месяцев и лет. К этому времени обычно удается снизить дозу глюкокортикоидов.
Критериями эффективности лечения цитостатиками являются:
- исчезновение или уменьшение клинических признаков болезни, в первую очередь нефрита;
- исчезновение или уменьшение кортикостероидной зависимости;
- стойкое снижение активности СКВ и отсутствие в дальнейшем рецидивов;
- предотвращение прогрессирования люпус-нефрита.
Наиболее эффективным цитостатиком при лечении СКВ является циклофосфамид. При высокой активности патологического процесса целесообразно начать лечение с циклофосфамида, но учитывая наибольшую его активность через 4-5 недель следует перейти на азатиоприн или лейкеран для дальнейшего лечения (В. А. Насонова, 1989).
В последние годы стали применять одновременно несколько цитосгатиков: азатиоприн + циклофосфами д (1 мг/кг в д ень внутрь) в сочетании с малыми дозами преднизолона; комбинация азатиоприна внутрь с внутривенным введением циклофосфамида (по 1000 мг/м 2 поверхности тела каждые 3 месяца). При таком комбинированном лечении замедляется прогрессирование люпус-нефрита. Предложена также методика только внутривенного введения циклофосфамида п о 1000 м г/м 2 1 раз в месяц в первые полгода, затем по 1000 мг/м 2 каждые 3 месяца в течение полутора лет на фоне низких доз преднизолона. М. М. Ивановой (1994) установлено, что циклофосфамид более эффективно снижает протеинурию и уменьшает изменения мочевого осадка, синтез антител к ДНК, азатиоприн — наиболее эффективен при диффузном поражении кожи.
О побочных действиях цитостатиков см. в гл. “Лечение ревматоидного артрита”.
5. Иммунотерапия
Разрабатываются следующие методы иммунотерапии СКВ: применение антиидиотипических моноклональных анти-СD4-антител при люпус-нефрите; внутривенное введение иммуноглобулинов (по 0.4 г/кг в сутки в течение 5 дней при выраженных формах СКВ с тромбоцитопенией); лечение любензаритом (подавляет синтез антител к ДНК, ингибирует синтез IgM-ревматоидного фактора); внутривенное введение рекомбинантных препаратов интерферона (а, у) ежедневно в течение 3 недель, а затем дважды в неделю в течен ие 2 м есяцев.
6. Интенсивная терапия
К интенсивной терапии СКВ относятся: пульс-терапия ударными дозами метилпреднизолона, комбинированная пульс-терапия метилпреднизолоном и циклофосфаном.
Показания:
- неэффективность пероральной (даже массивной) глюкокортикоидноЙ терапии, особенно при нефротическом синдроме;
- быстрое прогрессирование болезни и неэффективность обычной терапии СКВ.
Методика пульс-терапии : вводят внутривенно капельно п о 1000 мг метилпреднизолона в 100 м л изотонического раствора натрия хлорида в течение 3 дней подряд. В капельницу добавляют 5000 ЕД гепарина.
Во время пульс-терапии и после нее больные продолжают принимать внутрь ту же дозу преднизолона, что и прежде.
Под влиянием пульс-терапии быстро улучшается функциональное состояние почек, исчезают эритематозная сыпь на лице, капилляриты, полиартрит, в целом наблюдается выраженная положительная клиническая динамика.
Во время пульс-терапии возможны побочные явления: повышение АД, зуд и гиперемия кожи, судорожные подергивания, нарушения ритма сердца, описаны случаи внезапной остановки сердца. Учитывая это, пульс-терапия преднизолоном назначается строго по показаниям и в ходе ее проведения необходимо тщательно контролировать работу сердца.
R. Lugmani (1993) рекомендует после пульс-терапии применять циклофосфамид в дозе 200 мг в неделю в течение 3-6 месяцев в сочетании с преднизолоном в дозе 20-25 мг в сутки.
Этот вид интенсивной терапии применяется при СКВ с тяжелым, торпидным к лечению нефротическим синдромом и генерализованным васкулитом.
Методика: в первый день внутривенно капельно в 100 мл изотонического раствора натрия хлорида в течение 30-40 мин вводя т 1000 мг метилпреднизолона и 1000 мг циклофосфана, в последующие два дня больному вводят капельно по 1000 мг м етилпреднизолона, в капельницу добавляют 5000 ЕД гепарина.
Больным с высоким АД вводят гипотензивные и мочегонные средства. Начиная с четвертого дня, больным назначается преднизолон в той же дозе, что до пульс-терапии, но не ниже 40 мг в сутки в сочетании со средними дозами цитостатиков.
Метод комбинированной пульс-терапии метилпреднизолоном и циклофосфаном высокоэффективен, приводит к значительному клиническому улучшению, особенно это заметно у больных с нефротическим синдромом (снижается или нормализуется АД, повышается диурез, уменьшаются альбуминурия и отеки).
Побочные действия те же, что при пульс-терапии метилпреднизолоном, кроме того, возможны выпадение волос, лейкопения.
7. Лечение аминохинолиновыми соединениями
Механизм действия аминохинолиновых соединений описан в гл. “Лечение ревматоидного артрита”.
Эти препараты назначают больным хронической СКВ прежде всего при поражении кожи, суставов: делагил по 0.25-0.5 г в сутки и плаквенил по 0.2-0.4 г в сутки. Лечение продолжается длительно — месяцы, годы.
Кроме того, аминохинолиновые соединения могут применяться при люпус-нефрите. В. А. Насонова рекомендует в этом случае плаквенил по 0.2 г 4-5 раз в день (всего 0.8-1 г) в течение длительного времени — до года и более.
Аминохинолиновые соединения могут применяться в сочетании с глюкокортикоидами, что позволяет уменьшить дозы препаратов. При лечении аминохинолиновыми соединениями возможны побочные явления: лейкопения, анемия, алопеция, дегенерация сетчатки, диспептические явления. Лечение проводится под контролем анализа крови и исследования состояния глазного дна.
8. Применение НПВС
НПВС обладают выраженным противовоспалительным действием, умеренным иммунодепрессантным эффектом, стабилизируют лизосомальные мембраны.
НПВС назначаются при подостром течении (в ранней стадии) и хроническом течении СКВ, преимущественно при наличии артрита. Эти препараты применяются в обычных терапевтических дозах (как при ревматоидном артрите) длительно, до исчезновения воспаления в суставах и нормализации температуры тела. Однако при лечении НПВС необходимо учитывать нередкое развитие побочных эффектов (см. гл. “Лечение ревматоидного артрита”).
9. Лечение антикоагулянтами и антиагрегантами
Антикоагулянты и антиагреганты в комплексной терапии СКВ применяют при наличии поражения почек, ДВС-синдрома, при нарушениях микроциркуляции.
Из антикоагулянтов рекомендуется гепарин — 10,000-20,000 ЕД в сутки (4 инъекции под кожу живота) в течение нескольких месяцев.
В качестве антиагрегантов используются курантил в суточной дозе 150-200 мг, трентал — 400-600 мг в течение нескольких месяцев.
10. Эфферентная терапия
К эфферентной терапии относятся плазмаферез и гемосорбция.
Плазмаферез — метод эфферентной, экстракорпоральной терапии, направленной на освобождение организма от продуктов метаболизма, циркулирующих иммунных комплексов путем удаления плазмы больного.
Показанием к назначению плазмафереза при СКВ является наиболее тяжелое течение, когда обычная терапия глюкокортикоидами, включая и пульс-терапию метилпреднизолоном, а также применение цитостатиков, оказывается неэффективной.
На курс лечения рекомендуется от 3 до 5 процедур плазмафереза при однократном удалении 800-1000 мл плазмы.
Гемосорбция — экстракорпоральный метод очищения крови путем пропускания ее через колонку с гранулами активированного угля. Метод обладает иммунокорригирующим действием, а также повышает чувствительность клеток крови и тканей к действию глюкокортикоидов.
Показания к гемосорбции при СКВ:
- сохраняющаяся активность СКВ, несмотря на большие дозы глюкокортикоидов и цитостатиков;
- активный люпус-нефрит;
- упорный суставной синдром;
- васкулиты кожи с изъязвлениями;
- невозможность увеличения дозы глюкокортикоидов из-за развившихся осложнений.
М. М. Иванова (1985), учитывая высокую эффективность и хорошую переносимость гемосорбции, рекомендует проводить ее на ранней стадии болезни для более активного воздействия на иммунопатологическую реактивность.
На курс лечения рекомендуется от 3 до 5 процедур гемосорбции, проводимых еженедельно с применением отечественных активированных углей ИГИ, АДБ, ГСУ.
Плазмаферез и гемосорбция проводятся на фоне приема глюкокортикоидов и цитостатиков.
11. Лечение люпус-нефрита
Люпус-нефрит у больных СКВ может принимать тяжелое течение и определять прогноз.
Основными методами лечения люпус-нефрита являются:
- лечение глюкокортикоидами с начальной суточной дозой преднизолона 60-80 мг;
- пульс-терапия метилпреднизолоном;
- комбинированная терапия глюкокортикоидами и цитостатиками;
- пульс-терапия метилпреднизолоном и циклофосфаном;
- лечение аминохинолиновыми соединениями;
- применение гепарина и антиагрегантов;
- плазмаферез, гемосорбция;
- диета № 7 с коррекцией содержания белка в зависимости от уровня его потерь с мочой за сутки при нефротическом синдроме.
М. М. Иванова (1995) предлагает при недостаточной эффективности пульс-терапии проводить лечение метилпреднизолоном внутривенно по 250 мг в сутки в течение еще 2-3 недель.
При развитии у больного ХПН лечение проводится та к, как это описано в гл. “Лечение хронической почечной недостаточности”.
12. Диспансеризация
Диспансеризация больных СКВ осуществляется ревматологом, а при его отсутствии — терапевтом.
Частота наблюдений врачом: при минимальной активности — 2 раза в год, при II ст. активности — 4 раза в год.
ЛОР-врач, стоматолог, гинеколог офтальмолог осматривают больных 2 раза в год; невропатолог, психиатр, нефролог — по показаниям.
Перечень и частота необходимых лабораторных и инструментальных исследований при диспансеризации:
- клинический анализ крови, общий анализ мочи — 4-6 раз в год;
- число тромбоцитов — 2 раз а в год;
- при применении цитостатических препаратов — ежемесячный контроль анализов, рентгенография (флюорография) органов грудной клетк и 2 раза в год;
- рентгенография суставов — по показаниям;
- биохимическое исследование крови (фибриноген, серомукоид, белковые фракции, мочевина) — не реж е 2 раз в год;
- ЭхоКГ и ФКГ — по показаниям;
- исследование крови на содержание волчаночных клеток и антинуклеарного фактора — 2 раза в год.
Основным лечением является применение глюкокортикоидов и цитостатиков в индивидуально подобранных дозах; при III ст. активности — обязательно стационарное лечение.
Если вы нашли ошибку, пожалуйста, выделите фрагмент текста и нажмите Ctrl+Enter.
Лечение системной красной волчанки (СКВ) обычно комплексное, включает активную противовоспалительную и иммуносупрессивную терапию, а также реабилитационные мероприятия. Для индивидуализации терапии важнейшее значение имеет оценка начала и течения болезни, ее активности к моменту госпитализации или амбулаторного обследования больных. Необходимо исключить воздействие провоцирующих факторов: инсоляцию, инфекцию, вакцинации, стрессы, переохлаждение, физиотерапевтические процедуры. С осторожностью следует назначать лекарственные средства, провоцирующие развитие лекарственной волчанки (гидрализин, изониазид, антибиотики, витамины, метилдопа).
Лекарственными средствами первого ряда являются глюкокортикоиды и цитостатические иммунодепрессанты, самостоятельно или в сочетании.
Препаратом выбора в группе глюкокортикоидов является преднизолон (могут назначаться преднизолон, метилпреднизолон (медрол, урбазон), триамцинолон (полькортолон), дексаметазон (дексазон), бетаметазон) — 40-50 мг в сутки при остром и подостром течении (III степень активности), 60 мг и более при наличие нефротического синдрома и менингоэнцефалита; при остром и подостром течении II степени активности и хроническом течение II и III степени активности доза уменьшается до 30-40 мг в сутки, при I степени — до 15-20 мг в сутки. Продолжительность гормонотерапии — до уменьшения клинических признаков, в среднем составляет 3-6 месяцев, затем переход на поддерживающие дозы — 5-10 мг в сутки годами или пожизненно.
В тяжелых случаях при наличии нефротического синдрома, тяжелого церебрального васкулита, цитопении, системного васкулита как метод интенсивной терапии применяют пульс-терапию. При проведении пульс-терапии метилпреднизолон показан внутривенно капельно по 1000 мг на физиологическом растворе 3 дня подряд. В капельницу целесообразно добавить одновременно 5000 ЕД гепарина и 10 мл 10% хлористого калия. В настоящее время для проведения пульс-терапии практически не используется преднизолон, значительно чаще вызывающий побочные действия в сравнении с метилпреднизолоном или бетаметазоном. После больные продолжают принимать ту пероральную дозу кортикостероидных гормонов, которую принимали до процедуры.
С целью усиления противовоспалительного и иммунодепрессивного эффектов возможно проведение комбинированной пульс-терапии. При проведении комбинированной пульс-терапии в первый день внутривенно капельно вводится 1000 мг метилпреднизолона и 600-1000 мг (в зависимости от массы тела больного) циклофосфана. В последующие 2 дня больные получают капельно только по 1000 мг метилпреднизолона. Из побочных явлений комбинированной пульс-терапии следует отметить тошноту, неприятные ощущения в области сердца, тахикардию, редко лейкопению и выпадение волос.
Комбинированная пульс-терапия должна назначаться по строгим показаниям. Она может проводиться только у больных с торпидным и прогрессирующим люпус-нефритом, а также генерализованным васкулитом. При достижении терапевтического эффекта следует перейти к постепенному снижению дозы кортикостероидных гормонов. Принцип таков: чем выше исходная доза гормонального препарата, тем быстрее вначале можно ее уменьшать, и наоборот, чем ниже доза преднизолона, тем более медленным должен быть темп ее дальнейшей отмены. К примеру, если больной принимает 60 мг преднизолона в сутки, то начинать снижение дозы препарата можно по 5 мг в неделю до суточной дозы 50 мг, а затем продолжать снижение дозы в темпе 2,5 мг в неделю до суточной дозы 30-40 мг. В последующем темп снижения еще более замедляется — по 2,5 мг в 2 недели, а при суточной дозе 15-20 мг — по 2,5 мг в 3-4 недели. При этом систематически контролируются состояние больного и лабораторные данные (общий анализ крови и мочи).
Выбор поддерживающей дозы глюкокортикоидного гормона является одним из важных этапов лечения. Оптимальная поддерживающая доза позволяет контролировать течение заболевания на уровне клинико-лабораторной ремиссии или минимальной активности патологического процесса.
Поддерживающая доза преднизолона составляет обычно от 5 до 25 мг в сутки. Чем ниже величина этой дозы, тем надежнее состояние больного и глубже клинико-лабораторная ремиссия. Сравнительно высокая поддерживающая доза (15-25 мг) свидетельствует о сохранении активности процесса и возможности развития рецидива заболевания. Поддерживающую дозу кортикостероидных гормонов должны принимать годами или неопределенно долгий период.
При длительном приеме кортикостероидных гормонов, особенно в избыточной дозировке, развиваются побочные действия препаратов. Для уменьшения побочного действия кортикостероидов рекомендуется особый суточный ритм приема преднизолона, когда максимальная доза препарата (до 2/3 от суточной дозы) назначается в утренние часы, а оставшаяся доза распределяется на день и вечер. Целесообразно также, если необходимо, использовать одновременно препараты калия, кальция, анаболические гормоны.
Кроме кортикостероидных гормонов, большинству больных назначаются аминохинолиновые препараты (делагил, плаквенил, хингамин, хлорохин и др.). Делагил принимается вечером после еды по 1-2 таблетки (0,25-0,5 г в сутки), плаквенил — по 0,2-0,4 г в сутки. Они необходимы в течение многих месяцев или лет. Аминохинолиновые препараты наиболее показаны больным СКВ с поражением кожи и при хроническом течении заболевания.
Основными показаниями к назначению иммунодепрессантов являются: высокая активность и быстрое прогрессирование волчаночного процесса, активные нефротический и нефритический синдромы, недостаточная эффективность глюкокортикоидов, их плохая переносимость и развитие побочных реакций. Наиболее часто у больных системной красной волчанкой применяется азатиоприн (имуран) или циклофосфан (циклофосфамид) в дозе 2-3 мг/кг в сутки. В лечебной дозе препарат назначается на 3-4 месяца, а затем следует перейти на прием поддерживающих доз (50-100 мг в сутки в течение многих месяцев и даже лет. Азатиоприн принимается внутрь, а циклофосфан — парентерально (внутримышечно или внутривенно). При высокой иммунологической активности системной красной волчанки можно начать лечение с парентерального применения циклофосфана для получения более быстрого терапевтического эффекта, а спустя 2-3 недели перейти на прием азатиоприна.
Антиметаболиты (азатиоприн) лучше назначать ежедневно, а для алкилирующих препаратов (циклофосфан) предпочтительнее использовать альтернирующий способ введения. Циклофосфан, как правило, применяется по 200 мг внутривенно струйно через день или по 400 мг 2 раза в неделю.
Абсолютными противопоказаниями для назначения цитостатиков являются беременность и сопутствующий инфекционный процесс в активной фазе. Относительные противопоказания: далеко зашедшая стадия болезни, нарушение функции печени и почек, выраженная гемоцитопения, наличие очагов хронической инфекции, отсутствие возможности для последующего тщательного контроля над больным.
Наличие у больного системной красной волчанкой нефрита любой степени выраженности или признаков генерализованного васкулита является показанием для включения в комплексную терапию гепарина и дипиридамола. Гепарин, будучи антикоагулянтом прямого действия, подавляет внутрисосудистую коагуляцию, кроме того, снижает активность комплемента, оказывает противовоспалительное действие, уменьшает сосудистую проницаемость. На фоне его применения снижается артериальное давление, увеличивается диурез.
Гепарин назначается по 20000-30000 ЕД в сутки. Предпочтительнее вводить его под кожу живота по 5000 ЕД 4 раза в сутки или по другой схеме: вначале вводится 10000 ЕД внутривенно капельно, а оставшаяся суточная доза под кожу живота — в 2-3 инъекциях. Продолжительность курса гепаринотерапии должна составлять 3-10 недель. Гепарин вводится под контролем времени свертывания крови или толерантности плазмы к гепарину.
Дипиридамол (курантил) как дезагрегант препятствует агрегации тромбоцитов, благодаря чему повышается эффективность применения гепарина. Он назначается в суточной дозе 150-400 мг в течение 3-8 месяцев.
Курсы лечения с использованием гепарин-курантиловой схемы у больных с люпус-нефритом рекомендуется проводить 2-3 раза в год. Это позволяет на долгое время сохранить функцию почек в удовлетворительном состоянии.
При агрессивном течении болезни применяют методы экстракорпорального очищения (плазмоферез, лимфоцитоферез, гемосорбция, иммуносорбция), способствующие выведению из организма белковых и белково-липидных комплексов, аутоантител, циркулирующих иммунных комплексов, продуктов метаболизма клеток и других веществ. Плазмоферез проводится через день (3 сеанса в неделю), курс лечения — 3-6 процедур. Гемосорбция — еженедельно, курс лечения — 3-5 сеансов. Плазмоферез и гемосорбция проводятся на фоне терапии глюкокортикоидами и цитостатиками.
Существует несколько методик синхронной интенсивной терапии : 1) серия плазмаферезов из 3-6 последовательных процедур с дальнейшим коротким курсом мегадоз циклофосфамида внутривенно; 2) начальная серия процедур плазмофереза (обычно 3) синхронно с внутривенным введением циклофосфамида (1 г) и метилпреднизолона (3 г) и в дальнейшем по одной процедуре плазмофереза в 1-3 месяца в течение года, синхронно с 1 г циклофосфамида и 1 г метилпреднизолона. Вторая схема синхронной интенсивной терапии представляется более убедительной, так как обеспечивает программный контроль в течение года. Программное назначение комбинации плазмофереза и пульс-терапии метилпреднизолоном и циклофосфамидом показано в первую очередь больным с неблагоприятным жизненным прогнозом, обусловленным началом заболевания в подростковом и молодом возрасте, быстрым развитием нефротического синдрома, быстропрогрессирующим типом нефрита, стойкой артериальной гипертензией и с развитием угрожающих жизни состояний (церебральный криз, поперечный миелит, геморрагический пневмонит, тромбоцитопения и др.).
При поражении суставов при подостром и хроническом течении применяют нестероидные противовоспалительные препараты: диклофенак — 50 мг 2-3 раза в сутки, индометацин — 25-50 мг 2-3 раза в сутки, бруфен — по 400 мг 3 раза в сутки. У больных с поражением кожи и суставов и при умеренной активности патологического процесса применяют аминохинолиновые производные: делагил (0,25-0,5 г в сутки) или плаквенил (0,2-0,4 г в сутки).
Возможно лечение стволовыми клетками, которое основано на способности значительно укреплять иммунитет и направлено на восстановление соединительной ткани, внутренних органов и кожи. При лечении красной волчанки стволовые клетки останавливают прогрессирующее воспаление органов. Попадая в зону гибели клеток, замещают рубцовую ткань, восстанавливая функциональную способность органов.
В настоящее время разрабатывается новая методика лечения с применением подкожных инъекций пептида Р140. Было показано, что пептид не вызывает никаких побочных эффектов. Эффективность Р140 была подтверждена снижением в крови пациентов количества антител к ДНК, которые всегда обнаруживаются у больных системной красной волчанкой. Новый препарат имеет существенное преимущество перед другими препаратами, которые затрагивают работу всей иммунной системы. Р140 не приводит к снижению сопротивляемости организма вирусным инфекциям.
Климатобальнеологическое и физиотерапевтическое лечение противопоказано, возможно санаторно-куротное лечение в ревматологических и кардиологических санаториях.
Прогноз зависит от тяжести заболевания и наличия антифосфолипидного синдрома, при котором прогноз в отношении продолжительности жизни значительно снижается.
"Ревматология"
Т.Н. Бортная
Читайте также:





