Костные дефекты при эндопротезировании
На сегодняшний день эндопротезирование крупных и мелких суставов является одним из самых популярных видов хирургического вмешательства в области травматологии и ортопедии. В западных клиниках объем таких операций составляет в совокупности более 1 миллиона в год. Отечественные клиники эндопротезирования пока в несколько раз отстают, предоставляя услуги по протезированию только 40-50 тысячам больных, хотя потребность в имплантатах гораздо выше.
Методика доказала на практике свою эффективность, однако, даже самые совершенные технологии могут в долгой перспективе привести к возникновению осложнений. Нестабильность частей эндопротеза – самая часто встречающаяся патология, которая может вызвать нежелательные последствия и привести к необходимости повторной операции.
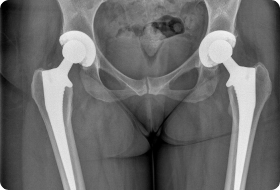
Симптомы нестабильности протеза тазобедренного сустава
Еще в период консультации у лечащего врача пациенту должны объяснить возможные побочные эффекты и осложнения после операции. Непосредственно сам хирург должен предвидеть такие негативные последствия на основании диагностических данных в период обследования больного. Неправильный подбор индивидуального протеза может привести к тому, что он выйдет из строя уже по истечении пяти лет после установки. Повторной операции эндопротезирования можно избежать, если соблюдать все меры предосторожности и не выполнять тех действий, которые могут повредить устойчивости имплантата.

Можно выделить следующие признаки нестабильности эндопротеза тазобедренного сустава:
- Возникновение перманентной ноющей боли в суставе как во время ходьбы, так и в состоянии покоя. Зачастую болевые ощущения усиливаются ближе к ночи (во время сна).
- Потеря опоры для искусственного сустава.
- Общая слабость в нижних конечностях, быстрая утомляемость при ходьбе.
Большинство пациентов заблуждаются, полагая, что перечисленные выше симптомы являются результатом последствий операции, которые пройдут сами по себе в течение короткого времени. на самом деле, все гораздо сложнее. Желательно как можно скорее обратиться к специалисту и пройти диагностические процедуры, которые покажут, требуется ли повторное хирургическое вмешательство.
Все дело в том, что установленный имплантат влияет на движения тазобедренного сустава, как при тотальном эндопротезировании, таки при замене лишь части поврежденного сустава. В результате процесс восстановления костной ткани может замедлиться. Расшатывание ножки протеза в большинстве случаев приводит к развитию местного остеопороза. Таким образом, ограничивается подвижность самого эндопротеза.
К сожалению, современные научные и лабораторные исследования не смогли определить материал для протезов, которые бы не наносил абсолютно никакого вреда здоровью человека. В результате трения компонентов имплантата друг о друга мельчайшие частицы оседают в окружающих тканях, вызывая инфекционные процессы и отмирание тканей. Также может нарушится локальное кровообращение. Поэтому при появлении первых признаков расшатывания эндопротеза тазобедренного сустава следует немедленно обратиться за помощью к лечащему врачу.
Последствия нестабильности
В результате данного явления вживленный имплантат не только теряет фиксацию и расшатывается, но и приводит к постепенному или резкому изменению длины ног. В таком случае требуется немедленная консультация у врача и повторная операция на конечности. К основным причинам можно отнести следующие:
- неправильная установка имплантата;
- недостаточный контакт между поверхностями сустава и протеза;
- сильные нагрузки на имплантат;
- непрочное соединение компонентов изделия.
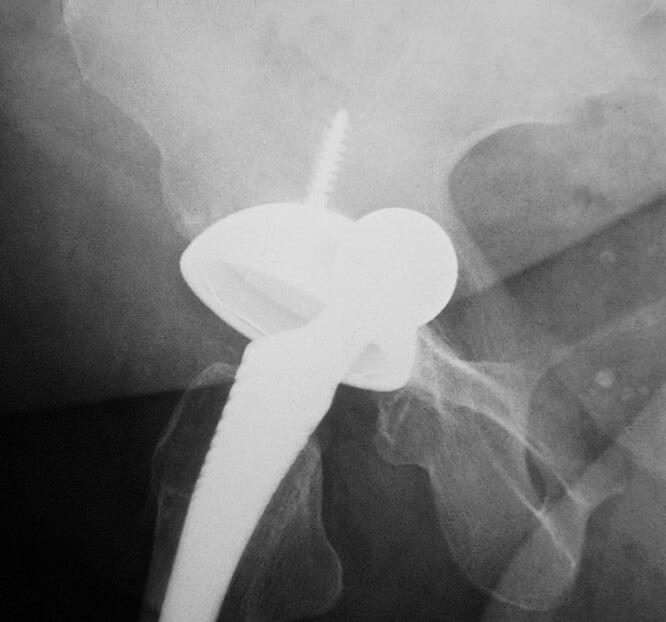
К образованию данного процесса может привести частичное или полное разрушение кости, которое наступает в результате взаимодействия компонентов протеза с живой тканью.
Диагностика переломов протеза, которые периодически случаются, дает основания предположить следующие причины таких последствий. К ним относится:
- неправильный подбор индивидуального имплантата;
- чрезмерная или преждевременная высокая физическая активность пациента;
- избыточный вес пациента.
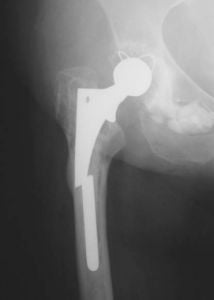
Чтобы предотвратить наступление таких последствий, требуется неукоснительно соблюдать рекомендации, данные врачом, и не заниматься чрезмерно двигательной деятельностью.
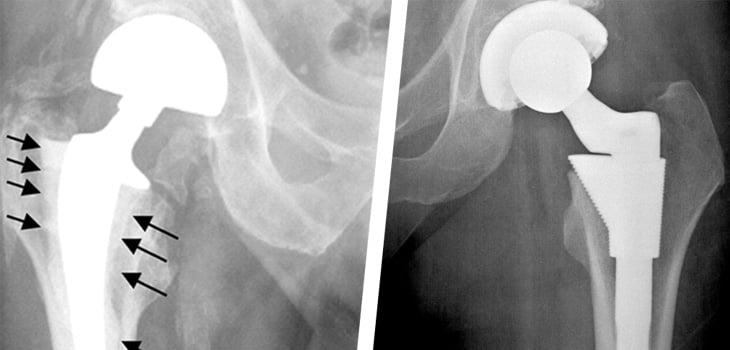
К особым случаям относится расшатывание и повреждение отдельных компонентов протеза. В достаточно короткий срок может разрушится структура полиэтиленового вкладыша или бедренной ножки. Вывих или перелом эндопротеза также случается достаточно часто. Поэтому в обязательном порядке следует соблюдать рекомендации специалистов, а также осуществлять диагностические и профилактические мероприятия. Это гарантировано поможет предотвратить появление негативных последствий операции.
Такие сгустки образуются в сосудах нижних конечностей. Данное осложнение не требует повторного хирургического вмешательства. Достаточно пройти терапевтический курс, назначенный врачом. Он может включать в себя различные физические упражнения для ног либо прием медикаментозных препаратов.
Для предотвращения развития инфекционных процессов специалисты рекомендуют в первые два года после установки протеза принимать антибиотики. Назначение лекарств в каждом случае рассматривается индивидуально, исходя из общего состояния организма пациента.
Диагностика нестабильности протеза
При наступлении первых симптомов нестабильности эндопротеза тазобедренного сустава либо до появления таковых не будет лишним пройти курс диагностических мероприятий. Врач назначит следующие виды обследования:
- рентгенологическое исследование тазобедренного сустава;
- проведение анализа состояния костной ткани и ее плотности с помощью метода денситометрии;
- анализ процессов метаболизма в костной ткани.
В некоторых случаях назначение перечисленных выше мероприятий происходит сразу же после хирургического вмешательства. Особую опасность представляет изначальное наличие у пациента остеопороза, так как именно данная особенность костной ткани может спровоцировать нестабильность протеза после установки.

Методы лечения нестабильности суставного имплантата
Избежать тяжелых последствий поможет своевременная диагностика и лечение. В данном случае удастся достаточно быстро нормализовать и стабилизировать процесс восстановления костной ткани. Также это положительным образом скажется на процессе интеграции протеза в организм человека.
В качестве превентивной меры может быть назначена временная ходьба с помощью костылей. Параллельно назначается курс приема соответствующих лекарственных препаратов. В некоторых случаях пациенту будут рекомендованы определенные физические упражнения для нижних конечностей.

По данным литературы, доля заболеваний коленного сустава среди всех случаев дегенеративно-дистрофических заболеваний суставов конечностей составляет от 21,9 до 29%, причем в 86% случаев страдают лица трудоспособного возраста, у которых прогрессирование заболевания в течение 10-15 лет приводит к инвалидности в 6,2-14,6% случаев [1]. Зачастую методом выбора при лечении пациентов с дегенеративно-дистрофическими заболеваниями суставов становится тотальное эндопротезирование. Одной из проблем, которую нужно решить в процессе тотального эндопротезирования сустава, это замещение костных дефектов в ложе эндопротеза. Их доля при заболеваниях коленного сустава составляет от 25 до 31% [2].
Причинами формирования дефектов и, как следствие, грубых деформаций являются:
- асептический некроз мыщелков, который, по данным различных авторов, составляет от 8 до 22% всех дегенеративно-дистрофических заболеваний коленного сустава,
- кистовидная перестройка эпифизов бедренной и большеберцовой костей,
- посттравматическая импрессия суставной поверхности 4.
Существует достаточное количество классификаций костных дефектов при первичном и ревизионном эндопротезировании коленного сустава [7]. Мы используем наиболее удобную, нашедшую широкое клиническое и научное применение классификацию AORI, разработанную G.A. Engh в Anderson Ortopaedic Research Institute (AORI США, 1997) [8]. Классификация основана на дооперационной рентгенологической оценке состояния костей, с помощью предварительно заданных критериев. В соответствии с этой классификацией выделяют четыре типа состояния бедренной или большеберцовой костей:
1 тип – интактная кость;
2А тип – повреждённая губчатая кость, кость противоположного мыщелка остается неизменной;
2В тип – симметричная потеря костной массы с вовлечением обоих мыщелков или плато;
3 тип – повреждение губчатой и кортикальной кости.
Классификация AORI достаточно четко показывает корреляцию наличия и размеров костных дефектов с ростом потребности использовать металлические блоки, клинья и/или структурированные трансплантаты. У данной методики существует лишь один минус. По современным данным, в группах I и IIA дефекты кости до 5 мм в 46% случаев посредством дооперационных рентгенограмм диагностированы не были [9].
При выполнении тотального эндопротезирования коленного сустава (ТЭКС) преследуется основная цель – создание долговременной надежной опоры для компонента эндопротеза. В случае имеющегося костного дефекта она может достигаться такими способами, как:
- резекция по дну дефекта,
- цементная пластика с армированием или без армирования,
- замещение металлическим блоком,
- костная аллопластика 10.
При детальном рассмотрении у каждого метода отмечаются свои преимущества и недостатки. Преимуществом замещения костного дефекта путем выполнения резекции по дну дефекта является простота и быстрота выполнения. Недостатком становится снижение количества ткани большеберцовой кости в дистальном направлении. Не исключена ситуация, что на максимальном вкладыше стабильность сустава не будет достигнута. Кроме того, при возникновении необходимости выполнения реэндопротезирования у этой группы пациентов хирург может столкнуться с такой проблемой, как обширный дефект большеберцовой кости. Таким образом, этот вариант замещения костного дефекта не является методом выбора. Его применение допустимо при неглубоких дефектах [12]. По нашим данным, резекция по дну дефекта выполнена у 5% пациентов с имеющимся костным дефектом.
Замещение костного дефекта путем цементной пластики с армированием или без армирования винтами также отличается простотой и дешевизной. Недостатки метода заключаются в том, что непросто добиться адекватной прессуризации цемента при нарушении целостности кортикальной кости. Изменение объема цемента во время полимеризации может достигать 2%. Неравномерное распределение нагрузки на подлежащую кость при эксцентрически действующих силах может приводить к нарушению прочности фиксации. Этот метод используется для замещения достаточно глубоких дефектов, при условии соблюдения правил прессуризации цемента и планирования вектора нагрузки [12]. По нашим данным, такое замещение выполнено у 82% пациентов с имеющимся костным дефектом.
Преимущество метода замещения костного дефекта путем костной аутопластики заключается в максимальном сохранении костной ткани метаэпифиза. К недостаткам метода относятся: существенные ограничения в выборе размера трансплантата, риск коллапса, если структура трансплантата повреждена патологическим процессом, и риск несращения. Метод применяется при наличии трансплантата с соответствующими характеристиками (размер, плотность). По нашим данным, такое замещение выполнено у 7% пациентов с имеющимся костным дефектом.
Достоинством замещения костного дефекта металлическим блоком или клином следует считать быстрое создание надежной опоры для имплантата, даже в условиях обширных дефектов. К недостаткам метода относятся ограничения по размеру и форме трансплантата, необходимость специальных инструментов и компонентов эндопротеза. Увеличивается общая стоимость имплантата. При наличии специального инструментария и соблюдении правил имплантации метод применим для замещения любых дефектов [12; 13]. По нашим данным, замещение костного дефекта этим методом выполнено у 6% пациентов.
Цель исследования: улучшить результаты первичного эндопротезирования коленного сустава у пациентов, имеющих костный дефект большеберцовой кости до 2А по AORI.
Материал и методы. В Новосибирском НИИТО за 2012-2015 годы выполнено 7096 операций первичного эндопротезирования коленных суставов. В 2157 (30,4%) случаях был диагностирован требующий замещения костный дефект как бедренной, так и большеберцовой кости [14].
С целью восстановления биомеханики коленного сустава и создания долговременной надежной опоры для компонентов эндопротеза у пациентов, имеющих костный дефект большеберцовой кости до 2А по AORI, нами разработан и внедрен в клиническую практику способ аутопластики большеберцовой кости при первичном эндопротезировании коленного сустава.
Данная методика выполняется соответственно стандартным этапам эндопротезирования, но имеет некоторые особенности: после выполнения резекции суставной поверхности большеберцовой кости определяется остаточный костный дефицит мыщелка большеберцовой кости. По классификации AORI для аутопластики допускается дефицит не больше T2А. При формирования межмыщелкового бокса бедренной кости производится одновременный забор аутокости. Производится обработка костного аутотрансплантата до придания ему правильной геометрической формы (рис. 1).
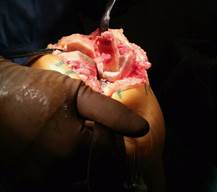
Рис. 1. Забор аутотрансплантата, придание ему правильной геометрической формы
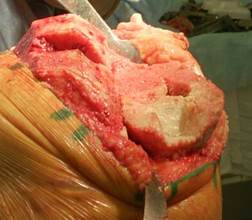
Рис. 2. Обработанный дефект большеберцовой кости со
сформированной опорной площадкой
В последующем аутотрансплантат устанавливается в сформированное ложе и производится импакция до фиксации (рис. 3).
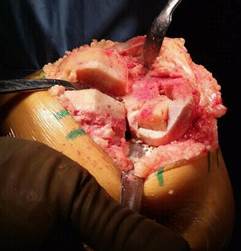
Рис. 3. Импакция аутотрансплантата в сформированном ложе
Дальнейший ход операции соответствует стандартным этапам при первичном эндопротезировании коленного сустава. Восстановительный период не имеет каких-либо особенностей по сравнению со стандартным течением [15].
Клинический пример. Пациент С., 65 лет. Диагноз: левосторонний посттравматический гонартроз 3 степени. Дефект медиального мыщелка левой большеберцовой кости. Варусная деформация левой нижней конечности. Комбинированная контрактура левого коленного сустава. Синдром левосторонней гоналгии (рис. 4).
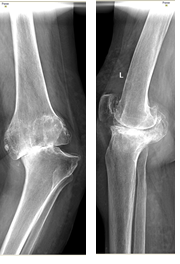
Рис. 4. Рентгенограмма коленного сустава в прямой и боковой проекциях
Пациенту проведено оперативное лечение: эндопротезирование левого коленного сустава с аутопластикой медиального мыщелка большеберцовой кости. Послеоперационный период протекал без особенностей, пациенту была проведена стандартная реабилитация.
На контрольных осмотрах через 6 месяцев, 1 и 2 года после проведенного хирургического лечения пациент отметил хороший результат проведенного лечения, выражающийся в увеличении объема движений в коленном суставе, повышении его стабильности и восстановлении нормальной оси конечности. На контрольной рентгенограмме коленного сустава через 2 года после операции аутотрансплантат состоятелен (рис. 5).
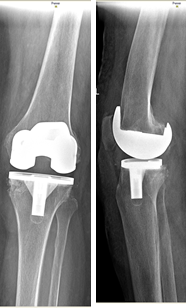
Рис. 5. Контрольная рентгенограмма коленного сустава в прямой и
боковой проекциях через 2 года после операции
Таким образом, у пациентов, имеющих костный дефект большеберцовой кости 2А по AORI, при первичном эндопротезировании коленного сустава выполнение аутопластики по разработанной методике приводит к хорошим результатам, выражающимся в создании долговременной надежной опоры для компонентов эндопротеза, что увеличивает срок его службы за счет нормализации распределения нагрузок в прооперированном коленном суставе.
1. При первичном эндопротезировании коленного сустава максимальное сохранение костной ткани облегчает хирургическую тактику при последующих хирургических вмешательствах, что очень важно у молодых пациентов.
3. Аутопластика должна выполняться при отсутствии противопоказаний.

КЛИНИЧЕСКАЯ ОЦЕНКА ПРИМЕНЕНИЯ КОСТНОЙ И ЦЕМЕНТНОЙ ПЛАСТИК ДЕФЕКТОВ МЫЩЕЛКОВ ТИБИАЛЬНОГО ПЛАТО ПРИ ЭНДОПРОТЕЗИРОВАНИИ КОЛЕННОГО СУСТАВА
М.Ж. Азизов1, А.П. Алимов2, А.М. Азизов3
1 доктор медицинских наук, профессор, директор,
2 кандидат медицинских наук, старший научный сотрудник,
3 младший научный сотрудник
Научно-исследовательский институт травматологии и ортопедии МЗ Республики Узбекистан (Ташкент), Узбекистан
При дефектах мыщелков тибиального плато наиболее часто применяется аутокостная пластика или полное цементирование зоны дефекта, при этом нет определенной ясности в каких случаях приемлем тот или иной метод восполнения при тотальном эндопротезировании коленного сустава.
Целью настоящего исследования является изучение исходов оперативного лечения больных с дефектами мыщелков тибиального плато после эндопротезирования коленного сустава.
У 34 больных с дефектами мыщелков большеберцовой кости было произведено эндопротезирование коленного сустава; с аутокостной пластикой у- 15 и цементным заполнением у-19. Клиническое обследование больных проводилось по оценочной шкале для коленного сустава Bristol Knee Score.
На месте остеоимпакции имелось сращении аутокости с плато большеберцовой кости, а в зоне остеосклероза наблюдали явления лизиса со смещением бедренного компонента в передне-заднем и боковом направлениях до 2,0 мм, большеберцового компонента в переднезаднем направлении также до 2,0 мм над зоной цементной мантии.
При эндопротезировании коленного сустава с дефектами мыщелков тибиального плато возможно применение обоих видов замещения, у лиц пожилого возраста предпочтительнее цементное замещение, в более в молодом возрасте костная аутопластика.
Ключевые слова: дефекты тибиального плато, цементная и костная пластика, эндопротезирование коленного сустава.
Наличие дефектов мыщелков пораженного сустава представляют особые сложности при тотальном эндопротезировании коленного сустава.
При значительных некрозах и дефектах мыщелков коленного сустава А.В. Каземирский и соавтор. [1] с целью создания надежной опоры большеберцовых компонентов предложили следующее в тактических решениях:
- резекцию проксимального отдела большеберцовой кости на уровне дна дефекта;
- заполнение дефекта костным цементом;
- костная аутопластика;
- армирование цемента в зоне дефекта;
- смещение большеберцового компонента в сторону непораженного мыщелка от дефекта;
- металлические тибиальные модульные блоки [1].
Дефекты мыщелков большеберцовой кости приводят к осевым деформациям коленного сустава. Выравнивание варусного угла деформации с устранением дефекта внутреннего мыщелка большеберцовой кости возможно с применением резецированных костных пластин тибиального плато и фиксацией спонгиозными винтами, затем проводится имплантация эндопротеза. При длительном сроке наблюдения отмечаются положительные функциональные исходы без резорбции костного трансплантата [4].
Несложный и эффективный метод реконструкции костного дефекта медиального края тибиального плато аутокостью с фиксацией винтом способствует восстановлению механической оси и стабильности в коленном суставе при эндопротезировании, но с осторожностью необходимо применять при склерозе тибиального плато, так как могут быть осложнения в виде латерального смещения компонента эндопротеза с увеличением линии суставной щели и разламывание костного трансплантата [5].
Экспериментальное ремоделирование биомеханического стресса при поверхностном и полном цементировании компонентов эндопротеза коленного сустава в сравнении выявляет положительные стороны полного цементирования, так как тибиальное плато более резистентной к стрессовой нагрузке при большей толщине цементного слоя, чем при поверхностном, когда происходит резорбция окружающей костной ткани, способствующая асептической нестабильности [3].
Эндопротезирование коленного сустава при наличии значительных некротических дефектов мыщелков большеберцовой кости требует их коррекции для обеспечения полноценной фиксации компонентов. Применение костного трансплантата позволяет выполнить экономную резекцию суставных поверхностей мыщелков, значительно уменьшить количество костного цемента, используемого при трансплантации эндопротеза, обеспечить надежную опору для компонентов эндопротеза [1].
При дефектах мыщелков тибиального плато наиболее часто применяется аутокостная пластика или полное цементирование зоны дефекта, при этом нет определенной ясности в каких случаях приемлем тот или иной метод восполнения при тотальном эндопротезировании коленного сустава. В клинике выработана тактика, при которой замещение дефектов мыщелков проводится в зависимости от размера и глубины недостающей зоны мыщелка.
Целью настоящего исследования является изучение исходов оперативного лечения больных с дефектами мыщелков тибиального плато после эндопротезирования коленного сустава.
МАТЕРИАЛ И МЕТОДЫ
В отделении взрослой ортопедии клиники НИИТО МЗ РУз у 34 больных (19 женщин, 15 мужчин; средний возраст 67 лет) с дефектами мыщелков большеберцовой кости было произведено эндопротезирование коленного сустава; с аутокостной пластикой у- 15 и цементным заполнением у-19.
Оперативное вмешательство проводилось стандартным образом. Парапателярным доступом вскрывался сустав, удалялись патологически измененные ткани. После проксимальной резекции большеберцового плато, если определялся значительный дефект, то для аутокостной пластики во время фигурной остеотомии дистального отдела бедренной кости из межмыщелковой зоны выкраивался аутотрансплантат, который после придания формы соответствующей ложу дефекта был имплантирован и фиксирован винтом, после чего проводилось эндопротезирование сустава с цементной фиксацией.
Всем больным до и после оперативного вмешательства были проведены клинико-рентгенологические, лабораторные и инструментальные методы исследования (денситометрия, допплерография). Клиническое обследование больных проводилось по оценочной шкале для коленного сустава Bristol Knee Score (по J.MacKinnon и соавт., 1988).
РЕЗУЛЬТАТЫ И ОБСУЖДЕНИЯ
Данные клинического обследования больных через 6 месяцев после операции, проводимое по оценочной шкале для коленного сустава Bristol Knee Score, в зависимости от вида замещения дефекта были распределены следующим образом. При аутокостной пластики у 9 больных был отмечен хороший исход (от 36 до 40 баллов), удовлетворительный результат (30-35 баллов) был получен у 6 больных. При цементном замещении у 10 больных был отмечен хороший исход, удовлетворительный был получен у 9 больных, неудовлетворительных результатов мы не отмечали.
При наблюдении за всеми больными через 1 год после операции клинические результаты были оценены как хорошие и удовлетворительные. Выраженный мышечный дисбаланс имелся у одного больного, который проявлялся дискомфортом в суставе. После принятия физиотерапевтических процедур и комплекса упражнений для укрепления и расслабления мышечных групп, данное чувство уменьшилось. На рентгенограмме определялся остеосклероз вокруг цементной мантии эндопротеза. На месте остеоимпакции имелось сращении аутокости с плато большеберцовой кости у больных более молодого возраста (от 50 до 58 лет), а в зоне остеосклероза наблюдали явления лизиса со смещением бедренного компонента в переднезаднем и боковом направлениях до 2,0 мм, большеберцового компонента в переднезаднем направлении также до 2,0 мм над зоной цементной мантии у лиц старшей возрастной категории (от 64 до 76 лет).
Денситометрические показатели позволили выявить остеопению в периферических сегментах скелета. Доплерографическое исследование - снижение кровотока по венам обоих голеней.
В качестве иллюстраций приводим случаи успешного тотального эндопротезирования коленных суставов.

Рис. 1 (а, б). Фотоснимки больной АХ. 52 года до и после лечения

Рис. 2. Фотоснимки коленного сустава больной А.Х. 52 года во время операции

Рис. 3 (а, б). Рентгенограммы правого коленного сустава больной АХ. 52 года до и после лечения

Рис. 4. Рентгенограммы левого коленного сустава больного М.Р. 56 лет до лечения

Рис. 5 (а, б). Фотоснимки коленного сустава больного М.Р. 56 лет во время операции

Рис. 6 (а, б). Рентгенограммы левого коленного сустава больного М.Р. 56 после лечения
По мнению Liu J, несложный и эффективный метод реконструкции костного дефекта медиального края тибиального плато аутокостью с фиксацией винтом способствует восстановлению механической оси и стабильности в коленном суставе при эндопротезировании. Эту методику с осторожностью необходимо применять при склерозе тибиального плато, так как могут быть осложнения в виде латерального смещения компонента эндопротеза с увеличением линии суставной щели и разламыванием костного трансплантата [5].
Мы применили данную методику у одного больного с внутренним дефектом мыщелка большеберцовой кости и отметили консолидирование аутотрансплантата

Рис. 7 (а, б). МСКТ картина и интраоперационный фотоснимок больного А.Н. 46 лет

Рис. 8 (а, б). Интраоперационные снимки фиксации костного аутотрансплантата больного А.Н. 46 лет

При эндопротезировании коленного сустава с дефектами мыщелков тибиального плато возможно применение обоих видов замещения, у лиц пожилого возраста предпочтительнее цементное замещение, в более в молодом возрасте костная аутопластика.
Цементное замещение незначительных дефектных зон мыщелков обеспечивают достаточную стабильную фиксацию имплантата.
Остеоимпакция аутокостью из резецированных пластин большеберцового плато приводило к её сращению с плато большеберцовой кости, а в зоне остеосклероза происходил лизис костной ткани вокруг цементной мантии тотального эндопротеза коленного сустава.
Материал поступил в редакцию 20.10.15.
CLINICAL EVALUATION OF USING AUTOLOGOUS BONE GRAFTING AND CEMENTED FILLING OF CONDYLE DEFECT OF THE TIBIAL PLATEAU AT TOTAL KNEE ARTHROPLASTY
M.Zh. Azizov1, A.P. Alimov2, A.M. Azizov3
1 Doctor of Medicine, Professor, Head,
2 Candidate of Medicine, Senior Researcher,
3 Junior Researcher
Abstract. At condyle defect of the tibial plateau, autologous bone grafting or full cemented filling of the defect is mostly used, herewith no determined clarity in what events one or another method of the filling at total knee arthroplasty is acceptable.
The aim of this research is studying outcomes of operative treatment ofpatients with tibial condyle defect after total knee arthroplasty.
Methods. 34 patients with tibial condyle defect had total knee arthroplasty; 15 with autologous bone grafting and 19 with cement filling. The Clinical examination sick was conducted scale for knee joint Bristol Knee Score.
Results. On osteoimpaction place hadjoining of the tibial plateau, but in osteosclerosis area observed the osteolysis offset of the hip component in front-back and lateral directions to 2,0 mms, tibial component in front-back direction also to 2,0 mms above of the cement mantle.
Conclusion. At total knee arthroplasty with tibial condyle defect, using both types is possible, cement filling is preferable at elderly patients, autologous bone grafting - at younger patients.
Keywords: condyle defect of the tibial plateau, autologous bone grafting and full cemented filling, total knee arthroplasty.
Читайте также:


