Метаэпифизарный остеомиелит что это такое



Острый гематогенный метаэпифизарный остеомиелит (МЭО) у детей ранней возрастной группы продолжает оставаться тяжелым гнойно-септическим заболеванием в педиатрической хирургической практике [1,2]. В последнее десятилетие он занимает одно из первых мест в гнойно-септической хирургии по частоте исхода в бактериальный сепсис. Динамика количества случаев заболевания не имеет четкой тенденции к снижению, что подтверждается высокой частотой встречаемости патологического процесса среди новорожденных, в т.ч. маловесных недоношенных детей, имеющих ряд физиологических и иммунологических особенностей, усугубляющих тяжесть течения заболевания [3]. Значимым в этиологии является патоморфоз возбудителей последнего десятилетия, характеризующийся уменьшением частоты роста культур моностафилококковой флоры (Stafilococcusaureus) до 50 %. Отмечается активный рост микст-культур эпидермального стафилококка с другими микроорганизмами (клебсиеллами, энтерококками), их ассоциации с анаэробами и культурами грибов рода Кандида [4]. Многообразие клинических проявлений процесса и наличие атипичных форм могут увести от своевременной постановки диагноза МЭО. Этиопатогенез заболевания отличается тем, что до оссификации эпифизов имеет место морфофункциональная незрелость ростковой зоны, хондробласты расположены хаотически, их упорядочивание происходит параллельно оссификации эпифиза (от центра зоны роста в направлении к периферии), и в соответствии с этим зона роста постепенно приобретает барьерные свойства. Вот почему при отсутствии ядра окостенения, воспалительный процесс пенентрирует зону роста в центральной части, при появлении ядра оссификации пенентрация происходит в периферической части.
Поражение эпифиза сопровождается деструкцией последнего, с вовлечением в патологический процесс сустава и возникновением артрита, который в свою очередь приводит к патологическому вывиху и параартикулярной флегмоне. Дискредитированная ростковая зона частично или полностью погибает, и это в дальнейшем обусловливает возникновение приобретенных пороков развития (укорочение или удлинение, деформации конечностей).
Таким образом, исходом заболевания могут быть ортопедические осложнения, влекущие инвалидизацию ребенка, от 10 до 40 % случаев. МЭО представляет собой один из наиболее сложных вариантов течения гнойно-воспалительного процесса, требующего детального анализа течения заболевания, а также применения доступных для использования эффективных методов диагностики [5].
Цель исследования: изучить особенности клинического течения метаэпифизарного остеомиелита, провести сравнительный анализ возможностей различных методов диагностики.
Материалы и методы
В исследование включено 64 ребенка в возрасте от 0 до 3-х лет с острым гематогенным метаэпифизарным остеомиелитом, находившихся на стационарном лечении по поводу данного заболевания в отделении гнойной и экстренной хирургии ДОКБ г. Твери с 2005 по 2015 г. Для уточнения особенностей клинического течения различных форм МЭО был проведен анализ результатов стандартного комплекса клинико-диагностических мероприятий, проведенного у всех поступивших. Диагноз ставился на основании анализа жалоб больного, данных анамнеза, клинического осмотра, использовались методы бактериологической и лабораторной диагностики, методы медицинской визуализации (рентгенография, ультразвуковое исследование, компьютерная томография, магнитно-резонансная томография).
Результаты исследования и их обсуждение
В структуре обследуемых больных наибольшую группу составили дети до 1 года (n=4875 %), наиболее часто заболевание возникало в возрасте до 1 месяца (n=30; 46.8 %), от 1 г. до 3-х лет госпитализировано 16 (25 %) детей (таблица 1).
Число пациентов, n
От 1 месяца до 1 года
От 1 года до 3-х лет
По половой принадлежности преобладали мальчики (n=39; 60.9 %). Больные из районов области составили 60.9 % (n=39). В первые трое суток болезни был госпитализирован 21 ребенок (32.8 %). Наибольшее число пациентов (n=33; 51.5 %) обратилось за помощью детского хирурга на 4–7 сутки заболевания. Оставшиеся в более поздние сроки (n=10; 15.5 %). Анализ сроков поступления в специализированный хирургический стационар выявил достаточно позднее обращение за медицинской помощью, что связано с трудностями ранней диагностики МЭО из-за многообразия клинических проявлений заболевания, отсутствия ранних патогномоничных жалоб, преобладания у малышей общих реакций над местными, особенностями психофизиологического статуса пациентов раннего возраста. Немаловажная роль принадлежит ошибкам диагностики на догоспитальном этапе. Учитывая распределение больных по месту обращения, замечено, что достаточно большая группа детей поступала из род. домов (n=17; 26.5 %), из стационара (отделение патологии новорожденных) – (n=21;32.8 %). По направлению участковых педиатров, хирургов травматологов (n=23;35.9 %), 3 человека обратились самостоятельно.
Для характеристики клинического течения МЭО использовалась классификация Т.П. Краснобаева. Встречалась местная форма (n= 53;82.8 %) заболевания, септикопиемическая (n= 11; 17.2 %), токсическая форма не зарегистрирована. Из септических осложнений на первом месте оказалась пневмония (n= 6;54.5 %). Также имели место перикардит (n=3;27.2 %), поражение почек (n=1; 9 %), средний гнойный отит (n=1;9 %). Локальная форма заболевания превалировала в возрастной группе от 1 г. до 3-х лет. Результаты оценки степени тяжести состояния показали, что дети поступали в стационар преимущественно в состоянии средней степени тяжести (n=36;56.2 %). В тяжелом состоянии доставлено 28 детей (43.7 %). Это связано с поздним обращением за специализированной хирургической помощью, низкой иммунологической резистентностью детского организма, быстрым нарастанием симптомов интоксикации ввиду выраженности альтеративного компонента воспалительной реакции в раннем возрасте. Дети, поступившие в тяжелом состоянии, были госпитализированы в отделение реанимации, где проводилось непрерывное мониторирование жизненно важных функций организма и интенсивная комплексная терапия заболевания. В типичных случаях заболевание начиналось остро: (n=52; 81.2%), возникала резкая боль в пораженной конечности (n= 49; 76.5 %). Появлялись и нарастали симптомы интоксикации: повышение температуры тела (n=60; 93.7 %), вялость, отказ от еды (n= 44; 68.7 %). В тяжелых случаях возникала тахикардия (n=9; 14 %), тахипноэ (n=8; 12.5 %) менингеальные явления (n=4; 6.25 %).
При клиническом осмотре обращало на себя внимание вынужденное положение конечности, ограничение или отсутствие активных движений, болезненность при пальпации и попытке пассивных движений. (n=56; 87.5 %), отмечалась выраженная стойкая контрактура суставов (n=48; 75 %), что связано с вовлечением в процесс связочного аппарата и параартикулярных тканей. В более поздние сроки появлялось увеличение объема сустава из-за наличия в его полости жидкости (2–5 сутки и позже), гиперемия над очагом поражения –(n= 43; 67 %).
Факторы риска развития заболевания выявлены в 34 (53.1 %) случаях. Это –неблагоприятный антенатальный период: внутриутробная гипоксия плода разной степени выраженности, очаги хронической инфекции, синдром интоксикации у матери, оперативные роды, травматизация в родах, недоношенность, перинатальное поражение ЦНС, катетеризация центральной вены, низкая оценка по шкале Апгар, предшествующие гнойные заболевания. Важная роль отводится гипоксии не только как промоутеру каскада метаболических нарушений, но и фактору, способствующему развитию генерализованных форм МЭО. Результаты проведенных исследований показали, что у всех больных с септикопиемической формой выявлены факторы риска [6,7].
По локализации остеомиелитического очага преобладало поражение эпифизов длинных трубчатых костей скелета с поражением суставов в виде гнойных артритов: бедренной кости с поражением тазобедренного сустава (n=26;40.6 %), большеберцовой (n=13; 20 %), малоберцовой (n=11; 17.1 %), костей предплечья (n=5;7.8 %). Множественное поражение костей при МЭО отмечено у 2 (3 %) детей.
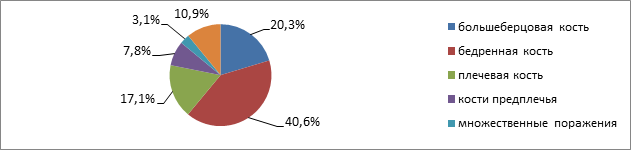
Рис.1. Локализация очага воспаления
С целью выявления этиологического фактора заболевания применялись бактериоскопический и бактериологический методы исследования с определением чувствительности микрофлоры к антибиотикам. При первичном заборе биоматериала идентифицирован возбудитель у 46(71.8 %) больных. Анализ полученных результатов показал, что в большинстве случаев основным этиологическим фактором является золотистый стафилококк (n=28;43.7 %), также были обнаружены другие виды стафилококка (n=4;8.6 %), энтерококк и клебсиелла (n=2;3.1 %) в равных количествах, гемолитический стрептококк (n=3;4,6 %), протей (n=1;1.5 %), кишечная и синегнойная палочка (n=2;3.1 %) и (n=1;1.5 %) соответственно, полифлора (n=3;4.6 %).
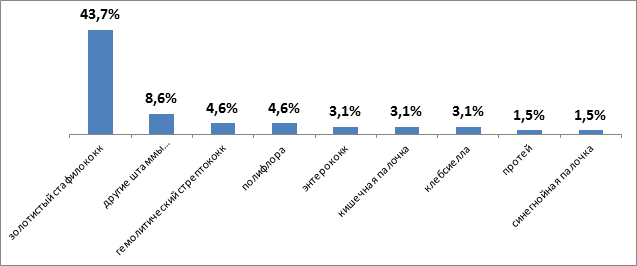
Рис. 2. Результаты высева микрофлоры из очага поражения
При анализе изменений состава периферической крови, констатирована анемия (n= 34;53.1 %), лейкоцитоз (n= 57;89 %), палочкоядерный сдвиг (n= 49; 76.5 %), ускорение СОЭ (n=28; 43.7 %). У больных с септикопиемической формой регистрировалась тромбоцитопения (n=11;7.2 %) у большинства пациентов имелись признаки системного воспалительного ответа (нейтрофильный лейкоцитоз со сдвигом формулы влево). В биохимическом анализе крови сохранялась нормогликемия (n=58; 90.6 %). Гипергликемия зарегистрирована с максимальным значением 13 ммоль/л (n=4; 6.25 %). Гипогликемия с минимальным значением 2.8 ммоль/л (n=2; 3.1%). Изменения белкового спектра крови проявлялись умеренной гипопротеинемией (n=29; 45.3 %). Повышение уровня С-реактивного белка как неспецифического маркера воспаления определялось качественным методом, было положительным (n= 44; 68.7 %) и резко положительным (n=13;20.3 %). Также имел место отрицательный результат (n= 7; 10.9 %). Лабораторные показатели, характеризующие функцию почек, оставались в пределах референтных значений. Средние значения электролитного обмена соответствовали возрастной норме. В ряде случаев отмечено изменение фибринолитической активности (n= 24;37.5 %).
В последнее десятилетие МЭО занимает одно из первых мест в гнойно-септической хирургии по частоте исхода в бактериальный сепсис. Для ранней диагностики септического процесса, в случае ухудшения состояния ребенка проводился прокальцитониновый тест сыворотки крови экспресс-методом по Brachms (n= 14; 21 %). Выполнение исследования позволило определить клиническую форму заболевания. В результате была диагносцирована местная форма (n=5;7.8 %) – прокальцитонин сыворотки крови 2 состояние трактовалось как сепсис, осложнивший остеомиелит – (n= 9;14 %).
На диагностическом этапе установления МЭО применяли различные методы медицинской визуализации. В качестве стандартизированного лучевого метода исследования опорно-двигательного аппарата стартовым являлась рентгенография пораженного отдела скелета. (n=64; 100 %). Метод позволял оценить форму, контуры, соотношения между костями. Ранние рентгенологические признаки заболевания в виде утолщения мягких тканей на уровне поражения, расширения суставной щели, размытости контуров эпифиза, остеопороза края метафиза выявлены в среднем на 3–5 день болезни (n=19;29.6 %). На 10–14 день болезни регистрировалась периостальная реакция и очаги деструкции в метаэпифизарной зоне (n= 47; 73.4 %). Рентгенографический метод не обладает достаточной чувствительностью к визуализации хрящевых структур в начальные периоды развития заболевания.
Магнитно-резонансная томография (МРТ) является высокоинформативным методом, обладающим высокой чувствительностью и достаточной специфичностью в интрамедуллярную фазу МЭО, позволяет выявить изменения костного мозга, определить так называемые участки патологической гидратации, а также оценить суставные поверхности и околосуставные мягкие ткани. К недостаткам метода следует отнести необходимость проведения анестезиологического пособия для исключения двигательной активности пациентов младшей возрастной группы во время исследования. МРТ использовали в качестве уточняющей методики в интрамедуллярную фазу (n=4 ;6.25 %) [8].
Компьютерная томография (КТ) – метод выбора для оценки суставных поверхностей, мягких тканей, изменений костного мозга, позволяет выявить отек мягких тканей и деструкцию кости, не замеченную на обычных рентгенограммах, наилучший метод выявления секвестров. КТ недавно внедрена в работу клиники (n=8;12.5 %). Сопряжена с лучевой нагрузкой, зарекомендовала себя как оптимальный способ ранней диагностики МЭО, уже на 2-е сутки заболевания в кортикальном слое проявляются отчетливые рентгенодеструктивные изменения костных структур.
Ультразвуковая диагностика выполнена всем пациентам с МЭО (n=64;100 %), в дебюте заболевания (n=29;45.3 %). Методика показала высокую информативность (80 %), верифицируемую во время операции. Проникающая способность ультразвука у детей раннего возраста большая, чем у более старших, что связано с незавершенным процессом остеогенеза, когда эпифизы костей состоят в основном из хрящевой ткани. Исследование позволило оценить состояние мягких тканей, определить анатомические взаимоотношения в суставе, состояние капсулы (уплотнение и утолщение), суставной полости, ядер окостенения, определить утолщение надкостницы, распознать поднадкостничные абсцессы, визуализировать участки деструкции кости в метаэпифизарной зоне [9,10]. В процессе проведения исследования были обнаружены следующие УЗ-признаки изменения анатомических структур: утолщение мягких тканей, повышение эхогенности, жидкостные парартикулярные скопления (n=32;50 %); изменения внутрисуставной полости (утолщение капсулы сустава, наличие внутрисуставной жидкости – n=39;60.9 %); изменения однородности эпифизарного хряща (n=34;53 %); изменение формы и структуры ядра окостенения эпифизарного конца конечности (n=27;42.1 %); изменения метаэпифизарной зоны (нечеткость, неровность дефект зоны предварительного обызвествления, анэхогенные участки и включения – n=43 67.1 %); изменения надкостницы (неровность наружного контура, утолщение, повышение эхогенности n=25;39 %). Основной УЗ-признак МЭО –изменения в метаэпифизарной зоне – появлялся на 4–7 день болезни.
Выводы и заключение
Т.о., резюмируя полученные результаты, отмечено, что метаэпифизарный остеомиелит наиболее часто встречается в группе новорожденных детей, у каждого из которых обнаружены факторы риска возникновения заболевания в виде внутриутробной гипоксии плода, наличия очагов хронической инфекции и синдрома интоксикации у матери, недоношенности. В большинстве случаев в дебюте заболевания преобладало наличие общей симптоматики. Локальные проявления прогрессировали медленно. Основным этиологическим фактором являлся золотистый стафилококк. Первичный очаг воспаления локализовался преимущественно в эпифизах длинных трубчатых костей нижних конечностей. В ранней диагностике заболевания методом выбора является компьютерная томография и ультразвуковое исследование.
 |  |  |  |
Метаэпифизарный остеомиелит встречается преимущественно у детей грудного возраста. Однако в этой возрастной группе новорожденные дети поражаются чаще. Гематогенным путем инфекция (чаще стафилококк) попадает в метафиз кости, где и развивается воспалительный процесс, однако вследствие особенностей кровоснабжения ме-таэпифизарной границы у детей раннего возраста он распространяется на ростковую зону и эпифиз, располагающийся внутри сустава. Поэтому основные клинические симптомы обусловливаются развитием острого артрита.
Клиническое течение. Метаэпифизарный остеомиелит, как правило, начинается остро с повышения температуры, вялости, отказа от еды, щажения больной конечности, при этом ребенок держит ее в вынужденном положении.
Морфологически в кости при остеомиелите у детей раннего возраста преобладают некротические процессы, сопровождающиеся гибелью и рассасыванием костной ткани в области метафиза, повреждением ростковой зоны и суставных поверхностей. Однако в этом возрасте репаративные процессы выражены хорошо, в связи с чем перехода этой формы остеомиелита в хроническую не происходит. Функциональные нарушения в отдаленные сроки могут быть выражены значительно и объясняются нарушением роста конечности, деформациями в суставах (рис. 69).

Рис. 69. Последствия эпифизарного остеомиелита, перенесенного в период новорожденности. Обширный дефект суставного конца бедренной кости. Рентгенограммы больного 12 лет. а — прямая проекция; б — боковая проекция.
Рентгенологические признаки остеомиелита выявляются раньше, чем при других формах. Уже на 8—10-й день можно найти ряд характерных симптомов: утолщение мягких тканей на стороне поражения, расширение суставной щели, легкую периостальную реакцию (рис. 70). Очаги деструкции в метафизе на рентгенограммах выявляются лишь на 3-й неделе от начала заболевания, а о степени разрушения эпифиза кости и зоны роста можно с достоверностью судить лишь после того, как появится ядро оскостенения (рис. 71). Наиболее часто поражаются дистальный и проксимальный концы бедренной кости, проксимальный—плечевой и большеберцовой костей.

Рис. 70. Рентгенограммы коленного сустава ребенка в возрасте 1 мес. Ранние рентгенологические признаки метаэпи-физарного остеомиелита: периостит, расширение суставной щели, утолщение мягких тканей.

Рис. 71. Рентгенограмма плечевого сустава ребенка 11/2 мес. Эпиметафизарный остеомиелит, выражена деструкция проксимального метафиза плечевой кости.
Лечение. При метаэпифизарном остеомиелите лечение имеет свои особенности. Общая терапия осуществляется по принципам лечения острой гнойной хирургической инфекции с учетом возраста ребенка. Применяют антибиотики широкого спектра действия и обладающие тропностью к костной ткани (линкомицин), дезинток-сикационную и иммунотерапию.
Важную роль играет иммобилизация, которую осуществляют с помощью вытяжения по Шеде (на нижней конечности) или повязки Дезо (на верхней конечности). Хирургические манипуляции в области ростковой зоны и гипсовые лонгеты у новорожденных не применяют. При явной клинике артрита лечение проводится с помощью пункций, удалением выпота из сустава с последующим введением в него антибиотиков.
При локализации процесса в проксимальном эпифизе бедренной кости по стихании острого воспалительного процесса с целью профилактики патологического вывиха бедра применяют повязки-распорки. Дети, перенесшие острый гематогенный метаэпифизарный остеомиелит, должны находиться под диспансерным наблюдением врача-ортопеда или хирурга.
Исаков Ю. Ф. Детская хирургия, 1983г
Эпифнэарный остеомиелит возникает преимущественно у детей грудного возраста, обычно являясь одним из проявлений сепсиса. Гнойное воспаление может локализоваться в любом эпифизе (чаще в бедренной и плечевой костях). Иногда встречаются множественные поражения.
Прогноз, а также функциональные и анатомические результаты лечения при эпифизарном остеомиелите зависят прежде всего от раннего распознавания заболевания и, следовательно, своевременного начала лечения.
Клиническая картина. По течению эпифизарные остеомиелиты можно разделить на токсико-септическую и местноочаговую формы.
Токсико-септическая форма эпифизарного остеомиелита характеризуется острым началом с быстрым подъемом температуры тела до 39—40 "С. Общее состояние резко ухудшается, ребенок отказывается от груди, появляется беспокойство, иногда судороги. Черты лица заостряются, кожа принимает серый оттенок. У некоторых детей выражена
общая слабость, понижена реакция на окружающее. Часто развиваются диспепсические явления: рвота, жидкий стул.
- Местноочаговая форма начинается менее бурно. Вначале появляются недомогание, потеря аппетита, постепенно повышается температура тела (37,5—38 °С). Общее состояние остается сравнительно удовлетворительным или расценивается как среднетяжелое. Интоксикация выражена умеренно.
При обеих формах эпифизарного остеомиелита наиболее постоянным признаком является боль в пораженной конечности, вначале без определенной локализации, Грудной ребенок реагирует на болевые ощущения изменением поведения — беспокойством или резким криком, которые усиливаются при всяких попытках движения. Если до болезни ребенок успокаивался после смены пеленок, то при возникновении остеомиелита всякое перекладывание, малейшее изменение положения тела вызывают громкий мучительный крик больного, который долго не может успокоиться. При расспросе матери выясняется, что ребенок в конце 1-х — начале 2-х суток стал особенно беспокоиться при дотрагивании до определенного отдела одной из конечностей. Он избегает всяких активных движений и кричит при попытке пассивного сгибания или разгибания конечности. При осмотре выявляется вынужденное положение пораженной конечности, которое характерно для каждой локализации ос-теомиелитического процесса. Более старшие дети обычно совершенно четко указывают место наибольшей болезненности.
При поражении верхнего эпифиза плечевой кости рука ребенка приведена к туловищу, неподвижна во всех суставах. Остеомиелит проксимального эпифиза лучевой или локтевой кости сопровождается сгиба-тельной контрактурой в локтевом суставе. Всякая попытка выпрямления руки или ротации предплечья вызывает плач ребенка. При поражении дистальных эпифизов костей предплечья отмечается свисание кисти, неподвижность пальцев.
Верхний эпифиз бедра поражается наиболее часто. При этой локализации процесса нижняя конечность слегка согнута в тазобедренном суставе, ротирована кнаружи и отведена. Активные движения в тазобедренном суставе отсутствуют, пассивные — резко болезненны, особенно ротационные. Поражение эпифизов в области коленного сустава сопровождается сгибательной контрактурой под тупым или даже прямым углом. Для более устойчивого положения конечности и уменьшения боли ребенок отводит ногу и ротирует ее кнаружи. Эпифизарный остеомиелит в области голеностопного сустава вызывает фиксированное подошвенное сгибание стопы, неподвижность пальцев.
В связи с поражением эпифиза кости, который расположен внутрису-ставно, быстро развиваются явления артрита. При осмотре можно выявить заметную припухлость сустава, сглаженность контуров. Однако процесс в области тазобедренного и плечевого суставов (который возникает наиболее часто) выявляется обычно позднее, так как сустав покрыт со всех сторон массивным слоем мышц. Надо иметь в виду, что первичные артриты у новорожденных практически не встречаются, поэ-
тому при наличии ярко выраженных симптомов гнойного или серозного поражения сустава следует думать об эпифизарном остеомиелите. Пальпация конечности над проекцией пораженного эпифиза вызывает резкую боль, беспокойство и сопротивление ребенка.
Кроме вышеуказанных ранних симптомов, для эпйфизарного остеомиелита характерны местные проявления, которые становятся заметными спустя 2—3 дня от начала заболевания. В области пораженного эпифиза появляется разлитая припухлость, которая обусловлена отеком окружающих тканей. В первые дни пальпаторно определяется пастозность, а затем плотный инфильтрат вокруг эпйфизарного конца кости. Кожа при этом некоторое время остается неизмененной. Все эти симптомы выявляются сравнительно рано, если поражены более поверхностно расположенные эпифизы (локтевой, лучезапястный, коленный и голеностопный суставы).
При прорыве поднадкостничного абсцесса в мягкие ткани или в сустав заметно повышается местная температура, появляется покраснение кожи, отчетливо выражена флюктуация. Если прорыв гноя произошел в глубину мягких тканей (верхний эпифиз плеча и бедра), то могут наблюдаться расширение подкожной венозной сети и синюшный оттенок кожи.
Анализы крови, произведенные в первые дни болезни, служат вспомогательным методом исследования. Изменения в крови сходны с данными, которые имеются и при других проявлениях сепсиса. Лейкоцитоз, по нашим данным, колеблется в пределах (12—30) х 10 9 /л. Обычно отмечается сдвиг в лейкоцитарной формуле влево. Появляются клетки Тюрка, при тяжелом течении болезни выражена эозинофилия, СОЭ в большинстве случаев увеличена. В последующие дни болезни нарастает анемия.
Рентгенологическое исследование. Первым рентгенологическим признаком эпйфизарного остеомиелита является некоторое расширение суставной щели, которое указывает на наличие выпота. Поэтому рекомендуют производить рентгенограмму больного и здорового суставов. Через 5—10 дней на рентгенограммах видны незначительные деструктивные изменения ядра окостенения, которые вначале выражаются разрежением костной структуры и нечеткостью рисунка. В сомнительных случаях изменения более четко выявляются при сравнительном осмотре снимков здоровой конечности. В области верхнего эпифиза бедренной кости или плеча при остеомиелитическом процессе (в поздних стадиях) часто наблюдаются большие дефекты, вплоть до полного рассасывания ядра окостенения головки. В таких случаях наступает патологический вывих. Переход воспаления на метафиз кости характеризуется пе-риостальными наслоениями в этой области (не раньше 10—14-го дня болезни). Позже здесь развивается деструкция (рис. 93). У старших детей может возникнуть патологический эпифизеолиз. Наряду с деструктивными изменениями при остеомиелите возникают и репаративные. Светлые очаги разрежения метафиза (деструкция) окружаются плотной склерозированной полоской.
Дифференциальную диагностику наиболее часто приходится проводить с глубокой мышечной флегмоной, артритом и переломами.
Флегмона обычно не вызывает настолько резкой болезненности при движении конечностей, как остеомиелит. Инфильтрация тканей, зыбле-ние при пальпации, местное повышение температуры при флегмоне проявляются значительно раньше. Трудность дифференциальной диагностики иногда приводит к ошибочным заключениям о характере воспалительного процесса. Однако ошибки в этих случаях не имеют практического значения, так как дети с этими заболеваниями нуждаются в срочной хирургической помощи. В ряде случаев только последующее рентгенологическое наблюдение позволяет уточнить диагноз.
Перелом костей (особенно поднадкостничный перелом бедра) может служить поводом для ошибочного диагноза в связи с возникающей при этом болью и припухлостью в месте повреждения, ограничением функции конечностей и повышением температуры тела, а также лейкоцитозом, который обычно выявляется у детей в первые сутки после травмы. Окончательный диагноз в таких случаях устанавливается на основании рентгенологического исследования.
Лечение. Основные положения по лечению остеомиелита, сохранившие свое решающее значение и до настоящего времени, были высказа-
ны еще Т. П. Краснобаевым в 1925 г. Отказ от чрезмерной хирургической активности и усиление общеукрепляющего лечения больных привели к резкому снижению летальности.
При лечении эпифизарного остеомиелита у новорожденных мы> придерживаемся комбинированного метода с применением наиболее щадящих хирургических вмешательств. Каждый больной нуждается в индивидуальном подходе при выборе плана лечения.
Общеукрепляющее лечение При токсико-септической форме эпифизарного остеомиелита ребенку сразу после по^упления начинают интоксикационную терапию. Назначают антибиотики широкого спектра действия. На очаг поражения и на область солнечного сплетения воздействуют электрическим полем УВЧ, применяют микроволновую терапию.
Хирургическое лечение. Хирургическое лечение проводят по срочным показаниям, как только устанавливают локализацию очага поражения. У большинства из наблюдаемых нами больных первым местным проявлением эпифизарного остеомиелита был артрит. При наличии выпота в суставе показана пункция. Удаленную при проколе жидкость по* сылают на посев и определение чувствительности микроорганизмов к антибиотикам. В сустав вводят раствор антибиотиков, оставляют тонкий дренаж для дальнейшей антибактериальной терапии. Всем детям проводят иммобилизацию конечности; характер фиксирующей повязки зависит от локализации процесса
Пункцию плечевого сустава осуществляют по задней поверхности у верхушки акромиона, продвигая иглу кпереди по направлению к клювовидному отростку, затем руку прибинтовывают к груди фиксирующей повязкой типа Дезо.
Пункцию локтевого сустава делают между локтевым отростком и наружным надмыщелком плеча, выше проекции головки лучевой кости. Иммобилизацию осуществляют легкой лонгетой, накладываемой от пальцев до плечевого сустава, при согнутом до прямого угла предплечье.
' Пункцию тазобедренного сустава осуществляют над вершиной большого вертела, продвигая иглу строго во фронтальной плоскости. Фиксацию конечности при поражении тазобедренного сустава проводят путем лейкопластырного горизонтального вытяжения. При наличии у новорожденного обильного выпота в суставе или заметной деструкции шейки бедра, угрожающей патологическим вывихом, мы пользуемся отводящей шиной, изготовляемой из винипласта. Шину накладывают на оба бедра
Пункцию коленного сустава производят у наружного края надколенника, иглу вкалывают перпендикулярно к бедренной кости. При поражении эпифизов, образующих коленный сустав, конечность фиксируют гипсовой лонгетой, которую накладывают от пальцев стопы до верхней трети бедра, верхнюю часть повязки закрывают тонкой клеенкой, предупреждая тем самым загрязнение ее испражнениями ребенка.
Если ежедневные пункции не имели успеха, общее состояние ребенка в течение 2 сут остается тяжелым и гнойная жидкость продолжает
скапливаться в суставе, то показана артротомия, которую проводят под местной анестезией. Разрезы должны быть небольших размеров (2— 3 см), раны не дренируют.
Вскрытие плечевого сустава. Положение — на здоровом боку, под лопатку подкладывают валик из свернутой пеленки. Разрез производят вертикально книзу, начиная его несколько кпереди от акро-миона. Рассекают кожу, подкожную клетчатку и фасцию. Волокна дельтовидной мышцы тупо расслаивают. Капсулу сустава прокалывают остроконечным скальпелем, расширяя затем отверстия тупым путем.
Вскрытие локтевого сустава. Разрез производят по задней поверхности нижней трети плеча, между локтевым отростком и головчатым возвышением плечевой кости. Обнажают и вскрывают капсулу сустава.
Вскрытие тазобедренного сустава. Ребенка укладывают на здоровый бок, несколько повернув на живот. Больную конечность слегка отводят, сгибают в коленном и тазобедренном суставах. Несколько кзади от большого вертела рассекают мягкие ткани до мышц, последние тупо расслаивают. Капсулу прокалывают скальпелем.
Вскрытие коленного сустава. Положение ребенка — на спине. Под колено подложен тонкий валик. Сустав вскрывают по боковой поверхности надколенника. Во всех случаях в сустав вводят антибиотики, накладывают асептические повязки и фиксирующую шину. При позднем поступлении, когда наряду с тяжелым общим состоянием имеет место прорыв гноя в мягкие ткани с образованием параартику-лярной флегмоны, показано вскрытие гнойника под кратковременным наркозом.
Техника операции. Разрез длиной не более 3—4 см производят над инфильтратом, в месте наибольшей болезненности или размягчения. Рассекают кожу, подкожную клетчатку и фасцию. Тупым путем расслаивают подлежащие мышцы и доходят до капсулы сустава. Последнюю вскрывают продольным разрезом (иногда она бывает расплавлена). Выделившийся гной берут на посев. В рану вводят тонкий узкий резиновый выпускник; при необходимости делают добавочные контрапертуры. Конечность фиксируют шиной.
Проводят общеукрепляющее, детоксикационное и антисептическое лечение. Перевязки и осмотр места поражения проводят ежедневно. В редких случаях при перевязках выявляют задержку гноя или затеки, которые необходимо вскрыть добавочными разрезами.
Обычно спустя 3—4 дня местный процесс начинает заметно стихать: отек уменьшается, выпот в суставе ликвидируется. Раны при благоприятном течении сравнительно быстро заживают. Фиксирующую повязку сохраняют до полного затихания воспалительного процесса. В ряде случаев при наличии значительных разрушений эпифиза необходимо фиксировать конечность более длительно.
Осложнения. При эпифизарном остеомиелите осложнения можно разделить на ранние и поздние.
Ранние осложнения. К ним относят возникновение множественных пиемических очагов и патологические вывихи.
Множественные пиемические очаги резко ухудшают прогноз заболевания. Наиболее часто наблюдается метастазирование гнойной инфекции в легкие У ребенка развивается вторичная стафилококковая пневмония с абсцедированием. Возникающий при этом пиопневмоторакс у грудных детей крайне сложен для лечения (ем. гл, 3). В ряде случаев эпифизарный остеомиелит осложняется гнойным перикардитом, который часто не диагностируют при жизни ребенка.
Патологические вывихи возникают, как правило, при локализации инфекционного процесса в верхнем эпифизе бедра. У части детей в связи с обильным выпотом в сустав и поздним началом лечения растягивается сумка сустава, и головка бедра выходит из впадины, смещаясь кнаружи, а затем кверху под действием сокращающихся ягодичных мышц. Возникает так называемый двстензионный патологический вывих. Для предупреждения последнего следует производить пункцию, а также фиксировать конечность в положении отведения и сгибания в коленном суставе на специальной отводящей шине. Если ребенок поступил с имеющимся патологическим дистензионным вывихом, то последний вправляют после затихания воспалительного процесса. Фиксацию конечности до вправления производят путем лейкопластырного вертикального вытяжения с небольшим грузом.
Вправление осуществляется под наркозом. Ребенка укладывают на спину, помощник двумя руками фиксирует таз больного. Хирург, захватив руками пораженную конечность, производит тягу по оси ее (низводит головку бедра), затем, не прекращая вытяжения, сгибает в тазобедренном суставе и постепенно отводит. В это время головка с характерным щелчком перемещается через задний край вертлужной впадины. Вправление производят очень медленно, не применяя значительной силы, так как существует опасность эпифизеолиза головки или перелома шейки бедра. Рентгенологически контролируют положение головки и накладывают отводящую фиксирующую повязку на 2—3 нед.
Разрушение воспалительным процессом головки и шейки бедренной кости ведет к образованию деструктивного патологического вывиха. В таких случаях конечность ребенка фиксируют отводящей шиной. Фиксацию проводят не менее 3 мес. Последующий рентгенологический контроль (1 раз в 6 мес) обычно выявляет некоторое восстановление кости в области шейки бедра, а иногда частично восстанавливается и головка.
Мы наблюдали нескольких детей, у которых в разгаре заболевания рентгенологически и клинически определялся патологический вывих с наличием полного разрушения головки и части шейки бедра Фиксация конечности у них проводилась отводящей шиной В процессе роста ребенка шейка и головка восстановились настолько полно, что отпала необходимость в сложных пластических операциях Параллельно восстановилась функция сустава У 3 детей образовалась деформация типа coxa vara, им в возрасте 4—6 лет произведена корригн рующая остеотомия.
Поздние осложнения возникают вследствие нарушения роста конечности в связи с поражением ростковой зоны кости. Хронического течения процесса с секвестрацией и свищами мы у новорожденных не наблюдали.
Нарушение нормального развития кости при поражении эпифиза выявляется с ростом ребенка. Анализируя отдаленные последствия эпифи-зарного остеомиелита, можно отметить определенную зависимость характера возникающих деформаций от локализации поражения. Наиболее резкое укорочение встречается при остеомиелите верхнего эпифиза плеча и нижнего эпифиза бедренной кости. Отставание в росте достигает максимума в возрасте 11 —12 лет и может составлять 10—12 см. В таких случаях возникает необходимость в пластическом удлинении кости. Поражение головки и шейки бедра при несоблюдении указанных выше правил лечения приводит к патологическим вывихам или порочному развитию верхнего эпиметафиза с нарушением нормального шееч-но-диафизарного угла.
Поражение эпифизов костей, образующих коленный сустав, ведет, кроме укорочения, к резкому изменению оси конечности и ограничению функции сустава.
Следует указать на необходимость диспансерного наблюдения за всеми детьми, перенесшими эпифизарный остеомиелит. Своевременное выявление возникающих деформаций позволит произвести более легкую и эффективную этапную пластическую операцию, которая улучшит условия дальнейшего роста и функции конечностей.
Читайте также:


