Пациент как потенциальный источник инфекции
На нашем языке постоянно обитает больше 600 видов известных микроорганизмов, но у нас больше шансов подхватить инфекцию в общественном транспорте. Что является источником инфекционного заболевания? Как действует механизм заражения?
Патогенность организмов
Заражение болезнетворными микроорганизмами называется инфекцией. Термин появился ещё в 1546 году благодаря Джироламо Фракасторо. В настоящее время науке известно приблизительно 1400 микроорганизмов, они окружают нас повсюду, однако инфекции не развиваются в нас ежесекундно.

Условно-патогенные микроорганизмы (кишечная палочка, гриб кандида) не вызывают у здорового человека никаких реакций. Они могут обитать в окружающей среде, быть частью микрофлоры нашего организма. Но при определенных условиях, например при слабом иммунитете, они становятся патогенными, то есть вредными.
Источник инфекций
Инфекционное заболевание может быть вызвано проникновением в организм патогенных грибков, вирусов, простейших, бактерий, прионов. Источником возбудителей инфекции является среда, которая способствует их развитию. Такой средой зачастую выступает человек или животное.
Попадая в благоприятные условия, микроорганизмы активно размножаются, а затем покидают источник, оказываясь во внешней среде. Там болезнетворные микроорганизмы, как правило, не размножаются. Их количество постепенно уменьшается вплоть до полного исчезновения, а различные неблагоприятные факторы только ускоряют этот процесс.
Окружающая среда как передатчик
Важно понимать, что окружающая среда - это не источник инфекции. Она всегда выступает лишь посредником для передачи микроорганизмов. Недостаточная влажность, отсутствие питательных веществ и несоответствующая температура внешней среды являются неблагоприятными условиями для их развития.
Воздух, предметы быта, вода, почва сначала сами подвергаются заражению, а уже потом транспортируют паразитов в тело хозяина. Если микроорганизмы находятся в этих средах слишком долго, они погибают. Хотя некоторые обладают особой стойкостью и могут сохраняться даже в неблагоприятных условиях на протяжении многих лет.
Сильной устойчивостью обладает возбудитель сибирской язвы. В почве он сохраняется несколько десятков лет, а при кипячении погибает только через час. Он также абсолютно равнодушен к дезинфицирующим препаратам. Возбудитель холеры Эль-Тор способен сохраняться в почве, песке, продуктах и фекалиях, а прогревание водоема до 17 градусов позволяет палочкам размножаться.

Источники инфекции: виды
Инфекции делятся на несколько типов, в соответствии с тем, в каких организмах они размножаются и кому могут передаваться. Исходя из этих данных, выделяют антропонозы, зооантропонозы и зоонозы.
Зооантронозы или антропозоонозы вызывают болезни, при которых источником инфекции является человек или животное. У людей заражение чаще всего происходит через животных, в особенности через грызунов. К зоонозным инфекциям относится бешенство, сап, туберкулез, лептоспироз, сибирская язва, бруцеллез, трипаносомоз.

Антропонозной болезнь является в том случае, когда источник инфекции – человек, и передаваться она может только другим людям. Сюда относится возвратный, сыпной и брюшной тиф, ветряная оспа, гонорея, грипп, сифилис, коклюш, холера, корь и полиомиелит.
Зоонозами называют инфекционные болезни, для которых благоприятной средой является организм животного. При определенных условиях заболевание может передаваться людям, но от человека к человеку - нет. Исключение составляют чума и желтая лихорадка, способные циркулировать среди людей.
Выявление инфекции
Зараженный человек или животное может стать причиной широкого распространения заболевания в пределах одного, нескольких населенных пунктов, а иногда и нескольких стран. Опасные заболевания и их распространения изучают эпидемиологи.
При обнаружении хотя бы одного случая инфекции врачи выясняют все подробности заражения. Происходит выявление источника инфекции, определение её вида и способов распространения. Для этого чаще всего применяется эпидемиологический анамнез, который заключается в опросе больного о недавних действиях, контактах с людьми и животными, дате проявления симптомов.
Полная информация о заразившемся является крайне полезной. С её помощью удается выяснить путь передачи инфекции, возможный первоисточник, а также потенциальный масштаб (станет ли случай единичным или массовым).
Первоначальный источник инфекции выявить не всегда легко, их может быть сразу несколько. Особенно это трудно сделать при антропозоонозных заболеваниях. В таком случае главной задачей эпидемиологов является определение всех потенциальных источников и путей передач.
Способы передачи
Существует несколько механизмов передачи инфекции. Фекально-оральный характерен для всех кишечных болезней. Вредоносные микробы в избытке находятся в кале или рвотных массах, в здоровый организм они попадают с водой или контактно-бытовым способом. Так происходит, когда источник инфекции (больной человек) плохо моет руки после туалета.
Респираторный, или воздушно-капельный действует при вирусных инфекциях, которые поражают дыхательные пути. Перенос микроорганизмов происходит при чихании или кашле вблизи незараженных объектов.
Трансмиссивный подразумевает передачу инфекции через кровь. Произойти это может при укусе переносчиком, например блохой, клещом, малярийным комаром, вшами. Контактным путем переносятся возбудители, которые располагаются на коже или слизистых. Проникают в организм через раны на теле или во время прикосновения к больному.
Половым путем передаются в основном венерические заболевания, как правило, непосредственно при половом контакте. Вертикальный механизм передачи представляет заражение плода от матери во время беременности.
Специфичность передачи инфекции
Для каждого вида микроорганизмов характерен свой механизм, благодаря которому вирусы или бактерии попадают в организм хозяина. Как правило, таких механизмов несколько, а определенные факторы внешней среды иногда могут поспособствовать передаче паразитов.
В то же время способ, который подходит одним микробам, совершенно не способствует переносу других. Например, многие возбудители респираторных инфекций абсолютно бессильны перед желудочным соком. Попадая в кишечно-желудочный тракт, они гибнут и не вызывают развития заболевания.
Некоторые механизмы попадания вредоносных микробов в организм могут, наоборот, ускорить развитие болезни. Так, попадание возбудителя сифилиса в кровоток при помощи зараженной медицинской иглы вызывает осложнения. Болезнь протекает интенсивнее.
Заключение
Инфекция представляет собой совокупность биологических процессов, возникающих и развивающихся в организме при внедрении в него патогенной микрофлоры. Недуг может поразить как человека, так и животного. Основными механизмами передачи является контактный, половой, воздушно-капельный, фекально-ротовой, вертикальный пути.
Источник инфекции – это среда, благоприятная для размножения и распространения микробов. Подходящими условиями зачастую обладают люди и животные. Окружающая среда, как правило, выступает в роли посредника.
Она обычно не обладает условиями для жизнедеятельности патогенных и условно-патогенных микроорганизмов. Продолжительное пребывание во внешней среде способствует их вымиранию. В отдельных случаях микроорганизмы способны сохраняться в почве, воде, песке от нескольких дне до десятилетий.
Проблема профилактики ВБИ является многоплановой и весьма трудна для решения по целому ряду причин - организационных, эпидемиологических, научно-методических. В ЛПУ независимо от профиля должны выполняться три важнейших требования:
- сведение к минимуму возможности заноса инфекции;
- исключение внутригоспитальных заражений;
- исключение выноса инфекции за пределы лечебного учреждения.
1 В целях профилактики возникновении и распространения внутрибольничных инфекций (ВБИ) разрабатывается план профилактических и противоэпидемических мероприятий, который, утверждается руководителем организации.
Профилактические мероприятия проводятся исходя из положения, что каждый пациент расценивается как потенциальный источник гемоконтактных инфекций (гепатит В, С, ВИЧ и других).
2. При плановом поступлении на стационарное лечение пациенты на догоспитальном этапе подлежат профилактическому обследованию на:
-туберкулез (флюорография, результаты действительны в течение года)
- маркеры гепатитов В и С, сифилис (в случае оперативного лечения);
-дифтерию и кишечные инфекции (пациенты психиатрических стационаров);
- кишечные инфекции (пациенты детских стационаров до 2 лет и сопровождающие лица, результаты действительны в течении 2 недель до госпитализации)
3.Дети, поступающие на стационарное лечение должны иметь сведения об отсутствии контактов с инфекционными больными в течение 21 дня до госпитализации.
4.Перед проведением плановых операций необходимо обеспечить выявление и санацию очагов имеющейся у пациента хронической инфекции на догоспитальном уровне.
5.Обеспечить коррекцию клинических показателей у пациентов в предоперационном периоде.
6.Следует максимально сокращать сроки пребывания пациента в стационаре (отделении) в период предоперационной подготовки.
7.При поступлении пациента на операцию, выполняемую в плановом порядке, предварительное обследование проводится в амбулаторно-поликлинических условиях с проведением хирургического вмешательства в стационаре (отделении) без повторного обследования. Каждый лишний день пребывания в стационаре увеличивает риск присоединения ВБИ.
8.Сроки выписки пациентов из хирургического стационара (отделения) определяются состоянием здоровья. С эпидемиологических позиций оправдана ранняя выписка пациентов.
9.Разрешается посещение пациентов родственниками, знакомыми. Порядок посещения отделения устанавливается администрацией лечебной организации.
10.Персонал должен соблюдать меры эпидемиологической предосторожности при работе с любым пациентом.
11.Независимо от использования перчаток, до и после контакта с пациентом, после снятия перчаток и каждый раз после контакта с кровью, биологическими жидкостями, секретами, выделениями или потенциально контаминированными предметами и оборудованием, проводится гигиеническая обработка рук.
12.При проведении манипуляций/операций, сопровождающихся образованием брызг крови, секретов, экскретов, персонал надевает маску, приспособления для защиты глаз (очки, щитки). При загрязнении любых средств индивидуальной защиты проводится их замена. Предпочтение отдается средствам защиты однократного применения.
13.Запрещается надевание колпачков на использованные иглы. После использования шприцы с иглами сбрасываются в непрокалываемые контейнеры. В случае необходимости отделения игл от шприцев необходимо предусмотреть их безопасное отсечение (специальные настольные контейнеры с иглоотсекателями или другими безопасными приспособлениями, прошедшими регистрацию в установленном порядке).
14.Острые предметы сбрасывают в непрокалываемые контейнеры.
15.Любой пациент рассматривается как потенциальный источник инфекции, представляющий эпидемиологическую опасность для медицинского персонала.
16.Пациентов с хирургической инфекцией изолируют в отделение гнойной хирургии, а при его отсутствии – в отдельную палату.
17.Перевязки пациентов, имеющих гнойное отделяемое, проводят в отдельной перевязочной или, при ее отсутствии, после перевязки пациентов, не имеющих гнойного отделяемого. Осмотр пациентов проводят в перчатках и одноразовых фартуках.
18.Персонал обрабатывает руки спиртосодержащим кожным антисептиком не только до осмотра и перевязки инфицированных пациентов, но и после.
19.Пациенты с острым инфекционным заболеванием подлежат госпитализации в специализированный стационар (отделение); по жизненным показаниям из-за оперативного вмешательства – изоляции в отдельную палату.
20.Все инвазивные диагностические и лечебные манипуляции проводятся в перчатках. Перчатки необходимы также при контакте со слизистыми оболочками пациентов и использованными инструментами.
21.Медицинский персонал, имеющий поражения кожи, отстраняется от работы и направляется на обследование и лечение.
22.При обработке операционного поля пациента перед хирургическим вмешательством и другими манипуляциями, связанными с нарушением целости кожных покровов и слизистых оболочек (пункции различных полостей, биопсии), предпочтение следует отдавать спиртосодержащим кожным антисептикам с красителем.
23.Не следует удалять волосы перед операцией, если только волосы возле или вокруг операционного поля не будут мешать её проведению. Если их необходимо удалять, то следует делать это непосредственно перед операцией, используя депиляторы (кремы, гели) или другие методы, не травмирующие кожные покровы.
24.При выборе антибиотиков следует отдавать предпочтение препаратам, активным в отношении ожидаемых (наиболее вероятных) при определенных операциях возбудителей инфекционных осложнений.
Профилактика внутрибольничных инфекций у медицинского персонала в стационарах (отделениях) хирургического профиля
Любое клинически выраженное заболевание микробного происхождения, которое поражает больного в результате его поступления в больницу или обращения за медицинской помощью вне зависимости от появления симптомов заболевания у пациента во время пребывания в стационаре или после его выписки, а также инфекционное заболевание сотрудника лечебной организации вследствие его инфицирования при работе в данной организации подлежит учету и регистрации как внутрибольничная инфекция.
1. При поступлении на работу в стационары (отделения) хирургического профиля медицинские работники проходят предварительный медицинский осмотр врачей: терапевта, невролога, гинеколога, дерматовенеролога, отоларинголога, офтальмолога. В дальнейшем осмотр у тех же специалистов проводится 1 раз в год. Дополнительные медицинские осмотры проводятся по показаниям.
2. Медицинские работники проходят следующие обследования:
- рентгенологическое обследование на туберкулез – крупнокадровая
флюорография грудной клетки (в дальнейшем – 1 раз в год);
- исследование крови на гепатит С (в дальнейшем – 1 раз в год);
- исследование крови на гепатит В не привитых (в дальнейшем – 1 раз в год); привитые обследуются через 5 лет, затем ежегодно при отсутствии ревакцинации;
- исследование крови на сифилис (в дальнейшем – по показаниям);
- исследование мазков на гонорею (в дальнейшем – по показаниям);
- исследование крови на ВИЧ-инфекцию (в дальнейшем – 1 раз в год).
- Проводятся лабораторные исследования: общий анализ крови и общий анализ мочи, в дальнейшем 1 раз в год перед периодическим медицинским осмотром.
3. В зависимости от появившейся (выявленной) у медицинских работников патологии проводятся другие диагностические исследования.
4. К работе не допускаются лица с изменениями в легких туберкулезного характера, а также лица с гнойно-воспалительными заболеваниями.
5. Плановое обследование медицинского персонала хирургических стационаров (отделений) на носительство золотистого стафилококка не проводят. Обследование медицинского персонала на носительство условно-патогенных микроорганизмов проводят только по эпидемиологическим показаниям.
6. Персонал стационаров (отделений) хирургического профиля подлежит профилактической иммунизации против гепатита B в обязательном порядке при поступлении на работу в случае отсутствия данных о прививке. Один раз в 10 лет персоналу проводится прививка против дифтерии и столбняка. В связи с задачей ликвидации кори в стране проводится дополнительная иммунизация лиц до 35 лет, не болевших корью и не привитых живой коревой вакциной или привитых однократно. Иммунизация против других инфекционных заболеваний проводится в соответствии с национальным календарем прививок, а также по эпидемиологическим показаниям.
7. В хирургических стационарах (отделениях) должен быть налажен учет травм и чрезвычайных ситуаций (порезы, уколы, попадание крови на видимые слизистые, поврежденные кожные покровы и др.), связанных с профессиональной деятельностью персонала, с указанием проведенных профилактических мероприятий (экстренная профилактика).
8. Весь персонал должен проходить ежегодное диспансерное наблюдение для своевременного выявления заболеваний и проведения соответствующих лечебных мероприятий.
9. Результаты периодических осмотров, лечения, сведения о профилактических прививках заносятся в контрольную карту диспансерного наблюдения и доводятся до сведения лица, ответственного за организацию и проведение мероприятий по профилактике ВБИ.
Не нашли то, что искали? Воспользуйтесь поиском:
Потенциальный источник инфекции для окружающих.
Отрицательное значение нормальной микрофлоры
Наряду с тем, что для каждого биотопа организма человека характерны определенные виды микроорганизмов, существуют индивидуальные различия в составе микроорганизмиоценозов. Эти различия могут быть качественными и (или) количественными. Поэтому при формировании новых коллективов (групп детских дошкольных учреждений, классов школ, групп других учебных заведений, а также в общежитиях, казармах, больницах, тюрьмах, семьях) происходит обмен микрофлорой между участниками коллектива. Период физиологической адаптации продолжается один месяц с момента устойчивого формирования коллектива. При этом обычно имеет место повышение уровня заболеваемости до формирования иммунитета.
Однако при нетяжелом течении заболеваний и отсутствии осложнений этот факт можно рассматривать как положительный: стимуляцию иммунной системы, что важно для поддержания ее нормального работоспособного состояния.
В неблагоприятных условиях, вызванных различными воздействиями на организм (см. причины дисбиоза) или на микрофлору (массивная антибиотикотерапия), а также при транслокации симбионтов в непривычные места обитания, мутуализм может превращаться в антагонизм и возникает дисбиоз или эндогенная инфекция. УП бактерии иногда могут вызывать гнойно-воспалительные заболевания: инфекции кожи и мягких тканей, ангину, пиелонефрит, пневмонию, перитонит, остеомиелит, эндокардит, сепсис.
3. Мутагенная функция: некоторые бактерии могут продуцировать сильные мутагены, способствуя возникновению и развитию опухолей.
4. Сенсибилизирующее действие и возможное развитие аллергических проявлений при нарушении иммунной регуляции.
5.Нормальная микрофлора содержит банк плазмидных генов, который может способствовать формированию патогенных клонов.
Онтогенез нормальной микрофлоры:
– - в утробе матери плод стерилен;
– - первичное заселение микроорганизмами организма ребенка происходит в процессе родов бактериями влагалища, где в норме преобладают лактобактерии и присутствует значительное количество бифидобактерий; при кесаревом сечении формирование микрофлоры отодвигается во времени и микроорганизмный пейзаж может изменяться;
– в послеродовом периоде микрофлора формируется под влиянием окружающей среды (микрофлора матери, воздух, руки медперсонала); в формировании микрофлоры детей первого года жизни существенную роль имеет естественное вскармливание;
– - количество и видовой состав микрофлоры расширяется и изменяется в зависимости от условий жизни и от особенностей функционирования иммунной системы ребенка. В течение ряда лет после рождения формируются микроорганизмиоценозы, наиболее сложные и многочисленные на коже, в полости рта, в носоглотке, в толстом кишечнике.
Нормальная микрофлора в количественном и качественном отношении представлена в различных биотопах организма человека неодинаково.
Эубиоз различных биотопов организма человека
На поверхности кожи человека находится от 25 млн до 1 млрд особей микроорганизмов. Максимальное количество микроорганизмов обнаруживается в местах, защищенных от действия света и высыхания — в складках кожи и вблизи естественных выходов из полостей. Наиболее постоянен состав микрофлоры в области устьев сально-волосяных фолликулов.
Собственная микрофлора кожи человека представлена стафилококками (эпидермальным, сапрофитным, золотистым), микрококками, сарцинами, некоторыми видами стрептококков, дифтероидами, бациллами, грибами рода Candida. В порах кожи обнаруживаются пропионобактерии. Количество микроорганизмов на разных участках кожи варьирует в зависимости от пола, возраста.
На коже могут присутствовать транзиторные микроорганизмы, быстро исчезающие под влиянием бактерицидных свойств кожи. Бактерицидность кожи отражает общую резистентность организма.
Большой способностью к самоочищению обладает чисто вымытая кожа. Размножению бактерий на коже способствует влажная теплая среда, которая создается при потоотделении. Выделение продуктов обмена бактерий создает неприятный запах. Для решения этой проблемы предлагаются два способа:
– уничтожение благоприятной среды для существования бактерий дезодорантами, содержащими антимикроорганизмные компоненты (триклозан, фарнезол, эфирные масла растений), ограничивающие размножение бактерий. На эффективность потоотделения они не влияют;
– предотвращение потоотделения путем временной закупорки каналов потовых желез дезодорантами-антиперспирантами, которые за счет вяжущих свойств солей алюминия сужают поры. Такие дезодоранты можно использовать в исключительных случаях (соли алюминия токсичны) и обязательно нужно смывать, так как полная блокировка пор недопустима (вместе с потом из организма выводятся многие токсические продукты обмена).
Неповрежденные кожные покровы непроницаемы для большинства микроорганизмов, благодаря кислотам, выделяемым микрофлорой и лизоциму пота.
Нарушение целостности эпидермиса (укус насекомых, укол, порез, травма) и снижение резистентности организма создает благоприятные условия для проникновения микроорганизмов.
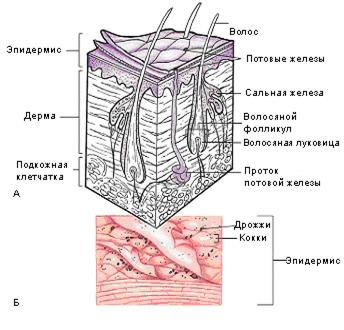
А. Эпидермис с железами и фолликулами (окрашены) богат разнообразной микрофлорой. Неокрашенные участки (дерма и подкожная клетчатка) стерильны.
Б. Вид кожи под очень большим увеличением, кожная поверхность покрыта кокковидными и палочковидными бактериями, дрожжевыми грибами.
Конъюнктива глазбедна микрофлорой, что обусловлено миганием и бактерицидными свойствами слезной жидкости (содержит лизоцим). На конъюнктиве глаза могут обнаруживаться стафилококки, дифтероиды (C. xerosis), пневмококки (S. pneumoniae), микоплазмы. При снижении естественной защиты организма, нарушении зрения, использовании контактных линз, гиповитаминозах нормальная микрофлора слизистых оболочек глаз может вызывать различные заболевания: конъюнктивиты и блефариты.
В наружнем слуховом проходе обнаруживаются те же микроорганизмы, что и на коже: непатогенные стафилококки, дифтероиды, дрожжеподобные и плесневые грибы (Aspergillus), которые в определенных условиях являются возбудителями патологических процессов.
Среднее и внутреннее ухо стерильны.
Микрофлора респираторного тракта
Носоглотка. В дыхательные пути вместе с воздухом попадают пылевые частички и микроорганизмы. Большая часть попавших микроорганизмов (3/4-4/5) задерживается в полости носа, удаляется или погибает вследствие обратного движения цилиарного эпителия, бактерицидного действия антимикроорганизмных веществ (лизоцима и sIgA), деятельности фагоцитов. Кашель и чиханье способствуют элиминации бактерий из носоглотки.
В состав облигатной микрофлоры носовых ходов входят стафилококки (может встречаться резидентное носительство S. aureus!), дифтероиды. Факультативная микрофлора представлена золотистым стафилококком, стрептококками, непатогенными нейссериями, бактероидами, вейлонеллами, микобактериями.
Многие патогены способны преодолевать слизистый барьер дыхательных путей за счет факторов инвазии. Поэтому некоторые микроорганизмы встречаются в гортани и верхних отделах трахее.
| Слизистые оболочки бронхови бронхиол свободны от микроорганизмов и защищены мукозной слизью, содержащей лизоцим, секреторными антителами и фагоцитами. При повреждении эпителия бронхов (ингаляционный наркоз, заболевания дыхательной системы, иммунодефицитные состояния) микроорганизмы могут проникать в бронхиальное дерево. Курение усугубляет этот процесс. | 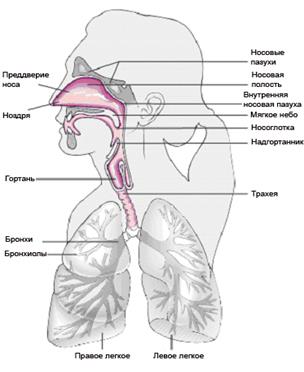 |
| Рис.. Колонизация микроорганизмами респираторного тракта Большинство слизистых оболочек носоглотки имеет пристеночную микрофлору (обозначена розовым цветом) |
Альвеолы и паренхима легкихстерильны. Незрелость детского организма, особенно у недоношенных (снижение синтеза сурфактанта, снижение продукции sIgA), способствует респираторным заболеваниям и их тяжелому течению.
Нам важно ваше мнение! Был ли полезен опубликованный материал? Да | Нет

Общие сведения
Частота регистрации ИСМП в разных странах варьирует в широких пределах. Так, в РФ этот показатель составляет 1-1,5% (40-60 тыс. случаев/год), США — 3-5 % (2,5 млн. случаев/год), Великобритании — 5-6 %, Германии —3,5 %, Китае — 7-8 %. Однако, эти показатели, особенно в странах СНГ и, в частности, России не отражают реальную эпидемиологическую ситуацию. Результаты научных исследований ведущих специалистов-эпидемиологов РФ свидетельствуют, что реальное количество ИСМП составляет в среднем около 10% и находится на уровне 2-2,5 миллионов случаев/год. Присоединение ИСМП к основному заболеванию увеличивает продолжительности лечения (пребывания в стационаре) пациента на 7-10 дней, а прямые затраты лечебных учреждений на 65-85 млрд рублей в год. Летальность при различных нозологических формах ИСМП варьирует в пределах 3,5-35%.
Наибольший удельный вес ИСМП приходится на хирургические и акушерские стационары (отделения травматологии, урологии, реанимации, абдоминальной хирургии, гинекологии, ожоговой травмы, стоматологии, отоларингологии, онкологии). Наиболее драматичны проявления ИСМП в отделениях интенсивной терапии и реанимации, где они в различных нозологических формах регистрируются в 25-30% случаев.
Патогенез
Патогенез внутрибольничных инфекций существенно различается и определяется видом заболевания, этиологическим фактором (видом возбудителя, факторами его вирулентности), механизмом и путями передачи инфекции.
Классификация
Прежде всего, различают две больших группы ИСМП (рис. ниже):
- Экзогенная инфекция — обусловлена заражением пациента инфекционным агентом в условиях посещения/нахождения в ЛПУ.
- Эндогенная инфекция — инфекции, вызванных условно-патогенными микроорганизмами, вегетирующими в пищеварительном тракте, на кожных и слизистых покровах, которые при неблагоприятных условиях становятся патогенными. В структуре ВБИ роль эндогенной инфекции незначительна.
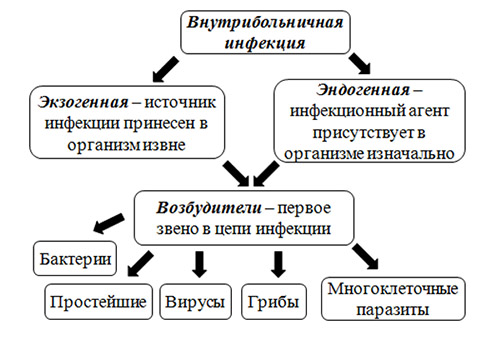
Группы и этиологический фактор ИСМП
В основу классификации ВБИ положены различные факторы. В зависимости от путей/факторов передачи различают воздушно-капельные, контактно-бытовые, контактно-инструментальные, постоперационные, постинфекционные, постэндоскопические, послеродовые, посттрансфузионные, постдиализные, посттравматические, постгемосорбционные и другие инфекции.
В зависимости от степени распространения инфекции различают:
- Генерализованные: бактериемия, септицемия, септикопиемия, токсико-септическая инфекция.
- Локализованные инфекции, включающие:
- Респираторные инфекции (ОРЗ, бронхит, плеврит, пневмония, легочный абсцесс и др.).
- Инфекции подкожной клетчатки/кожи (послеожоговые, послеоперационные, послетравматические), дерматомикозы, постинъекционные — абсцессы/флегмоны подкожной.
- Стоматологические инфекции (абсцесс, стоматит).
- ЛОР-инфекции (ринит, отиты, синуситы, ангина, ларингит, фарингит).
- Урологические инфекции.
- Инфекции пищеварительного тракта (энтерит, колит, гастроэнтероколит, холецистит, гепатиты др.).
- Постоперационные инфекции (перитонит, абсцессы брюшины).
- Инфекции глаза (конъюнктивит).
- Инфекции урологической и половой системы (пиелонефрит, уретрит, цистит, бактериурия, эндометрит, сальпингоофорит).
- Инфекции костно-cуставного аппарата (остеомиелит, бурсит, артрит).
- Инфекции сердечно-сосудистой системы (миокардит, эндокардит, перикардит, инфекции артерий и вен).
- Инфекции ЦНС (менингит).
- По характеру течения: острые, подострые, хронические. По тяжести течения: легкие, тяжёлые и среднетяжелые.
Причины
Этиологическим фактором ИСМП может быть чрезвычайно широкий спектр микроорганизмов (около 250 видов), принадлежащих к разным таксономическим группам: бактерии, вирусы, простейшие, грибы. При этом, инфекционным агентом могут быть патогенные, условно-патогенные микроорганизмы, а в ряде случаев и сапрофитная микрофлора. Наибольшей удельный вес в этиологической структуре ИСМП принадлежит возбудителям гнойно-септических инфекций (80-85%), кишечных инфекций (8-10%), вирусам гепатитов В, С, D (6-7%), инфекции дыхательных путей (2-3%). В целом, структура ВБИ изменчива и зависит преимущественно от профиля отделения/вида стационара и микробного пейзажа конкретного лечебного отделения (рисунок ниже).
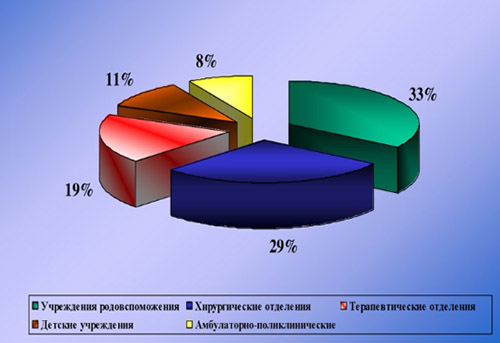
К возбудителям ВБИ, имеющими наибольшее значение относятся:
- грамположительная флора: стафилококки (золотистый, эпидермальный), стрептококки (пневмококк, энтерококк, пиогенный стрептококк);
- грамотрицательная флора: энтеробактерии (эшерихия, сальмонелла, шигелла, синегнойная палочка, клебсиелла, протей, иерсиния).
- вирусы (аденовирусной инфекции, простого герпеса, кори, ветряной оспы, гриппа, парагриппа, респираторно-синцитиальной инфекции, эпидпаротита, ротавирусы, риновирусы, энтеровирусы, возбудители вирусных гепатитов);
- грибы (рода Candida, аспергиллы).
Значимость различных видов ИСМП во многом определяется профилем ЛУ. Так, в гинекологических и родильных отделениях ведущую роль играет стафилококковая инфекция (золотистый стафилококк), кишечная палочка, энтерококки, диплоидный грибок (молочница); в ожоговых стационарах — синегнойная инфекция; в урологических отделениях — грамотрицательная микрофлора: кишечная, синегнойная палочка; в детских отделениях — вирусы краснухи, кори, эпидемического паротита, ветряной оспы.
Формирование госпитального штамма (с приобретенной устойчивостью) обеспечивается за счет их преимущества (доминирования) перед другими представителями микробной популяции. Основными отличиями госпитального штамма микроорганизма от стандартного являются: повышенная вирулентность (патогенность), формирующаяся за счет многократного пассажа через организм больных ЛПУ, высокая устойчивость к воздействию неблагоприятных факторов (дезинфектантам, антисептикам, химиопрепаратам, применяемым в конкретном мед. учреждении) и способность к длительному выживанию, постоянная циркуляция в среде больничного стационара среди больных и персонала.
Основную массу всех форм ВБИ (около 80%) составляют:
- инфекции мочевыделительной системы;
- ОРЗ и вентилятор-ассоциированные пневмонии;
- послеоперационные раневые гнойно-септические инфекции;
- кожные инфекции;
- интраабдоминальные инфекции;
- ангиогенные катетер-ассоциированные инфекции.
Любая нозологическая форма ВБИ развивается только при наличии всех звеньев эпидемического процесса: источника инфекции, механизма (факторов) передачи и восприимчивого организма человека.
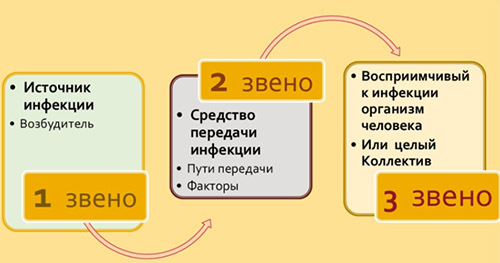
Основные источники внутрибольничной инфекции:
- больные и носители, находящиеся в стационаре;
- персонал лечебных учреждений;
- лица, ухаживающие за больными и посетители стационаров (студенты, лица, навещающие пациентов).
Аэрогенный — процесс заражения осуществляется через воздушную среду. Выделяют:
- воздушно-капельный путь (этим путем возбудитель передается при большинстве ОРЗ, пневмониях) при разговоре, кашле;
- воздушно-пылевой путь (передаются заболевания, возбудитель которых устойчив во внешней среде — кишечные инфекции, туберкулез, зоонозы).
- Контактно-бытовой путь – инфекционный агент передается через грязные рук, предметы личной гигиены, игрушки, посуду.
- Пищевой (реализуется через зараженные продукты питания при нарушениях технологии приготовления или хранения готовых блюд и пищевых продуктов).
- Водный (через воду).
- Прямой — передача возбудителя непосредственно через физический контакт между резервуаром инфекции (инфицированный индивидуум/контаминированный предмет) с кожей, слизистой или раневой поверхностью восприимчивого организма человека.
- Непрямой — посредством механического переноса инфекционного агента через руки медицинского персонала, предметы обихода, инструменты и оборудование лечебного учреждения. Непрямой контакт является наиболее часто задействованным путем распространения. Этот путь передачи часто называют артифициальным (искусственным) или парентеральным путем передачи возбудителя, который реализуется путем проведения различных инвазивных манипуляций (инъекции, забор крови, инструментальные манипуляции, вакцинацию, местные/общие операции) или использовании специальной аппаратуры при проведении гемодиализа, ИВЛ.
- Гемоконтактный — передается через кровь при обширных хирургические вмешательствах, инфузионной терапии, программном гемодиализе.
Заболеваемость ИСМП носит преимущественно эндемический характер и обусловлена индивидуальными факторами риска и клиническими процедурами. Значительно реже ИСМП протекают в виде локальных эпидемий. Развитию эпидемических вспышек способствует несвоевременная диагностика стертых форм заболевания и выявление носителей инфекционных агентов, как среди поступающих пациентов, так и среди медицинского персонала, контаминация предметов общего пользования, систематическое нарушение методов асептики при выполнении инструментальных процедур.
Специфичны для каждого вида инфекционного возбудителя. Однако, в целом для большинства нозологических форм ИСМП определяющими факторами являются параметры, характеризующие организм хозяина:
- возраст (пожилой/старческий, дети — новорожденные и раннего возраста, особенно недоношенные, со сниженной сопротивляемостью организма и перенесшие родовую травму);
- пациенты, страдающие тяжелыми хроническими заболеваниями, с алиментарной дистрофией;
- длительно находящиеся в стационаре и особенно на постельном режиме;
- беременные/роженицы;
- пациенты, получающие лучевую/иммуносупрессивную терапию;
- имунноскомпрометированные лица;
- больные после обширных хирургических операций, получающие кровезаместительную/инфузионную терапию, с программным гемодиализом, находящиеся на ИВЛ.
Факторы риска ИСМП, связанные с предметами окружающей среды (загрязнение поверхностей, воздуха, воды в распространении инфекции) имеют меньшую значимость.
Возникновению и распространению ИСМП способствуют:
Симптомы
Симптоматика внутрибольничных инфекций определяется конкретной нозологической формой и симптомами основного заболевания, формой и тяжестью их течения, вирулентностью инфекционного агента и состоянием организма больного.
Анализы и диагностика
К ВБИ относятся случаи, отвечающие следующим критериям:
- Повторное поступление пациента в стационар с установленной инфекцией (с клиническими признаками, данными инструментальных и лабораторных методов исследовани — микробиологических, серологических и методов экспресс-диагностики), являющееся следствием предыдущей госпитализации.
- Период развития клинической симптоматики заболевания ВБИ после поступления в лечебный стационар должен составлять не менее 48 часов и более.
- Выявляется четкая взаимосвязь между симптоматикой заболевания и проведенными вмешательства инвазивного типа (после ингаляции, инъекций, перевязки и т.д.) или в ряде случаев — с выявленным источником инфекционного агента (поступивший больной со стертой формой заболевания/носитель) и фактором ее распространения.
Для точной диагностики заболевания и определения конкретного штамма возбудителя инфекции, требуется проведение лабораторных—бактериологических/серологических исследований различных биоматериалов (мазок из зева, мокрота, кровь, моча, кал, раневое отделяемое).
Лечение
Проблема лечения госпитальных инфекций представляет значительную трудность, что обусловлено неэффективностью большинства широко применяемых антибиотиков, в частности цефалоспоринов. Для лечения таких инфекций применяются карбапенемы (Меропенем, Дорипенем), имеющие широкий спектр антимикробной активности, в частности к микроорганизмам, устойчивым к пенициллинам/цефалоспоринам или в ряде случаев комбинированные лекарственные препараты пенициллинов с ингибиторами бета-лактамаз (Пиперациллин + Тазобактам, Тикарциллин, Амоксициллин-Клавуланат и др.).
Карбапенемы используются для лечения тяжелых нозокомиальных пневмоний и других инфекций верхних дыхательных путей; инфекций органов малого таза, гинекологических, абдоминальных, мочеполовых инфекций; кожи и мягких тканей; сепсиса. Однако, препараты этой группы могут вызывать побочные реакции в виде крапивницы, сыпи, диспепсических расстройств, поражения печени и почек, дисбактериоза.
При выявлении метициллинрезистентных штаммов золотистого стафилококка, являющегося частым возбудителем внутрибольничных резистентных стафилококковых инфекций для лечения, используются гликопептидные антибиотики (Ванкадицин, Тейкопланин-Тева, Ликованум, Таргоцид и др.), которые высокоактивны по отношению к грамположительным аэробным/анаэробным инфекционным агентам — стафилококкам, стрептококкам, пневмококкам, энтерококкам, клостридиям, листериям, коринебактериям и другим. Показаниями к назначению являются тяжелые инфекции, вызванные энтерококками, инфекционный эндокардит, ассоциированный с зеленящими стрептококками, менингит и пневмонии, вызванные пневмококком, катетер-ассоциированный сепсис, перитонит, антибиотик-ассоциированная диарея и других инфекций, угрожающих жизни. В ряде случае гликопептидные антибиотики сочетаются с цефалоспоринами 3 поколения (Цефтибутен, Цефиксим, Цефотаксим, Цефоперазон, Цефтазидим и др.) или фторхинолонами (Офлоксацин, Ципрофлоксацин, Пефлоксацин, Норфлоксацин, Левофлоксацин и другие).
Необходимо отметить, что спектр возбудителей внутригоспитальных осложнений, а также их антибиотикорезистентность существенно различаются в отделениях различного профиля, поэтому при выборе антибиотика следует ориентироваться на чувствительность выделенной микрофлоры к ним, в также учитывать эпидемиологическую ситуацию в каждом конкретном лечебном учреждении.
Кроме антибиотикотерапии назначается специфическое лечение при той или иной конкретной нозологической форме ВБИ с учетом клинических проявлений, тяжести течения, риска развития осложнений. В индивидуальном порядке проводится симптоматическое лечение. В качестве дополнительной терапии назначают иммуностимуляторы: интерферон; бактериофаги, витаминно- минеральные комплексы.
В настоящее время для борьбы с тяжелыми проявлениями ВБИ разработана стратегия деэскалационной терапии, базирующаяся на нескольких принципах:
- Безотлагательное начало проведения антибактериальной терапии.
- Выбор антимикробных препаратов (АМП) с учетом чувствительности микроорганизмов и способности проникать в ткани, при отсутствии таких данных — использование антибиотиков широкого спектра действия.
- Назначение высоких доз антибиотиков, подбираемых индивидуально.
Эта стратегия предполагает безотлагательное назначение стартового антибиотика широкого спектра действия (комбинации антибиотиков) с целью максимально полного охвата спектра вероятных возбудителей с последующим переходом на антибиотик, к которому отсутствует устойчивость согласно данным микробиологического исследования. Именно своевременная и адекватная антимикробная терапия является ключевым условием и благоприятным прогностическим фактором, увеличивающей вероятность благоприятного исхода заболевания.
Читайте также:


