При бас мышцы не болят
Какими лекарственными препаратами можно облегчить сильные боли при боковом амиотрофическом склерозе? Боль в руках, плечах, груди.
Вообще, типично ли такое течение болезни?
Был у врача в местной больнице, тот посоветовал капельницу с обезболивающим препаратом (еще, кажется, и гормонами, но я не помню) - не помогает, еще хуже становится. Кеторол - просто не помогает.
У меня мама болеет, я понимаю, что ничего хорошего в недалеком будущем не будет, но до слёз обидно, когда она от боли корчится, а сделать ничего невозможно.
Заранее благодарю.
Боюсь, что Вам придется взять маму к себе, т.к. с течением времени могут присоединиться нарушения глотания.
С уважением и удачи!
Arch Phys Med Rehabil. 2005 Jun;86(6):1155-63. Links
Chronic pain in persons with neuromuscular disease.Jensen MP, Abresch RT, Carter GT, McDonald CM.
Department of Rehabilitation Medicine, University of Washington School of Medicine, Box 356490, Seattle, WA 98195-6490, USA. [Ссылки могут видеть только зарегистрированные и активированные пользователи]
OBJECTIVE: To examine the nature and scope of pain in persons with neuromuscular disorder (NMD). DESIGN: Survey study. SETTING: University-based rehabilitation research programs. PARTICIPANTS: Adults with NMD (N=193). INTERVENTIONS: Not applicable. MAIN OUTCOME MEASURES: Pain presence or absence, pain severity, pain quality (Neuropathic Pain Scale), pain interference (Brief Pain Inventory), pain site, quality of life (Medical Outcomes Study 36-Item Short-Form Health Survey [SF-36]), and pain treatment. RESULTS: Seventy-three percent of the sample reported pain, with 27% of these reporting that this pain was severe (> or =7 on a 0-10 scale), on average. "Deep," "tiring," "sharp," and "dull" were the words used most frequently to describe NMD pain. Patients with amyotrophic lateral sclerosis and myotonic muscular dystrophies reported the greatest pain interference, and patients with Charcot-Marie-Tooth the least, among all NMD diagnoses. The most frequent pain site, overall, was back (49%), followed by leg (47%), shoulder (43%), neck (40%), buttock and hip(s) (37%), feet (36%), arm(s) (36%), and hand(s) (35%). The study participants reported significantly greater dysfunction than subjects in the SF-36 normative sample (persons without health problems) on a number of the SF-36 scales. However, we found no significant differences between the study participants and the US norms on the SF-36 role-emotional or mental health scales. A number of pain treatments were used by the study sample, but no treatment appeared to be effective for all participants, and some of the treatments reported as most effective (eg, chiropractic care) were used by very few participants. CONCLUSIONS: Pain is a common problem among patients with NMDs. There are many similarities, but also some important differences, between NMD diagnostic groups on the nature and scope of pain and its impact. More research is needed to identify and test effective treatments for NMD-related pain.
PMID: 15954054 [PubMed - indexed for MEDLINE]
Am J Hosp Palliat Care. 2002 Jan-Feb;19(1):39-48. Links
Assessment of pain and health-related quality of life in slowly progressive neuromuscular disease.Abresch RT, Carter GT, Jensen MP, Kilmer DD.
University of California, Davis, Department of Physical Medicine and Rehabilitation, USA.
Few studies have examined the effect of pain on the quality of life of individuals with slowly progressive neuromuscular disease (NMD). The purpose of this study was to determine the frequency and extent to which subjects with slowly progressive NMD report pain and the association between pain and health-related quality of life in persons with NMD. The study design was a descriptive, nonexperimental survey. Of a total of 1,432 subjects with slowly progressive NMDs recruited from a university-based NMD clinic and the membership rosters of worldwide NMD support organizations, 859 agreed to participate. The primary measurement tool used was the Medical Outcomes Study SF-36 health survey. Our results indicated that, with the exception of adult spinal muscular atrophy (SMA), the frequency and severity of pain reported in slowly progressive NMDs was significantly greater than levels of pain reported by the general US population and was comparable to pain reported by subjects with osteoarthritis and chronic low back pain. There was a significant correlation between increased pain and lower levels of general health, vitality, social function, and physical role. Pain was moderately associated with increased fatigue, inability to cope adequately with stress, and sleep disturbance. In conclusion, with the exception of adult SMA, the frequency and severity of pain reported in slowly progressive NMDs was significant.
PMID: 12173612 [PubMed - indexed for MEDLINE]
Neurology. 2002 Aug 13;59(3):428-31. Links
The final month of life in patients with ALS.Ganzini L, Johnston WS, Silveira MJ.
Behavior Health and Clinical Neurosciences Division, Portland VA Medical Center, PO Box 1034, Portland, OR 97207, USA. [Ссылки могут видеть только зарегистрированные и активированные пользователи]
OBJECTIVE: To study the health care experiences and palliative care needs of patients with ALS in their final month of life. METHODS: Caregivers of decedent patients with ALS completed a single survey focused on the final month of life. They reported the patients' physical and emotional symptoms, preferences for end-of-life care, completion of advance directives, and preparation for death. The caregiver reported which life-sustaining treatments were administered, withheld, or withdrawn; whether the patient was enrolled in hospice; and their own satisfaction with the patient's medical care. RESULTS: Fifty caregivers completed the survey. Caregivers reported that the most common symptoms in the last month of life included difficulty communicating (62%), dyspnea (56%), insomnia (42%), and discomfort other than pain (48%). Pain was both frequent and severe. One-third of caregivers were dissatisfied with some aspect of symptom management. Caregivers reported an advance directive was completed by 88% of patients and the patients' goals of care were honored by 88% of health care practitioners. Two-thirds of patients were enrolled in hospice. Compared to nonhospice patients, hospice patients were significantly more likely to: 1) die in their preferred location; 2) die outside the hospital; and 3) receive morphine. Most caregivers reported that their loved one was at peace, and prepared for and was accepting of death. CONCLUSIONS: Caregivers report that many patients with ALS still experience distressing physical symptoms in the last month of life, despite enrollment in hospice. Most patients with ALS, however, anticipate and plan for their deaths and have their wishes respected.
PMID: 12177378 [PubMed - indexed for MEDLINE]
[Ссылки могут видеть только зарегистрированные и активированные пользователи]
Am J Hosp Palliat Care. 2004 Mar-Apr;21(2):95-104. Links
Survey of cannabis use in patients with amyotrophic lateral sclerosis.Amtmann D, Weydt P, Johnson KL, Jensen MP, Carter GT.
Department of Rehabilitation Medicine, University of Washington School of Medicine, Seattle, Washington, USA.
Cannabis (marijuana) has been proposed as treatment for a widening spectrum of medical conditions and has many properties that may be applicable to the management of amyotrophic lateral sclerosis (ALS). This study is the first, anonymous survey of persons with ALS regarding the use of cannabis. There were 131 respondents, 13 of whom reported using cannabis in the last 12 months. Although the small number of people with ALS that reported using cannabis limits the interpretation of the survey findings, the results indicate that cannabis may be moderately effective at reducing symptoms of appetite loss, depression, pain, spasticity, and drooling. Cannabis was reported ineffective in reducing difficulties with speech and swallowing, and sexual dysfunction. The longest relief was reported for depression (approximately two to three hours).
PMID: 15055508 [PubMed - indexed for MEDLINE]
Уважаемые коллеги! Откройте PubMed и наберите сами Pain in lateral amyotrophic sclerosis.
Ваши заблуждения насчет отсутствия боли при БАС извинительны, поскольку лечению, диагностике и эпидемиологии хронических болевых синдромов в нашей стране внимания практически никто не уделяет и эта проблема просто выпадает из поля зрения профильных специалистов.
Я не сам поставил диагноз БАС,не мне его и снимать. Мое дело разобраться с болевым синдромом, каковой на мой (достаточно просвещенный) взгляд имеет у пациентки смешанный характер - соматический (crampi and spastity) и нейропатический (потеря чувствительности и онемение). Для подтверждения был рекомендован опросник для выявления нейропатической боли DN4.
Все препараты были рекомендованы в минимальной дозировке с последующим титрованием дозы. Поэтому решительная редактура поста модераторм мне представляется неправильной. Тем более, что предложенная "консультация с лечащим врачом" для больной представляется достаточно затруднительным делом.
В заключение хочется порекомендовать следующий принцип, рекомендуемый IASP: сначала обезболь, затем разбирайся в диагнозе.
Так Вы все рекомендации потерли напрочь.
Итак, повторюсь:
Препараты, направленные на лечение спастики "центральные миорелаксанты", предпочтительно - баклофен, начиная с минимальной дозировки, с титрованием дозы по эффекту.
Побочное действие
Со стороны ЦНС и периферической нервной системы: сонливость, головокружение, нарушение походки, повышенная утомляемость, спутанность сознания, апатия, эйфория, депрессия, парестезии, атаксия, тремор, нистагм, парез аккомодации, галлюцинации, судороги, снижение судорожного порога.
Со стороны пищеварительной системы: тошнота, рвота, сухость во рту, запор, диарея.
Со стороны мочевыделительной системы: задержка мочи, дизурия, энурез; при длительном применении - нарушение функции почек.
Со стороны сердечно-сосудистой системы: артериальная гипотензия.
Прочие: миалгия, мышечная слабость.
– психозы;
– болезнь Паркинсона;
– эпилепсия;
– судороги (в анамнезе);
– хроническая почечная недостаточность;
– беременность;
– лактация (грудное вскармливание);
– повышенная чувствительность к баклофену
Препараты, "модулирующие" предачу болевого импульса, габапентин (нейронтин=тебантин), начиная с минимальной дозировки, с титрованием дозы по эффекту.Побочное действие
Со стороны ЦНС: возможны сонливость, головокружение, слабость, головная боль, атаксия, тремор, диплопия, нистагм, амблиопия, возможны повышенная раздражительность, амнезия, дизартрия, судороги.
Со стороны пищеварительной системы: возможны тошнота, рвота, диспепсия; редко - панкреатит, изменения функциональных проб печени.
Со стороны дыхательной системы: возможны ринит, фарингит, кашель.
Прочие: возможны увеличение веса, миалгия, синдром Стивенса-Джонсона.
Панкреатит, повышенная чувствительность к габапентину, детский возраст до 12 лет.
Сильные боли при БАСе все же характерны для последних стадий болезни, когда больной уже обездвижен. Нейропатические боли, если бывают при БАС, то обусловлены сопутствующей полинейропатией, например диабетической.
Спасибо за полезную информацию.
Вы могли бы сказать, что в лечении боли при БАСе используются такие-то лекарства, без указания дозировок. И рекомендовать обсудить лечение со своим лечащим врачом. В конце концов можно порекомендовать показать лечащему врачу распечатку данного обсуждения.
Peebody понял меня правильно: родители, в том числе и мама, живут в сельской местности, до районного центра - 15 километров. Маме уже тяжело сидеть, поэтому возить её в больницу невозможно. В больнице этого районного центра невропатолога нет. Приезжает он из областного центра только раз в месяц, чтобы в течение рабочего дня принимать больных, потом на месяц уезжает обратно. Т. е. фактически лечащий врач - это местый терапевт, в достаточной квалификации которого в области неврологии и неврохирургии я сомневаюсь.
А то, что руководствуясь Вашими рекомендациями сын пойдет и купит лекарства и сам будет давать их маме, тем более сейчас все можно купить без рецепта. Кто будет отвечать в случае ухудшения состояния, развития побочных реакций? ИМХО, не правильно это.
Да, пойду и куплю, потому что хуже уже быть не может. Вы же врач, и должны понимать, что состояние здоровья при таком диагнозе ухудшается постоянно, тем более, что течение болезни злокачественное.
Отвечать за все последствия буду я, разумеется. Вы мне дали консультации, голову на плечах я имею, могу здраво рассудить и последствия взвесить.
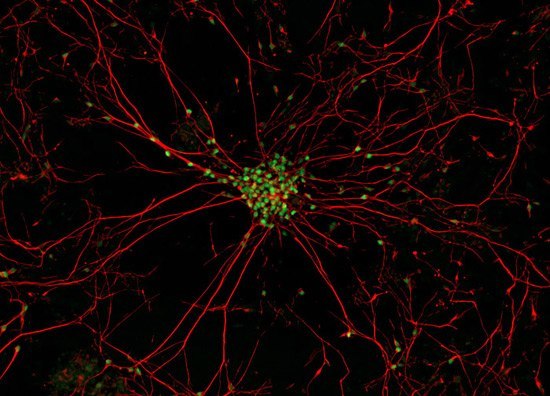
Настоящее фото мотонейрона (двигательного нейрона в передних рогах спинного мозга) - закупорка межсинаптических щелей (зелёные точки) - блокада передачи импульсов через медиаторы (вещества для передачи импульсов) в синапсы (места соединения) отростков нервных клеток.
В центре - тело мотонейрона.
Красные линии -длинные отростки мотонейрона - аксоны и короткие -дендриты.
Причина появления блокады передачи импульсов в межсинаптических щелях учёными мира не найдена. Предположительно - мутация гена,кодирующего фермент передачи этих импульсов через нейромедиаторы - супероксиддисмутазы. (СОД).
Предрасположенность к мутациям гена может иметь наследственный характер по аутосомно-рецессивному типу.
Эндемические (массовые вспышки) случаи этого заболевания зафиксированы у групп военных, живущих в островах на тихом океане. Чаще болеют мужчины от 40 до 60 лет.Следовательно не исключается инфекционная причина развития заболевания.
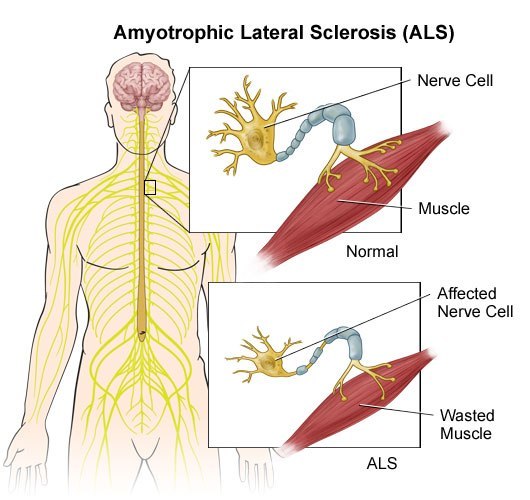
Боковой амиотрофический склероз. (БАС)..
Показано истончение нервных волокон в случае БАС и нарушение иннервации (передачи нервных импульсов) к мышцам. Как следствие - уменьшение работы мышцы и её последующая атрофия. (уменьшение размеров, обратное развитие.)
Блокада передачи нервных импульсов к мышцам (как к поперечно-полосатым которыми мы управляем сами своей волей так и к к гладким, работающим, независимо от нашего сознания, усилий и воли) пищеварительной и дыхательной системы ведёт к смерти из-за невозможности совершать эти жизненно важные моменты работы мускулатуры.
Две статьи из медицинских источников:
1) Теория аксостаза бокового амиотрофического склероза. Аксональная теория бокового амиотрофического склероза
Теория аксостаза основана на анализе патологических процессов, происходящих в аксональном транспорте мотонейронов [Chou S., 1992]. Наибольшими нейронами организма являются двигательные мотонейроны передних рогов спинного мозга и пирамвды Беца. Они должны поддерживать интеграцию дендритов, часто протяженностью более 1 см, и аксон, достигающий 100 см. В аксоне имеются непрерывные потоки, через которые клеточное тело направляет структурные и функциональные белки на периферию и получает обратные сигналы. Ортоградный транспорт бывает 2 видов: а) быстрый — 400 мм в день, идущий в обоих направлениях и транспортирующий связанные с мембраной белки и гликопротеиды, б) медленный — несколько миллиметров в день, транспортирующий сети микрофиламентов, микротрубочек, нейрофиламентов, как компонент "а" (0,1—2 мм в день), а также большой комплекс растворимых белков, как компонент "б" (2—4 мм в день). Ретроградный аксональный транспорт несет эндогенные (аминокислоты, фактор роста нервов) и экзогенные (токсин столбняка, вирус полиомиелита, простого герпеса, бешенства, лектин пероксидазы хрена и др.) субстанции от терминальных аксонов к клеточному телу со скоростью свыше 75 мм в день. Морфологические исследования аксонального транспорта в биоптатах двигательных веточек периферических нервов больных боковым амиотрофическим склерозом выявили уменьшение скорости ретроградного аксонального транспорта и, следовательно, связи терминального аксона с перикарионом [Bieuer A. et al., 1987]. В межреберных нервах больных АБС еще до развития признаков нейрональной дегенерации появляются изменения белков микротрубочек [Binet S. et al., 1988].
Улыраструктурные исследования проксимального аксона и аксонального бугорка мотонейронов переднего рога спинного мозга больных, умерших от бокового амиотрофического склероза [Sasaki S. et al., 1996], показали нарушение быстрого аксонального транспорта. Гладкий эндо-плазматический ретикулум теряет структуру: происходит скопление митохондрий, лизосом, Леви-подобных телец, эозино-фильных и гиалиновых включений, липофусциновых гранул, особенно в аксональном бугорке. Присутствие этих необычных структур является отражением дисфункции аксонального транспорта. Применительно к возможной этиологии АБС еще ранее выдвинута концепция "аксостаза" [Chou S., 1992]. Ней-ротоксические факторы путем ретроградного транспорта избирательно поражают нейрон, создавая феномен "суицидцального транспорта". Ухудшение медленного транспорта в аксоне сопровождается скоплением нейрофиламентов, набуханием проксимального аксона и последующей дистальнои аксональной атрофией, а также вторичной демиелинизацией, характерной для центральной дистальнои аксонопатии или "ретроградного умирания" — "dying back". Определенную значимость в развитии ранних морфологических изменений мотонейронов при АБС имеет теория аутоиммунитета [Smith R. et al., 1996], основанная на появлении антител к зарядам входа кальциевых каналов. Пассивный перенос фракций, содержащих иммуноглобулин, мышам вызывает изменения нервно-мышечных соединений, сходные с таковыми при спорадическом АБС. У животных эти изменения отражают расстройства внутриклеточного Са2+ гомеостаза, и раннее повреждение пластинчатого комплекса в мотонейронах в форме набухания и фрагментации. Иммуноглобулины от больных спорадическим боковым амиотрофическим склерозом вызывают зависимый от Са2+ апоптоз клеток вследствие оксидативных повреждений. Апоптоз, обусловленный иммуноглобулином от указанных больных, регулируется присутствием связанных белков, которые могут модулировать избирательную ранимость нейронов при спорадическом АБС.
2) Боковой амиотрофический склероз
Несмотря на более чем 100-летнее изучение, боковой амиотрофический склероз (БАС) остается фатальным заболеванием центральной нервной системы. Заболевание характеризуется неуклонно прогрессирующим течением с избирательным поражением верхнего и нижнего мотонейронов, что приводит к развитию амиотрофий, параличей и спастичности. До настоящего времени вопросы этиологии и патогенеза остаются невыясненными, в связи с чем не разработаны специфические методы диагностики и лечения этого заболевания. Рядом авторов отмечено повышение частоты встречаемости заболевания среди лиц молодого возраста (до 40 лет).
МКБ-10 G12.2 Болезнь двигательного неврона
ЭПИДЕМИОЛОГИЯ
Боковой амиотрофический склероз дебютирует в возрасте 40 – 60 лет. Средний возраст начала заболевания 56 лет. БАС - болезнь взрослых, и не наблюдается у лиц моложе 16 лет. Несколько чаще заболевают мужчины (отношение мужчины-женщины 1,6-3.0: 1).
БАС является спорадическим заболеванием и встречается с частотой 1,5 – 5 случая на 100 000 населения.
В 90% случаев БАС носит спорадический, а в 10% - семейный или наследственный характер как с аутосомно-доминантным (преимущественно), так и с аутосомно-рецессивным типами наследования. Клинические и патоморфологические характеристики семейного и спорадического БАС практически идентичны.
В настоящее время возраст является основным фактором риска при БАС, что подтверждается нарастанием заболеваемости после 55 лет, и в этой возрастной группе уже не наблюдается различий между мужчинами и женщинами. Несмотря на достоверную связь БАС с возрастом, старение является только одним из предрасполагающих факторов развития патологического процесса. Вариабельность заболевания как в различных возрастных группах, так и среди лиц одного возраста предполагает существование определённых факторов риска: дефицит, или наоборот, наличие определённых нейропротективных факторов, к которым в настоящее время относят: нейростероиды или половые гормоны; нейротрофические факторы; антиоксиданты.
Некоторые исследователи отмечают особо благоприятное течение заболевания у молодых женщин, что подтверждает несомненную роль половых гормонов, в особенности эстрадиола и прогестина, в патогенезе бокового амиотрофического склероза. Подтверждением этому являются: большая частота встречаемости БАС у мужчин до 55 лет (при этом у них отмечается более раннее начало и быстрое прогрессирование заболевания по сравнению с женщинами); с наступлением менопаузы женщины болеют также часто, как и мужчины; единичные случаи заболевания боковым амиотрофическим склерозом во время беременности. К настоящему времени существуют единичные работы по изучению гормонального статуса больных с боковым амиотрофическим склерозом, и ни одной, посвящённой определению концентраций гормонов у молодых пациентов.
Этиология заболевания не ясна. Обсуждается роль вирусов, иммунологических и метаболических нарушений.
В развитии семейной формы БАС показана роль мутации в гене супероксиддисмутазы-1 (Cu/Zn-супероксиддисмутазу, SOD1), 21q22-1 хромосома, выявлен также БАС, связанный с 2q33-q35 хромосомой.
Синдромы, клинически не отличимые от классического БАС, могут возникать в результате:
•опухоли большого затылочного отверстия
•спондилез шейного отдела позвоночника
•артериовенозная аномалия спинного мозга
•бактериальные - столбняк, болезнь Лайма
•вирусные - полиомиелит, опоясывающий лишай
Интоксикации, физические агенты:
•токсины - свинец, алюминий, другие металлы.
Что такое боковой амиотрофический склероз?
Боковой амиотрофический склероз (БАС) — является очень серьезным заболеванием центральной и периферической нервной системы. Он известен уже более 100 лет и встречается во всем мире.
Причина её возникновения неизвестна, за исключением редких наследственных форм. Аббревиатура бокового амиотрофического склероза (БАС) не имеет ничего общего с рассеянным склерозом, это две совершенно разные болезни.
БАС ежегодно обнаруживается у каждого второго из 100 000 человек. Заболевание обычно начинается в возрасте от 50 до 70 лет, но редко поражает молодых людей. Мужчины болеют чаще, чем женщины (1,6: 1). Частота БАС в мире с каждым годом увеличивается. Уровень заболеваемости у разных пациентов сильно различается, продолжительность жизни сокращается.
Боковой амиотрофический склероз влияет почти исключительно на двигательную нервную систему. Ощущение осязания, боли и температуры, зрения, слуха, обоняния и вкуса, функции мочевого пузыря и кишечника остаются нормальными в большинстве случаев. У некоторых пациентов могут наблюдаться слабые умственные способности, которые обычно обнаруживаются только при определенных обследованиях, но серьезные проявления встречаются редко.

Заболевание двигательных нервных клеток в спинном мозге и их отростки к мускулатуре, приводит к непроизвольным подергиваниям мышц (фасцикуляция), мышечной атрофии (атрофии) и мышечной слабости (парезы) на руках и ногах и в дыхательных мышцах.
Когда поражаются двигательные нервные клетки в стволе мозга, речь, жевательные и глотательные мышцы ослабляются. Эта форма БАС также называется прогрессирующим бульбарным параличом.
Болезнь двигательных нервных клеток в коре головного мозга и связывание его со спинным мозгом, приводит как к параличу мышц, так и к повышению мышечного тонуса (спастический паралич) с увеличением рефлексов.
Боковой амиотрофический склероз (БАС) прогрессирует быстро и неумолимо в течение нескольких лет. На сегодняшний день лечения нет, причина в значительной степени неизвестна. Заболевание начинается во взрослом возрасте, как правило, между 40-а и 70-ю годом жизни. Регрессирование варьируются в зависимости от скорости прогрессирования и порядка симптомов и потери функции. Поэтому надежный прогноз для каждого отдельного пациента дать невозможно.
Боковой амиотрофический склероз до сих пор является одним из самых смертельных заболеваний человека. В частности, это предъявляет огромные требования к больным пациентам, а также к их родственникам и заботливым врачам: больной человек испытывает постепенное снижение его мышечной силы с полной интеллектуальной целостностью. Члены семьи требуют огромного количества терпения и сочувствия.
Причины и факторы риска
Как нервное заболевание, боковой амиотрофический склероз известен давно, однако причины заболевания до сих пор в значительной степени не изучены. Болезнь возникает, как вследствие наследственной предрасположенности, так и спонтанно. Большинство случаев все же происходит спонтанно.
Каждая 100 страдающих БАС имеет наследственную или вновь возникающую мутацию в определенном гене, которая важна для клеточного метаболизма.
Это препятствует образованию фермента, который удаляет свободные радикалы кислорода в клетке. Неудаленные радикалы могут нанести значительный ущерб нервным клеткам, мешая передаче команд мышцам — в результате мышечная слабость и, наконец, полный паралич.
Формы БАС
Есть 3 различные формы БАС:
- Семейная форма: болезнь передается через гены (C9ORF72-ген).
- Спорадическая форма: причина заболевания неизвестна.
- Эндемическая форма: БАС встречается гораздо чаще, также по неясным причинам.
Симптомы бокового амиотрофического склероза
Первые симптомы могут возникать в разных местах у отдельных пациентов. Например, мышечная атрофия и слабость могут проявляться только в мышцах предплечья и кистей на одной стороне тела, прежде чем они распространятся на противоположную сторону и на ноги.
Редкое признаки начинают проявляться сначала в мышцах голени и стопы или в мышцах плеча и бедра.
У некоторых пациентов первые симптомы возникают в области речи, жевания и глотания мышц (бульбарный паралич). Очень редко первые симптомы выражаются в виде спастических параличей. Даже на ранних стадиях БАС больные часто жалуются на непроизвольное подергивание мышц (фасцикуляция) и болезненные мышечные спазмы.
Как правило, болезнь прогрессирует равномерно медленно в течение многих лет, распространяется на другие области тела и сокращает продолжительность жизни. Однако известны и очень медленные случаи развития болезни в течение 10 лет и более.
Осложнения
БАС, как хроническое прогрессирующее заболевание, вызывает проблемы с дыханием у большинства пациентов. Они вызваны поражением 3 различных групп мышц: вдыхательные и выдыхательные мышцы и мышцы горла/гортани (бульбарная мускулатура).
Последствия поражения вдыхательных мышц, главной мышцы диафрагмы — является недостаточная вентиляция легких (альвеолярная гиповентиляция). В результате уровень углекислого газа в крови увеличивается, а содержание кислорода в крови снижается.
Слабость мышц выдоха — в первую очередь брюшных мышц — приводит к ослаблению кашляющего импульса. Существует опасность накопления секреции в дыхательных путях с частичным полным их закрытием (ателектаз) или вторичной инфекцией в результате колонизации плохо вентилируемых компонентов легких бактериями.
У пациентов с боковым амиотрофическим склерозом регулярно слабый приступ кашля, если поражены одна или несколько групп мышц, описанных выше. Последствия — накопление секреций в дыхательных путях, инфекции, одышка и удушье.
Диагностика БАС
Ответственным за постановку диагноз является невролог (специалист по нервным заболеваниям). Пациент первоначально осматривается клинически, в частности, должны оцениваться мышцы с точки зрения мышечного тонуса, силы и фасцикуляций.
Также важна оценка речи, глотания и дыхательной функции. Должны быть проверены рефлексы пациента. Кроме того, необходимо исследовать другие функции нервной системы, которые обычно не затрагиваются боковым амиотрофическим склерозом, чтобы обнаружить похожие, но причинно различные заболевания и избежать ошибочного диагноза.
Важным дополнительным обследование заболевания является электромиография (ЭМГ), которая может доказать поражение периферической нервной системы. Обширные исследования скорости нервной проводимости дают дополнительную информацию.
Кроме того, необходимы анализы крови, мочи и при первоначальном диагнозе в основном цереброспинальной жидкости (ликвора). Различные диагностические исследования (магнитно-резонансная томография или рентген) также являются частью диагностики. По сути, дополнительный диагноз должен исключать другие типы заболеваний, например воспалительные или иммунологические процессы, которые могут быть очень похожи на БАС, но могут быть более излечимыми.
Варианты лечения бокового амиотрофического склероза
Поскольку причина возникновения БАС еще не известна, нет причинно-следственной терапии, которая могла бы остановить или вылечить болезнь.
Снова и снова эффективность новых лекарств, которые должны задерживать течение болезни, тщательно изучаются и тестируются. Первый препарат, Рилузол, вызывает умеренное увеличение продолжительности жизни.
Этот препарат уменьшает повреждающее действие клеток глутамата нерва. Первый рецепт этих препаратов должен, если возможно, быть выписан неврологом, имеющим опыт лечения БАС. Другие препараты находятся на разных стадиях клинических испытаний и могут быть одобрены в ближайшие несколько лет.
Кроме того, существует ряд методов лечения, ориентированных на симптомы, которые могут облегчить признаки бокового амиотрофического склероза и улучшить качество жизни пострадавших. На переднем плане стоит физиотерапевтическое лечение. Основное внимание уделяется поддержанию и активации функционирующих мышц, терапии сокращения мышц и связанных с этим ограничений подвижности суставов.
Основная цель терапии при БАС состоит в том, чтобы смягчить осложнения и последствия заболевания как часть доступных вариантов с помощью соответствующих концепций лечения и как можно дольше сохранять самостоятельность в повседневной жизни пострадавших людей.
Методы и цели терапевтического лечения основаны на результатах и индивидуальной ситуации пациента. Также обратите внимание на текущую стадию заболевания. В основе терапии лежат индивидуальные возможности пострадавшего человека.

Течение заболевания при БАС очень отличается с точки зрения тяжести, продолжительности и симптомов, и представляет особую проблему для больных и терапевтов.
Курс может варьироваться от быстрого прогрессирования с помощью респираторной помощи в течение нескольких месяцев до медленного прогрессирования в течение нескольких лет. В зависимости от того, какие двигательные нервные клетки повреждены, могут присутствовать компоненты спастического движения, но это также может быть проявления вялого паралича.
Все эти симптомы могут различаться в разных частях тела. Иногда случается, что пациент все еще может ходить, но мышцы плеча и предплечья демонстрируют почти полный паралич (синдром чужой руки).
Другие формы характеризуются восходящим параличом мускулатуры, начиная с нижних конечностей до туловища, верхних конечностей, шеи и головы. С другой стороны, бульбарная форма БАС начинается с нарушения глотания и речи. Сенсорные и вегетативные функции обычно остаются в вертикальном и неповрежденном состоянии.
Сложность и многоуровневый характер индивидуального течения заболевания требует широкого спектра специальных знаний, а также тщательного изучения механизмов БАС.
Поскольку последующие ограничения вряд ли могут быть специально предусмотрены, всегда требуется постоянная критическая оценка содержания выбранной терапии. Использование различных терапевтических методов для работы мышц, облегчения боли, расслабления, стимулирования дыхания и соответствующего вспомогательного обеспечения может дать пациенту возможность сделать свою повседневную жизнь как можно более длительной.
В дополнение к физиотерапии, она также включает в себя логопедическую терапию.Течение заболевания требует тщательного медицинского и терапевтического наблюдения для адекватного противодействия возникающим проблемам. Таким образом, интенсивное междисциплинарное сотрудничество терапевтов оправдывает себя.
Логопедическая терапия необходима
Пациенты, страдающие БАС, могут сталкиваться с повседневными и специфическими для заболевания чрезвычайными ситуациями.
Практически все чрезвычайные ситуации влияют на дыхательную систему пациентов. Уже существующая слабость мышц вдоха и выдоха, а также мышц горла и гортани (бульбарной мускулатуры) резко и значительно усиливается за счет дополнительного ухудшения дыхательного фактора.
Примером этого является инфекция нижних дыхательных путей, которая приводит к приступам удушья, бронхиальной обструкции и необходимости искусственной вентиляции посредством секреторной инфильтрации при наличии ранее существовавшей слабости кашля.
Даже такие операции, как в области живота, могут привести к острой дыхательной недостаточности и возобновлению искусственного дыхания после окончания анестезии.
Терапия в чрезвычайных ситуациях, связана с дыхательной системой, предлагают различные варианты лечения: введение кислорода может уменьшить респираторный дистресс, при пневмонии антибиотики и общие физиотерапевтические меры для ослабления секреции и удаления секреции.
Особенно при ослабленном кашле может потребоваться высасывание патологического секрета из дыхательных путей — просто через катетер или посредством бронхоскопии. Часто бывает необходим прием лекарств от респираторных расстройств и симптомов тревоги. Опиаты (например, Морфин) и транквилизаторы (например, Тавор®) подходят для этого. Несмотря на все эти меры, искусственное дыхание иногда неизбежно.
Искусственное дыхание — комплекс мер, направленных на поддержание оборота воздуха через легкие у человека, переставшего дышать.
Неинвазивная вентиляция с помощью лицевой маски является хорошей альтернативой инвазивной вентиляции, поскольку естественные дыхательные пути пациента остаются нетронутыми. Тем не менее, это может быть невозможно, особенно при параличе мышц глотки. Интубация с последующим искусственным дыханием часто проводится без разрешения пациента и редко по явному желанию пациента.
В результате основного заболевания, попытки постоянно вынимать вентиляционную трубу обычно заканчиваются неудачей, что приводит к возобновлению искусственной вентиляции и последующей трахеотомии.
Если поражены дыхательные мышцы, такая чрезвычайная ситуация может произойти непредсказуемо внезапно. Часто нет предупреждающих симптомов, которые указывают на медленное ухудшение респираторной ситуации.
Для врачей важно обсудить возможное возникновение таких чрезвычайных ситуаций с пациентом и его родственниками в ходе обследования во время постановки диагноза и совместно определить процедуру, например, на основе желания больного: врачи уточнят следует ли проводить вентиляционную терапию в дополнение к медицинскому лечению.
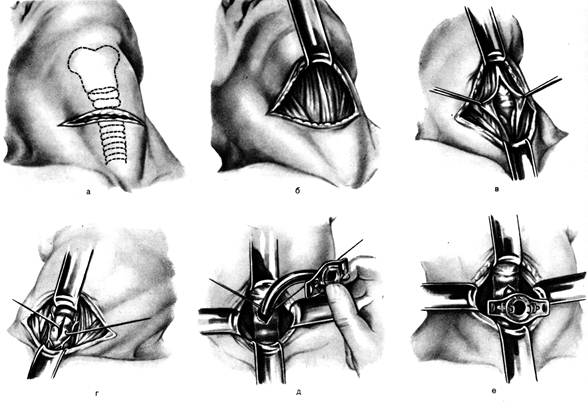
Однако трахеостомия также представляет собой возможный вариант при симптоматическом лечении БАС. Блокировка канюли в трахее может значительно снизить частоту и тяжесть переноса материала из желудочно-кишечного тракта (так называемая аспирация).
Если вентиляция необходима из-за слабости дыхательного насоса, устраняется проблема утечек и точек давления, например, на переносице, которая возникает с различной частотой при проведении неинвазивной вентиляции маской и может являться причиной ограниченной эффективности неинвазивной вентиляции.
Возможными показаниями для трахеотомии — с последующей вентиляцией или без нее — являются, соответственно, повторные тяжелые аспирации, часто в сочетании с ослабленным кашлем, или отказ неинвазивной вентиляции в случае явной слабости дыхательного насоса. В обеих ситуациях трахеотомия является плановой процедурой, для которой преимущества и недостатки должны быть подробно обсуждены заранее с пациентом и его родственниками.
Очевидными преимуществами являются уменьшение аспирации и обычно беспроблемная инвазивная вентиляция через трахеостомическую трубку — по имеющимся данным это часто приводит к продлению жизни. Это компенсируется недостатками, такими как необходимость интенсивного контроля во время инвазивной вентиляции, частой аспирации и значительного увеличения усилия по уходу.
Как правило, требования по уходу за больными с боковым амиотрофическим склерозом не могут быть выполнены только родственниками, поэтому необходимо проконсультироваться с медсестрами, имеющей опыт работы в области респираторной помощи.
Основываясь на опыте более 200 пациентов с БАС, нуждающиеся в официальной терапии, сознательно выбрали трахеостомию лишь
Читайте также:


