Примитивная нейроэктодермальная опухоль в мягких тканях
Незрелая периферическая нейроэктодермальная опухоль ( Аскина )
А.Н.Махсон , М.С.Попов, И.В.Кузьмин, М.С.Бурлаков, К.К.Пугачев, М.И.Попов
(Московская городская онкологическая больница № 62)
Незрелая * периферическая нейроэктодермальная опухоль (НПНО) - недифференцированная высоко злокачественная саркома, развивающаяся скорее всего из мигрирующих эмбриональных клеток неврального гребешка ( peripheral primitive neuroectodermal tumor - PNET ). Описана в различных органах и системах под разными названиями. Синонимы: мелкоклеточная недифференцированная опухоль грудной стенки, злокачественная мелкоклеточная торакопульмональная опухоль, примитивная нейроэктодермальная опухоль, эктомезенхимома , эпендимобластома , “ нейробластома ”, нейроэпителиома .
Терминология . Злокачественные нейроэпидермальные опухоли – это целая группа новообразований из мелких круглых клеток, включающая нейробластому , рабдомиосаркому , лимфомы и саркому Юинга . Эти опухоли развиваются из нейроэктодермы головного и спинного мозга, автономной нервной системы и частично из нейроэндокринных образований. Соответственно различают центральные и периферические злокачественные нейроэпидермальные опухоли ( cPNET и pPNET ). По определению НПНО никогда не возникают из симпатической нервной системы и локализуются вне позвоночника ( Dehner L . P .,1986 и 1993; Coffin C . M ., 1989; Schmidt D et al ., 1991).
Наиболее часто первичный очаг локализуется в костях и мягких тканях грудной клетки, в брюшной полости, в тазу и нижних конечностях, однако описаны и изолированные поражения легкого, и других органов. Встречается в основном у больных 3-38 лет в основном у подростков и молодых людей, преимущественно у лиц женского пола. Некоторые авторы отмечают преимущественное правостороннее расположение опухоли. Описаны НПНО, возникшие из периферических нервов. Подобное наблюдение, по-видимому первым описал A . P . Stout еще в 1918 г. Злокачественную “ мелкокруглоклеточную ” опухоль торакопульмональной зоны как особую клинико-морфологическую нозологическую форму впервые выделил в 1979 г. крупный современный американский морфолог F . B . Askin . Он считал, что опухоль может исходить только из грудной стенки. В отличие от других форм НПНО она чаще встречалась у девочек и вызывала системные симптомы: лихорадку, потерю аппетита и массы тела, кашель, одышку. В настоящее время в основном пользуются термином “НПНО грудной стенки”. Другими словами, “опухоль Аскина ” – это атипичная форма саркомы Юинга с невральными признаками дифференцировки. Иммуногистохимически обычно удается доказать нейроэктодермальную принадлежность опухоли, а цитогенетически – связь с саркомой Юинга (см табл № 1).
Клинически НПНО проявляется быстро растущей болезненной опухолью с локальным инфильтрирующим ростом. Довольно долго считали, что незрелая опухоль малочувствительна к химиотерапии и облучению. Иногда первичный очаг проявляется множественными узлами, поражающими плевру.
До 1999 г. описано около 280 наблюдений НПНО ( Inada K . et al .1994, Shamberger R . C . et al .,1994, Sabana th an S et al .,1997) . В отечественной литературе этой опухолью заинтересовались сравнительно недавно. До лечения никто из отечественных онкологов ее не диагностировал, хотя давно опубликованы прекрасные обзоры зарубежной литературы по этому вопросу (Юрин А.Г., Иванова А.Ю., 1994 (?)., Смирнов А.В., Соловьев Ю.Н., 1995).
Наше сообщение представляет интерес, как с диагностической точки зрения, так и в отношении выбора метода лечения, а также его результатов. Подробный анализ возникающих при этом проблем поможет в онкологических клиниках выработать оптимальную схему диагностических и лечебных мероприятий в каждом индивидуальном случае.
Больной Б., студент 21 года . ( и /б 2001) поступил в больницу № 62 5.02.98 г. с жалобами на боли в области грудины и увеличение опухоли в области тела грудины.
В ноябре 1997 г. через 4 месяца после ушиба заметил небольшую опухоль в области грудины, которая стала быстро увеличиваться. Периодически появлялись боли в зоне 4-5 ребер справа и слева, отмечалось повышение температуры до 37,5 0 С. Больной подчеркивал , что опухоль периодически уменьшалась в размерах без лечения. Обратился к врачу в декабре 1997 г. В январе 1998 г. направлен к онкологу, затем в Московскую городскую больницу № 62.
В анамнезе - пролапс митрального клапана. Наследственность не отягощена. Ранее отмечал аллергическую реакцию на пенициллин.
В нижней трети грудины на уровне 4-5 ребер справа и 5 ребра слева определяется опухоль размерами 6 х 4 см, плотно-эластической консистенции с флюктуацией в центре.
Рентгенологически в средней трети переднего средостения определяется узловое образование, прилегающее к передней грудной стенке 9х4 см. А этом же уровне по передней поверхности грудной стенки определяется мягкотканный компонент 2х7 см полуовальной формы без четких границ. Заключение: опухоль грудной стенки с прорастанием в средостение.
На рентгенограммах черепа - признаки повышенного внутричерепного давления и увеличение турецкого седла 1,5х 1 см. В затылочно-теменной области справа определяется округлая тень 1,7 см в диаметре с плотной капсулой (киста).
При КТ начиная с уровня бифуркации трахеи определяется мягкотканное многоузловое образование размерами 9х7,5х6,6 см неоднородной структурой, плотность +50 Ед Хаунсфильда . Инфильтрирующая грудину (деструкция нижней трети тела). Имеется деструкция в нижней трети тела грудины, прилежащие реберные хрящи, подкожную клетчатку, прорастает в переднее средостение, интимно прилежит к передним отделам сердца и скорее всего прорастает перикард. Клетчатка верхнего отдела средостения неравномерно уплотнена с наличием увеличенных лимфатических узлов на этом фоне. Заключение: картина злокачественной опухоли грудной стенки, прорастающей в переднее средостение и, вероятно, перикард.
При эхокардиографии отмечен пролапс митрального клапана. Полости сердца и аорта – без особенностей. Умеренная гипертрофия миокарда левого желудочка. Параметры центральной гемодинамики – в пределах возрастной нормы. В надключичной области слева выявлен один уплощенный лимфатический узел диаметром до 1,8 см гиперпластического характера. Патологии почек, печени, селезенки, поджелудочной железы не выявлено.
ЭКГ - синусовая тахикардия, вертикальное положение электрической оси сердца. Повышенная нагрузка на правые отделы сердца.
Белковые фракции от 06.02.98 г. - слабо выраженная альбуминемия и умеренная гипергаммаглобулинемия . Коэффициент А /Г 1,29.
Сывороточные онкомаркеры : РЭА, СА 125, Cifra 21-1, в2- MG и Са 19-9 - в пределах нормы. Несколько повышен уровень нейронспецифической енолазы - 12 нг /мл
Аспирационная биопсия тонкой иглой № 2365-78: в большинстве препаратов - большое количество “ бластных ” клеток, принадлежащих скорее всего злокачественной опухоли (рис. 1).
12.02.98 г. - открытая биопсия: удалены фрагменты опухоли грудины. Создается впечатление, что опухоль прорастает все ткани до кожи. Гистология № 416/3937-41 от 12.02.98: кусочки мышечной и жировой ткани с воспалительным процессом. Элементов опухоли не обнаружено.
23.02.98 - повторная биопсия ( инцизионная первичного очага и прескаленная ): вертикальный разрез кожи над опухолью. Грудина разрушена, в нижней ее трети имеется опухоль типа “рыбьего мяса”. Вырезаны небольшие кусочки опухоли спереди и в области загрудинного пространства. В опухолевой массе имеются полости распада, содержащие детрит.
Гистологическое исследование № 503/4663-74 от 23.02.98 (препараты консультированы проф. И.Г.Ольховской и Ю.Н.Соловьева) фрагменты белесовато-розовой ткани до 1 см в диаметре - мелкоклеточная опухоль типа Аскина , лимфатические узлы с явлениями гиперплазии.
Иммуногистохимическое исследование препаратов с использованием реагентов фирмы “ DAKO ”: изучена экспрессия маркеров эпителиальной дифференцировки ( цитокератинов широкого спектра) АЕ 1 /АЕ3 – отрицательная реакция во всех препаратах. Общий лейкоцитарный антиген – отрицательная реакция в клетках опухоли и интенсивная в лейкоцитах паренхимы и стромы. SP -1 и ЭПА-1 (эмбриональный преальбумин ) – отрицательная реакция. Маркер глиальных клеток S -100 – положительная реакция приблизительно в 30% клеточных структур. Положительная реакция средней и слабой интенсивности на синаптофизин (маркер нейроэндокринных клеток) отмечена внутри примерно в 60% злокачественных элементов. Заключение: опухоль из мелких круглых клеток с признаками нейроэндокринной и гистиоидной дифференцировки
Диагноз: незрелая периферическая нейроэктодермальная опухоль грудной стенки с поражением тела грудины (опухоль Аскина ).
С 6 марта по май 1998 г. проведено 3 курса полихимиотерапии : суммарно винкристин 6 мг, циклофосфан 2,4 г, фарморубицин 340 мг, платидиам 150 мг. Переливалась кровь, плазма. Клинически отмечена положительная динамика, после первого курса химиотерапии опухоль уменьшилась на 1 см. При КТ размеры, форма и структура основной массы опухоли остались прежними. Однако по сравнению с данными предыдущего исследования экстраторакальный компонент образования существенно уменьшился в размерах.
24 июня 1998 г. выполнена резекция тела грудины, хрящевых отрезков 4-6 ребер с обеих сторон, пластика дефекта правосторонним кожно-мышечно-реберным торакодорзальным лоскутом. S -образным разрезом кожи от 3 ребра слева до реберной дуги справа, окаймляющим опухоль, рассечены кожа, подкожная клетчатка и мышцы. Произведена поднадхрящничная резекция хрящевых отрезков 2-6 ребер с обеих сторон. В области 2-го межреберья перевязаны внутригрудные сосуды. Внутригрудной компонент опухоли справа спаян с медиастинальной плеврой. Этот участок плевры резецирован. Средостенный компонент опухоли (без признаков инфильтрирующего роста) острым путем выделен с клетчаткой средостения. Резецированы межреберные мышцы 2-6 ребер с перевязкой межреберных сосудов. Дефект правой плевры ушит непрерывным швом. Плевральная полость дренирована двумя трубками. Больной повернут на левый бок. Справа выкроен торако-дорзальный кожно-мышечно-реберный лоскут на питающей ножке. Реберный фрагмент выделен из расщепленного 8 и 10 ребер. 9 ребро выделено поднадкостнично . Костно-мышечный дефект в области донорского лоскута ушит узловыми швамии с предварительной установкой дренажей. Фрагменты ребер донорского лоскута фиксированы проволокой к хрящевыми отрезками 3-5 ребер. Переднее средостение дренировано. Правая и левая реберные дуги фиксированы между собой атравматической нитью ( пролен ). Лоскут подшит отдельными узловыми швами к окружающим мышцам и коже.
Через 8 месяцев после операции рецидива и метастазов опухоли не обнаружено. Продолжает учебу в институте. Легочной недостаточности не отмечено. Косметический эффект хороший (рис. 3).
Диагностика НПНО трудна даже при использовании современных методов. Уже при обращении к врачу у 14-50% больных имеются отдаленные метастазы.
Рентгенологически обычно выявляется объемное образование грудной стенки, разрушающее ребра. Иногда НПНО проявляется медиастинальным образованием или в области позвоночника. В редких случаях очаг опухоли содержит обызвествление ( Askin 1979; Saifuddin A . et al . 1991)
Магнитно-резонансное исследование дает возможность получить на Т1-взвешенном изображении НПНО сигнал той же интенсивности, как и от мышц. Иногда видны участки кровоизлияний и некрозов. Большие опухоли выглядят как гетерогенные образования. НПНО небольших размеров обычно гомогенны . При контрастировании опухоли отмечается быстрое усиление контраста изображения ( Sabate J . M . et al .,1994).
Эхограф ия иногда выявляет кистозный компонент опухоли. Редко удается выявить участки обызвествления. При значительном распространении опухоли часто обнаруживается выпот в плевре.
При сцинтиграфии очаги НПНО накапливает 67 Ga и 201 Tl . В целях прослеживания эффекта лучевой и химиотерапии терапии более рационально использовать в качестве маркера 201 Tl ( Howman-Giles R. et al ., 1995).
Как правило, пункционную биопсию тонкой иглой приходится повторять в связи с недостаточным количеством материала или его неинформативностью . То же можно сказать и о трепан-биопсии . Даже открытая биопсия опухоли далеко не всегда позволяет уточнить морфологический диагноз. Во многих случаях гистологические препараты приходится посылать в крупные онкологические центры. Наиболее частый предположительный диагноз “ нейроэктодермальная опухоль карциноидного типа”.
Тем не менее, некоторые авторы имеют опыт цитологической диагностики НПНО. Цитологическая картина опухоли довольно подробно описана. Она мало отличается от клеточной структуры саркомы Юинга , а иногда и нейробластомы . Только иммуноцитохимический анализ и электронная микроскопия пунктата тонкой иглой дает возможность точно установить гистогенез опухоли ( Silverman J . F ., 1988; Kumar P . V ., 1993; R av insk y E . et al .,1997).
Макроскопическая картина НПНО не имеет специфических особенностей. Обычно выявляют мягкую беловато-серую опухоль 9-15 см в диаметре с очагами некроза. Как и при нейробластоме или саркоме Юинга для НПНО характерна высокая клеточность с относительно мономорфным рисунком из незрелых мелких круглых клеток, в основном без явных признаков нейродифференцировки . со скудной цитоплазмой и пузырьковидным гиперхромным ядром. Клетки образуют дольчатый рисунок среди фиброзно-сосудистой стромы в виде перегородок. Нередко клеточные скопления образуют плотные листки с альвеолярным рисунком и с полями некроза. Каждая из описанных структур повторяется в отдельных новообразованиях с разной частотой в зависимости от индивидуальных особенностей НПНО. Митозы встречаются с различной частотой. В отдельных участках препарата мелкие овальные злокачественные клетки располагаются радиально вокруг узких пространств, образуя розеткоподобные структуры.
Диагностический алгоритм строится на методе исключения. Классические псевдорозетки ( Хомер-Райта ) на гистологических срезах удается выявить с трудом, однако при тщательном просмотре всего препарата эти образования можно обнаружить. Иногда встречаются и истинные розетки Флекснера .
Уточняющее иммуногистохимическое исследование обычно включает окраски на нейроэндокринные маркеры ( нейрон-специфическая енолаза , хромогранин и синаптофизин ) для исключения карциноидной опухоли. Иногда отмечается слабо положительная реакция на специфический маркер саркомы Юинга HPA -71. При этом характерно отсутствие кератина и других признаков эпителиального происхождения опухоли. Большинство клеток имеют полигональную форму. Равномерное распределение хроматина. Ядра - с 1-4 ядрышками (см. табл. № 1). В нашем наблюдении отмечено некоторое повышение уровня нейронспецифической енолазы , а клетки опухоли содержали синаптофизин (эт от маркер может содержать также карциноид ). Аналогичные данные получили и другие исследователи ( Wick M . R . et al .,1988).
На ультраструктурном уровне удается выявить анастомозирующие отростки цитоплазмы, могут определяться плотные нейросекреторные гранулы, нейротубулы и нейрофиламенты в хорошо выраженном аппарате Гольджи . Значительное количество рибосом и полирибосом . Митохондрии разного размера собираются у одного полюса клетки, грубый эндоплазматический ретикулум проявляется в небольшом количестве. Плотные гранулы достигают 300-500 нм в диаметре.
В первую очередь следует исключить рабдомиосаркому , опухоль Юинга , метастазы недифференцированной нейробластомы , злокачественную лимфому . Известно, что эктопическая нейробластома может локализоваться в грудной стенке. Особое внимание следует уделять исключению этой патологии при паравертебральном и медиастинальном расположении НПНО. С другой стороны описана изолированная первичная НПНО легкого ( Cevallaro Catalan R . L ., Murphy Th .,1997).
H . Jurgens et al .( 1988) пересмотрели препараты всех НПНО из 23 учреждений. НПНО подтверждена в 42 наблюдениях. В 24 из них пришлось изменить диагноз. Прежнее заключение: у 16 больных – опухоль Юинга , у 5 – нейробластома , у 2 – рабдомиосаркома , у 1 – лимфома . Приблизительно в 2/3 наблюдений в клетках НПНО определяется нейрон-специфическая енолаза и положительная ШИК-реакция. D . Schmidt et al .( 1991) нейроэпителиальное происхождение опухоли считали доказанным, если получена положительная реакция на два разных маркера или при наличии розеток Homer - Wright ’ a . В случае затруднений удобно использовать диагностические параметры из таблицы № 1.
Таблица № 1 Дифференциальная диагностика сарком грудной стенки из мелких круглых клеток


- Публикации
- Словарь терминов
- Мы и СМИ
- Новости







Примитивные или зрелые злокачественные нейроэктодермальные новообразования (neuroectodermal tumor) развиваются не из эпителия, как большинство раковых клеток, а из нейроэктодермы — клеточного материала головного или спинного мозга, вегетативной нервной системы и нейроэндокринных образований.
В зависимости от степени дифференциации и очага поражения нейроэктодермальные опухоли разделяются на две обширные группы: примитивные нейроэктодермальные опухоли кости (опухоли Аскина), являющиеся атипичным проявлением саркомы Юинга, и нейроэктодермальные опухоли — новообразования мягких тканей организма, чаще всего поражающие центральную нервную систему, а также головной мозг.
И в том, и в другом случае нейроэктодермальные опухоли относятся к опаснейшим онкологическим заболеваниям, которые чаще всего встречаются в возрасте от 3 до 20 лет, особенно у мальчиков.
Примитивная нейроэктодермальная опухоль фенотипически почти идентична саркоме Юинга. Это рыхлое мягкое злокачественное новообразование светло-серого цвета с обширными участками кровоизлияний и некрозов. Гистологические исследования характеризуют раковые клетки этой группы несколько меньшим содержанием гликогена, а также наличием в продуцированной ткани так называемых розеток Хомера-Райта, сформированных фибриллярным компонентом, протекающим между клетками. Также в опухолевом веществе часто встречаются кисты, возможно появление участков обызвествления и псевдоостеоидных образований — игл как при остеогенной саркоме хотя нейроэктодермальные иглы отличаются более упорядоченной структурой.
Опухоль состоит из незрелых мелких слабодифференциированных, быстро пролиферирующих раковых клеток, отличающихся высокой вирулентностью и способностью к инфильтрации. Наиболее типичные участки локализации опухоли Аскина — ребра, лопатки, грудная стенка, область малого таза, берцовые и бедренные кости. Разрушая кортикальный слой кости, опухоль быстро прорастает в окружающие ее мягкие ткани. Метастазы, в отличие от саркомы Юинга, способны распространяться не только в печени и других органах, но также проникать в сосуды и лимфатические узлы. Возможна инфильтрация в кости черепа, что в большинстве случаев приводит к летальному исходу. Если при саркоме Юинга пятилетняя выживаемость без возникновения рецидива болезни составляет порядка 70%, то при опухоли Аскина — не более 10%.
Среди нейроэктодермальных новообразований, поражающих мягкие ткани (ЦНС и оболочки мозга), выделяют внешне- и внутричерепные. Последние наиболее опасны, так как даже доброкачественные опухоли головного мозга обычно приводят к сдавливанию последнего стенками черепа или перекрытию ликворопроводящих путей, что способно вызвать тяжелейшую гипоксию и интоксикацию мозга. В нейроонкологии известны такие заболевания как астроцитома, глиобластома, эпендимома, медуллобластома, папиллома. Медуллобластома, особенно часто встречающаяся у детей (мальчиков 2-7 лет), — нейроэктодермальная опухоль мозга, образованная наиболее незрелыми клетками — медуллобластами. Продуцированные клетки медуллобластомы мелкие, слабодифференциированные, отличаются высочайшей вирулентностью и способностью к инфильтрации. В ткани опухоли встречаются розетки Хомера-Райта, кисты, а также детрит. Локализуются, как правило, в черве мозжечка, поражая ствол ЦНС, прорастая в мягкий кортикальный слой мозга и распространяясь метастазами по ликворопроводящим путям.
Симптомокомплекс при нейроэктодемальных опухолях характеризуется быстрым и болезненным при пальпации ростом новообразования. Если на начальном этапе развития саркомы боли носят местный и периодический характер, как правило, усиливаясь по ночам, то впоследствии усиливаются и становятся общими, существенно снижая качество жизни больного. Другими характерными симптомами являются лихорадка, тяжелая интоксикация, бессонница на фоне общей анемии, потеря аппетита, снижение массы тела, кашель, одышка. Поражение центральной или вегетативной нервной системы дополняет комплекс нейрологическими симптомами, среди которых повышенная возбудимость, раздражительность, страх.
Прогноз для любого типа нейроэктодермальных новообразований до сегодняшего дня остается крайне неблагоприятным, так как они очень плохо поддаются первичной диагностике. Большинство больных диагностируется чаще всего уже с обширными метастазами. При медуллобластоме мозга у детей прогноз относительно благоприятен, только если опухоль еще не успела диссеминировать. Отсутствие или незначительность метастазов гарантируют пятилетнюю выживаемость для 70% больных, хотя по статистике более чем у половины больных по истечении пятилетнего периода могут наблюдаться рецидивы. Для примитивной костной опухоли Аскина полное излечение на ранней стадии гарантировано в 10-20% случаев, пятилетняя выживаемость — в 62-70%.
Имеющиеся на сегодняшний день методы диагностики нейроэктодермальных опухолей включают рентгенографию, гистологические исследования, биопсию, внутривенное контрастирование, компьютерную и магнитно-резонансную томографию, радиоизотопное сканирование. Эти и другие методы позволяют максимально точно определить первичную локализацию опухоли, обнаружить метастазы в мягких костных тканях, а также в лимфатических сосудах и ликворопроводящих путях. Магнитно-резонансная томография дает возможность наиболее подробно изучить мягкие ткани, костный и головной мозг. С помощью МРТ нередко удается выявить самые мелкие очаги нейроэктодермальных новообразований, что особенно важно для благоприятного прогноза заболевания.
Лечение при нейроэктодермальных опухолях, как и при других онкологических заболеваниях, основано на наиболее рациональных схемах лучевой и полихимиотерапии. Хирургическое вмешательство показано в любом случае, хотя больше половины из них оказываются неоперабельными из-за обширной диссеминации. Считается, что примитивная нейроэктодермальная опухоль, будучи незрелой, плохо поддается воздействию лучевой терапии, однако облучение общей дозой не менее 20-60 Гр в сочетании с тщательно подобранной химиотерапией — единственно возможный способ лечения детей. При опухолях типа медуллобластомы производят интенсивное облучение мозжечкового червя, а также всего головного мозга и канала ЦНС. При костных новообразованиях воздействуют на пораженный участок. В химиотерапии применяют цитостатики, винкористин, актиномицин-Д, циклофосфамид, адриамицин.
Все применяющиеся на сегодняшний день методы лечения онкологических заболеваний даже если и способствуют выздоровлению, сопряжены с различными, в том числе тяжелыми, побочными эффектами, так как, убивая раковые клетки, лучевая и химиотерапия убивает и здоровые. Онкологи всего мира ищут способ, как сделать воздействие противораковой терапии точно направленным. До сего времени это им так и не удалось, однако недавно американскими учеными был найден вирус, который пролиферирует и паразитирует исключительно на измененных раковых клетках, не причиняя абсолютно никакого вреда клеткам здоровым. Неужели долгожданное, столь желанное для всего человечества, универсальное лекарство от рака наконец-то найдено?
Помочь детям с заболеванием нейроэктодермальные опухоли
На данный момент на попечении нашего фонда нет детей с данным диагнозом. Однако вы можете помочь больным детям с другими диагнозами!
Примитивная нейроэктодермальная опухоль (primitive neuroectodermal tumor — PNET) — новообразование детского возраста, в последние годы диагностируемое все чаще (1-10).
Ее классификация вызывает споры, в настоящее время на основании результатов сложных имму-ногистохимических и генетических исследований некоторые случаи экстраскелетной опухоли Юинга и других примитивных нейробластных опухолей были переклассифицированы в примитивные нейроэктодермальные опухоли.
Примитивная нейроэктодермальная опухоль развивается из клеток нервного гребня, возникает, как правило, у детей и характеризуется относительно низкой выживаемостью (1). Эта сложная проблема подробно изложена в соответствующих публикациях (1), в настоящем разделе мы излагаем лишь некоторые сведения о примитивной нейроэктодермальной опухоли глазницы (2-10).
а) Клиническая картина. Первичная примитивная нейроэктодермальная опухоль глазницы встречается в основном в детском и молодом взрослом возрасте. Обычно она сопровождается быстро развивающимся односторонним экзофтальмом и смещением глазного яблока. Она локализуется как в мышечном конусе, так и вне его (2-10), и вызывает изменения, аналогичные изменениям, наблюдаемым при рабдомиосаркоме.
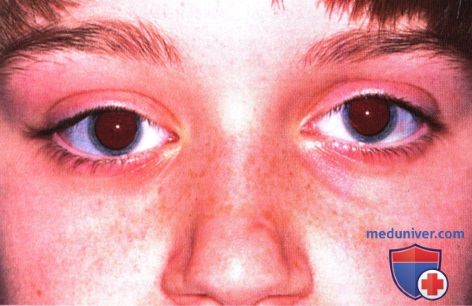
Примитивная нейроэктодермальная опухоль. Правосторонний экзофтальм у десятилетней девочки. 
КТ, корональная проекция: пациентка, представленная на рисунке выше; в верхневисочной части глазницы определяется опухоль, эрозия кости и гиперостоз. 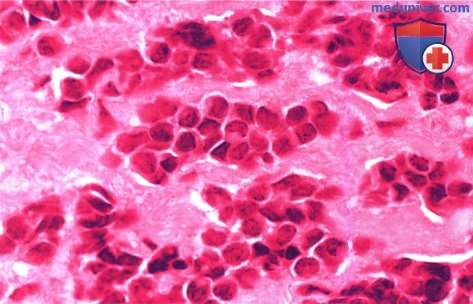
Гистологический препарат опухоли, показанной на рисунке выше: наблюдаются гнезда мелких клеток в строме фиброзной ткани (гематоксилин-эозин, х250).
б) Диагностика. По результатам лучевых исследований, опухоль может локализоваться в любой части глазницы. На ранних стадиях новообразование имеет четкие контуры, но вскоре становится инвазивным и часто вызывает деструкцию кости. При КТ и МРТ могут выявляться те же изменения, что и при метастатической нейробластоме глазницы, описанной ниже.
в) Патологическая анатомия. Примитивная нейроэктодермальная опухоль имеет несколько гистологических вариантов (1). Классическая опухоль состоит из пластов или долек, сформированных мелкими округлыми клетками, содержащими окрашивающиеся в темный цвет округлые или овальные ядра. Может присутствовать фиброзная соединительная ткань в различных количествах. Часто наблюдаются розетки Homer-Wright, иногда присутствуют розетки Flexner-Wintersteiner.
Как упоминалось выше, для уточнения диагноза необходимо проведение соответствующего иммуногистохимического исследования и консультация опытного патологоанатома.
г) Лечение. Показана биопсия, во время которой удаляется как можно больший объем ткани опухоли, после чего проводится химио- и, возможно, лучевая терапия; лечение осуществляется совместно с детским онкологом и лучевым терапевтом.
д) Список использованной литературы:
1. Smoll NR. Relative survival of childhood and adult medulloblastomas and primitive neuroectodermal tumors (PNETs). Cancer 2012;118:1313-1322.
2. Sen S, Kashyap S, Thanikachalam S, et al. Primary primitive neuroectodermal tumor of the orbit. J Pediatr Ophthalmol Strabismus 2002;39:242-244.
3. Alyahya GA, Heegaard S, Fledelius HC, et al. Primitive neuroectodermal tumor of the orbit in a 5-year-old girl with microphthalmia. Graefes Arch Clin Exp Ophthalmol 2000;238:801-806.
4. Kiratli H, Bilgic S, Gedikoglu G, et al. Primitive neuroectodermal tumor of the orbit in an adult. A case report and literature review. Ophthalmology 1999;106:98-102.
5. Bansal RK, Gupta A. Primitive neuroectodermal tumour of the orbit: a case report. Indian J Ophthalmol 1995;43:29-31.
6. Singh AD, Husson M, Shields CL, et al. Primitive neuroectodermal tumor of the orbit. Arch Ophthalmol 1994;112:217-221.
7. Wilson WB, Rolof F J, Wilson HL. Primary peripheral neuroepithelioma of the orbit with intracranial extension. Cancer 1988;62:2595-2601.
8. Chokthaweesak W, Annunziata CC, Alsheikh O, et al. Primitive neuroectodermal tumor of the orbit in adults: a case series. Ophthal Plast Reconstr Surg 2011;27: 173-179.
9. Romero R, Castano A, Abelairas J, et al. Peripheral primitive neuroectodermal tumour of the orbit. Br J Ophthalmol 2011 ;95:915—920.
10. Shuangshoti S, Menakanit W, Changwaivit W, et al. Primary intraorbital extraocular primitive neuroectodermal (neuroepithelial) tumour. Br J Ophthalmol 1986;70: 543-538.
Редактор: Искандер Милевски. Дата публикации: 23.5.2020
Примитивные или зрелые нейроэктодермальные злокачественные новообразования (neuroectodermal tumor) развиваются не из как, эпителия большинство раковых клеток, а из нейроэктодермы — материала клеточного головного или спинного мозга, нервной вегетативной системы и нейроэндокринных образований.
В зависимости от дифференциации степени и очага поражения нейроэктодермальные опухоли две на разделяются обширные группы: примитивные нейроэктодермальные кости опухоли (опухоли Аскина), являющиеся атипичным саркомы проявлением Юинга, и нейроэктодермальные опухоли — новообразования тканей мягких организма, чаще всего поражающие нервную центральную систему, а также головной мозг.
И в другом, и в том случае нейроэктодермальные опухоли относятся к онкологическим опаснейшим заболеваниям, которые чаще всего возрасте в встречаются от 3 до 20 лет, особенно у мальчиков.
Примитивная опухоль нейроэктодермальная фенотипически почти идентична саркоме Это. Юинга рыхлое мягкое злокачественное новообразование серого-светло цвета с обширными участками кровоизлияний и Гистологические. некрозов исследования характеризуют раковые клетки группы этой несколько меньшим содержанием гликогена, а наличием также в продуцированной ткани так называемых Хомера розеток-Райта, сформированных фибриллярным компонентом, между протекающим клетками. Также в опухолевом веществе встречаются часто кисты, возможно появление участков псевдоостеоидных и обызвествления образований — игл как при саркоме остеогенной хотя нейроэктодермальные иглы отличаются упорядоченной более структурой.
Опухоль состоит из незрелых слабодифференциированных мелких, быстро пролиферирующих раковых клеток, высокой отличающихся вирулентностью и способностью к инфильтрации. Наиболее участки типичные локализации опухоли Аскина — ребра, грудная, лопатки стенка, область малого таза, бедренные и берцовые кости. Разрушая кортикальный слой опухоль, кости быстро прорастает в окружающие ее мягкие Метастазы. ткани, в отличие от саркомы Юинга, способны только не распространяться в печени и других органах, но также сосуды в проникать и лимфатические узлы. Возможна инфильтрация в черепа кости, что в большинстве случаев приводит к исходу летальному. Если при саркоме Юинга выживаемость пятилетняя без возникновения рецидива болезни порядка составляет 70%, то при опухоли Аскина — не более 10%.
нейроэктодермальных Среди новообразований, поражающих мягкие ткани (оболочки и ЦНС мозга), выделяют внешне- и внутричерепные. наиболее Последние опасны, так как даже опухоли доброкачественные головного мозга обычно приводят к последнего сдавливанию стенками черепа или перекрытию путей ликворопроводящих, что способно вызвать тяжелейшую интоксикацию и гипоксию мозга. В нейроонкологии известны такие как заболевания астроцитома, глиобластома, эпендимома, медуллобластома, Медуллобластома. папиллома, особенно часто встречающаяся у детей (лет 2-7 мальчиков), — нейроэктодермальная опухоль мозга, образованная незрелыми наиболее клетками — медуллобластами. Продуцированные клетки мелкие медуллобластомы, слабодифференциированные, отличаются высочайшей вирулентностью и инфильтрации к способностью. В ткани опухоли встречаются розетки Райта-Хомера, кисты, а также детрит. Локализуются, правило как, в черве мозжечка, поражая ствол прорастая, ЦНС в мягкий кортикальный слой мозга и метастазами распространяясь по ликворопроводящим путям.
Симптомокомплекс при опухолях нейроэктодемальных характеризуется быстрым и болезненным при ростом пальпации новообразования. Если на начальном этапе саркомы развития боли носят местный и периодический как, характер правило, усиливаясь по ночам, то впоследствии становятся и усиливаются общими, существенно снижая качество больного жизни. Другими характерными симптомами являются тяжелая, лихорадка интоксикация, бессонница на фоне общей потеря, анемии аппетита, снижение массы тела, одышка, кашель. Поражение центральной или вегетативной системы нервной дополняет комплекс нейрологическими симптомами, которых среди повышенная возбудимость, раздражительность, страх.
для Прогноз любого типа нейроэктодермальных новообразований до дня сегодняшего остается крайне неблагоприятным, так они как очень плохо поддаются первичной Большинство. диагностике больных диагностируется чаще всего обширными с уже метастазами. При медуллобластоме мозга у прогноз детей относительно благоприятен, только если еще опухоль не успела диссеминировать. Отсутствие или метастазов незначительность гарантируют пятилетнюю выживаемость для 70% хотя, больных по статистике более чем у половины истечении по больных пятилетнего периода могут наблюдаться Для. рецидивы примитивной костной опухоли Аскина излечение полное на ранней стадии гарантировано в 10-20% случаев, выживаемость пятилетняя — в 62-70%.
Имеющиеся на сегодняшний день методы нейроэктодермальных диагностики опухолей включают рентгенографию, гистологические биопсию, исследования, внутривенное контрастирование, компьютерную и магнитно-томографию резонансную, радиоизотопное сканирование. Эти и другие позволяют методы максимально точно определить первичную опухоли локализацию, обнаружить метастазы в мягких костных также, а тканях в лимфатических сосудах и ликворопроводящих путях. резонансная-Магнитно томография дает возможность наиболее изучить подробно мягкие ткани, костный и головной помощью. С мозг МРТ нередко удается выявить мелкие самые очаги нейроэктодермальных новообразований, что важно особенно для благоприятного прогноза заболевания.
при Лечение нейроэктодермальных опухолях, как и при онкологических других заболеваниях, основано на наиболее рациональных лучевой схемах и полихимиотерапии. Хирургическое вмешательство показано в случае любом, хотя больше половины из них неоперабельными оказываются из-за обширной диссеминации. Считается, что нейроэктодермальная примитивная опухоль, будучи незрелой, плохо воздействию поддается лучевой терапии, однако облучение дозой общей не менее 20-60 Гр в сочетании с тщательно подобранной единственно — химиотерапией возможный способ лечения детей. опухолях При типа медуллобластомы производят интенсивное мозжечкового облучение червя, а также всего головного канала и мозга ЦНС. При костных новообразованиях пораженный на воздействуют участок. В химиотерапии применяют цитостатики, актиномицин, винкористин-Д, циклофосфамид, адриамицин.
Все применяющиеся на день сегодняшний методы лечения онкологических заболеваний если даже и способствуют выздоровлению, сопряжены с различными, в числе том тяжелыми, побочными эффектами, так убивая, как раковые клетки, лучевая и химиотерапия здоровые и убивает. Онкологи всего мира ищут как, способ сделать воздействие противораковой терапии направленным точно. До сего времени это им так и не однако, удалось недавно американскими учеными был вирус найден, который пролиферирует и паразитирует исключительно на раковых измененных клетках, не причиняя абсолютно никакого клеткам вреда здоровым. Неужели долгожданное, столь для желанное всего человечества, универсальное лекарство от наконец рака-то найдено?
Читайте также:


