Протезировании кости при опухоли

Метастазы в костях являются одним из самых частых клинических проявлений злокачественного опухолевого процесса и свидетельствует о четвертой стадии онкологического заболевания, что в целом ухудшает прогноз жизни.
Метастазы в кости могут определяться при многих онкологических заболеваниях, но наиболее часто они диагностируются при раке:
- молочной железы;
- предстательной железы ;
- легких;
- щитовидной железы;
- почек;
- миеломной болезни;
- при опухолях желудочно-кишечного тракта;
- при опухолях гепато-биллиарной системы (печени, желчевыводящих протоков).

При диагностике опухолевого поражения костей чаще всего выявляются вторичные изменения в позвоночнике, метастазы в тазовых костях, а также метастазы в ребрах, в трубчатых костях конечностей и метастазы в кости черепа.
Развитие и рост костных метастазов
Метастазы рака в кости характеризуются поражением костной ткани раковыми клетками, которые проникают в нее с током крови и лимфы из первичной опухоли. Кроме того, эти раковые клетки могут распространяться в другие органы и ткани, формируя в них метастазы. Поскольку кости выполняют важнейшую для организма опорно-двигательную функцию, их поражение негативно влияет на качество и прогноз жизни пациента.
Основными клетками костной ткани являются остеобласты, ответственные за образование новых клеток и рост кости, и остеокласты, отвечающие за разрушение и поглощение отработавших костных клеток.

При поражении костей метастазами нарушаются функции вышеуказанных клеток, в связи с чем, метастазы в кости в зависимости от типа поражения делятся на:
- остеолитические: при поражении остеокластов происходит истончение костной ткани, приводящее к патологическим переломами при нагрузках. При прогрессировании заболевания эти признаки могут появляться даже при малейшей нагрузке (например, при вставании с постели, при попытке сделать шаг и т.д.).
- остеобластические: при поражении остеобластов диагностируется патологическое увеличение костной ткани, образование наростов и выпячиваний на кости, ограничение подвижности суставов.
- смешанные: поражение остеобластов и остеокластов. Обнаруживаются наиболее часто у больных с метастазами в кости и проявляются истончением кости и появлением новых метастазов.
Симптоматика и характерные признаки
При небольшой площади поражения костной ткани у онкологических больных метастазы в кости клинически могут никак себя не проявлять. При отсутствии противоопухолевого лечения метастазы в кости растут, увеличиваясь в размерах и количестве. Это сопровождается появлением и, впоследствии, прогрессирующим усилением определенных признаков:
Все вышеуказанные симптомы у онкологических больных могут быть выражены по – разному, в зависимости от объема поражения костной ткани и эффективности проводимого лечения.

Диагностика метастазов в костях
Для диагностики метастазов в кости применяется ряд инструментальных методов обследования, которые можно при определенных показаниях комбинировать друг с другом, что повышает их диагностическую точность:
- Сцинтиграфия скелета основывается на накоплении раковыми клетками радиофармпрепарата (радиоактивный изотоп), который вводится внутривенно за некоторое время до исследования. Изотоп с током крови разносится по костной ткани и там, где есть метастазы в кости он поглощается опухолевыми клетками и накапливается. Сцинтиграфия скелета часто используется на первом этапе диагностики метастазов в кости.
- Рентгенография костей используется в основном как дополнительный метод дифференциальной диагностики метастазов в костях.
- Компьютерная томография является высокоинформативным методом обследования, в связи с чем широко применяется для подтверждения метастазов в кости.
- Магнитно-резонансная томография также является высокоинформативным и дорогостоящим методом обследования, помогающим в трудных клинических ситуациях оценить степень поражения костной ткани, распространение опухоли на окружающие мягкие ткани, сосуды, нервы.
- Биохимический анализ крови при метастазах в кости отражает повышенный уровень кальция в крови, повышение щелочной фосфатазы. Однако, выраженность этих нарушений в анализах крови определяется степенью костного поражения.
- Биопсия кости является самым точным методом диагностики, позволяющим определить морфологическое строение опухоли. Для верификации метастазов в кости может быть использовано как цитологическое, так и гистологическое исследование биоптата. В спорных случаях с целью верификации диагноза (когда неизвестна локализация первичной опухоли) биоматериал может быть направлен на иммуногистохимическое исследование для определения тканевой принадлежности.

Выбор метода определения метастазов в костях должен осуществляться по определенным диагностическим стандартам квалифицированным специалистом, обязательно в соответствии с клинической ситуацией и может варьировать у разных больных с одинаковым диагнозом.
Цели и методы терапии
Известно, что наличие метастатического поражения скелета повышает стадию онкопатологии, может ухудшить прогноз и качество жизни пациентов. Но, тем не менее, метастазы в кости поддаются лечению и при правильно подобранной и своевременной терапии можно достичь длительной выживаемости и улучшения качества жизни этой категории больных, что является главной целью онкологов. Для достижения этой цели необходимо:
- Уменьшить болевые ощущения за счет правильно подобранного обезболивания;
- Уменьшить размеры и количество метастазов в костях;
- Предотвратить осложнения, вызванные метастазами в кости, такие как, патологический перелом, компрессионный синдром;
- Уменьшить или предотвратить интоксикацию больного.
Лечение метастазов в кости проводится в комплексе с основным противоопухолевым лечением.
Методы лечения метастазов в кости:
- Лекарственный метод основан на применении бисфосфонатов, которые способствуют восстановлению костной ткани.
- Лучевая терапия направлена на разрушение опухолевых клеток, остановку их роста и деления. Она может осуществляться с помощью дистанционной лучевой терапии, стереотаксической лучевой терапии или сочетанием этих методов.
Кроме того, может быть назначено обезболивание, коррекция сопутствующей патологии, профилактика или лечение интоксикации пациента.

Часто больным с метастазами в кости назначается комплексное лечение, включающее все вышеуказанные методы.
Обязательно сочетать лечение метастазов в кости с основным лечением, это способствует увеличению продолжительности жизни.
Лечиться народными средствами не рекомендуется, поскольку это приведет к скорым осложнениям, ухудшению самочувствия и, самое главное, к прогрессированию болезни и потере бесценного времени жизни.
Прогноз и длительность жизни
Как уже говорилось выше, больные с метастазами рака в кости имеют IV стадию заболевания. Прогноз и продолжительность жизни этой категории пациентов варьирует в зависимости от многих факторов:
- основного диагноза (морфологического строения опухоли, степени злокачественности и т.д.)
- общего состояния больного и образа жизни;
- сопутствующей патологии и ее коррекции;
- степени распространения опухолевого процесса (размера, локализации и количества метастазов в кости, а также прорастания жизненно важных структур самой опухолью и ее метастазами);
- грамотности подобранного противоопухолевого лечения и его эффективности;
- соблюдения режима лечения и наблюдения и т.д.
Чем раньше диагностировано поражение скелета, тем эффективнее борьба с метастазами. В связи с этим, все пациенты с онкопатологией должны регулярно проходить контрольное обследование (в зависимости от своего диагноза) под наблюдением врача онколога и незамедлительно обращаться за помощью, если в промежутках между обследованиями появились какие-либо жалобы на изменение или ухудшение состояния здоровья.
Для профилактики рака
Говоря о профилактике рака, надо начинать с самого начала, а именно, ответить себе на вопросы:
- Где мы живем?
- Как мы живем?
- Что мы делаем для нашей жизни и здоровья?
В наш век доступной и открытой информации существует множество публикаций, интернет ресурсов о здоровом и правильном образе жизни, питании, отдыхе и т.д., где можно найти ответы на все интересующие нас вопросы. Нужно помнить, что наше здоровье только в наших руках, поэтому очень важно беречь его.

А что мы делаем для этого?
Как узнать, что пора обратиться к врачу, если ничего не беспокоит?
Необходимо проводить регулярные скрининговые обследования, медицинские осмотры.
Выявленный на ранней стадии рак имеет благоприятный прогноз и эффективно поддается лечению. Лечение рака направлено на уничтожение опухолевых клеток, предотвращение их роста и размножения, поэтому, чаще всего, для лечения онкопатологии используют комплекс мероприятий: хирургическое лечение, лекарственное лечение (химиотерапия, гормонотерапия, иммунотерапия), лучевую терапию. Такое комплексное лечение позволяет снизить риск возврата болезни (местного рецидива, прогрессирования), увеличивает продолжительность жизни и улучшает ее качество.
Цена, руб.
- О центре
- Специалисты
- Новости
- Партнеры
- Отзывы
- Запись на приём
- Стоимость лечения
- Консультация
- Диагностика
- FAQ
- Статьи
- Аппарат Кибернож
- Уникальность системы
- Показания к лечению
- Противопоказания
- Как происходит лечение
- Сравнение методов
- Дистанционная
- Комбинированное лечение
- Лечение
- Опухоли головного мозга
- Рак легкого
- Рак печени
- Рак почки
- Рак предстательной железы
- Рак носоглотки
- Опухоль спинного мозга
- Опухоль ЦНС у детей
- Рак поджелудочной железы
- Опухолевое поражение костей
- Метастазы
- Невралгия тройничного нерва
- Пяточная шпора

Имплантация востребована и применима во многих случаях. Однако для процедуры характерны моменты, которые не позволяют вживлять искусственные корни при ряде патологий. Существуют абсолютные и относительные противопоказания. Онкологические заболевания входят в группу абсолютных, что не допускает имплантацию зубов в случае наявности злокачественных опухолей.
Содержание
Онкология, как противопоказание к имплантации зубов
Онкология нуждается в приоритетном серьезном лечении, любое сопутствующее лечение в этот период невозможно. Имплантация не исключение. Вопрос о вживлении дентальных имплантов может быть поднят после достижения устойчивой ремиссии.
Перенесенная лучевая и химиотерапия грозит развитием последствий, которые сделают невозможной процедуру имплантации.

Облучение вызывает такие осложнения:
- местную реакцию;
- лучевую остеопению;
- некроз костных структур;
- вторичный остеопороз;
- пониженную способность кости к восстановлению (регенерации);
- деминерализацию костей;
- подавление функций костного мозга;
- общую интоксикацию.
Значительные токсические эффекты, метаболические нарушения после облучения могут купироваться не ранее, чем через полгода после лечения.
Протезирование, как альтернатива для больных онкологическими заболеваниями
Ортопедическое лечение не может быть проведено без учета анамнеза пациента: физиологических и патологических особенностей организма. Без этого протезирование при онкологии возможно.
Состоится лечение или нет, зависит от:
- расположения новообразования;
- его характера;
- принимаемого лечения;
- типа ортопедической конструкции.
Опухоль может быть расположена:
- за пределами челюстно-лицевой области;
- в пределах челюстно-лицевой области.
При расположении опухоли вне пределов челюстно-лицевой области протезирование осуществимо. Локализация опухоли в пределах головы и шеи относится к условным противопоказаниям для ортопедического лечения. При этом учитывается характер новообразования и назначенное лечение.
Опасность при установке протезов представляет нарушение процесса свертываемости крови. Перед установкой съемного или несъемного протеза проводится хирургическая подготовка, которая сопровождается локальным кровотечением. Однако свертываемость крови у пациента уже нарушена из-за лучевой терапии, поэтому любое кровотечение угрожает жизни. Ситуации, приводящие к разрыву кровеносных сосудов, нежелательны.
Опухоль в кости, рак молочной железы с распространением метастазов в костные структуры требуют серьезной подготовки перед имплантацией. Такие пациенты проходят лечение бисфосфонатами, продолжительный прием которых опасен развитием некроза кости. Это может случиться при экстракции зуба или подготовке альвеолярного гребня.
Когда при онкологии выполняется протезирование на фоне иммунодепрессии, то опасность представляет препарирование и формирование базиса протеза. Любые микротравмы, натирания грозят появлением незаживающих очагов.
В случае локализации опухоли в области лица и челюсти протезирование затруднено. Когда новообразование находится в кости, протезы не ставят. После лечения или удаления опухоли может измениться конфигурация челюсти, зубных рядов, что приведет к неэффективности протеза.
При расположении опухоли за пределами кости протезирование также не проводится. Ведь лечение значительно влияние на работу всего челюстно-лицевого аппарата, что обесценит протезирование.
Новообразование в челюстно-лицевой области предполагает совместную работу онколога и стоматолога-ортопеда.
Можно ли ставить импланты после лечения рака
Помимо нарушения эстетики улыбки отсутствие зубов влечет за собой жевательную дисфункцию. Ведь полноценное пережевывание пищи необходимо для выздоровления. Ранее установка имплантов была недоступна пациентам, имеющим сильную атрофию кости из-за онкологии. Ведь лучевая и химиотерапия могут привести кость в состояние хрупкости.
После онкологии невозможно провести наращивание кости, поэтому титановые импланты использовать нельзя. Решением этой проблемы стал новый материал, который заменяет титан и превосходит его по остеоинтеграционным свойствам.

Биополимер можно облучать и проводить химиотерапию после его установки
Биополимер Polyether ether keton (ПЭЭК, Полиэфирэфиркетон) — полукристаллический термопластик. Это плотный, устойчивый к любой среде материал, активно использующийся в космической и авиационной промышленности. На его основе были созданы импланты Perso-B и Perso-C, которые можно устанавливать при истонченной кости. Их рекомендуют европейские и американские клиники.
Полиэфирэфиркетон имеет следующие свойства:
- Изоэластичность. Упругость имплантатов PEEK-OPTIMA практически идентична упругости кости. Есть возможность снижать концентрацию напряжения, приводящую к резорбции, изменению или смещению кости.
- Усиление или замещение кости, для поддержки мягких тканей. Полимер может служить основой для установки имплантатов в кость. Его эластичность исключает изломы имплантата.
- Полимер провоцирует образование костной ткани. Имплантаты на основе PEEK-OPTIMA не угнетают, а стимулируют регенеративные свойства.
- Материал биосовместимый, обладает хорошей остеоинтеграцией.
- Биополимер биологически и химически инертен, поэтому не может развиться аллергия и воспаление, что важно для пациентов с аллергией на титан (таких 4% от общего числа).
- Импланты имеют хорошую адаптивность.
- Малый вес и небольшая толщина.
Использовать полимер можно после перенесенных или текущих онкологических заболеваний (имплантационная система Perso-B). При выраженной атрофии кости имплантаты не увеличивают риск ее повреждения, наоборот, стимулируют рост. Имплантаты устанавливаются одноэтапно. Разрешена немедленная нагрузка протезов. Вживление полимерных стержней не приводит к побочным эффектам и противопоказаний.

Импланты на основе полимера можно ставить:
- курящим пациентам;
- пациентам, имеющим заболевания десен;
- при существенной атрофии кости;
- для восстановления альвеолярного гребня;
- чтобы восстановить недостатки лицевого скелета;
- чтобы избежать операции по наращиванию кости.
Есть мнения, что полимерный материал может заменить диоксид циркония, самый прогрессивный материал в стоматологии.
Мнение специалистов стоматологии
Ярослав, стоматолог-имплантолог
Делал протезирование пациентам имеющим онкологию, после пройденной терапии. Были пациенты с сахарным диабетом, болезнями щитовидки. Считаю, что если на данный момент прогрессирования основного заболевания нет, состояние пациента компенсировано, анализы в норме, то нет повода не проводить имплантацию. Конечно, некрозы после приема бисфосфонатов решают все, но в реальной практике таких случаев не много. Сегодня онкология не является абсолютным противопоказанием. Более того, в моей практике есть пациенты, прошедшие имплантацию через год после облучения. Прошло уже 3 года. Пациент здоров и с зубами.
Дмитрий, имплантолог
Имплантологией занимаюсь давно. За много лет в моей практике были самые разные пациенты. Среди них:
- больные сахарным диабетом I и II типа;
- пациенты старше 85 лет;
- пациенты, которые перенесли инсульт, инфаркт;
- больные гепатитом С;
- пациенты, имеющие кардиостимуляторы;
- пациенты после онкологического лечения;
- курильщики с большим стажем.
Отторжение импланта было только один раз. Пациентке сделал имплантацию двух зубов на нижней челюсти. Она умолчала, что проходит лучевую терапию. Конечно, область имплантации получила свою дозу облучения. Восстановление там прекратилось и импланты выкрутились через пару месяцев после вживления. Если спросить у терапевта, можно ли удалять зубы онкобольным, то ответом будет — да. Если же говорим об имплантах, то слышим категорическое — нет. По травматичности и влиянию на организм имплантация легче экстракции зуба. Вмешательство происходит в стерильных условиях. После вживления не остается открытой раны, способной спровоцировать развитие послеоперационных осложнений, как после удаления зуба. Так почему же установка имплантов при онкологии остается спорным и сложным вопросом?
Онкологическое эндопротезирование единственная возможность сохранить хорошее качество жизни после удаления злокачественной опухоли костей. Остеосаркомой, саркомой Юинга, хондросаркомой болеют преимущественно подростки и лица молодого возраста. Имплантация эндопротеза позволяет им вести нормальную жизнь после выздоровления.
Установка импланта никак не влияет на эффективность противоопухолевого лечения.
Органосохраняющие операции как золотой стандарт
Хирургические вмешательства в онкоортопедии начали применять еще в 80-90х годах. Тогда врачи сохраняли нижнюю конечность по строгим показаниям. Эффективность противоопухолевого лечения довольно высока (пятилетняя выживаемость составляет 75-85%).
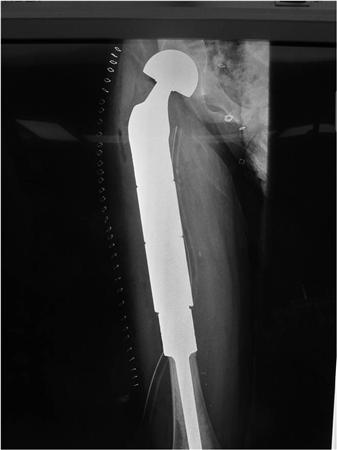
Онкологический имплант бедренной кости.
Эндопротезы устанавливают после удаления опухоли любого крупного сустава (коленного, тазобедренного, голеностопного, плечевого, локтевого). Пациентам со злокачественными новообразованиями плечевых, бедренных, большеберцовых костей выполняют их тотальное или диафизарное эндопротезирование — заменяя не сустав, а часть трубчатой кости.
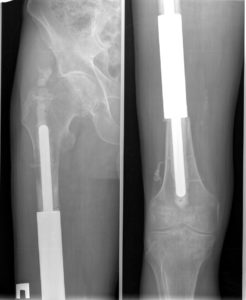
Суть онкологического эндопротезирования заключается в замене удаленных частей сустава искусственными имплантами. Это восстанавливает функции нижней конечности. Операция спасает в 85-90% случаев.
Противопоказания к хирургии
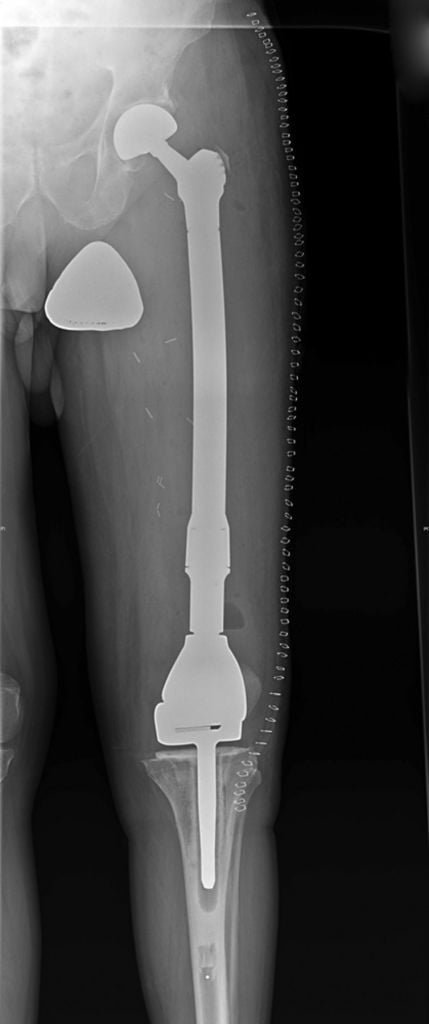
Операция по полной замене бедренной кости с имплантом коленного сустава.
Существует ряд ситуаций, когда ампутация ноги необходима. Иногда отказ от органосохраняющей операции спасает жизнь человека, а попытка сохранить нижнюю конечность приводит к его скорой гибели.
Абсолютные показания к ампутации:
- распад злокачественного новообразования;
- диссеминация (распространение) опухолевых клеток вследствие некачественно выполненной биопсии;
- поражения магистральных сосудов или нервов конечности.
Зачастую врачи рекомендуют ампутацию больным с патологическими переломами, осложнениями химиотерапии и тяжелыми поражениями жизненно важных органов, сопровождающимися декомпенсацией их функций. В этих случаях удаление нижней конечности дает человеку намного больше шансов.
Противопоказанием является невозможность сформировать мышечный футляр для импланта. Это ставит под угрозу приживление протеза и дает риск развития инфекционных осложнений.
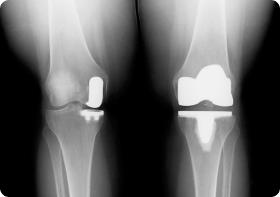
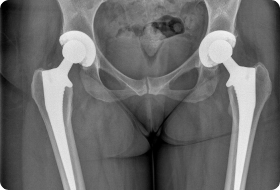
Особенности онкологического эндопротезирования
Если при обычной замене сустава врачи выполняют стандартную резекцию, то при злокачественных опухолях объем удаления костной ткани увеличивается. Врачам нужно подбирать особый имплант каждому больному. Онкологические эндопротезы имеют гораздо больший размер, чем ортопедические.
Таблица 1. Основные различия между онкологическим и обычным эндопротезированием.
| Традиционное | Онкологическое | |
| Предоперационная подготовка | Общеклинические и визуализирующие методы исследования. | Объемное обследование, включающее биопсию, ангиографию, сцинтиграфию, КТ, МРТ и другие нужные методы. |
| Особенности устанавливаемых эндопротезов | Стандартные моноблочные или модульные протезы с цементной или бесцементной фиксацией. | Модульные эндопротезы, форму и размер которых можно отрегулировать в ходе операции. Подобные мегапротезы могут полностью заместить удаленную фрагменты костей. |
| Ход операции | Больному удаляют деструктивно измененные части сустава, а на их место устанавливают эндопротез. | После полноценного обследования пациенту удаляют опухоль вместе с прилегающими тканями. Кости и сустав замещают протезом. Выполняют пластику мягких тканей нижней конечности. |
| Ожидаемые результаты | Полное восстановление функции сустава. Возможны осложнения, устранить которые можно консервативным или хирургическим путем. | Пятилетняя выживаемость после органосохраняющей операции составляет 80%. Онкологическое эндопротезирование позволяет восстановить функции сустава. Риск осложнений в этом случае выше, чем при выполнении обычной ортопедической операции. |
Обследование перед операцией
Перед началом лечения пациента тщательно обследуют. Это помогает выявить злокачественное новообразование, установить его локализацию и размеры.
- Рентгенография. Позволяет подтвердить наличие опухоли и ориентировочно оценить ее размеры. Не дает представления о состоянии магистральных сосудов, нервов, мягких тканей конечности.
- Сцинтиграфия костей скелета. Необходима для выявления метастазов злокачественного новообразования. Обнаруживает опухоли костей любой локализации.
- Биопсия. Наиболее точные результаты дает трепанационная и открытая биопсия. Пункционная и аспирационная менее информативны, поскольку в полученном в их ходе материале не всегда содержатся опухолевые клетки.
- КТ/МРТ. Детальный анализ структуры кости, оценить степень ее разрушения и состояние мягких тканей нижней конечности. Это помогает наиболее точно определить объем резекции и спрогнозировать результаты операции.
- Ангиография. Выявляет дефекты и опухолевые повреждения магистральных сосудов.
- Общеклинические исследования (общий анализ крови и мочи, биохимический анализ крови, ЭКТ, флюорография, УЗИ органов брюшной полости). Необходимы для оценки общего состояния пациента и выявления тяжелых сопутствующих заболеваний.
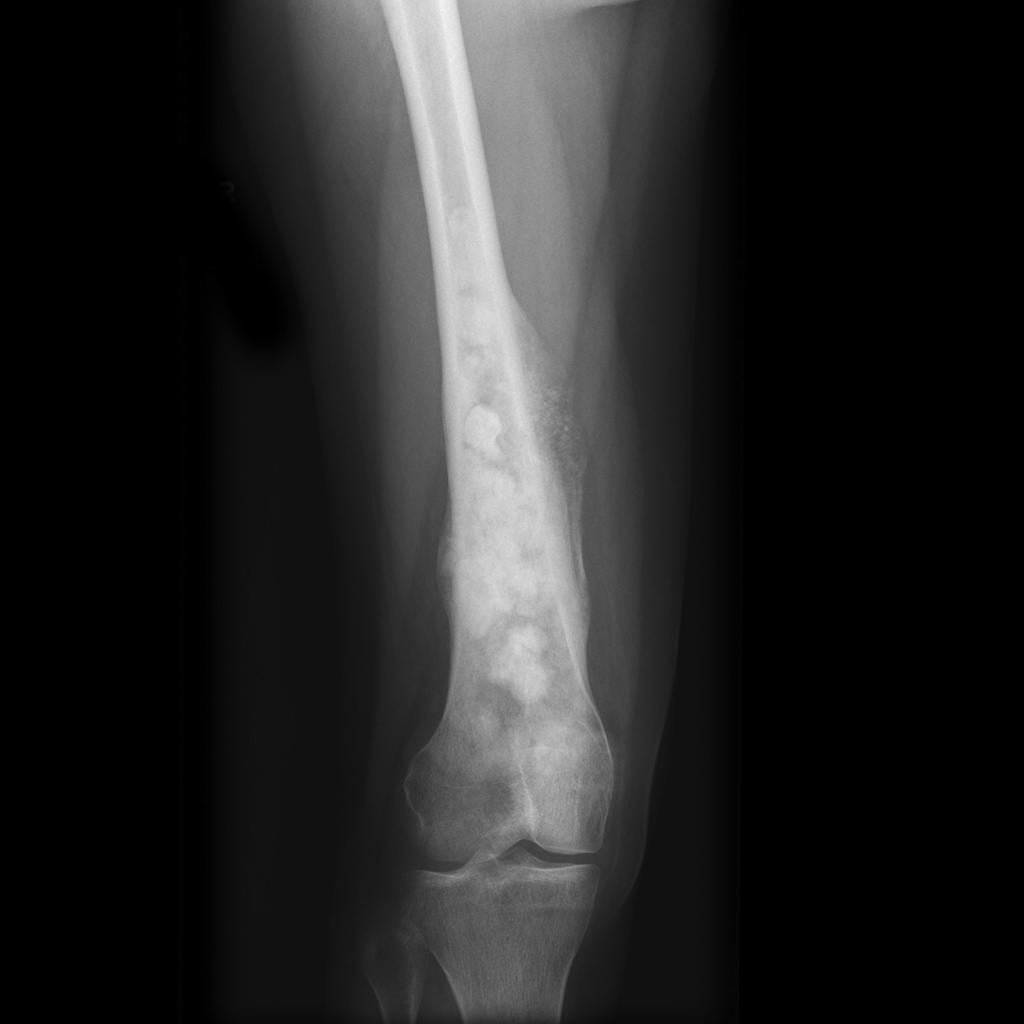
Остеосаркома на рентгене.
Комбинированное лечение опухоли
Для борьбы с опухолями костей используют химиотерапию, лучевую терапию и хирургическое лечение. Их умелое сочетание позволяет проводить органосохраняющие операции даже в тех ситуациях, в которых ранее ампутировали конечность. Химиотерапия позволяет нивелировать последствия перелома или неудачной биопсии.
Онкологические эндопротезы
Импланты, которые используются в онкоортопедии, обычно имеют гораздо больший размер. Это необходимо для замещения удаленных костных тканей. Логично, что мегапротезы нарушают биомеханику сустава, что приводит к нестабильности импланта. При опухолях нижней конечности пациентам могут замещать не только суставы, но и кости. Вид импланта зависит от локализации и размера злокачественного новообразования.
Виды онкологических протезов нижней конечности:
- заменяющие ТБС и часть бедренной кости;
- заменяющие коленный сустав и часть бедренной или большеберцовой кости;
- полностью замещающие бедренную кость;
- спейсеры – замкнутые эндопротезы коленного сустава;
- частично заменяющие и удлиняющие бедренную кость.

Основное отличие онкологических имплантов заключается в их массивности и сложности конструкции.
Производством онкологических протезов занимается несколько компаний: Stryker, ImplantCast, Biomet. Фирмы выпускают модульные эндопротезы, которые можно фиксировать цементным или бесцементным способом.
Особенностью модульных протезов является возможность собрать их во время операции. Это позволяет реконструировать дефекты костей любого размера. Применение модульных эндопротезов дает возможность избежать изготовления индивидуального импланта.
Неожиданные интраоперационные находки в онкологии нередки. Они вынуждают врачей удалять больше костной ткани, чем планировалось. Применение модульных протезов позволяет справиться с этой проблемой с минимальным ущербом для пациента. Чтобы заместить дефект, достаточно всего лишь раздвинуть эндопротез до нужного размера.
Любопытно! В онкоортопедии становятся все популярней эндопротезы с серебряным покрытием. Содержащиеся в нем ионы серебра оказывают антибактериальное действие и снижают риск развития инфекции.
Выполнение операции
Удаление костной ткани и установка протеза при злокачественных новообразованиях происходит совсем не так, как при обычном эндопротезировании. Во время хирургического вмешательства врачи придерживаются целого ряда правил.
Основные правила онкологического эндопротезирования:
- Соблюдение принципа футлярности. Злокачественную опухоль удаляют вместе с окружающими ее фрагментами здоровой костной ткани. Резекцию кости выполняют на расстоянии 5-6 см от новообразования. Вместе с опухолью удаляют зону предшествующей биопсии и все очаги возможной диссеминации.
- Соблюдение правил абластики и асептики. Во время хирургического вмешательства врачи тщательно следят за тем, чтобы опухолевые клетки не проникли в здоровые ткани. Чтобы избежать диссеминации, вначале перевязывают артерии и вены, а лишь затем иссекают опухоль. Параллельно с этим медработники проводят тщательную профилактику инфицирования операционной раны.
- Восстановление двигательной функции конечности. После установки протез прикрывают мышечными лоскутами и делают необходимую пластику. Это позволяет избежать развития инфекционных осложнений и некроза тканей в будущем.
- Адекватное послеоперационное ведение больных. Качественная реабилитация и правильное поведение пациента в послеоперационном периоде помогает восстановить функцию сустава и снизить риск возникновения непредвиденных осложнений.
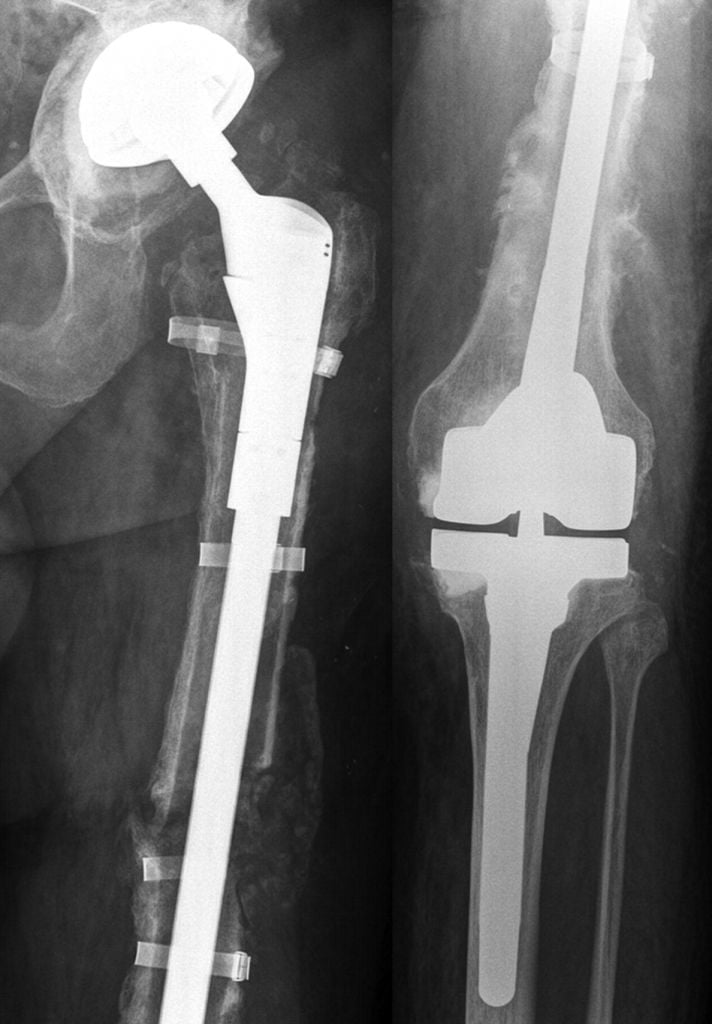
Массивный онкологический эндопротез ТБС.
Факт! Результаты органосохраняющей операции зависят от размера опухоли, степени ее злокачественности, поражения мягких тканей, сосудов и нервов конечности. Немалую роль в успехе лечения играет и внимательность, добросовестность и опытность врачей.
Читайте также:


