Респираторно-синцитиальная инфекция у детей клинические рекомендации

Возбудитель инфекции
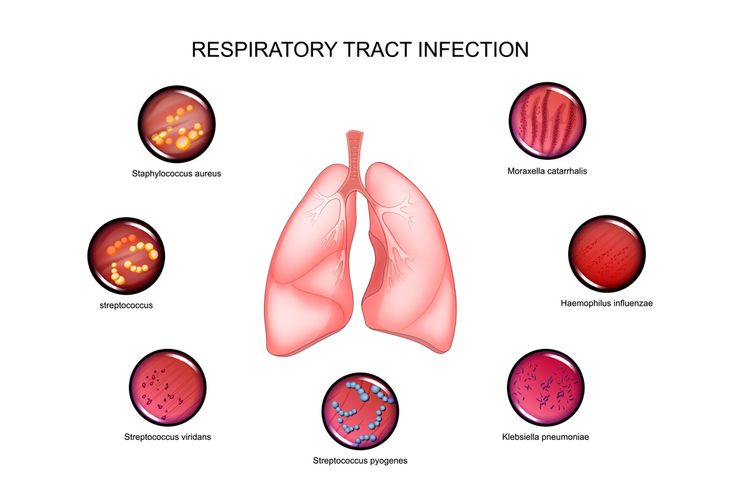
Респираторно-синцитиальная инфекция: причины и симптомы
Респираторно-синцитиальное поражение нижних дыхательных путей связано с одноименным РНК-вирусом. В окружающей среде возбудитель быстро погибает, так как не способен жить вне организма человека.
Передаются вирусные частицы воздушно-капельным путем. Источником заражения является больной человек или вирусоноситель, который не имеет симптомов болезни. Для респираторно-синцитиального поражения характерна динамика вспышек, которые возникают внутри семьи или организованных коллективов — в детском саду или педиатрических отделениях.
Респираторно-синцитиальная инфекция имеет благоприятный прогноз. Однако если у пациента имеется иммунодефицит или он получает неправильную терапию, поражение легких может быстро прогрессировать.
Вирусная инфекция редко приводит к заболеванию взрослых. Наибольшей чувствительностью к ней обладают дети в возрасте от 6 месяцев до 3 лет, а также недоношенные. По данным Всемирной организации здравоохранения, каждый второй ребенок перенес респираторно-синцитиальное поражение легких. Диагноз при этом ставится не всегда, так как требует проведения серологических или молекулярно-генетических методов анализа.
Клинические проявления
Симптомы инфекционного заболевания зависят от того, какой отдел дыхательной системы поражен вирусом. Педиатры выделяют 4 варианта течения инфекции: назофарингит, бронхит, бронхиолит и пневмония. Инкубационный период достигает 6-7 дней. Патология развивается постепенно. У ребенка появляются субфебрильная температура (до 38 градусов), легкий озноб, головная боль и насморк. Эти проявления соответствуют острому назофарингиту. При распространении вируса вглубь дыхательной системы появляется сухой кашель, плохо поддающийся лечению.
В отсутствии адекватной терапии или на фоне иммунодефицита прогрессирование респираторно-синцитиальной инфекции приводит к пневмонии. В этом случае появляются лихорадка с температурой до 39 градусов и выраженные симптомы интоксикации: головная боль, тошнота, беспокойство или апатия ребенка. Больные жалуются на боли в груди, которые усиливаются при кашле. Характерный признак — удушье, возникающее в виде отдельных приступов. Кашель становится влажным и сопровождается отхождением большого количества мокроты.
Детям требуется проводить комплексное лечение
У детей развивается дыхательная недостаточность. Она сопровождается тремя клиническими проявлениями: одышкой на выдохе, цианозом губ и акроцианозом. Возможно развитие обструктивного бронхита и бронхиолита. В этих случаях лечение требует госпитализации больного и проведения интенсивной терапии для устранения дыхательной недостаточности.
Продолжается заболевание 10-14 дней. Если отмечается пневмония, то полное выздоровление наступает через 2-3 недели. При респираторно-синцитиальном поражении возможны осложнения: бактериальная пневмония, гнойный отит, судорожные приступы и т.п. Тяжелое течение, сопровождающееся дыхательной недостаточностью, может стать причиной гибели ребенка.
Диагностика заболевания
Основной метод диагностики — изучение имеющихся жалоб, особенностей развития заболевания и внешний осмотр. Симптомы дыхательной недостаточности, развивающиеся медленно и сопровождающиеся интоксикацией, характерны для респираторно-синцитиального поражения. Помимо этого, детям проводят следующие исследования:
- рентгенологическое исследование органов грудной клетки. На рентгенограмме отмечаются затемнение полей легкого и усиление рисунка бронхиального дерева. При развитии пневмонии легочной рисунок в одной доле органа может полностью исчезать;
- спирография для оценки функции органов дыхания и установления типа дыхательной недостаточности;
- иммуноферментный анализ с определением уровня иммуноглобулинов. При повышении концентрации IgM в крови врачи говорят о подтверждении диагноза. Если же увеличен уровень IgG, то инфекция связана с другим микроорганизмом;
- серологические исследования: реакция нейтрализации, реакция связывания комплемента и др.
Дифференциальная диагностика проводится с другими заболеваниями, вызывающими схожую клиническую картину. К ним относят коклюш, бронхиальную астму и аллергический бронхит.
Подходы к лечению
Респираторно-синцитиальное поражение — вирусная инфекция
Детям при выявлении респираторно-синцитиального поражения легких требуется комплексная терапия. Госпитализация показана только при тяжелых формах заболевания. Дети грудного возраста госпитализируются при средней степени тяжести инфекции. Острая фаза болезни — показание для постельного режима и лечебной диеты.
Клинические рекомендации выделяют этиотропную, патогенетическую и симптоматическую терапию. Препаратов этиотропного лечения РСВ инфекции на сегодняшний день не существует.
Медикаменты назначает только врач. Препараты имеют показания и противопоказания к использованию. Если их не учитывать, то возможны прогрессирование инфекционного процесса и появление побочных эффектов от приема лекарств.
Симптоматические средства позволяют устранить клинические признаки болезни и улучшить самочувствие больного. Основными препаратами для данной группы являются жаропонижающие и сосудосуживающие капли для носа. Снижать температуру с помощью лекарств следует при ее повышении выше 38 градусов. Назальные капли используются при сильном насморке и заложенности носа.
Патогенетическая терапия включает в себя несколько групп медикаментов. Антигистаминные средства, уменьшающие отечность и тонус гладкой мускулатуры в бронхиальном дереве. Препараты, разжижающие мокроту, облегчают ее выведение из легких и уменьшают выраженность одышки. По возможности ребенку проводят небулайзерные ингаляции с щелочными растворами или бронхолитиками. Это позволяет улучшить отхождение мокроты и нормализовать дыхание.
При появлении первых проявлений болезни родителям необходимо обратиться к врачу. Своевременное назначение лечения улучшает прогноз на выздоровление и снижает риск развития осложнений.
Респираторно-синцитиальная инфекция имеет благоприятный прогноз. Комплексная терапия, включающая средства для этиотропного и патогенетического лечения, позволяет остановить прогрессирование патологии. Ребенок в этот период нуждается в постельном режиме и уходе со стороны родителей. В отсутствии терапии или при самолечении у детей развиваются бронхиолит и пневмония. Оба состояния способны привести к дыхательной недостаточности, угрожающей здоровью и жизни ребенка.
[youtube.player]Версия: Клинические рекомендации РФ (Россия)
Общая информация
СОЮЗ ПЕДИАТРОВ РОССИИ
КЛИНИЧЕСКИЕ РЕКОМЕНДАЦИИ ПО ИММУНОПРОФИЛАКТИКЕ РЕСПИРАТОРНО-СИНЦИТИАЛЬНОЙ ВИРУСНОЙ ИНФЕКЦИИ У ДЕТЕЙ (2016)
Главный внештатный детский специалист по профилактической медицине Минздрава России Акакдемик РАН Л.С. Намазова-Баранова
Этиология и патогенез
Эпидемиология
Факторы и группы риска
Клиническая картина
Лечение
Профилактика
Моноклональные антитела – это антитела, синтезируемые и секретируемые одним клоном антитело-образующих клеток. Все свойства моноклональных антител (класс иммуноглобулинов, структура полипентидных цепей и активных центров), то есть их антительная специфичность идентичны. Они распознают только один антиген и взаимодействуют только с ним. В связи с этим значительно повышается и специфичность всех иммунологических реакций, протекающих с участием моноклональных антител.
Применение паливизумаба позволяет снизить частоту госпитализаций по поводу РСВ инфекции, сократить их длительность, уменьшить продолжительность кислородотерапии, а также предотвратить необходимость перевода в отделение интенсивной терапии или сократить длительность пребывания в нем. Однако, на сегодняшний день, высокая стоимость курса терапии не позволяет охватить иммунизацией всех пациентов, для которых применение препарата принесло бы ощутимую пользу. На сегодняшний день сформулированы дифференцированные критерии для назначения данной терапии пациентам разных групп риска по развитию РСВ инфекции.
Назначение иммунопрофилактики показано в соответствии с сезонным пиком заболеваемости. По данным Российского эпидемиологического исследования, пик заболеваемости РСВ инфекцией в Российской Федерации приходится на период ноябрь–апрель.
• пациенты с БЛД до 12 мес жизни, нуждающиеся в постоянной медикаментозной терапии и/или дополнительной оксигенации в связи с тяжелым течением заболевания в последние 6 месяцев, не менее 3 инъекций в период сезона инфекции (1А);
• дети с ВПС после операции на сердце с использованием АИК или ЭКМО, которым проводилась иммунопрофилактика РСВ инфекции, требуют дополнительного введения Паливизумаба сразу после стабилизации состояния (следует помнить, что при использовании АИК/ЭКМО отмечается снижение концентрации препарата в плазме крови более чем на 50%) (2А).
Принятие решения о проведении пассивной иммунизации паливизумабом пациентам с перечисленными выше патологиями осуществляет консилиум специалистов на основании результатов оценки риска развития РС-вирусной инфекции тяжелого течения.
Введение паливизумаба может сопровождаться аллергическими реакциями немедленного типа, включая анафилактические, поэтому пациенты должны находиться под медицинским наблюдением не менее 30 мин, а помещение, в котором осуществляется введение, должно быть обеспечено средствами противошоковой терапии.
Информация
Авторы подтверждают отсутствие финансовой поддержки/конфликта интересов, который необходимо обнародовать.
Оценка значимости в соответствии с рейтинговой схемой (табл. 1).
| Степень достоверности рекомендаций | Соотношение риска и преимуществ | Методологическое качество имеющихся доказательств | Пояснения по применению рекомендаций | ||||
| Польза отчетливо превалирует над рисками и затратами, либо наоборот | Сильная рекомендация, которая может использоваться в большинстве случаев у преимущественного количества пациентов без каких-либо изменений и исключений | ||||||
| Польза отчетливо превалирует над рисками и затратами, либо наоборот | Доказательства, основанные на результатах РКИ, выполненных с некоторыми ограничениями (противоречивые результаты, методологические ошибки, косвенные или случайные и т.п.), либо других веских основаниях. Дальнейшие исследования (если они проводятся), вероятно, окажут влияние на нашу уверенность в оценке соотношения пользы и риска и могут изменить ее. | Сильная рекомендация, применение которой возможно в большинстве случаев | |||||
| Польза, вероятно, будет превалировать над возможными рисками и затратами, либо наоборот | Доказательства, основанные на обсервационных исследованиях, бессистемном клиническом опыте, результатах РКИ, выполненных с существенными недостатками. Любая оценка эффекта расценивается как неопределенная. | Относительно сильная рекомендация, которая может быть изменена при получении доказательств более высокого качества. | |||||
| Польза сопоставима с возможными рисками и затратами | Польза сопоставима с рисками и осложнениями, однако в этой оценке есть неопределенность | Неоднозначность в оценке соотношения пользы, рисков и осложнений; польза может быть сопоставима с возможными рисками и осложнениями. | Доказательства, основанные на обсервационных исследованиях, бессистемного клинического опыта или РКИ с существенными недостатками. Любая оценка эффекта расценивается как неопределенная. | Очень слабая рекомендация; альтернативные подходы могут быть использованы в равной степени. |
• Систематические обзоры с таблицами доказательств.
[youtube.player]Профессор С.Г. Чешик, Р.В. Вартанян
НИИ вирусологии имени Д.И. Ивановского РАМН, Москва
Респираторно-синцитиальная вирусная инфекция (РСВИ) занимает важное место в патологии органов дыхания, как у детей, так и у взрослых. Респираторно-синцитиальный вирус (РСВ) - наиболее частая причина поражения Нижних дыхательных путей (НДП) у детей раннего возраста, причем заболевание может привести к летальному исходу. У детей старшего возраста и взрослых РСВ вызывает более легкое поражение респираторного тракта, проявляющееся ринофарингитом, бронхитом, включая обострение хронического бронхита, пневмонией.
Этиология и эпидемиология
РСВ входит в состав семейства Paramyxoviridae, являясь представителем рода Pneumovirus. Свое название вирус получил в результате характерного цитопатического действия в культуре клеток, ведущего к образованию синцития и симпластов. РСВ не содержит гемагглютинина и нейраминидазы.
РСВИ является, по существу, эндемичной, и в отдельные периоды происходит подъем заболеваемости. Вспышки наблюдаются в различное время года, чаще осенью и зимой. Подъем заболеваемости РСВИ нередко совпадает с эпидемией гриппа, и тогда у детей можно диагностировать микст-инфекцию. Как и грипп, РСВИ увеличивает количество осложнений и летальность от гриппа и пневмонии.
Продолжительность эпидемического подъема заболеваемости ограничивается 3-5 месяцами. Такие вспышки, как правило, имеют место ежегодно в одной и той же местности. В это время РСВ вызывает не только бронхиолиты и пневмонии, но также и легкие заболевания верхних дыхательных путей (ВДП) у детей. Вспышки РСВИ могут протекать в виде ограниченных локальных эпидемий в учреждениях для детей раннего возраста.
Источником инфекции являются больные и вирусоносители. Вирусы выделяются вместе с секретом слизистой оболочки ВДП во время разговора, кашля, чихания, и передача возбудителя здоровым осуществляется воздушно-капельным путем. Опасность заражения от больного человека сохраняется в течение 5-7 дней. Восприимчивость к РСВ очень высока, особенно у детей раннего возраста.
О распространении РСВИ среди различных возрастных групп населения позволяют судить серологические исследования. У большинства новорожденных имеются антитела, полученные от матери. Однако врожденный пассивный иммунитет довольно быстро утрачивается, и уже у детей 4-6-месячного возраста антитела не удается обнаружить. В этот период дети становятся высоко восприимчивыми к РСВ, заболеваемость возрастает, в результате чего увеличивается число детей, которые приобрели антитела, а вместе с ними и иммунитет. У детей в возрасте 5-10 лет антитела к РСВ обнаруживаются у 63-68% обследованных. Примерно такой же результат был получен и при обследовании здоровых взрослых (67%). Заболевания, вызванные РСВ, наблюдаются и среди взрослых различного возраста, при этом у большинства из них имеет место реинфекция, так как болезнь возникает несмотря на наличие нейтрализующих и комплементсвязывающих антител.
Клиника и патогенез
Инкубационный период длится не менее 3 дней, чаще 4-5 дней. Начинается заболевание как остро, так и подостро. У детей грудного возраста чаще наблюдается вовлечение в процесс НДП, в то время как у старших детей и у взрослых изменения обычно ограничиваются областью ВДП и протекают в виде ринита, фарингита, ларингита. Ринит отмечается у большинства пациентов, выделения из носа необильные серозно-слизистые. В ротоглотке может наблюдаться умеренная гиперемия слизистой. Наиболее частый симптом РСВИ - кашель, вначале непродуктивный, затем на 3-4 день болезни появляется мокрота.
Через 2-3 дня от начала болезни, а иногда и в более поздние сроки, обнаруживаются признаки поражения НДП с развитием бронхита, бронхиолита или бронхо-бронхиолита, обусловливающие возникновение БОС. Появляется одышка с втяжением уступчивых мест грудной клетки, обычно экспираторного типа. Дыхание шумное, свистящее.
При бронхите у большинства пациентов на фоне жесткого дыхания выслушивается большее или меньшее количество сухих свистящих хрипов, у части больных - средне- и крупнопузырчатые влажные хрипы. Выдох удлинен. Для бронхиолита характерно обилие мелкопузырчатых влажных и крепитирующих хрипов, выслушиваемых по всей поверхности обоих легких, обычно в конце вдоха. Из-за вздутия легких при перкуссии грудной клетки определяется коробочный звук.
Одним из важных признаков, характеризующих БОС, является цианоз. У детей первых месяцев жизни с бронхиолитом отмечается общий цианоз, дети становятся чугунного цвета. Поражение органов дыхания происходит на фоне лихорадки, которая в отдельных случаях может и отсутствовать.
При рентгенологическом обследовании наиболее характерным признаком РСВИ является повышение прозрачности легочных полей, расширение межреберных промежутков, усиление легочного рисунка за счет расширения крупных сосудистых стволов и обогащения его мелкими линейными тенями. Наблюдается перестройка всего легочного рисунка по сетчато-трабекулярному типу.
В крови в первые дни болезни может обнаруживаться лейкоцитоз за счет гранулоцитов, однако чаще имеет место нормоцитоз или, реже, лейкопения. СОЭ обычно повышена.
Общая продолжительность РСВИ составляет от 5-7 дней до 3-х недель.
У новорожденных и детей второго месяца жизни, особенно недоношенных, при РСВИ могут возникать приступы апноэ. Такие приступы, хотя часто повторяются во время острой инфекции, обычно купируются самостоятельно и, как правило, не сопровождаются неврологическими или системными повреждениями, но требуют наблюдения.
У детей старшего возраста и взрослых РСВИ обычно протекает в стертой форме или проявляется только как афебрильное заболевание ВДП, но может иметь и клиническую симптоматику гриппа. Полагают, что РСВ служит причиной 15% обострений хронического бронхита.
Особого внимания заслуживают тяжелые формы РСВИ у детей раннего возраста, проявляющиеся бронхиолитом или бронхо-бронхиолитом с бронхообструктивным синдромом (БОС), требующие неотложной помощи и могущие привести к летальному исходу. Половина больных этой группы приходится на детей первых 3 месяцев жизни, начиная с раннего неонатального периода. Бронхиолиты в изолированном виде обычно наблюдаются у детей первых месяцев жизни, однако в большинстве случаев, наряду с бронхиолитом, имеются клинические признаки поражения и крупных бронхов. Клинически эту группу больных характеризует выраженная дыхательная недостаточность, определяющая тяжесть болезни, в то время как явления интоксикации выражены слабо или в умеренной степени.
Клиническая диагностика РСВИ представляет определенные трудности ввиду сходства с другими респираторными заболеваниями. И все же некоторые клинические особенности отличают РСВИ от других ОРВИ. Для РСВИ в типичных случаях характерно поражение НДП с развитием бронхита или бронхиолита и возникновением БОС. Дифференциальная диагностика у детей первого полугодия жизни должна включать все другие причины острых заболеваний НДП - вирусы парагриппа, особенно 3 типа, аденовирусы, вирусы гриппа, риновирусы, а также Chlamydia trachomatis. Последняя вызывает интерстициальную пневмонию с кашлем, и, в некоторых случаях, затрудненное дыхание, хотя лихорадка обычно отсутствует. У детей с иммунодефицитом должна быть принята во внимание возможность инфекции Pneumocystis carinii. При бактериальной пневмонии шумного выдоха обычно не бывает, а симптомы общей интоксикации более выражены.
Для диагностики РСВИ имеют значение и эпидемиологические данные. Если это семейный очаг, то взрослые и дети старшего возраста переносят обычное, легкое респираторное заболевание, в то время как у детей раннего возраста наблюдается тяжелое течение, и у них часто возникает бронхит или бронхиолит.
Таким образом, имеющихся клинико-эпидемиологических данных нередко бывает достаточно для предположительного диагноза. Для окончательной верификации диагноза РСВИ используются различные лабораторные методы диагностики.
В практической работе в настоящее время наиболее широко используют экспресс-методы, направленные на определение антигена РСВ в материалах от больных. Антиген РСВ можно обнаружить методом иммунофлюоресценции либо ИФА. Оба метода достаточно специфичны и чувствительны и, по существу, имеют равновеликую ценность. Ответ получают через несколько часов.
Образцы для исследования лучше забирать при аспирации, устанавливая катетер над входом в гортань. Материал можно также получить из полости носа, используя сухой ватный тампон на металлическом стержне, реже пользуются носоглоточными смывами. Взятие материала из НДП для рутинного диагноза не является необходимым, хотя это может повысить результативность диагностики.
У умерших детей исследуют ткань легких, трахеи и бронхов на антиген РСВ или они используются для выделения вируса.
Специфический антиген выявляют методом иммунофлуоресценции в цитоплазме эпителиальных клеток носа с первых дней болезни и в последующие 10 дней. Однако при тяжелых формах болезни мы обнаруживали антиген РСВ до 29-49 дней от начала болезни.
При легких формах РСВИ, которые широко распространены, применяются симптоматические средства, и они не требуют каких-либо специфических мер.
При тяжелых формах заболевания, сопровождающихся БОС, необходима госпитализация детей. Лечение тяжелых форм РСВИ с поражением НДП носит неотложный характер. Первоочередными являются следующие мероприятия:
Несомненно, что главной задачей терапии является обеспечение адекватной оксигенации крови, что достигается как прямой ингаляцией кислорода, так и воздействием на различные механизмы БОС. Уже такое простое мероприятие, как своевременное удаление с помощью электроотсоса слизи, накапливающейся в ВДП, может привести к улучшению дыхательной функции.
При БОС показано применение средств, уменьшающих отек слизистой дыхательных путей, гиперсекрецию и бронхоспазм. Применяются бронходилятаторы и муколитики.
В связи с возникновением тяжелых, иногда критических состояний при БОС в качестве неотложной терапии показано применение глюкокортикоидов, которые применяют в сочетании с бронхолитиками. Преднизолон или гидрокортизона гемисукцинат вводят внутривенно, а затем переходят на пероральный прием. Преднизолон назначается из расчета 2-3 мг/кг, а гидрокортизона гемисукцинат 5-6 мг/кг в сутки.
Патогенетически обосновано применение диуретиков быстрого действия (фуросемид) в лечении обструктивного синдрома, если он обусловлен бронхиолитом. Фуросемид вводится в разовой дозе 1 мг/кг внутривенно или внутримышечно. Повторное введение фуросемида следует проводить с осторожностью, и чаще всего в его повторном введении в ближайшие 24 часа нет необходимости. Бикарбонат натрия для коррекции декомпенсированного ацидоза у детей с БОС не применяется.
Оптимальным вариантом поддержания функционального состояния слизистой дыхательных путей является пребывание ребенка в условиях кислородного аэрозоля (тумана) и применение медикаментозных аэрозольных ингаляций. Получение тумана достигается с помощью производителя аэрозолей эжекционного типа. Аэрозоль направляют под тент-палатку ДКП-1 или под колпак кювеза (для детей первых месяцев жизни). В камере создается кислородный аэрозольный туман с 50-60% содержанием кислорода и высокой влажностью (100%). С помощью производителя аэрозолей распыляют обычную воду, 2% раствор бикарбоната натрия, физиологический раствор, которые оказывают муколитическое действие и способствуют отхождению мокроты и снижению потери жидкости.
Постоянная ингаляционная терапия позволяет достичь, прежде всего, удовлетворительной оксигенации крови. При этом улучшаются и другие показатели газового состава крови и кислотно-щелочного состояния, особенно уменьшается метаболический компонент ацидоза.
С целью поддержания гомеостаза почти всем детям проводится инфузионная терапия, тем более, что полноценное энтеральное кормление часто не может быть обеспечено из-за тяжести состояния, однако она осуществляется в небольших объемах (20-25 мл/кг массы) и кратковременно. Обычно вводится 10% раствор глюкозы с электролитами.
В терапии БОС, особенно при выраженном бронхо-спазме, могут быть использованы бронходилятаторы короткого действия из группы b2-агонистов. Например, сальбутамол (0,2 мг/кг в день) при бронхиолите у детей в возрасте 1-9 месяцев.
Из средств этиотропной терапии для лечения РСВИ у детей раннего возраста в настоящее время в мире препаратом выбора является рибавирин, который является синтетическим нуклеозидом и принадлежит к противовирусным препаратам широкого спектра действия. Условием назначения рибавирина является лабораторно подтвержденный диагноз и ранние сроки заболевания. Показаниями для ингаляций рибавирина являются тяжелые формы РСВИ у детей раннего возраста и больные с врожденными пороками сердца. Применяется в виде длительных ингаляций аэрозолей в дозе 10 мг/кг в сутки. Длительность курса лечения 3-5 дней.
У детей первого года жизни с тяжелой формой БОС, обусловленной РСВ, ингаляции рибавирина и кислорода осуществляются посредством специального аэрозольного генератора малых частиц (SPAG-2). Средний диаметр частиц составляет около 1,5 мкм, а 95% этих частиц имеют диаметр меньше 5 мкм. При применении препарата около 70% ингалированных частиц оседает в дыхательных путях. Продолжительность ингаляции - до 18-20 часов в сутки.
Применение рибавирина приводит к уменьшению тяжести клинической картины заболевания, сокращению длительности БОС, быстрой элиминации возбудителя, ускорению выздоровления.
При применении рибавирина следует самым строгим образом учитывать предупреждения о возможных токсических проявлениях.
В последнее время появились сообщения об использовании иммунотерапии для лечения детей раннего возраста с РСВИ. Клинические испытания иммуноглобулина G для внутривенного введения (в дозе 2 г/кг в день) показали сходный эффект с тем, что наблюдается при применении рибавирина, хотя иммунотерапия не уменьшила сроков госпитализации леченных больных.
Создание вакцин против РСВИ имеет долгую и поучительную историю. Более чем за 30 лет были получены инактивированные, живые аттенуированные и субъединичные РСВ-вакцины. Однако все они оказались неэффективными. Более того, после применения инактивированной вакцины естественное заражение РСВ приводило к более тяжелому течению заболевания. Тем не менее, усилия по созданию новых вакцин против РСВИ не ослабевают, и есть надежда, что эффективная вакцина будет разработана.
1. Медицинская микробиология (под ред. В.И. Покровского и О.К. Поздеева). М.: Гэотар Медицина,1998.
2. Simoes E.A. Respiratory syncytial virus infection. Lancet 1999; 354: 847-52.
3. Domachowske J.B., Rosenberg H.F. Respiratory syncytial virus infection: immune response, immunopathogenesis, and treatment. Clin Microbiol Rev 1999; 12: 298-309.
4. Rodriguez W.J. Management strategies for respiratory syncytial virus infections in infants. J Pediatr 1999; 135: 45-50.
5. Ottolini M.G., Hemming V.G. Prevention and treatment recommendations for respiratory syncytial virus infection. Background and clinical experience 40 years after discovery. Drugs 1997; 54: 867-84.
6. Hussell T.; Openshaw P. Recent developments in the biology of respiratory syncytial virus: are vaccines and new treatments just round the corner? Curr Opin Microbiol 1999; 4: 410-4.
[youtube.player]
Этиология
РС-вирус (Human respiratorysyncytiae virus) относится к семейству Paramyxoviridae (подсем. Paramyxovirinae), роду Pneumovirus .
Цикл репродукции происходит в цитоплазме с прикрепления вируса к клеточной поверхности и слияния вирусной оболочки с плазматической мембраной. Наружная липопротеиновая оболочка вириона содержит белок F, который несет функцию белка при прикрепления вирусной оболочки с клеточной мембраной. Эффективное распространение вируса от клетки к клетке обеспечивает связывание белков F и HN с остатками сиаловой кислоты в олигосахаридах, входящих в состав поверхностных гликопротеинов и гликолипидов.


Эпидемиология
В мире ежегодно регистрируется 64 млн случаев РС-вирусной инфекции.
Респираторно-синцитиальное вирусное заболевание встречается повсеместно, регистрируется в течение всего года с наиболее высокими показателями заболеваемости в холодное время. Как правило, отмечается двухволновой подъем с пиком в начале зимы и весной, часто совпадающий с эпидемией гриппа, что приводит к формированию смешанных форм инфекции. Продолжительность эпидемического подъема составляет 3–5 мес.
Источником заражения является больной с клинически выраженной или стертой формой болезни, реже — вирусоносители. Передача возбудителя происходит воздушно-капельным путем при близком общении и через инфицированные предметы обихода, игрушки, а также при контаминации рук назальным секретом. На поверхности предметов вирус сохраняется до 10–12 ч. Больной заразен в течение 5–7 дней. Болеют в основном дети, большинство из которых инфицируется РС-вирусом уже к 2–4 годам, в возрасте 5–10 лет специфические антитела обнаруживаются у 63–75% обследованных.
Факторами риска тяжелого течения РСвирусной инфекции являются недоношенность при рождении (≤35 нед), бронхолегочная дисплазия, врожденный порок сердца, а также возраст до 6 мес. К эпидемиологическим рискам относятся многодетные семьи, посещение детских учреждений, отсутствие грудного вскармливания. РС-вирусная инфекция является одной из самых опасных для детей в возрасте до 5 лет (WHO, 16 April 2010). В семейных очагах РС-вирусная инфекция развивается у 30% взрослых. Группу риска по развитию тяжелой формы заболевания составляют лица старшего возраста, отягощенные хроническими заболеваниями органов дыхания и сердечно-сосудистой системы.
Патогенез
Вирус реплицируется в эпителиальных клетках слизистой оболочки респираторного тракта, поражая практически все его отделы. Созревание вирионов осуществляется на цитоплазматической мембране (освобождение их происходит через почкование), вызывая гибель клеток. Ведущим звеном в патогенезе синдрома острой бронхиальной обструкции является нарушение дренажной функции бронхиального дерева из-за отека, утолщения стенки бронха, обусловленной воспалительной клеточной инфильтрацией, а также закупорки просвета бронхов клетками слущенного эпителия и слизью.
Особенно быстро этот процесс развивается у детей раннего возраста. Все это приводит к ателектазам и эмфиземе легких. Нарушение бронхиальной проходимости затрудняет процессы газообмена в легких, развиваются гипоксемия, гиперкапния и респираторный ацидоз. В возникновении пневмонии важную роль играет активизация бактериальной флоры. Примерно у каждого 5-го ребенка в раннем возрасте РС-вирусное заболевание протекает с пневмонией, из которых у 50% выражен астмоидный компонент.
При патоморфологическом исследовании в средних и мелких бронхах выявляются сосочкообразные разрастания эпителия, группирование их в многоядерные конгломераты, утолщение межальвеолярных перегородок. Антигены РС-вируса обнаруживаются в циркулирующих мононуклеарных лейкоцитах. В тяжелых случаях у больных с выраженной иммуносупрессией антиген вируса определяется в печени, почках, миокарде.
Важное значение в патогенезе хронизации РСвирусной инфекции имеют состояние иммунитета и цитокиновый статус больных. РС-вирус обладает иммуносупрессивным действием, вызывает иммунопатологические реакции за счет длительной циркуляции иммунных комплексов. Выраженное снижение активности Т-супрессоров, длительное, более 10 дней, определение специфических иммуноглобулинов IgM, низкий уровень IgG к концу 3–4-й недели заболевания создают условия для персистенции вируса и формирования хронической инфекции.
Тяжелое течение инфекции у пожилых связано с увеличением числа повторных эпизодов заболевания и преобладанием Th2 типа иммунного ответа. У детей на фоне иммунопатологических реакций содержание специфических IgG снижено, что препятствует элиминации вируса и способствует длительному течению болезни. Высокая активность Th2 опосредованных реакций (высокий уровень IgE, IgA в крови) у детей раннего возраста является прогностически неблагоприятным из-за высокого риска формирования в дальнейшем атопии и астмы. Сывороточные и секреторные антитела продуцируются в ответ на инфекцию, как правило, в низких титрах и не защищают от реинфекции.
Клиническая картина
Инкубационный период в среднем составляет 4–5 дней, с колебаниями от 2 до 8 дней. Заболевание может начинаться как остро, так и постепенно. Клиническая форма зависит от возраста больного и его иммунологического статуса. Риск развития тяжелых бронхитов и дыхательной недостаточности высок у детей раннего возраста, у лиц с хроническими заболеваниями сердца, бронхолегочной системы и иммунодефицитным состоянием, включая больных после трансплантации органов, инфицированных вирусом иммунодефицита человека (ВИЧ) и стариков. У взрослых заболевание протекает относительно легко и ограничивается областью верхних отделов респираторного тракта, преобладанием катаральных симптомов (назофарингит, ларингит). Наиболее частым симптомом является кашель — непродуктивный в первые дни болезни, затем приобретает влажный характер, появляется мокрота.
У детей раннего возраста чаще наблюдается вовлечение в процесс нижних дыхательных путей: бронхиолиты и пневмонии. Заболевание начинается с ринофарингита, на 2–3-й день появляются признаки поражения нижних дыхательных путей с развитием бронхита и бронхиолита. Возникает синдром острой бронхиальной обструкции. Тяжесть состояния больного в этот период определяет нарастающая дыхательная недостаточность. Появляются одышка и цианоз. В легких при бронхите на фоне жесткого дыхания при аускультации выслушиваются сухие свистящие хрипы, у части больных — множество рассеянных мелких и среднепузырчатых влажных хрипов; для бронхиолита характерно обилие мелкопузырчатых влажных и крепитирующих хрипов. Характерен коробочный оттенок перкуторного звука из-за развившейся эмфиземы.
Одышка (60–80 в мин), как правило, смешанного типа с преобладанием затруднения экспирации, с втяжением мышц эпигастральной области и межреберных промежутков. Кашель приступообразный, мучительный. Может регистрироваться апноэ, существует угроза развития крупа, особенно у детей первых лет жизни (10%).
Рентгенологическое обследование выявляет резкое вздутие легких, повышение прозрачности легочных полей, усиление легочного рисунка за счет расширения крупных сосудов и обогащения его мелкими линейными тенями. Могут наблюдаться очаговые тени и ателектазы.
При развитии пневмонии состояние больных ухудшается — повышается температура до фебрильных значений, нарастают дыхательная недостаточность, цианоз, увеличены печень и селезенка, в периферической крови — лейкоцитоз, высокая скорость оседания эритроцитов (СОЭ). Частым осложнением (40%) является острый средний отит, развивающийся в результате обструкции евстахиевой трубы. Длительность заболевания зависит от его формы и тяжести. Летальность среди госпитализированных составляет 0,5–1,5%. При синдроме внезапной детской смертности в легких на аутопсии обнаруживается РС-вирус.
У детей старшего возраста РС-вирусное заболевание часто протекает в стертой форме, без лихорадочной реакции, у взрослых — в виде бронхита.
Диагностика
Лабораторная диагностика РС-вирусной инфекции включает изоляцию возбудителя на культуре клеток, индикацию антигена или РНК в назофарингеальных смывах или аспирата методами флюоресценции, ПЦР, ИФА. Серологическим подтверждением перенесенного заболевания является 4-кратное нарастание титров антител в непрямом методе флюоресцирующих антител.
Лечение
Этиотропная терапия включает противовирусные препараты. Применяется рибавирин (в ингаляционной форме) у детей раннего возраста; широкое его применение ограничено из-за серьезных побочных эффектов.
При отсутствии обструктивного синдрома проводится симптоматическое лечение, включая муколитические и отхаркивающие средства у больных с вязкой, трудноотделяемой мокротой.
Важной задачей лечения является обеспечение адекватной оксигенации крови посредством прямой ингаляции кислорода, а также мероприятий, направленных на улучшение проходимости дыхательных путей. Основные лечебные мероприятия при острой бронхиальной обструкции включают:
- борьбу с отеком и воспалительным процессом в бронхах;
- купирование бронхоспазма и улучшение кровообращения;
- разжижение и удаление секрета из дыхательных путей;
- восстановление дренажной функции бронхов;
- уменьшение гипоксемии.
При тяжелом обструктивном синдроме в качестве неотложной терапии показано применение ГК, оказывающих противовоспалительное и противоотечное действие. ГК применяют в сочетании с бронхолитиками. В период наиболее тяжелого состояния преднизолон или дексаметазон вводят внутривенно, затем переходят на прием внутрь или в виде ингаляции. Продолжительность ГК-терапии определяется состоянием больного и стойкостью обструктивного синдрома. Патогенетически обосновано применение диуретиков быстрого действия с целью уменьшения отека слизистой оболочки бронхов, улучшения бронхиальной проходимости.
Лечение тяжелых форм, осложненных пневмонией, включает антибактериальную терапию.
Дети, перенесшие РС-заболевание с обструктивным синдромом, нуждаются в диспансерном наблюдении. Выздоровление наступает в 72% случаев, в 15% — развивается рецидивирующий обструктивный бронхит, а в 10% — бронхиальная астма (БА).
Профилактика
Для иммунопрофилактики рекомендуется паливизумаб (Синагис ® ) детям из групп высокого риска. Вводится внутримышечно в дозе 15 мг/кг массы тела. Проводится 5 инъекций препарата с интервалом 1 мес в течение сезонного подъема заболеваемости. Для лечения РС-вирусной инфекции не используется.

Грипп: диагностика, лечение, эффективные препараты, профилактика, вакцинопрофилактика, прививки от гриппа
Лечебный алгоритм гриппа состоит из базисной (противовирусной) терапии и терапии, которая индивидуализирует больного (респираторная поддержка, антибиотики, патогенетическая и симптоматическая терапия). Противовирусную терапию следует назначать не позднее 48 ч (оптимально — 24–36 ч), что обусловлено сроками начального накопления вирусных частиц в организме больного

Парагрипп: возбудитель, патогенез, симптомы, диагностика, лечение
Парагрипп распространен повсеместно. Подъем заболеваемости — в осенне-весенний период, спорадические случаи регистрируются в течение года. Источник инфекции — больной человек в первые дни болезни, когда катаральные симптомы (кашель, ринит) наиболее выражены. Путь передачи — воздушно-капельный, возможен контактно-бытовой
[youtube.player]Читайте также:


