Ротавирусная инфекция эпидемиология патология вакцинопрофилактика
- КЛЮЧЕВЫЕ СЛОВА: вакцинопрофилактика, инфекции, ОРВИ, ротавирус, вакцинация, фенол, крезол, формалин, РотаТек
Проблема внутрибольничной циркуляции ротавируса
Сокрытие нозокомиальных ротавирусных инфекций (РВИ) – повсеместная практика, связанная с невыполнимыми требованиями СанПиН о выявлении вирусоносителей, изоляции контактов, реконвалесцентов, обследовании персонала детских учреждений и больниц. Подобные инфекции не регистрируются и диагностируются как острые респираторные вирусные инфекции (ОРВИ) с кишечным синдромом.
Следует отметить, что ротавирусы устойчивы к хлору, эфиру, хлороформу, детергентам, гипохлориту, ультразвуку и инактивируются только фенолами, крезолом, формалином.
Ротавирусы достаточно долго персистируют:
- в водопроводной воде – до 60 дней;
- во внешней среде – от десяти до 30 дней;
- в фекалиях – до семи месяцев;
- на фруктах – от пяти до 30 дней;
- шерстяных и хлопковых тканях – от 12 до 45 дней;
- различных поверхностях – до десяти дней.
Заражение РВИ происходит не только контактным путем, но и через загрязненные предметы и поверхности, а также воздушным путем (ротавирус обнаружен в воздухе больничных палат). К слову сказать, важный фактор распространения нозокомиальных РВИ внутри больничной палаты – медперсонал (несоблюдение гигиены, в частности мытья рук) и матери, остающиеся с больными детьми 1 .
Высокая температура тела, интоксикация, рвота в отсутствие диареи, характерные для начального этапа ротавирусного гастроэнтерита (РВГЭ), приводят к госпитализации в соматическое отделение. Такая картина наблюдается у 7% пациентов с РВГЭ, значительно чаще при ранней госпитализации.
Ротавирус – ведущий возбудитель нозокомиальных диарей в детской популяции. Например, в Европе им заражаются 5–27% госпитализированных детей в возрасте до двух лет.
Частота нозокомиальной РВИ в эпидемический сезон:
- в Европе: общая – 2,9 на 100 госпитализаций, в детской популяции (в возрасте до двух лет) – 8,1 на 100 госпитализаций 2–4 ;
- Бразилии: 4,9 на 1000 койко-дней и 5,5 на 100 больных 5 ;
- Канаде: 0,5 на 1000 койко-дней 6 .
Следует отметить, что РВИ удлиняет госпитализацию на три – пять дней и в половине случаев требует внутривенной регидратации.
Не последнюю роль в распространении ротавируса играет нозокомиальная РВИ. По данным разных авторов, доля полученных в больнице РВИ от всех пациентов с ротавирусом, находившихся в этой больнице на лечении, – 23,8–43,0%. В частности, в Польше данный показатель составляет 4,5–45,4% 1 , США – 25% 7 .
Из всех случаев ротавирусных диарей больничное происхождение имеют:
- в Австралии – 56,9%;
- Германии – 69,0%;
- Швейцарии – 48,6%;
- Польше – 72% 8, 9 .
Единственный метод контроля нозокомиальной инфекции – массовая вакцинация. Профессор В.К. Таточенко представил данные снижения частоты госпитализаций после вакцинации. Так, во Франции вакцинация (три дозы, охват – 47%), проводимая с 2008 г., позволила снизить частоту госпитализаций среди детей в возрасте до двух лет по поводу РВГЭ на 98% по сравнению с невакцинированными 10 . В Финляндии среди вакцинированных (три дозы ротавирусной вакцины, охват – 90%) не зафиксировано случаев РВГЭ 11 .
Наряду со снижением частоты госпитализаций массовая вакцинация позволила снизить частоту нозокомиальных РВГЭ: в Австрии и Германии – на 72% 12 , США (в первые два года) – на 60% 13 .
В заключение докладчик еще раз подчеркнул, что только массовая вакцинация способна противостоять ротавирусной инфекции.
Эпидемиология ротавирусной инфекции в России
По словам Александра Тихоновича ПОДКОЛЗИНА, к.м.н., заведующего лабораторией молекулярной диагностики и эпидемиологии кишечных инфекций Центрального научно-исследовательского института эпидемиологии, показатель заболеваемости РВИ в России не характеризует активность эпидемического процесса в популяции, а лишь отражает адекватность надзора за данной патологией.
Эпидемиология РВИ имеет региональные особенности. В большинстве регионов, согласно объединенным данным по 61 субъекту РФ за 2008–2015 гг., пик заболеваемости РВИ приходится на холодные месяцы года (с декабря по май). Однако территории с субтропическим климатом, такие как Краснодарский край и Республика Крым, характеризуются атипичной сезонностью РВИ с пиком заболеваемости в летние месяцы, особенно в августе. Атипичный подъем РВИ на указанных территориях обусловлен не только особенностями климата, но и активной рекреацией людей из других регионов: количество отдыхающих в курортный сезон практически в три раза превышает численность постоянно проживающего населения. Аналогичная ситуация и на зарубежных курортах. Решить данную проблему только за счет увеличения объема противоэпидемических мероприятий в курортный сезон практически невозможно.
К сожалению, заболевания, связанные с РВИ у детей, способны приводить к летальным исходам. А.Т. Подколзин перечислил основные патологии, выявленные по результатам патологоанатомических и лабораторных исследований у 55 детей в возрасте до пяти лет с синдромом диареи и развитием летальных исходов за период 2011–2016 гг. В 20% случаев это были пневмонии без возбудителей острых кишечных инфекций (ОКИ), в 17% – пневмонии в сочетании с ОКИ, в 50% случаев – ОКИ.
В этиологической структуре основных возбудителей ОКИ доминировал ротавирус как по показателю клинически значимой концентрации в острой фазе заболевания (23,6%), так и по общей частоте выявления патогенов (30,9%). На долю аденовируса пришлось 1,8 и 10,9%, норовируса – 7,3 и 9,1%, сальмонеллы – 5,5 и 7,3% соответственно. В большинстве своем ротавирусы были представлены генотипами G4P[8], G9P[8], G1P[8], G3P[8] и G2P[4].
По мнению А.Т. Подколзина, защитить детей от ротавируса и обеспечить необходимый эпидемиологический эффект способна только широкомасштабная вакцинация. Однако, как показывает статистика, в 2016 г. охват вакцинацией пятивалентной ротавирусной вакциной (РВ5) на территории РФ был весьма незначительным – менее 1%. Лидерами по охвату вакцинацией детского населения стали Ненецкий автономный округ (47%), Сахалинская область (39%), Камчатский край (19%) и Московская область (18%).
Итоги вакцинации от ротавируса в мире и Российской Федерации: текущая ситуация
Как отметил Александр Васильевич ГОРЕЛОВ, д.м.н., профессор, член-корреспондент РАН, руководитель клинического отдела инфекционной патологии Центрального научно-исследовательского института эпидемиологии, парадигма, долгое время определявшая РВИ исключительно как кишечную инфекцию, сегодня кардинально изменилась. Описаны случаи внекишечной локализации:
- неврологические осложнения: судороги, энцефалит, менингит, церебеллит;
- респираторные осложнения: средний отит, ларингит, фарингит, пневмония;
- поражения органов брюшной полости: гепатит, печеночный абсцесс, панкреатит, сахарный диабет, нефрит;
- прочие проявления: синдром Кавасаки, ДВС-синдром, гемофагоцитарный лимфогистиоцитоз, внезапная смерть ребенка грудного возраста во время сна 14 .
Согласно данным Всемирной организации здравоохранения (ВОЗ), пневмококк (32%) и ротавирус (30%) – основные причины детской смертности. Заболеваемость ОКИ сравнима с заболеваемостью ветряной оспой – 528,10 и 594,00 на 100 тыс. населения соответственно. Однако затраты на лечение ветряной оспы несопоставимы с затратами на лечение РВИ. Один случай госпитализации в 2010 г. при РВИ обходился в 20 300 руб. Сегодня это уже 27 000 руб. В 2015 г. доля РВИ в структуре заболеваемости ОКИ превысила 50%. Ущерб, нанесенный РВИ, сопоставим с ущербом от других более массовых заболеваний.
Единственный способ борьбы с РВИ – вакцинация. В Концепции и стратегии глобальной иммунизации ВОЗ предусмотрено, что ротавирусные вакцины должны быть включены во все национальные программы иммунизации. Применение таких вакцин должно стать частью комплексной стратегии борьбы с заболеваниями, сопровождающимися диареей, направленной на снижение детской смертности, прежде всего с помощью вакцинации против РВИ.
Вакцина против ротавирусов успешно используется уже на протяжении 20 лет. В 88 странах мира проводят ротавирусную вакцинацию.
Безопасность вакцины РотаТек изучали в трех плацебоконтролируемых клинических исследованиях с участием 71 725 детей в возрасте до года, а также в пост-регистрационный период среди 81 000 детей, получавших РВ5. Вакцина продемонстрировала хороший профиль безопасности в до- и пострегистрационный период 15–18 .
Абсолютно очевидна и эффективность вакцинации. В 2008 г. в США были получены первые положительные результаты вакцинации по поводу РВИ: количество идентифицированных случаев РВИ снизилось на 64%, количество госпитализаций – на 45% 19 . Согласно другим данным, внедрение вакцинации против РВИ позволило в два раза уменьшить число госпитализаций по поводу ОКИ любой этиологии среди детей младше трех лет (рис. 1) 20 .
Следует отметить, что, согласно европейским и американским стандартам, госпитализации подлежат дети в состоянии шока, с тяжелой дегидратацией (более 9% массы тела), неврологическими нарушениями (летаргия, судороги и т.д.), неукротимой рвотой, после хирургического вмешательства. То есть речь идет о крайне тяжелых ситуациях. Поэтому снижение частоты госпитализаций в два раза – экономически ощутимый результат.
В США было проведено постмаркетинговое обсервационное исследование эффективности вакцины РотаТек в отношении снижения уровня госпитализации, посещений отделений скорой помощи и обращений за амбулаторной медицинской помощью у пациентов с диагностированным РВГЭ. 33 140 детей первой группы получили три дозы вакцины РотаТек, 26 167 детей второй группы – АКДС. Последующий мониторинг проводился в течение двух ротавирусных сезонов и начинался через 14 дней после получения третьей дозы в обеих группах или в начале каждого сезона. Запланированное наблюдение продолжалось до конца каждого сезона.
Согласно полученным результатам, эффективность вакцины против РВГЭ достигла 100% (95%-ный доверительный интервал (ДИ) 87–100) при госпитализации и посещениях отделений скорой помощи и 96% (95% ДИ 76–100) – при обращениях за амбулаторной медицинской помощью. Эффективность вакцины (госпитализация и посещения отделений скорой помощи) против гастроэнтерита любого вида составила 59% (95% ДИ 47–68) 21 .
Интересные результаты были получены в исследовании B.A. Lopman и соавт. Внедрение в 2006 г. вакцинации против РВИ в Америке обеспечило популяционный эффект. В 2008 г. заболеваемость РВИ среди невакцинированных значительно снизилась в возрастных группах от ноля до четырех, от пяти до 14, от 15 до 24 лет. Кроме того, наблюдалось значительное уменьшение заболеваемости в марте (исторический пик РВИ) во всех возрастных группах. Частота РВГЭ среди невакцинированных лиц в возрасте от пяти до 14 лет уменьшилась на 71%. По оценкам, сумма предотвращенных расходов на лечение РВГЭ у лиц от пяти до 24 лет составила 204 млн долл. 22
По словам профессора А.В. Горелова, в развивающихся странах, как и в России, этиологическая расшифровка диарей и гастроэнтеритов не проводится. Согласно опубликованным данным, в Мексике и Бразилии результативность вакцинации была высокой и привела к снижению заболеваемости РВГЭ на 79–94% 23–25 . Внедрение вакцинации позволило снизить смертность от ОКИ. Показатели ее снижения коррелируют с долей РВИ: в Мексике – на 46%, Бразилии – на 22% 26, 27 .
В странах Европы проведение вакцинопрофилактики способствовало не только снижению риска госпитализаций, но и частоты обращений за врачебной помощью в поликлиники. На основании данных, опубликованных в 2015 г., вследствие применения вакцины РотаТек в 2006–2008 гг. (г. Темпере, Финляндия) частота госпитализаций и обращений в поликлиники в 2009–2011 гг. снизилась на 59% по поводу ОКИ, на 80% по поводу РВИ.
Первый положительный эффект вакцинации РВИ в нашей стране был продемонстрирован в Тюмени и Ачинске. По данным профессора О.А. Рачковой, вакцинация в Тюмени способствовала снижению заболеваемости ОКИ в группе привитых детей по сравнению с непривитыми в два раза (124 против 62) и РВИ в 21 раз (4 против 86) (рис. 3).
По данным профессора Г.П. Мартынова, в Ачинске вакцинация способствовала снижению госпитализаций по поводу ОКИ в 1,4 раза у детей до года и 2,4 раза – у детей от года до трех лет (рис. 4).
Сказанное подтверждает эффективность вакцинации.
В заключение профессор А.В. Горелов отметил, что в странах, внедривших вакцинацию против РВИ, на следующий год отмечается снижение:
- заболеваемости РВИ на 70–90%;
- частоты госпитализаций на 50% и смертности по поводу любых ОКИ на 20–40%;
- заболеваемости РВГЭ в возрастных группах, не подлежащих вакцинации, на 15–70%.
Вакцинация против ротавируса рекомендована для включения в национальный календарь прививок РФ и региональные программы иммунопрофилактики.
Внедрение ротавирусной вакцинации позволяет уменьшить частоту заболеваемости и распространения возбудителя в детской популяции. Введение трех доз пятивалентной ротавирусной вакцины РотаТек предотвращает среднетяжелые и тяжелые формы РВИ у детей раннего возраста, снижает смертность от РВГЭ, потребность в экстренной медицинской помощи, частоту госпитализаций, амбулаторного приема, нозокомиальной инфекции, а также способствует снижению заболеваемости непривитых детей в коллективах за счет уменьшения циркуляции ротавируса. Для достижения необходимого результата важен массовый охват вакцинацией детского населения.
[youtube.player]Версия: Клинические рекомендации РФ (Россия)
Общая информация
СОЮЗ ПЕДИАТРОВ РОССИИ
Вакцинопрофилактика ротавирусной инфекции у детей
Год утверждения (частота пересмотра): 2017 (пересмотр каждые 3 года)
Ротавирусная инфекция (РВИ) – антропонозное высококонтагиозное острое инфекционное заболевание, характеризующееся преимущественным поражением желудочно-кишечного тракта (ЖКТ) в виде гастроэнтерита с симптомами диареи и рвоты, развитием общей интоксикации, дегидратации и нередко наличием респираторного (катарального) синдрома в начальном периоде болезни.
Этиология и патогенез
Эпидемиология
ЭПИДЕМИОЛОГИЯ РОТАВИРУСНОЙ ИНФЕКЦИИ
Эпидемиология ротавирусной инфекции в мире
До сих пор пневмония и инфекционные диареи являются основной причиной смертности детей первых 5 лет жизни в результате инфекционных заболеваний. Ежегодно более 1 млн детей грудного и раннего возраста умирает от пневмококковой инфекции и ротавирусной диареи. На долю последних приходится до 9,9% в структуре общей смертности детей за 2011 г., причем значительную часть из них (70%) составляют дети в возрасте младше 2 лет [4]. Основываясь на данных европейских эпидемиологических исследований, за последнее столетие среди возбудителей острых гастроэнтеритов у детей значительно превалируют вирусы. Среди них наибольший удельный вес приходится на Rotavirus и в меньшей степени Norovirus (англ. Norwalk Virus), тогда как Campylobacter и Salmonella — основные бактериальные агенты —серьезно уступают [5, 6].
В развивающихся странах случаи заболеваний РВИ регистрируются практически круглый год, тогда как в развитых государствах отмечается зимняя сезонность, взаимосвязанная с сопутствующей интеркуррентной заболеваемостью, вызванной нозокомиальной флорой.
1 Оценка степени тяжести РВИ проводится на основании комплекса лабораторных параметров, включающего отдельные показатели периферической крови (число лейкоцитов, нейтрофилов, лимфоцитов, гемоглобин), уровень С-реактивного белка, калия и натрия, рН, мочевины, глюкозы, печеночных трансаминаз. Согласно шкале Везикари (Timo Vesikari), течение заболевания у пациентов с суммой показателей ниже 9 баллов расценивается как легкое, от 12 до 15 —как среднетяжелое, от 16 до 20 —как тяжелая форма РВИ.
Клиническая картина
Более чем у половины заболевших одним из первых симптомов является рвота, которая нередко бывает повторной, но в большинстве случаев прекращается в первые сутки болезни. У отдельных пациентов рвота возникает одновременно с диареей. Позывы к дефекации внезапны, часты, императивны; испражнения носят выраженный энтеритный характер (жидкие, водянистые, пенистые), в тяжелых случаях ― холероподобный; частота стула может достигать 20−30 в сутки. У большинства пациентов имеют место умеренно выраженные но-ющие или схваткообразные боли с локализацией в эпи- и мезогастрии, метеоризм и урчание в животе.
Диагностика
Основным методом диагностики является иммуноферментный анализ, определяющий ротавирусный антиген в кале. Менее чувствительные методы, но простые в употреблении и дающие быстрый результат, — тест-полоски и реакция латекс-агглютинации. Обратно-транскриптазная полимеразная цепная реакция, высокочувствительная в отношении малых концентраций РВ в копрологическом субстрате, используется для идентификации штамма и дальнейшей дифференциации возбудителя.
Профилактика
ПРОФИЛАКТИКА РОТАВИРУСНОЙ ИНФЕКЦИИ
САНИТАРНО-ПРОСВЕТИТЕЛЬНЫЕ МЕРОПРИЯТИЯ В СИСТЕМЕ ПРОФИЛАКТИКИ РОТАВИРУСНОЙ ИНФЕКЦИИ
2 ИЕ ― инфекционная единица.
Информация
Авторы подтверждают отсутствие финансовой поддержки/конфликта интересов, который необходимо обнародовать.
[youtube.player]Внешний вид вирусных частиц напоминает колесо с широкой ступицей, короткими спицами и четко очерченным ободком, поэтому их стали называть ротавирусами (лат. rotа — колесо). Рисунок 1. Слизистая оболочка толстой кишки при ротавирусном гаст
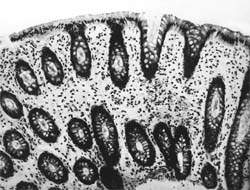 |
| Рисунок 1. Слизистая оболочка толстой кишки при ротавирусном гастроэнтерите. Минимально выраженный катаральный колит. х 100. |
Ротавирусы представляют собой род семейства Reoviridae, который объединяет большое количество сходных по морфологии и антигенной структуре вирусов, вызывающих гастроэнтерит у человека, млекопитающих и птиц. Систематическое изучение ротавирусов человека началось с 1973 года, когда они были обнаружены при электронной микроскопии ультратонких срезов биоптатов слизистой оболочки двенадцатиперстной кишки, полученных от больных острым гастроэнтеритом детей Австралии (Р. Бишоп и соавторы). В том же году Т. Флеветт обнаружил сходный вирус в копрофильтратах больных гастроэнтеритом методом электронной микроскопии при негативном контрастировании препаратов.
Вирусные частицы имеют диаметр от 65 до 75 нм. При проникновении контрастирующего вещества в вирион выявляется электронно-плотный центр диаметром 38 — 40 нм, который представляет собой так называемую сердцевину, окруженную электронно-прозрачным слоем. Внешний вид вирусных частиц напоминает колесо с широкой ступицей, короткими спицами и четко очерченным ободом, поэтому их стали называть ротавирусами (лат. rota — колесо).
Ротавирусы имеют две белковые оболочки — наружный и внутренний капсиды. Сердцевина содержит внутренние белки и генетический материал, представленный двунитчатой фрагментированной РНК. Геном ротавирусов человека и животных состоит из 11 фрагментов, которые могут быть разделены при электрофорезе в полиакриламидном геле (ПААГ) или агарозе. В составе ротавирусов обнаружено четыре антигена; основной из них — это групповой антиген, обусловленный белком внутреннего капсида. С учетом группоспецифических антигенов все ротавирусы делятся на пять групп: A, B, C, D, E. Ротавирусы одной группы имеют общий групповой антиген, который выявляется иммунологическими реакциями: иммуноферментный анализ, иммунофлюоресценция, иммунная электронная микроскопия и др. Большинство ротавирусов человека и животных относятся к группе A.
| Источником инфекции при ротавирусном гастроэнтерите является инфицированный человек — больной манифестной формой заболевания или бессимптомно выделяющий ротавирусы с фекалиями |
Источником инфекции при ротавирусном гастроэнтерите является инфицированный человек — больной манифестной формой заболевания или бессимптомно выделяющий ротавирусы с фекалиями. Вирусы в фекалиях заболевших появляются одновременно с развитием клинических симптомов, наибольшая концентрация их в кале (до 109 — 1011 вирусных частиц в 1 г) регистрируется в первые 3 — 5 дней болезни. В эти дни больные представляют наибольшую эпидемиологическую опасность для лиц, контактирующих с ними. Наиболее частым источником заболевания для детей первого года жизни являются инфицированные ротавирусом матери; для взрослых и детей более старшего возраста — дети, в основном из детских коллективов. Возможность заражения человека от животных не доказана.
Патогенез ротавирусной инфекции характеризуется проникновением вируса в эпителиоциты слизистой оболочки желудочно-кишечного тракта, преимущественно тонкой кишки, что приводит к их повреждению и отторжению от ворсинок. Вследствие этого на ворсинках тонкой кишки появляются функционально и структурно незрелые энтроциты с низкой способностью синтезировать пищеварительные ферменты. При ротавирусном гастроэнтерите это проявляется снижением уровня дисахаридаз, развивается вторичная дисахаридазная недостаточность, при которой в просвете тонкой кишки накапливаются нерасщепленные дисахариды, что создает повышенное осмотическое давление и приводит к выводу в просвет кишечника воды и электролитов из тканей организма. Это является основной причиной диареи и дегидратации и определяет основные клинические проявления болезни.
Ротавирусный гастроэнтерит как инфекционное заболевание имеет циклическое течение. Инкубационный период продолжается чаще всего от 12 — 24 часов до двух суток. Клиническая картина ротавирусного гастроэнтерита характеризуется в основном острым началом, однако в ряде случаев может иметь место продромальный период длительности от 12 до 48 — 72 часов. В этот период больные отмечают недомогание, общую слабость, повышенную утомляемость, снижение аппетита, головную боль, познабливание, урчание и неприятные ощущения в животе, умеренно выраженные катаральные явления: заложенность носа, першение в горле, легкий кашель.
В клинической картине ротавирусного гастроэнтерита в период развернутых клинических проявлений ведущими являются синдромы гастроэнтерита и интоксикации. Выраженность диареи и обусловленной ею той или иной степени дегидратации организма, а также токсикоза, продолжительность этих симптомов в значительной мере определяет тяжесть течения заболевания.
Синдром гастроэнтерита характеризуется развитием диареи, снижением аппетита, появлением урчания и болей в животе, тошноты и рвоты. Наиболее типичен для ротавирусного гастроэнтерита обильный водянистый пенистый стул желтого или желто-зеленого цвета. У больных с легким течением заболевания стул может быть кашицеобразным. Как правило, патологические примеси в стуле отсутствуют. Боль локализуется преимущественно в верхней половине живота или является диффузной, она может быть разной интенсивности. Почти всегда она сопровождается громким урчанием в животе.
Синдром интоксикации появляется в самом начале заболевания. Слабость, зачастую резкая, является наиболее частым проявлением этого синдрома; реже отмечается головная боль. При более тяжелом течении имеют место головокружение, обморочное состояние, коллапс. Обращает на себя внимание следующая особенность ротавирусного гастроэнтерита: два ведущих в клинической картине болезни синдрома развиваются в процессе заболевания не всегда однонаправленно; у некоторых больных на фоне сравнительно слабо выраженных диспепсических явлений могут наблюдаться резко выраженные симптомы общей интоксикации, особенно слабость.
Повышение температуры тела не всегда может отмечаться при ротавирусном гастроэнтерите, особенно у взрослых. У некоторых больных может быть озноб без повышения температуры. В то же время нередко в разгар заболевания выраженность лихорадочной реакции варьируется от субфебрильных цифр и выше и может достигать 38 — 39°С как у детей, так и у взрослых.
Важным в диагностическом плане для ротавирусного гастроэнтерита считается сочетание двух ведущих клинических синдромов с симптомами поражения верхних дыхательных путей. Катаральный синдром встречается приблизительно у 50% больных и проявляется в виде гиперемии и зернистости слизистых оболочек мягкого неба, небных дужек, язычка, задней стенки глотки, а также насморка, заложенности носа, кашля, болей в горле. В ряде случаев катаральные симптомы наблюдаются уже в продромальном периоде, до проявления симптомов гастроэнтерита.
В разгар болезни отмечается изменение функционального состояния сердечно-сосудистой системы, чаще у пациентов с более тяжелым течением и при наличии сопутствующих заболеваний органов кровообращения. У большинства пациентов отмечается тенденция к артериальной гипертензии, тахикардия, определяется глухость сердечных тонов при аускультации. У больных с тяжелым течением заболевания, как правило, возникают обмороки и коллапсы из-за выраженных расстройств гемоциркуляции, в генезе которых наряду с токсическими воздействиями существенное значение имеет гиповолемия. Потери жидкости и электролитов вследствие рвоты и диареи могут быть значительными и приводят к развитию дегидратации. Клинические проявления дегидратации зависят от ее степени. При легком и среднетяжелом течении ротавирусного гастроэнтерита отмечается жажда, сухость во рту, слабость, бледность (дегидратация I — II степени), при тяжелом течении наряду с этими симптомами наблюдаются также осиплость голоса, судороги мышц конечностей, акроцианоз, снижение тургора кожи, уменьшение диуреза (дегидратация III степени).
В связи с развитием при ротавирусном гастроэнтерите возможных осложнений, главным образом циркуляторных расстройств, острой сердечно-сосудистой недостаточности, нарушений гомеостаза, выделяют группы больных повышенного риска, в которые включают новорожденных, детей младшего возраста, лиц пожилого возраста, а также больных с тяжелыми сопутствующими заболеваниями. Описанные в литературе и наблюдавшиеся нами случаи ротавирусного заболевания с летальным исходом относятся именно к этим группам.
Выделяются две основные клинические формы ротавирусного заболевания — гастроэнтерическая и энтерическая. Симптомы только острого гастрита (гастритический вариант) встречаются в 3 — 10% случаев. Функциональные и морфологические нарушения со стороны желудочно-кишечного тракта, возникающие при ротавирусном гастроэнтерите в случае наличия у пациентов фоновой гастроэнтерологической патологии, нередко способствуют развитию таких осложнений основного заболевания, как обострение сопутствующих болезней: хронического гастрита, энтероколита, панкреатита, часто в сочетании с выраженными явлениями дисбактериоза кишечника, требующими коррекции при лечении.
При ротавирусном гастроэнтерите гемограмма изменяется следующим образом: в остром периоде заболевания с высокой частотой выявляются лейкоцитоз с нейтрофилезом и повышенная СОЭ. В периоде реконвалесценции картина крови обычно нормализуется полностью. Изменения урограммы у большинства больных имеют кратковременный характер и проявляются чаще всего небольшой протеин-, лейкоцит- и эритроцитурией; в редких случаях в моче появляются гиалиновые цилиндры в незначительном количестве. При тяжелом течении заболевания нарушения функции почек могут быть более выраженными, с повышением уровня мочевины крови, олигоурией или анурией, снижением клубочковой фильтрации. На фоне проводимой терапии указанные изменения быстро исчезают и при повторных обследованиях не отмечаются.
В качестве примера, иллюстрирующего особенности клинического течения ротавирусного гастроэнтерита, приводим выписку из истории болезни.
Лечение: обильное питье солевых растворов, парентеральная регидратационная и дезинтоксикационная терапия — трисоль 1000 мл внутривенное капельное введение, внутрь ферментные препараты: абомин, панкреатин, тансол, карболен. Течение заболевания без осложнений. На третий день болезни — субфебрильная температура, оставалась слабость; боли в животе прекратились. Стул кашицеобразный до пятого дня от начала заболевания. Полное выздоровление наступило на седьмой день болезни.
Дифференциальный диагноз у больных ротавирусным гастроэнтеритом проводят с другими острыми кишечными инфекциями как вирусной так и бактериальной этиологии, прежде всего в тех случаях, когда в клинической картине на первый план выступает синдром гастроэнтерита: с вирусными диареями различной этиологии (аденовирусы, коронавирусы, астровирусы, калицивирусы, вирус Норфолк, энтеровирусы Коксаки и ЕСНО); с гастроинтестинальной формой сальмонеллеза, с гастроэнтеритическим и гастроэнтероколитическим вариантами острой дизентерии, с пищевыми токсикоинфекциями, вызванными условно-патогенными бактериями; с холерой.
Обнаружение специфических антител и нарастание их титра в сыворотке крови больных и переболевших ротавирусным гастроэнтеритом при помощи серологических реакций с целью текущей диагностики на практике в настоящее время широкого распространения не получило и используется в основном для ретроспективного анализа различных эпидемиологических ситуаций.
Методы обнаружения вирусспецифической РНК, которые можно назвать высокочувствительными и специфичными, имеют, однако, ряд недостатков, ограничивающих их практическое применение (необходимость наличия специальной аппаратуры, реактивов, квалифицированного персонала и др.) Наиболее простой метод в этой группе — электрофорез ротавирусной РНК в полиакриламидном геле. Этот метод, позволяющий идентифицировать штаммы вирусов, вызвавшие заболевание, и дать характеристику штаммов, циркулирующих на данной территории, в основном применяется при эпидемиологических исследованиях.
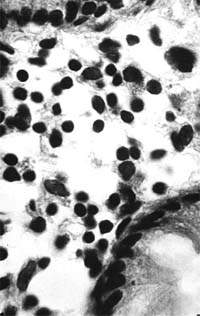 |
| Рисунок 2. Слизистая оболочка толстой кишки при ротавирусном гастроэнтерите. Минимальное содержание плазматических клеток в собственной пластинке, увеличение в ней числа макрофагов. х 400 |
В клинической практике врач нередко сталкивается с обстоятельствами (сомнительные результаты вирусологических и серологических исследований, случаи микст-инфекций), когда возникает необходимость в применении дополнительных методов для верификации диагноза. С этой целью может быть использован доступный для практического здравоохранения интрументальный метод исследования — ректороманоскопия с аспирационной биопсией слизистой оболочки толстой кишки. При гистологическом, морфометрическом и гистохимическом исследованиях биоптатов при ротавирусном гастроэнтерите выявляются характерные изменения в виде поверхностного минимально выраженного катарального колита с незначительной дистрофией эпителия (рис. 1), снижения числа серотонинсодержащих желудочно-кишечных эндокриноцитов (ЕС-клетки) в эпителиальном пласте кишечных желез, умеренной инфильтрацией собственной пластинки плазматическими клетками и увеличением в ней числа макрофагов (рис. 2). Эти особенности имеют дифференциально-диагностическое значение, поскольку отличаются указанным показателем от других острых кишечных инфекций, что может быть использовано в диагностически сложных случаях.
Здравоохранение в настоящее время не располагает препаратами, обладающими специфическим антиротавирусным действием, поэтому терапия ротавирусного гастроэнтерита является патогенетической. Основные ее цели — борьба с дегидратацией, токсикозом и связанными с ними наиболее часто встречающимися при ротавирусном гастроэнтерите нарушениями функции жизненно важных органов — сердечно-сосудистой системы и органов мочевыделения, степень выраженности которых во многом определяет тяжесть течения заболевания и его прогноз.
Для правильного выбора характера и объема проводимой регидратационной терапии в первую очередь необходимо установить степень дегидратации у того или иного пациента. При эксикозе I — II степени следует ограничиваться пероральной регидратационной терапией (препараты регидрон, глюксолан и др.). При дегидратации III степени целесообразно прибегать к комбинированной парентеральной и пероральной регидратации. Для парентеральной регидратации применяют растворы трисоль, квартасоль, ацесоль и др. С целью дезинтоксикации и улучшения гемодинамики при среднетяжелом и тяжелом течении заболевания показаны коллоидные растворы (гемодез, полиглюкин и др.).
| Для ротавирусной инфекции характерно сочетание гастроэнтерита, интоксикации и симптомов поражения верхних дыхательных путей |
Современными представлениями о патогенезе диарейного синдрома при ротавирусном гастроэнтерите обусловлено и назначение соответствующих средств, способствующих нормализации состояния пищеварительного тракта, а также диеты. Учитывая нарушения активности ряда пищеварительных ферментов, в частности лактазы, рекомендуется исключить в острый период заболевания из пищевого рациона больных молоко и молочные продукты. Кроме того, по этой же причине целесообразно ограничивать и пищу, богатую углеводами. В связи с вышеизложенным, в острый период необходимы энзимные препараты (панзинорм-форте, фестал и др). Кроме того, в остром периоде заболевания могут быть использованы адсорбирующие и вяжущие средства, способствующие ускоренному формированию стула (смекта, карболен и др.) также возможно применение хилака-форте. Высокой частотой дисбактериозов кишечника различной степени выраженности у больных ротавирусным гастроэнтеритом обусловлена необходимость применения в комплексной терапии бактерийных биологических препаратов. Лучшая терапевтическая эффективность при ротавирусном гастроэнтерите отмечена при применении лактосодержащих бактерийных биологических препаратов (ацилакт, лактобактерин и др.), что, по-видимому, связано с заместительным действием бактериальной лактазы, содержащейся в лактобактериях. В последние годы в комплексной терапии ротавирусного гастроэнтерита начал применяться комплексный иммуноглобулиновый препарат (КИП), который разработан и выпускается в МНИИЭМ им. Г. Н. Габричевского. Это первый отечественный иммуноглобулиновый препарат для энтерального применения. КИП характеризуется повышенной концентрацией антител к микроорганизмам, возбудителям острых кишечных инфекций, в том числе ротавирусам, сальмонеллам, шигеллам, эшерихиям и др. Применение КИП в комплексной терапии больных ротавирусным гастроэнтеритом оказывает отчетливый положительный терапевтический эффект, существенно сокращая продолжительность интоксикации и диареи, что открывает новые возможности в лечении этого заболевания.
Литература
1. Букринская А. Г., Грачева Н. М., Васильева В. И. Ротавирусная инфекция. М., 1989.
2. Дроздов С. Г., Покровский В. И., Шекоян Л. А., Машилов В. П. и др. Ротавирусный гастроэнтерит. М., 1982.
3. Новикова А. В. и др. Архив патологии, 1989, №6.
4. Щербаков И. Т. и др. Архив патологии, 2995, №3.
5. Юшук Н. Д., Царегородцев А. Д.. Лекции по инфекционным болезням. М., 1996.
Читайте также:


