Суставной синдром при паранеопластическом синдроме
Считается, что в основе большинства паранеопластических ревматических проявлений лежат гиперергические иммуновоспалительные реакции реагинового, иммунокомплексного либо аутоиммунного типа на метастазирующие злокачественные клетки или поступающие в кровоток "чужеродные" опухолевые антигены, которые могут перекрестно реагировать с антигенами нормальных тканей. Имеет значение образование в нормальных тканях под влиянием циркулирующих продуктов жизнедеятельности неоплазмы неоантигенов, участвующих в развитии иммунокомплексного воспаления. Полагают, что характер паранеопластических ревматических проявлений определяется как антигенными свойствами опухоли, так и индивидуальными иммунными реакциями больного, в частности генетически детерминированным или приобретенным дисбалансом основных звеньев иммунной системы. Иммунологические сдвиги в организме могут появляться на самых ранних стадиях злокачественной трансформации тканей, когда новообразование ввиду своих незначительных размеров при обследовании еще не определяется. Рассматривается также роль активации латентной вирусной инфекции в развитии ревматических воспалительных реакций у больных злокачественными новообразованиями. Подтверждением взаимосвязи ревматических проявлений со злокачественными опухолевыми заболеваниями являются многочисленные случаи развития рака различной локализации у больных ревматоидным артритом, синдромом Шегрена и другими системными заболеваниями соединительной ткани. Возможно, эти наблюдения подтверждают, с одной стороны, иммунологическую взаимосвязь двух патологических процессов, с другой — свидетельствуют о проонкогенной роли иммуносупрессивной терапии, проводимой таким больным в связи с ревматическим заболеванием. Наряду с этим успехи современной медицины привели к значительному увеличению продолжительности жизни больных ревматическими заболеваниями, и они стали "доживать до ракового возраста" вследствие чего злокачественная опухоль возникает у них как вторая болезнь. Однако наблюдаются случаи, когда симптомы ревматического заболевания, длительно существовавшего до появления признаков злокачественной опухоли, исчезали после радикального ее удаления.
Поражение суставов у онкологических больных могут быть самыми разнообразными — от синдрома фибромиалгии, объединяющего артралгии, миалгии, оссалгии, иногда в сочетании с тендинитом, до клинически развернутой картины артрита. Артралгия при злокачественных новообразованиях может быть как паранеопластической, так и вызванной метастазами в кости. Паранеопластическая артралгия наблюдается при остром лейкозе, лимфомах, нейробластомах.
Суставной синдром при паранеопластических ревматических реакциях может протекать по типу реактивного артрита или ревматоидного артрита с явлениями синовита. В первом случае развивается асимметричный полиартрит, реже моноартрит, с поражением крупных суставов преимущественно нижних конечностей, во втором — симметричный полиартрит с вовлечением мелких суставов кистей и стоп. У некоторых больных наблюдаются подкожные ревматоидные узелки, рентгенологические признаки длительно текущего ревматического процесса — эрозивные изменения суставных поверхностей эпифизов. Изредка паранеопластический суставной синдром проявляется поражением позвоночника с симптомами анкилозирующего спондилоартрита (болезни Бехтерева). У ряда больных генерализованная иммуновоспалительная реакция протекает под маской ревматоидного артрита с висцеральными проявлениями по типу синдрома Стилла либо системного заболевания соединительной ткани (дерматомиозита, узелкового полиартериита). Экстраартикулярные паранеопластические ревматические проявления, так же как и артрит, могут возникать уже на ранних стадиях злокачественного роста, они отличаются резистентностью к глюкокортикостероидам и цитостатикам, применяющимся для лечения этих заболеваний, и чаще всего исчезают после радикального удаления опухоли. У отдельных больных ослабление или даже исчезновение системных ревматических реакций происходит по мере прогрессирования неопластического процесса и нарастания раковой интоксикации. Воспалительные изменения суставов, в том числе возникающие раньше манифестации симптомов злокачественного новообразования, могут сопровождаться признаками общей интоксикации, анемией, лейкопенией, тромбоцитопенией, повышением скорости оседания эритроцитов, гипергаммаглобулинемией, криоглобулинемией, повышением в крови уровня циркулирующих иммунных комплексов, появлением антинуклеарных антител, LE-клеток, ревматоидного фактора. У разных больных один и тот же паранеопластический ревматический синдром может быть признаком опухолей различной локализации и неодинакового морфологического строения и, наоборот, при опухолях одной и той же локализации и сходного морфологического строения могут быть различные ревматические проявления. Отмечено также, что у одного и того же больного последовательно возникающие на протяжении жизни (метахронные) опухоли разной локализации способны вызывать различные паранеопластические ревматические синдромы. Для рецидивирующих и метастазирующих опухолей характерна однотипность ревматических симптомов с исходной опухолью. В некоторых случаях они возникают после оперативного лечения злокачественного новообразования (в том числе иногда через несколько лет), что может быть связано с развитием метастазов первичной опухоли либо с появлением нового очага злокачественного роста той же или другой локализации.
В ряде случаев паранеопластический артрит сочетается с пальмарным апоневрозитом, проявляющимся узелковым утолщением ладонного апоневроза в сочетании с болезненной сгибательной контрактурой пальцев кисти, напоминающей таковую при системной склеродермии. При этом достаточно часто пальмарному апоневрозиту сопутствует синдром Рейно, который может выступать также в качестве самостоятельной паранеопластической ревматической реакции.
При некоторых злокачественных новообразованиях наряду с паранеопластическим артритом может развиться синдром Мари—Бамбергера (гипертрофическая остеоартропатия). Основное проявление данного синдрома — деформация концевых фаланг обеих рук по типу "барабанных палочек" и изменение ногтей в виде "часовых стекол". Сочетание обоих признаков носит название "пальцев Гиппократа". В основе этих изменений лежат пролиферация фибробластов, разрастание коллагена и отек мягких тканей, обусловленные местной тканевой гипоксией, нарушениями вегетативной иннервации и, возможно, воздействием продуктов опухолевых клеток. Наряду с "пальцами Гиппократа" при паранеопластическом синдроме Мари—Бамбергера появляется периостит в области концевых отделов длинных трубчатых костей (чаще предплечий и голеней), а также костей кистей и стоп. В местах периостальных изменений могут отмечаться выраженная оссалгия или артралгия и локальная пальпаторная болезненность, при рентгенологическом исследовании выявляется двойной кортикальный слой, обусловленный наличием узкой плотной полоски, отделенной от компактного костного вещества светлым промежутком (симптом "трамвайных рельсов"). Считают, что синдром Мари—Бамбергера патогномоничен для рака легкого, реже он возникает при других первичных интраторакальных опухолях (доброкачественные новообразования легких, мезотелиома плевры, тератома, липома средостения). Изредка данный синдром встречается при раке желудочно-кишечного тракта, лимфоме с метастазами в лимфатические узлы средостения, лимфогранулематозе. Вместе с тем синдром Мари—Бамбергера развивается и при неонкологических заболеваниях — амилоидозе, хронической обструктивной болезни легких, туберкулезе, бронхоэктазах, врожденных и приобретенных пороках сердца и др. Одной из отличительных черт данного синдрома при неопухолевых заболеваниях является длительное (в течение лет) развитие характерных изменений костно-суставного аппарата, в то время как, при злокачественных новообразованиях этот процесс исчисляется неделями и месяцами. После радикального оперативного лечения рака синдром Мари—Бамбергера регрессирует и полностью исчезает в течение нескольких месяцев.
Весьма характерным для рака верхушки легкого (опухоль Панкоста), реже злокачественной опухоли другой локализации, является развитие синдрома "плечо кисть" (рефлекторная симпатическая дистрофия, или альгонейродистрофия). Данный синдром проявляется острым односторонним плече лопаточным периартритом в сочетании с вазомоторными и трофическими изменениями кисти на стороне поражения. Больных беспокоят упорная ноющая боль в плечевом суставе с иррадиацией в шею и заднюю поверхность руки, резкое ограничение активных движений, которые совершаются с участием сухожилий, вовлеченных в патологический процесс. На этом фоне возникают нейротрофические нарушения в области кисти: плотный отек, похолодание, цианоз, усиление потоотделения, парестезии с постепенным развитием сгибательной контрактуры пальцев вследствие фиброзных изменений ладонного апоневроза, склеродермоподобным истончением кожи, атрофией мышц тенара и гипотенара. При этом локтевой сустав остается интактным. В отдельных случаях указанные изменения, так же как и синдром Мари—Бамбергера, выступают в качестве единственных паранеопластических ревматических проявлений.
У больных злокачественными новообразованиями возможно развитие метастатического моно- или полиартрита или вторичной подагры на фоне гиперурикемии, возникшей в результате быстрого распада опухоли под влиянием цитостатиков. Кроме того, при раке поджелудочной железы артрит может быть обусловлен расплавлением жировой ткани суставов выходящими в кровоток панкреатическими ферментами. Иногда появление артрита связано с медикаментозной терапией злокачественного новообразования. Описаны случаи развития артрита при лечении интерлейкином-2, альфа-интерфероном, вакциной БЦЖ (Bacillum Calmette Guerin, BCG), антиэстрогеном тамоксифеном и др. специфическими препаратами.
Дифференциальная диагностика суставного синдрома и системных заболеваний соединительной ткани как самостоятельной нозологической формы или паранеопластической реакции нередко весьма затруднительна.
Признаки, на которые следует обращать внимание при выявлении у больного симптомов ревматической реакции:
- первые проявления системных заболеваний соединительной ткани и полиартрита в возрасте старше 50 лет, и, напротив, появление в более молодом возрасте признаков заболеваний, встречающихся в пожилом и старческом возрасте (болезнь Хортона, ревматическая полимиалгия);
- несоответствие тяжелого общего состояния больного и высоких лабораторных показателей активности воспалительного процесса, с одной стороны, и относительно умеренно выраженных признаков артрита и других ревматических проявлений — с другой;
- отсутствие отдельных типичных клинических и лабораторных признаков, характерных для системного заболевания соединительной ткани, реактивного артрита или ревматоидного артрита;
- отсутствие полового диморфизма, типичного для некоторых ревматических заболеваний (системная красная волчанка у мужчин или анкилозирующий спондилоартрит у женщин);
- упорное течение или нехарактерное для конкретного ревматического заболевания быстрое прогрессирование клинических проявлений, нередко значительно опережающее клиническую манифестацию злокачественного новообразования;
- немотивированное резкое ухудшение общего состояния больного на фоне стабилизации ревматического процесса, а также появление новых, не свойственных данному заболеванию симптомов, обусловленных локальным ростом опухоли или развитием ее метастазов;
- лихорадка, устойчивая к лечению антибиотиками и противовоспалительными препаратами;
- резистентность к специфической противовоспалительной терапии ревматического заболевания.
Таким образом, ориентировочные признаки, касающиеся, в частности, времени появления и особенностей клинического течения ревматических заболеваний позволяют заподозрить паранеопластический процесс и обосновать диагностический поиск с целью исключения злокачественного новообразования, в том числе с использованием специфических лабораторных параметров — альфафетопротеина, карциноэмбрионального антигена и других маркеров злокачественной трансформации (в частности, у мужчин специфического простатического антигена и антигена Са-125) и др.
Паранеопластические синдромы развиваются редко, но могут иметь огромное влияние на диагностику и исход онкологических заболеваний. Ревматолог должен быть знаком с несколькими типичными костно-мышечными манифестациями злокачественных новообразований, чтобы иметь возможность рано постановить диагноз и своевременно начать противоопухолевое лечение. В данном обзоре описываются характерные черты различных паранеопластических артритов и васкулитов, ассоциированного с опухолями миозита, гипертрофической остеоартропатии и опухоль-индуцированной остеомаляции. В дополнение к этому обсуждаются текущие представления о механизма, лежащих в основе данных синдромов.
1. Введение
Ревматические симптомы могут быть связаны со злокачественными заболеваниями различными способами. Опухоли могут возникать из мезенхимальных клеток костей, хрящей, мышц или соединительной ткани. Также костно-мышечная система может подвергнуться инвазии метастазами опухолей других локализаций или инфильтрации клетками гематологических опухолей. Кроме того, некоторые варианты противоопухолевой терапии могут вызывать множество ревматических проявлений. Особый интерес для ревматолога представляют скелетно-мышечные симптомы, вызванные ингибиторами ароматазы, БЦЖ-индуцированный реактивный артрит при карциноме мочевого пузыря, а в последнее время к этому списку также добавились различные аутоиммунные проявления и симптомы, связанные с лечением ингибиторами контрольных точек иммунного ответа. Этот обзор фокусируется на третьем возможном механизме, который связывает рост злокачественных клеток и аутоиммунитет: паранеопластический ревматический синдром.
Паранеопластические синдромы редки, но имеют характерные черты, которые могут быть чрезвычайно значимы для раннего выявления и терапии скрытого злокачественного заболевания. Они не вызываются напрямую опухолью или метастазами, но опосредуются растворимыми факторами, такими как гормоны и цитокины, или гуморальными и клеточными иммунными механизмами, направленными против опухолевых клеток. Поэтому клинические проявления паранеопластических синдромов могут наблюдаться в удалении от основной опухоли и включать поражение суставов, фасций, мышц, сосудов и костей.
Чтобы классифицировать ревматическое заболевание как истинно паранеопластическое, должна быть продемонстрирована причинная связь между злокачественной опухолью и костно-мышечной патологией. Для обоснования подобной связи и отличия от простого совпадения более 50 лет назад были предложены критерии Брэдфорда Хилла. В случае паранеоплазии, помимо силы и специфичности ассоциации между диагнозом опухоли и ревматическими симптомами, их временные отношения являются критическим вопросом. Синдром обычно считается паранеопластическим, если костно-мышечная манифестация возникла одновременно или не более, чем за год (в некоторых исследованиях — два года) до обнаружения злокачественного новообразования. Лучшее доказательство причинности устанавливается ретроспективно, в том случае, когда возможно полностью устранить опухоль, а ревматические симптомы претерпевают полную ремиссию.
Исходя из этих соображений будет представлен обзор клинических характеристик и текущего патофизиологического понимания различных форм паранеопластического полиартрита, миозита, ассоциированного с раковыми опухолями, паранеопластического васкулита, гипертрофической остеоартропатии и остеомаляции, вызванной опухолью. Для других ревматических расстройств, таких как ревматическая полимиалгия или болезнь Стилла взрослых, потенциальная связь с лежащим в основе злокачественным заболеванием была признана недостаточно сильной, чтобы отнести их к истинным паранеоплазиям.
2. Паранеопластический артрит (ПА)
В прошлом было описано множество клинических случаев, а также их серий, в которых возникший de novo синовит с активным воспалением предшествовал или приводил к выявлению лежащей в основе злокачественной опухоли. Недавно была описана группа из 65 пациентов с ПА и их клинические и демографические характеристики сравнили с таковыми у 50 пациентов с впервые выявленным ревматоидным артритом (РА). Средний возраст начала паранеопластического артрита составил 50 лет, преобладание мужчин составило 65 %, что резко контрастирует с РA. Синовит обычно начинается как острый асимметричный (91 %) поли- (34 %), олиго- (48 %) или моноартрит (18 %) с высоким уровнем лабораторных маркеров воспаления. Диагностическая дилемма при ПА возникает из-за того, что 23 % пациентов имеют положительный результат исследования на ревматоидный фактор и 11 % на антитела против цитруллинированных белков (АЦЦП). Поэтому в отдельных случаях диагноз затруднен и часто единственным клиническим намеком на необходимость поиска опухоли остается несколько атипичное вовлечение суставов и плохой ответ на стандартную противоревматическую терапию, особенно на кортикостероиды. До сих пор не была выдвинута последовательная теория, способная объяснить патогенез. Только в одном случае рака почки ученым удалось определить клоны Т-клеток с идентичными реаранжировками рецепторов среди инфильтрировавших опухоль иммунных клеток и в синовиальных тканях, что указывает на кросс-реактивность злокачественных клеток и синовиальных антигенов при ПА. Недавно цитруллинированный виментин был признан важным опухолевым антигеном злокачественных опухолей эпителиального происхождения. Также был определен Т-клеточный иммунный ответ против раковых клеток, экспрессирующих цитруллинированный виментин, который запускал противоопухолевый ответ. Следовательно, по крайней мере некоторые формы ПА, особенно те, которые ассоциированы с положительным тестом на АЦЦП, могут быть основаны на иммунных ответах против цитруллинированных опухолевых антигенов.
3. Пальмарный (ладонный) фасциит и синдром полиартрита (Palmar fasciitis and polyarthritis syndrome, PFPAS)
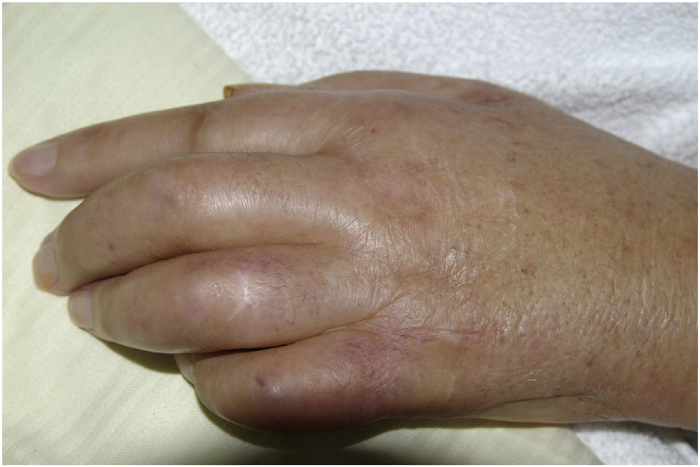
Рисунок 1. Сгибательная контрактура из-за ладонного фасциита у пациента с PFPAS и карциномой яичников.
4. Ремиттирующий серонегативный симметричный синовит с мягкими отеками
Этот артрит, начинающийся в пожилом возрасте, характеризуется симметричным отеком тыльной поверхности кистей и стоп, обычно не чувствителен к кортикостероидам и имеет хороший общий прогноз. Однако в объединенных данных из различных европейских и американских исследований частота злокачественных новообразований у таких пациентов составила 31 %. В японской группе из 33 пациентов с данным синдромом, у восьми развились раковые заболевания в течение двух лет от начала артрита. У этих пациентов наблюдалось значительное повышение уровня металлопротеиназы 3 в сыворотке. В целом, у любого пациента серонегативный симметричный синовит с мягкими отеками и плохим ответом на кортикостероиды следует считать красным флагом и склоняться к поиску скрытой злокачественной опухоли.
5. Панкреатический панникулит и полиартрит (ППП)
Полиартрит в сочетании с панникулитом, напоминающим узловатую эритему, неоднократно описывался у пациентов с панкреатитом и высоким уровнем сывороточной липазы. Такие же проявления можно наблюдать и при ацинарно-клеточном раке поджелудочной железы, который также приводит к чрезвычайно высоким концентрациям липазы в кровотоке (Рис. 2). Это вызывает обширные некротические поражения подкожной жировой клетчатки с окружающей воспалительной реакцией. Полиартрит чаще всего поражает голеностопные, коленные, лучезапястные и пястно-фаланговые суставы. В более чем 130 публикациях ППП ассоциируется с неблагоприятным прогнозом.
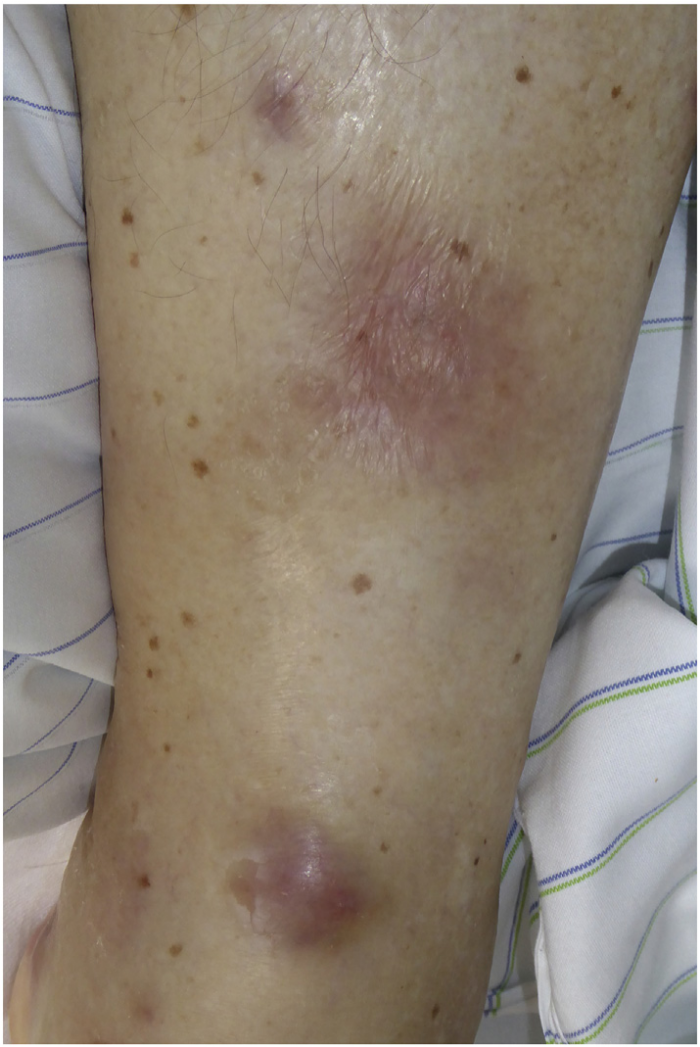
Рисунок 2. Узелковое воспаление подкожной клетчатки у пациента с панкреатическим панникулитом и полиартритом и ацинарно-клеточным раком поджелудочной железы.
6. Паранеопластический васкулит
Хотя для различных васкулитов сообщалось о временной связи со злокачественными заболеваниями, наиболее распространенной манифестацией является кожный лейкоцитокластический васкулит. Гематологические выступают причиной этого васкулита в более чем половине случаев, при этом наиболее частыми диагнозами являются миелодиспластический синдром и неходжкинские лимфомы. Среди солидных опухолей наиболее распространенными причинами паранеопластического васкулита являются рак легких, молочной железы и урогенитальные опухоли. В недавнем ретроспективном анализе 421 взрослого пациента с клинически явным или подтвержденным биопсией кожным васкулитом 16 (3,8 %) были паранеопластическими (9 гематологических, 7 солидных злокачественных новообразований). У четырех были дополнительные суставные симптомы, у двоих из них были желудочно-кишечные поражения или нефропатия. В таком контексте представляется интересным, что у взрослых пациентов с гистологически подтвержденной пурпурой Шенлейна-Геноха неоднократно были диагностированы злокачественные опухоли. При этом в качестве возможного патогенетического механизма предлагается отложение иммунных комплексов, содержащих опухолевые антигены и IgA.
7. Миозит, ассоциированный со злокачественными опухолями (Cancer-associated myositis, CAM)
В многочисленных эпидемиологических исследованиях проанализирована взаимосвязь между воспалительными заболеваниями мышц и злокачественными новообразованиями. Мета-анализ подтвердил, что дерматомиозит связан с неоплазией примерно в 24 % случаев. Стандартизованное отношение заболеваемости (SIR) варьирует от 3,8 до 7,7. Для полимиозитов ассоциация значительно слабее (SIR 1,7–2,2) и в случае клинических признаков overlap-синдрома при сочетании с другими заболеваниями соединительной ткани (например, интерстициальное поражение легких, феномен Рейно) риск наличия опухоли не возрастает. Аналогичным образом, наличие различных аутоантител, указывающих на заболевание соединительной ткани (таких как антисинтетазные, анти-Ro52 или антитела, ассоциированные с системным склерозом), снижает риск развития ассоциированного с опухолями миозита. Однако существует один тип аутоантител, четко связанный с данным миозитом. Сывороточные аутоантитела к внутриклеточному белку с массой 155 кДа (anti-p155) были первоначально описаны при ювенильном дерматомиозите, но также обнаружены у одного из шести взрослых пациентов с дерматомиозитом. Из этих взрослых пациентов с анти-p155 антителами у 65 % злокачественное заболевание развилось в течение трех лет после начала миозита. Эта связь была подтверждена в ряде других групп с миозитом. В дальнейшем аутоантиген p155 идентифицировали как промежуточный фактор транскрипции-1γ (TIF-1γ), член семейства белков, участвующих в различных функциях (убиквитинирование опухолевого супрессора р53, апоптоз), связанных с канцерогенезом. Таким образом, противоопухолевый иммунный ответ может приводить к образованию антител против TIF-1γ и способствовать развитию ассоциированного с опухолями миозита путем перекрестной реакции с тканевыми антигенами мышц. Еще одно аутоантитело (анти-MJ), которое связывает белок ядерной матрицы NXP2, было описано у пациентов с CAM, но число пациентов все еще слишком мало, чтобы уверенно делать выводы.
8. Гипертрофическая легочная остеоартропатия (ГЛО)
ГЛО, или синдром Мари-Бламбергера, представляет собой классическую костно-мышечную паранеоплазию и часто описывается в ревматологической литературе. Синдром характеризуется двумя отличительными симптомами: одним из них является утолщение дистальных фаланг пальцев рук и/или пальцев ног в виде барабанных палочек, а другой — воспалительный пролиферативный периостит, вызывающий костные и суставные боли, а иногда и синовит с выпотом в полости сустава. Преобладающими локализациями являются большеберцовая и малоберцовая кости, коленные и голеностопные суставы (Рис. 3). Это периостальное воспаление вызывает активацию остеобластов, что легко обнаруживается благодаря усиленному поглощению контраста при остеосцинтиграфии и оссификации надкостницы вдоль трубчатых костей при обычной рентгенографии. При ретроспективном анализе частота ГЛО при первичном раке легкого была близка к 1 %, однако ГЛО иногда также может возникать и при других типах злокачественных новообразований (преимущественно внутригрудных). Из-за характерной акральной активации фибробластов и периостальной активации остеобластов этот синдром первоначально считался вариантом акромегалии. Сегодня стало ясно, что тромбоцитарный фактор роста (PDGF) или фактор роста эндотелия сосудов (VEGF), продуцируемые опухолевыми клетками, могут способствовать развитию ГЛО.
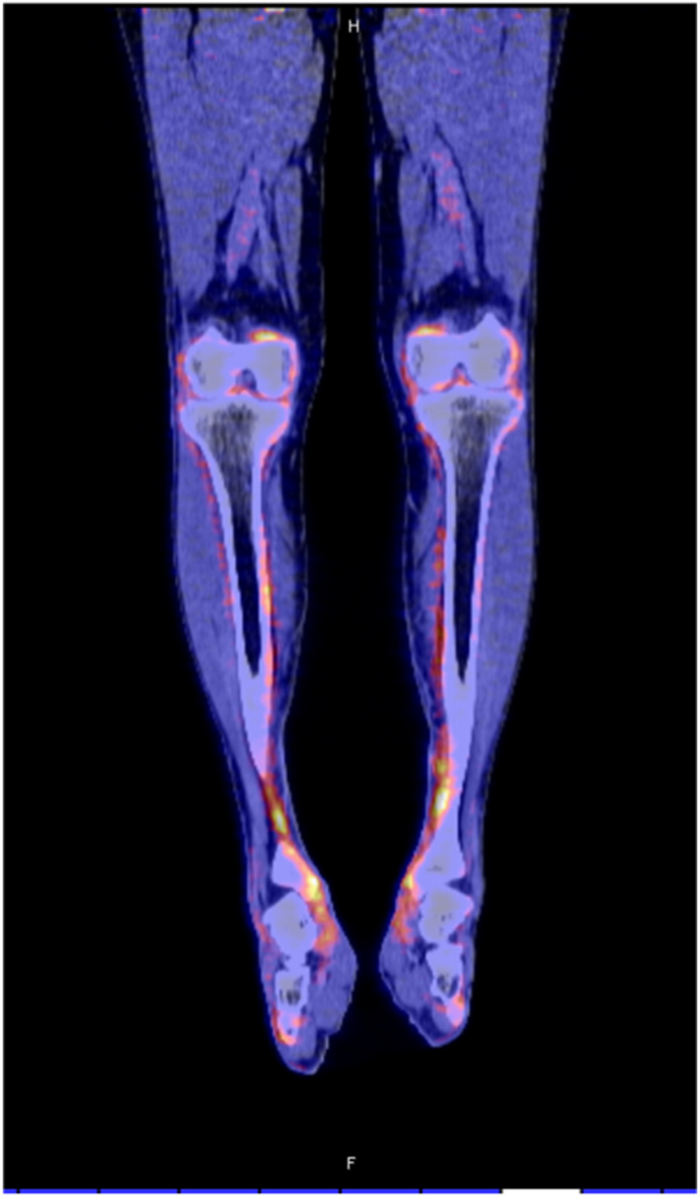
Рисунок 3. ПЭТ КТ показывает значимое поглощение 18 F-флюородеоксиглюкозы вдоль контуры большеберцовой кости у пациента с ГЛО и аденокарциномой бронхов.
9. Опухоль-индуцированная остеомаляция
Паранеопластическая остеомаляция клинически неотличима от других форм остеомаляции с прогрессирующей костной болью, спонтанными переломами, мышечной слабостью и усталостью. Биохимическая картина состоит из гипофосфатемии, гиперфосфатурии, нормального уровня кальция и паратиреоидного гормона, нормального или сниженного уровня кальцитриола и повышенной щелочной фосфатазы. Причиной дисбаланса в фосфатно-кальциевом обмене является значимая потеря фосфата почками из-за высоких концентраций циркулирующего фактора роста фибробластов 23 (FGF23, фосфатонин). FGF23 ингибирует реабсорбцию фосфата в проксимальных канальцах и подавляет дифференцировку остеобластов и минерализацию матрикса в кости. В большинстве случаев FGF23 продуцируется мезенхимальными опухолями (смешанный соединительнотканный вариант), опухолями с другими гистологическими типами (гемангиоперицитома, гигантоклеточная опухоль, остеосаркома) —значительно реже. Из 300 случаев опухоль-индуцированной остеомаляции внутрикостная опухоль была обнаружена в 40 % случаев, в 55 % новообразование было в мягких тканях. Только 8 % опухолей были злокачественными. Успешная локализация и удаление новообразования обычно приводят к полному устранению всех симптомов.
10. Заключение
Костно-мышечные паранеоплазии имеют важное клиническое значение по ряду причин: они часто предшествуют другим клиническим проявлениям новообразований и могут способствовать своевременной диагностике и потенциальному излечению от злокачественного заболевания. После успешного удаления злокачественных клеток паранеопластические симптомы обычно стихают, но повторное появление симптомов со стороны опорно-двигательного аппарата может указывать на рецидив или метастазирование, хотя клинически это не является надежным критерием. Паранеопластические симптомы также могут оказывать значительное влияние на качество жизни, заболеваемость и смертность пациентов с опухолями. В последние годы выяснены некоторые из основных механизмов паранеопластических синдромов, что улучшает наше понимание патогенеза ревматических и неопластических заболеваний.
*Импакт фактор за 2018 г. по данным РИНЦ
Журнал входит в Перечень рецензируемых научных изданий ВАК.
Читайте в новом номере
Паранеопластический артрит относится к паранеопластическим реакциям – неонкологическим заболеваниям и синдромам, возникающим в организме под влиянием опухолевого роста. Причем этот рост происходит не вследствие прямого локального действия неоплазмы или ее метастазов на органы и ткани либо побочного действия химиотерапии и сопутствующих инфекций, а в результате влияния на метаболизм, иммунную, эндокринную и другие системы организма.
В целом тот или иной паранеопластический синдром диагностируют у 7–10% больных со злокачественными новообразованиями. Связь злокачественных новообразований с паранеопластической реакцией подтверждается быстрой регрессией или полным исчезновением последней после радикального удаления опухоли и появлением вновь тех же ревматических симптомов при рецидиве неоплазмы или метастазировании [1].
Паранеопластические ревматические реакции возникают преимущественно при низкодифференцированных злокачественных новообразованиях эпителиального происхождения (рак различной локализации) и опухолевом поражении иммунной системы (тимомы, лимфомы). Ревматические паранеопластические синдромы (РПНС) часто сочетаются с другими органными и системными паранеопластическими проявлениями. Наиболее часто РПНС сопровождают бронхогенный рак легкого, рак молочной железы, нефрокарциному, рак яичников, предстательной железы, матки, реже – рак пищевода, поджелудочной железы, яичек, надпочечников [2].
У разных больных один и тот же РПНС может быть признаком опухоли различной локализации и неодинакового морфологического строения и, наоборот, при опухолях одной и той же локализации и сходного морфологического строения могут быть сходные ревматические проявления. Более того, у одного и того же больного последовательно возникающие на протяжении жизни (метахронные) опухоли разной локализации способны вызывать различные РПНС. Для рецидивирующих и метастазирующих опухолей характерна однотипность ревматических симптомов и исходной опухоли [3].
Неопластический процесс может стать причиной как острой, так и хронической воспалительной реакции с патологическим изменением соединительной ткани и сосудов в различных органах и системах. Спектр РПНС самый разнообразный – от локальной (в виде артралгии, артрита) до системной воспалительной реакции. В одних случаях они развиваются одновременно с неопластической трансформацией, в других – на фоне уже имеющегося опухолевого процесса, иногда предшествуют возникновению его местных симптомов за несколько месяцев и даже лет [4].
В патогенезе паранеопластических реакций могут принимать участие:
- иммунные реакции;
- прямое токсическое действие опухолевых субстанций;
- обменные нарушения, вызываемые опухолью: гиперкальциемия, гиперурикемия, потребление растущей опухолью компонентов, необходимых для нормального функционирования и структурной целостности здоровых тканей;
- эктопическая продукция гормонов и гормоноподобных субстанций, например адренокортикотропного или антидиуретического гормона, рилизинг-фактора, гормона роста, паратгормона, инсулиноподобного фактора роста, эритропоэтина;
- активация латентной вирусной инфекции, роль которой не исключается в развитии ревматических воспалительных реакций у больных со злокачественными новообразованиями [4, 5].
Обсуждается также роль общности этиологических факторов и генетической предрасположенности в развитии ревматических заболеваний и неопластического процесса, по меньшей мере опухолевых заболеваний иммунной системы, в пользу чего свидетельствуют данные о трансформации синдрома Шегрена в В-клеточную лимфому [6, 7].
Определенную роль в развитии РПНС, вероятно, играет непосредственное действие биологически активных веществ, выделяемых опухолевыми клетками. Полагают, что иммунологические сдвиги в организме могут быть на самой ранней стадии злокачественной трансформации тканей, когда новообразование ввиду незначительного размера при исследовании еще не определяется. Описаны злокачественные образования у больных, в течение многих лет страдавших хроническими ревматическими воспалительными заболеваниями, например, ревматоидным артритом или системными заболеваниями соединительной ткани. Считается, что эти случаи могли быть связаны с длительной предшествующей иммуносупрессивной терапией, развившимися в результате ревматического воспаления фиброзом и эпителиальной перестройкой органов, а также генетической предрасположенностью к заболеваниям обоих типов.
Клинические проявления РПНС весьма разнообразны. Поражение суставов у онкологических больных иногда проявляется лишь упорной артралгией, которая в ряде случаев сочетается с тендинитом, оссалгией и миалгией. В других случаях возникает манифестный артрит, механизм развития которого и клиническая картина у разных больных могут быть неодинаковыми.
Чаще возникает артрит, обусловленный иммунным синовитом. При этом клиническая картина суставного синдрома может напоминать таковую при ревматоидном артрите, реактивном артрите. В первом случае развивается симметричный полиартрит мелких суставов кистей и стоп, во втором – асимметричный олиго- или моноартрит крупных суставов преимущественно нижних конечностей. У некоторых больных наблюдаются ревматоидные узелки и ревматоидный фактор в сыворотке крови, а при затяжном течении артрита – эрозивные изменения суставных поверхностей эпифизов. Изредка РПНС протекает с поражением позвоночника по типу анкилозирующего спондилоартрита. Воспалительные изменения суставов, в т. ч. возникающие раньше манифестации злокачественного новообразования, сопровождаются общей интоксикацией, увеличением СОЭ, повышением острофазовых показателей [9].
В большинстве случаев причиной паранеопластического синдрома Мари – Бамбергера является рак легких, реже – другие интраторакальные опухоли, в частности доброкачественные новообразования легких: мезотелиома плевры, тератома, липома средостения. Изредка синдром встречается при раке ЖКТ, лимфоме и лимфогранулематозе с метастазами в лимфатические узлы средостения. Иногда гипертрофическая остеоартропатия бывает единственным проявлением РПНС. При этом помимо основного синдрома наблюдаются симптомы общей интоксикации, нарастающее исхудание, значительное увеличение СОЭ [1, 3, 10].
У некоторых больных паранеопластический артрит сочетается с апоневрозитом – узелковым утолщением ладонного апоневроза и болезненной сгибательной контрактурой пальцев, напоминающей таковую при системной склеродермии. Сходство с системной склеродермией придает также наличие типичного для данного заболевания синдрома Рейно.
Помимо паранеопластического артрита иммунного генеза у больных со злокачественными новообразованиями возможно развитие моно- или олигоартрита вследствие метастатического поражения синовиальной оболочки опухолевыми клетками либо вторичной подагры на фоне гиперурикемии в результате быстрого распада опухоли под влиянием цитостатиков.
У некоторых больных с онкологическими заболеваниями наряду с поражением суставов наблюдаются экстраартикулярные паранеопластические ревматические проявления: лихорадка неправильного типа, не поддающаяся терапии антибиотиками и глюкокортикоидами, лимфаденопатия, гепато- и спленомегалия, выпотной серозит (плеврит, перикардит), миопатия, периферическая нейропатия, энцефалопатия, узловатая эритема, рецидивирующая крапивница, геморрагическая сыпь, панникулит, синдром Стивенса–Джонса, поражение слизистых оболочек, выраженное увеличение СОЭ, гипергаммаглобулинемия, повышение в крови уровня циркулирующих иммунных комплексов, наличие антинуклеарных антител, LE-клеток, ревматоидного фактора, анемия, лейкопения и тромбоцитопения [1, 2, 11].
Диагностика паранеопластического артрита и других РПНС нередко трудна. Вместе с тем определенные признаки, выявляемые у больных с ревматическими симптомами и синдромами, должны вызвать у врача-онколога настороженность. К числу таких признаков относятся:
- возникновение ревматической патологии у лиц старше 50 лет, т. е. в более позднем возрасте, чем это характерно для большинства ревматических заболеваний, либо, напротив, появление в молодом возрасте признаков болезни Хортона, ревматической полимиалгии, свойственных пожилым и старикам;
- отсутствие полового деморфизма, типичного для многих ревматических заболеваний;
- острое или подострое течение артрита;
- несоответствие тяжести артрита общему тяжелому состоянию больного и высоким показателям активности воспалительного процесса;
- лихорадка, устойчивая к лечению антибактериальными и противовоспалительными препаратами;
- отсутствие отдельных клинических и лабораторных признаков, типичных для того или иного ревматического заболевания;
- упорное течение артрита, нередко опережающее клиническую манифестацию злокачественного образования;
- появление новых, не свойственных данному ревматическому заболеванию симптомов, обусловленных локальным ростом опухоли или развитием ее метастазов [11, 12].
Существенную роль в постановке диагноза играют полноценное объективное обследование, а также результаты инструментальных и лабораторных тестов.
Необходимо учитывать, что у онкологических больных иногда возникают поражения внутренних органов неревматического генеза: бронхоспастический синдром, неинфекционный эндокардит клапанов сердца, тромбоэмболии ветвей легочной артерии, рецидивирующий мигрирующий тромбофлебит, нефротический синдром, тромбоцитопеническая пурпура. В некоторых случаях, чаще при опухоли легкого и почки, наблюдаются признаки эктопической гормональной активности опухолей, в частности акромегалия, гинекомастия, галакторея, синдром Иценко–Кушинга. Может быть также паранеопластический дерматоз, возникновение которого у лиц старше 40 лет в большинстве случаев указывает на наличие злокачественного новообразования. К числу таких дерматозов относятся:
- черный акантоз;
- кольцевидная эритема Гаммела;
- акрокератоз Базе;
- гипертрихоз пушковых волос;
- приобретенный ихтиоз;
- кольцевидная эритема Дарье.
Метастатическое поражение костного мозга, особенно на фоне раковой интоксикации, может приводить к гипопластической анемии, нередко в сочетании с лейкопенией и тромбоцитопенией [5, 7].
Таким образом, РПНС – это актуальная проблема, требующая со стороны врача внимания к пациенту, знания клиники, возможностей диагностики ревматических паранеопластических проявлений.
Только для зарегистрированных пользователей
Читайте также:


