Внутриутробная инфекция плода и новорожденного цитомегалия токсоплазмоз
3 февраля 2017, 10:52 Эксперт статьи: Блинова Дарья Дмитриевна 0 833
Внутриутробным токсоплазмозом называют серьезный недуг, который возникает при инфицировании организма возбудителем Toxoplasma gondii. Врожденный токсоплазмоз достаточно распространенный недуг, количество больных новорожденных составляет примерно 1—5%. Само инфицирование происходит еще в утробе матери. Чаще заражение происходит в третьем триместре беременности, но самым опасным является первый триместр, когда происходит закладка жизненно важных органов малыша.
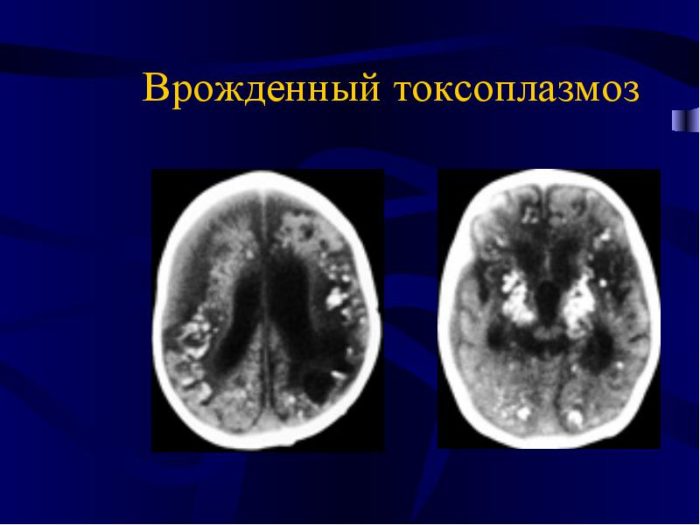
Что это такое?
Токсоплазмозом у новорожденного называют заражение ребенка внутриклеточным паразитом токсоплазмой. Это происходит при контакте матери в период вынашивания ребенка с домашними животными-носителями описываемого недуга. Инфекция крайне опасна, так как появляются некрозы с фиброзами, происходит кальцификация тканей зараженного организма.
Если внутриутробным токсоплазмозом будущая мама заразилась на начальном сроке вынашивания ребенка, то, скорее всего, произойдет самопроизвольное прерывание беременности. Редко получается избежать выкидыша, но ребенок в таком случае рождается с серьезными отклонениями. Поэтому акушеры практически в один голос рекомендуют беременность прерывать.
Современная медицина, конечно, на сегодняшний день способна вылечить многие заболевания. Но она не творит чудеса, и вылечить врожденный токсоплазмоз, приобретенный в первые недели беременности, невозможно. Когда заражение произошло в последний триместр беременности, то ребенок рождается раньше предварительной даты родов — примерно на 38-й неделе.
Главной причиной заболевания матери и ее плода являются контакты с домашними животными, особенно с кошками. К другим путям заражения относят:
- Присутствие в рационе зараженных продуктов, которые не прошли нужную термическую обработку. Особенно опасна свинина.
- Заражение от распространителей инфекции. Опасны такие насекомые, как комары или мухи.
- Плохая гигиена беременной. Например, когда после уборки кошачьего туалета или контакта с землей, где ходит домашнее животное, будущая мама не помыла руки. Тогда попадание паразитов в организм неизбежно.
- Через кровь или открытую рану (при переливании крови или пересадки органов). К счастью, процент таких заражений крайне мал.
Обычно врожденный токсоплазмоз у новорожденных начинает проявляться уже в первые месяцы жизни крохи. Одним из распространенных симптомов внутриутробной инфекции у новорожденных является наличие проблем с глазами, вплоть до развития слепоты. Присутствуют патологии центральной нервной системы, не полностью развиваются головной и спинной мозг. Происходит дисфункция внутреннего уха, которая сопровождается проблемами со слухом. Часто при внутриутробном токсоплазмозе наблюдается отклонения в физическом здоровье ребенка: отставание в росте в сравнении со сверстниками, ухудшение аппетита либо его полное отсутствие.
Бывают случаи, что врожденный токсоплазмоз не проявляется на ранних этапах жизни у грудного ребенка, а происходит это уже в подростковом возрасте. Но зачастую в первые недели развития крохи появляются такие симптомы:
- сыпь на коже;
- повышенная температура;
- высокое внутричерепное давление;
- признаки заболевания печени;
- проявления дисфункции других жизненно важных органов.
В будущем к этим проявлениям внутриутробного токсоплазмоза добавляются отставание в психическом развитии, плохая речь, слабоумие, эпилепсия и другие. Именно поэтому крайне важно провести своевременную диагностику и назначить правильную лечебную терапию. Многим больным с этим диагнозом часто назначается химиотерапия.
В чем опасность, и какие последствия?
Врожденный и приобретенный токсоплазмоз несет в себе массу проблем со здоровьем у новорожденных и детей постарше. Например:
Диагностика
Диагностировать заболевания можно внутриутробно и/или уже в новорожденного. Внутриутробную диагностику именуют дородовой либо пренатальной. В этом случае происходит забор крови плода, а также амниотической жидкости. Дополнительно проводится исследование на наличие антител на токсоплазмы у матери и ее ребенка. С целью изучения состояния нервной системы у еще не рожденного малыша назначается УЗИ.
После рождения малыша у врачей больше возможностей для определения/подтверждения диагноза и своевременного лечения. Проводятся такие исследования:
- анализ пуповинной крови на наличие антител к инфекции;
- компьютерная томография и МРТ, проводимые для изучения деятельности головного мозга;
- обследование у невролога;
- консультация офтальмолога;
- комплекс анализов на предрасположенность к TORCH-инфекциям.
Лечение внутриутробного токсоплазмоза
При повторной беременности нет риска заражения токсоплазмозом, так как организм вырабатывает иммунитет к этому недугу.
Можно ли предупредить?
Важный и актуальный вопрос, так как внутриутробная инфекция несет в себе массу отрицательных последствий: существует ли способ предупреждения заражения? Ответ утвердительный. Для этого женщинам, которые планируют вынашивать ребенка, или уже находятся в интересном положении рекомендуется сдать анализы на предрасположенность к TORCH-инфекциям. Самыми уязвимыми считаются обладатели домашних животных. Для профилактики стоит периодически проверять питомцев на наличие паразитов, а систематически давать таблетки от глистов. А еще лучше ограничить общение с питомцами, если только женщина не жила в непосредственной близости с кошками (в этом случае у нее вырабатывается иммунитет).
Следует обратить внимание на рацион. Употреблять только термически обработанные продукты. Придерживаться правил личной гигиены, мыть руки с антибактериальным мылом, особенно после контакта с животными, кушать только хорошо очищенные фрукты и овощи. И при малейших проявлениях симптомов заболевания у беременной нужно обратиться к доктору, который назначит эффективное лечение. Это поможет минимизировать риски заражения плода.
[youtube.player]Одна из причин, почему будущие мамы не любят поездок в общественном транспорте и вообще больших скоплений людей, — опасность инфекции для ребеночка в животике. Согласно медицинской статистике, не менее чем у 10% новорожденных действительно можно с помощью микробиологических, вирусологических и иммунологических исследований доказать инфицирование во время гестации, либо при прохождении по родовым путям. Но лишь 10% таких детей имеют клинические патологические проявления в периоде новорожденности. По другим данным, эти цифры даже меньше 1–2%.
ПРИЧИНЫ И СЛЕДСТВИЯ
Пути проникновения возбудителя к ребенку могут быть различными. До родов инфекционный агент попадает к плоду трансплацентарно(гематогенно) или через инфицированные околоплодные воды. Околоплодные воды могут быть инфицированы восходящим (из влагалища) и нисходящимпутем (из маточных труб), а также через околоплодные оболочки (при эндометрите, плацентите). Инфицирование при прохождении по естественным родовым путям называется контаминационным.
Инфекционный процесс у матери может протекать остро, субклинически с неспецифической симптоматикой и даже латентно (скрыто). Если говорить о непосредственном влиянии инфекционного агента на будущего ребенка, то характер поражения зависит от сроков инфицирования и вида возбудителя. В первый триместр беременности происходит закладка и формирование всех органов плода. В этот период он максимально чувствителен к повреждающим влияниям. Необходимость внимательно относиться к своему здоровью остается у будущей мамы и в двух следующих триместрах: формообразовательный период мозга продолжается всю беременность, и этот важнейший орган уязвим до самого окончания гестации.
Внутриутробная цитомегаловирусная инфекция
Цитомегаловирус (ЦМВ) из группы герпес-вирусов проникает к плоду чаще гематогенным путем, но может иметь место и восходящий путь инфицирования. По зарубежным данным, среди беременных женщин, чувствительных к ЦМВ (то есть неиммунных) частота первичной инфекции составляет 1–4%, при этом передача ее плоду происходит приблизительно в 40% случаев. 10–15% инфицированных детей имеют клинически очевидную болезнь, но даже среди них у 10% в последующем отмечается нормальное развитие. Для успешного лечения необходимо знать, что поздние осложнения вероятны у такого же процента ребят без клинических проявлений вскоре после рождения.
Хотя это происходит много реже, но все же возможно развитие внутриутробной цитомегаловирусной инфекции и у женщин, инфицированных до беременности. Причиной тому может быть какой-то иммунодефицит, который не позволяет защитить плод от инфекционного процесса.
Сравнительно эффективным и безопасным методом лечения при цитомегалии считается лишь применение специфического антицитомегаловирусного иммуноглобулина. Существующий специфический противовирусный препарат Ганцикловир у новорожденных применяют лишь при жизнеугрожающем течении болезни. Специфическая профилактика цитомегаловирусной инфекции во время беременности пока не разработана.
Внутриутробная герпетическая инфекция
ВУИ может быть вызвана вирусами простого герпесаIи II типа, причем с последним связано 80–90% случаев заболевания. Вирус способен инфицировать плод гематогенным путем, восходящим (при герпесе гениталий) или контаминационным. Риск заражения вирусом герпеса II типа в момент родов по естественным путям при герпесе гениталий, возникшем у матери впервые во время беременности, — 40%, но лишь 8% — если у матери был рецидивирующий генитальный герпес до беременности (и в таком случае у ребенка риск неонатального герпеса — менее 0,5%).
Наблюдается положительный эффект лечения женщин с генитальным герпесом до беременности курсом специфической противогерпетической вакцинации. Если у будущей мамы есть клинические проявления генитального герпеса или доказано наличие вируса или его антигенов в родовых путях, то целесообразно родоразрешение с помощью планового кесарева сечения (до отошедших околоплодных вод).
При герпетической инфекции у новорожденных показана специфическая терапия как системная(Ацикловир или Видарабин), так и местная. Лечение значительно улучшает жизненный прогноз и снижает частоту тяжелых неврологических последствий.
Внутриутробная хламидийная инфекция
Хламидиоз гениталий — широко распространенная инфекция, передаваемая половым путем. Известно, что инфицированность хламидиями беременных женщин достигает 10–15%. Хламидии могут попадать к плоду восходящим путем или контаминационным — в родах. При внутриутробном инфицировании пороки развития не характерны, но возможны иные последствия. Поздние осложнения хламидиоза у детей не отмечаются.
Хламидии, обнаруженные в мазках из родовых путей, или доказанный иммунологически хламидиоз — показания для назначения будущей маме курсовой терапии антибиотиком Эритромицином после 12 недель беременности. Безусловно, целесообразно одновременно лечить и полового партнера.
Микоплазмы выявляются у беременных женщин в 20–50% случаев. Возможные пути инфицирования плода — гематогенный и восходящий. Степень риска инфицирования однозначно оценить трудно. Микоплазменное обсеменение рассматривают как проявление иммунологической недостаточности у ребенка. Считается, что микоплазмоз в период беременности может приводить к порокам развития у 15% инфицированных детей. С профилактической целью будущим мамам, в родовых путях которых обнаружены микоплазмы, проводится курс терапии Эритромицином и местное вагинальное лечение.
Внутриутробная уреаплазменная инфекция
Уреаплазмы (известные ранее как Т-микоплазмы) часто обнаруживают в половых путях мужчин и женщин и нередко у здоровых будущих мам (50–75% случаев по зарубежным данным). Однако выявлена связь между уреаплазменной инфекцией и недонашиванием беременности. Риск инфицирования плода составляет около 45%. Колонизация половых путей уреаплазмами у новорожденных происходит во время родов, эта инфекция гораздо реже встречается у детей, рожденных с помощью операции кесарева сечения. Уреаплазмы недолго сохраняются в половых путях ребенка, и в большинстве случаев дети свободны от них.
Токсоплазмы — паразитические простейшие, окончательным хозяином которых обычно являются кошки, промежуточным — многие млекопитающие и птицы. Кошки чаще всего и представляют источник инфекции для человека. Приобретенный токсоплазмоз чаще развивается при заражении алиментарным путем (с инфицированными пищевыми продуктами), а также через кожу.
Факт инфицирования неиммунных беременных женщин регистрируется в 7–8 случаях на 1000 будущих мам, а клинические признаки токсоплазмоза — у 1 из 1000. В большинстве случаев заражение женщины происходит незаметно и остается не выявленным. Легкая форма заболевания характеризуется в основном увеличением лимфатических узлов и температурной реакцией.
Внутриутробный путь инфицирования токсоплазмами — гематогенный. Если инфицирование женщины в первые 8 недель беременности приводит к поражению эмбриона, то беременность прерывается. При токсоплазмозе, перенесенном с 9 до 29 недель беременности, возможно прерывание беременности или формирование пороков развития у плода. При текущем инфекционном процессе у 85–90% внутриутробно инфицированных детей клинические проявления развиваются по окончании периода новорожденности.
Специфическая терапия должна быть проведена в каждом случае врожденного токсоплазмоза или внутриутробного инфицирования токсоплазмами, даже когда имеется субклиническое или латентное течение. В зависимости от варианта заболевания требуется различное по продолжительности лечение (максимальная длительность — до 1 года). При рано начатой терапии у детей даже с острым врожденным токсоплазмозом возможно нормальное развитие.
О профилактических мерах: поскольку алиментарный путь заражения токсоплазмами является основным, нужно тщательно мыть фрукты и овощи, пить только кипяченую воду. Будущей маме не стоит пробовать на вкус термически необработанный мясной фарш при приготовлении пищи. Во время беременности или незадолго до нее не следует заводить кошекили посещать семьи, где они есть.
Всем беременным не менее чем двукратно делают анализ на токсоплазмоз. При доказанной первичной инфекции назначается соответствующее лечение. И все же специфическое лечение во время беременности бывает необходимым крайне редко, а инфицирование токсоплазмами задолго до беременности ребенку, как правило, не угрожает.
Процент серопозитивных, то есть имеющих антитела к вирусу краснухи, женщин в детородном возрасте составляет 80–95%. В эпидемический период частота инфекции в период беременности — от 4 до 2000 случаев на 100000 родов. Внутриутробное инфицирование происходит гематогенным путем. Поражение на ранних сроках беременности может привести к ее прерыванию. Дети с пороками развития от числа инфицированных составляют до 10%. Врожденные пороки развития отмечаются у 50% новорожденных, если мать болела в 1-й месяц беременности; у 25–14% — на 2–3-м месяце, и у 3–8%, если болела позже.
При поражении в периоде новорожденности больной выделяет вирус до 1,5–2 лет, поэтому краснуха относится к группе медленных инфекций. У 2/3 детей врожденная краснуха проявляется в конце 1-го месяца жизни и позднее. Специфической терапии врожденной краснухи нет. В лечении используются препараты рекомбинантного интерферона и симптоматические средства.
Если беременная женщина имеет контакт с больным краснухой, ей рекомендуется обследование на наличие противокраснушных антител. Обнаружение антител указывает на то, что она серопозитивна и защищена от заражения. Если антитела не определяются, через 3–4 недели исследование повторяют и при появлении антител такую женщину следует считать больной краснухой, тогда как отрицательные результаты указывают на то, что заражения не произошло. Непростой вопрос о прерывании беременности может быть поставлен в случае возникновения клиники краснухи или очевидного контакта с больным краснухой в сочетании с наличием противокраснушных антител в первом триместре беременности.
Профилактика осуществляется иммунизацией серонегативных женщин до беременности живой ослабленной вакциной. Вакцинацию следует проводить не менее чем за 3 месяца до планируемой беременности. В случае более раннего наступления беременности излишне волноваться не стоит, хотя лучше этого избежать.
ЛЕЧЕНИЕ И ПРОФИЛАКТИКА
Для профилактики ВУИ особое значение имеет лечение мочеполовой инфекции у женщин детородного возраста до наступления беременности, соблюдение во время беременности элементарных санитарно-гигиенических правил, в том числе в половых отношениях, а также целенаправленная профилактика ВУИ. Ранняя диагностика и лечение ВУИ позволяют сохранить жизнь ребенку, но не во всех случаях дают возможность прогнозировать полное выздоровление.
Во многих случаях большую роль в переходе от инфицирования к болезни играют условия, в которые попадает после рождения инфицированный в родах ребенок. В целом, они и определяют состояние детского здоровья на всю жизнь. К благоприятным факторам относят постоянное совместное пребывание матери и ребенка, грудное вскармливание и раннюю выписку из родильного стационара, когда ко всему этому нет противопоказаний.
[youtube.player]Цель изучения темы:формирование профессиональныхкомпетенций по вопросам детских инфекционных болезней
и внутриутробных инфекций.
В результате изучения темы студент должен:
Уметь: пользоваться учебной литературой, сетью Интернетдля получения современной информации по изучаемой теме; работать с макро- и микропрепаратами; обосновывать харак-тер патологического процесса и его клинические проявления, принципы классификации болезней, понятия этиологии, па-тогенеза, морфогенеза, прогноза при менингококковой инфек-ции, скарлатине и дифтерии и внутриутробных инфекциях.
Владеть: навыками описания морфологических измене-ний, изучаемых по теме, макропрепаратов, микропрепара-тов, электронограмм; навыками оценки характера патологи-ческого процесса и его клинических проявлений на основа-нии макро- и микроскопических изменений в органах и тка-нях при менингококковой инфекции, скарлатине и дифте-рии и внутриутробных инфекциях.
Менингококковая инфекция- острая респираторная ин-фекционная болезнь, вызываемая менингококком, характе-ризующаяся широким диапазоном клинических проявлений - от бессимптомного бактерионосительства до сепсиса. Возбу-дитель - Neisseria meningitides. Менингококковая инфекция - строгий антропоноз. Путь передачи - воздушно-капельный от больного или бациллоносителя (20%). Может иметь эпидеми-ческий характер. Патогенез: микроорганизмы выделяют эндо-токсин, факторы проницаемости, пенетрируют через стенки сосудов, формируя периваскулярные зоны воспаления.
Формы: 1. Острый назофарингит- катаральное воспале-ние слизистой оболочки носа и глотки. У детей раннего воз-раста возбудитель к концу первых суток, преодолев гемато-энцефалический барьер, проникает в мягкие мозговые обо-лочки, вызывая серозное, а затем гнойное воспаление. 2. Ме-нингит - воспаление мягкой мозговой оболочки головно-го и спинного мозга. Поражение твердой мозговой оболоч-ки - пахименингит, мягкой и паутинной - лемтоменингит. По течению - острый, подострый и пролонгированный. По виду экссудата - серозный и гнойный. 3. Менингококковая септи-цемия - связана с бактериемией и эндотоксинемией, приво-дящих к эндотоксиновому шоку и развитию синдрома дис-семинированного внутрисосудистого свертывания. Харак-терно поражение сосудов микроциркуляции. У больных от-мечается сливная геморрагическая сыпь с локализацией на ягодицах, нижних конечностях и склерах, петехиальные кро-воизлияния в паренхиматозные органы, серозный менин-гит, серозные артриты, некротический нефроз. При разви-тии ДВС-синдрома - кровоизлияния в надпочечники (син-дром Уотерхауса-Фридерихсена). Исход: смертельный исход связан с развитием бактериального шока, острой почечной недостаточности, массивными кровоизлияниями.
Скарлатина- острое стрептококковое заболевание с пре-имущественным поражением зева, сопровождающееся рас-
пространенной экзантемой и общей интоксикацией. Возбу-дитель: бета-гемолитический стрептококк группы А. Забо-левание обычно встречается у детей в возрасте о 3 до 5 лет. Инкубационный период – 3 - 7 дней. Относится к воздушно-капельным антропонозам. Патогенез: эритрогенный токсин (токсическая фракция и аллергизирующая), микробная ин-вазия и аллергические реакции. Выделяют два периода скар-латины. Первый период занимает 1 – 2 недели и характери-зуется развитием первичного инфекционного комплекса: ка-таральная или некротическая ангина и лимфаденит шейных узлов. На 2-е сутки на туловище одновременно появляется мелкопапулезная сыпь, которая в дальнейшем заканчивается пластинчатым шелушением. По тяжести течения различают:
легкую, среднетяжелую и тяжелую формы. Тяжелая формаскарлатины может быть септической или токсикосептиче-ской. Осложнения первого периода скарлатины связаны с рас-пространением инфекции: гнойный отит, мастоидит, си-нусит, абсцесс мозга, лептоменингит, септикопиемия, флег-мона челюстно-лицевой области и шеи. Второй период скар-латины наступает на 3 - 4 неделе, его развитие связано саллергизацией организма по типу ГЗТ. Характерно развитие постстрептококкового гломерулонефрита, миокардита, ва-скулитов, синовитов и артритов.
Дифтерия- острое инфекционное контагиозное заболева-ние, характеризующееся формированием фибринозных пле-нок в дыхательных путях и глотке, а также токсическим по-вреждением миокарда, нервов и других тканей. Возбудитель - Corynebacterium diphteriae, выделяющая экзотоксин. Инку-бационный период - 3 - 10 суток. Болеют дети до 5 - 7 лет.
Источник заражения - больной, реконвалесцент (длитель-ность носительства - 2 - 7 недель), бактерионоситель. Эпи-демиологическую опасность представляют больные со стер-тыми и атипически протекающими случаями болезни. Па-тогенез: экзотоксин обладает некротическим и вазопарали-
тическим действием. Местное поражение при дифтерии ха-рактеризуется развитием первичного инфекционного ком-плекса: первичного аффекта (фибринозное воспаление сли-зистой оболочки в области входных ворот), лимфангит, лим-фаденит. Формы дифтерии по локализации: дифтерия зева, дифтерия дыхательных путей, дифтерия носа, реже - глаз, кожи и ран. Дифтерия зева и миндалин, помимо массивногоместного действия, оказывает и общее токсическое, так как фибринозная пленка (дифтеритическая) на многослойном эпителии длительно не отторгается и способствует всасыва-нию токсина. На слизистых оболочках, покрытых однослой-ным цилиндрическим эпителием (гортань, трахея, бронхи), развивается крупозное воспаление, пленка отторгается легко и может способствовать механической закупорке просвета. Это может привести к развитию истинного крупа (удушье). Закупорка мелких бронхов способствует развитию очаговой пневмонии. При дифтерийной интоксикации поражаются: нервная система, сердечно-сосудистая система и надпочеч-ники. Поражение нервной системы: характерно поражениесимпатических узлов и периферических нервов. Поражение языкоглоточного нерва приводит к параличу мягкого неба и нарушению глотания, гнусавости голоса. Микроскопическое исследование выявляет очаговую демиелинизацию, воспали-тельные инфильтраты, нарушение кровообращения и дене-генеративные изменения. Паренхиматозный неврит приво-дит к развитию позднего паралича сердца. Токсический па-ренхиматозный миокардит, развившийся в начале 2-й неде-ли заболевания, часто заканчивается острой сердечной не-достаточностью и смертью от раннего паралича сердца. При микроскопии находят жировую дистрофию и очаги миоли-за кардиомиоцитов. Поражение надпочечников может при-вести к коллапсу.
Цитомегалия.Возбудитель - цитомегаловирус, относя-щийся к бета- группе вирусов герпеса. Пути инфицирования:
восходящая инфекция (трансцервикально) или гематогенная
Токсоплазмоз- паразитарное заболевание из группы ан-тропозоонозов. Возбудитель - Toxoplasma gondii. Источни-ки заражения людей - кошки и свиньи, грызуны. Заражение алиментарным путем, чаще - через загрязненное мясо. Пато-генез: размножаются в клетках РЭС, образуют псевдоцисты,выделяют токсин, разрушающий клетки и вызывающий ал-лергическую перестройку организма. Токсоплазмы могут об-разовывать и истинные цисты, сохраняя жизнеспособность годами, находясь в клетках головного мозга, глаза, сердца и других органов. Формы: приобретенная и врожденная. Врож-денная форма возникает в результате заражения через пла-центу при обострении заболевания у матери в период гене-
рализации инфекции. В зависимости от периода заражения плода различают 3 основные формы.
1. При раннем внутриутробном инфицировании плода в период от начала 9 до 29 недели беременности - ранняя фе-топатия.Ребенок рождается с явлениями внутриутробно про-текающего менингоэнцефалита и задержкой формирования и дифференцировки головного мозга, истинное недоразвитие глаза (анофтальмия, микрофтальмия, колобомы, катаракты).
2. Поздняя фетопатия - в период с 29 недели беременно-сти до начала родов.Сразу после родов у ребенка наблюда-ется картина альтеративно-продуктивного менингоэнцефа-лита и развитие гранулематозного воспаления. Поражение глаз характеризуется развитием острых очагов некробиоза с реактивным воспалением в сетчатке и в сосудистом трак-те. Образуются гранулемы - продуктивно-некротический эн-дофтальмит.
3. При генерализации токсоплазмоза незадолго до ро-дов или во время родов, ребенок рождается с явлениями общего инфекционного заболевания.Кроме поражения го-ловного мозга, наблюдаются гепатоспленомегалия, желтуха, язвенные поражения кишечника, миокардит, интерстици-альная пневмония.
ликулярно, проникают в альвеолоциты, затем в лимфоузлы и в кровеносное русло, с последующей генерализацией и пора-жением других органов и ЦНС. Морфологически характери-зуется нарушением кровообращения во внутренних органах: внутрисосудистой коагуляцией, тромбообразованием, ге-моррагиями, отеком, дистрофией и некрозом паренхиматоз-ных элементов, наличием лимфолейкоцитарной инфильтра-ции, гиперплазией и плазматизацией лимфатических узлов. Выделяют респираторный и нереспираторный микопламоз.
Листериоз- острое инфекционное заболевание, протека-ющее в виде сепсиса с поражением нервной системы, лим-фатических узлов, печени и селезенки. Распространение по-всеместное, относится к антропозоонозам. Заражение проис-ходит через инфицированных животных контактным путем, алиментарным при употреблении в пищу загрязненных про-дуктов. Входные ворота - ротоносоглотка, конъюнктива глаза и ЖКТ. В ранней детской смертности на долю листериоза при-ходится 0,15 - 4%. На беременных женщин и новорожденных приходится 75% всех зарегистрированных случаев. Зараже-ние плода чаще с 4 – 5-го месяца беременности и в более позд-ние сроки. Часты преждевременные роды и аборты. Внутриу-тробный путь заражения – единственный при передаче забо-левания от человека человеку (трансплацентарный, аспира-ционный). Патоморфологическую основу листериоза состав-ляет гранулематозный процесс с образованием листериом в печени, легких и других органах. Клинико-морфологические формы: ангиозно-септическая (катаральная и некротическаяангина, возможна генерализация процесса), нервная (у де-тей в возрасте до 1 месяца с развитием менингита, энцефа-лита, абсцессов мозга, и поражением периферической нерв-ной системы), глазо-железистая (конъюнктивит, лимфаде-нит), септико-гранулематозная. Для плодов и новорожден-ных характерна септико-гранулематозная форма. Для этой формы характерен генерализованный гранулематозный про-
цесс с образованием листериом в различных органах и тка-нях. При распространении инфекции на головной мозг воз-никает гнойный менингит и гидроцефалия. В легких развива-ется гнойно-геморрагическая пневмония.
КОНТРОЛЬНЫЕ Вопросы
1. Особенности течения инфекционного процессав раз-личных возрастных группах. Понятие о реактивности орга-низма и общей морфологии инфекционного процесса. Бо-лезни, вызываемые бактериями. Общая морфологическая характеристика. Своеобразие инфекции в связи с особенно-стями возбудителя и способом его передачи.
2. Менингококковая инфекция:
а) этиология, пути заражения и механизм распространения; б) современные учения о патогенезе менингококковой
инфекции; в) основные морфологические особенности менингокок-
ковой инфекции, с учетом различных форм заболевания; г) менингококковый назофарингит, частота его развития
с учетом инвазии менингококка в слизистую носоглотки; д) гнойный менингит, связь его развития с незрелостью
гематоэнцефалического барьера; е) менингококцемия, зависимость ее развития от состоя-
ния иммунной реактивности организма; ж) исходы и осложнения менингококковой инфекции с
учетом форм заболевания, причины смерти.
3. Скарлатина:
а) характеристика болезни, этиология и патогенез, частота заболевания в различных возрастных группах;
б) патологическая анатомия первого периода скарлати-ны: раскройте морфологию скарлатинозной ангины, распро-странение инфекции и общие изменения в тканях;
в) охарактеризуйте токсическую форму болезни;
г) морфологическая картина септической и токсико-септической форм заболевания;
д) патологическая анатомия второго периода скарлатины, особенности возникновения и течения;
е) осложнения и причины смерти при тяжелом течении скарлатины.
4. Дифтерия:
а) определение болезни, этиология и патогенез, клинико-анатомические формы болезни;
в) общие изменения в тканях при дифтерии, охарактери-зуйте процессы в нервной, сердечно-сосудистой системах, в надпочечниках и свяжите их с клиническими проявлениями болезни.
5. Внутриутробные инфекции. Цитомегалия:
а) определение болезни, этиология и патогенез, пути про-никновения инфекции в организм плода;
б) клинико-морфологическая характеристика острой и хронической форм врожденной цитомегалии;
в) цитомегаловирусный метаморфоз клеток паренхима-тозных органов, анатомические единицы, где преимуще-ственно локализуются цитомегалические клетки.
6. Токсоплазмоз:
а) определение болезни, этиология и патогенез, диагно-стика врожденного токсоплазмоза;
б) особенности внутриутробного инфицирования в зави-симости от срока беременности, исходы;
в) поражения головного мозга и других органов при раз-личных формах врожденного токсоплазмоза;
г) осложнения токсоплазмоза.
7. Микоплазмоз:
а) морфологические и клинические особенности мико-плазменной инфекции, пути проникновения в организм;
б) клинико-морфологическая характеристика респира-торного микоплазмоза, диагностика;
в) клинико-морфологическая характеристика внереспи-раторного поражения органов: легких, печени, почек, ЦНС, сосудов;
г) урогенитальные микоплазмы, поражение органов при острой и хронической формах;
д) роль генитальных микоплазм в генезе врожденных по-роков ЦНС, особенности врожденного микоплазмоза плода
8. Листериоз:
а) определение болезни, этиология и патогенез, диагно-стика врожденного листериоза;
б) клинико-морфологическая характеристика формы ли-стериоза:
в) особенности течения септико-гранулематозной формы листериоза у плода и новорожденного, осложнения, исход.
РЕКОМЕНДУЕМАЯ ЛИТЕРАТУРА
Основная литература
1. Пальцев, М. А. Патологическая анатомия: Учебник. – Т. 1, 2 (ч. 1, 2). / М. А. Пальцев, Н. М. Аничков. – М.: Медицина, 2005. – Т. 1. – 304 с., т. 2, ч. 1. – 512 с., ч. 2. – 504 с.
2. Пальцев, М. А. Руководство к практическим заня-тиям по патологической анатомии. / М. А. Пальцев, Н. М. Аничков, М. Г. Рыбакова. – М.: Медицина, 2002. – 896 с.
3. Пальцев, М. А. Патология: Учебник. В 2 т. / М. А. Паль-цев, В. С. Пауков. – М.: ГЭОТАР-Медиа, 2008. – Т. 1. – 512 с., т. 2. – 488 с.
4. Пальцев, М. А. Атлас по патологической анатомии. – 2-е изд. / М.А. Пальцев, А. Б. Понамарев, А. В. Бересто-ва. – М.: Медицина, 2005. – 432 с.
5. Струков, А. И. Патологическая анатомия: Учебник. – 5-е изд., стер. / А. И. Струков, В. В. Серов. – М.: Литте-ра, 2010. – 848 с.
Дополнительная литература
1. Пальцев, М. А. Руководство по биопсийно-секцион-ному курсу. Учебное пособие для студентов мед. вузов. –
2 изд., стер./ М. А. Пальцев, В. Л. Коваленко,
Н. М. Аничков. – М.: Медицина, 2004. – 256 с.
2. Патологическая анатомия. Атлас. / под ред. О. В. За-ратьянц. – М.: ГЭОТАР-Медиа, 2010. – 472 с.
Последнее изменение этой страницы: 2016-06-26; Нарушение авторского права страницы
[youtube.player]Читайте также:


