Болезнь Беста (вителлиформная макулярная дистрофия)
Добавил пользователь Alex Обновлено: 27.01.2026
Болезнь Беста — относительно редкая форма макулярной дистрофии, характеризующаяся двусторонним стадийным течением. Описаны случаи формирования хориоидальной неоваскулярной мембраны (ХНМ) в процессе развития заболевания, однако истинная частота данного осложнения и тактика ведения таких пациентов не определены. В последние годы в клиническую практику активно внедряется новый перспективный метод обследования — ОКТ-ангиография (ОКТА). Неизвазивный характер и бесконтактность ОКТА открывают широкие возможности применения метода при различной патологии, в частности в детской практике. Целью работы явилась оценка перспектив использования ОКТА в диагностике и мониторинге болезни Беста. Пациенты и методы. Проведен анализ данных стандартного комплексного офтальмологического обследования и ОКТА заднего полюса глазного яблока 5 пациентов с болезнью Беста: 4 детей в возрасте от 5 до 12 лет и 25-летней женщины, наблюдающейся по поводу данного заболевания с детского возраста. Результаты. У всех пациентов заболевание носило двусторонний характер. В 7 из 9 глаз (1 из 10 глаз был исключен из анализа вследствие наличия на момент обследования отслойки сетчатки) болезнь находилась в стадии резорбции кисты, в 1 — в стадии вителлиформной кисты, в 1 — в стадии формирования рубца. Острота зрения на момент обследования составляла от 0,02 до 1,0. Клинически наличие ХНМ можно было предположить в 4 глазах. По данным ОКТА ХНМ выявлена в 7 случаях, в 3 из них отмечены признаки активности мембраны. Заключение. Проведение ОКТА позволило установить, что формирование ХНМ при болезни Беста происходит уже в стадии резорбции кисты и в половине случаев не сопровождается развитием клинических симптомов. Исследование позволяет оценить локализацию, размеры и активность мембраны, что необходимо для мониторинга и определения тактики лечения данного осложнения. Проведение дальнейших исследований позволит определить истинную частоту, факторы риска развития и особенности ХНМ при болезни Беста, что обеспечит разработку оптимальной тактики ведения таких пациентов.
Ключевые слова
Об авторах
доктор медицинских наук, профессор, заместитель директора по научной работе, начальник отдела патологии глаз у детей
ул. Садовая-Черногрязская, 14/19, Москва, 105062, Российская Федерация
кандидат медицинских наук, старший научный сотрудник отдела патологии глаз у детей
ул. Садовая-Черногрязская, 14/19, Москва, 105062, Российская Федерация
кандидат медицинских наук, старший научный сотрудник отдела патологии глаз у детей
ул. Садовая-Черногрязская, 14/19, Москва, 105062, Российская Федерация
доктор медицинских наук, старший научный сотрудник отдела патологии глаз у детей
ул. Садовая-Черногрязская, 14/19, Москва, 105062, Российская Федерация
кандидат медицинских наук, научный сотрудник отдела патологии глаз у детей
ул. Садовая-Черногрязская, 14/19, Москва, 105062, Российская Федерация
аспирант отдела патологии глаз у детей
ул. Садовая-Черногрязская, 14/19, Москва, 105062, Российская Федерация
Список литературы
1. Катаргина Л.А., Денисова Е.В., Рябцев Д.И. Болезнь Беста: клиническое наблюдение семейного случая. Российская педиатрическая офтальмология. 2015;10(2):15–19.
2. Marmorstein A.D., Kinnick T.R., Stanton J.B., Johnson A.A., Lynch R.M., Marmorstein L.Y. Bestrophin-1 influences transepithelial electrical properties and Ca2+ signaling in human retinal pigment epithelium. Molecular Vision. 2015;21:347–59.
3. Gass J.M.D. Best’s disease. In: Stereoscopic Atlas of Macular Disease. Diagnosis and Treatment. St. Louis-London-Philadelphia-Sydney-Toronto: Mosby; 1997:304–313.
4. Parodi M.B., Iacono P., Campa C., Turco C., Bandello F. Fundus autofluorescence patterns in Best vitelliform macular dystrophy. Am. J. Ophthalmol. 2014;158:1086–1092. DOI: 10.1016 / j.ajo.2014.07.026
5. Chhablani J., Jalali S. Intravitreal bevacizumab for choroidal neovascularization secondary to Best vitelliform macular dystrophy in a 6-year-old child. Eur. J. Ophthalmol. 2012;22(4):677–679. DOI: 10.5301/ejo.5000095
6. Elkhoyaali A., Chatoui S., Bercheq N., Elouatassi N., Zerrouk R., Elasri F., Reda K., Oubaaz A. Choroidal neovascularization complicating Best’s vitelliform macular dystrophy in a child. J. Fr. Ophtalmol. 2016;39(1):69–73. DOI: 10.1016/j.jfo.2015.05.008 (In French).
7. Leu J., Schrage N.F., Degenring R.F. Choroidal neovascularisation secondary to Best’s disease in a 13-year-old boy treated by intravitreal bevacizumab. Graefes Arch. Clin. Exp. Ophthalmol. 2007;245(11):1723–1725. DOI: 10,1007 / s00417-007-0604-7
8. Schatz P., Sharon D., Al-Hamdani S., Andréasson S., Larsen M. Retinal structure in young patients aged 10 years or less with Best vitelliform macular dystrophy. Graefes Arch. Clin. Exp. Ophthalmol. 2016;254(2):215–221. DOI: 10.1007/s00417-015-3025-z
9. Duncker T., Greenberg J.P., Ramachandran R., Hood D.C., Smith R.T., Hirose T., Woods R.L., Tsang S.H., Delori F.C., Sparrow J.R. Quantitative Fundus Autofluorescence and Optical Coherence Tomography in Best Vitelliform Macular Dystrophy. Invest. Ophthalmol. Vis. Sci. 2014;55(3):1471–1482. DOI: 10.1167/iovs.13-13834
10. Sulzbacher F., Pollreisz A., Kaider A., Kickinger S., et al. Identification and clinical role of choroidal neovascularization characteristics based on optical coherence tomography angiography. Acta Ophthalmol. 2017;95(4):414–420. DOI: 10.1111/aos.13364
Мультимодальная диагностика мультифокальной формы вителлиформной макулярной дистрофии взрослых (клинический случай)
Вителлиформная макулярная дистрофия (или болезнь Беста) впервые была описана в 1905 г. немецким офтальмологом Бестом Ф. Наследуется по аутосомно-доминантному типу. Выраженность заболевания вариабельна. Мутации в одном из генов BEST1 или PRPH2 ответственны за развитие заболевания. Менее чем в четверти случаев мутации возникают в обоих генах. Причина же возникновения заболевания у взрослых остается неизвестной. Степень тяжести заболевания может существенно различаться. Большинство же сохраняют сравнительно высокую остроту зрения до 50 лет и дольше [6, 7]. Ген болезни Беста идентифицирован под названием «bestrophin» ген. Белковый продукт гена располагается на базолатеральной плазматической мембране клеток пигментного эпителия, где входит в состав хлорного ионного канала. Предполагается, что нарушение транспорта жидкости вследствие дефекта переноса хлора в пигментном эпителии ведет к накоплению жидкости и клеточного дебриса между пигментным эпителием и фоторецепторами и между пигментным эпителием и мембраной Бруха с последующей отслойкой и вторичной дегенерацией фоторецепторов. У пациентов с вителлиформной макулярной дистрофией выявлены мутации в гене BEST1, который кодирует белок bestrophin [3, 5, 9]. У большинства больных с мутациями гена BEST1 имеются изменения на электроокулограмме (ЭОГ), что указывает на распространённую дисфункцию пигментного эпителия, однако у части пациентов ЭОГ нормальная [8]. Суммарная ЭРГ остаётся нормальной. Выделяют две основные формы заболевания – юношескую, или форму с ранней манифестацией, и форму взрослых. В типичных формах заболевание протекает в несколько последовательных фенотипических стадий: превителлиформную, вителлиформную, стадию псевдогипопиона, стадию разрыва кисты и атрофическую. В 2-9% случаев у пациентов с вителлиформной макулярной дистрофией описана хориоидальная неоваскуляризация, которая сложна для диагностики.
Поводом для обращения к офтальмологу чаще всего служат жалобы на снижение остроты зрения или метаморфопсии (похожие жалобы предъявляют больные с возрастной макулярной дегенерацией сетчатки). В классическом случае болезнь Беста проявляется в форме субретинального отложения круглой или овальной формы в макулярной области (вителлиформного образования) [1]. Вителлиформное образование расценивается как аккумуляция липофусцина в толще пигментного эпителия. Аутофлуоресценция вителлиформного материала – характерный признак болезни Беста. На средней и поздней фазах флуоресцентных ангиограмм вителлиформный материал, как правило, гипофлуоресцентный за счёт полного экранирования фоновой хориоидальной флуоресценции.
Мультифокальная (многофокусная) форма вителлиформной макулярной дистрофии – это атипичная редкая форма заболевания, которая характеризуется наличием нескольких вителлиформных фокусов в области заднего полюса глазного дна. Во взрослом возрасте может проявиться остро и быть сложной для диагностики. Для постановки диагноза необходимо наличие совокупности следующих признаков: двустороннее поражение с размером вителлиформных фокусов от 0,5 до 2 ДДЗН, аутофлуоресценция фокусов и экранирование ими флуоресценции на ангиограммах глазного дна с флуоресцеином. При офтальмоскопии определяются множественные мелкие округлые желтые очаги (вителлиформные фокусы), но, как правило, всегда присутствует макулярный фокус более крупного размера [4]. Для верификации диагноза необходимо использование комплексного обследования, включающего современные методы исследования структурных и функциональных изменений сетчатки [2].
Проанализировать результаты мультимодальной диагностики в постановке диагноза мультифокальной формы вителлиформной макулярной дистрофии взрослых.
Материал и методы.
Представлен клинический случай 33-летнего пациента с редкой мультифокальной формой вителлиформной макулярной дистрофии взрослых. Офтальмологическое обследование включало визометрию с определением максимально корригированной остроты зрения (МКОЗ); непрямую офтальмоскопию с помощью бесконтактной линзы MaxField 78D (Ocular Inc., США); оптическую когерентную томографию (ОКТ) с использованием растрового протокола и аутофлуоресценцию в коротковолновом режиме (488 нм), выполняемые на приборе «Spectralis HRA+OCT» (Heidelberg Engineering, Inc., Германия); исследование пороговой светочувствительности сетчатки на микропериметре МP-1 (Nidek technologies, Vigonza, Италия). Исследование макулы проводилось в зоне 12о с центром в фовеа в 45 точках по программе macula_12о 10 dB и пороговой стратегией 4-2. Фоторегистрацию глазного дна проводили на фундус-камере Visucam 500 (Zeiss, Германия). Срок наблюдения составил 5 мес.
Клинический случай. Пациент Ш., 33 года, обратился к офтальмологу с жалобами на появление пятна перед глазами. В анамнезе поливалентная аллергия. Офтальмологом районной поликлиники был поставлен диагноз – OU «Центральная серозная хориопатия». Пациент был направлен в ФГАУ «МНТК «Микрохирургия глаза» им. акад. С.Н. Федорова» для уточнения диагноза и тактики лечения.
OU: МКОЗ 1,0. Передний отрезок без патологических изменений. Диск зрительного нерва бледно-розовый, контуры чёткие, Э/Д=0,2. В макулярной зоне определяется округлый кистовидный очаг d=1 ДДЗН, желтого цвета, незначительно проминирующий, напоминающий «желток в яичнице-глазунье». Вдоль верхней сосудистой аркады множественные меньшего размера жёлтые округлые очаги, слегка возвышающиеся над уровнем сетчатки (рис. 1а, б). Крайняя периферия глазного дна без особенностей.
Аутофлуоресценция OU. Выявлена центральная область усиленной аутофлуоресценции (гипераутофлуоресценция), что может являться маркером высокого уровня внутриклеточного липофусцина – область вителлиформного очага (рис. 2а, б).
ОКТ OU. В макулярной области отмечается отслойка нейросенсорной сетчатки с отложением гиперрефлективного материала, что соответствует вителлиформной стадии заболевания (рис. 3). Вдоль верхней сосудистой аркады выявлены множественные волнообразные отслойки пигментного эпителия с отложением гиперрефлективного материала.
При исследовании светочувствительности макулярной зоны выявлено снижение средней светочувствительности центральной зоны сетчатки OD до 17,6 дБ и OS до 18,6 дБ, что соответствовало зоне гипераутофлуоресценции.
Установлен диагноз – мультифокальная вителлиформная макулярная дистрофия, вителлиформная стадия. В настоящее время лечения заболевания не существует.
При осмотре больного Ш. через 5 мес. выявлено снижение МКОЗ OU до 0,8. Биомикроскопия. OU: передний отрезок без патологических изменений. Диск зрительного нерва бледно-розовый, контуры чёткие, Э/Д=0,2. В макулярной зоне определяется очаг желтого цвета только в нижней части прежнего фокуса. Множественные более мелкие очаги сохраняют желтый цвет только в нижней части, что соответствует неравномерному распределению вителлиформного материала с его преобладанием в нижней части фокусов. Такая картина соответствует стадии фрагментации, «яичницы-болтуньи», когда вителлиформный материал начинает дезорганизовываться, оставаясь в пределах исходных границ.
Аутофлуоресценция OU. Зона гипераутофлуоресценции определяется только в нижней части прежних фокусов и по краям.
ОКТ OU. Горизонтальный оптический срез, проходящий через нижнюю часть зоны поражения, выявляет гиперрефлективную зону аккумуляции вителлиформного материала. Зоны резорбции материала выглядят гипорефлективными.
При исследовании светочувствительности макулярной зоны выявлено постепенное понижение средней светочувствительности центральной зоны сетчатки через 5 мес. наблюдения OD до 16,9 дБ и OS до 17,5 дБ.
Таким образом, диагноз – мультифокальная вителлиформная макулярная дистрофия. Стадия разрыва кисты. В настоящее время лечения заболевания не существует. Обследование членов семьи обязательно.
Представленный клинический случай демонстрирует редкую форму мультифокальной вителлиформной макулярной дистрофии взрослых. Мультимодальный подход в исследовании, включающий данные аутофлуоресценции, оптической когерентной томографии, микропериметрии помогает в диагностике и проведении мониторинга сложных форм макулярной патологии.
Дистрофия Беста у ребенка
Офтальмологи Фэнтези – врачи доказательной медицины, лечат по современным протоколам, назначают только эффективное лечение. Мы решаем конкретные проблемы, не перенаправляя в специализированные центры. У нас в клинике есть все возможности для консервативного лечения заболеваний глаз у детей. Наши специалисты диагностируют и лечат все патологии – в том числе сложные и редкие.
Что такое дистрофия Беста?
Это заболевание сетчатки относится к числу врожденных и проявляется обычно в детском или подростковом возрасте. Дистрофию Беста у ребенка вызывает генная мутация, поэтому болезнь может наследоваться от родителей на протяжении нескольких поколений.
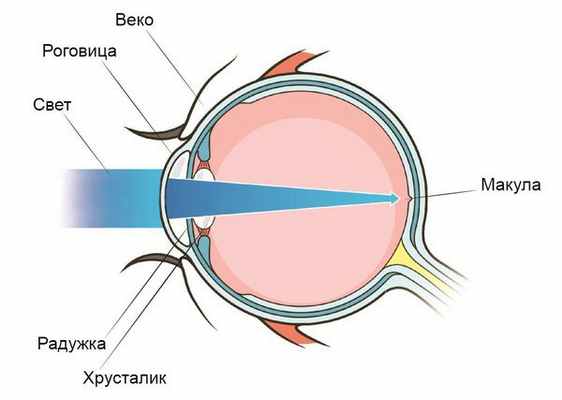
Болезнь поражает центральную область сетчатки - ее называют макула или желтое пятно (второе название дано из-за ее характерного цвета). Именно здесь располагаются фоторецепторы - светочувствительные нейроны, которые дают человеку возможность хорошо видеть и различать предметы в разных условиях. Среди них есть колбочки, их «зона ответственности» - помогать различать мелкие детали и цвета. Именно эти фоторецепторы преобладают в макуле и становятся объектом поражения.
При дистрофии Беста у ребенка на сетчатке образуются мелкие очаги, напоминающие желток - округлой или овальной формы и желто-красного цвета. Эти очаги с развитием болезни превращаются в кисты, которые впоследствии разрываются. В заключительной стадии болезни в макуле образуется атрофический очаг или рубец.
К чему может привести дистрофия Беста у ребенка?
Подобная макулярная дегенерация может привести к серьезным осложнениям, даже к полной потере зрения.
В частности, она может стать причиной:
- субретинальной неоваскулярной мембраны (СНМ) - новообразование сосудов в области глазного дна, что приводит к снижению глазной функции.
- кровоизлияний в глазу;
- разрывов или отслойки сетчатки.
Как родителям распознать симптомы?
Обычно на начальных стадиях болезнь себя никак не проявляет и может быть обнаружена только случайно, при обследовании глазного дна. Первые признаки заболевания обычно появляются на этапе формирования кист, обычно это:
- затуманивание зрения;
- снижение его остроты, в том числе возникновение трудностей с различением мелких деталей, например, букв;
- искажение зрительного восприятия (метаморфопсия), больной видит предметы в искаженном виде, неправильно воспринимая их форму, размер или цвета.
Диагностика дистрофии Беста у ребенка
Окончательный диагноз может быть поставлен только врачом-офтальмологом. Поскольку это наследственное заболевание, врач подробно расспросит о семейных болезнях. Также офтальмолог проведет целый ряд диагностических исследований, включая:
- офтальмоскопию (обследование глазного дна);
- флуоресцентную ангиографию (ФАГ). Врач вводит краситель флуоресцеина и затем наблюдает, как он проходит по сосудам. Гиперфлюоресценция здесь свидетельствует об атрофии тканей, ее отсутствие - о наличии кисты.
- электроретинографию (ЭРГ). Доктор воздействует пучками света на сетчатку и смотрит, как реагируют фоторецепторы. Стоит отметить, что в начальных стадиях дистрофии Беста у ребенка показания ЭРГ обычно соответствуют норме, и нарушения отмечаются на поздних стадиях болезни (при формировании кист и рубца).
- электроокулографию (ЭОГ), или анализ электрической активности глаза. Для измерения электропотенциала тканей к веку пациента прикрепляют электроды, которые регистрируют разницу потенциалов при движении глазного яблока.
После диагностики детский офтальмолог назначит терапию и индивидуальный график осмотров.
Болезнь Беста - симптомы и лечение
Что такое болезнь Беста? Причины возникновения, диагностику и методы лечения разберем в статье доктора Рытик Нины Петровны, офтальмолога со стажем в 13 лет.
Над статьей доктора Рытик Нины Петровны работали литературный редактор Маргарита Тихонова , научный редактор Сергей Федосов и шеф-редактор Лада Родчанина
Определение болезни. Причины заболевания
Болезнь Беста — это генетическое заболевание глаз, которое вызывает изменения в центральной области сетчатки, так называемой макуле. Первоначально оно протекает бессимптомно, но постепенно приводит к ухудшению остроты зрения и появлению слепого участка в центре поля зрения.
Возникновение и развитие болезни связано с дефектами в наследственном аппарате — мутациями гена VMD2 [3] . Область, в которой локализуется ген VMD2, известна врачам как область скопления генов, отвечающих за развитие большой группы гетерогенных генетических заболеваний с поражением глаз в комплексе с умственной отсталостью , ожирением , тугоухостью и другими патологиями органов и систем [11] .
Болезнь Беста наследуется по аутосомно-доминантному пути, т. е. вероятность возникновения заболевания не зависит от пола и тяжести течения болезни у родителей.
У данного заболевания высокая пенетрантность, т. е. болезнь развивается у большинства людей с патологическим геном. Несмотря на это, выраженность клинических проявлений у родственников варьирует от минимальных изменений и сохранения 100 % зрения до выраженного снижения остроты зрения (вплоть до 0,02) и инвалидизации. Проследить семейную отягощённость удаётся не всегда, даже при комплексном обследовании [2] .
Заболевание считается редким. Его распространённость составляет около 1 случая на 10000 населения [1] . Впервые упоминание о нём в литературе появилось в 1905 году: офтальмолог Ф. Бест описал его как двустороннюю макулодистрофию, которую он наблюдал у восьми членов одной семьи.
Факторов, способствующих манифестации заболевания при наличии наследственной предрасположенности, не выявлено.
При обнаружении схожих симптомов проконсультируйтесь у врача. Не занимайтесь самолечением - это опасно для вашего здоровья!
Симптомы болезни Беста
На начальных стадиях заболевание никак не проявляется, поэтому обычно оно диагностируется случайно при медицинском осмотре. Симптомы появляются только на более поздних стадиях патологии.
Манифестирует болезнь в возрасте 5-15 лет. Ребёнок жалуется на прогрессирующее, обязательно двустороннее снижение чёткости зрения: он начинает испытывать затруднение при чтении мелкого шрифта вблизи. Также его беспокоят "вспышки", "мерцание огоньков" и ухудшение цветовосприятия (в основном наблюдается цветослабость на жёлто-зелёный, зелёный, сине-зелёный цвета).
Изменения в большинстве случаев несимметричные, но возникают на обоих глазах. Острота зрения в зависимости от стадии болезни значительно колеблется: от 0,01 до 1,0.
Важно отличать болезнь Беста от вителлиформной макулодистрофии взрослых. Это заболевание также является генетическим, но возникает и прогрессирует оно в зрелом возрасте (около 40-50 лет). Для него характерно двустороннее, как правило, симметричное субретинальное поражение в центральной области сетчатки. Изменения так же, как при болезни Беста, имеют локальную, очерченную, круглую форму, желтоватый оттенок, но их размер всегда значительно меньше и они не прогрессируют [10] .
Патогенез болезни Беста
Патофизиологический механизм болезни Беста на данный момент неизвестен. Предполагается, что при данной патологии происходит аномальное накопление вещества, подобного липофусцину — жёлто-коричневому пигменту гликопротеиновой природы, который встречается во всех тканях и органах человека. Это вещество скапливается между пигментным эпителием сетчатки и слоем светочувствительных клеток — фоторецепторов. В результате нарушается мембрана Бруха (самый внутренний слой сосудистой оболочки глаза) и разрушаются нервные элементы сетчатки.
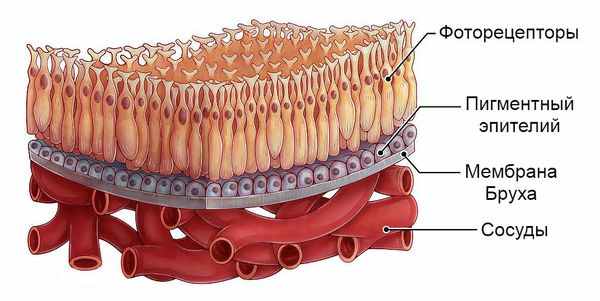
Большинство наружных сегментов фоторецепторов разрушается полностью, при этом во внутренних сегментах светочувствительных клеток скапливаются продукты кислых мукополисахаридов, вызывая изменения в сетчатке. Слой пигментного эпителия отделяется от слоя фоторецепторов, из-за чего формируется немного проминирующее (выбухающее) жёлтоватое образование, т.е. киста, которая локализуется в центральной или околоцентральной области сетчатки [3] .
Классификация и стадии развития болезни Беста
Заболевание относится к наследственным ретинальным дистрофиям. В Международной классификации болезней (МКБ-10) ему присвоен код H35.5.
Болезнь Беста всегда протекает с прохождением четырёх определённых стадий, которые завершаются образованием рубца в центральной области сетчатки [1] .
- Первая стадия — превителлиформная. Она предшествует формированию кисты. В макуле наблюдаются изменения пигментации в виде множества маленьких желтоватых очажков. Во время электроокулографии фиксируются аномальные изменения.
- Вторая стадия — вителлиформная. Формируется классическая вителлиформная киста, которая при осмотре очень похожа на "яичный желток" довольно крупных размеров (до 1 диаметра диска зрительного нерва). Изменения асимметричны и практически всегда поражают оба глаза. Офтальмоскопические изменения не соответствуют высокой остроте зрения: даже у пожилых пациентов этот показатель находится в пределах от 0,4 до 0,9.
- Третья стадия — разрыв кисты и её резорбция, т. е. рассасывание. Острота зрения снижается, пациентам становится трудно читать мелкий текст.
- Четвёртая стадия — формирование фиброглиального рубца на месте кисты. Также на этой стадии возможно развитие субретинальной неоваскуляризации — образование новых сосудов под сетчаткой [3] . Острота зрение падает ещё сильнее, в поле зрения появляются слепые зоны.
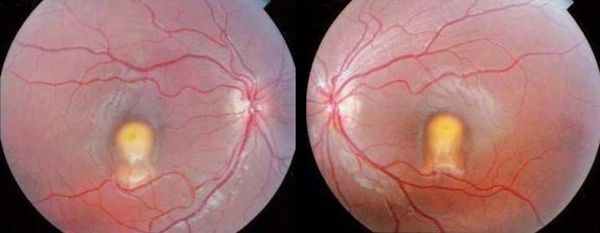
Осложнения болезни Беста
На поздних стадиях заболевания начинают развиваться осложнения. Самые частые — это образование сквозных разрывов в макулярной области, потеря центральной остроты зрения и формирование "пятна перед глазами". Возникновение отслойки сетчатки встречается реже.

Одним из частых осложнений так же является субретинальная неоваскуляризация — образование новых сосудов в зоне глазного дна [11] . Она является одной из причин инвалидизации при болезни Беста, так как приводит к стойкому снижению центральной остроты зрения. При этом полная слепота не развивается.
Диагностика болезни Беста
Для постановки диагноза "болезнь Беста" необходим ряд обследований. В первую очередь нужно зарегистрировать специфическую офтальмоскопическую картину глазного дна, характерную для каждой стадии заболевания. Затем, чтобы оценить состояние сетчатки, следует выполнить электроокулографию (ЭОГ) и электроретинографию (ЭРГ). В последние годы, с развитием генетики, стало обязательным молекулярное генетическое исследование пациента. Вместе с этим производят офтальмологическое и генетическое обследование других членов семьи.
Офтальмоскопия позволяет обнаружить первые признаки болезни Беста на первом и втором десятилетии жизни. На первых стадиях в макуле появляются желтоватые очажки, затем формируются виттелиформные кисты, при разрывах которых глазное дно напоминает картину "яичницы-глазуньи". На последних стадиях в макуле формируется атрофические глиальные рубцы, а при осложнениях — неоваскулярная мембрана и сквозные макулярные отверстия.
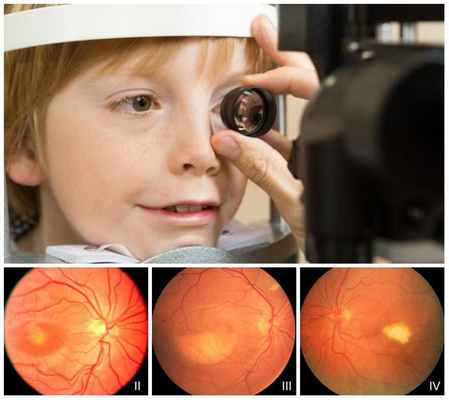
Электроокулография является очень важным методом диагностики при болезни Беста. С её помощью можно выявить такой специфический признак заболевания, как снижение коэффициента Ардена — соотношения биопотенциала глаз в темноте и при свете. Данный показатель будет снижен даже на нулевой стадии болезни при нормальной офтальмоскопической картине. В случае вителлиформной макулодистрофии взрослых электроокулография изменений не выявит.

Флюоресцентная ангиография позволяет диагностировать болезнь Беста даже на доклиническом этапе. Изменения сетчатки зависят от стадии заболевания. На начальном этапе болезни видны мелкие окончатые дефекты и участки с локальной гиперфлюоресценцией (свечением). При наличии сформированной кисты флюоресценция полностью отсутствует. На третьей стадии болезни гиперфлюоресценция наблюдается только в верхней части кисты, а в нижней её части отсутствует [8] .
При электроретинографии (общей и ритмичной) наблюдается снижение амплитуды "а" волн, увеличение латентных периодов "а" и "b" волн, а также угнетение ответа от центральных отделов сетчатки [9] .
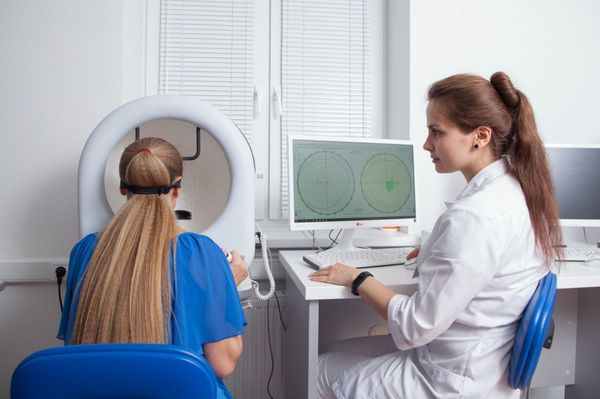
Статическая компьютерная периметрия выявляет снижение чувствительности макулярной области, а при разорвавшейся вителлиформной кисте — центральную абсолютную скотому (слепое пятно) . При этом границы поля зрения по периферии остаются в норме.
Дифференциальная диагностика
Болезнь Беста необходимо отличить от других заболеваний:
- болезни Коатса и других макулярных дистрофий пигментного эпителия сетчатки (Х-образной макулярной дистрофии);
- острого хориоретинита (в первую очередь токсоплазмозной этиологии);
- болезни Штаргардта;
- вителлиформной дистрофии взрослых;
- отслойки пигментного эпителия сетчатки [11] .
Болезнь Коатса — врождённая ненаследственная патология, при котором наблюдаются аномалии сосудов сетчатки глаза. Она может стать причиной частичной или полной слепоты. На первых стадиях болезнь Коатса так же, как и болезнь Беста, течёт без симптомов и в большинстве случаев диагностируется у детей 2-8 лет при случайных профилактических осмотрах, проводимых в детских садах или школах. В отличие от болезни Беста, при болезни Коатса, как правило, в патологический процесс вовлекается только один глаз. Лишь у 5-8 % больных наблюдаются двусторонние изменения. Мальчики заболевают им в 3 раза чаще, чем девочки [9] .
У большинства пациентов с заболеванием Коатса во время первого офтальмологического обследования в центральной области сетчатки выявляют возвышающийся округлый очаг твёрдого желтоватого экссудата, очень похожий на вителлиформные изменения, встречающиеся при болезни Беста. Данные экссудаты в центральной области сетчатки очень часто сочетаются с кровоизлияниями за сетчаткой и образованием новых сосудов, что тоже характерно для болезни Беста.
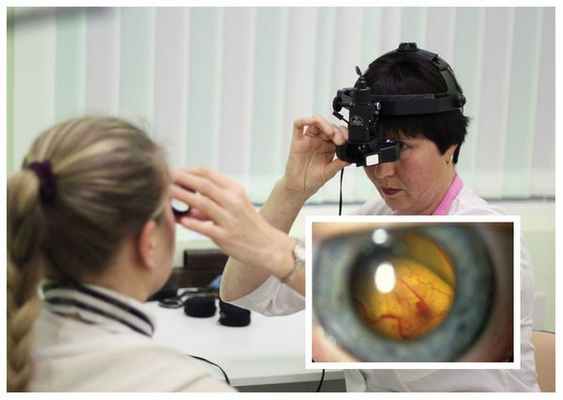
Диагностика болезни Коатса основывается на результатах осмотра глазного дна (офтальмоскопии), а также центральной области и периферии глазного дна с применением или налобного офтальмоскопа с линзами 20-30 дптр, или офтальмобиомикроскопии с трёхзеркальной линзой Гольдмана. У большинства пациентов с болезнью Коатса во время данного обследования обязательно выявляются аномалии сосудов: микро- и макроаневризмы, телеангиэктазии ( сосудистые звёздочки ), артериовенозные шунты. Чаще всего эти аномалии располагаются в височной половине сетчатки.
Изменения при электроокулографии в начальной и развитой стадиях заболевания, как и при болезни Беста, не выявляются. Но острота зрения у больных с ретинитом Коатса низкая: при наличии изменений в центральной области сетчатки она не превышает 0,4, а при болезни Беста длительно сохраняются в норме [7] .
Острый токсоплазмозный хориоретинит — это паразитарное заболевание глаз, для которого характерно в основном скрытое или хроническое течение. Как правило, оно поражает только один глаз, в отличие от болезни Беста. При неадекватном и несвоевременном лечении может привести к стабильному снижению остроты зрения.
Трудности при диагностике обычно возникают при обследовании больных с приобретённым токсоплазмозом и экссудативно-геморрагическими изменениями в центральной области сетчатки, которые похожи на вителлиформные очажки с субретинальными геморрагиями, как при болезни Беста. Хориоретинальные поражения при токсоплазмозе сочетаются с выпотом в стекловидное тело различной степени тяжести, а порой и изменениями переднего отрезка глаза.
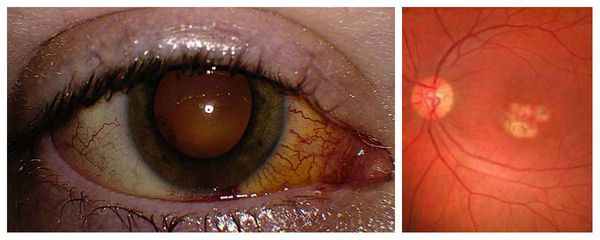
Пациенты, как правило, предъявляют жалобы на внезапное, резкое и значительное снижение центральной остроты зрения, которая в ряде случаев изменяется до 0,01-0,2. При статической периметрии регистрируется повышенный порог яркостной чувствительности, относительная или абсолютная центральная скотома. Электроокулография, как правило, не изменена.
Для подтверждения и верификации токсоплазмоза необходимо выполнить иммунологические исследования, определить антитела к токсоплазме или выделить её методом ПЦР (полимеразной цепной реакции). В 95 % случаев токсосплазмозный хориоретинит хорошо поддаётся лечению, острота зрения может восстановиться до исходных значений [12] .
Болезнь Штаргардта иначе называют ювенильной макулярной дегенерацией. Впервые это заболевание описал немецкий врач-офтальмолог К. Штаргардт как врождённое поражение макулы, которое передавалось по наследству в одной семье.
Как правило, болезнь Штаргардта начинается в молодом (ювенильном) возрасте и сопровождается поражением центральной области сетчатки, как и болезнь Беста. Её отличает быстрое прогрессирование, вплоть до инвалидизации. Медленное ухудшение зрения встречается крайне редко (при доминантном типе наследования) [9] .
Данное заболевание всегда двустороннее и симметричное. Его характерными признаками являются различные процессы: атрофия хориоидеи (сосудистой оболочки глаза), "бычий глаз", очаг дистрофии цвета "битой (кованой) бронзы" и др. При далеко зашедшем процессе фовеолярный рефлекс (центральная ямка макулы) отсутствует. В макулярной области на уровне пигментного эпителия сетчатки наблюдаются скопления коричневатого, тёмного пигмента, который окружён участками гипер- и депигментации. Эти скопления отличаются от вителлиформных жёлтых очагов при болезни Беста.
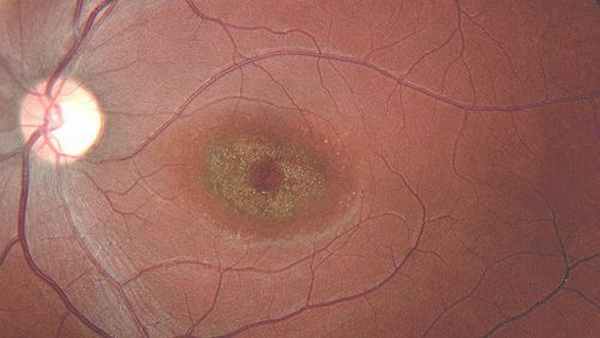
Вителлиформная макулодистрофия взрослых , в отличие от болезни Беста, развивается у людей 40-50 лет. Для неё характерно двустороннее симметричное поражение макулы с локальными изменениями. Очаги патологии, как правило, имеют округлую форму и жёлтый оттенок. Их отличает отсутствие прогрессирования и небольшие размеры: диаметр поражений достигает 0,3-0,5 размера диска зрительного нерва. При этом нарушения зрительных функций минимальны.
Вещества, подобные липофусцину, скапливаются диффузно в различных местах: в пигментном эпителии, внутренней части фоторецепторов, мюллеровских клетках и даже в стекловидном теле.
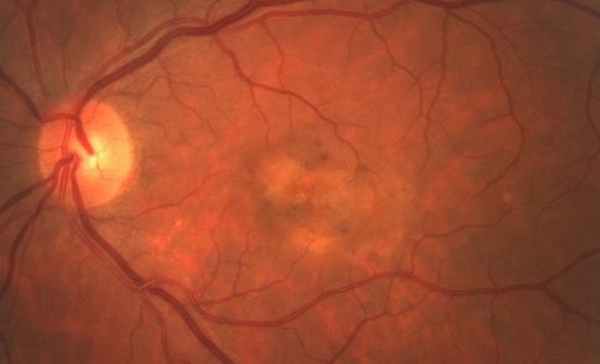
Отслойка пигментного эпителия сетчатки возникает при нарушении нормального соединения пигментного эпителия сетчатки с мембраной Бруха. К причинным факторам относятся сосудистые, воспалительные и дистрофические процессы.
Длительное время болезнь может существовать без какой-либо динамики, спонтанно исчезать, а вследствие инвазии сосудов из хориоидеи трансформироваться в геморрагическую отслойку. Сложности в диагностике могут возникнуть при атипичной клинической картине заболевания и экссудативных изменениях в центральной области сетчатки.
Обычно болезнь поражает только один глаз. Общая электроретинография не меняется, локальная — может быть снижена. Электроокулография, как правило, в норме. При флюоресцентной ангиографии на последней стадии отслойки регистрируется гиперфлюоресценция.
Лечение болезни Беста
Лечения болезни Беста на сегодняшний момент не существует. Можно лишь затормозить формирование кист, предотвратить их разрывы и наступление осложнений, которые сильно влияют на остроту зрения пациента. С этой целью применяется антиоксидантная и вазоактивная терапия, а также витамины С, Е и А. Вазоактивные препараты улучшают кровоснабжение сетчатки, а витамины являются мощными антиоксидантами [5] .
Вероятно, что в будущем при лечении болезни Беста будет применяться генная инженерия или терапия, направленная на нормализацию тока жидкости через пигментный эпителий сетчатки, торможение накопления липофусцина и воздействия на другие этапы патогенеза [13] .
Прогноз. Профилактика
Прогноз для зрения относительно благоприятный. Так как заболевание протекает медленно, острота зрения снижается постепенно, при этом страдает только центральное зрение. Благодаря сохранению периферического зрения человек хорошо адаптируется, часто сохраняя работоспособность и возможность чтения.
При обнаружении заболевания врач должен проинформировать больного о вариабельности течения заболевания, рисках его возникновения у будущих детей и функциональных прогнозах. Желательно проконсультироваться с врачом-генетиком.
Все члены семьи пациента обязательно должны пройти обследование у офтальмолога. Сам пациент должен регулярно наблюдаться у своего лечащего врача [14] .Чтобы дети и подростки не отставали в развитии, необходимо вовремя применять технические средства реабилитации слабовидящих [1] .
Болезнь Беста (вителлиформная макулярная дистрофия)
Болезнь Беста (вителлиформная макулярная дистрофия)
Болезнь Беста (Best’s disease, BD) — аутосомно-доминантная наследственная макулярная дистрофия, проявляющаяся появлением в макулярной области округлых или овальных желтых субретинальных отложений, ярко флюоресцирующих при исследовании аутофлюоресценции. Хотя у большинства носителей патогенных генов при электроокулографии отмечается снижение амплитуды потенциала на свету, фенотипические изменения сетчатки вариабельны.
У некоторых носителей патогенных генов изменения глазного дна вообще отсутствуют. Фенотип подразделяется на четыре стадии:
Стадия 0: превителлиформная — нормальное глазное дно у бессимптомного носителя при наличии изменений ЭОГ.
Стадия I: небольшие изменения ПЭС.
Стадия II: классическая картина изменений макулы по типу «яичного желтка». При ФАГ определяется соответствующая клиническим изменениям зона экранированной флюоресценции хориоидеи. Обычно такая картина наблюдается в течение первого или второго десятилетия, часто при почти нормальной остроте зрения.
Стадия IIа: «яичный желток» начинает распадаться вследствие резорбции желтого субстрата, скопившегося между пигментным эпителием сетчатки и слоем фоторецепторов; обычно сопровождается заметным ухудшением зрения.
Стадия III: псевдогипопион — часть скопившегося под сетчаткой субстрата резорбировалась, в макулярной области наблюдается картина «уровня жидкости».
Стадия IVa: желтый субстрат полностью резорбировался, атрофия пигментного эпителия макулярной области.
Стадия IVb: субретинальный фиброз.
Стадия IVc: хориоидальная неоваскуляризация.
Гистологически выявляется скопление липофусцина на всем протяжении пигментного эпителия сетчатки. Хотя офтальмоскопические изменения обычно ограничены макулярной зоной, развивается более обширное поражение сетчатки. Прогноз для зрения хороший; большинство пациентов в возрасте старше пятидесяти лет сохраняют способность к чтению. У носителей, в молодом возрасте имеющих минимальные изменения макулярной зоны или картину нормального глазного дна (но сопровождающуюся изменениями на ЭОГ), обычно сохраняется хорошая острота зрения.

а) Электрофизиология. Ганцфельд-ЭРГ не изменена; при ЭОГ регистрируется снижение или отсутствие роста потенциала на свету, что свидетельствует об обширной дисфункции пигментного эпителия сетчатки. У большинства носителей мутации гена, вызывающего болезнь Беста, BEST1, регистрируется аномальная ЭОГ, но офтальмоскопическая картина макулярной области может оставаться нормальной. Истинная нулевая пенетрантность встречается редко.
б) Молекулярная генетика и патогенез. Болезнь Беста вызывается мутациями BEST1, кодирующего протеин бестрофин, локализующийся в базолатеральной плазматической мембране клеток пигментного эпителия сетчатки. Он формирует кальций-активируемые хлоридные каналы, которые поддерживают транспорт хлоридов и регулируют ток жидкости через ПЭС. Согласно данным ОКТ, нарушение транспорта жидкости в пигментном эпителии сетчатки вследствие нарушения транспорта хлоридов вызывает скопление жидкости и/или отложение твердого субстрата между ПЭС и фоторецепторами и между ПЭС и мембраной Бруха, что приводит к отслойке и вторичной дегенерации фоторецепторов.
Причины вариабельности экспрессии болезни Беста остаются невыясненными: разнообразие клинических проявлений может определяться дополнительными генетическими влияниями и/или факторами среды.
Идентифицированы рецессивные мутации гена BEST1, вызывающие появление множественных вителлиформных ретинальных отложений и макулопатию: аутосомно-рецессивную бестрофинопатию (autosomal recessive bestrophinopathy, ARB). Часто наблюдается дальнозоркость, отмечается повышенная частота закрытоугольной глаукомы. У детей ретинопатия характеризуется появлением двусторонних мультифокальных субретинальных желтых отложений, лучше всего заметных при исследовании аутофлюоресценции.
в) Перспективные методы лечения. В будущем для лечения, вероятно, будут применяться генные методы терапии или терапевтические вмешательства, направленные или на нормализацию работы кальций-активируемых хлоридных каналов и тока жидкости через пигментный эпителий сетчатки, или на замедление зрительного цикла и торможение накопления липофусцина, или же на прямое ингибирование токсического конечного продукта А2Е, как это описано выше в разделе о болезни Штаргардта.
Болезнь Беста.
Частично резорбированное желтое субретинапьное макулярное отложение (стадия IIа). Болезнь Беста.
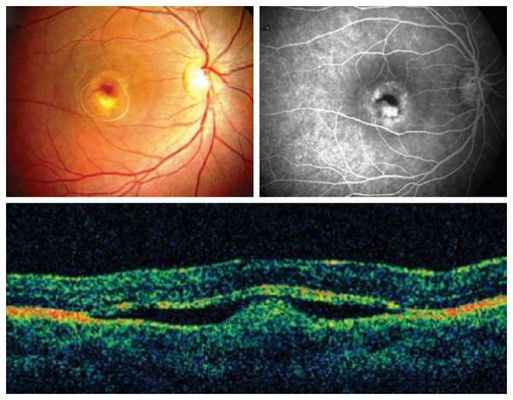
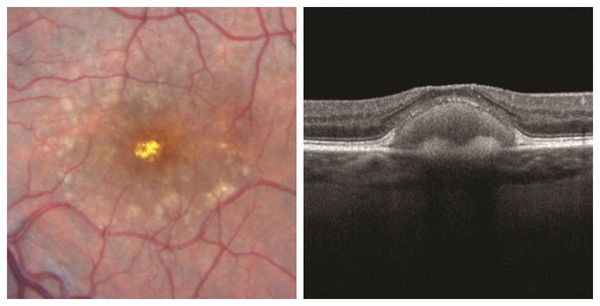
Классические вителлиформные изменения (стадия II) (А) ярко флюоресцируют при исследовании аутофлюоресценции (Б)
и выглядят как гомогенное субретинальное отложение при спектральной ОКТ (В). Болезнь Беста. (А) Классическое вителлиформное поражение (стадия II), напоминающее яичный желток в яичнице-глазунье.
(Б) При флюоресцентной ангиографии выявляется соответствующая офтальмоскопическим изменениям зона экранирования флюоресценции хориоидеи. Продолжение.
(В) Вителлиформное поражение с хориоидальной неоваскуляризацией и субретинальным кровоизлиянием (стадия IVc).
(Г) Флюоресцентная ангиография.
(Д) При ОКТ выявляется хориоидальная неоваскулярная мембрана, приподнимающая вышележащую сетчатку. Аутосомно-рецессивная бестрофинопатия. Видны мультифокальные субретинальные желтые отложения (А),
ярко флюоресцирующие при исследовании аутофлюоресценции (Б) и часто сопровождаются отеком сетчатки и скоплением субретинальной жидкости,
что можно наблюдать клинически и на ОКТ (В).
Редактор: Искандер Милевски. Дата обновления публикации: 18.3.2021
Читайте также:
