Цитомегаловирусный колит - диагностика
Добавил пользователь Валентин П. Обновлено: 27.01.2026
Цитомегаловирусная инфекция желудочно-кишечного тракта является относительно распространенным проявлением у больных, получающих иммуносупрессивную терапию,ВИЧ-инфицированных или реципиентов органов и тканей. Однако в некоторых случаях, у иммунокомпетентных лиц также может развиваться цитомегаловирусная болезнь с поражением кишечной стенки. В особенности недавние исследования выявили потенциальную связь между ЦМВ-индуцированным колитом и различными формами воспалительных заболеваний кишечника (ВЗК). Стандартная диагностика цитомегаловирусной инфекции в биопсийном материале основана на выявлении типичных внутриядерных включений при окраске гематоксилин-эозином. Однако чувствительность данного метода для диагностики ЦМВ низкая. Иммуногистохимическое исследование биопсийного материала является чувствительным и высокоспецифичным методом. В настоящее время считается, что метод иммуногистохимии для диагностики ЦМВ является «золотым» стандартом. Некоторыми авторами сделан вывод, что наличие ЦМВ инфекции играет важную роль в усугублении течения болезни в группе больных ВЗК. Эти исследования предполагают, что у некоторых пациентов цитомегаловирусное поражение кишечной стенки может лежать в основе рефрактерного к терапии течения ВЗК.
Ключевые слова
Полный текст
Об авторах
Дарья Олеговна Маркова
ГБОУ ВПО «Санкт-Петербургский государственный педиатрический медицинский университет» Минздрава России
Руслан Абдуллаевич Насыров
ГБОУ ВПО «Санкт-Петербургский государственный педиатрический медицинский университет» Минздрава России
Мария Олеговна Ревнова
ГБОУ ВПО «Санкт-Петербургский государственный педиатрический медицинский университет» Минздрава России
Список литературы
- Ершов Ф. И., Оспельникова Т. П. Современный арсенал антигерпетических лекарственных средств // Consilium Medicum. — 2001. — Т. 04, № 3.
- Никонов А. П., Асцатурова О. Р. Цитомегаловирусая инфекция // Consilium Medicum (Педиатрия). — 2009, № 1.
- Румянцев В. Г., Щиголева Н. Е. Болезнь Крона в детском возрасте // Consilium Medicum. — 2002. — Т. 04, № 6.
- Самохин П. А. Цитомегаловирусная инфекция у детей: Клинико-морфологические аспекты. — М.: Медицина, 1987. — 159 с.
- David A. Bobak. Gastrointestinal Infection Caused by Cytomegalovirus // Current Infectious Disease Reports. — 2003. — Vol. 5. — P. 101–107.
- Doherty P. Immunologist. — 1995. — Vol. 3(5). — P. 231–233.
- Dubinsky M. C. Serologic and laboratory markers in prediction of the disease course in inflammatory bowel disease // World J. Gastroenterol. — 2010. — Vol. 16(21). — P. 2604–2608.
- Haywood L., Abernathy B. Infection // Sem Perinatol. — 1998. — Vol. 22(4). — P. 260–266.
- Herpesvirus Infections in Pregnancy // The 7th Ann. Meeting of the International Herpes Management Forum /Whitley R. J., Weber T., Pass R. Eds. — 1999. — P. 40–60.
- Kaniel A., Lashner B. Cytomegalovirus colitis complicating inflammatory bowel disease // Am. Journal Gastroenterology. — 2006. — Vol. 101. — P. 2857–2865.
- Karakozis S., Gongor E., Caceres M. et al. Life-threatening cytomegalovirus colitis in the immunocompetent patient: report of case and review of the literature. // Dis. Colon. Rectum. — 2001. — Vol. 44. — P. 1716–1720.
- Klemola E., Kaariainen L. Cytomegalovirus as a possible cause of a disease resembling infections mononucleosis // BMJ. — 1965. — Vol. 2. — P. 1099–1102.
- Maha M. Maher, Mahmoud I. Nassar. Acute Cytomegalovirus Infection Is a Risk Factor in Refractory and Complicated Inflammatory Bowel Disease. — Springer Science+Business Media, LLC. — 2008.
- Sissons J. G. P., Carmishael A. J. Clinical aspects and management of cytomegalovirus infection // J. Infection. — 2002. — Vol. 44 — P. 78–83.
© Маркова Д.О., Насыров Р.А., Ревнова М.О., 2013
Эта статья доступна по лицензии Creative Commons Attribution 4.0 International License.
ЦИТОМЕГАЛОВИРУСНАЯ ИНФЕКЦИЯ У ПАЦИЕНТОВ СО СРЕДНЕТЯЖЕЛОЙ И ТЯЖЕЛОЙ АТАКАМИ ЯЗВЕННОГО КОЛИТА
ЦЕЛЬ: определение частоты и оценка значимости диагностики и лечения сопутствующей цитомегаловирусной инфекции (ЦМВИ) у пациентов со среднетяжелой и тяжелой атаками язвенного колита (ЯК), а также определение частоты колэктомий в зависимости от наличия ЦМВИ и от проводимой терапии.
ПАЦИЕНТЫ И МЕТОДЫ: в исследование включено 67 пациентов с тяжелой или среднетяжелой атакой язвенного колита. Всем пациентам было проведено эндоскопическое исследование толстой кишки с взятием биоптатов слизистой для определения в них ДНК цитомегаловируса методом полимеразной цепной реакции. Пациенты, у которых не был обнаружен вирус (группа ЦМВ-отр), получали терапию согласно текущим клиническим рекомендациям. Пациенты, у которых был обнаружен вирус (группа ЦМВ-пол), дополнительно к стандартной терапии получали противовирусную терапию ганцикловиром. У последних вирусная нагрузка в биоптатах из толстой кишки оценивалась до лечения и на 19-21 день терапии. В случае ухудшения состояния пациента и невозможности дальнейшего проведения консервативного лечения выполнялась колэктомия. Успех проводимой терапии в обеих группах оценивали по доле проведенных колэктомий в течение госпитализации.
РЕЗУЛЬТАТЫ: в нашем исследовании частота ассоциации тяжелой и среднетяжелой атак язвенного колита с цитомегаловирусной инфекцией составила 43,2%. Предшествующая терапия не влияла на частоту обнаружения вируса. В группе ЦМВ-пол острые атаки встречались достоверно чаще, чем в группе ЦМВ-отр (20% и 2,6%, соответственно) (р=0,02).
Эффективность противовирусной терапии в нашем исследовании составила 69%. Ни один из пациентов, ответивших на противовирусную терапию, не был оперирован. Неудача противовирусной терапии у пациентов с ассоциированной цитомегаловирусной инфекцией достоверно увеличивала частоту операций (0 – у пациентов, ответивших на противовирусную терапию, против 22,2% из не ответивших).
ЗАКЛЮЧЕНИЕ: исследование показало, что в 43% случаев тяжелая и среднетяжелая атаки ЯК проходят на фоне персистирующей ЦМВИ. ЦМВИ является фактором резистентности к проводимому консервативному лечению. Добавление таким пациентам специфической противовирусной терапии улучшает непосредственные результаты лечения и прогноз.
Ключевые слова
Об авторах
Александров Тимофей Леонидович
ФГБУ «НМИЦ колопроктологии имени А.Н. Рыжих» Минздрава России
Россия
ул. Саляма Адиля, д. 2, г. Москва, 123423
ФГБУ «НИЦЭМ имени почетного академика Н.Ф. Гамалеи» Минздрава России, НИИ вирусологии имени Д.И. Ивановского
Россия
ул. Гамалеи, д. 18, г. Москва, 123098
ФГБУ «НМИЦ колопроктологии имени А.Н. Рыжих» Минздрава России
Россия
ул. Саляма Адиля, д. 2, г. Москва, 123423
ФГБУ «НМИЦ колопроктологии имени А.Н. Рыжих» Минздрава России
Россия
ул. Саляма Адиля, д. 2, г. Москва, 123423
Список литературы
2. Жукова Л.И., Лебедев В.В., Гордин В.Н. и соавт. Острая цитомегаловирусная инфекция у взрослых не ВИЧ-инфицированных пациентов. Инфекционные болезни. 2013; т. 11, № 1, с. 37-43.
3. Cotte L, Drouet E, Bissuel F. et al. Diagnostic value of amplification of human cytomegalovirus DNA from gastrointestinal biopsies from human immunodeficiency virus-infected patients. J Clin Microbiol. 1993;31(8):2066-9.
4. Руководство по вирусологии. Вирусы и вирусные инфекции человека и животных. /под редакцией Д.К. Львова – Москва, 2013; 1197 с.
5. Ciccocioppo R, Racca F, Scudeller L, et al. Differential cellular localization of Epstein-Barr virus and human cytomegalovirus sin the colonic mucosa of patients with active or quiescent inflammatory bowel disease. Immunol Res. 2016;64(1):191-203.
6. Аглямова Т.А., Хаертынова И.М., Нугманов Р.Т. и соавт. Популяционные аспекты эпидемиологии герпесвирусных инфекций в крупном промышленном городе. Практическая медицина. 2017; № 4(105), с. 56-62.
8. Goodgame RW. Gastrointestinal cytomegalovirus disease. Ann Intern Med. 1993 1;119(9):924-35.
9. Iida T, Ikeya K, Watanabe F, Abe J. et al. Looking for endoscopic features of cytomegalovirus colitis: a study of 187 patients with active ulcerative colitis, positive and negative for cytomegalovirus. Inflamm Bowel Dis. 2013;19(6):1156-63.
10. Nowacki TM, Bettenworth D, Meister T, et al. Novel score predicts risk for cytomegalovirus infection in ulcerative colitis. J Clin Virol. 2018;105:103-108.
11. Johnson J, Affolter K, Boynton K. et al. CMV Disease in IBD: Comparison of Diagnostic Tests and Correlation with Disease Outcome. Inflamm Bowel Dis. 2018;24(7):1539-1546.
13. Pfau P, Kochman ML, Furth EE. еt al Cytomegalovirus colitis complicating ulcerative colitis in the steroid-naïve patient. Am J Gastroenterol. 2001;96(3):895-9.
15. Li Y, Xu H, Xu T, et al. Case-Control Study of Inflammatory Bowel Disease Patients with and without Clostridium difficile Infection and Poor Outcomes in Patients Coinfected with C. difficile and Cytomegalovirus. Dig Dis Sci. 2018;63(11):3074-3083.
16. Rowan C, Judge C, Cannon MD et al. Severe Symptomatic Primary CMV Infection in Inflammatory Bowel Disease Patients with Low Population Seroprevalence. Gastroenterol Res Pract. 2018;28;2018:1029401.
17. Tsuchido Y, Nagao M, Matsuura M et al. Real-time quantitative PCR analysis of endoscopic biopsies for diagnosing CMV gastrointestinal disease in non-HIV immunocompromised patients: a diagnostic accuracy study. Matsuura Eur J Clin Microbiol Infect Dis. 2018;37(12):2389-2396.
19. Schroeder KW, Tremaine WJ, Ilstrup DM. Coated Oral 5-aminosalicylic acid Therapy for midly to moderate active ulcerative colitis. A randomized study. N Engl J Med, 1987;317(26):1625-9.
20. Fajfr M, Stepánová V. Cytomegalovirus and its relationship to chronic inflammatory bowel diseases and tumors. Klin Mikrobiol Infekc Lek. 2013;19(3):103-6.
Цитомегаловирусное поражение ЖКТ на фоне иммунотерапии
У пациентов, получающих ипилимумаб и имеющих диарею или другие симптомы колита и не отвечающих на стероидную терапию (лечение иммуноопосредованного колита), должны быть исключены инфекционные причины симптомов, как например, цитомегаловирусная инфекция. Согласно данным постмаркетингового исследования, на фоне иммунной терапии возможно развитие гастроинтестинальной цитомегаловирусной инфекции, включая фатальные случаи.
Рекомендации для специалистов здравоохранения
- колит является частным побочным эффектом терапии ипилимумабом у больных с прогрессирующей меланомой. Заболевание проявляется диареей, кровью в стуле и абдоминальной болью.
- если у пациента на фоне терапии ипилимумабом возникают вышесказанные симптомы, необходимо исключить инфекционную причину симптомов, в частности, цитомегаловирусную инфекцию.
- если у пациента диагностирован стероид-резистентный вариант иммуноопосредованного колита, следует исключить другие причины симптомов (цитомегаловирус, Clostridium difficile, паразиты).
Случаи гастроинтестинальной цитомегаловирусной инфекции
Риск тяжелой диареи и колита на фоне терапии ипилимумабом
Результаты клинических исследований свидетельствуют что диарея является частым побочным эффектом терапии ипилимумабом в дозе 3 мг/кг. При этом частота диареи составляет 27%, частота колита 8%. А вот частота тяжелой диареи и колита (степень 3 и 4) достигает 5%.
В клинических исследованиях среднее время от начала терапии до развития гастроинтестинальных симптомов составило 8 недель (от 5 до 13 недель).
У пациентов с тяжелой диареей или колитом терапия должна быть отменена и назначена высокодозовая кортикостероидная терапия.
Источник: Drug Safety Update volume 12, issue 6: January 2019: 2.
Всероссийская Образовательная Интернет-Сессия
Информация и материалы, представленные на настоящем сайте, носят научный, справочно-информационный и аналитический характер, предназначены исключительно для специалистов здравоохранения, не направлены на продвижение товаров на рынке и не могут быть использованы в качестве советов или рекомендаций пациенту к применению лекарственных средств и методов лечения без консультации с лечащим врачом.
Лекарственные препараты, информация о которых содержится на настоящем сайте, имеют противопоказания, перед их применением необходимо ознакомиться с инструкцией и проконсультироваться со специалистом.
Мнение Администрации может не совпадать с мнением авторов и лекторов. Администрация не дает каких-либо гарантий в отношении cайта и его cодержимого, в том числе, без ограничения, в отношении научной ценности, актуальности, точности, полноты, достоверности научных данных представляемых лекторами или соответствия содержимого международным стандартам надлежащей клинической практики и/или медицины основанной на доказательствах. Сайт не несет никакой ответственности за любые рекомендации или мнения, которые могут содержаться, ни за применимость материалов сайта к конкретным клиническим ситуациям. Вся научная информация предоставляется в исходном виде, без гарантий полноты или своевременности. Администрация прикладывает все усилия, чтобы обеспечить пользователей точной и достоверной информацией, но в то же время не исключает возможности возникновения ошибок.
Статьи: Поражение толстой кишки, обусловленное вирусами семейства Herpesviridae.
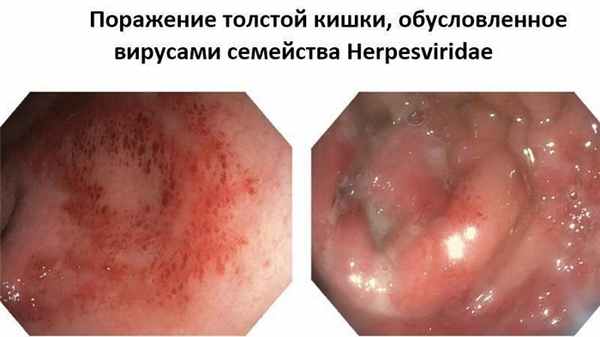
Поражение толстой кишки, обусловленное вирусами семейства Herpesviridae.
Аникина М.С. врач-эндоскопист ГБУЗ НСО «ГНОКБ»
Распространенность герпесвирусных инфекций неуклонно возрастает во всем мире. Считается, что к 18 годам 60 - 90% жителей городов инфицируются одним или несколькими типами клинически значимых герпесвирусов. Рост заболеваемости в значительной мере связан с распространением бессимптомной и недиагностированной герпетической инфекции. Это вызвано легкостью распространения инфекции (возможны контактно-бытовой, половой, воздушно-капельный, вертикальный, трансфузионный и трансплантационный механизмы передачи). Универсальный тропизм герпесвирусов обусловил значительный полиморфизм клинических проявлений, которые попадают в поле зрения врачей различных специальностей. [5]
В настоящее время известно около 200 в разной степени изученных герпесвирусов. Это крупные оболочечные ДНК-содержащие вирусы. Из них патогенными для человека являются 8 типов:
1.Вирус простого герпеса – ВПГ тип 1 (Herpes simplex virus тип 1 – HSV-1), или герпесвирус человека ГВЧ-1.
2. Вирус простого герпеса – ВПГ тип 2 (HSV-2), или ГВЧ-2.
3. Вирус ветряной оспы – опоясывающего герпеса (Varicella-zoster virus – VZV), или ГВЧ-3.
4. Вирус Эпштейна-Барр – ВЭБ (Epstein-Barr virus – EBV), или ВГЧ-4.
5. Цитомегаловирус – ЦМВ (CMV), или ГВЧ-4.
6. Герпесвирус человека тип 6 – ГВЧ-6 (Human herpesvirus – HHV6).
7. Герпесвирус человека тип 7 – ГВЧ-7 (HHV7).
8. Герпесвирус человека тип 8 – ГВЧ-8 (HHV8).
Все они относятся к семейству Herpesviridae, которое делится на три подсемейства: α-herpesviruses, β-herpesviruses и γ-herpesviruses, в зависимости от характера поражения вирусом клетки, скорости репликации, места латенции и персистенции.
Альфа-вирусы (вирус простого герпеса 1 и 2 типа, вирус варицела Зостер). Характеризуются быстрой репликацией, 4—8 часов), способностью к цитолизу и бессимптомным персистированием в нейрональных клетках.
Бета-вирусы (цитомегаловирус, герпесвирус человека тип 6, герпесвирус человека тип 7) Медленно реплицируются, вызывают цитомегалическую трансформацию клеток, а основными очагами латенции являются моноциты и их предшественники, эндотелиальные клетки сосудов микроциркуляторного русла, альвеолярные макрофаги, Т-лимфоциты и стромальные клетки костного мозга.
Гамма-вирусы (вирус Эбштейн-Барр (синоним ВГЧ4), ВГЧ-8). Трансформирующие вирусы человека, способствующие развитию злокачественного перерождения клеток. Пожизненно персистируя в В-лимфоцитах или находясь в латентном состоянии, обладают способностью делать их злокачественными.
Персистенция бета- и гамма-вирусов в иммунокомпетентентных клетках может приводить к развитию вторичной иммунной недостаточности с выраженной депрессией клеточного иммунитета.
Формы взаимодействия герпесвирусов с организмом хозяина различны. Инфекционный процесс может протекать:
1 В острой форме.
2 В хронической форме (более 6 месяцев).
3 В инаппарантной (бессимптомной) форме.
4 В форме медленной вирусной инфекции — длительный инкубационный период (месяцы и годы) с последующим медленным прогрессирующим течением, с развитием тяжелых клинических симптомов и в итоге — смертью больного.
Уникальным биологическим свойством всех ГВ человека является их способность к персистенции и латенции в организме инфицированного человека. Персистенция представляет собой непрерывное и цикличное размножение (репликацию) вируса в инфицированных клетках тропных тканей, что является причиной развития инфекционного процесса. Латенция герпесвирусов клинически себя не проявляет, а диагностируется только при наличии специфических IgG против вируса (серопозитивность) в невысоких титрах, а сам вирус в этот период в периферической крови не определяется даже таким высокочувствительным методом, как ПЦР. В состоянии латенции нарушается полный цикл репродукции вируса, и он находится в клетках хозяина в виде субвирусных структур. [4; 5]
Таблица 1 Классификация клинических форм заболеваний, обусловленных герпесвирусами [4]
Первичная инфекция
Реактивация после латенции
Вирус простого герпеса I типа — ВПГ-1-ВГЧ-1 —
Герпес кожи. Лабиальный герпес. Гингивостоматит. Офтальмогерпес. Генитальный герпес. Неонатальный герпес. Энцефалит (редко). Невропатии
Рецидивирующий орально-лабиальный герпес. Рецидивирующий аногенитальный герпес.
Вирус простого герпеса II типа — ВПГ-2-ВГЧ-2 — HSV-2
Генитально-ректальный герпес. Неонатальный герпес. Менингоэнцефалит. Крестцовый
Генитальный герпес. Менингоэнцефалит. Хроническая кожно-слизистая форма
Вирус варицелла зостер-ВВЗ — вирус герпеса человека III типа — ВГЧ3-VZV
Опоясывающий герпес. Постгерпетическая невралгия
Вирус герпеса человека IV типа — ВГЧ-4 — Эпштейна-Барр вирус —
Инфекционный мононуклеоз. Саркома мышц. Энцефалит у новорожденных. Лимфоидная интерстициальная пневмония у детей
Лимфома Беркитта. Назофарингиальная карцинома.
Волосатая лейкоплакия языка.
EBV-ассоциированный лимфопролиферативный синдром.
Синдром хронической усталости и иммунной депрессии.
Вирус герпеса человека V типа — ВГЧ-5 — Цитомегаловирус — ЦМВ-СМV
CMV-колит/холангит. CMV-адреналовая недостаточность.
Реакция отторжения трансплантата. Атеросклероз
Летальный энцефаломиелит при инфицировании людей
Вирус герпеса человека VI типа —
Внезапная экзантема у детей. Гетерофильно-негативный мононуклеоз. Васкулит
Интерстициальная пневмония у лиц с иммунодефицитом.
Синдром хронической усталости и иммунной депрессии.
Аутоиммунная патология. Психозы
Вирус герпеса человека VII типа — ВГЧ-7-HHV-7
Возможна экзантема у детей
Синдром хронической усталости и иммунной депрессии.
Заболевания кожи и ЦНС аутоиммунной природы. Рак желудка
Саркома Капоши.
Лимфопролеферативное заболевание болезнь Кастлемана
Таким образом, поражение слизистых нижних отделов желудочно-кишечного тракта может быть обусловлено вирусами простого герпеса 1 и 2 типа, цитомегаловирусом (ВГЧ 5 типа) и вирусом герпеса человека 8 типа.
Герпесвирусы 1 и 2 типов
Герпетическая инфекция, вызванная вирусом простого герпеса (ВПГ, Herpes simplex virus — HSV), — это заболевания с пожизненной персистенцией вирусов в нервных клетках (особенно в нервных ганглиях), характеризующиеся периодическими обострениями с появлением клинических признаков, локализующихся на постоянных для каждого больного «Locus minoris» — глаза, кожа, слизистые. Более чем 90 % населения планеты являются носителями ВПГ. Первичная герпетическая инфекция (ГИ) возникает при первом контакте человека с ВПГ. После короткого инкубационного периода (от 2 до 14 дней) в крови начинают определяться антитела к ВПГ, и у 80—90 % лиц первичное инфицирование протекает в латентной форме. У 10—20 % лиц имеют место клинические проявления инфекции, для которых характерен общеинфекционный синдром с лихорадкой и другими признаками интоксикации, респираторные проявления или афтозный стоматит. Возможны поражения кожи и слизистых, в том числе конъюнктивы или роговицы. Первичная ГИ, независимо от клинической формы проявления и места поражения, сопровождается проникновением ВПГ в ганглии дорсальных корешков и реже — в вегетативные ганглии и завершается их острой инфекцией с последующим установлением латентности в нейронах.
Вторичная (рецидивирующая) ГИ встречается в любом возрасте после первичного герпеса. Поскольку рецидивы возникают на фоне наличия противовирусных антител, то они протекают со слабовыраженным общеинфекционным синдромом и, как правило, на фоне болезней и/или состояний, снижающих иммунитет.
В зависимости от распространенности процесса клинически выделяются следующие формы вирусной инфекции:
1. Локализованная форма, при которой отмечается так называемый "замкнутый круг хождения вируса: входные ворота - нервный ганглий - входные ворота". Как правило, при обострении заболевания патологические изменения всегда локализуются в одном месте.
2. Распространенная форма, при которой наблюдаются отсевы вируса из очага первичной инвазии в близлежащие зоны (например, лабиальный герпес – герпетический эзофагит)
3. Генерализованные формы (висцеральная и диссеминированная), которые наиболее часто встречаются у иммунокомпрометированных пациентов.
В течение заболевания выделяют две стадии: 1 стадия - везикулов и 2 стадия - образования дефектов слизистой оболочки.
Макроскопически при 1-й стадии обнаруживаются характерные изменения слизистой оболочки пораженного сегмента толстой кишки: множественные рассеянные или сгруппированные пузырьки диаметром 0,1-0,3 см с серозным или мутным содержимым. Пузырьки склонны к слиянию. Окружающая слизистая оболочка может быть не изменена или с явлениями очагового умеренно выраженного поверхностного воспаления.
При колоноскопии во 2-й стадии заболевания имеются множественные поверхностные дефекты слизистой оболочки округлой формы, размерами до 0,5 см с четко очерченными эритематозными приподнятыми краями и некротическим налетом в дне ("вулканические" изъязвления). При тяжелых генерализованных формах инфекции дефекты слизистой оболочки сливаются с образованием обширной изъязвленной поверхности (Морозова СВ., Пархоменко Ю.Г., 2002). Контактная кровоточивость выражена умеренно, на окружающей слизистой оболочке имеются множественные субэпителиальные кровоизлияния. При морфологическом исследовании тканей, взятых из краев изъязвления, на фоне воспалительной инфильтрации слизистой оболочки выявляются типичные для этой инфекции гигантские клетки с мультинуклеацией и феноменом "глаза совы" или (в более поздние сроки) внутриядерные включения, окруженные светлой зоной (Cirillo N.W. et al., 1993). Таким образом, для герпетических колитов характерны следующие эндоскопические признаки: поражение имеет сегментарный характер, сегменты короткие, могут локализоваться в любом анатомическом отделе, но чаще обнаруживаются в прямой кишке. Макроскопические изменения в пределах пораженного сегмента однородны. (Рис.1) При хроническом прогрессирующем течении заболевания отмечаются протяженные поражения толстой кишки с элементами герпетического процесса на разных стадиях его развития. [3: 9]
Рис.1 герпетический проктит [9]
Эндоскопическая картина слизистой оболочки прямой кишки. (а) эритема, рыхлость и множественные язвенные поражения слизистой оболочки прямой кишки. (B) кроме множественных язв на поверхности слизистой присутствует слизисто-гнойный экссудат.
Клинически распознавание герпетической инфекции в типичных случаях основывается на выявлении характерной сыпи в виде группы мелких пузырьков на фоне инфильтрирации. Для подтверждения диагноза используют методы выделения вируса и серологические реакции для выявления антител. Внутриядерные вирусные включения можно обнаружить при микроскопии окрашенных по Романовскому-Гимзе соскобов и биоптатов основания везикул. Однако такие включения обнаруживаются лишь у 60% больных герпетической инфекцией. Наиболее чувствительным и достоверным методом является выделение вируса на культуре тканей. Серологические реакции (РСК, реакция нейтрализации) имеют малую информативность. Нарастание титра антител в 4 раза и более можно выявить лишь при первичной инфекции, при рецидивах лишь у 5% больных отмечается нарастание титра. Наличие положительных реакций без динамики титров можно выявить у многих здоровых людей (за счет латентной герпетической инфекции). Важно одновременно использовать несколько методов диагностики. В качестве скринингового метода рекомендуется использовать метод ПЦР, иммуноферментный анализ (ИФА) и реакцию иммунофлюоресценции (РИФ), а в качестве подтверждающего — метод выделения ВГ на чувствительных клеточных культурах. Вирусологический метод является «золотым стандартом» в диагностике ГВИ. Отличительной особенностью данного метода является высокая степень достоверности полученных результатов, а также высокая чувствительность (85— 100 %) и специфичность (100 %), возможность получения чистой культуры возбудителя для его дальнейшего изучения, в частности испытания чувствительности к антивирусньм препаратам; недостатком — длительность проведения (от 2 до 5—14 дней). [2; 4]
ЦИТОМЕГАЛОВИРУСНАЯ ИНФЕКЦИЯ
Цитомегаловирусная инфекция (ЦМВИ) — общее инфекционное заболевание, вызываемое β -герпесвирусом человека, характеризующееся многообразием форм (от бессимптомных до генерализованных), морфологически проявляющееся образованием в слюнных железах, висцеральных органах и ЦНС цитомегалов — гигантских клеток с типичными внутриядерными и цитоплазматическими включениями. Инфекция относится к антропонозам. Отличается различными механизмами передачи: капельный, гемоконтактный, контактный. Пути передачи: воздушно-капельный; артифициальный (парентеральный); контактно-бытовой (в том числе при непосредственном контакте со слюной); половой; вертикальный, трансфузионный, трансплантационный. Иммунитет нестойкий, нестерильный. Механизм развития ЦМВИ зависит от дозы вируса, путей заражения, возраста пациента, генетических особенностей и состояния иммунитета в момент заражения.
При персистенции ЦМВ выделяют две стадии: стадию продуктивной репликации и стадию латенции. Обе стадии персистирующей инфекции не являются стабильными в течение жизни человека, сменяя одна другую. В популяции не менее 10 % населения являются вирусовыделителями. Реактивация ЦМВИ обычно не сопровождается какими-либо симптомами и для организма человека протекает незаметно.
Цитомегаловирусная инфекция (ЦМВ)
Цитомегаловирус (ЦМВ, вирус герпеса человека 5 типа) может вызывать инфекции широкого диапазона тяжести. Синдром, инфекционного мононуклеоза без тяжелого фарингита, – распространенное явление. Тяжелое очаговое заболевание, включая ретинит, может развиться у зараженных ВИЧ пациентов, а также у реципиентов органов и других пациентов с ослабленным иммунитетом. Тяжелое системное заболевание может развиться у новорожденных и пациентов с ослабленным иммунитетом. Лабораторный диагноз, целесообразный при тяжелой болезни, может включать культуру, серологический анализ, биопсию или выявление нуклеиновой кислоты или антигена. Ганцикловир и другие противовирусные препараты используются для лечения тяжелого заболевания, особенно ретинита.
(См.также Обзор инфекций, вызванных герпесвирусами (Overview of Herpesvirus Infections) Обзор инфекций, вызванных герпесвирусами (Overview of Herpesvirus Infections) Людей заражают восемь типов герпесвирусов ( Герпесвирусы, которые заражают людей). После первичного инфицирования все герпесвирусы остаются латентными в пределах определенных клеток-хозяев и. Прочитайте дополнительные сведения а также Врожденная и перинатальная цитомегаловирусная инфекция (Congenital and Perinatal Cytomegalovirus Infection) Врожденная и перинатальная цитомегаловирусная (ЦМВ) Цитомегаловирусная инфекция может быть приобретена пренатально или перинатально и является наиболее распространенной врожденной вирусной инфекцией. Признаками при рождении, если они присутствуют. Прочитайте дополнительные сведенияЦитомегаловирус (герпесвирус человека тип 5) передается через кровь, или другие биологические жидкости, а также с пересаженными при трансплантации органами. Инфекция может быть приобретена трансплацентарно или во время рождения.
Распространенность увеличивается с возрастом; у 60–90% взрослых имеется цитомегаловирусная инфекция (результат длительно существующей латентной инфекции). Группы с низким социально-экономическим статусом склонны иметь более высокую распространенность.
Врожденная ЦМВ-инфекция Врожденная и перинатальная цитомегаловирусная (ЦМВ) Цитомегаловирусная инфекция может быть приобретена пренатально или перинатально и является наиболее распространенной врожденной вирусной инфекцией. Признаками при рождении, если они присутствуют. Прочитайте дополнительные сведенияПриобретенные инфекции являются часто бессимптомными.
Острое заболевание с лихорадкой, которое называется ЦМВ-мононуклеозом, может привести к развитию гепатита с повышением уровня аминотрансфераз (обычно субклинического, без желтухи) и атипичным лимфоцитозом, сходным с инфекционным мононуклеозом Инфекционный мононуклеоз Инфекционный мононуклеоз вызывается вирусом Эпштейна – Барр (ЭБВ, герпесвирус человека тип 4), проявлениями заболевания является общая слабость, лихорадка, фарингит и увеличение лимфатических. Прочитайте дополнительные сведенияПостперфузионный синдром (после переливания) может развиться через 2–4 недели после переливания препаратов крови, содержащих цитомегаловирус. Это состояние сопровождается лихорадкой, длящейся 2–3 недели, и такими же проявлениями, как при цитомегаловирусном мононуклеозе.
У пациентов с ослабленным иммунитетом цитомегаловирус – главная причина заболеваемости и смертности. Болезнь часто следует после реактивации скрытого вируса. Легкие, желудочно-кишечный тракт или ЦНС могут быть поражены. На последней фазе СПИДа цитомегаловирусная инфекция вызывает ретинит Герпесвирусы: Цитомегаловирус Увеит вызывают ряд инфекционных заболеваний (см. таблицу Инфекционные причины увеита). Наиболее распространены токсоплазмоз, вирус простого герпеса и вирус опоясывающего лишая. Различные организмы. Прочитайте дополнительные сведенияДиагностика цитомегаловируса
Обнаружение антигенов или ДНК ЦМВ
Культура мочи у младенцев
Часто биопсия у пациентов с ослабленным иммунитетом
ЦМВ-инфекцию можно подозревать у следующих категорий лиц:
Здоровые люди с мононуклеозоподобными синдромами
Пациенты с иммунодефицитом и симптомами нарушений желудочно-кишечного тракта, ЦНС или сетчатки
Новорожденные с системным заболеванием
Цитомегаловирусный мононуклеоз можно дифференцировать от инфекционного мононуклеоза Инфекционный мононуклеоз Инфекционный мононуклеоз вызывается вирусом Эпштейна – Барр (ЭБВ, герпесвирус человека тип 4), проявлениями заболевания является общая слабость, лихорадка, фарингит и увеличение лимфатических. Прочитайте дополнительные сведения .
При сероконверсии происходит появление антител к цитомегаловирусу, что указывает на развитие новой ЦМВ-инфекции. Однако в организме человека с ослабленным иммунитетом многие формы ЦМВ-заболеваний обусловлены реактивацией скрытой инфекции. Реактивация цитомегаловируса может привести к распространению вируса в мочу, другие жидкости тела или ткани, но наличие ЦМВ в жидкостях тела или тканях не всегда указывает на болезнь, а может просто представлять собой распространение вируса по организму. Поэтому биопсия, доказываюшая наличие вызванных цитомегаловирусом отклонений, часто необходима, чтобы подтвердить поражение того или иного органа. Количественное обнаружение антигена цитомегаловируса или ДНК в периферической крови может также быть очень полезным, потому что повышенная или прогрессирующая вирусная нагрузка цитомегаловируса очень часто наводит на размышления об актуальном инфекционном процессе.
Диагноз у ЦМВ-инфекции у младенцев может быть сделан при посеве мочи.
Лечение цитомегаловируса
При тяжелой болезни – противовирусные средства (например, ганцикловир, валганцикловир, фоскарнет, цидофовир)
Ретинит, вызванный цитомегаловирусом, который в основном встречается у больных СПИДом, лечат системными противовирусными средствами.
Препараты против цитомегаловируса используются, чтобы лечить тяжелую болезнь, а не ретинит, но являются менее последовательно эффективными, чем при ретините.
ЦМВ-ретинит
Препараты, применяемые для лечения ЦМВ-ретинита при индукционных и поддерживающих схемах терапии включают
Ганцикловир или валганцикловир
Фоскарнет, с ганцикловиром или без него
Большинство пациентов, получают индукционную терапию одним из следующих препаратов:
Ганцикловир назначают по 5 мг/кг внутривенно каждые 12 часов в течение 2 - 3 недель
Валацикловир 900 мг перорально каждые 12 часов в течение 21 дня
Если индукция терпит неудачу не один раз, должен использоваться другой препарат.
Поддерживающая (супрессивная) терапия назначается после индукции и состоит из:
Ганцикловир 5 мг/кг внутривенно 1 раз в день
Валганцикловир 900 мг перорально 1 раз в день
В качестве альтернативы можно давать фоскарнет с или без ганцикловира. Дозировка такова:
Индукция: Фоскарнет по 60 мг/кг внутривенно каждые 8 часов в течение 2-3 недель
Поддерживающяя терапия: Фоскарнет по 90-120 мг/кг внутривенно 1 раз в день
Побочные эффекты внутривенного фоскарнета являются существенными и включают нефротоксичность, симптоматическую гипокальцимию, гипомагниемию, гиперфосфатемию, гипокалиемию и воздействие на ЦНС. Комбинированная терапия ганцикловиром и фоскарнетом увеличивает и эффективность, и отрицательные воздействия.
Терапия цидофовиром - однин из альтернативных методов лечения. Она состоит из
Индукции: Цидофовир по 5 мг/кг внутривенно 1 раз в неделю в течение 2 недель
Поддерживающей терапии: Цидофовир по 5 мг/кг внутривенно 1 раз в две недели
Эффективность цидофовира такая же, как ганцикловира или фоскарнета. Существенные отрицательные воздействия, включая почечную недостаточность, ограничивают использование цидофовира. Данный препарат может вызвать воспаление радужной оболочки или гипотонию глаз (внутриглазное давление ≤ 5 мм рт.ст.). Потенциал для нефротоксичности может быть уменьшен, если давать пробенецид и проводить предварительную гидратацию с каждой дозой. Однако побочные эффекты пробенецида, включая сыпь, головную боль и лихорадку, могут быть достаточно существенными, чтобы его не использовать.
При любой из схем лечения лечащий врач может рассматривать возможность прекращения поддерживающей терапии после 3 месяцев терапии ЦМВ у ВИЧ-инфицированных пациентов, которые принимают антиретровирусную терапию Лечение Инфекция вирусом иммунодефицита человека (ВИЧ) вызывается одним из 2 похожих ретровирусов (ВИЧ-1 и ВИЧ-2), которые разрушают CD4+ лимфоциты и ослабляют клеточный иммунитет, увеличивая риск оппортунистических. Прочитайте дополнительные сведенияИнтравитреальная противовирусная терапия должна использоваться в сочетании с системной терапией у пациентов с ЦМВ-ретинитом, при котором прогрессивно ухудшается зрение (т.е. заболевания зрительного нерва или возле него, макулы). Даже пациенты, получающие глазные инъекции, нуждаются в системной терапии, чтобы предотвратить развитие цитомегаловирусной инфекции в другом глазу и тканях, расположенных вне глаза.
Профилактика цитомегаловируса
Профилактика или превентивное лечение (активный мониторинг пациентов по уровню вирусной нагрузки и назначение противовирусных препаратов пациентам с признаками инфекции) являются эффективными способами предотвращения развития цитомегаловирусной инфекции у пациентов после трансплантации органов или реципиентов гемопоэтических клеток, инфицированных ЦМВ и с риском развития ЦМВ инфекции. Используемые препараты включают ганцикловир, валганцикловир и фоскарнет. Летермовир является более современным препаратом с новым механизмом действия, который может быть использован для профилактики при трансплантации костного мозга. Для предотвращения ЦМВ-инфекции у реципиентов трансплантата может рассматриваться анти-ЦМВ-гипериммунный иммуноглобулин, но вопрос о его применении является спорным.
Основные положения
60–90% взрослых людей имеют латентную цитомегаловирусную инфекцию.
У здоровых детей и взрослых могут проявляться легкие неспецифические симптомы или иногда синдром, подобный мононуклеозу (при первом инфицировании ЦМВ).
Врожденная инфекция может привести к мертворождению или тяжелым, иногда фатальным постнатальным осложнениям, включая обширное повреждение печени или ЦНС.
У пациентов с тяжелым иммунодефицитом могут развиться тяжелые формы заболевания, с поражением сетчатки, легких, желудочно-кишечного тракта или ЦНС.
Противовирусные препараты могут помочь в лечении ретинита, но менее эффективны в случае повреждения других органов.
Пациентам после трансплантации с риском развития цитомегаловирусной инфекции требуется прием профилактических противовирусных препаратов или тщательный мониторинг для раннего диагностирования инфекции.
Авторское право © 2022 Merck & Co., Inc., Rahway, NJ, США и ее аффилированные лица. Все права сохранены.
Читайте также:
- Периферический вестибулярный анализатор. Клетки вестибулярного анализатора.
- Флегмонозное воспаление клетчатки язычной миндалины. Хроническое воспаление миндалин (хронический тонзиллит)
- Галакторея
- Лимфаденит при хламидиозе. Лимфаденопатия при сифилисе, роже
- Яичники. Циклические изменения в яичниках. Примордиальный, преантральный, антральный, доминантный фолликул.
