Дедифференцированная липосаркома - лучевая диагностика
Добавил пользователь Morpheus Обновлено: 27.01.2026
Липосаркома – злокачественное новообразование, происходящее из клеток жировой ткани.
По данным медицинской статистики липосаркома относится к редкому типу опухолей, поскольку частота заболеваемости составляет 2,5 случаев на 1 миллион населения. В 24% случаев липосаркомы развиваются на конечностях, а в 45% случаев - в забрюшинном пространстве. Заболеваемость среди женского и мужского населения практически одинакова. Развитие опухоли происходит преимущественно после 50 лет.
Симптомы
Симптомы липосаркомы на начальных стадиях заболеваний могут отсутствовать. По мере прогрессирования патологического процесса пациенты начинают предъявлять жалобы на появление уплотнения в мягких тканях, которое болезненное при пальпации. По мере прорастания опухоли в окружающие ткани, боль усиливается. Нарастают также признаки раковой интоксикации – слабость, потеря массы тела, повышение температуры, развивается анемия.
Клиническое течение липосарком напрямую связано с гистологическим типом опухоли.
Миксоидные липосаркомы чаще локализуются в мягких тканях конечностей, чаще - в области бедра. Этот тип липосаркомык склонен к рецидивированию и метастазированию в кости и позвоночник.
Плеоморфная липосаркома отличается высокой злокачественностью, чаще всего она локализуется в нижних конечностях, метастазирование происходит преимущественно в легкие.
Высокодифференцированная липосаркома (атипичная липоматозная опухоль) характеризуется невысоким темпом роста без метастазирования. Забрюшинная высокодифференцированная опухоль способна перерождаться в дедифференцированную форму с увеличением числа рецидивов. Метастазирование опухоли чаще происходит в печень и легкие, а также в костную ткань, яичники, почки.
Формы
Формы липосаркомы отличаются по гистологическому строению. Различают опухоли местно-агрессивные – высокодифференцированная липосаркома, составляющая до 45% от всех липосарком, и злокачественные формы – дедифференцированная (около 5%), миксоидная (до 35%) и плеоморфная (до 15%) липосаркомы.
Причины
Причины опухолевая трансформация нормальных клеток жировой ткани и превращения их в липосаркому точно не выяснены.
Причиной развития опухоли, возможно, является комплекс различных состояний - предрасполагающих факторов, к которым относят изменения в генетическом аппарате клеток (наличие мутаций), влияние окружающей среды (действие канцерогенов - токсическое влияние химических веществ, радиации), наличие вредных привычек и травмы. Считается, что злокачественное перерождение липом (доброкачественное новообразование жировой ткани) происходит в очень редких случаях.
Методы диагностики
Диагностика липосаркомы осуществляется врачом-онкологом или хирургом на основании жалоб, данных анамнеза, клинического осмотра, обязательного применения лабораторных (включая генетические) и инструментальных методов обследования. Диагностика направлена на определение клинической формы заболевания, тяжести состояния и возникающих осложнений.
Стандартные биохимические и общеклинические исследования на начальных стадиях развития опухоли могут быть не изменены.
На поздних этапах онкологического процесса в клиническом анализе крови можно обнаружить признаки анемии (снижение содержания гемоглобина), увеличение СОЭ. При метастатическом поражении различных органов возможно изменение активности ферментов печени в сыворотке крови, при наличии метастазов в кости – увеличение активности щелочной фосфатазы.
Диагноз устанавливается на основании гистологического исследования ткани опухоли, полученной путём толстоигольной или открытой биопсии. Все опухоли требуют гистологической верификации до начала лечения.
К основным методам инструментальной диагностики липосарком относят – УЗИ мягких тканей, компьютерная томография (КТ), рентгенография позвоночника, магнитно-резонансная томография (МРТ), остеосцинтиграфию (сцинтиграфия костей).
Для оценки наличия опухоли и ее связи с другими тканями, а также с магистральными сосудами проводят УЗИ пораженной области. Рекомендуется ультразвуковое исследование органов брюшной полости, забрюшинного пространства, периферических лимфатических узлов для исключения метастазов и выявления сопутствующей патологии.
МРТ позволяет оценить поражение мышц, вовлечение сосудов и нервов в опухолевый процесс, оценить распространенность опухолевого процесса, а также наличие отдаленных метастазов
Проведение компьютерной томографии органов грудной клетки и брюшной полости, а также сцинтиграфии костей скелета позволяют исключить или выявить наличие отдаленных метастазов.
Необходимость выполнения ангиографического исследования возникает для выявления возможного поражения сосудов.
Во многих случаях окончательную точку в диагностике можно поставить только после выполнения молекулярно-генетических исследований.
Белок, закодированный в гене MDM2, является регулятором работы другого белка – р53, который обладает способностью подавлять рост опухоли (является онкосупрессором). Увеличение экспрессии гена MDM2 приводит к снижению количества р53. Амплификация участка хромосомы, где локализуется ген CDK4, также связана с нарушением клеточного цикла и делением клеток, что ассоциировано с развитием рака.
Амплификация (увеличение количества) локуса гена MDM2 и локуса гена CDK4 являются диагностическими маркерами дедифференцированной липосаркомы.
Были выявлены изменения в генах FGFR1 и FGFR3 (примерно в 22% случаев) при дедифференцированной липосаркоме. Мутации в этих генах приводя к нарушению регуляции деления, роста и дифференцировки клеток.
При дедифференцированной липосаркоме обнаруживаются генные перестройки, заключающиеся в транслокации (переносе части генов) между хромосомами 12 и 16. В результате сливаются гены CHOP и TLS с образованием гибридного белка FUS-CHOP. Ген CHOP в норме кодирует белок, ответственный за блокаду роста опухоли и нормальную дифференцировку жировых клеток (адипоцитов). Образование фактически нового гена при липосаркоме после его встраивания в молодые жировые клетки (преадипоциты) приводит к угнетению роста нормальных жировых клеток и их злокачественному перерождению.
Понимание механизмов опухолевой трансформации клеток на генном уровне, помимо диагностической ценности, является крайне необходимым условием для создания лекарственных препаратов, и проведения, так называемой таргетной (целевой) терапии.
Основные используемые лабораторные исследования:
- Клинический анализ крови, лейкоцитарная формула, СОЭ;
- Биохимический анализ крови, расширенный (включая ЛДГ, мочевую кислоту).
- Гистологическое изучение ткани (биопсия).
- Иммуногистохимическое исследование биопсийного материала (исследованию онкогенов MDM2 и CDK4).
Основные используемые инструментальные исследования:
- Рентгенография пораженной области.
- УЗИ пораженной области.
- КТ/МРТ исследование (диагностика метастазов).
- Ангиография (при необходимости/поражение сосудов).
Лечение
Для лечение липосаркомы применяют хирургическое вмешательство, лучевую терапию, химиотерапию, а также комбинации этих методов.
Радикальным методом устранения злокачественного новообразования при локализованной стадии является хирургическое вмешательство – широкое иссечение опухоли. При наличии опухолей высокой степени злокачественности дополнительно применяют лучевую и химиотерапию
В ряде исследований было показано, что применение лучевой терапии, как до хирургического лечения, так и после, не влияло на выживаемость пациентов.
При лечении местно-распространенных форм опухоли высокой злокачественности с высоким риском рецидивирования используются комбинированные методики – лучевая терапия, химиотерапия, гипертермия в сочетании с химиотерапией, изолированная (регионарная) перфузия опухолей конечностей высокими дозами цитостатиков – мелфалана, совместно с цитокинами (например, с фактором некроза опухоли ФНО-альфа).
При диссеминированных формах с целью уменьшения размеров опухоли и ее дальнейшего хирургического удаления применяют неоадъювантную терапию (терапия до хирургического вмешательства) – лучевую и химиотерапию.
Осложнения
Осложнения лимфосаркомы - метастазирование в легкие, печень, кости и другие органы, рецидив опухоли, сдавление нервов и сосудов. Сдавление растущей опухолью нервовприводит к развитию парезов и параличей. Сдавление кровеносных сосудов может стать причиной тромбозов и флебитов. Прогрессирование заболевания сопровождается развитием анемии.
Профилактика
Специфической профилактики липосарком не существует. Следует избегать контактов с химически вредными веществами, травмирования мягких тканей, радиационного облучения.
Какие вопросы следует задать врачу
Возможно ли образование липосаркомы из липомы ?
Может ли образоваться липосаркома на бедре, если несколько лет назад в этой области был нанесен сильный удар?
Советы пациенту
При наличии болезненного образования под кожей следует незамедлительно обратитесь к врачу.
ПЕРВИЧНАЯ ДЕДИФФЕРЕНЦИРОВАННАЯ ЛИПОСАРКОМА ПЕЧЕНИ: ПЕРВОЕ В РУССКОЯЗЫЧНОЙ ЛИТЕРАТУРЕ КЛИНИЧЕСКОЕ НАБЛЮДЕНИЕ. ОПИСАНИЕ СЕМИОТИКИ ПРИ МРТ С ГАДОКСЕТОВОЙ КИСЛОТОЙ
Первичная липосаркома печени - чрезвычайно редкое заболевание, на настоящий момент в зарубежной литературе опубликовано всего 13 случаев. Мы представляем клиническое наблюдение пациента с первичной липосаркомой печени и первый опыт применения гепатоспецифического магнитно-резонансного контрастного средства (гадоксетовой кислоты) для ее диагностики. Пациент 69 лет обратился с жалобами на боли в правом подреберье и субфебрильную температуру. При МРТ в обеих долях печени определялось многоузловое образование, неоднородного повышенного на Т2-ВИ МР-сигнала с участками гипоинтенсивного сигнала на последовательностях с подавлением жира (FatSat). Образование ограничивало диффузию на DWI и ADC-картах. При динамическом контрастировании в паренхиматозную фазу отмечалось равномерное распределение контрастного препарата по перегородкам и в многочисленных узлах образования. В гепатоспецифические фазы контрастирования отмечалось медленное вымывание КВ из отдельно лежащих узлов и перегородок образования. После хирургического удаления опухоли макропрепарат представлял собой красно-желтую, мягко-эластичную распадающуюся опухоль с наличием кровоизлияний и очагов некроза. При последующем гистологическом и иммуногистохимическом исследовании - ткань опухоли соответствует дедифференцированной липосаркоме.
Ключевые слова
Об авторах
Список литературы
1. Peterson J. J., Kransdorf M. J., Bancroft L. W., O’Connor M. I. Malignant fatty tumors: classification, clinical course, imaging appearance and treatment // Skeletal Radiology.- 2003.- Vol. 32, № 9.- Р. 493-503.
2. Fletcher C. D. M., Unni K. K., Mertens F World Health Organization Classification of Tumours. Pathology and Genetics of Tumours of Soft Tissue and Bone.- Lyon: IARC Press, 2002
3. Sung M. S., Kang H. S., Suh J. S., Lee F. H., Park J. M., Kim J. Y. et al. Myxoid liposarcoma: appearance at MR imaging with histologic correlation // Radiographics.- 2000.- Vol. 20.- Р. 1007-1019.
4. Tateishi U., Hasegawa T., Beppu Y., Satake M., Moriyama N. Primary dedifferentiated liposarcoma of the retroperitoneum. Prognostic significance of computed tomography and magnetic resonance imaging features // J. Comput. Assist. Tomogr.- 2003.- Vol. 27.- Р. 799-804.
5. Gebhard S., Coindre J. M., Michels J. J. et al. Pleomorphic liposarcoma: clinicopathologic, immunohistochemical, and follow-up analysis of 63 cases: a study from the French Federation of Cancer Centers Sarcoma Group // Am. J. Surg. Pathol.- 2002.- Vol. 26.- Р. 601-616.
6. Garces C. A., Reith J. D., Grobmyer S. R., Hochwald S. N. Isolated metastatic extremity liposarcoma to the liver, an uncommon and transient finding // World J. Surg. Oncol.- 2008.- Vol. 6.- Р. 108.- doi: 10.1186/1477-7819-6-108.
7. Wolloch Y., Dintsman M., Garti I. Primary malignant tumors of the liver // Israel Journal of Medical Sciences.- 1973.- Vol. 9, № 1.- Р. 6-11.
8. Kim T. W., Reyes C. V. Myxoid liposarcoma mimicking fuid density // Journal of Surgical Oncology.- 1985.- Vol. 30, № 2.- Р. 80-82.
9. Kim Y. I., Yu E. S., Lee K. W., Park E. U., Song H. G. Dedifferentiated liposarcoma of the liver // Cancer.- 1987.- Vol. 60, № 11.- Р. 2785-2790.
10. Golebiowski L., Abycht K. Primary liposarcoma of the liver // Wiad Lek.- 1987.- Vol. 40.- Р 1064-1066.
11. Chen W. J., Lee J. C., Hung W. T. Primary malignant tumor of liver in infants and children in Taiwan // J. Pediatr. Surg.- 1988.- Vol. 23.- Р 457-461.
12. Soares F. A., Landell G. A. M., Peres L. C., Oliveira M. A., Vicente Y. A. M. V A., Tone L. G. Liposarcoma of hepatic hilum in childhood: Report of a case and review of the literature. Medical and Pediatric Oncology.- 1989.- Vol. 17, № 3.- Р 239-243.
13. Aribal E., Berberoglu L. Primary liposarcoma of the liver // American Journal of Roentgenology.- 1993.- Vol. 161.- Р 1331-1332.
14. Wright N. B., Skinner R., Lee R. E. J., Cra A. W. Myxoid liposarcoma of the porta hepatis in childhood // Pediatric Radiology.- 1993.- Vol. 23, № 8.- Р 620-621.
15. Nelson V., Fernandes N. F., Woolf G. M., Geller S. A., Petrovic L. M. Primary liposarcoma of the liver: a case report and review of literature // Archives of Pathology & Laboratory Medicine.- 2001.- Vol. 125.- Р 410-412.
16. Khan A., Sherlock D. J., Wilson G. et al. Sonographic appearance of primary liver liposarcoma // J. Clin Ultrasound.- 2001.- Vol. 29.- Р. 44-47.
17. Kuo L. M., Chou H. S., Chan K. M., Yu M. C., Lee W. C. A case of huge primary liposarcoma in the liver // World Journal of Gastroenterology.- 2006.- Vol. 12, № 7.- Р 1157-1159.
18. Kim J. L., Woo J. Y., Lee M. J. et al. Imaging findings of primary well-differentiated liposarcoma of the liver: a case report // Acta Radiologica.- 2007.- Vol. 48, № 10.- Р 1061-1065.
19. Fang S. C., Chang C. K., Lin Y. C., Yu C.Y., Liu C. H., Huang G. S. Primary hepatic liposarcoma diagnosed by dynamic computed tomography // J. Radiol Sci.- 2011.- Vol. 36.- Р 113-117.
20. Steven G., Silverberg R., Delelis A. Principles and Practice of Surgical Pathology and Cytopathology.- 3rd ed.- New York: Churchill Levingstone, 2004.
21. Murphey M. D., Arcara L. K., Fanburg-Smith J. From the archives of the AFIP: imaging of musculoskeletal liposarcoma with radiologic-pathologic correlation // Radiographics.- 2005.- Vol. 25.- Р 1371-1395.
22. Sommer W. H., Sourbron S., Huppertz A., Ingrisch M., Reiser M. F. Zech Contrast agents as a biological marker in magnetic resonance imaging of the liver: conventional and newapproaches // C. J. Abdom. Imaging.- 2012.- Vol. 37 (2).- Р 164-179.
Дедифференцированная липосаркома - лучевая диагностика
М.Д. Алиев
Российский онкологический научный
центр им. Н.Н. Блохина РАМН, г. Москва
Онкологическая ортопедия — мультидисциплинарная наука, появившаяся в конце XX в. и объединившая в себе новейшие достижения онкологии. Научные и практические достижения школы академика Трапезникова Н.Н. послужили всеобщему признанию онкоортопедии. Химиотерапия, радиотерапия, ортопедия, травматология, общая хирургия, микро- и сосудистая хирургия, реконструктивная восстановительная хирургия, нейрохирургия, патоморфология, лучевая диагностика – это далеко не весь перечень специальностей составляющих онкологическую ортопедию. Специалисты, занимающиеся диагностикой и лечением опухолей опорно-двигательного аппарата, должны владеть широкими знаниями и навыками в различных разделах фундаментальной и прикладной медицинской науки.
Отличительной особенностью современной онкоортопедии является тесное сотрудничество клиницистов различных специальностей – хирургов, патоморфологов, радиологов, нейрохирургов, химиотерапевтов, ортопедов, и именно это позволяет в результате мультидисциплинарного подхода получить хорошие результаты всего лечения.
В течение последних 20 лет тактика лечения сарком костей и мягких тканей претерпела значительные изменения. Использование современных методов лекарственной, лучевой терапии и расширенных хирургических вмешательств при метастатическом поражении костей, наряду с первичными опухолями, привело к резкому увеличению контингента пациентов, нуждающихся в онкоортопедическом пособии. С применением комбинированных методов лечения с использованием химиотерапии и лучевой терапии удалось значительно увеличить результаты общей и безрецидивной выживаемости у этой группы больных. Реальное улучшение качества жизни пациентов с вторичными поражениями длинных трубчатых костей, позвоночного столба, костей таза приводит к расширению возможностей дальнейшей терапии больных раком молочной железы, почки, легких, колоректального рака, лимфом и т. д.
В то же время прослеживается тесное сотрудничество клиницистов с представителями фундаментальных наук.
Только совместные усилия единой команды специалистов – патологи, биохимики, диагносты, химиотерапевты, ортопеды, микрохирурги, пластические хирурги, неврологи, нейрохирурги, лучевые терапевты и т. д., могут привести к улучшению результатов лечения сарком костей и мягких тканей.
Для дальнейшего кооперирования разных специалистов в различных клиниках нашей страны в 2009 г. создана «Восточно-европейская группа по изучению сарком». Основной задачей единомышленников является улучшение качества оказания высокотехнологичной медицинской помощи больным саркомами костей, мягких тканей и опухолями кожи на территории Российской федерации и стран СНГ, а также научная и образовательная деятельность в этой сфере.
Стандартизация диагностических и лечебных походов позволит резко улучшить качество оказания медицинской помощи больным с злокачественными опухолями костей, мягких тканей и кожи. Использование единых систем классификации, стадирования, шкал оценок эффективности лечения, показаний к различным методам лечения, онкологических, функциональных эстетических результатов существенно облегчит коммуникацию различных клиник. Все это позволит грамотно и на одном языке излагать резуль таты терапии, проводить совместные научные, клинические исследования.
Злокачественные опухоли мягких тканей
Саркомы – сравнительно редкая группа опухолей. В России регистрируется около 10 000 новых случаев, что составляет 1% всех злокачественных новообразований. Заболеваемость составляет 30 случаев на 1 000 000 населения и 80% составляют саркомы мягких тканей. В детском возрасте частота выше и составляет 6,5%.
Гистологический спектр сарком очень широк, это объясняется тем, что они происходят из эмбриональных мезенхимальных клеток, которые впоследствии могут дифференцироваться в клетки поперечно-полостатой, гладкой мускулатуры, жировую или соединительную ткань, кости или хрящи. К саркомам мягких тканей принято также относить опухоли периферических нервов, которые имеют эктодермальное происхождение, но схожи по тактике лечения, клинике и прогнозам с саркомами мягких тканей.
В настоящее время выделяется более 50 различных гистологических подвидов, обладающих вариабельной чувствительностью к многокомпонентному лечению, что требует кардинально отличающихся лечебных подходов и алгоритмов. Саркомы, объединенные в одном гистологическом варианте, но имеющие разную степень злокачественности G1–G3, представляют собой три абсолютно разные по течению, прогнозу и лечебной тактике опухоли.
С конца прошлого века верифицированный диагноз «диссеминированная саркома мягких тканей» для большинства химиотерапевтов означал, что необходимо следовать определенному алгоритму лечебных мероприятий, в наши дни эта концепция полностью изменилась. Сейчас без гистологического и иммуногистохимического определения типа саркомы с указанием степени злокачественности построение лечебной тактики просто невозможно.
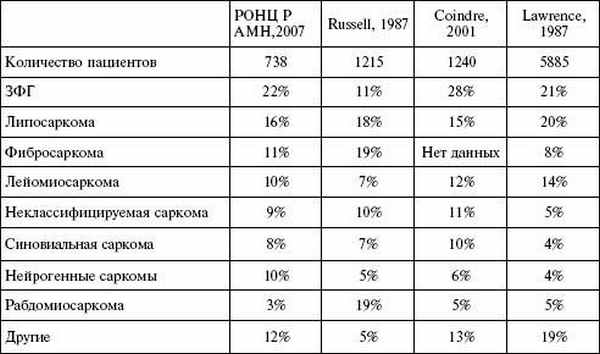
В табл. 1 представлены данные по частоте встречаемости различных гистологических подтипов за последние 20 лет.
Важное место в изучении мягкотканых сарком занимает гистологическая техника. Идентификация гистиопринадлежности опухоли в ряде случаев возможна только с исправлением электронной микроскопии, иммуноморфологических методов, исследовании некоторых маркеров к элементам цитоскелета.
Опухоли из жировой ткани
- Дедифференцированная липосаркома
- Миксоидная липосаркома
- Плеоморфная липосаркома
- Круглоклеточная липосаркома
- Смешанная липосаркома
Опухоли фиброгистиоцитарного ряда
- Плеоморфоная злокачественная фиброзная гистиоцитома/недифференцированная плеоморфная саркома
- Гигантоклеточная злокачественная фиброзная гистиоцитома/дедифференцированная плеоморфная саркома с гигантскими клетками
- Злокачественная фиброзная гистиоцитома с выраженным воспалительным компонентом/недифференцированная плеоморфная саркома с выраженным воспалительным компонентом
ЗФГ - злокачественная фиброзная гистиоцитома
Ниволумаб с ипилимумабом и без него, а также лучевая терапия при лечении пациентов с рецидивирующей или резектабельной недифференцированной плеоморфной саркомой или недифференцированной липосаркомой до операции
Исследование фазы II неоадъювантной блокады контрольных точек у пациентов с хирургически резектабельной недифференцированной плеоморфной саркомой и недифференцированной липосаркомой
В этом исследовании фазы II изучается, насколько хорошо ниволумаб с ипилимумабом и без облучения терапия перед операцией работает при лечении пациентов с недифференцированным плеоморфная саркома или дедифференцированная липосаркома, которые можно удалить хирургическим путем. Иммунотерапия моноклональными антителами, такими как ниволумаб и ипилимумаб, может помочь иммунная система организма атакует рак и может препятствовать способности опухолевых клеток к расти и распространяться. Лучевая терапия использует рентгеновские лучи высокой энергии для уничтожения и уменьшения опухолевых клеток. опухоли. Назначение ниволумаба, ипилимумаба и лучевая терапия могут лучше помочь в лечении пациенты с недифференцированной плеоморфной саркомой.
ОСНОВНЫЕ ЗАДАЧИ: I. Оценить патологический ответ на монотерапию ниволумабом и ниволумабом и ипилимумабом. комбинированная терапия, проводимая в условиях неоадъювантной терапии, с лучевой терапией и без нее в пациенты с первичными или местно-рецидивирующими операбельными недифференцированными, ранее не получавшими лечения плеоморфная саркома и дедифференцированная липосаркома. ВТОРИЧНЫЕ ЗАДАЧИ: I. Чтобы оценить изменение процента жизнеспособных опухолевых клеток, процента гиалинизации и некроза, пролиферация фосфогистоном H3 в образцах биопсии, полученных на исходном уровне и во время лечения и хирургические образцы. II. Оценить изменение иммунного инфильтрата в ответ на неоадъювантный ниволумаб. монотерапия и неоадъювантная комбинированная терапия ниволумабом и ипилимумабом у пациентов с резектабельная недифференцированная плеоморфная саркома и дедифференцированная липосаркома. III. Оценить частоту объективного ответа (ЧОО) монотерапии ниволумабом и ниволумабом и Комбинированная терапия ипилимумабом, назначаемая в условиях неоадъювантной терапии, по оценке с помощью изображений (Критерии оценки ответа на солидные опухоли [RECIST] 1.1 и иммунный ответ Критерии [irRC]) у пациентов с резектабельной недифференцированной плеоморфной саркомой и дедифференцированная липосаркома. IV. Оценить 12- и 24-месячную безрецидивную выживаемость (RFS) и общую выживаемость (OS) пациентов с операбельной недифференцированной плеоморфной саркомой и дедифференцированной липосаркома, леченная неоадъювантной монотерапией ниволумабом или ниволумабом и ипилимумабом комбинированная терапия. V. Оценить безопасность монотерапии ниволумабом и комбинации ипилимумаба и ниволумаба. в неоадъювантных условиях и в периоперационном периоде в соответствии с Общими критериями терминологии для неблагоприятных События (CTCAE) версии 4.0 критерии. ИССЛЕДОВАТЕЛЬСКИЕ ЗАДАЧИ: I. Определить иммунологические и геномные маркеры, коррелирующие с клиническим ответом на монотерапия ниволумабом и ипилимумаб с комбинированной терапией ниволумабом. II. Оценить качество жизни пациентов с дедифференцированной липосаркомой и недифференцированная плеоморфная саркома, подвергающаяся неоадъювантной иммунотерапии с последующей хирургическая резекция. III. Анализировать микробиом, чтобы определить роль микробиома в развитии и ответ на терапию. ПЛАН: Пациенты рандомизированы в 1 из 4 групп. ARM A: пациенты получают ниволумаб внутривенно (IV) в течение 1 часа в дни 1, 15 и 29 в отсутствие прогрессирования заболевания или неприемлемая токсичность. Затем пациенты проходят стандартную хирургическая операция в течение 2 недель после 43-го дня. ARM B: пациенты получают ниволумаб, как в группе A. Пациенты также получают ипилимумаб внутривенно более 90 лет. минут в день 1 при отсутствии прогрессирования заболевания или неприемлемой токсичности. Пациенты затем пройти стандартную хирургическую операцию в течение 2 недель после 43-го дня. ARM C: пациенты получают ниволумаб внутривенно более 1 часа в дни 1, 15, 29 и 43. Пациенты также проходить лучевую терапию (ЛТ) один раз в день (QD) в течение 5 дней в течение 15-47 дней при отсутствии прогрессирование заболевания или неприемлемая токсичность. Затем пациенты проходят стандартную хирургическую операцию. в течение 2 недель после 71 дня. ARM D: пациенты получают ниволумаб, как в группе C, ипилимумаб, как в группе B, и ЛТ, как в группе C, в отсутствие прогрессирования заболевания или неприемлемая токсичность. Затем пациенты проходят стандартную операции по уходу в течение 2 недель после 71 дня. После завершения исследуемого лечения пациенты наблюдаются через 6 и 18 недель, а затем каждые 3 месяца на срок до 2 лет.
Современные методы лечения липосаркомы в Израиле
Липосаркома – самый распространенный вид сарком мягких тканей. Эта опухоль составляет более 20% всех сарком, которые выявляются у взрослых. Новообразование возникает из клеток жировой ткани.
Причины липосарком неизвестны. Доказано, что крайне редко эти опухоли развиваются из доброкачественных жировых опухолей – липом. В некоторых случаях липосаркомы образуются после перенесенных травм.
Заболевание чаще диагностируется у мужчин, чем у женщин. Средний возраст пациентов на момент постановки диагноза составляет 50 лет. У детей этот вид опухоли встречается крайне редко.
Симптомы заболевания
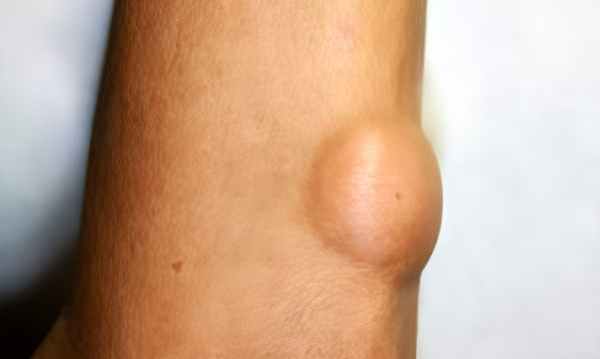
Первым симптомом липосаркомы становится шишка – безболезненная, мягкая или твердая на ощупь. Шишка медленно увеличивается в размерах. Болезненность возникает лишь тогда, когда липосаркома вырастает настолько, что начинает сдавливать окружающие ткани.
Липосаркомы брюшной полости на ранних стадиях не вызывают симптомов, поэтому они чаще всего обнаруживаются тогда, когда достигают значительной величины: в некоторых случаях опухоль при ее первичном обнаружении весит около 1 кг или даже больше.
На более поздних стадиях развития заболевания возникают:
- Болезненный отек в пораженной области;
- Ограничение диапазона движений пораженной конечности;
- Онемение конечности;
- Утомляемость;
- Боль в животе (при саркоме забрюшинного пространства);
- Немотивированная потеря веса;
- Тошнота;
- Рвота.
Виды липосарком
Выделяют 5 видов липосарком:
- Атипичная липоматозная опухоль (хорошо дифференцированные липосаркомы) – наиболее распространенный тип липосаркомы, отличающийся низкой степенью злокачественности;
- Дедифференцированная липосаркома – опухоль, образующаяся при постепенном злокачественном перерождении неагрессивной липосаркомы;
- Миксоидная липосаркома – опухоль средней и высокой степени злокачественности;
- Плеоморфная липосаркома – наиболее злокачественный вид липосаркомы;
- Миксоидная плеомаорфная липосаркома.
Расположение липосарком обычно связано с их видом. Хорошо дифференцированные липосаркомы чаще всего образуются в мягких тканях конечностей и забрюшинного пространства. Миксоидные и плеоморфные опухоли обнаруживаются преимущественно в конечностях, а дедиференцированные – в забриющинном пространстве.
Диагностика
Для выявления липосарком и их отличия от доброкачественных образований применяются следующие методы диагностики:
У врача вызывают подозрение любые шишки, размер которых превышает 5 см, расположенные в глубине тканей и прикрепленные к структурам, расположенными ниже. При обнаружении таких образований доктор назначает пациенту дополнительные исследования.
- Чем отличается липосаркома от липомы на УЗИ?
Основное отличие липомы от липосаркомы на УЗИ – это отсутствие кровотока в тканях доброкачественного образования. В липосаркоме, как в других раковых опухолях, фиксируется васкулярицация – кровеносные сосуды, по которым к опухоли поступает кровь. Кроме того, плотность липомы равномерна – в отличие от липосаркомы, которая включает участки как повышенной, так и пониженной плотности.
Эти исследования позволяют определить тип липосарком: они различаются по внешнему виду на снимках. Кроме того, компьютерная томография грудной клетки считается оптимальным методом обнаружения метастазов саркомы в легких.

Исследование дает возможность обнаружить кровеносные сосуды, питающие опухоль, и таким образом отличить злокачественное образование от доброкачественного. Ангиография нередко применяется для планирования хирургической резекции опухоли.
Этот метод визуализации позволяет обнаружить метастазы опухоли. Он также используется для оценки злокачественности опухоли и определения прогноза заболевания.
При липосаркомах чаще всего проводится открытая биопсия. При небольших поверхностных опухолях выполняется эксцизионная биопсия, т.е. новообразование удаляется целиком. Взятый материал направляется в лабораторию для анализа.
Как сэкономить на лечении
Фото клиники Ихилов












Методы лечения
Основной вид лечения липосарком – хирургическое удаление опухоли. Однако при крупных новообразованиях или при саркомах высокой степени злокачественности применяется комбинированное лечение, включающее операцию и химиотерапию или лучевую терапию.
Операция может стать единственным видом лечения небольших липосарком, не распространившихся на близлежащие органы и ткани. Если опухоль расположена на конечности, в 95% случаев израильским хирургам удается сохранить пораженную руку или ногу.
Облучение часто проводится в комплексе с хирургической операций. Это позволяет избежать рецидивов в 85-90% случаев. Радиотерапия может быть проведена при липосаркоме до операции или после нее. Используется также интраоперационная лучевая терапия, которая проводится непосредственно во время операции – сразу после удаления опухоли.
В клинике Топ Клиник Ихилов для терапии метастатических липосарком применяется современные химиопрепараты:
Клинические испытания показали улучшение выживаемости пациентов при применении этих препаратов.
Отзыв пациентки о лечении онкологического заболевания в Top Clinic Ichilov
Чтобы получить точную цену лечения в Top Clinic Ichilov и записаться на диагностику и лечение:
Читайте также:
