Эффективность перевязки легочной артерии. Перевязка легочной артерии при пневмэктомии
Добавил пользователь Alex Обновлено: 27.01.2026
Алмабаев Ы.А. 1 Алмабаева А.Ы. 2 Мусаев А.Т. 1 Серикпаев Ж.Ж. 2 Лесбекова Р.Б. 3 Нурмуханбетова Д.К. 3 Махатов Б.М. 4 Угланов Ж.Ш. 1 Жолдыбаев С.С. 1 Исмайлов Д.И. 3 Бухарбеков Б.Б. 3 Алдабергенов Е.Н. 1 Колбекова А.А. 3 Ермаханова А.Б. 3
Проведено экспериментальное исследование на животных, у которых изучались показатели состояния гемодинамики в катамнезе после пульмонэктомии. Радиоизотопным методом изучено состояние легочного артериального, легочного тканевого и портального кровотоков от момента перевязки легочной артерии до одного месяца после пульмонэктомии. Оценка состояния гемодинамики проводились на 1 и 3 часы, 1; 3 и 7 сутки и через месяц. У исследуемых собак изучены давления в легочном стволе, в левом предсердии, в воротной вене и в бедренной артерии при пульмонэктомии. Результаты исследования показали, что пульмонэктомия одного легкого значительно нарушает кровоток оставшегося легкого, которое наступает в момент перевязки легочной артерии. При пульмонэктомии самое критическое снижение кровотока наступает в течение первых трех суток после операции.
2. Малахова М. Я. Эндогенная интоксикация как отражение компенсаторной перестройки обменных процессов в организме // Эфферентная терапия. – 2000. – № 6. – С. 3-14.
3. Мороз В. В. Стратегия и тактика применения антигипоксантов при критических состояниях // Фундаментальные проблемы реаниматологии (Избранные лекции и обзоры). Труды института общей реаниматологии РАМН. – М., 2005. – № 4. – С. 210-220.
4. Пестряков Е. В., Яковлев И. И., Мороз В. В. Патофизиологические механизмы развития острого паренхиматозного повреждения легких с сепсисом и септическим шоком // Анестезиол и Реаниматол. – 2003. – № 6. – С. 65-72.
5. Паршин В. Д., Белов Ю. В., Выжигина М. А., Чарчан Э. Р., Паршин В. В., Головинский С. В. Пневмонэктомия слева с резекцией и протезированием нисходящего отдела аорты, по поводу рака легкого // Хирургия. – 2010. – № 9. – С. 61-63.
6. Bellance N., Benard G., Furt F., et al. Bioenergetics of lung tumors: alteration of mitochondrial biogenesis and respiratory capacity // Int J Biochem Cell Biol. – 2009. – № 41. – P. 2566-2577.
7. Fehrenbach H., Voswinckel R., Michl V., Mehling T., Seeger W. and Nyengaard J. R., Neoalveolarisation contributes to compensatory lung growth following pneumonectomy in mice // EurRespir J, 2008. – Vol. 27, no.1 (Jan), pp.73-76. ISSN 0903-1936.
8. Martin G. S., Bernard G. R., Airway and lung in sepsis. Intensive care // International Sepsis Forum. Med 2001. – № 27:Suppl 1, pp. 63-79.
9. Jackson S.R., Lee J., Reddy R., Williams G.N., Kikuchi A., Freiberg Y., Warburton D. and Driscoll B. Partial pneumonectomy of telomerase null mice carrying shortened telomerase initiates cell growth arrest resulting in a limited compensatory growth response// Am J Physiol, 2011. – Vol. 281, no. 5 (Nov), pp. L1279-1287,ISSN1040-0605.
Актуальность проблемы. Заболевания органов дыхания на сегодняшний день являются одним из самых распространенных во всем мире [2,3]. В повышении эффективности лечения больных с патологией органов дыхания одним из важных мест занимают хирургические методы [1,5]. Признанным радикальным методом хирургического лечения больных раком, туберкулезом легкого и неспецифическими нагноительными заболеваниями легких является пульмонэктомия [6]. Пульмонэктомия, сопровождающаяся значительным уменьшением объема сосудистого русла малого круга кровообращения и дыхательной поверхности, дает высокий процент послеоперационных осложнений и летальности [4,7]. Несмотря на это, удельный вес пульмонэктомии среди всех операций, выполненных по поводу туберкулеза, рака и неспецифических заболеваний органов дыхания, остается на высоком уровне [8,9]. Анализ литературных данных показал, что тяжесть и своеобразие течения послеоперационного периода определяется нарушениями гемодинамики и функции жизненно важных органов, что определяет актуальность данной проблемы.
Цель исследования. Изучить показатели состояния гемодинамики в катамнезе при пульмонэктомии у экспериментальных животных.
Объем и методы исследований. Объектом экспериментальных исследований явились 45 беспородных взрослых собак. Все животные до операции наблюдались в карантине, где изучались контрольные данные гемодинамики.
Для решения поставленных задач нами были проведены 2 серии экспериментов:
1 серия – контрольная торакотомия выполнена только слева;
2 серия – пульмонэктомия слева общим методом (без шунтирования), что способствовало удалению 42–43 % массы легочной ткани.
Радиоизотопным методом изучено состояние легочного артериального, легочного тканевого и портального кровотоков от момента перевязки легочной артерии до одного месяца после пульмонэктомии. Оценка состояния гемодинамики проводились на 1 и 3 часы, 1; 3 и 7 сутки и через месяц.
Результаты и обсуждения. Результаты изучения давления в легочном стволе, в левом предсердии, в воротной вене и бедренной артерии в ходе операции пульмонэктомии слева представлены в диаграмме 1. Из диаграммы следует, что после торакотомии давление в легочной артерии составило 20±1,0 мм рт. ст., в левом предсердии – 10,0±0,4 мм рт. ст., в воротной вене – 9±0,4 мм рт. ст., а в бедренной артерии – 93±2,2 мм рт. ст.
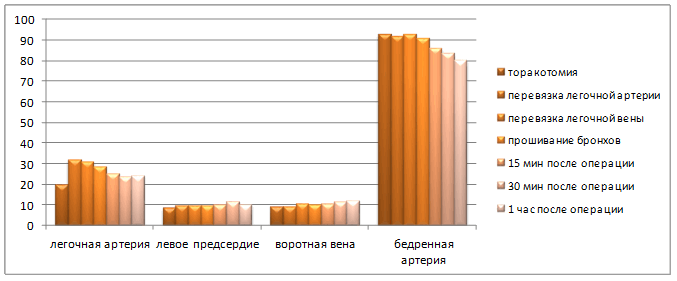
Диаграмма 1. Показатели давления в ходе операции пульмонэктомии слева (М±m мм рт. ст.)
Через час после левосторонней пульмонэктомии общепринятым способом давление в легочном стволе было на 30 % больше, чем у торакотомированных животных, и было статистически достоверным. Устойчивое повышение давления в системе легочных артерий, возникающее после пульмонэктомии вследствие уменьшения сосудистого русла, в свою очередь, приводит к снижению давления в левом предсердии (10,1±0,8 мм рт. ст.) на 20,2 %, а в воротной вене, наоборот, к повышению давления на 33,3 %. На этом фоне отмечается дальнейшее снижение давления в бедренной артерии до 13,0 % (р<0,05). Следовательно, повышение давления в легочном стволе может привести к развитию флебогипертензии в бассейне воротной вены и снижению системного артериального давления. Увеличение давления в левом предсердии на этапах операции мы объясняем перевязкой легочных сосудов, так как они являются барорецепторными полями малого круга кровообращения. В дальнейшем необходимо было проследить влияние нарушенной гемодинамики после пульмонэктомии на состояние кровотока в воротной вене и тканях и сосудах легкого.
В диаграмме 2 представлены данные кровотока после пульмонэктомии. Из диаграммы видно, что контрольные замеры в легочном артериальном кровотоке равнялся 128±4,8, легочном тканевом кровотоке – 84±3,7 мл/мин/100г и в портальном кровотоке – 68±2,0 мл/мин/100г.
Перевязка левой легочной артерии приводит к достоверному снижению легочного артериального кровотока на 24,2 %, легочного тканевого кровотока на 7,1 %, а портальный кровоток находится на уровне исходных величин.
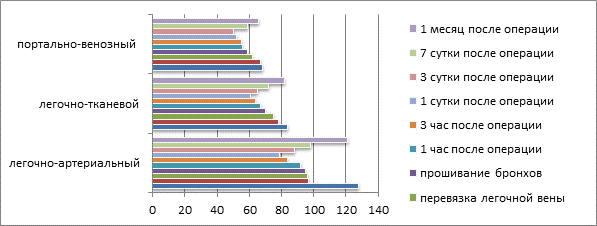
Диаграмма 2. Показатели кровотока при пульмонэктомии слева (М±m мл/мин/100г)
Прошивание бронхов вызвало достоверное снижение легочного артериального кровотока на 25,8 %, что, в свою очередь, привело к снижению легочного тканевого кровотока и составило 70±1,6 мл /мин/ 100г. Этот показатель на 16,7 % ниже контрольной величины. Установленные нарушения кровотока в малом круге кровообращения привели к нарушению портальной гемодинамики. Портальный венозный кровоток достоверно снижается (р<0,05) до 59±2,9 мл/мин/100г, что на 13,2 % меньше исходных величин.
Через один час после пульмонэктомии, легочной артериальный кровоток снизился на 28,1 %, локальный легочной тканевой кровоток – на 28,2 %, портальный венозный кровоток – на 17,7 %. При этом снижение кровотоков было статистически достоверным (р<0,05).
Через 3 часа после операции во всех изучаемых объектах продолжается дальнейшее достоверное снижение кровотока в исследуемых органах. При этом легочный артериальный кровоток составил 84±4,3 мл/мин/100г, локальный лёгочно-тканевой – 64±1,8 мл/мин/100г и портально-венозный – 55±2,5 мл/мин/100г.
Максимальное снижение легочного артериального, легочного тканевого кровотока наступило через сутки после операции, а портально-венозного кровотока – на 3-е сутки. На 7-е сутки после пульмонэктомии отмечается тенденция к повышению изучаемых кровотоков по сравнению с предыдущим сроком. При этом легочной артериальный кровоток составил 98±3,8 мл/мин/100г, легочно-тканевой кровоток – 72±2,4 мл/мин/100г и портальный венозный кровоток – 59±1,4 мл/мин/100г. Однако при сравнительном изучении с контрольным показателем цифры указывали на их достоверное снижение. Анализ полученных данных через месяц после операции показал, что отмечается значительное улучшение гемодинамики в легком, но полного восстановления изучаемых показателей кровотока не наступает.
Выводы. Удаление одного легкого значительно нарушает гемодинамику оставшегося легкого, которое наступает в момент перевязки легочной артерии. Нарушение легочного кровотока в свою очередь приводит к нарушению портально-венозного кровотока, которое наступает в момент прошивания бронха, а нарушение локального кровотока документируется через 3 часа после пульмонэктомии.
При этом самое критическое снижение кровотока наступает в течение первых трех суток после операции. Необходимо отметить, что даже через один месяц после операции пульмонэктомии полной компенсации легочного кровотока не наступает.
Эффективность перевязки легочной артерии. Перевязка легочной артерии при пневмэктомии
Перевязка легочной артерии, как самостоятельная операция, введена у нас — в Советском Союзе. Впервые она была произведена в 1946 году в клинике А. Н. Бакулева, а затем очень широко применялась в клинике Ф. Г. Углова, который доказывал ее несомненный лечебный эффект при нагноительных заболеваниях легких. Фтизиохирурги Л. К. Богуш и П. И. Костромин одно время широко пользовались перевязкой легочной артерии при легочных кровотечениях, главным образом, у туберкулезных больных. В других клиниках торакальные хирурги относятся к перевязке легочной артерии очень сдержанно, и П. А. Куприянов прямо говорит, что эффективность ее при нагноительных процессах ничтожна. В клинике Б. Э. Линберга сделали 10 перевязок легочной артерии, причем эффект отмечался не часто. Мы со своей стороны оцениваем эту операцию как самостоятельное вмешательство не высоко и допускаем ее как вынужденную меру в тех случаях, когда нельзя произвести резекции легкого.
Перевязкой легочной артерии мы вынуждены иногда ограничиваться в тех случаях, когда из-за ухудшения состояния больного в ходе операции не удается произвести пневмонэктомию. В таких случаях эту операцию рассматривают, как первый этап радикального вмешательства.
Обезболивание. Если операция предпринимается по абсолютным показаниям, при тяжелых легочных кровотечениях, то приходится обычно пользоваться местной анестезией. Преимуществом местной анестезии является сохранение кашлевого рефлекса и возможность откашливать мокроту и кровь, если в ходе операции повторяется легочное кровотечение. При пользовании интратрахеальным наркозом, при значительном кровотечении отсасывать всю кровь с помощью насоса очень трудно, и больной может погибнуть от асфиксии.
Если применять перевязку легочной артерии как самостоятельную паллиативную операцию, то можно выполнять ее под любым видом обезболивания.
Оперативные доступы. Наиболее удобным доступом является передне-боковой, поскольку легочная артерия располагается кпереди от бронха. Однако при левостороннем вмешательстве перевязку легочной артерии можно с успехом выполнить из задне-бокового доступа, так как слева артерия значительно выдается над бронхом. Справа перевязка легочной артерии из заднего доступа без пересечения бронха невозможна.
Методика операции. При переднем оперативном доступе слева плевральную полость вскрывают по 3-му или 4-му межреберью, с пересечением хрящей соседних ребер. Раздвигают рану, легкое отслаивают от перикарда до корня. Производят внутригрудную анестезию с введением новокаина в переднее средостение по направлению вверх с тем, чтобы новокаинный инфильтрат распространился на бронхи, блуждающие нервы и частично на симпатический ствол. По достижении корня надсекают переходную складку плевры, идущую с перикарда на легкое. При этом обнажаются сосуды. Ближе всех к перикарду располагается верхняя легочная вена и особенно ее передняя сегментарная веточка, идущая косо по направлению к верхушке. Эта ветвь закрывает легочную артерию и для удобства доступа ее надо перевязать и пересечь между лигатурами.
После этого обнажается крупная ветвь легочной артерии, идущая к переднему и апикальному сегменту. Недостаточно квалифицированные хирурги часто принимают эту ветвь за основной ствол легочной артерии и перевязывают ее вместо последней.
Основной ствол легочной артерии расположен несколько в каудальном направлении в отношении верхней сегментарной ветви, и она быстро уходит вглубь легочной ткани. Для доступа к артерии нужно отодвинуть складку перикарда в медиальном направлении, и под ней можно видеть основной ствол легочной артерии, выходящий из перикарда. В этом месте ее перевязывают. Предпочтительным является не только перевязка легочной артерии, но и пересечение ее между двумя лигатурами, с наложением на центральный конец дополнительной прошивной лигатуры. Это особенно важно, когда операция выполняется как первый этап последующего радикального вмешательства, например, при тяжелом туберкулезном или гнойном процессе, осложненном кровотечением. Первой операцией мы рассчитываем спасти больного от кровотечения, чтобы в последующем удалить легкое, поскольку оно тяжело поражено. Простая перевязка легочной артерии, особенно при недостаточном затягивании узлов, сопровождается восстановлением небольшого просвета артерии с повторными кровотечениями.
После перевязки или пересечения легочной артерии рану зашивают с введением межреберного дренажа. Дренаж необходим потому, что часто при отслаивании легкого повреждается его ткань и возможен напряженный пневмоторакс, а также и кровотечения, в связи с тем, что операция в большинстве случаев производится в спешке при крайне тяжелом состоянии боль юго.
При правостороннем вмешательстве из переднего оператив.юго доступа операция производится в таком же порядке; отслаивается и рассекается переходная складка плевры, верхняя полая вена, прикрывающая устья легочных сосудов,отводится в медиальном направлении, после чего удается обнаружить основной ствол легочной артерии. В некоторых случаях можно увидеть два ствола —один тонкий, представляющий собой верхнюю сегментарную артерию, другой более толстый, быстро уходящий в глубину легочной ткани, является основным стволом легочной артерии. Верхняя сегментарная вена и здесь может значительно прикрывать латеральные отделы легочной артерии и ее приходится предварительно перевязывать.
При перевязке легочной артерии из заднего доступа операция производится как один из моментов пневмонэктомии.
Операционные и послеоперационные осложнения ничем не отличаются от возникающих при резекциях и будут описаны далее.
Эффективность перевязки легочной артерии. Перевязка легочной артерии при пневмэктомии
Эффективность перевязки легочной артерии. Перевязка легочной артерии при пневмэктомии
О'Шонесси в 1936 г. собрал в мировой литературе 17 случаев перевязки ветвей легочной артерии у человека, которая оказалась малоэффективной. Автор подчеркивает, что он не нашел в литературе примеров перевязки главной ветви легочной артерии у человека как самостоятельной операции.
Просмотрев обширную литературу более позднего времени (до 1947 г.), как советскую, так и зарубежную, мы также не встретили примеров такой перевязки как самостоятельной операции. Между тем, теоретически она вполне обоснована и подтверждена экспериментальными работами.
При перевязке главного ствола легочной артерии наблюдается картина острого малокровия соответствующего легкого. В то время как приток крови происходит только за счет маленькой бронхиальной артерии, отток осуществляется двумя мощными легочными венами, которые как бы «высушивают» легкое. Наступающее при этом малокровие с его ишемическим выпотеванием форменных элементов приводит к развитию своеобразного индуративного процесса, который через некоторое время ведет к сморщиванию легкого. Так как коллатерали здесь или не развиваются вовсе, или возникают только со стороны грудной стенки через спайки, то сморщивание захватывает все легкое и постепенно прогрессирует.
Если принять за единицу все крупные ветви обеих легочных артерий, то в эксперименте можно перевязать 3/5 их с обеих сторон без признаков сердечной недостаточности.
Перевязка легочной артерии при пневмэктомии даже у пожилых людей не влечет за собой тяжелых сердечных нарушений. Отдельные хирурги у немолодых людей, страдающих раком легкого, несколько раз применяли перевязку легочной артерии как первый этап операции. Через 5—7 дней они удаляли все легкое, и за эти дни у больных не проявлялось каких-либо нарушений сердечнососудистой деятельности.
7/I 1947 г., предполагая произвести пневмэктомию по поводу множественных абсцессов правого легкого, мы из-за тяжелого состояния больного ограничились перевязкой главного ствола правой легочной артерии. Больной поправился. Ни кашля, ни мокроты у него нет в течение 6 лет. После этого мы произвели одностороннюю перевязку главного ствола легочной артерии еще ряду больных с обширными бронхэктазиями и множественными абсцессами легкого. Удаление легкого у них представлялось нам чрезвычайно опасным из-за мощных сращений с медиастинальной плеврой.
Наши первые наблюдения над односторонней перевязкой главной ветви легочной артерии показали: 1) что эта операция менее опасна и технически более проста, чем удаление легкого; 2) что она не только не несет за собой каких-либо вредных последствий, но является, безусловно, полезной при гнойных заболеваниях, захвативших все легкое.
В мае 1947 г. на I Всесоюзной конференции по грудной хирургии А. В. Герасимова сообщила об одном благоприятном результате после такой перевязки, а в 1949 г. опубликовала работу, в которой приводит данные, касающиеся перевязок различных сосудов как при раке, так и при гнойных заболеваниях легкого. Эта работа показывает, что перевязка главной ветви легочной артерии применялась ими несколько раз с апреля 1946 г. при гнойных заболеваниях как самостоятельная операция и в ряде случаев принесла очень хорошие результаты.
В последующем в печати появилось несколько статей, посвященных вопросу перевязки легочной артерии как самостоятельной операции при нагноительных процессах и раке легкого. Данные работы показывают, что ряд больных от этой операции получает значительное улучшение состояния вплоть до полного излечения, а в ряде случаев такого эффекта не отмечается. Наша задача — выяснить механизм ее действия, чтобы заранее знать, в каких случаях можно ждать эффекта от одной перевязки легочной артерии и в каких она будет безуспешной.
Однако перевязка легочной артерии как самостоятельная операция принесла хирургам несомненную помощь, так как открыла для них выход из затруднительного положения, когда по ряду причин нельзя сделать пневмэктомию без серьезной угрозы гибели больного.
Информация на сайте подлежит консультации лечащим врачом и не заменяет очной консультации с ним.
См. подробнее в пользовательском соглашении.
Эффективность перевязки легочной артерии. Перевязка легочной артерии при пневмэктомии
Тематические страницы > Исторические очерки о вятской медицине > Академик Александр Николаевич Бакулев как сердечный хирург
Среди медицинской профессуры СССР есть не так много хирургов, которые бы сочетали в себе яркую и крупную личность, безусловный научный авторитет, высочайшее хирургическое мастерство и деятельность государственного масштаба. Одним из них, без сомнения, был Герой Социалистического труда, лауреат Ленинской и Государственной (Сталинской) премий, заслуженный деятель науки, депутат Верховного Совета СССР, Президент АМН СССР, академик Александр Николаевич Бакулев.
А.Н. Бакулев родился 12 декабря 1890 г. в деревне Бакули Слободского уезда Вятской губернии в семье крестьянина-середняка. Его обычная для тех мест фамилия происходит от исконно вятского слова «бакулить», что означает балагурить, рассказывать байки, шутить. Соответственно, «бакулями» звали весельчаков-балагуров, населявшие в приснопамятные времена деревню Бакули и ее окрестности.
Помимо крестьянства его пращуры занимались литейным делом. В местном краеведческом музее хранятся их колокола с гордой надписью – «Отлито Бакулевыми», а один из колоколов когда-то даже украшал звонницу знаменитого на всю Россию Соловецкого монастыря.
Из детских лет академика упомянем еще один любопытный факт: его другом детства и полным тезкой был личный секретарь И.В. Сталина Александр Николаевич Поскребышев, живший неподалеку в селе Успенском. Они вместе росли, учились в школе, пели в церковном хоре. Их в детстве даже звали одинаково – Поскребеня и Бакуленя.
Конец учебы А.Н. Бакулева в Саратовском университете совпал с 1-й мировой войной, в которой Александр Николаевич участвовал «зауряд-врачом» и был удостоен боевого ордена Св. Станислава 3-й ст. с мечами.
В годы Гражданской войны он трудился врачом, но не хирургом, а инфекционистом и терапевтом госпиталей РККА, в период НЭПа – инспектором Наркомздрава РСФСР, а в голодомор 20-х годов – особо уполномоченным Американо-Российской Ассоциации – АРА, помогавшей Советской республике техникой, продуктами, одеждой и медикаментами.
Сравнительно поздно, в возрасте 30 с лишним лет, он стал обучаться хирургии в госпитальной клинике Саратовского университета у профессора Сергея Ивановича Спасокукоцкого, который знал его еще студентом и сумел разглядеть в уже немолодом ординаторе перспективного хирурга и ученого. Не случайно в 1926 г. один из немногих вслед за учителем А.Н. Бакулев переехал в Москву и стал работать ассистентом, а затем – доцентом кафедры факультетской хирургии имени ее основателя, профессора Федора Александровича Рейна 2-го МГУ, которой пригласили заведовать Спасокукоцкого. Мало кому известно, что одно время А.Н. Бакулев подрабатывал хирургом Мытищинской городской больницы.
В те годы его научные интересы касались многих проблем, которые разрабатывала клиника С.И. Спасокукоцкого – хирургии пищевода и желудка, легких и перикарда, 12-перстной кишки и почек. Но особенно его увлекла становившаяся самостоятельной дисциплиной нейрохирургия. В 1935 г. causa honore А.Н. Бакулев получил кандидатскую степень, а в 1939 г. защитил докторскую диссертацию на тему «Консервативное лечение абсцессов мозга (пункциями)», в которой одним из первых в мире обосновал закрытый способ лечения гнойников головного мозга.
В том же году он возглавил кафедру госпитальной хирургии педиатрического факультета 2-го МГМИ, а осенью 41-го года, в самые трудные месяцы Великой Отечественной войны, оборонял Москву в должности главного хирурга Резервного фронта, командовал которым, кстати говоря, будущий Маршал Победы Георгий Константинович Жуков.
Одновременно А.Н. Бакулев был консультантом по хирургии Главного управления эвакогоспиталей Москвы и в течение 1942 г. заведовал кафедрой общей и военно-полевой хирургии 1-го Московского медицинского института. В военные годы он разработал ряд операций на спинном мозге, способ надлобкового свища при ранениях поясничного отдела позвоночника и глухой шов проникающих ран головы.
В 1943 г., после смерти своего учителя, А.Н. Бакулев возглавил кафедру факультетской хирургии лечебного факультета 2-го МГМИ, получившую имя академика и орденоносца С.И. Спасокукоцкого, которой заведовал более 20 лет. Одновременно до 1947 года он руководил хирургическим отделением Кремлевской больницы, которое также получил «в наследство» от Спасокукоцкого, а затем в течение 5 лет работал главным хирургом Лечебно-санитарного управления Кремля. Эти факты уже сами по себе говорят о его высоком в те годы хирургическом авторитете.
Столь же стремительно развивалась и академическая карьера Александра Николаевича. В 1946 г. он стал заслуженным деятелем науки, в 1948 г. – действительным членом АМН СССР, в 1949 г. – лауреатом Сталинской, а 10 лет спустя – Ленинской премии. В 1953 г. его избрали Президентом АМН, в 1958 г. – академиком «большой» академии, а к 70-летию он был удостоен звания Герой Социалистического труда. И вполне возможно, что мы говорили бы сейчас о крупном отечественном абдоминальном, грудном или нейрохирурге А.Н. Бакулеве, если бы не еще одно его страстное увлечение, которому он посвятил последнюю четверть жизни.
В 1948 г. одним из первых в стране (совместно с Е.Н. Мешалкиным) он внедрил и стал развивать эндотрахеальный наркоз и ангиокардиографию, выполнил первую в стране операцию при врожденном пороке сердца, в 1952 г. провел первые в стране операции при митральном стенозе и мешотчатой аневризме восходящей аорты, а в 1955 г., на XXIV Всесоюзном съезде хирургов, на котором он был председателем, впервые поднял вопрос о создании в стране ВНИИ торакальной хирургии с кардиологическим отделением.
В 1956 г. Распоряжением Совета Министров СССР такой институт, названный Институтом грудной хирургии АМН СССР, был создан, а его директором был утвержден 66-летний Бакулев. С этого времени для него начался новый отсчет времени, спрессованный в несколько лет. Ведь грудной хирургией в то время занимались многие.
Требовалось в кратчайшее время решить сразу несколько задач: найти помещение для нового института, создать коллектив, наладить научные исследования и широким, как тогда говорили, фронтом начать операции на легких, пищеводе, сердце и магистральных сосудах, которые к тому времени уже делались в нескольких клиниках страны. При этом Бакулев, с детства приучивший себя добиваться максимального результата, поставил перед собой цель не только опередить коллег, но и доказать лидирующую роль нового института в решении этих проблем.
Впервые в мире в начале 1950-х гг. А.Н. Бакулев сформулировал концепцию коррекции врожденных пороков сердца «синего» типа наложением кавопульмонального анастомоза, а в 1956 г. его ученик Е.Н. Мешалкин первым в мире выполнил эту операцию в клинике.
Во второй половине 1950-х гг. под руководством А.Н. Бакулева были проведены приоритетные научные исследования в области разработки методов диагностики и хирургического лечения приобретенных и врожденных пороков сердца, хронической коронарной недостаточности, нарушения ритма и проводимости, заболеваний аорты, ее ветвей и магистральных сосудов, искусственного кровообращения и внедрения их в практику. Проще говоря, нет ни одного направления современной кардиохирургии, где Александр Николаевич или его ученики не оставили бы своего вклада.
Приведем только один пример его научной прозорливости и умения идти на определенный для своего реноме риск ради достижения цели, заложившей основы выше перечисленных достижений.
Известно, что первым в СССР в условиях гипотермии на сердце стал оперировать друг и соратник А.Н. Бакулева П.А. Куприянов из Ленинграда, а в 1957 г. А.А. Вишневский, применив советский аппарат искусственного кровообращения «АИК-57», первым в стране выполнил серию успешных паллиативных операций при тетраде Фалло на открытом сердце.
А что же А.Н. Бакулев? Неужели он, начав сердечную хирургию по закрытым методикам, так просто отдал приоритет хирургии открытого сердца? Так получилось, что как раз в эти годы происходило становление созданного А.Н. Бакулевым Института грудной хирургии АМН СССР, в котором в 1957 – 1958 гг. произошла смена руководства. Вместо Александра Николаевича его возглавил Алексей Андреевич Бусалов. В это время ведущие хирурги института (А.Н. Бакулев, С.А. Колесников, А.А. Бусалов) оперировали в основном приобретенные пороки сердца по закрытым методикам. Но мысль проводить радикальные операции на больных сердцах условиях искусственного кровообращения, которые в СССР действительно начались не в его институте, А.Н. Бакулева как научного руководителя коллектива и виднейшего кардиологического хирурга страны, не покидала.
Конечно, будучи патриотом своей страны, А.Н. Бакулев мог бы пойти по пути А.А. Вишневского и терять больных один за другим из-за несовершенства тогдашней отечественной техники. Однако, хорошо зная низкое качество первых советских АИК’ов и исповедуя гиппократов принцип no nocere, А.Н. Бакулев пошел совершенно неординарным путем. Выяснив, у какой команды хирургов самые низкие в мире показали летальности, он пригласил в институт группу английских специалистов в области сердечной хирургии и кардиологии во главе с профессором H. Bentall (его имя носит операция протезирования корня аорты), хирургом W. Clеland и физиологом, изобретателем дискового оксигенатора D. Melrose.
В первую декаду мая 1959 г. англичане вместе с хирургами института, опытным С.А. Колесниковым и молодым, но перспективным хирургом, тогда – аспирантом, а в будущем – академиком РАМН В.А. Бухариным, выполнили 4 операции в условиях полного ИК – две паллиативных и 2 радикальных. Они прошли успешно, что дало возможность закрепить успех.
После отработки техники искусственного кровообращения в эксперименте, в апреле 1960 г. ставший директором института профессор С.А. Колесников выполнил первые в институте успешные операции на открытом сердце. Учитывая тот факт, что после этих операций к радикальным вмешательствам на сердце при его пороках, закупив импортную аппаратуру, приступили и другие клиники страны, следует признать, что решение А.Н. Бакулева перенять передовой мировой опыт вместо «изобретения велосипеда» было правильным. В дальнейшем советские инженеры «довели до ума» советские АИК’и, которые также были внедрены и в Институте грудной хирургии.
О хирургической смелости и большом научном авторитете Александра Николаевича говорят факты начала разработки в основанном им институте и под его руководством первых в стране имплантируемых электрокардиостимуляторов. У истоков проблемы стояли его ближайшие ученики – будущие академики В.С. Савельев и Ю.Ю. Бредикис.
В характере А.Н. Бакулева как большого ученого и педагога была черта, перенятая им у С.И. Спасокукоцкого. Все разработанные проблемы он передавал для продолжения ученикам, оставлял за собой новые и неизведанные. Так, в первой половине 1960-х гг. проблему хирургического лечения приобретенных пороков сердца в условиях ИК он передал С.А. Колесникову, врожденных пороков – В.И. Бураковскому, хирургии аорты и магистральных сосудов – Ю.Е. Березову, а затем – А.В. Покровскому, нарушений ритма сердца и электрокардиостимуляции – А.С. Ровнову и В.С. Савельеву, взяв «под свое крыло» абсолютно новую тогда проблему хирургии ХКН. И хотя первые в мире операции прямой реваскуляризации миокарда выполнил ленинградский хирург В.И. Колесов, нами установлено, что успеха он достиг только после того, как работавшие под руководством А.Н. Бакулева Н.Б. Доброва и Л.С. Зингерман презентовали изобретенный ими инструмент для наложения сосудистого шва в условиях непрерывного кровотока.
Но, все же, с какого момента А.Н. Бакулев заинтересовался сердечной хирургией? Впервые интерес к абсолютно новому в то время направлению он испытал в 1920-х гг., когда одним из первых в стране стал проводить операции кардиолиза при слипчивом перикардите.
В нашем Музее хранится предмет, который документирует второй шаг А.Н. Бакулева по пути к началу хирургии сердца. Это – книга Н.Н. Теребинского об открытых доступах к атриовентрикулярным клапанам, подаренная им А.Н. Бакулеву с автографом в 1944 г. Известно, что годом позже вместе с В.М. Молотовым А.Н. Бакулев побывал в США, где познакомился с хирургией сердца в клиниках A. Blalock в Рочестере и C. Bailey в Филадельфии, привез оттуда (по словам Е.Н. Мешалкина) зажим для ушка сердца и горячее желание начать хирургию сердца в СССР.
Ну, а последним этапом перед взятием новой для советской хирургии вершины стало увлечение А.Н. Бакулева в первые послевоенные годы легочной хирургией и пионерские операции пневмонэктомии, когда он вслед за Л.К. Богушем начал перевязывать легочные сосуды в средостении.
Недавно мы отыскали инструмент под названием «ушиватель корня бронха» под №1, принадлежавший А.Н. Бакулеву. Теперь он украшает экспозицию нашего Музея, посвященную Александру Николаевичу.
Таким образом, изучая на протяжении последнего десятилетия проблему начала хирургии сердца в нашей стране, мы показали, что практически во всех направлениях хирургии сердца и сосудов А.Н. Бакулев и его ученики были первыми. А в некоторых не только в стране, но и в мире.
Приоритетность в той или иной области хирургии, по нашему мнению, дает возможность начать параллельное движение в данном направлении другим хирургам, указывает им вектор движения, поощряет к нему.
Перечислим еще раз основные вехи развития сердечно-сосудистой хирургии в Советском Союзе, указав приоритеты А.Н. Бакулева и его школы: 1920-е гг. – первые в СССР операции при слипчивом перикардите (в хирургическом лечении этого заболевания А.Н. Бакулев имел самый большой опыт и лучшие результаты); 1929–1940 г. – труды Н.Н. Теребинского по экспериментальной хирургии сердца (1944 г. – знакомство А.Н. Бакулева с его трудами); 1945 г. – поездка А.Н. Бакулева в США; 1946 г. – первая в стране пневмонэктомия при раке (А.Н. Бакулев), начало систематической перевязки легочных сосудов в клинике факультетской хирургии 2-го МГМИ; 1948 г. – первая в стране перевязка незаращенного артериального протока (А.Н. Бакулев, В.А. Жмур, А.В. Герасимова), внедрение в сердечную хирургию наркоза и управляемого дыхания (А.Н. Бакулев, Е.Н. Мешалкин); 1951 г. – первые в стране операции создания межсосудистых анастомозов (А.В. Гуляев, Е.Н. Мешалкин), впервые в мире сформулированная концепция создания кавопульмонального анастомоза (А.Н. Бакулев, начало 1950-х гг.); 1952 г. – первые в стране операции при приобретенных пороках сердца (А.В. Гуляев, А.Н. Бакулев) и заболеваниях аорты (А.Н. Бакулев), начало разработки во ВНИИЭХАиИ аппаратов искусственного кровообращения (А.Н. Бакулев, М.Г. Ананьев); 1955 г. – первая в СССР монография «Врожденные пороки сердца» (А.Н. Бакулев, Е.Н. Мешалкин); 1956 г. – создание первого в мире специализированного Института грудной хирургии (А.Н. Бакулев), первая в мире операция кавопульмонального анастомоза (Е.Н. Мешалкин); 1957 г. – первая в стране операция при аортальном пороке сердца (В.С. Савельев); 1958 г. – первое в стране руководство для врачей «Хирургическое лечение митральных стенозов», написанное сотрудниками Института грудной хирургии под редакцией А.Н. Бакулева; 1959 г. – первые в стране радикальные операции при врожденных пороках сердца в условиях искусственного кровообращения (С.А. Колесников, В.А. Бухарин); 1961 г. – реорганизация института в Институт сердечно-сосудистой хирургии (А.Н. Бакулев, С.А. Колесников), первая в стране радикальная операция при тетраде Фалло (В.И. Бураковский); 1962 г. – создание первых в мире трехлепестковых искусственных клапанов сердца (С.А. Колесников, Г.Т. Голиков), первая в мире операция протезирования легочного клапана (В.И. Бураковский), создание отечественных электрокардиостимуляторов; 1963 г. – первая в стране имплантация ЭКС (В.С. Савельев), первая в стране операция протезирования аортального клапана (С.А. Колесников); 1965 г. – начало операций на сердце у детей раннего возраста (Б.А. Константинов); 1967 г. – смерть А.Н. Бакулева.
Так закончилась целая эпоха в советской кардиохирургии, заложившая прочнейший фундамент ее развитии на будущее.
Мы прекрасно понимаем, что без мощной поддержки как на самом верху советской государственной и политической системы в лице И.В. Сталина, В.М. Молотова, А.Н. Поскребышева, Н.С. Хрущева, Л.И. Брежнева, А.Н. Косыгина, без дружеской, соревновательной конкуренции коллег – хирургов П.А. Куприянова, А.А. Вишневского, Б.В. Петровского, а также более молодых – Н.М. Амосова, Б.А. Королева, Ф.Г. Углова, как и без мощного коллектива бакулевской клиники и института ее глава не сделал бы так много.
Назовем только – в алфавитном порядке – основных его учеников, оставивших след в становлении грудной хирургии в нашей стране и защитивших под руководством А.Н. Бакулева докторские – А.А. Бусалов, А.В. Гуляев, В.А. Жмур, Е.С. Лушников, О.Ю. Марина, Е.Н. и И.Н. Мешалкины, В.С. Савельев, Г.А. Рябов, М.Г. Сироткина и другие; и кандидатские диссертации – В.А. Бухарин, В.М. Буянов, Г.Г. Гельштейн, Е.А. Дамир, Р.П. Зубарев, В.П. Смольников, В.С. Работников, А.А. Спиридонов, В.И. Францев и многие другие.
Ну, а в том, что дело А.Н. Бакулева живет и побеждает в современной России, «виноват», прежде всего, нынешний коллектив нашего центра, носящего гордое имя – «Дом Сердца» и отпраздновавший недавно свое 10-летие. Все 2500 его сотрудников, называющих себя бакулевцами.
Сегодня наши хирурги выполняют весь спектр операций на сердце, включая пересадку и гибридные вмешательства, и делают ежегодно самое большое количество операций на открытом сердце в мире – более 7500, в том числе более 3500 операций у новорожденных и детей до 1 года, что является «высшим пилотажем» современной кардиохирургии!
И мы горды тем, что приезжающие в Центр гости, в том числе иностранные, уже как само собой разумеющееся называют его просто «Бакулевским», отдавая дань памяти его выдающемуся создателю, бывшему крестьянскому пареньку из далекой Вятской деревни Бакули.
И слава о нем, таким образом, продолжает расти и разноситься по всей земле российской и за ее пределами, как в свое время малиновый звон колоколов его знаменитых предков.
ПЕРЕВЯЗКА СОСУДОВ КОРНЯ ЛЕГКОГО В ПОЛОСТИ ПЕРИКАРДА ПРИ ПНЕВМЭКТОМИИ

Метод раздельной обработки элементов корня легкого при пневмэктомии является общепринятым. При этом выделяют и перевязывают сосуды легкого в корне и средостении, что удается относительно легко при отсутствии выраженных склеротических и воспалительных изменений в клетчатке и лимфатических узлах. Однако, патологический процесс (воспалительный и опухолевый) нередко поражает клетчатку корня легкого, в него вовлекается адвентиций сосудов. Выделение легочной артерии, легочных вен при этом чревато опасностью их повреждения и нередко — рокового кровотечения на операционном столе.
Ключевые слова
Полный текст
Метод раздельной обработки элементов корня легкого при пневмэктомии является общепринятым. При этом выделяют и перевязывают сосуды легкого в корне и средостении, что удается относительно легко при отсутствии выраженных склеротических и воспалительных изменений в клетчатке и лимфатических узлах. Однако, патологический процесс (воспалительный и опухолевый) нередко поражает клетчатку корня легкого, в него вовлекается адвентиций сосудов. Выделение легочной артерии, легочных вен при этом чревато опасностью их повреждения и нередко — рокового кровотечения на операционном столе.
Б-ной Ю. М., 24 лет, поступил в хирургическое отделение Республиканского противотуберкулезного диспансера 7 декабря 1955 г. Диагноз: левосторонний неэффективный искусственный пневмоторакс, по поводу фиброзно-кавернозного туберкулеза легких, БК +.
В связи с неэффективностью антибактериальной терапии и лечебного пневмоторакса больному решено произвести операцию — верхнюю лобэктомию слева.
1/ІІ-56 г. операция под местной инфильтрационной анестезией ¼% раствором новокаина после вагосимпатической блокады на стороне операции. Выделение доли происходит с большими трудностями в связи с очень плотными сращениями в области средостения и по междолевой борозде. При препаровке в верхнем отделе междолевой щели повреждена ветвь легочной артерии. Для временной остановки кровотечения наложен зажим. Продолжено выделение ветвей легочной артерии в междолевой щели. Верхняя легочная вена и бронх обработаны типично. Доля удалена. Выделение основного ствола левой легочной артерии было рискованным из-за резких склеротических изменений клетчатки вокруг него. Попытка наложить лигатуру на поврежденную ветвь легочной артерии привела к соскальзыванию зажима и бурному кровотечению. Состояние больного резко ухудшилось, появились судороги, наступила остановка сердца, затем и дыхания. Кровотечение с большим трудом остановлено прижатием кровоточащего места пальцем, а затем грубо наложен зажим. Больному срочно в аорту перелито 20 мл крови, усилено внутривенное переливание крови. Вскоре состояние больного улучшилось, артериальное давление установилось в пределах 80-70. Для окончательной остановки кровотечения из легочной артерии, захваченной в зажиме, решено перевязать ее интраперикардиально. Перикард вскрыт продольным разрезом, длиной 6 см позади диафрагмального нерва над легочной артерией. После рассечения задней стенки перикарда у нижней полуокружности легочной артерии позади нее проведен зажим Федорова, конец которого выведен над верхним краем артерии в полости перикарда. Через проложенный таким образом туннель проведена шелковая лигатура, которая и была завязана. Зажим с артерии снят, небольшое кровотечение остановлено наложением лигатуры. Операция закончена без дренажа плевральной полости.
В послеоперационном периоде у больного была длительная лихорадка, увеличилось количество выделяемой мокроты. Комбинированное применение антибиотиков привело к постепенному улучшению общего состояния больного, нормализации температуры тела. Через 30 дней после операции больной был выписан для санаторного лечения с небольшой апикальной остаточной полостью.
Через три года после операции состояние больного вполне удовлетворительное, жалоб не предъявляет, кашель редкий, мокроты не выделяет, стойко абациллярен. Работает; одышки, сердцебиения нет. При рентгено-томографическом исследовании выраженные плевральные наложения в верхнем отделе плевральной полости слева, высокое стояние и ограничение подвижности левого купола диафрагмы.
В этом наблюдении при уже возникшем кровотечении из легочной артерии закрытие просвета ее в полости перикарда явилось единственным средством остановки смертельно опасного кровотечения. Вынужденное выключение главного ствола легочной артерии при лобэктомии не сказалось отрицательно на ближайших результатах операции. Отдаленные результаты вмешательства указывают на допустимость этого, вопреки литературным данным.
В другом случае перикард был вскрыт для перевязки легочных вен.
Б-ная 3. А., 24 лет, поступила в хирургическое отделение Республиканского диспансера 3/I-57 г. по поводу левостороннего фиброзно-кавернозного туберкулеза легких. Больной 11/III-57 г. был произведен верхний экстраплевральный пневмолиз слева. Операция оказалась неэффективной. Состояние больной продолжало ухудшаться, постоянно сохранялось бацилловыделение, количество мокроты — до 60 мл в сутки, иногда зловонная.
Добиться компенсации процесса при помощи длительной антибактериальной терапии и постельного режима не удалось. Температура тела периодически субфебрильная. Пульс — 86. Укорочение перкуторного звука над левым легким почти на всем протяжении, на фоне бронхиального дыхания большое количество разнокалиберных влажных хрипов, больше сзади, ниже угла лопатки. Жизненная емкость легких — 1400 мл. При рентгено-томографическом исследовании легких отмечается смещение сердца и средостения влево, почти тотальное затемнение левого легкого с множественными просветлениями в верхнем отделе. Небольших размеров верхушечный экстраплевральный пневмоторакс с утолщенными стенками. Диагноз: левосторонний хронический фиброзно-кавернозный туберкулез легких, ателектаз верхней доли, обсеменение нижней доли.
Левосторонняя пневмонэктомия (10/III-57 г.), выполненная под местной инфильтрационной анестезией раствором новокаина, была технически трудной из-за обширных рубцовых плевральных сращений на всем протяжении плевральной полости. Острым путем разрушены рубцовые ткани впереди корня легкого и по верхнему его полюсу. Выделены легочная артерия и легочные вены. Первая обработана типично, с прошиванием центрального отрезка. Экстраперикардиальная часть легочных вен оказалась короткой (1 см).
Выделение ветвей вен в корнях долей легкого было рискованным из-за склеротических и воспалительных изменений вокруг них. Чтобы надежно закрыть просвет легочных вен и избежать непоправимых осложнений, решено их перевязать трансперикардиально. Перикард вскрыт продольным разрезом позади диафрагмального нерва над корнем легкого. Затем перикард рассечен по нижнему краю верхней и нижней легочных вен. Лигатура при помощи зажима проведена через сделанные отверстия в задней стенке перикарда над верхним краем нижней и верхней легочных вен. Вторая лигатура наложена вне полости перикарда. Так как лигатуры на венах были фиксированы в задней стенке перикарда, необходимость в прошивной лигатуре отпала. Дефект в перикарде ушит двумя швами, так как из его полости отмечалось выпадение ушка левого предсердия.
Послеоперационный период протекал гладко. Через две недели после операции у больной наблюдался приступ сердечной слабости, ликвидированный внутривенным применением строфантина с глюкозой и эвакуацией экссудата из плевральной полости.
Через полгода после операции состояние больной вполне удовлетворительное, кашля и мокроты нет, температура нормальная. Жизненная емкость легкого - 1700 мл. После длительной ходьбы отмечает сердцебиение. Рентгенологически — фиброторакс слева.
Мы полагаем, что трансперикардиальный доступ к сосудам корня легкого имеет преимущества перед интраперикардиальным, так как при первом все манипуляции по выделению и обработке сосудов производятся под контролем зрения. При интраперикардиальном доступе проведение лигатуры позади сосудов производится вслепую, что нельзя считать безопасным. При этом доступе, однако, лигатура оказывается фиксированной в листке перикарда, и необходимость в прошивной лигатуре отпадает. Во втором нашем наблюдении мы фиксировали лигатуру в заднем листке перикарда по верхнему краю легочных вен, но выделение их произвели в основном трансперикардиально. Таким образом, использованы положительные стороны обоих доступов — интраперикардиального и трансперикардиального.
Представленные наблюдения подтверждают литературные данные о целесообразности интра- и трансперикардиальной перевязки сосудов корня легкого для предупреждения возможного кровотечения и воздушной эмболии при экстраперикардиальном их выделении и ликвидации уже возникшего кровотечения.
Читайте также:
