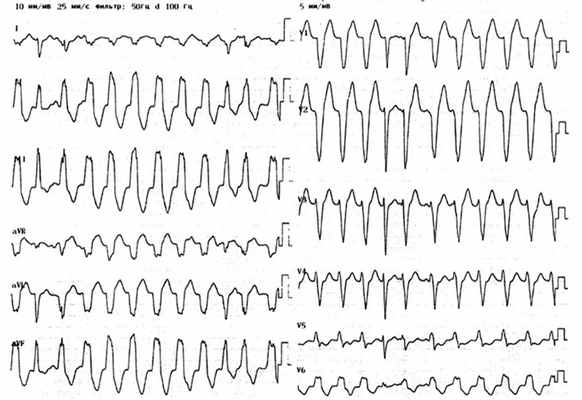
ЭКГ при двунаправленной желудочковой тахикардии
Добавил пользователь Дмитрий К. Обновлено: 27.01.2026
Похожие темы научных работ по клинической медицине , автор научной работы — Снежицкий В. А., Раков А. В., Зайцев В. И., Мадекина Г. А., Фаддеев Г. И.
Текст научной работы на тему «Случай двунаправленной веретенообразной желудочковой тахикардии у больной с множественными проявлениями дисплазии соединительной ткани сердца»
УДК 616.12-008.313.3: 616.12-018.2-007.17
СЛУЧАЙ ДВУНАПРАВЛЕННОЙ ВЕРЕТЕНООБРАЗНОЙ
ЖЕЛУДОЧКОВОЙ ТАХИКАРДИИ У БОЛЬНОЙ С МНОЖЕСТВЕННЫМИ ПРОЯВЛЕНИЯМИ ДИСПЛАЗИИ СОЕДИНИТЕЛЬНОЙ ТКАНИ СЕРДЦА
В.А. Снежицкий1, A.B. Раков1, В.И. Зайцев3, Г.А. Мадекина2, Г.И. Фаддеев2, Е.А. Снежицкая2, Л.А. Азарова2Г В.И. Шишко2,
Двунаправленную веретенообразную желудочковую тахикардию (ДВЖТ) относят к полиморфным желудочковым тахикардиям [2]. ДВЖТ может наблюдаться у больных с синдромом удлиненного интервала Q-T электрокардиограммы (СУИ QT) и при нормальном интервале Q-T. В свою очередь, СУИ QT может быть врожденным и приобретенным. Врожденный СУИ QT в настоящее время достаточно изучен, на основе результатов молекулярно генетических исследований выделены 7 типов данного заболевания. Приобретенный СУИ QT встречается гораздо чаще, чем приобретенный [2], ввиду этого и значение его для клиники значительно больше, ввиду необходимости профилактики приобретенного СУИ QT при назначении антиаритмических средств.
ДЖВТ без удлинения интервала Q-T на электрокардиограмме отличается от случаев СУИ QT по ряду признаков [1, 2]. Во-первых, ДВЖТ с нормальным интервалом Q-T заметно чувствительнее к антиаритмическим препаратам I класса, во-вторых, длительное назначение кордарона больным с ДВЖТ, вызванной антиаритмическими препаратами I класса, достаточно эффективно, в третьих, течение этого типа ДВЖТ более доброкачественно. Среди этиологических причин ДЖВТ без удлинения интервала Q-T называют лекарственные воздействия (антиаритмическими препаратами I класса), пролапс митрального клапана, спортивное сердце.
Больная М., 43 лет, поступила в кардиологическое ГОКД 22 февраля 2006 года (история болезни
№ 671) с жалобами на периодические колющие боли в области сердца.
Причиной госпитализации явилось выявление при холтеровском мониторировании электрокардиограммы (ХМ ЭКГ) пароксизма желудочковой тахикардии. Боли в области начали беспокоить примерно за 10 дней до госпитализации.
Из перенесённых заболеваний отмечает редкие простудные заболевания. Наследственность не отягощена. Больная родила троих детей.
Объективно: общее состояние удовлетворительное, правильного телосложения, удовлетворительного питания. Кожные покровы и видимые слизистые бледно-розовой окраски. В легких прослушивается везикулярное дыхание. Размеры сердца не увеличены. Тоны ритмичные, звучность 1-го тона сохранена, акцент 2-го тона над легочной артерией. Над верхушкой прослушивается мягкий короткий систолический шум и более грубый систолический шум над легочной артерией. Частота сердечных сокращений (ЧСС) - 76 уд/мин. Артериальное давление 120/75 мм рт. ст. Живот мягкий, безболезненный. Печень не увеличена. Отеков нет.
Данные лабораторного и инструментального обследования:
♦ общий анализ мочи (от 23.02.06): светло-желтая, удельный вес - 1017, белок - отрицательный, сахар - отрицательный, лейкоциты - 1-2 в поле зрения, эпителий - 3-4 в поле зрения.
♦ общий анализ крови (от 23.02.06): эритроциты: 4,29*10^12 л, гемоглобин - 123 г/л, лейкоциты -5,0*10А9 л, формула: с - 68%, л - 29%, п - 2%, э -1%. СОЭ 5 мм/час.
♦ биохимический анализ крови (от 13.01.03): глюкоза - 4,09 ммоль/л, мочевина - 4,6 ммоль/л, холестерин - 6,6 ммоль/л, АСТ - 0,5 ммоль/ч л, АЛТ - 0,19 ммоль/ч л, К+ - 4,7 ммоль/л, № - 147 ммоль/л, СРБ < 6мг/л.
СЛУЧАЙ ИЗ ПРАКТИКИ
Журнал ГрГМУ 2007 № 1
Ультразвуковое исследование сердца (от 10.01.03): Аорта - 35 мм, левое предсердие - 46 мм, толщина межжелудочковой перегородки -11/17 мм, толщина задней стенки левого желудочка - 9/16 мм, КСР/КДР - 36/62 мм, КСО/КДО -54/195 мл, ФВ - 72%, ПЖ - 28 мм. В области меж-предсердной перегородки (МПП) определяется аневризма с основанием 26 мм и высотой 10 мм. В области аневризмы МПП определяется прерывистость контура МПП 4 мм и 1,5 мм. Створки аортального клапана не изменены. Створки митрального клапана измены миксоматозно, движение их разнонаправленное, признаки неполного расщепления задней створки. Трикуспидальный клапан и клапан легочной артерии без патологических изменений. При допплерографии выявлена митральная регургитация - скорость потока 4,9 м/с. Заключение: врожденный порок сердца: аневризма МПП, множественные дефекты МПП. Миксома-тоз створок митрального клапана. Пролапс митрального клапана 3 степени, митральная регурги-тация 2-3 степени. Частичное расщепление задней створки митрального клапана. Расширение полости левого желудочка и левого предсердия.
Электрокардиограмма (ЭКГ): ритм синусовый нерегулярный, редкие ранние желудочковые экстрасистолы. Интервал Q-T = 0,39 с, Q-Tc = 0,35 с. ЧСС - 80 ударов в минуту, отклонение электрической оси сердца (ЭОС) влево (угол а - 13°).
Анализ интервала Q-T ЭКГ (определение дисперсии - система «Поли-Спектр»): Q-T = 383 мс, Q-Tc = 439 мс, Q-Td = 49 мс, Q-Tcd = 56 мс, Q-Tcdn = 16 у.е.
Анализ ЭКГ на ППЖ: длительность QRS = 107 мс, RMS40 = 25 мкВ, LAS40 = 38 мс, StdQRS = 85 мс. Заключение: ППЖ не регистрируется.
Вариабельность ритма сердца (ВСР) от 23.02.06. R-Rmin - 704 мс, R-Rmax - 905 мс, R-RNN - 856 мс, SDNN - 41 мс, RMSSD - 55 мс, р№К50 - 2,3%, СУ - 5,29%, TP - 1721 мсА2, VLF -834 мсА2, LF - 354 мсА2, ОТ - 533 мсА2, -31%, - 20,6%, %VLF - 48,5%, LF/HF - 0,66. Заключение: общая мощность спектра нейрогумо-ральной модуляции - умеренная. Состояние ней-рогуморальной регуляции характеризуется умеренным уровнем вагальных и гуморально-метаболи-ческих (церебральных эрготропных) при низком уровне симпатических влияний в модуляции сердечного ритма. Баланс отделов вегетативной нервной системы (ВНС) характеризуется смешанным типом модуляции. Вариабельность сердечного ритма снижена.
Флюрография N° 42749 от 11.01.06. Норма.
ХМ ЭКГ от 16.02.06 г. (амбулаторно): длитель-
Рис. 1. Фрагмент ХМ ЭКГ: начало веретенообразной желудочковой тахикардии
Рис. 2. Фрагмент ХМ ЭКГ: продолжение веретенообразной желудочковой тахикардии
ХМ ЭКГ (от 27.02.06 г., на фоне приема амио-дарона): длительность наблюдения 21 час 38 минут. ЧСС средняя днем - 82 удара в минуту, ЧСС минимальная днем - 62 удара в минуту, ЧСС максимальная днем - 112 ударов в минуту, ЧСС средняя ночью - 64 удара в минуту, ЧСС минимальная ночью - 58 ударов в минуту, ЧСС максимальная ночью - 77 ударов в минуту. Одиночных наджелу-дочковых ЭС - 10 (днем - 5, ночью - 5). Парных наджелудочковых ЭС - 1 (в 3:16). Групповых над-желудочковых ЭС 1 (в 22:32). Одиночных желудочковых экстрасистол - 9 (днем - 1, ночью - 8).
ДИАГНОЗ: Врожденный порок сердца: аневризма МПП, множественные дефекты МПП. Миксо-матоз створок митрального клапана. Пролапс митрального клапана 3 степени, митральная регурги-тация 2-3 степени. Частичное расщепление задней створки митрального клапана. Пароксизмы желу-
дочковой веретенообразной тахикардии. Желудочковая и суправентрикулярная ЭС. Пароксизмы предсердной тахикардии. Н0.
Больной назначено лечение амиодароном, начиная с дозы 600 мг в сутки (10 дней), с последующим уменьшением до 400 мг в сутки (2 недели), далее длительно - 200 мг в сутки.
После выписки больная наблюдалась в кабинете нарушений ритма Гродненского ОКД, регулярно принимала амиодарон. Самочувствие оставалось удовлетворительным.
Больная повторно обследована в ОКД ноябре 2006 года (история болезни № 3484). Отмечает улучшение самочувствия, нарушений ритма не было, периодически беспокоят головные боли.
ЭКГ от 6.11.06 г. Ритм синусовый регулярный, ЧСС - 68 в 1 минуту, горизонтальное положение ЭОС. P-Q = 0,17 с, QRS = 0,1 с, Q-T = 0,38 с, Q-Tc = 0,35 с. Невыраженные нарушения реполяризации в области боковой стенки левого желудочка (уплощен зубец Т в отведениях V5-V6).
Анализ ВСР: структура ВСР указывает на патологическую стабилизацию модуляции с переходом его регуляции с рефлекторного, вегетативного уровня руководства на более низкий - гумораль-но-метаболический. Общая мощность спектра в пределах нормы. Снижение уровня вагальных и симпатических влияний и умеренными метаболическими влияниями в модуляции сердечного ритма. Баланс отделов ВНС - смешанный. ВСР снижена (SDNN - 33 мс).
Анализ ЭКГ на поздние потенциалы желудочков (ППЖ): tot QRS = 114 мс, RMS40 = 14 мкВ, LAS40 = 41 мс, Std QRS = 90 мс. Имеются 3 критерия наличия ППЖ.
Механизмы развития ДВЖТ более детально изучены у больных с СУИ QT, чем у больных с ДВЖТ без удлинения интервала Q-T. Известно, что у больных с СУИ QT в возникновении ДВЖТ основное значение имеет нарушение реполяризации, вызванное нарушением функции мембран кардио-миоцитов, вызванную фенотипической экспрессией генов, их кодирующих [3, 5]. Механизм развития этих нарушений реполяризации многофактор-
ный - генетическое нарушение функций ионных каналов, повышенная триггерная активность, региональная и временная негомогенность экспрессии функций реполяризации и проводимости (gap)
В возникновении ДВЖТ могут играть роль уровень половых гормонов и вегетативная нервная система [6]. Так, известно, что у женщин частота сердечных сокращений в покое и длительность интервала Q-T электрокардиограммы больше, чем у мужчин. У женщин также больше частота встречаемости врожденного и приобретенного интервала Q-T. Частота внезапной сердечной смерти в 3 раза выше также у женщин. Однако прогноз при ДВЖТ хуже у мужчин. Причины, лежащие в основе гендерных различий при ДВЖТ, до сих пор в деталях не выяснены.
Особенностью приводимого в данной работе случая является наличие множественных проявлений дисплазии сердца у наблюдаемой нами пациентки. По-видимому, у больных с дисплазиями соединительной ткани сердца, наряду с дефектами в генах, кодирующих структурную и функциональную информацию развития соединительной ткани сердца, имеются и нарушения в генах, кодирующих мембранные ионные токи (возникают так называемые мембранопатии или каналопатии) [4]. Литература
1. Бокерия Л.А., Ревишвили А.Ш., Проничева И.В. Синдром удлиненного интервала QT - клиника, диагностика и лечение. Анналы аритмологии // 2005. №4. - С. 7-17.
2. Кушаковский М.С. Аритмии сердца. Руководство для врачей. СПб.; ИКФ «Фолиант», 1999. - С. 347-356
3 . Antzelevich C. The role of sodium channel current in modulating transmural dispersion of repolarization and arrhythmogenesis. J. Cardiovasc Electrophysiol. 2006. Vol. 17. Suppl. 1.- S.79-85.
5. Poelzing S., Rosenbaum D.S. Cellular mechanisms of torsade de pointes // Novartis Found Symp. 2005. Vol. 266. P. 204-217.
Желудочковая тахикардия (ЖТ)
Желудочковая тахикардия это ≥ 3 последовательных желудочковых комплексов с частотой ≥ 120 ударов в минуту. Симптомы зависят от длительности и могут варьировать от их полного отсутствия до ощущения сердцебиения, коллапса гемодинамики и смерти. Диагностируется по электрокардиографии. Лечение продолжительных эпизодов проводится посредством кардиоверсии или антиаритмиков, в зависимости от симптомов. При необходимости проводится долгосрочное лечение посредством имплантируемого кардиовертера-дефибриллятора.
Некоторые эксперты используют для верификации желудочковой тахикардии (ЖТ) частоту ритма ≥ 100 ударов в минуту. Повторяющиеся желудочковые ритмы с меньшей частотой называются ускоренными идиовентрикулярными ритмами, или медленной ЖТ; как правило, они являются благоприятными и не требуют лечения при отсутствии клинической симптоматики.
Большинство пациентов с ЖТ имеют значимое заболевание сердца, в частности перенесенный инфаркт миокарда Острый инфаркт миокарда (ИМ) Острое поражение миокарда - это миокардиальный некроз в результате резкой обструкции коронарной артерии. Симптоматика данных состояний включает дискомфорт в грудной клетке, сопровождающийся. Прочитайте дополнительные сведенияЖелудочковая тахикардия может быть мономорфной и полиморфной, а также неустойчивой и устойчивой.
Мономорфная ЖТ: одиночный патологический фокус или механизм риентри и регулярные, идентичные по морфологии QRS комплексы
Полиморфная ЖТ: нескольких различных фокусов или дополнительных путей и неправильной формы QRS комплексы
Неустойчивая ЖТ: длится < 30 секунд
Устойчивая ЖТ: продолжительность ≥ 30 секунд или меньше вследствие гемодинамического коллапса
ЖТ часто переходит в фибрилляцию желудочков Фибрилляция желудочков (ФЖ) Фибрилляция желудочков вызывает нескоординированное дрожание желудочков с отсутствием эффективного сокращения. Она вызывает незамедлительное синкопе и смерть в течение нескольких минут. Лечение. Прочитайте дополнительные сведенияСимптомы и признаки желудочковой тахикардии
Короткая по длительности или с медленной частотой желудочковая тахикардия может быть асимптомной. Устойчивая ЖТ почти всегда симптомная, вызывающая сердцебиения, симптомы недостаточности гемодинамики или внезапную сердечную смерть.
Диагностика желудочковой тахикардии
Диагноз желудочковой тахикардии устанавливается по ЭКГ (см. рисунок Желудочковая тахикардия с широкими QRS Желудочковая тахикардия с широкими QRS. ). Любая тахикардия с широкими QRS комплексами (QRS ≥ 0,12 секунды) должна рассматриваться как ЖТ пока не доказана другая тахикардия.
Диагноз подтверждается при наличии на ЭКГ диссоциации зубцов Р, сливных комплексов или наджелудочковых «захватов», униформности векторов QRS в грудных отведениях (конкордантности) с дискордантным вектором Т-волны (противоположные векторы QRS), и расположении оси QRS во фронтальной плоскости в северо-западном квадранте. Дифференциальный диагноз проводится с суправентрикулярной тахикардией Пароксизмальная суправентрикулярная тахикардия (СВТ), включая синдром Вольфа-Паркинсона- Уайта В возникновении наджелудочковых тахикардий по механизму риентри (НЖТ) участвуют электрические проводящие пути, расположенные выше бифуркации пучка Гиса. У пациентов возникают эпизоды внезапного. Прочитайте дополнительные сведения из-за блокады ножек пучка Гиса или через дополнительный путь проведения (см. рисунок Модифицированные критерии Бругада для желудочковой тахикардии Модифицированные критерии Бругада для желудочковой тахикардии ). Однако по причине того, что некоторые пациенты переносят ЖТ удивительно хорошо, заключение о том, что хорошо переносимая тахикардия с широкими комплексами, вероятно, является суправентрикулярной, является ошибкой. Использование лекарств, подходящих для лечения суправентрикулярной тахикардии (например, верапамил, дилтиазем) у пациентов с ЖТ, может вызвать гемодинамический коллапс и смерть.
Здравый смысл и предостережения
По причине того, что некоторые пациенты переносят желудочковую тахикардию удивительно хорошо, ошибочным является заключение о том, что хорошо переносимая тахикардия с широкими комплексами, вероятно, является суправентрикулярной.
Пируэтная тахикардия - это специфическая форма полиморфной ЖТ у пациентов с синдромом удлиненного интервала QT. Она характеризуется быстрыми нерегулярными QRS-комплексами, которые выглядят как «переворачивающиеся» вокруг изолинии электрокардиограммы (ЭКГ). Эта аритмия может спонтанно прекратиться или трансформироваться в фибрилляцию желудочков. Она вызывает значимую недостаточность гемодинамики и часто смерть. Главным диагностическим методом является регистрация ЭКГ. Лечение внутривенно магнезией под контролем длительности QT интервала и электрическая дефибрилляция при трансформации ее в фибрилляцию желудочков.
Синдром удлиненного интервала QT, при котором может возникнуть желудочковая тахикардия, может быть врожденным и лекарственно-индуцированным. Удлинение интервала QT предрасполагает к аритмии за счет пролонгирования фазы реполяризации, которая индуцирует ранние постдеполяризации и пространственную дисперсию рефрактерности.
Врожденный синдром удлиненного интервала QT
Описано по меньшей мере 10 отдельных форм врожденного синдрома удлиненного интервала QT. Большинство случаев попадают в первые 3 подгруппы:
- Синдром удлиненного интервала QT 1-го типа (LQT1), вызываемый потерей функции за счет мутации гена KCNQ1, который кодирует катехоламин-чувствительный кардиальный калиевый ток (I Ks I)
- Синдром удлиненного интервала QT 2-го типа (LQT2), вызываемый потерей функции за счет мутации гена HERG, который кодирует другой сердечный калиевый канал I Kr
- Синдром удлиненного интервала QT 3-го типа (LQT3), вызываемый мутацией гена SCN5A, который нарушает быструю инактивацию сердечного натриевого канала I Na
Эти формы наследуются как аутосомно-доминантные заболевания с неполной пенетрацией и в прошлом относились к синдрому Романо-Уорда. В редких случаях у пациентов с 2 патологическими копиями генетической аномалии (в особенности LQT1) нарушение ассоциировано с глухотой и в прошлом называлось как синдром Джервелла - Ланге - Нильсена.
Пациенты с синдромом удлиненного интервала QT склонны к рецидивирующим синкопе и внезапной смерти, вторичными по отношению к желудочковой тахикардии, трансформирующейся в фибрилляцию желудочков .
Медикаментозно-индуцированный синдром удлиненного интервала QT
Более часто пируэтная желудочковая тахикардия (ЖТ) возникает вследствие действия лекарств, обычно антиаритмических препаратов Ia, Ic или III классов. К другим препаратам, которые могут индуцировать пируэтную желудочковую тахикардию, относятся трициклические антидепрессанты, фенотиазины и некоторые противовирусные и противогрибковые препараты (см. CredibleMeds для ознакомления с актуальным списком).
Клинические проявления
У пациентов часто наблюдается синкопе вследствие прекращения перфузии мозга при частоте сокращения желудочков 200-250 ударов в минуту. У пациентов в сознании обычно отмечается сердцебиение. Иногда удлиненный интервал QT обнаруживается после успешной реанимации.
ЭКГ при двунаправленной желудочковой тахикардии

Желудочковая пароксизмальная тахикардия
Желудочковая пароксизмальная тахикардия (ЖТ) —это внезапно начинающийся и так же внезапно заканчивающийся приступ учащения желудочковых сокращений до 100–200 уд. в мин. при сохранении правильного сердечного ритма. Импульсы образуются в клетках ножек пучка Гиса и их разветвлений или в непосредственно в миокарде самих желудочков.
Желудочковая пароксизмальная тахикардия занимает первое место среди всех жизнеугрожающих аритмий, так как способна перейти в трепетание и фибрилляцию желудочков, при которых происходит сбой сердечного ритма и без оказания реанимационных мероприятий асистолия (клиническая смерть).
У мужчин желудочковая тахикардия развивается в 2 раза чаще, чем у женщин.
Пациенты с желудочковыми пароксизмальными тахикардиями госпитализируются в экстренном порядке в отделения кардиологической реанимации.
Патогенез
- Повторный вход волны возбуждения (re-entry), локализующийся в проводящей системе или в миокарде желудочков.
- Эктопический очаг повышенного автоматизма.
- Эктопический очаг триггерной активности.
Классификация желудочковых пароксизмальных тахикардий
- Клиническая классификация желудочковых пароксизмальных тахикардий
- Пароксизмальные неустойчивые желудочковые тахикардии.
- Характеризуются появлением трех и более подряд эктопических комплексов QRS, регистрирующихся при мониторной записи ЭКГ в пределах не более 30 с.
- Такие пароксизмы не оказывают влияния на гемодинамику, но повышают риск ФЖ и внезапной сердечной смерти .
- Продолжаются более 30 с.
- Эта разновидность желудочковых тахикардий отличается высоким риском внезапной сердечной смерти и сопровождается значительными изменениями гемодинамики (аритмогенный шок, острая левожелудочковая недостаточность).
- Особые формы желудочковых тахикардий
- Двунаправленная желудочковая тахикардия.
Правильное чередование комплексов QRS, обусловленное распространением импульсов из двух различных участков желудочков или разным проведением импульсов из одного источника.
Неустойчивая (до 100 комплексов) двунаправленная желудочковая тахикардия с волнообразным нарастанием и снижением амплитуды комплексов QRS. Ритм неправильный, с частотой 200 -300/мин. и выше. Развитию «пируэта» обычно предшествует удлинение интервала QT и ранние желудочковые экстрасистолии. Неустойчивая двунаправленная желудочковая тахикардия с волнообразным нарастанием и снижением амплитуды комплексов склонна к рецидивированию.
Возникает при наличии более двух эктопических очагов.
Возобновляется после периодов основного ритма.
Этиология желудочковых пароксизмальных тахикардий
- 85% всех желудочковых тахикардий развивается у больных ИБС (острый инфаркт миокарда, постинфарктная аневризма, реперфузионные аритмии).
- Некоронарогенные желудочковые пароксизмальные тахикардии могут развиваться при остром миокардите, постмиокардическом кардиосклерозе, гипертрофической кардиомиопатии, дилатационной кардиомиопатии, рестриктивной кардиомиопатии, пороках сердца, артериальной гипертензии, пролапсе митрального клапана,
- Амилоидоз, саркоидоз,
- Операции на сердце.
- Дигиталисная интоксикация.
- Аритмогенное действие лекарств и желудочковые аритмии на фоне электролитных нарушений.
- «Сердце спортсмена». Возможна внезапная аритмическая смерть на фоне большой нагрузки или после нее.
- Генетически детерминированные заболевания, при которых желудочковые экстрасистолии \ желудочковые пароксизмальные тахикардии являются основным клиническим проявлением.
10. В 2% случаев желудочковая тахикардия регистрируется у пациентов, не имеющих достоверных клинических и инструментальных признаков органического поражения сердца (“идиопатическая” форма желудочковой тахикардии).
Клиника
Нарушения ритма и проводимости могут протекать как бессимптомно, так и с яркой симптоматикой, которая выразается в виде ощущений сердцебиения, артериальной гипотензией, болями в области сердца, обмораками и проявлениями острой сердечной недостаточности.
Диагностика
- ЭКГ.
- Мониторирование ЭКГ по Холтеру.
- Внутрисердечное электрофизиологическое исследование (ЭФИ) сердца.
- Чреспищеводная ЭКГ.
- Эхокардиография.
- Физикальное обследование.
- Пробы с физической нагрузкой.
Дифференциальная диагностика
Наджелудочковые тахикардии. Аритмии.
Общие принциы купирования пароксизма желудочковой тахикардии
Немедленное лечение требуется при любом приступе желудочковой тахикардии.
При выраженных нарушениях гемодинамики проводят экстренную дефибрилляцию.
При невозможности использования дефибриллятора кардиоверсии предшествует прекордиальный удар, непрямой массаж сердца и искусственная вентиляция легких.
При утрате больным сознания дефибрилляция повторяется на фоне в/в струйного введения адреналина 1.0 мл 10% р-ра на 10.0 мл физраствора.
При отсутствии пульса введение необходимо произвести в подключичную вену или внутрисердечно.
Вместе с адреналином вводятся антиаритмические препараты (под контролем ЭКГ!):
Необходима немедленная отмена препарата, который мог вызвать желудочковую тахикардию.
Медикаментозное купирование пароксизма желудочковой тахикардии.
После купирования пароксизмов желудочковой тахикардии в/в введение противоаритмических препаратов и/или препаратов калия показано в течение 24 часов.
Профилактика
1. Антиаритмическая терапия.
Поддерживающая антиаритмическая терапия проводится главным образом амиодароном или соталолом. К сожалению, подбор антиаритмической терапии возможен только у 50% больных злокачественными желудочковыми аритмиями.
2. У больных после инфаркта миокарда назначают аспирин, ингибиторы АПФ, статины и блокаторы рецепторов альдостерона, а также бета-блокаторы.
3. При недостаточной эффективности медикаментозной терапии используют следующие методики:
Противопоказана установка кардиовертер-дефибрилляторов больным с репрерывно рецидивирующей желудочковой тахикардией, с WPW – синдромом, терминальной застойной недостаточностью и др.
После имплантации кардиовертер-дефибрилляторов необходимость в назначении антиаритмиков сохраняется в 70% случаев, главным образом для снижения частоты желудочковой тахикардии и уменьшения ЧСС во время пароксизмов желудочковой тахикардии. При этом только амиодарон (возможно в сочетании с бетаблокаторами) и соталол не оказывают влияния на порог дефибрилляции, что необходимо для эффективной работы имплантируемого кардиовертер-дефибриллятора.
Аневризмэктомия является предпочтительным вмешательством у больных с желудочковыми экстрасистолиями \ желудочковыми пароксизмальными тахикардиями с постинфарктной аневризмой.
Прогноз
Нормальная функция левого желудочка указывает на низкий риск возникновения в ближайшее время нарушений желудочкового ритма высоких градаций, в том числе фибрилляции желудочков, а также внезапной сердечной смерти.
Низкая фракция выброса, как правило, ассоциируется с высоким риском возобновления желудочковых аритмий или возникновения внезапной сердечной смерти.
Прогноз при двунаправленной (веретенообразной) желудочковой тахикардии типа “пируэт” всегда серьезен: часто возникает трансформация полиморфной желудочковой тахикардии в фибрилляцию желудочков или устойчивую мономорфную желудочковую тахикардию. Риск внезапной сердечной смерти при этом достаточно высок.
Нестойкая желудочковая тахикардия
Нестойкую желудочковую тахикардию рассматриваüt как промежуточный вид желудочковых аритмий между триггерными - экстрасистолами и стойкой желудочковой тахикардией и фибрилляцией желудочков.
Поскольку нестойкая желудочковая тахикардия быстро проходит и, как правило, протекает бессимптомно, она выявляется в основном при длительном мониторировании ЭКГ.
Причины и распространенность. За редким исключением аритмия связана с органической патологией сердца. Ее частота в бессимптомных случаях составляет 0-3 %.
Из всех заболеваний сердца нестойкую желудочковую тахикардию вызывает идиопатическая дилатационная кардиомиопатия в 50 % случаев и гипертрофическая кардиомиопатия в 15-28 % случаев.
Нестойкая желудочковая тахикардия - весьма распространенное осложнение раннего периода острого инфаркта миокарда.
Этиология
- Поражение венечных артерий сердца.
- Аневризмы левого желудочка.
- Дисфункция.
- Системная артериальная гипертензия с гипертрофией левого желудочка,.
- Ревматические пороки сердца.
- Вторичные кардиомиопатии.
Симптомы
Нестойкая желудочковая тахикардия в большинстве случаев протекает бессимптомно и обнаруживается лишь при длительном мониторировании ЭКГ.
Диагностика
Течение и прогноз.
Нестойкая желудочковая тахикардия является фактором риска фатальных желудочковых аритмий у больных с гипертрофической кардиомиопатией и острым инфарктом миокарда.
Стойкая мономорфная желудочковая тахикардия
В большинстве случаев частота ритма желудочков при стойкой мономорфной желудочковой тахикардии находится в пределах 100-220 в 1 мин.
Причины
- ИБС.
- Аневризма сердца.
- Дилатационная кардиомиопатия.
- Гипертрофическая кардиомиопатия.
- Воспалительные и инфильтративные кардиомиопатии.
- Саркоидоз сердца.
- Лекарственное происхождение - передозировка сердечных гликозидов, а также прием антиаритмических препаратов I класса.
Симптомы
Артериальная гипотензия: головокружение, резкая слабость, нарушения зрения, появление или усугубление одышки.
При клиническом обследовании в случае отсутствия существенных нарушений гемодинамики отмечается лишь тахикардия. У большинства пациентов определяется артериальная гипотензия различной степени выраженности, потливость, нарушение сознания - от возбуждения и оглушенности до его отсутствия при резком снижении мозгового кровотока. Возможно развитие клиники кардиогенного шока.
Больным, перенесшим стойкую желудочковую тахикардию или имеющим в анамнезе обмороки, показано углубленное обследование, которое включает:
- Эхокардиографию,
- нагрузочное тестирование для выявления желудочковых эктопических аритмий, связанных с физической нагрузкой,
- ЭФИ.
Осложнения
- потеря сознания вследствие острой ишемии головного мозга
- возникновение фибрилляции желудочков и внезапная остановка кровообращения;
- острая сердечная недостаточность - отек легких и кардиогенный шок;
- усугубление застойной сердечной недостаточности.
Специфическая профилактика повторных приступов стойкой мономорфной желудочковой тахикардии включает медикаментозную антиаритмическую терапию, хирургическую или катетерную абляцию и имплантацию кардиовертера-дефибриллятор а.
ЭКГ при двунаправленной желудочковой тахикардии
ФГБУ «НМИЦ эндокринологии» Минздрава России, Москва, Россия
ФГБУ "Эндокринологический научный центр" Минздрава России, Москва
ФГБУ «Эндокринологический научный центр» Минздрава России, Москва, Российская Федерация
Эндокринологический научный центр, Москва
ФБГУ "Эндокринологический научный центр" Минздравсоцразвития России, Москва
Московский государственный университет им. М.В. Ломоносова, Москва, Российская Федерация
ФГБУ «Эндокринологический научный центр» Минздрава России
Устойчивая желудочковая тахикардия у пациента с единственным желудочком сердца и феохромоцитомой
Журнал: Проблемы эндокринологии. 2019;65(2): 107‑112
ФГБУ «НМИЦ эндокринологии» Минздрава России, Москва, Россия
Феохромоцитома – редкая опухоль, развивающаяся из адреномедуллярных хромаффинных клеток и продуцирующая один или несколько катехоламинов (адреналин, норадреналин, дофамин), редко – гормонально неактивная. Цианотические пороки сердца также являются относительно редкой патологией, и одним из наиболее редких их вариантов является единственный желудочек сердца. Предположительно, у пациентов с цианотическими пороками сердца частота встречаемости феохромоцитом и параганглиом может быть выше вследствие наличия определенных герминативных и соматических мутаций. При цианотических пороках сердца развитие злокачественных аритмий является одной из частых причин смерти. Казуистически редко сочетание феохромоцитом с единственным левым желудочком сердца: в литературе описано всего восемь таких случаев. Нами описан уникальный случай сочетания единственного левого желудочка сердца, феохромоцитомы и устойчивой желудочковой тахикардии у молодого пациента. Причиной желудочковой тахикардии, по всей видимости, в данном случае являлась неадекватная медикаментозная терапия (назначение верапамила). Проведение хирургического лечения феохромоцитомы и направление пациента на кардиохирургическое лечение стало возможно только после коррекции антигипертензивной и антиаритмической терапии: замены верапамила на комбинацию доксазозина и амиодарона с достижением синусового ритма и относительно удовлетворительных показателей АД.
ФГБУ «НМИЦ эндокринологии» Минздрава России, Москва, Россия
ФГБУ "Эндокринологический научный центр" Минздрава России, Москва
ФГБУ «Эндокринологический научный центр» Минздрава России, Москва, Российская Федерация
Эндокринологический научный центр, Москва
ФБГУ "Эндокринологический научный центр" Минздравсоцразвития России, Москва
Московский государственный университет им. М.В. Ломоносова, Москва, Российская Федерация
ФГБУ «Эндокринологический научный центр» Минздрава России
Актуальность
Цианотические пороки сердца (ЦПС) – подгруппа врожденных нарушений нормальной анатомии сердца, которые проявляются вскоре после рождения признаками системной гипоксии и гипоксемии, обусловленными нарушениями внутрисердечной гемодинамики. Частота встречаемости врожденных пороков сердца среди новорожденных колеблется от 7,05 на 1000 новорожденных в европейской популяции до 13,08 на 1000 новорожденных в азиатской популяции. Во взрослой популяции врожденные пороки сердца встречаются с частотой 4,09 случая на 1000 человек [1, 2].
Феохромоцитома (ФХ) – опухоль, развивающаяся из адреномедуллярных хромаффинных клеток, продуцирующая один или несколько катехоламинов (адреналин, норадреналин, дофамин), редко – гормонально-неактивная [3]. Частота встречаемости ФХ у пациентов с артериальной гипертонией или инциденталомами надпочечника составляет соответственно 0,1 и 4% [4]. Встречаемость Ф.Х. в общей популяции оценивается как 1 случай на 100 000 человек в год и менее [5–6].
Среди ЦПС одним из наиболее редких является единственный желудочек сердца. По данным L. Coats и соавт., опубликованным в 2015 г., частота встречаемости этого порока в Великобритании составляет 16 на 100 000 новорожденных, 2 на 100 000 взрослых [7]. Еще более редко его сочетание с феохромоцитомой: в литературе описано всего 8 таких случаев [8–14].
Интересно, что 70–80% пациентов с феохромоцитомами и параганглиомами (ПГ, производные вненадпочечниковых хромаффинных клеток нервного гребня) имеют определенное сочетание специфических герминативных и соматических мутаций. По данным Cancer Genome Atlas (TCGA), вовлеченные в эти комплексы мутаций гены разделены на три кластера: группу псевдогипоксии (включающую SDHA, SDHB, SDHC, SDHD, SDHAF2, VHL и HIF2α); группу Wnt-сигнального пути (CSDE1 и MAML3); группу киназных сигнальных путей (RET, NF1, TMEM127, MAX, HRAS). Мутации в генах псевдогипоксической группы были ассоциированы с нарушением регуляции фактора, индуцируемого гипоксией (HIF) – кислородзависимого фактора, вовлеченного в клеточный и тканевой ответ на гипоксию (заключающийся в неоангиогенезе, модуляции апоптоза, пролиферативных реакций, изменении уровня метаболизма клетки) [15].
Эти генетические данные позволяют по-новому взглянуть на многие классические работы, посвященные тканевым и клеточным изменениям в условиях истинной гипоксии. Так, например, известно, что гломусные клетки каротидного синуса чувствительны к концентрации кислорода в крови, как и хромаффинные клетки надпочечников в постнатальный период. Более того, хроническая гипоксемия приводит к гиперплазии каротидного синуса, а у людей, проживающих в высокогорье, риск развития ФХ и ПГ выше, чем у жителей равнин [16]. Также в клетках ФХ и ПГ нарушено строение митохондрий (основных органелл клеточного дыхания), а в одной из работ был описан случай регрессии ПГ после достижения ремиссии хронической гипоксии. Почти 25% (5/21) пациентов с диагностированной в Университете Джона Хопкинса с 1901 по 1962 г. ФХ имели ЦПС, также опубликованы несколько случаев сочетания этих патологий. Более того, по данным аутопсии, частота встречаемости врожденных пороков сердца при периферических опухолях из производных нервного гребня значимо выше, чем в среднем в популяции [16].
Соответственно предполагается, что у пациентов с ЦПС повышена частота встречаемости ФХ и ПГ [16].
Несмотря на казуистически редкое сочетание синих пороков сердца и ФХ, А. Opotowsky и соавт. в 2015 г. удалось провести исследование, показавшее, что частота встречаемости ФХ и ПГ у пациентов, госпитализируемых в связи с ЦПС, значительно выше, чем у остальных пациентов, причем эта разница не зависела от других известных факторов риска развития опухолей из хромаффинных клеток (исследование проведено ретроспективно на основании американской базы данных Nationwide Inpatient Sample, включавшей почти 17 тыс. случаев) [17].
Ретроспективное исследование R. George и соавт. [18] также продемонстрировало значимо более высокую частоту встречаемости пороков развития сердца у пациентов с нейробластомами по сравнению с таковой у пациентов с лейкемией (20 и 3,6% соответственно). Тем не менее доказательная база взаимосвязи хронической гипоксии и развития ФХ и ПГ остается недостаточной. В последние годы выживаемость пациентов с врожденными ЦПС увеличивается и, благодаря этому, могут быть получены данные, позволяющие подтвердить или опровергнуть наличие описанных закономерностей [16].
В литературе описано достаточно много случаев желудочковой тахикардии (ЖТ) у пациентов с ФХ [19–25]. G. Stenstrom и соавт. в 1988 г. описали 31 пациента с ФХ: средний интервал QT в данной выборке был нормальным на момент постановки диагноза (440±40 мс), несколько укорачивался после назначения феноксибензамина (430±20 мс) и снижался до 410±20 мс после хирургического лечения. При этом у 35% пациентов на момент постановки диагноза QTc был больше 440 мс, а послеоперационно эти явления сохранились лишь у двух пациентов [25]. По данным других авторов, увеличение интервала QT встречается у 35% пациентов с ФХ, однако к формированию желудочковых нарушений ритма это приводит в единичных случаях [26].
При ЦПС развитие злокачественных аритмий является одной из частых причин смерти. В большом мультицентровом исследовании пациентов с различными формами врожденных пороков сердца причиной 14% летальных исходов стали именно аритмии, в подавляющем большинстве случаев – фибрилляция желудочков [27].
В то же время смертность пациентов, перенесших операцию Фонтена (формирование тотального кавапульмонального соединения), лишь в 9,2% случаев обусловлена внезапной сердечной смертью (в частности, желудочковыми аритмиями). Этот показатель значительно уступает летальности после самой операции Фонтена (68%) и сопоставим со смертностью от хронической сердечной недостаточности (ХСН) (6,6%) и тромбоэмболий (7,2%) [28]. Эпидемиологических данных о частоте мономорфных желудочковых тахикардий у пациентов с единственным левым желудочком сердца нам не удалось найти.
Поэтому описанный в данной статье пациент представляет особенный интерес в связи с редкостью сочетания имеющихся у него патологий. От всех предыдущих опубликованных в литературе пациентов описываемый случай отличается наличием рецидивирующей желудочковой тахикардии.
Описание случая
Результаты физикального, лабораторного и инструментального исследования
При поступлении на ЭКГ регистрировалась желудочковая тахикардия (рис. 1),
![]()
Рис. 1. Электрокардиограмма при поступлении. Регистрируется мономорфная желудочковая тахикардия. которая сопровождалась артериальной гипотонией до 90/70 мм рт.ст.
Тахикардия длилась от нескольких минут до 1 часа, купировалась спонтанно, но рецидивировала. Для контроля ритма больному был отменен верапамил, перорально назначены амиодарон в насыщающих дозах (200 мг 2 раза в день), бета-адреноблокаторы (метопролола сукцинат 12,5 мг 2 раза в день с последующим увеличением до 25 мг 2 раза в день), продолжена терапия альфа-адреноблокаторами (доксазозин 6 мг 2 раза в сут). В течение 2 сут удалось достичь устойчивого синусового ритма. В то же время развилось повышение АД до 200/100 мм рт.ст., в связи с чем к терапии была добавлена пролонгированная форма нифедипина 30 мг на ночь, иАПФ (эналаприл 5 мг 2 раза в день).
Клинико-лабораторное обследование:
При ЭхоКГ (рис. 2)
![]()
Рис. 2. Данные эхокардиографии. а – короткая парастернальная позиция на уровне митрального клапана; б – верхушечная 4-х камерная позиция, диастола; в – верхушечная 4-х камерная позиция, систола. отмечалась митральная и трикуспидальная регургитация II–III степени, функционирующее овальное окно диаметром 4–5 мм, единственный двуприточный левый желудочек, фракция выброса левого желудочка – 75%.
При компьютерной томографии выявлено образование правого надпочечника с четкими и ровными контурами, размером 39×37×43 мм, нативная плотность – 44 HU.
Дифференциальный диагноз
Для исключения МЭН-синдрома проведено УЗИ щитовидной и околощитовидных желез, дополнительных образований не выявлено, также были исключены функциональные нарушения щитовидной железы. Таким образом, была диагностирована ФХ.
Лечение
Назначен доксазозин в начальной дозе 6 мг в сут, рекомендовано оперативное лечение в объеме правосторонней адреналэктомии.
Учитывая часто рецидивирующую желудочковую тахикардию, сердечную недостаточность, пациенту была продолжена терапия амиодароном (400 мг в сут) и метопрололом (50 мг в сут). Для достижения оптимальных показателей АД были назначены эналаприл 10 мг в сут, нифедипин 30 мг в сут.
Исход и результаты последующего наблюдения
Спустя 5 мес пациент был вновь госпитализирован в ФГБУ НМИЦ эндокринологии МЗ Р.Ф. Назначенной ранее терапии пациент придерживался, за прошедшее время доза доксазозина была увеличена до 16 мг в сут. На этом фоне достигались показатели АД в пределах 110–170/70–100 мм рт.ст. На сериях ЭКГ регистрировалась синусовая тахикардия с ЧСС 90–100/мин, жалоб на нарушения ритма сердца пациент не предъявлял, синкопальных и предсинкопальных состояний не отмечал.
На момент госпитализации симптомы ХСН выражены умеренно, на уровне 2-го функционального класса по NYHA. По данным Холтеровского мониторирования ЭКГ, желудочковых нарушений ритма не было.
Учитывая персистирующее повышение уровня калия в крови (до 5,8 ммоль/л) и креатинина (до 123 мкмоль/л, рСКФ по CKD-EPI – 72 мл/мин/1,73 м 2 ), иАПФ были отменены. В связи с высокой ЧСС покоя (90–100/мин) была увеличена доза метопролола сукцината до 50 мг в сут. Блокатор кальциевых каналов (нифедипин) был отменен в связи с оптимальным контролем АД на фоне терапии альфа- и бета-адреноблокаторами. Терапия амиодароном была продолжена.
В условиях отдела хирургии ФГБУ НМИЦ эндокринологии МЗ РФ пациенту была выполнена лапароскопическая правосторонняя адреналэктомия. Полученный гистологический материал соответствовал феохромоцитоме альвеолярного типа гистологического строения с фиброзной дегенерацией в центре. Послеоперационный период протекал без особенностей, рецидивов желудочковой тахикардии не отмечалось, АД контролировалось оптимально. Пациент был выписан на 10-е сутки после оперативного вмешательства и направлен к кардиохирургам для проведения хирургического лечения порока сердца.
Несмотря на крайне редкое сочетание ФХ и врожденных пороков сердца, такие случаи могут встретиться в клинической практике кардиолога, эндокринолога и хирурга.
Лечение таких пациентов требует особенно внимательного подхода, поскольку некоторые препараты, рутинно назначаемые при одной патологии, могут быть противопоказаны при наличии сопутствующих заболеваний. Вероятно, именно назначение пациенту верапамила в описываемом случае (с единственным желудочком сердца, ХСН и ФХ) на фоне морфологических изменений миокарда и отмены бета-адреноблокаторов привело к развитию у него устойчивой ЖТ. В литературе уже были описаны случаи ЖТ, инициированных назначением верапамила [29]. После отмены верапамила и назначения больших доз альфа-, бета-адреноблокаторов и амиодарона удалось достичь нормализации ритма сердца, что позволило провести хирургическое лечение ФХ и планировать дальнейшие этапы лечения врожденного порока сердца.
Возможно, удлинение интервала QT при ФХ (на фоне высоких концентраций катехоламинов в крови) в некоторых случаях может быть расценено как проявление синдрома удлиненного QT первого типа – состояния, связанного с одновременным наличием двух популяций калиевых каналов в миокарде – дисфункциональных и интактных. Этот тип синдрома характеризуется парадоксальным ответом на введение катехоламинов – QT удлиняется более чем на 30 мс, тогда как у здоровых людей при повышении концентрации катехоламинов в крови – QT укорачивается [30, 31].
Также необходимо отметить, что, помимо верапамила, вклад в развитие ЖТ могли внести как слабость синусового узла, так и отмена бета-блокаторов у пациента с ФХ.
Срочное хирургическое лечение ЖТ у больного с ЦПС и ФХ, на наш взгляд, было неоправданно. Его следовало рассматривать при неэффективности антиаритмической терапии после нормализации уровня катехоламинов. Имплантация кардиовертера-дефибриллятора не была рекомендована в силу вероятной обратимости причины Ж.Т. Частота жизнеугрожающих нарушений ритма сердца у пациентов с ФХ остается неопределенной, что требует проведения дальнейших исследований.
Заключение
Данный клинический случай отражает сложную комбинацию потенциально жизнеугрожающих заболеваний: единственного левого желудочка сердца и ФХ у молодого пациента. Назначение недигидропиридинового кальциевого блокатора (верапамила) привело к развитию рецидивирующей устойчивой Ж.Т. Хирургическое лечение ФХ и направление пациента на кардиохирургическое лечение стали возможны только после коррекции антигипертензивной и антиаритмической терапии: замены верапамила на комбинацию доксазозина и амиодарона с достижением синусового ритма и относительно удовлетворительных показателей АД.
Дополнительная информация
Источник финансирования. Статья подготовлена на личные средства авторского коллектива.
Согласие пациента. Пациент добровольно подписал информированное согласие на публикацию персональной медицинской информации в обезличенной форме в журнале «Проблемы эндокринологии».
Конфликт интересов. Авторы декларируют отсутствие явных и потенциальных конфликтов интересов, связанных с публикацией настоящей статьи.
Участие авторов: все авторы внесли значимый вклад в подготовку статьи, прочли и одобрили финальную версию перед публикацией.
Читайте также:
- Пароксизмальные неустойчивые желудочковые тахикардии.