Хирургическое лечение диффузного токсического зоба. Профилактика тиреотоксического криза
Добавил пользователь Дмитрий К. Обновлено: 27.01.2026
Большинство наиболее авторитетных исследователей в области тиреоидологии сходятся во мнении о том, что идеальное лечение при диффузном токсическом зобе (ДТЗ) должно обеспечивать быстрое устранение клинических симптомов тиреотоксикоза и сопровождаться минимальным риском осложнений для больного [1, 2, 7]. К сожалению, в настоящее время клиническая практика не располагает методом лечения, в полной мере отвечающим этим требованиям. Выбор метода лечения при ДТЗ во многом определяется приверженностью специалистов и их опытом в применении того или иного метода лечения, особенностями национальных эндокринологических и хирургических школ, возможностями конкретного лечебного учреждения, в также полом, возрастом больного, вариантами клинического течения заболевания, пожеланиями пациента и рядом других факторов. Можно отметить, что рекомендации, даваемые специалистами в Европе, США и Японии, различны. Консервативная терапия антитиреоидными препаратами достаточно широко распространена в странах Европы, однако низкая частота достижения стойкой ремиссии заболевания не удовлетворяет эндокринологов [1,5, 32, 40, 42]. Терапия радиоактивным йодом, широко используемая в США и странах Западной Европы, являющаяся достаточно эффективным методом лечения ДТЗ, приводит с течением времени к развитию гипотиреоза практически у всех больных [16, 20], также необходимо учитывать риск развития рака щитовидной железы, молочных желез, бесплодия и тяжелого остеопороза у женщин в пременопаузальном периоде [10, 13, 18, 19]. Хирургическое лечение занимает значительное место в терапии ДТЗ, обеспечивая пациенту наиболее быстрое достижение эутиреоидного состояния, однако, как любое оперативное вмешательство, сопровождается рядом характерных осложнений [2, 46]. Тем не менее в Японии тиреоидэктомия считается основным методом лечения ДТЗ.
Ключевые слова
Для цитирования:
For citation:
Большинство наиболее авторитетных исследователей в области тиреоидологии сходятся во мнении о том, что идеальное лечение при диффузном токсическом зобе (ДТЗ) должно обеспечивать быстрое устранение клинических симптомов тиреотоксикоза и сопровождаться минимальным риском осложнений для больного [1, 2, 7]. К сожалению, в настоящее время клиническая практика не располагает методом лечения, в полной мере отвечающим этим требованиям. Выбор метода лечения при ДТЗ во многом определяется приверженностью специалистов и их опытом в применении того или иного метода лечения, особенностями национальных эндокринологических и хирургических школ, возможностями конкретного лечебного учреждения, в также полом, возрастом больного, вариантами клинического течения заболевания, пожеланиями пациента и рядом других факторов. Можно отметить, что рекомендации, даваемые специалистами в Европе, США и Японии, различны. Консервативная терапия антитиреоидными препаратами достаточно широко распространена в странах Европы, однако низкая частота достижения стойкой ремиссии заболевания не удовлетворяет эндокринологов [1,5, 32, 40, 42]. Терапия радиоактивным йодом, широко используемая в США и странах Западной Европы, являющаяся достаточно эффективным методом лечения ДТЗ, приводит с течением времени к развитию гипотиреоза практически у всех больных [16, 20], также необходимо учитывать риск развития рака щитовидной железы, молочных желез, бесплодия и тяжелого остеопороза у женщин в пременопаузальном периоде [10, 13, 18, 19]. Хирургическое лечение занимает значительное место в терапии ДТЗ, обеспечивая пациенту наиболее быстрое достижение эутиреоидного состояния, однако, как любое оперативное вмешательство, сопровождается рядом характерных осложнений [2, 46]. Тем не менее в Японии тиреоидэктомия считается основным методом лечения ДТЗ.
Показаниями к хирургическому лечению ДТЗ, по мнению многих авторов, являются зоб больших размеров с признаками компресии окружающих органов и анатомических структур (независимо от тяжести тиреотоксикоза), сочетание ДТЗ с неопластическими процессами в щитовидной железе, тиреотоксикоз тяжелой степени, отсутствие стойкого эффекта от комплексной консервативной терапии, непереносимость тиреостатических препаратов, наличие загрудинно расположенного зоба [2, 26, 30, 34]. Кроме того, некоторые исследователи считают оправданным оперативное вмешательство при невозможности постоянного контроля за консервативным лечением больного, а также при настоятельном желании пациента, обусловленном необходимостью быстрого возвращения к работе [30].
Публикации последних лет свидетельствуют о том, что в специализированных хирургических стационарах послеоперационной летальности и развития послеоперационного тиреотоксического криза практически не наблюдается, что в первую очередь обусловлено оптимизацией предоперационной подготовки больных, адекватной интенсивной терапией в раннем послеоперационном периоде. Однако в литературе имеются данные о том, что послеоперационная летальность может достигать 3,1% [27, 31, 45]. Грозным осложнением является кровотечение в области операционной раны, которое может привести к летальному исходу в результате развития гематомы и асфиксии и поэтому требует срочного повторного вмешательства с эвакуацией излившейся крови и сгустков из раны и остановкой кровотечения. При субтотальной тиреоидэктомии может быть поврежден возвратный гортанный нерв, причем в случае одностороннего его поражения развивается дисфония, которая обычно проходит в течение нескольких недель, а при двустороннем повреждении может развиться обструкция дыхательных путей, которая требует наложения трахеостомы. Частота развития паралича голосовых связок при хирургическом лечении ДТЗ, поданным ряда авторов, достигает 4,4% [27, 451. Послеоперационный гипопаратиреоз может быть транзиторным или постоянным. Транзиторный гипопаратиреоз развивается в результате удаления части паращитовидных желез и нарушения кровоснабжения оставшихся желез. Симптомы гипопаратиреоза развиваются на 1—7-й день после операции, обусловлены снижением уровня кальция в крови и проявляются клинически наличием парестезий и повышенной нервно-мышечной возбудимости с развитием приступов тетании, появлением характерных симптомов Хвостека, Труссо, Вейса, Шлезингера. Частота развития этого осложнения не превышает 3,6% [27, 45]. При выраженном транзиторном гипопаратиреозе необходимо внутривенное введение глюконата кальция, а в качестве постоянной заместительной терапии рекомендуется назначение витамина D в сочетании с препаратом кальция. К поздним послеоперационным осложнениям относят рецидив тиреотоксикоза, частота которого варьирует между 0,6 и 17,9%, гипотериоз, развивающийся с частотой 4—29,7% [27, 41,45, 50], хотя некоторые авторы не рассматривают послеоперационный гипотиреоз у больных, оперированных по поводу ДТЗ, как осложнение, считая его свидетельством эффективной операции [35].
Следовательно, обсуждая общие тенденции в хирургическом лечении ДТЗ, можно отметить, что в последние годы хирурги рекомендуют оставлять меньше ткани щитовидной железы, полагая, что рецидив тиреотоксикоза является тяжелым осложнением. Большинство авторов сходятся во мнении о целесообразности оставления 4—8 г ткани щитовидной железы. Вместе с тем некоторые исследователи считают, что тиреоидный остаток менее 5 г в большинстве наблюдений ведет к развитию стойкого гипотиреоза [39]. По мнению многих авторов, степень лимфоидной инфильтрации ткани щитовидной железы следует рассматривать в качестве фактора риска развития послеоперационного гипотиреоза [20, 38, 39, 47, 53]. Несмотря на то что лимфоцитарная инфильтрация является весьма характерным признаком аутоиммунного тиреоидита (болезни Хашимото), она также выявляется при ДТЗ, составляя 57,6 и 83,5% наблюдений соответственно [39|. Отмечено влияние лекарственных препаратов на выраженность лимфоидной инфильтрации, в частности лечение пропранололом в предоперационном периоде увеличивает лимфоидную инфильтрацию по сравнению с применением тиреостатических препаратов [48]. Имеется мнение о том, что гипотиреоз развивается в 50% наблюдений при наличии лимфоидной инфильтрации и в 22% при ее отсутствии [49]. Тем не менее другие авторы не установили какой-либо связи между лимфоидной инфильтрацией щитовидной железы и частотой развития послеоперационного гипотиреоза [15]. Мнения о роли антител к тиреоидной пероксидазе также неоднозначны, а порой и противоречивы. Некоторые исследователи полагают, что более высокий титр антител к тиреоидной пероксидазе связан с высоким риском развития гипотиреоза после операции [38], тогда как другие авторы указывают на то, что высокий титр антимикросомальных антител является прогностически неблагоприятным фактором в плане развития рецидива тиреотоксикоза после оперативного лечения [23]. Проведены работы, показавшие, что антитела к тиреоидной пероксидазе обнаруживаются не более чем у половины больных ДТЗ и их титр не коррелирует с тяжестью тиреотоксикоза. Это позволило авторам сделать вывод о том, что указанный вид антител является маркером аутоиммунного процесса в щитовидной железе, но не определяет специфики ее поражения ]6]. Важно отметить, что установлена выраженная прямая корреляционная связь между титром антител к тиреоидной пероксидазе и степенью лимфоидной инфильтрации щитовидной железы [3]. Значительное прогностическое значение в послеоперационном функциональном состоянии щитовидной железы имеет уровень тиреостимулирующих антител. Отмечено, что у больных с высоким дооперационным уровнем антител к рецептору ТТГ, который остается повышенным и после операции, чаще развивается рецидив тиреотоксикоза [37, 43, 44|. Данные выводы подтверждаются и другими работами, в которых показано, что послеоперационный уровень антител к рецептору ТТГ у больных с рецидивным тиреотоксикозом был значительно выше, чем у больных в эутиреоидном или латентном гипотиреоидном состоянии, у которых он практически всегда был в пределах нормы [39]. Последнее исследование выявило 2 закономерности: во-первых субтотальная тиреоидэктомия может вызвать иммунологическую ремиссию, во-вторых, повышенный уровень тиреостимулирующих антител является достоверным прогностическим фактором развития послеоперационного рецидива (если у больного нет иммунологической ремиссии, рецидив тиреотоксикоза может возникнуть и без наличия других осложняющих факторов) [39|. Группа авторов предложили новый маркер для прогнозирования послеоперационного рецидива тиреотоксикоза — изменение уровня тиреостимулирующих антител на фоне консервативной терапии: при отсутствии изменений их титра значительно возрастает риск послеоперационного рецидива тиреотоксикоза [49, 53]. Однако эти интересные данные требуют дальнейшего уточнения на большом клиническом материале. Проведены работы, показавшие зависимость частоты рецидива тиреотоксикоза после субтотальной резекции щитовидной железы у больных с ДТЗ от потребления йода с водой и пищей. Выявлено, что рецидив чаше встречается у жителей районов с высоким средним потреблением йода, тогда как в районах, эндемичных по зобу (где существует дефицит йода), рецидивы выявляются реже [21, 51].
Исходя из вышесказанного, очевидно, что масса оставшейся ткани щитовидной железы должна рассчитываться с учетом ряда других факторов. В зависимости от мнения авторов о роли тех или иных показателей в прогнозировании послеоперационной тиреоидной функции рекомендации по их учету при расчете массы тиреоидного остатка различны. Разработана методика расчета массы оставшейся ткани щитовидной железы с учетом возраста больного, длительности заболевания ДТЗ, длительности лечения тиреостатическими препаратами, гистологической структуры ткани, которая позволила авторам значительно снизить частоту развития послеоперационного гипотиреоза [3]. Некоторые исследователи при определении остаточной массы щитовидной железы считают значимыми факторами титр антител к рецептору ТТГ, тиреоидной пероксидазе, рекомендуя у пациентов с высоким титром указанных антител оставлять меньшую массу железы [48 ]. В позднее опубликованной работе эти же авторы рекомендуют учитывать изменение уровня антител к рецептору ТТГ и оставлять менее 4 г ткани щитовидной железы у больных без уменьшения титра антител к рецептору ТТГ на фоне антитиреоидной терапии. Проведены исследования, показавшие, что масса оставшейся ткани щитовидной железы у больных с высоким титром антител к тиреоидной пероксидазе должна составлять 5 г [25]. Имеются данные, о том что рецидив ДТЗ чаше отмечается у тех больных, у которых заболевание сопровождается эндокринной офтальмопатией, в связи с чем авторы считают целесообразным более радикальное хирургическое лечение при сочетании ДТЗ и эндокринной офтальмопатии [4]. Однако в другой работе, оценивающей отдаленные результаты хирургического лечения ДТЗ, не выявлено зависимости между наличием эндокринной офтальмопатии, объемом щитовидной железы до лечения, функциональным состоянием железы в предоперационном периоде и функцией щитовидной железы в отделенном периоде после субтотальной резекции щитовидной железы [9]. Существует мнение о том, что для улучшения результатов хирургического лечения необходимо идентифицировать пациентов, склонных к рецидиву тиреотоксикоза, по высокому уровню тиреостимулирующих антител и HLAтипированию и использовать у этой группы больных более радикальную операцию, а у пациентов с низким риском рецидива оставлять около 10 г железы, тем самым снижая вероятность гипотиреоза [37, 42J. Другие авторы рекомендуют прогнозировать рецидивы тиреотоксикоза с учетом 3 показателей — наличия антител к рецептору ТТГ, антигенов HLA-B8 и HLA-DR3 и состояния клеточного иммунитета (по снижению соотношения Т-хелперов и Т-супрессоров), считая, что при сочетании указанных факторов вероятность развития рецидивов достигает 80% [8].
Необходимо отметить, что в литературе, появившейся за последний год, имеются рекомендации по увеличению объема оперативного вмешательства при ДТЗ вплоть до тиреоидэктомии [23, 24, 29]. Мнение некоторых авторов заключается в том, что концепция проведения хирургического лечения ДТЗ без развития рецидива тиреотоксикоза и послеоперационного гипотиреоза неверна [23]. Исследования показывают, что тотально-субтотальная резекция щитовидной железы или тиреоидэктомия с последующей замещающей терапией являются методом выбора в лечении ДТЗ в связи с тем, что существует прямая корреляция между частотой рецидива и объемом операции (причем рецидивы исключаются при удалении возможно большего объема ткани щитовидной железы), а достоверных различий в частоте осложнений после субтотальной резекции и тиреоидэктомии не отмечено [23, 24]. Нам представляются интересными работы, прослеживающие течение офтальмопатии после различных видов лечения ДТЗ (наиболее часто сравнивают лечение радиоактивным йодом и хирургическое вмешательство). После тиреоидэктомии у большинства пациентов отмечается различной степени улучшение течения офтальмопатии, в то время как радиоактивный йод чаше вызывает прогрессирование офтальмопатии. Тем не менее необходимо отметить, что в работах, оценивающих влияние субтотальной резекции щитовидной железы и тиреоидэктомии, показано, что субтотальная резекция щитовидной железы может сопровождаться ухудшением течения офтальмопатии, что авторы связывают с увеличением уровня антител к рецепторам ТТГ [29].
По мнению многих авторов, которое совпадает и с нашей точкой зрения, при назначении пациенту с ДТЗ консервативной терапии необходимо прогнозировать ее результат с учетом тяжести заболевания, степени лимфоидной инфильтрации ткани, объема железы, иммунологических показателей (уровня антител к рецептору ТТГ), генетических маркеров (наличия определенных антигенов системы HLA), и при неблагоприятном их сочетании более настоятельно рекомендовать хирургическое лечение. При проведении оперативного лечения ДТЗ очевидна необходимость индивидуального подхода к расчету объема оставшейся ткани щитовидной железы с учетом прогностических факторов, что подтверждается исследованиями, проводимыми и в наших клиниках. Очевидно, что риск осложнений при проведении субтотальной тиреоидэктомии во многом зависит от квалификации и опыта хирургической бригады.
Для выбора правильной тактики лечения этой сложной категории больных необходимо их сосредоточение в специализированных терапевтических и хирургических стационарах, работающих в тесном контакте и обладющих значительным опытом диагностики и лечения пациентов с различными заболеваниями щитовидной железы. Исследования, результаты которых мы обсуждаем, проводили в крупных медицинских центрах, число обследованных больных составляло 250—300 человек. Для изучения частоты развития послеоперационного гипотиреоза и рецидива тиреотоксикоза при хирургическом лечении ДТЗ в России необходимо также проведение многоцентровых рандомизированых исследований.
Диффузный токсический зоб (болезнь Грейвса, Базедова болезнь)
Информация, представленная на странице, не должна быть использована для самолечения или самодиагностики. При подозрении на наличие заболевания, необходимо обратиться за помощью к квалифицированному специалисту. Провести диагностику и назначить лечение может только ваш лечащий врач.
Содержание статьи:
Что такое диффузный токсический зоб?
Болезнь Грейвса (Базедова болезнь, диффузный токсический зоб, ДТЗ) – аутоиммунная патология, характеризующаяся избытком тиреоидных гормонов, продуцируемых щитовидной железой. Повышенный уровень этих гормонов провоцирует тиреотоксикоз – состояние, при котором иммунная система человека атакует собственный организм, как следствие, поражаются практически все органы и системы.
Тиреотоксикоз и болезнь Грейвса – не синонимы. Тиреотоксикоз – синдром, сопутствующий ДТЗ, но он также может присутствовать при других патологиях и быть вызванным другими причинами (передозировка L-тироксина, опухоли, метастазы).
Женщины страдают Базедовой болезнью примерно в 5 раз чаще мужчин. В большинстве случаев патология манифестирует в возрасте от 20 до 50 лет, однако случаи заболевания фиксируются у детей и пожилых людей. Существует версия, что заболеванию более подвержены люди, испытывающие хронический стресс. ДТЗ считается опасным для жизни, так как приводит к необратимым изменениям в органах и тканях Источник:
Диффузный токсический зоб. Пашенцева А.В., Вербовой А.Ф. Клиническая медицина, 2017. с. 780-788 .
Классификация и степени тяжести диффузного токсического зоба
Клинические рекомендации по диагностике, лечению и профилактике болезни Грейвса предлагают несколько вариантов ее классификации:
- по О. В. Николаеву;
- рекомендованная Всемирной организацией здравоохранения (ВОЗ);
- по степени тяжести тиреотоксикоза – I и II вариант.
Классификация Базедовой болезни по О. В. Николаеву
Эта классификация имеет преимущества перед предложенной ВОЗ, так как содержит больше степеней градации заболевания, что позволяет клиницистам применять более точные лечебные назначения на каждой стадии.
Классификация, рекомендованная ВОЗ
Классификация по степени тяжести тиреотоксикоза: I вариант
В зависимости от объема поражения щитовидной железы и имеющихся симптомов, выделяют три степени тяжести заболевания:
- легкая – снижение работоспособности, тахикардия – увеличение частоты сердечных сокращений (ЧСС) до 100 ударов в минуту (уд/мин), снижение массы тела на 10-15 %;
- средняя – характеризуется высокой нервной возбудимостью, ЧСС достигает 100-120 ударов в минуту, потеря веса превышает 20 %;
- тяжелая – тахикардия свыше 120 уд/мин, потеря веса может превышать более половины от изначальной массы тела, появляются тяжелые осложнения, приводящие к полной утрате трудоспособности.
Классификация по степени тяжести тиреотоксикоза: II вариант
Предложена в 2007 году В. В. Фадеевым и Г. А. Мельниченко. Как и I вариант, основывается на степени выраженности клинических проявлений и гормональных нарушений. Учитывает содержание в крови гормонов щитовидной железы.
Субклинический тиреотоксикоз (легкая степень). Для нее характерно отсутствие клинических симптомов или их стертые проявления. Содержание тиреотропного гормона (ТТГ) снижено, содержание свободного (св.) Т4 и свободного (св.) Т3 – в пределах нормы.
Манифестный тиреотоксикоз (средняя степень). Описывается развернутой клиникой, существенно сниженным содержанием ТТГ, повышением концентрации св. Т4 и св. Т3.
Осложненный тиреотоксикоз (тяжелая степень). Выраженная сочетанная симптоматика, психотические явления, резкое снижение массы тела. Содержание ТТГ существенно ниже нормы, концентрации св. Т4 и Т3 повышены.
Причины Базедовой болезни
Болезнь Грейвса – аутоиммунное заболевание. При этом состоянии возникает аутоиммунная агрессия – иммунная система, под воздействием определенных факторов, начинает вырабатывать антитела, действующие на органы-мишени. В первую очередь – это щитовидная железа, которая в ответ начинает вырабатывать гормоны в неправильном режиме.
Основная причина ДТЗ – генетическая предрасположенность. В большинстве случаев она этнически ассоциирована – гаплотипы, отвечающие за развитие болезни, обнаруживаются у людей европейской расы.
Диффузный токсический зоб может возникнуть на фоне других аутоиммунных патологий эндокринной системы – сахарного диабета I типа, первичного гипокортицизма.
Симптомы заболевания
Симптоматика ДТЗ обусловлена повышенной продукцией гормонов щитовидной железы, воздействующих практически на весь организм человека. Основными признаками Базедовой болезни являются симптомы тиреотоксикоза, которые можно разделить на группы, в зависимости от того какую систему они затрагивают Источник:
Морфологические критерии диагностики диффузного токсического зоба. Боташева В.С., Эльканова А.Б., Лавриненко А.А. Медико-фармацевтический журнал «Пульс», 2019. с. 6-11 .
Симптомы со стороны центральной и периферической нервной системы:
- раздражительность, возбудимость, суетливость, плаксивость, нарушения сна;
- симптом Мари – тремор (дрожание) вытянутых пальцев рук;
- симптом «телеграфного столба» – тремор всего тела;
- повышение сухожильных рефлексов;
- иногда – развитие тиреотоксического психоза.
Симптомы при поражении сердечно-сосудистой системы:
- синусовая тахикардия, увеличение ЧСС;
- повышение систолического (верхнего) артериального давления и снижение диастолического (нижнего);
- увеличенное пульсовое давление (разница между систолическим и диастолическим);
- при тяжелой степени заболевания – мерцательная аритмия или ее пароксизмы;
- миокардиодистрофия, возникновение недостаточности кровообращения.
Симптоматика, появляющаяся при поражении желудочно-кишечного тракта:
- повышение аппетита;
- частый жидкий стул;
- нарушение работы печени вплоть до тиреотоксического гепатоза.
Симптомы поражения других эндокринных желез:
- дисфункция яичников, сбой менструального цикла, снижение либидо у женщин;
- гинекомастия и нарушения потенции у мужчин;
- относительная надпочечниковая недостаточность;
- нарушение толерантности к глюкозе, провоцирующее сахарный диабет II типа.
Синдром эктодермальных нарушений:
- ломкость ногтей;
- сечение и выпадение волос;
- кожный зуд, горячая, влажная на ощупь кожа;
- появление витилиго.
Гиперметаболизм (ускоренный обмен веществ):
- прогрессирующая потеря веса на фоне повышенного аппетита;
- чувство жара, субфебрильная температура тела;
- миастения (слабость мышц), адинамия;
- остеопороз.
Наличие зоба – важный признак болезни Грейвса, который имеется практически у всех пациентов, однако степень выраженности этого симптома различна, а тяжесть заболевания не зависит от величины зоба.
Эндокринная офтальмопатия (ЭОП) – еще один признак ДТЗ. Она, в большинстве случаев, проявляется примерно на год позже синдрома тиреотоксикоза, имеет разную степень выраженности.
Симптомы ЭОП:
- экзофтальм (выпученные глаза), часто несимметричного характера;
- блеск глаз;
- редкое мигание;
- светобоязнь, слезотечение, резь и жжение в глазах;
- отечность и пигментация век;
- диплопия (удвоение изображения) при взгляде вверх или в сторону.
В редких случаях, у 3-4 % пациентов, при Базедовой болезни развивается претибиальная микседема – одно- или двустороннее четко очерченное уплотнение багрово-синюшного цвета на передней поверхности голени, затрагивающее кожу и подкожно-жировую клетчатку.
У детей ДТЗ развивается остро, у пожилых пациентов – чаще протекает бессимптомно или со стертой симптоматикой. У женщин тяжелая форма заболевания препятствует наступлению беременности, повышает риск выкидышей, мертворождения.
Осложнения болезни Грейвса
При поздней диагностике и отсутствии адекватной терапии ДТЗ приводит к необратимым поражениям всех органов и полной инвалидизации организма. Не исключен и летальный исход из-за нарушения функций сердечно-сосудистой системы и тяжелой аритмии. Заболевание может вызвать следующие осложнения:
- остеопороз;
- сахарный диабет II типа;
- тиреотоксический гепатоз.
Наиболее грозное осложнение Базедовой болезни – тиреотоксический криз. Он может развиться вследствие стресса, сопутствующих заболеваний, оперативного лечения, выраженной физической нагрузки, резкой смены климата. Состояние требует неотложной помощи.
Симптомы тиреотоксического криза:
- резкое возбуждение;
- повышение температуры тела до 40° C;
- увеличение ЧСС до 200 ударов в минуту;
- повышение пульсового давления;
- фибрилляция предсердий;
- надпочечниковая недостаточность – гиперпигментация, нитевидный пульс, нарушения микроциркуляции.
Диагностика ДТЗ
План диагностики диффузного токсического зоба включает следующие мероприятия:
- сбор анамнеза;
- общий осмотр – состояние кожи, волос, ногтей, наличие тремора рук;
- физикальное обследование – измерение веса, роста, артериального давления, частоты пульса;
- осмотр и пальпация щитовидной железы;
- офтальмологический осмотр;
- УЗИ или МРТ щитовидной железы;
- лабораторные исследования – общий анализ и биохимия крови, определение содержания ТТГ, св. Т3, св. Т4, гормонов гипофиза, титра антител к рецептору ТТГ, титра «классических» антител к щитовидной железе;
- дополнительные методы обследования (по показаниям) – электрокардиография, изотопная сцинтиграфия, тонкоигольная пункционная биопсия щитовидной железы Источник:
Диагностика и лечение болезни Грейвса. Фадеев В.В. Медицинский совет, 2014. с. 44-48 .
Лечение Базедовой болезни
Пациентов с болезнью Грейвса курирует терапевт или эндокринолог. Диффузный токсический зоб лечится тремя способами:
- медикаментозная терапия тиреостатическими препаратами;
- радиойодтерапия;
- хирургическое лечение Источник:
Тактика лечения диффузного токсического зоба. Бебезов Б.Х., Иуралиев М.А., Какчеева Т.Т., Салиева Б.Е., Чазымов Р.М. Клиническая медицина, 2013. с. 61-67 .
Тиреостатические препараты для лечения диффузного токсического зоба назначаются, если объем щитовидной железы не превышает 40 куб. см, нет признаков сдавления окружающих тканей и больших узлов в железе, отсутствуют осложнения заболевания. Если после курса терапии тиреостатиками случился рецидив, повторный курс лечения не назначается. Продолжительность тиреостатической терапии – 12-18 месяцев, во время ее проведения пациентам с диффузным токсическим зобом необходим постоянный контроль показателей общего анализа крови.
Радиойодтерапия заключается в приеме внутрь рассчитанной индивидуально для каждого больного дозы йода-131, который после накопления в щитовидной железе и последующего распада приводит к лучевой деструкции тироцитов (клеток щитовидной железы), что, по сути, является нехирургическим методом ее удаления. Метод мало распространен в России. Противопоказан беременным женщинам и в период лактации Источник:
Высокодозная радиойодтерапия болезни Грейвса. Солодкий В.А., Фомин Д.К., Галушко Д.А., Пестрицкая Е.А. Вестник Российского научного центра рентгенорадиологии Минздрава России, 2013 .
Хирургическое лечение подразумевает удаление всей щитовидной железы или ее большей части. После операции больному назначается пожизненная заместительная терапия препаратом «Левотироксин», доза которого рассчитывается индивидуально.
Лечение диффузного токсического зоба народными средствами неэффективно и, вследствие затягивания с обращением к врачу, может привести к развитию непоправимых осложнений. При появлении признаков тиреотоксикоза необходимо обратиться за медицинской помощью.
Прогноз и профилактика заболевания
При своевременной диагностике и правильном лечении прогноз диффузного токсического зоба благоприятный. Препараты для лечения ДТЗ общедоступны, адекватная заместительная терапия приводит к нормализации метаболизма и исчезновению симптомов. При позднем обращении к врачу возможно возникновение осложнений заболевания и ухудшение прогноза, вплоть до утраты работоспособности, инвалидизации и летального исхода вследствие необратимых поражений органов и систем.
Для профилактики Базедовой болезни людям, входящим в группу риска (диагностированный ДТЗ у родственников) рекомендуется отказаться от курения, избегать стрессовых ситуаций, нормализовать режим питания и рацион, периодически, по назначению врача, контролировать ТТГ.
Хирургическое лечение диффузно-токсического зоба

Врач-эндокринолог. Доктор медицинских наук. Профессор. Заведующая кафедрой эндокринологии лечебного факультета РНИМУ им. Н.И. Пирогова.
Сегодня мы ответим на самые распространенные вопросы пациентов с сахарным диабетом, которые любят путешествовать.
Остеопороз – заболевание скелета, характеризующееся снижением костной массы и как следствие переломами при минимальной травме.
О том, что у меня диабет, я узнал случайно, когда проходил диспансерное обследование на работе. У меня не было никаких жалоб, я ощущал себя совершенно здоровым. В анализе крови выявлено повышение сахара крови – 6.8 ммоль/л. Меня направили к эндокринологу. Доктор сказала, что это выше нормы (норма меньше 6.1 ммоль/л) и нужно провести дополнительное обследование: тест с сахарной нагрузкой. Мне измерили сахар натощак (он снова был выше нормы – 6.9 ммоль/л) и дали выпить стакан очень сладкой жидкости – глюкозы. При измерении сахара крови через 2 часа он был также выше нормы – 14.0 ммоль/л (должен быть не более 7.8 ммоль/л). Также я сдавал анализ крови на гликированный гемоглобин (показывыает «средний» уровень сахара за 3 месяца). Он был тоже высоким – 7 % (а допускается не более 6%).
Диффузно-токсический зоб, или Базедова болезнь – это заболевание, при котором происходит увеличение щитовидной железы (зоб), которое сопровождается усиленной выработкой тиреоидных гормонов Т3 и Т4(гипертиреоз) и отравление ими организма (тиреотоксикоз).
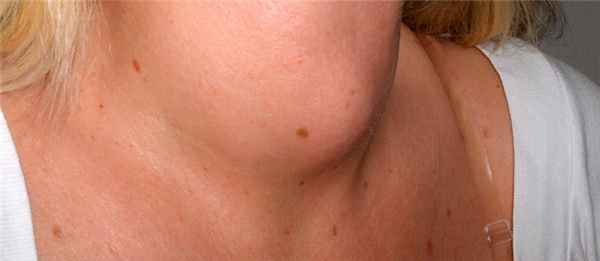
Почему возникает диффузно-токсический зоб?
Диффузный токсический зоб образуется в результате аутоиммунного процесса, который может быть спровоцирован инфекционным заболеванием и нервными стрессами. У женщин диффузно-токсический зоб образуется в три раза чаще, чем у мужчин. Преимущественный возраст развития заболевания – 20-50 лет. Большую роль в развитии диффузного токсического зоба играет наследственный фактор. Другие провоцирующие факторы– злоупотребление антивирусными препаратами, курение, избыток йода в организме.
При каких симптомах следует безотлагательно обратиться к врачу?
Гормоны щитовидной железы регулируют обменные процессы. При диффузном токсическом зобе образуется их избыток, что приводит к активизации обменных процессов и энергетическому истощению организма. В первую очередь от этого страдают нервная и сердечно-сосудистая системы.
Главные симптомы диффузно-токсического зоба – пучеглазие и увеличение щитовидной железы. Другие характерные симптомы – дрожание пальцев (тремор), повышенная возбудимость, резкие перепады настроения, тревога, беспокойство, раздражительность, плаксивость, бессонница, похудание, потливость, одышка, учащение пульса, повышение артериального давления, диарея, субфебрильная температура и другие признаки тиреотоксикоза.
Наиболее опасное осложнение диффузно-токсического зоба –тиреотоксический криз, при котором сильная возбужденность, доходящая до психоза, и двигательная гиперактивность резко сменяются апатией. Этот процесс сопровождается тошнотой, тахикардией, жаром (лихорадкой) с возможным развитием мерцательной аритмии и сердечной недостаточности.
В каких случаях показано оперативное лечение диффузно-токсического зоба?
Показания к хирургическому лечению диффузно-токсического зоба:
- значительные размеры зоба,
- сдавление зобом трахеи и нарушении дыхания,
- сдавление зобом пищевода и крупных сосудов,
- наличие осложнений (мерцательной аритмии, сердечной недостаточности)
- при неэффективности медикаментозной терапии,
- аллергия к препаратам, применяемым для лечения тиреотоксикоза,
- стойкое снижение уровня лейкоцитов в крови.
Как проводится операция?
Хирургическое лечение диффузно-токсического зоба означает полное удаление щитовидной железы (ВОЗ 2011). Такая операция называется Тиреоидэктомия. До операции проводится медикаментозная терапия для достижения компенсированного состояния, назначается УЗИ-обследование.
Хирургическое лечение диффузного токсического зоба выполняется под общим наркозом. По намеченным линиям выполняется разрез, щитовидная железа выделяется, пересекаются сосуды щитовидной железы, отделяется околощитовидная железа. Щитовидная железа удаляется с оставление паращитовидных желез. После этого сшиваются мышцы шеи, устанавливается дренаж, накладываются нерассасывающиеся или рассасывающиеся косметические швы.
Послеоперационный период
После операции назначается заместительная терапия L-тироксином. Первые 3,6 месяцев необходимо наблюдение эндокринологом, контролировать уровень гормонов, соблюдать врачебные рекомендации и принимать прописанные препараты. Непосредственно после операции могут быть назначены процедуры для нормальной функции бронхо-легочной системы после наркоза (ингаляции, отхаркивающие средства и др.). Стероидные препараты отменяются на 3-5 сутки после операции.
Первые два-три дня после операции показано жидкое или полужидкое питание с повышенным содержанием калорий и витаминов, постельный режим.
Мы стремимся оказывать качественные услуги с высоким уровнем сервиса. Мы благодарны нашим пациентам за оказанное доверие и отзывы о нашем медицинском центре.
Хирургическое лечение диффузного токсического зоба. Профилактика тиреотоксического криза
Хирургическое лечение диффузного токсического зоба. Профилактика тиреотоксического криза
Хирургическое лечение в виде субтотальной субфасциальной резекции щитовидной железы является также одним из распространенных методов лечения токсического зоба, которое направлено на уменьшение массы избыточно функционирующей щитовидной железы. Показанием для операции являются средняя и тяжелая форма диффузного и смешанного токсического зоба при отсутствии эффекта консервативной терапии, узловые и загрудинные формы, тнреотоксическая аденома, токсический зоб в детском и юношеском возрасте, период беременности (I—II триместр), лактации, токсический зоб, осложненный мерцанием предсердии (применяется и лечение I131).
Противопоказанием служит токсический зоб, осложненный психозом.
Учитывая возможность возникновения тиреотоксического криза в послеоперационном периоде, больные со средней и тяжелой формой заболевания нуждаются в предоперационной подготовке мерказолилом. Критерием степени подготовленности больных к хирургическому вмешательству является значительное уменьшение токсических признаков заболевания и доведение больных в отдельных случаях до эутиреоидного состояния, что в свою очередь является гарантией предупреждения обострения тиреотоксикоза в послеоперационном периоде.
Лечение мерказолилом вызывает некоторую пролиферативную реакцию ткани щитовидной железы, что несколько осложняет хирургическое вмешательство, но служит надежной гарантией сохранения жизни больного. Уменьшения пролифератпппон реакции можно добиться путем добавления препаратов микродоз йода в течение 2-3 недель, предшествующих операции.

Хирургический метод лечения является высокоэффективным, но не лишен осложнений, таких, как гипотиреоз, тетания, тиреотоксические послеоперационные кризы, парезы возвратного нерва, рецидивы заболевания, кровоизлияние в диафрагмальный нерв и др.
Обращает на себя внимание появление поздних гипотиреозов после хирургического лечения и терапии I131, которые безусловно не связаны с избыточным удалением количества щитовидной железы или введения большой дозы I131. Изучение патогенеза этого вида гипотиреозов показало, что у подобных больных наблюдается значительное увеличение по сравнению с нормой титра антител к щитовидной железе и тиреоглобулину. Этот факт свидетельствует о том, что при хирургическом вмешательстве или лечении I131 повреждение щитовидной железы сопровождается попаданием в кровь белков щитовидной железы, в том числе и тиреоглобулина, что стимулирует образование в организме аутоантител, способствующих дальнейшему повреждению ткани щитовидной железы.
Таким образом, поздние гипотиреозы можно отнести к группе аутоагрессивных заболеваний. Из этого следует, что в лечении данных форм гипотиреозов, кроме заместительной терапии тиреоидином и трийодтиропином, важное значение приобретает лечение глюкокортикоидами, способствующими уменьшению титра аутоантител. Особое внимание следует уделять применению глюкокортикоидпых препаратов в комплексном лечении токсического зоба.
Основанием этого служит снижение глюкокортикоидной функции коры надпочечников параллельно степени тяжести токсического зоба. В результате ускорения метаболизма кортизола, имеющего место при токсическом зобе, функция коры надпочечников постепенно истощается, что подтверждается секционными данными, свидетельствующими о гипоплазии и атрофии коры надпочечников при тяжелых формах токсического зоба. Поэтому в клинической практике у больных тяжелой формой заболевания, особенно в пожилом возрасте, вместе с аптитиреоидной терапией рекомендуется использовать глюкокортикоидные препараты (преднизолои в дозах 5-20 мг в день).
Диффузный токсический зоб (базедова болезнь)
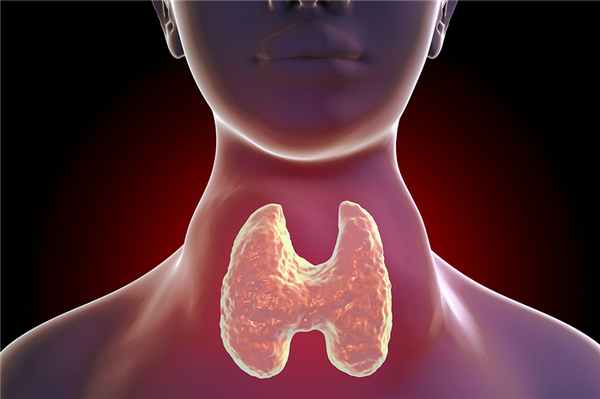
В последние годы отмечается неуклонный рост заболеваний щитовидной железы во всем мире, включая и такое заболевание как диффузный токсический зоб (болезнь Грейвса, Базедова болезнь).
Причины возникновения диффузного токсического зоба:
Диффузный токсический зоб является аутоиммунным заболеванием, то есть в основе его развития лежит врожденный дефект в иммунной системе. На фоне предрасполагающих факторов (стресс, беременность), может начаться повышенный синтез аутоантител к рецепторам тиреотропного гормона (ТТГ), расположенных на мембране фолликулярных клеток щитовидной железы. Это приводит к формированию зоба и тиреотоксикозу.
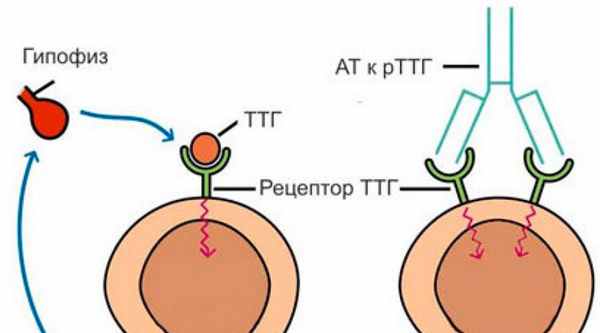
Основные проявления диффузного токсического зоба:
- разнообразные проявления, которые затрагивают сердечную деятельность – ощущение сердцебиения, повышение артериального давления, появление одышки. При осмотре - тахикардия. Очень часто на ЭКГ регистрируется нарушение ритма – фибрилляция предсердий. Именно поэтому, когда впервые на ЭКГ регистрируется данное нарушение ритма обязательно надо исключить заболевание щитовидной железы.
- эндокринные нарушения, которые подразумевают снижение веса, повышение температуры тела, нарушение менструального цикла у женщин, снижение потенции у мужчин.
- нарушение процессов пищеварения – диарея, тошнота.
- неврологические нарушения, которые проявляются выраженным тремором рук, головными болями, постоянным беспокойством, бессонницей, тревогой, раздражительностью, эмоциональной неустойчивостью.
- при длительном нелеченном тиреотоксикозе может развиться снижение костной массы - остеопения. Снижение костной плотности, особенно у пожилых, является фактором риска развития переломов.
- может быть увеличение размеров щитовидной железы (зоб).
- Примерно у 40 % пациентов с ДТЗ развивается эндокринная офтальмопатия, которая характеризуется поражением мягких тканей орбиты: ретробульбарной клетчатки, глазодвигательных мышц; с вовлечением зрительного нерва и вспомогательного аппарата глаза (век, роговицы, коньюктивы, слезной ретробульбарная боль, боль при движениях глазами, эритема век, отек или припухлость век, гиперемия конъюнктивы, глазодвигательных мышц.
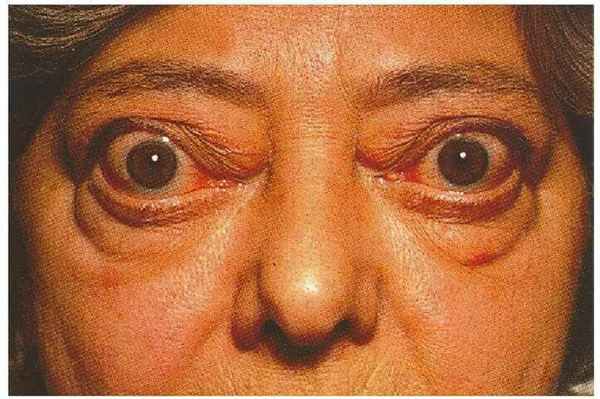
Как поставить диагноз:
- Определение функции щитовидной железы:
Проводится определения содержания тиреоидных гормонов в крови: св. Т4 и св. Т3, базального уровня ТТГ. Концентрация ТТГ при тиреотоксикозе должна быть низкой (< 0.1 мЕ/л), содержание в сыворотке свТ4 и свТ3 повышено.
Антитела к рТТГ выявляются у 99-100% больных диффузным токсическим зобом. В процессе лечения или спонтанной ремиссии заболевания антитела могут снижаться или исчезать.
С помощью УЗИ определяется объем и эхоструктура ЩЖ. В норме объем ЩЖ у женщин не должен превышать 18 мл, у мужчин 25 мл.
Лечение диффузного токсического зоба:
Методы лечения тиреотоксикоза:
- консервативное (прием антитиреоидных препаратов)
- оперативное (тиреоидэктомия)
- лечение радиоактивным йодом
Немного о каждом варианте лечения:
Консервативное лечение
Назначается для достижения эутиреоза в качестве базового длительного курса лечения, который, в некоторых случаях, приводит к стойкой ремиссии или перед оперативным лечением или радиойотерапией. Важным моментом планирования длительной тиростатической терапии является готовность пациента следовать четко всем рекомендациям врача и наличие доступной эндокринологической помощи (регулярность посещения врача и своевременный контроль анализов).
Тиамазол (тирозол, мерказолил ) является препаратом выбора для всех пациентов, которым планируется проведение консервативного лечения диффузного токсического зоба, за исключением лечения в первом триместре беременности, тиреотоксического криза и развития побочных эффектов на тиамазол, когда предпочтение следует отдать пропилтиоурацилу (ПТУ, пропицилу).
Тиамазол в начале назначаются в относительно больших дозах: 30 — 40 мг (на 2-3 приема) или ПТУ — 300 – 400 мг (на 3 — 4 приема). На фоне такой терапии спустя 4 недели у большинства больных с тиреотоксикозом удается достичь эутиреоидного состояния (нормализация св. Т4 и св. Т3). Уровень ТТГ может еще долго оставаться пониженным. На период до достижения эутиреоза, а зачастую и на более длительный срок, пациентам с явным тиреотоксикозом целесообразно назначение бета-адреноблокаторов (конкор 5 мг/сут., атенолол — 50-100 мг/сут, метопролол 50-100 мг/сут). При тяжелом тиреотоксикозе и при наличии симптомов надпочечниковой недостаточности (выраженная слабость, гипотония) назначаются глюкокортикоиды: преднизолона –10-15 мг в сутки перорально или гидрокортизона 50-75 мг в сутки внутримышечно.
После того как произошла нормализация уровня св. Т4 - больному диффузным токсическим зобом начинают снижать дозу Тиамазола до поддерживающей - 10 мг в день.
При развитии гипотиреоза на фоне приема Тиамазола назначается Л-тироксин в средней дозе 25 — 50 мкг в день, до нормализации ТТГ крови. Цель терапии - поддержание нормального уровня св. Т4 и ТТГ.
Перед началом терапии Тиамазолом рекомендуется выполнить клинический анализ крови, биохимический анализ крови (АЛТ, АСТ, общий билирубин). У всех пациентов, получающих тиреостатики при фебрильных состояниях и при фарингите, ангине следует незамедлительно отменить терапию, определять уровень лейкоцитов и лейкоцитарную формулу и срочно посетить эндокринолога для оценки возможных побочных действий препарата.
Лечение продолжается в течение 12-18 месяцев, после чего она постепенно отменяется, при условии стабильно нормального уровня ТТГ и антител к рецептору ТТГ. При правильно проведенном лечении частота рецидивов после отмены тиреостатических препаратов составляет 70% и более. Если после отмены Тиамазола вновь развивается тиреотоксикоз, необходимо рассмотреть вопрос о проведении радиойодтерапии или тиреоидэктомии.
Хирургической лечение
Оперативное лечение показано при загрудинном расположения зоба, диффузных и зловых формах зоба с компрессионным синдромом, отказе пациента от РЙТ. В настоящее время, в связи с большим процентом рецидивов после операции выполняется полное удаление щитовидной железы - тотальная тиреоидэктомия. После тиреоидэктомии по поводу ДТЗ рекомендуется определение уровня кальция, и, при необходимости, назначение дополнительно препаратов кальция и витамина Д. Пациент должен знать что после такой операции пожизненно принимается гормональнозаместительная терапия левотироксином. Левотироксин (эутирокс, L-тироксин) назначают сразу в полной заместительной дозе из расчета, ориентировочно, 1.7 мкг/кг веса пациента, с контролем ТТГ крови через 6 недель после назначения терапии.
Радиойодтерапия
Радиойодтерапия – при ДТЗ проводится в случае рецидива тиреотоксикоза после проведенного консервативного лечения, невозможности приема тиреостатических репаратов (лейкопения, аллергические реакции), отсутствия условий для консервативного лечения и наблюдения за больным. Цель радиойодтерапии – уменьшение гиперфункционирующей ткани щитовидной железы и достижение стойкого гипотиреоидного состояния, с назначением в последующем заместительной терапии левотироксином.
Читайте также:
- Брадикардия при инфаркте миокарда
- Актиновые филаменты и актиновый цитоскелет клетки
- Кардиоверсия при фибрилляции предсердий. Кардиоверсия при трепетании предсердий
- Фолликулярная карцинома щитовидной железы. Медуллярная, анапластическая карцинома щитовидной железы
- Аномалии кишечника. Дискинезии тощей и подвздошной кишки
