Кроветворение. Кроветворение плода. Экстрамедуллярный гемопоэз.
Добавил пользователь Алексей Ф. Обновлено: 29.01.2026
кроветворение
гемопоэз
Процесс размножения, развития и созревания клеток крови путем последовательных дифференциаций из исходной стволовой клетки; специализация клеток крови и снижение их способности к митозу при К. генетически детерминированы; у беспозвоночных К. связано с полостной жидкостью, у позвоночных - со специализированными кроветворными органами (костный мозг, селезенка и др.).
[Арефьев В.А., Лисовенко Л.А. Англо-русский толковый словарь генетических терминов 1995 407с.]
Тематики
Синонимы
4 hemopoiesis
5 hemopoiesis
6 hemopoiesis
7 hemopoiesis
8 hemopoiesis
9 hemopoiesis
10 hemopoiesis-stimulating drug
11 arrest of hemopoiesis
12 bone-marrow hemopoiesis
13 extramedullary hemopoiesis
14 fetal hemopoiesis
15 hematopoiesis (hemopoiesis)
16 hepatic hemopoiesis
17 phys hemopoiesis
18 pronephric hemopoiesis
19 arrest of hemopoiesis
20 extramedullary hemopoiesis
См. также в других словарях:
hemopoiesis — hemopoiesis. См. гемопоэз. (Источник: «Англо русский толковый словарь генетических терминов». Арефьев В.А., Лисовенко Л.А., Москва: Изд во ВНИРО, 1995 г.) … Молекулярная биология и генетика. Толковый словарь.
hemopoiesis — hemopoiesis. = hematopoiesis (см.). (Источник: «Англо русский толковый словарь генетических терминов». Арефьев В.А., Лисовенко Л.А., Москва: Изд во ВНИРО, 1995 г.) … Молекулярная биология и генетика. Толковый словарь.
hemopoiesis — noun Etymology: New Latin Date: circa 1900 hematopoiesis • hemopoietic adjective … New Collegiate Dictionary
hemopoiesis — hemopoietic /hee meuh poy et ik, hem euh /, adj. /hee meuh poy ee sis, hem euh /, n. hematopoiesis. [HEMO + POIESIS] * * * … Universalium
hemopoiesis — noun Formation of new cellular components of the blood in myeloid or lymphatic tissue. Syn: hematopoiesis See Also: hemopoietic … Wiktionary
hemopoiesis — The process of formation and development of the various types of blood cells and other formed elements. SYN: hematogenesis, hematopoiesis, hematosis (1), hemogenesis, sanguification. [hemo + G. poiesis, a making] * * * he·mo·poi·e·sis or chiefly… … Medical dictionary
hemopoiesis — he·mo·poi·e·sis … English syllables
hemopoiesis — he•mo•poi•e•sis [[t]ˌhi mə pɔɪˈi sɪs[/t]] n. phl biochem. hematopoiesis he mo•poi•et′ic ˈɛt ɪk adj … From formal English to slang
hemopoiesis — noun the formation of blood cells in the living body (especially in the bone marrow) • Syn: ↑hematopoiesis, ↑haematopoiesis, ↑haemopoiesis, ↑hemogenesis, ↑haemogenesis, ↑hematogenesis, ↑haematogenesis, ↑sanguificat … Useful english dictionary
Hematopoiesis — The production of all types of blood cells generated by a remarkable self regulated system that is responsive to the demands put upon it. The levels of the different types of the white blood cells in the granulocyte series (the neutrophils,… … Medical dictionary
hemopoietic — adjective pertaining to the formation of blood or blood cells hemopoietic stem cells in bone marrow • Syn: ↑hematopoietic, ↑haematopoietic, ↑haemopoietic, ↑hematogenic, ↑haematogenic • Pertains to noun: ↑ … Useful english dictionary
Кроветворение. Кроветворение плода. Экстрамедуллярный гемопоэз.
Экстрамедуллярный гематопоэз (EMH или иногда EH ) относится к гематопоэзу, происходящему за пределами продолговатого мозга кости (костный мозг ). Он может быть физиологическим или патологическим.
Физиологическая ЭМГ возникает в основном во время эмбрионального и эмбрионального развития. Это было сделано во многих разных местах, в зависимости от момента или типа кроветворения, который необходим в этот момент.
Патологическая ЭМГ может возникнуть во взрослом возрасте, когда физиологический гемопоэз не может работать должным образом в костном мозге и гемопоэтические стволовые клетки (HSC) должны мигрировать в другие ткани, чтобы продолжить работу. образование клеточных компонентов крови. Патологическая ЭМГ может быть вызвана миелофиброзом, талассемией или нарушением кроветворной системы.
Содержание
- 1 Физиологическая EMH
- 1.1 Первичный гемопоэз
- 1.2 Окончательный гематопоэз
- 1.3 Легочный гематопоэз
- 2.1 Места EMH
- 2.1.1 Селезенка
- 2.1.2 Печень
- 2.1.3 Лимфатические узлы
- 2.1.4 Другие участки
Физиологическая EMH
Во время внутриутробного развития происходит гемопоэз в основном в печени плода с последующей локализацией в костном мозге. Гематопоэз также имеет место во многих других тканях или органах, таких как желточный мешок, область мезонефроса аорты и гонад (AGM), селезенка и лимфатические узлы. В процессе развития позвоночные животные проходят первичную и окончательную фазы кроветворения. Легкие также играют роль в производстве тромбоцитов у взрослых.
Примитивный гематопоэз
Примитивный гематопоэз происходит в желточном мешке во время раннего эмбрионального развития. Он характеризуется образованием предшественников эритроидов или ядерных эритроцитов, также известных как эритробласты или мегалобласты. Основной целью производства этих клеток будет облегчение оксигенации тканей для поддержки быстрого роста эмбриона. Эта примитивная фаза является преходящей, и продуцируемые клетки экспрессируют эмбриональные глобины, не являются плюрипотентными и не способны к самообновлению.
Окончательный гемопоэз
Окончательный гемопоэз отличается от примитивной фазы продуцированием гемопоэтических стволовых клеток. Формирование этих клеток происходит в AGM на более позднем этапе развития. Позже они мигрируют в печень плода, где происходит большая часть физиологических ЭМГ. Наконец, когда костный мозг развился, они мигрируют туда. Они также могут мигрировать в селезенку и лимфатические узлы, где может происходить гемопоэз, но в меньшей степени.
Легочный гемопоэз
Легочный гемопоэз также играет важную роль у взрослых. По сравнению с костным мозгом, в котором происходит трехлинейное кроветворение, легкие предпочтительно вносят вклад в продукцию тромбоцитов резидентной популяцией мегакариоцитов. Это подтверждается исследованиями, показывающими, что кровь, покидающая легкие, содержит больше тромбоцитов и меньше клеток-предшественников, чем кровь, поступающая в легкие. Было замечено, что в случаях тяжелой тромбоцитопении легочные мегакариоциты мигрируют из легких в костный мозг, где они помогают восполнить запасы истощенного костного мозга.
Патологическая ЭМГ
У взрослых большая часть гемопоэза происходит в костном мозге. Значительная продукция в любом другом органе обычно является результатом патологического процесса. Когда количество эритроцитов низкое, организм запускает гомеостатический механизм, направленный на увеличение синтеза эритроцитов, обычно за счет выработки эритропоэтина. Если потеря эритроцитов становится серьезной, гемопоэз будет происходить в экстрамедуллярных пространствах за пределами кости.
Причиной патологической ЭМГ может быть одно из многих гематологических заболеваний, таких как миелофиброз или как в результате облучения костного мозга. Талассемия и вытекающая из нее гемолитическая анемия - еще одна важная причина патологической ЭМГ. EMH наблюдается при многих других доброкачественных гематологических заболеваниях, таких как серповидноклеточная анемия, наследственный сфероцитоз, врожденная дизеритробластная анемия и идиопатическая тромбоцитопеническая пурпура. EMH также может рассматриваться как часть ответа на системное воспаление или инфекцию.
Сайты EMH
Сайты EMH могут быть широко распространены, однако наиболее распространенные локализации находятся в селезенка, печень и лимфатические узлы. Другие проявления возникают в тимусе, сердце, груди, предстательной железе, широких связках, почках, надпочечниках, плевре, забрюшинной ткани, коже, периферических и черепных нервах и спинномозговом канале.
Селезенка
В послеродовой период селезенка становится частым участком ЭМГ, тогда как на эмбриональных стадиях гемопоэза это лишь второстепенный фактор. Несмотря на гипоксические / кислые условия микросреды селезенки, снабженной легионом макрофагов, делающих ее негостеприимной для HSC, EMH обычно возникает в красной пульпе. Среди различных органов, связанных с EMH, селезенка представляет собой уникальное место для оценки взаимодействий гемопоэтических стволовых клеток (HSC) / ниши.
Печень
Это нормально для младенцев с печеночной EMH, поскольку они развиваются примерно до 5-недельного возраста. С другой стороны, печеночная ЭМГ у взрослых может указывать на патологическое состояние. Это включает трансплантацию, опухоли печени, заболевания печени или сепсис. Гепатобластома, аденомы и гепатоцеллюлярные карциномы также могут приводить к ЭМГ у взрослых. Кроме того, ЭМГ часто наблюдается в синусоидах печени.
Лимфатические узлы
ЭМГ в лимфатических узлах обычно ассоциируется с лежащими в основе кроветворными новообразованиями. Миелопролиферативные новообразования (MPN) обычно приводят к EMH. Если EMH обнаруживается в лимфатических узлах взрослого или младенца, необходимо выполнить гематологическое обследование, включая подсчет клеток крови, мазок периферической крови и, возможно, биопсию костного мозга.
Другие участки
Следующие ткани также могут быть связаны с ЭМГ: тимус, сердце, грудь, простата, жировая ткань, надпочечники, почка, надкостница, плевральная полость, околопозвоночные области, внутрипозвоночная ткань, забрюшинная ткань, кожа, периферические и черепные нервы, позвоночный канал, прекакральная область, носоглотка, придаточные пазухи носа и многочисленные типы доброкачественных / злокачественных новообразований. Наиболее частыми локализацией ЭМГ, связанной с неопластическим заболеванием, являются селезенка, лимфатические узлы, кожа, кости, тонкий кишечник, глазница, грудь, шейка матки, носовые пазухи, средостение и мозг.
Микроокружение ЭМГ
Среди различных органов, связанных с EMH, селезенка предлагает уникальный сайт для оценки взаимодействий HSC / ниши, поскольку это один из наиболее распространенных сайтов EMH, однако он не играет важной роли в эмбриональном / онтогенетическом гематопоэзе. Высокие уровни экспрессии CXCL12 были обнаружены в селезенках человека у EMH-положительных пациентов по сравнению с теми, которые были EMH-отрицательными. Высокая экспрессия CXCL12, кандидата в маркеры ниш костного мозга, составляющих клетки, указывает на взаимодействия HSC / ниши в селезенке. Исследования показали, что CXCL12 локализуется в эндотелиальных клетках синуса красной пульпы в EMH-положительной селезенке; тогда как CXCL12 экспрессировался во всех эндотелиальных клетках сосудов белой пульпы в селезенках в EMH-отрицательных и -положительных случаях. Тот факт, что ЭМГ часто встречается в красной пульпе, подтверждается текущими данными, которые предполагают, что эндотелиальные клетки синуса селезенки, экспрессирующие CXCL12, могут способствовать прикреплению и рекрутированию циркулирующих гемопоэтических клеток-предшественников, формируя подобные нише костного мозга области ЭМГ у человека. селезенка.
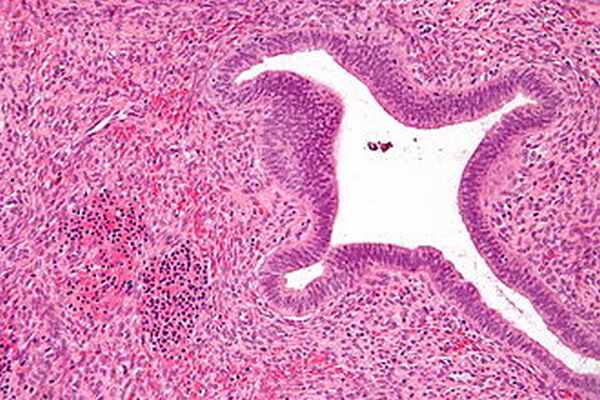
Экстрамедуллярный гемопоэз - Extramedullary hematopoiesis
![]()
Микрофотография показывая ядросодержащие эритроциты (внизу слева изображения), один из элементов, необходимых для вызова экстрамедуллярного кроветворения, в полип эндометрия. H&E пятно.
Экстрамедуллярный гемопоэз (EMH или иногда EH [1] ) относится к кроветворение происходящие за пределами мозгового вещества кости (Костный мозг ). [2] Он может быть физиологическим или патологическим.
Физиологическая ЭМГ возникает во время эмбриональный и плод развитие в основном. Это было сделано во многих разных местах, в зависимости от момента или типа кроветворения, который необходим в этот момент.
Патологическая ЭМГ может возникнуть в зрелом возрасте, когда физиологический гемопоэз не может работать должным образом в костном мозге и костном мозге. гемопоэтические стволовые клетки (HSC) должны мигрировать в другие ткани, чтобы продолжить образование клеточные компоненты крови. Патологическая ЭМГ может быть вызвана: миелофиброз, [3] талассемии или нарушения, вызванные кроветворной системой.
Содержание
Физиологическая ЭМГ
Во время внутриутробного развития гемопоэз происходит в основном в печень плода с последующей локализацией в костном мозге. [4] Гематопоэз также имеет место во многих других тканях или органах, таких как желточный мешок, то аорта-гонадный мезонефрос (AGM) регион, селезенка, и лимфатический узел. В процессе развития позвоночные животные проходят первичную и окончательную фазы кроветворения. Легкие также играют роль в производстве тромбоцитов у взрослых. [5]
Примитивный гемопоэз
Примитивный гемопоэз возникает в желточном мешке на раннем этапе эмбрионального развития. Он характеризуется производством эритроидные предшественники или ядросодержащие эритроциты, также известные как эритробласты или мегалобласты. Основной целью производства этих клеток будет облегчение оксигенации тканей для поддержки быстрого роста эмбриона. Эта примитивная фаза носит временный характер, и производимые клетки экспрессируют эмбриональную глобины не плюрипотентный, и не способны к самообновлению.
Окончательный гемопоэз
Окончательный гемопоэз отличается от примитивной фазы производством гемопоэтические стволовые клетки. Формирование этих клеток происходит в AGM на более позднем этапе развития. Позже они мигрируют в печень плода, где происходит большая часть физиологических ЭМГ. Наконец, как только костный мозг развился, они мигрируют туда. Они также могут мигрировать в селезенку и лимфатические узлы, где может происходить гемопоэз, но в меньшей степени.
Легочный гемопоэз
Легочный гемопоэз также играет важную роль у взрослых. [5] По сравнению с костным мозгом, в котором происходит трехлинейное кроветворение, легкие преимущественно способствуют выработке тромбоцитов через постоянное население мегакариоциты. Это подтверждается исследованиями, показывающими, что кровь, покидающая легкие, содержит больше тромбоцитов и меньше клеток-предшественников, чем кровь, поступающая в легкие. Было замечено, что в случаях тяжелых тромбоцитопения, легочные мегакариоциты мигрируют из легких в костный мозг, где они помогают восполнить истощенную популяцию костного мозга.
Патологическая ЭМГ
У взрослых большая часть кроветворения происходит в костном мозге. Значительное производство в любом другом органе обычно является результатом патологического процесса. Когда красные кровяные тельца (эритроциты) Если количество низкое, организм вызывает гомеостатический механизм, направленный на увеличение синтеза эритроцитов, обычно за счет выработки эритропоэтина. Если потеря эритроцитов становится серьезной, кроветворение будет происходить в экстрамедуллярных пространствах за пределами кости. [6]
Причиной патологической ЭМГ может быть одно из многих гематологических заболеваний, например: миелофиброз, или в результате облучения костного мозга. Талассемия и его результат гемолитическая анемия еще одна важная причина патологической ЭМГ. EMH наблюдается при многих других доброкачественных гематологических заболеваниях, таких как серповидноклеточная анемия, наследственный сфероцитоз, врожденная дизеритробластная анемия и идиопатическая тромбоцитопеническая пурпура. [6] EMH также можно рассматривать как часть ответа на системное воспаление или инфекционное заболевание.
Сайты EMH
Сайты EMH могут быть широко распространенными, однако наиболее частые локализации находятся в селезенке, печени и лимфатических узлах. Другие проявления возникают в тимусе, сердце, груди, простате, широких связках, почках, надпочечниках, плевре, забрюшинной ткани, коже, периферических и черепных нервах и спинномозговом канале. [6] [7]
Селезенка
В послеродовой период селезенка часто становится участком ЭМГ, тогда как на эмбриональных стадиях гемопоэза это лишь второстепенный фактор. Несмотря на гипоксические / кислые условия микросреды селезенки, снабженной легионом макрофагов, делающих ее негостеприимной для HSC, EMH обычно возникает в красной пульпе. Среди различных органов, связанных с EMH, селезенка представляет собой уникальное место для оценки взаимодействий гемопоэтических стволовых клеток (HSC) / ниши. [8] [7]
Печень
Это нормально для младенцев с печеночной ЭМГ, поскольку они развиваются примерно до 5-недельного возраста. [9] С другой стороны, печеночная ЭМГ у взрослых может указывать на патологическое состояние. Это включает трансплантацию, опухоли печени, заболевания печени или сепсис. Гепатобластома, аденомы и гепатоцеллюлярные карциномы также могут приводить к ЭМГ у взрослых. [10] [11] Кроме того, ЭМГ часто наблюдается в синусоидах печени.
Лимфатический узел
EMH в лимфатических узлах обычно связана с лежащими в основе кроветворными новообразованиями. Миелопролиферативные новообразования (MPN), как правило, приводят к EMH. [12] Если EMH обнаруживается в лимфатических узлах взрослого или младенца, необходимо выполнить гематологическое обследование, включая подсчет клеток крови, мазок периферической крови и, возможно, биопсию костного мозга. [7]
Другие сайты
Следующие ткани также могут быть связаны с ЭМГ: вилочковая железа, сердце, грудь, предстательная железа, жировая ткань, надпочечники, почка, надкостница, плевральная полость, паравертебральные области, внутриспинная ткань, забрюшинная ткань, кожа, периферические и черепные нервы, позвоночный канал, прекакральная область, носоглоточная область, околоносовые пазухи и многочисленные типы доброкачественных / злокачественных новообразований. Наиболее частыми участками EMH, связанными с неопластическим заболеванием, являются селезенка, лимфатические узлы, кожа, кости, тонкий кишечник, глазница, грудь, шейка матки, носовые пазухи, средостение и мозг. [7] [13] [14] [15]
Микросреда ЭМГ
Из различных органов, связанных с EMH, селезенка представляет собой уникальный сайт для оценки взаимодействий HSC / ниши, поскольку это один из наиболее распространенных сайтов EMH, однако он не играет важной роли в эмбриональном / онтогенетическом гематопоэзе. [7] Высокий уровень экспрессии CXCL12 были обнаружены в селезенке человека у EMH-положительных пациентов по сравнению с EMH-отрицательными. Высокая экспрессия CXCL12, кандидата в маркеры ниш костного мозга, составляющих клетки, указывает на взаимодействия HSC / ниши в селезенке. [16] Исследования показали, что CXCL12 локализуется в эндотелиальных клетках синуса красной пульпы в EMH-положительной селезенке; тогда как CXCL12 экспрессировался во всех эндотелиальных клетках сосудов белой пульпы в селезенках в EMH-отрицательных и -положительных случаях. [16] Тот факт, что ЭМГ часто встречается в красной пульпе, подтверждается текущими данными, которые предполагают, что эндотелиальные клетки синуса селезенки, экспрессирующие CXCL12, могут способствовать прикреплению и рекрутированию циркулирующих гемопоэтических клеток-предшественников, формируя нишеподобные области ЭМГ костного мозга у человека. селезенка. [16]
ЭКСТРАМЕДУЛЛЯРНЫЙ ГЕМОПОЭЗ
Русско-английский перевод ЭКСТРАМЕДУЛЛЯРНЫЙ ГЕМОПОЭЗ
Чибисова О.И., Смирнов Н.Н.. Новый Русско-Английский биологический словарь. New Russian-English biological dictionary . 2003
Еще значения слова и перевод ЭКСТРАМЕДУЛЛЯРНЫЙ ГЕМОПОЭЗ с английского на русский язык в англо-русских словарях и с русского на английский язык в русско-английских словарях.
More meanings of this word and English-Russian, Russian-English translations for the word «ЭКСТРАМЕДУЛЛЯРНЫЙ ГЕМОПОЭЗ» in dictionaries.
- — Haematopoiesis
Русско-Американский Английский словарь — 1) blood formation 2) hemapoiesis 3) hematogenesis 4) hematopoiesis 5) hematosis 6) hemogenesis 7) hemopoiesis 8) sanguification
Новый Русско-Английский биологический словарь — hematopoiesis, hemopoiesis
Русско-Английский биологический словарь — физиол. haemopoiesis
Большой Русско-Английский словарь — экстрамедуллярный гемопоэз, внекостномозговое кроветворение
Новый Англо-Русский словарь по биологии — физиол. кроветворение, гемопоэз (физиологическое) кроветворение, гемопоэз
Большой Англо-Русский словарь — (физиологическое) кроветворение, гемопоэз
Большой Англо-Русский словарь — Гемопоэз
Американский Англо-Русский словарь — n физиол. кроветворение, гемопоэз
Англо-Русско-Английский словарь общей лексики - Сборник из лучших словарей — физиол. кроветворение, гемопоэз
Англо-Русский научно-технический словарь — (n) гемопоэз; кроветворение
English-Russian Lingvistica'98 dictionary — (n) гемопоэз; кроветворение
English-Russian Lingvistica'98 dictionary — n физиол. кроветворение, гемопоэз
Новый большой Англо-Русский словарь - Апресян, Медникова — n физиол. кроветворение, гемопоэз
Большой новый Англо-Русский словарь — кроветворение, гемопоэз
Новый Англо-Русский словарь по биологии — гемопоэз, кроветворение - extramedullary hemopoiesis - fetal hemopoiesis
Новый Англо-Русский словарь по биологии — гемопоэз, кроветворение
Новый Англо-Русский словарь по биологии — гемопоэз, кроветворение см. тж. hemopoiesis
Новый Англо-Русский словарь по биологии — гемопоэз, кроветворение см. тж. hemopoiesis
Новый Англо-Русский словарь по биологии — гемопоэз, кроветворение см. тж. hemopoiesis
Новый Англо-Русский словарь по биологии — гемопоэз, кроветворение см. тж. hemopoiesis
Новый Англо-Русский словарь по биологии — фетальный гемопоэз, внутриутробное кроветворение плода
Новый Англо-Русский словарь по биологии — кровеобразование, кроветворение, гемопоэз
Новый Англо-Русский словарь по биологии — кроветворение, гемопоэз
Новый Англо-Русский биологический словарь — гемопоэз, кроветворение - extramedullary hemopoiesis - fetal hemopoiesis
Новый Англо-Русский биологический словарь — гемопоэз, кроветворение
Новый Англо-Русский биологический словарь — гемопоэз, кроветворение см. тж. hemopoiesis
Новый Англо-Русский биологический словарь — гемопоэз, кроветворение см. тж. hemopoiesis
Новый Англо-Русский биологический словарь — гемопоэз, кроветворение см. тж. hemopoiesis
Новый Англо-Русский биологический словарь — гемопоэз, кроветворение см. тж. hemopoiesis
Новый Англо-Русский биологический словарь — фетальный гемопоэз, внутриутробное кроветворение плода
Новый Англо-Русский биологический словарь — экстрамедуллярный гемопоэз, внекостномозговое кроветворение
Новый Англо-Русский биологический словарь — экстрамамиллярный рак Педжета, экстрамедуллярный дерматоз Педжета
Новый Англо-Русский медицинский словарь — физиол. кроветворение, гемопоэз (физиологическое) кроветворение, гемопоэз
Новый большой Англо-Русский словарьНовый Русско-Английский биологический словарь
Особенности органов кроветворения у детей. Становление гемопоэза в антенатальном и постнатальном периодах. Особенности гемограммы и коагулограммы новорожденного ребенка. Особенности кроветворения у детей. Показатели крови в различные возрастные периоды. А
После рождения у человека в кроветворении участвуют следующие органы:
Красный костный мозг (КМ) – центральный орган гемопоэза, который сообщается с кровотоком посредством капиллярной сети. У взрослого человека КМ составляет примерно 4,5% от общей массы тела, он находится в трубчатых костях, ребрах, грудине, позвонках, костях черепа, таза. В КМ образуются все виды клеток крови – лейкоциты (в том числе иммунные В-лимфоциты), эритроциты и тромбоциты.
Тимус – орган образования и дифференцировки Т-лимфоцитов.
Селезенка и лимфатическая ткань (лимфатические узлы и лимфоидные образования в коже, слизистых оболочках глотки, бронхов и кишечника) – являются местом образования только лимфоцитов.
Экстрамедуллярное кроветворение – явление образования лейкоцитов и эритроцитов вне костного мозга: в селезенке, лимфоузлах, печени, почках, надпочечниках, легких, в клетчатке различных органов (в норме в эмбриональном периоде и при патологии).
Органы кроворазрушения
РЭС (система мононуклеарных фагоцитов) - макрофаги КМ, селезенки , лимфатических желез, легких, купферовские клетки печени, гистиоциты соединительной ткани.
Особенности крови лабораторных животных
В целом клеточный состав крови человека и лабораторных животных (собак, кроликов, морских свинок, крыс, мышей) является сходным. Однако имеются и некоторые различия. Так, например, если у человека ОКЛ составляет 4-8*10 9 /л (Г/л), то у животных оно колеблется в более широком диапазоне – от 5 до 18 Г/л. Кроме того, у крыс и мышей формирование ядра полиморфноядерных лейкоцитов происходит по кольцевидному типу. В результате ядра созревающих гранулоцитов у этих животных имеют вид не «палочек» (как у человека), а «колец». У кроликов и морских свинок зернистость гранулоцитов имеет более высокое сродство к кислым красителям по сравнению с человеческими лейкоцитами. Такие клетки называют «псевдоэозинофилами», поскольку данным свойством у человека обладают исключительно эозинофильные лейкоциты. У морских свинок в цитоплазме лимфоцитов и моноцитов могут обнаруживаться белково-полисахаридные зерна – тельца Курлова (признак старения клеток), у человека их нет.
К ПРАКТИЧЕСКОМУ ЗАНЯТИЮ
IV курс специальность «Педиатрия»
Дисциплина: «Пропедевтика детских болезней с курсами здорового ребенка и общим уходом за детьми»
АНАТОМО-ФИЗИОЛОГИЧЕСКИЕ ОСОБЕННОСТИ
ОРГАНОВ КРОВЕТВОРЕНИЯ У ДЕТЕЙ И ПОДРОСТКОВ.
Продолжительность занятия__ _часа
Вид занятия – практическое занятие.
ЦЕЛЬ ЗАНЯТИЯ: Изучить анатомо-физиологические особенности системы кроветворения у детей.
ОСНОВНЫЕ ВОПРОСЫ ТЕМЫ:
1. Этапы эмбрионального гемопоэза и их роль в понимании возникновения очагов экстрамедуллярного кроветворения при патологии кроветворных органов у детей и подростков.
2. Полипотентная стволовая клетка и этапы ее дифференцировки.
3. Закономерности изменения лейкоцитарной формулы с возрастом детей.
4. Эритроцитарный росток и его изменения в постнатальном периоде.
5. Гранулоцираная система кроветворения.
6. Лимфоидная система кроветворения.
7. Система гемостаза у детей и подростков
Вопросы для самостоятельного изучения студентами.
1. Современная схема кроветворения.
- Осмотр больного, оценка данных исследования периферической крови у больного с нормой.
ОСНАЩЕНИЕ ЗАНЯТИЯ: таблицы, схемы, истории болезни.
МЕТОДИЧЕСКИЕ УКАЗАНИЯ.
Кровь – одна из наиболее лабильных жидкостных систем организма, постоянно вступающая в контакт с органами и тканями, обеспечивающая их кислородом и питательными веществами, отводящая к органам выделения отработанные продукты обмена, участвующая в регуляторных процессах поддержания гомеостаза.
В систему крови включаются органы кроветворения и кроверазрушения (красный костный мозг, печень, селезенка, лимфатические узлы, другие лимфоидные образования) и периферическая кровь, нейрогуморальные и физико-химические регуляторные факторы.
Составными частями крови являются форменные элементы (эритроциты, лейкоциты, тромбоциты) и жидкая часть – плазма.
Общее количество крови в организме взрослого человека составляет 7% массы тела и равно 5 л, или 70 мл на 1 кг массы тела. Количество крови у новорожденного составляет 14% массы тела или 93-147 мл на 1 кг массы тела, у детей первых трех лет жизни – 8%, 4-7 лет – 7-8%, 12-14 лет 7-9% массы тела.
Эмбриональное кроветворение.
Кроветворение во внутриутробном периоде развития начинается рано. По мере роста эмбриона и плода последовательно меняется локализация гемопоэза в различных органах.
Табл. 1. Развитие гемопоэтической системы человека (по Н.С. Кисляк, Р.В. Ленской, 1978).
Начинается кроветворение в желточном мешке на 3-й неделе развития человеческого эмбриона. В начале оно сводится в основном к эритропоэзу. Образование первичных эритробластов (мегалобласты) происходит внутри сосудов желточного мешка.
В селезенке кроветворение начинается с 12-й недели, образуются эритроциты, гранулоциты, мегакариоциты. С 20-й недели миелопоэз в селезенке сменяется интенсивным лимфопоэзом.
Первые лимфоидные элементы появляются на 9-10 неделе в строме тимуса, в процессе их дифференцировки образуются иммунокомпетентные клетки – Т-лимфоциты. К 20-й неделе тимус по соотношению малых и средних лимфоцитов сходен с тимусом доношенного ребенка, к этому времени в сыворотке крови плода начинают обнаруживаться иммуноглобулины М и G.
Костный мозг закладывается в конце 3-го месяца эмбрионального развития за счет мезенхимальных периваскулярных элементов, проникающих вместе с кровеносными сосудами из периоста в костномозговую полость. Гемопоэтические очаги в костном мозге появляются с 13-14 недели внутриутробного развития в диафизах бедренных и плечевых костей. К 15-й неделе в этих локусах отмечается обилие юных форм грануло-, эритро- и мегакариоцитов. Костномозговое кроветворение становится основным к концу внутриутробного развития и на протяжении всего постнатального периода. Костный мозг в пренатальном периоде красный. Его объем с возрастом плода увеличивается в 2,5 раза и к рождению составляет порядка 40 мл. и он присутствует во всех костях. К концу гестации начинают появляться в костном мозге конечностей жировые клетки. После рождения в процессе роста ребенка масса костного мозга увеличивается и к 20 годам составляет в среднем 3000 г, но на долю красного костного мозга будет приходиться порядка 1200 г, и он будет локализоваться в основном в плоских костях и телах позвонков, остальная часть будет замещена желтым костным мозгом.
Основным отличие состава форменных элементов крови плода является постоянное нарастание числа эритроцитов, содержания гемоглобина, количества лейкоцитов. Если в первой половине внутриутробного развития (до 6 месяцев) в крови обнаруживаются много незрелых элементов (эритробластов, миелобластов, промиелоцитов и миелоцитов), то в последующие месяцы в периферической крови плода содержатся преимущественно зрелые элементы.
Изменяется и состав гемоглобина. Вначале (9-12 нед) в мегалобластах находится примитивный гемоглобин (HbP), который заменятся фетальным (HbF). Он становится основной формой в пренатальном периоде. Хотя с 10-й недели начинают появляться эритроциты с гемоглобином взрослого типа (HbA), доля его до 30 недели составляет лишь 10%. К рождению ребенка фетальный гемоглобин составляет приблизительно 60%, а взрослый – 40% всего гемоглобина эритроцитов периферической крови. Важным физиологическим свойством примитивного и фетального гемоглобинов является их более высокое сродство к кислороду, что имеет важное значение во внутриутробном периоде для обеспечения организма плода кислородом, когда оксигенация крови плода в плаценте относительно ограничена по сравнению с оксигенацией крови после рождения в связи с установлением легочного дыхания.
ТЕМА: Особенности кроветворения у детей. Показатели крови в различные возрастные периоды. Анемии у детей. Понятие об иммунитете. Геморрагический синдром. Вазопатии, тромбоцитопатии, тромбоцитопении, коагулопатии. Врачебная тактика.
Кроветворение в период внутриутробного развития
Эмбриональное кроветворение начинается очень рано: к концу 2 – началу 3 недели гестации, проходит с различной интенсивностью, со сменой преимущественной локализации кроветворения в различные гестационные сроки. Его характерными особенностями можно считать следующее:
– последовательное изменение тканей и органов, являющихся основными плацдармами формирования элиментов крови,-желточный мешок, печень, селезенка, тимус, л/у и, наконец, костный мозг;
– изменение типа кроветворения и продуцируемых клеток – от мегалобластического к нормобластическому.
В период в/утробного развития топографически можно выделить 4 этапа гемопоэза:
1) мезобластический (внеэмбриональный)
2) печеночный (экстрамедулярный)
3) селезеночный (экстрамедулярный)
Мезобластический этап Тип кроветворения – мегалобластический. Кроветворения возникает в желточном мешке, стебле хориона к концу 2-й началу – 3-й недели гестации. Из периферических клеток желточного мешка образуются сосуды, а из центральных – гемопоэтические клетки, которые имеют овальную форму, крупные размеры (до 30 мкм), базофильную цитоплазму, ядро с ядрышками. Их называют примитивными эритробластами (внешне похожи на мегалобласты). В этих клетках постепенно накапливается Hb. С 6-й недели гестации в крови эмбриона встречаются клетки без ядер – мегалоциты. В этот период происходит преимущественно эритропоэз, но уже можно обнаружить клетки-предшественницы всех гемопоэтических ростков, включая полипептонные стволовые клетки (отличаются повышенной способностью к самовоспроизведению). Т. о. в желточном мешке имеются клетки, способные дифференцироваться в различных гемопоэтических направлениях и именно из него клетки-предшественницы гемопоэза мигрируют в др. органы.
Печеночный этап (6-27 нед) гемопоэза возникает с 5-й недели гестации, и в период 3 – 6 мес. (пик в 12-20 нед.) гестации печень является главным гемопоэтическим органом и местм образования эритропоэтина (ЭП). Тип кроветворения – макро-нормобластический .
ЭП – гуморальный регулятор кроветворения (эритропоэа). Основным, но не единственным местом выработки являются почки. Основными продуцентами внепочечного ЭП являются макрофаги-моноциты. Вероятно, в неактивном состоянии он поступает в плазму, где под влиянием специфического фермента – эритрогенина – превращается в активный ЭП. Основным регулятором выработки ЭП является содержание О2 в крови, вернее его доступность для тканей. Метаболизм ЭП медленный. Около 10 % ЭП выделяется из организма с мочой.
Первоначально в печени происходит интенсивный эритропэз – к 9-10-й нед гестации до 93,4% ядерных клеток составляют примитивные эритробласты (первичные), которые постепенно замещаются вторичными эритробластами, и к 32-й нед эритроидные клетки составляют 40%.
Селезеночный этап начинается с 12-й нед гестации. Первоначально определяются грануло-, эритро - и мегакариоцитопоэз (частично). С 15-й нед появляются В-Л.
В возрасте 19-25 нед гестации 85% клеток селезенки лимфоидной природы. Появляются Л с внутриклточным содержанием Ig M и Ig G. Интенсивный лимфопоэз продолжается в селезенке в течение всей жизни человека.
Гемопоэз в селезенке достигает своего максимума к 4-му месяцу гестации, затем идет на убыль и прекращается в возрасте 6,5 мес. в/утробного развития.
Снижение экстрамедулярного гемопоэза совпадает с появлением первых признаков костномозгового кроветворения.
У взрослого человека селезенка:
– плацдарм иммуногенеза , отвечающего за гуморальное, В-клеточное звено иммунитета, здесь в т. ч. вырабатываются IgG и M, антитела , аутоантитела.
– принимает участие в регуляции созревания и выхода из костного мозга клеток эритро - и гранулопоэза, тромбоцитов и лимфацитов.
– является органом кроверазрушения (в ретикулоэндотелии пульпы и синусов происходит разрушение стареющих эритроцитов (Er) и тромбоцитоа (Tr))
– учавствует в межуточном обмене железа (Fe), орган депонирования Fe.
– важное депо крови (вмещает 20% циркулирующей крови).
– гуморальным путем влияет на процесс обезъядривания Er; после спленэктомии появляются Er с тельцами Жолли.
Костномозговое кроветворение начинается с 3-го мес гестации и достигает максимума к 30 нед. с 20 нед. он является основным органом кроветворения и остается им до конца жизни человека. Тип кроветворения – макро-нормобластический .
В последние 10 нед в/утробного развития объем мозга существенно не изменяется.. Первоначально костный мозг возникает в телах позвонков длиной 95 мм. В 11-14 нед гестации в подвздошной кости определяются незрелые гемопоэтические клетки и эритроциты; через 23-27 нед выявляются элименты всех 3-х ростков кроветворения на всех стадиях развития.
В возрасте 13-14 нед в/утробного развития появляются первые очаги кроветворения в диафизах плечевой и бедренной кости. По мере роста скелета роль костномозгового кроветворения возрастает, через 30 нед костный мозг представлен всеми гемопоэтическими клетками, он становится главным источником образования клеток крови.
В пренатальный период весь костный мозг является крастным, т. е. гемопоэтическим. С 32-недельного возраста все промежутки костной ткани (т. е. все полости плоскихи трубчатых костей) заполнены гемопоэтической тканью, т. е объем костного мозга равен объему гемопоэтических клеток. К моменту рождения ребенка кроветворение практически полностью представленно костным мозгом. У новорожденного ребенка костный мозг составляет в среднем 1,4% от массы ребенка (у взрослого – 4,6%)
Начиная с первого года жизни в диафизах длинных трубчатых костей появляются жировые клетки (липолизация костного мозга), которые постепенно увеличиваются и в 12-14 лет красный костный. мозг исчезает из диафизов, а к 20-25 годам – из эпифизов трубчатых костей, и в 16-18 лет крастный костный мозг сохраняется только в телах позвонков, ребрах, грудине, костях таза, черепа. Наиболее активные участки кроветворения определяются в костях с большим содержанием губчатого вещества.
Жировое перерождение костного мозга продолжается в течение всей жизни, но не должно превышать 50-75%. Если оно составляет больше 75%, речь идет о патологическом гипопластическом состоянии кроветворения. % жирового перерождения костного мозга уточняется путем проведения трепанобиопсии. Клетки крови в костном мозге образуются вне сосудов (экстраваскулярно), достигнув зрелости поступают в общий поток крови через стенку эндотелиальных синусов.
В костном мозге происходят процессы лейкопоэза, эритропоэза и тромбоцитопоэза. В костном мозге существуют эритроидный, гранулоцитарно-моноцитарный и мегакариоцитарный ростки кроветворения, производящие соответствующие клетки.
Пунктируют грудину, подвздошную кость ближе к позвоночнику, у новорожденных – пяточную кость. Делают 5 мазков
Всего клеток нейтрофильного ряда – 36-66%
Всего клеток эозинофильного ряда – 0,5-12,6%
Всего клеток базофильного ряда – 0-1,8%
Всего клеток эритроидного ряда – 10-26%
Ядерные миелокариоциты – 60-400´109/л
С возрастом изменяется соотношение: Л больше, чем клеток эритроидного ряда;
Лецкозритробластическое соотношение – 3-4:1
Индекс созревания L – 0,6-0,9
Развитие лимфоидной ткани вилочковой железы происходит на 6-7-й нед гестации. Первые л/у появляются на 10-й нед, а лимфоидный аппарат кишечника – на 14-16-й нед. Первоначально в л/у определяется миелопоэз, который вскоре сменяется лимфоцитопоэзом. К моменту рождения у ребенка определяется 220 л/у. Однако окончательное формирование синусов и стромы л/у происходит в постнатальном периоде.
В примитивных эритрокариоцитах на ранних этапах онтогенеза обнаруживается Hb. У эмбриона до 5-6 нед гестации преобладает HbP (примитивный), который доминирует до 12 нед. Затем он быстро сменяется на HbF (фетальный) и после 12 нед гестации является основным. HbA (взрослого) начинает синтезироваться с 3-й нед гестации, возрастает медленно, и к моменту рождения не превышает 10-15%.
Показатели крови в различные возрастные периоды
Основным отличием состава форменных элементов крови плода является постоянное нарастание числа Er, содержания Hb, количества L. Если до 6 мес в/у развития в крови обнаруживается много незрелых элементов (эритробластов, миелобластов, про - и миелоцитов), то в последующие месяцы в периферической крови плода содержатся преимущественно зрелые элементы.
Красная кровь. Сразу после рождения у ребенка в крови отмечается повышенное содержание Hb и числа Er.
К рождению HbF составляет 60-80% (обладает большим сродством к О2)
В 1-е сутки Hb–180-240г/л и Er–6-8*1012/л
Со 2-го дня показатели Hb и Er снижаются, и в возрасте 9-15 дней в среднем составляют 188 г/л (134-198 г/л) и 5,41´1012/л соответственно. Максимальное снижение Hb отмечается к 10 дню, Er – к 5-7.
В 1 мес жизни Hb 107-171 г/л, Er 3,3-5,3´1012/л
Содержание Rt повышено в течение 1-х суток после рождения (5-6%), затем постепенно снижается и к 5-7 дню достигает минимальных значений. После года количество Rt =1%. Все это свидетельствует об интенсивном эритропоэзе. Транзиторный ретикулоцитоз бывает так же в 5-6 мес, что объясняется низким содержанием меди и железа в рационе питания до введения прикормов.
После рождения гипоксия сменяется гипероксией, что приводит к снижению выработки эритропоэтина, подавляется эритропоэз+укороченная жизнь Er (12 дней,)+склонность Er, содержащих HbF, к гемолизу. В результате этого после периода новорожденности число Er и Hb продолжает снижаться, причем в большей степени уменьшается количество Hb. Минимальных значений эти показатели достигают к 2-4 мес (Hb до 116-90 г/л, Er до3,0*1012/л) – “физиологическая анемия” , отмечается тенденция к гипохромии, уменьшение гемоглобинизации Er.
Физиологическое анемическое состояние обусловлено:
Переходом от HbF к HbА, с последующим гемолизом Er
Незрелостью эритроцитарного ростка костного мозга
Недостатком эритропоэтинов и слабой чувствительностью к ним клеток-предшественников
Истощением запасов Fe, интенсивным распадом Er, содержащих HbF.
Продолжительность жизни Er здорового взрослого человека составляет 120 дней.
Минимальная осмотическая резистентность Er снижена.
Затем в связи с повышением выработки эритропоэтина сначало числи Rt, а затем Er и Hb начинает воостанавливаться. К середине 1-го года жизни число Er превышает 4´10 12/л, а Hb – 110-120 г/л. В последующем в течение 1-го года жизни эти показатели не изменяются и мало отличаются от их уровня у взрослых.
Анемия в первые недели жизни диагностируется при уровне Hb 35,0´10 9/л
Лейкопения –L 15,0-17,0 ´10 9/л, лейкопения – при уровне L 12,0´10 9/л, лейкопения – при уровне L
Читайте также: