Лабораторная диагностика аутоиммунной тромбоцитопении - анализы
Добавил пользователь Валентин П. Обновлено: 28.01.2026
Лабораторная диагностика аутоиммунной тромбоцитопении - анализы
Клинический анализ крови при аутоиммунной тромбоцитопении. Основным признаком аутоиммунной тромбоцитопений при исследовании периферической крови является снижение количества тромбоцитов при нормальном уровне лейкоцитов и эритроцитов (после значительных кровотечений может наблюдаться постгеморрагическая анемия); СОЭ в пределах нормы.
Характерен полиморфизм тромбоцитов, среди которых преобладают гигантские и молодые формы. Лейкоцитарная формула не изменена, однако при значительной кровопотере возможен сдвиг в лейкоцитарной формуле влево.
Миелограмма при аутоиммунной тромбоцитопении является одним из наиболее важных лабораторных исследований при аутоиммунной тромбоцитопений. В аспирате костного мозга при нормальной клеточности, как правило, выявляется увеличенное количество клеток мегакариоцитарного ряда. При длительном течении заболевания и отсутствии адекватного лечения может наблюдаться и уменьшение числа мегакариоцитов.
В этих случаях нельзя исключить воздействие на мегакариоциты аутоантител. Кроме определения количества мегакариоцитов в камере Фукса-Розенталя и в миелограмме, необходимо произвести подсчет парциальной мегакариоцитограммы с указанием качественной характеристики мегакариоцитов и их функционального состояния. При аутоиммунной тромбоцитопений отмечается сдвиг мегакариоцитограммы влево (преобладают базофильные формы) и отсутствие видимой отшнуровки тромбоцитов. Последнее ранее связывали с нарушением функции мегакариоцитов («недеятельные» мегакариоциты).
В настоящее время установлено, что это обусловлено резко повышенным разрушением тромбоцитов, а не их недостаточным образованием.

При нормальном или уменьшенном количестве мегакариоцитов в миелограмме необходимо проведение гистологического исследования костного мозга. Трепанобиопсия дает более полное представление о количестве мегакариоцитов и позволяет исключить апластическую анемию (при аутоиммунной тромбоцитопении в трепанобиоптате обнаруживается усиление мегакариоцитопоэза и нормальное соотношение между жировой тканью и кроветворным костным мозгом).
Некоторое диагностическое значение могут иметь лабораторные исследования, характеризующие функцию тромбоцитов. У больных аутоиммунной тромбоцитопенией часто увеличена длительность кровотечения, уменьшена ретракция кровяного сгустка. У ряда пациентов снижена адгезия и нарушена агрегация тромбоцитов (при низком количестве тромбоцитов эти исследования неинформативны). Время свертывания, содержание плазменных факторов и другие показатели коагулограммы (фибринолитическая активность, продукты деградации фибриногена) при аутоиммунной тромбоцитопении, в отличие от коагулопатий, не изменены.
Биохимические исследования крови и анализ мочи при аутоиммунной тромбоцитопении — без патологии (при глубокой тромбоцитопении возможна микрогематурия). Для подтверждения аутоиммунного характера тромбоцитопении необходимо обнаружение антитромбоцитарных антител, однако следует помнить, что их определение связано с большими методическими трудностями. До настоящего времени в повседневной практике используется тест Штеффена (тест потребления антиглобулина), не обладающий высокой чувствительностью.
Кроме того, в этой реакции часто используется сыворотка крови больного, а не его тромбоциты, и выявляемые антитела могут иметь изоиммунный характер. Более информативен метод Диксона, который основан на количественном определении IgG на поверхности тромбоцитов (при аутоиммунной тромбоцитопении выявляется повышенный уровень поверхностного IgG). Могут использоваться также меченые очищенные антитела и иммунофлюоресцентная техника.
Косвенно подтверждает аутоиммунный характер тромбоцитопении эффективность глюкокортикостероидов. В ряде случаев наблюдается сочетание аутоиммунной тромбоцитопении с аутоиммунной гемолитической анемией (так называемый синдром Фишера-Эванса). В настоящее время считают, что это не единый синдром, а сочетание двух вариантов аутоиммунных цитопений.
Редактор: Искандер Милевски. Дата обновления публикации: 18.3.2021
Лабораторная диагностика идиопатической тромбоцитопенической пурпуры - анализы
Согласно отборной схеме с целью диагноза геморрагического синдрома, лабораторные исследования при идиопатической тромбоцитопенической пурпуре должны начинаться, на первом этапе, с наиболее простых тестов: время кровотечения и время коагуляции, гемограмма с подсчетом тромбоцитов, реакция сгустка. На следующем этапе показаны тесты для этиопатогенетического диагноза клинической формы идиопатической тромбоцитопенической пурпуры.
В разгаре острого приступа идиопатической тромбоцитопенической пурпуры время кровотечения, как и при любой другой форме тромбопенической пурпуры, значительно увеличивается, порой достигая одного часа. При менее суровых случаях, с умеренными сокращениями тромбоцитов, если метод Дюка (Duke) не показывает значительного увеличения, следует применять метод Иви (Ivy). В качестве клинической пробы, тест жгута оказывается интенсивно положительным в период наибольшей тромбоцитопении, иногда оставаясь положительным долгое время, даже если тромбоциты возросли выше критического числа 50—60 000, а пурпура исчезла.
Глобальное время коагуляции и время Howell остаются в норме при любой форме тромбопенической пурпуры, идиопатической или вторичной; ретракция сгустка однако — дефицитная, а в случае значительных сокращений тромбоцитов, ниже 25 000, при нулевой ретракции даже спустя 24—48 часов, начинается фибринолиз без ретракции сгустка.
Тромбэластограмма показывает уже известные характерные изменения, с приближением обоих ветвей кривой, обычно в связи с сокращением числа тромбоцитов и дефицитом ретракции сгустка.
Эти легко выполняемые тесты в медицинских лабораториях любого уровня, сопоставляемые с клиническим характером кожных геморрагии, достаточны для постановки диагноза идиопатической тромбоцитопенической пурпуры.
Число тромбоцитов, детерминируемое в рамках гемограммы путем прямого подсчета или в относительном значении по сравнению с числом эритроцитов показывает сокращения, которые в течение острого периода понижаются ниже 50 000, достигая 20 000 или даже 10 000; в некоторых случаях сокращение настолько большое, что невозможно определить их число, так как существует периферический атромбоцитоз. Состояния атромбоцитоза сопровождаются выраженными кожными и висцеральными расстройствами благоприятствующие менингоцеребральным геморрагиям.
В настоящем опыте существуют однако случаи идиопатической тромбоцитопенической пурпуры с сильно выраженной тромбоцитопенией вплоть до атромбоцитоза, но с незначительными геморрагическими явлениями.
Пониженное число тромбоцитов сопровождается наличием крупных тромбоцитов диаметром в 2—3 микрона, по сравнению с диаметром нормальных тромбоцитов в 1,5 микрона. Вообще средний диаметр не бывает ниже 2 микронов, хотя на мазке встречаются и мелкие, круглые формы. С морфологической точки зрения, тромбоциты менее гранулированные или обладают некоторными эозинофильными грануляциями, отличающимися от грануломера нормальных тромбоцитов. Реже встречаются, наряду с крупными тромбоцитами, мелкие фрагменты цитоплазмы мегакариоцитов, как признак увеличенного турновера тромбоцитов.
Эксплорация тромбоцитопоэза, с изучением мегакариоцитов в костном мозге, представляется необходимой для диагноза идиопатической тромбоцитопении, так как прежние авторы считают мегакариограмму характерной для болезни Верльгофа. Вообще, после первоначальных исследований Франка, считалось, что при идиопатической тромбоцитопении существуют в изобилии медуллярные мегакариоциты. После подсчета при помощи текущих методов на мазке или в счетной камере, утвердилось мнение, что число мегакариоцитов при болезни Верльгофа в 2—3 раза больше, чем в нормальном костном мозге. По сравнению с числом медуллярных кариоцитов, существует около 0,6— 1% мегакариоцитов, в то время как при болезни Верльгофа они насчитывают около 2—3%, что означает в абсолютных цифрах соответственно 40—80 мегакариоцитов/мм3 и 100—300 мегакариоцитов/мм3 при болезни Верльгофа.
Имея в виду классическую патегенетическую гипотезу болезни Верльгофа, считается, что эффект функционального гиперспленизма детерминирует ингибицию в образовании тромбоцитов из-за дефекта созревания мегакариоцитов. По схеме Heilmeyer, в нормальной мегакариограмме появляются 4 группы мегакариоцитов. При болезни Верльгофа преобладают юные формы группы 1 и 2, в размере 50—75%, при этом тромбоцитообразующие формы спадают ниже 10—15% вплоть до исчезновения. Эта мегакариограмма с выраженным отклонением влево считается характерной для дефицита тромбоцитопоэза, признанного ранее как патогенетическое расстройство при идиопатической тромбоцитопении.
Однако уже давно известно, что методы оценки тромбоцитопоэза по миэлограмме на мазках являются весьма произвольными. Попытки оценки числа мегакариоцитов делались и у нас до 1960 г. (Berceanu и Sasarman); подсчет на срезах медуллярных фрагментов является повидимому наиболее достоверным но менее использованным в практике методом.
За последние 10—15 лет систематическое изучение мегакариопоэза и тромбоцитопоэза, даже если и не вошло в клиническую практику, сумело уточнить патогенетические характеристики идиопатической тромбоцитопении как синдрома по поводу повышенного уничтожения тромбоцитов на периферии, некомпенсированного значительным ускорением медуллярного тромбоцитопоэза. Эти данные потребовали внедрения новых специальных тестов для определения продолжительности жизни тромбоцитов путем мечения 51Cr; при помощи этого приема прослеживаются кривые сокращения и исчезновения меченных тромбоцитов из плазмы, параллельно с их включением и секвестрацией в печени и селезенке. Данный метод дополнился детерминированием общей массы мегакариоцитов путем волюметрической оценки на гистологических срезах (Harker и сотр., Ebbe и сотр., Branehog и сотр.); определение скорости производства тромбоцитов соотнесенной к скорости их уничтожения на периферии привело к определению тромбоцитного турновера на основе математических формул (Murphy и сотр., Branehog и сотр.).
В результате этих новых методов удалось установить при идиопатической тромбоцитопении известные изменения новых констант, которые свидетельствуют о повышенном тромбоцитопоэзе с целью компенсации очень высокого тромбоцитолиза: число мегакариоцитов на мм2 фиксированного среза медуллярной ткани равняется 39±2 (норма — 19±2), величина мегакариоцитов равняется 328±10 uм2 (норма 296 uм2); общее, число мегакариоцитов в костном мозге составляет у нормального лица 58 x 105/мм3 костного мозга, в то время как у больных с идиопатической тромбоцитопенией оно составляет 127 х 105мм3 костного мозга.
Темне менее, мегакариограмма в более новых исследованиях Branehog не отличается значительно от классических данных. Она показывает рост юных мегакариоцитов, но понижение по сравнению с нормой тромбоцитообразовательных мегакариоцитов, лишь в относительном значении. В абсолютном значении тромбоцитообразующие мегакариоциты повышены и объясняют увеличенный тромбоцитопоэз, определяемый вышеуказанными методами.
Ниже мы приводим средние значения по 4 группам мегакариоцитов у нормального лицами у больного с идиопатической тромбоцитопенией:
| Гр. I | Гр. II | Гр. III | Гр. IV | |
| Норма | 1,5% | 25,4% | 67,1% | 5,9% |
| ИТП | 6,6% | 34,1% | 51,3% | 8% |
Средний диаметр тромбоцитов у нормального лица ссотавляет 1,70', а при идиопатической тромбоцитопении — 2,65 u.
Значения турновера у нормальных лиц составляют 43000 ± 3000/uл сутки и 105 000 ± 10 000 uл/сутки при идиопатической тромбоцитопении, что означает скорость производства почти в 3 раза больше при идиопатической тромбоцитопении. Повышенная скорость турновера однако не компенсируется скоростью уничтожения, так как продолжительность жизни у нормального лица составляет 6,9±0,3 дней (4,2-8,5), в то время как при идиопатической тромбоцитопении сокращения очень значительны, составляя 0,02—1,83 дня, в среднем 0,57±0,11 дня.
Несмотря на то, что не все эти новые исследования вошли в диагностическую практику идиопатической тромбоцитопении, их изучение имеет важное значение для познания механизма возникновения тромбоцитопении при различных формах идиопатической тромбоцитопении.
Иммуносерологические исследования являются также новыми тестами, доказавшими автоиммунную природу форм идиопатической тромбоцитопении, изменив таким образом классическую патогенетическую концепцию. В первом периоде было налажено множество серологических методов с целью выявления наличия агглютининов, тромбоцитарных лизинов, а также и антител, фиксирующих комплемент (Harrington и сотр., Dausset, Tullis) или антител, дающих положительные реакции в тесте Стеффена на расход антигаммаглобулина (Steffen). Тест Кумбса на тромбоциты, хотя и очень трудный с технической точки зрения, считался положительным в высоком проценте случаев на статистике Stefanini и Dameshek. Проявленный в первое время энтузиазм убавился в дальнейшем, вследствие отрицательных резульаттов, полученных другими авторами, нашедших агглютинины на тепле и на холоде лишь у 5—10% случаев, как они существуют и в нормальных сыворотках (Cohen и сотр., Shulmann). Иммуносерологические тесты имеют здесь значение скорее для патогенетического исследования, чем для диагноза.
В настоящее время, большинство авторов утверждает, что из всех более 20 методов тестирования автоантител при идиопатической тромбоцитопении ни один не оказался настолько специфическим, чтобы его можно было применять как диагностический метод для определения автоиммунной природы идиопатической тромбоцитопении. Даже если и существуют сывороточные антитела, они находятся в низком титре и не оказывают эффектов агглютинации или лизиса на нормальные тромбоциты. Реакции положительной агглютинации вероятно неспецифичны, а детерминированы спонтанной агглютинацией тромбоцитов, которые после промывания высвобождают факторы адгезивности и агглютинации, как ADP; возможно также, что в сыворотке больных идиопатической тромбоцитопенией персистирует тромбин и другие факторы коагуляции (Baldini).
Позднее, при помощи других методов кажется удалось выявить специфические антитела при идиопатической тромбоцитопении, но эти приемы трудно внедрить в текущую практику. Таким является тест на лизис тромбоцитов при пароксизмальной ночной гемоглобинурии меченных 51Cr, которые будучи более чувствительными, высвобождают изотоп как маркер явления тромбоцитолиза вследствие действия цитотоксических сывороточных антител. Hanna и Nelken, нашли посредством двумоментного теста агглютинации неполноценные антитела в 50% случаев, которые можно обнаружить и посредством теста Кумбса с сывороткой анти-Fab, IgG (Mc Millan). Тест Карпаткина, цель которого состоит в высвобождении F3 из нормальных тромбоцитов под действием сыворотки от идиопатической тромбоцитопении, кажется наиболее чувствительным, давая положительные реакции почти в 80% случаев (на 234 больных).
Тест оказывается положительным и при тромбопенических пурпурах, в которых несомненно существуют антитела, то есть при формах изоиммунизации или при формах по поводу сенсибилизации к медикаментам. На основании этого теста Karpatkin считает доказанным автоиммунный механизм и предлагает название аутоиммунной тромбоцитопении (автоиммунной). Несмотря на то, что большинство авторов считает, что ни один метод не является специфическим, в настоящее время признается автоиммунная природа данного заболевания, независимо от того, идет ли речь о первичных идиопатических формах или о вторичных формах на почве вирусных инфекций (Shulmann и сотр., Baldini).
Другие методы, которые использовал первоначально Harrington и разработал затем Shulmann, свидетельствуют о существовании антитромбоцитарных факторов в сыворотке больных, но они трудно применимы в практике. Мы их приводим в порядке значения, так как они изложены в труде «Иммунология, иммунохимия и иммунопатология »(под редакцией Месробяну и Берчану), где приводятся и технические подробности:
1) Тромбоцитопенизирующее действие плазмы или сыворотки больных, иньецированной в дозе 0,4—6 мл/кг веса тела нормальному лицу, с сокращением до 20 000 тромбоцитов, персистирующих 2—3 дня, способной вызывать и пурпуру. Следует подчеркнуть, что тромбоцитопенизирующее действие на лиц, подвергавшихся спленектомии, происходит лишь в результате очень высоких доз — 19 мл/кг веса тела. Эффект оказывается нулевым если предварительно сыворотка абсорбируется с нормальными тромбоцитами.
2) Тромбоцитопенизирующий эффект после инъецирования сыворотки или плазмы у обезьян или кроликов (Berceanu и сотр.).
3) Тромбоцитопенизирующий эффект собственной сыворотки, взятой в период острого приступа, замороженной и затем инъецированной во время периода ремиссии, когда число тромбоцитов нормальное или почти нормальное.
4) Сокращение продолжительности жизни нормальных тромбоцитов, меченых 51Cr и инъецирование больным с идиопатической тромбоцитопенией, является важным тестом, доказывающим присутствие сывороточных тромбоцитопенизириющих факторов, а следовательно автоиммунную природу заболевания; сцинтиграфия селезенки доказывает лишний раз секвестрацию сенсибилизированных тромбоцитов в печени и селезенке.
Современные методы (Davey и Lander, Najean и сотр., Shulmann) прослеживают эволюцию радиоактивных кривых в плазме и органах, определяя таким образом сокращение на половину жизни тромбоцитов и интенсивность их секвестрации в печени и селезенке. Более новые наблюдения показали однако, что существует множество факторов ошибки и что следовательно спленическая секвестрация не является достаточно достоверным тестом, подтверждающим благоприятный эффект спленектомии (Baldini, Aster).
Другие наблюдения показывают однако, что спленическая секвестрация — ценный тест и является характерным для менее суровых форм, в то время как гепатическая секвестрация — признак суровой эволюции благодаря тромбоцитам обильно окутаным антителами (Shulmann и сотр., Aster и Keene). Najean и сотр. утверждают, что гепатическая секвестрация — признак устойчивости к кортикотерапии, но все же полагают, что спленектомия дает хорошие результаты тем, что таким образом удаляется орган, секретирующий автоантитела (Karpatkin и сотр., McMillan и сотр.).
Тесты на клеточный иммунитет, применяемые в последнее время являются особенным аргументом в пользу состояния автоиммунизации, зависящего от лимфоцитов Т, но эти тесты не вошли в клиническую практику. Разработанный Wybran тест показывает, что лимфоциты больных (в 14 из 16 случаев) инкорпорируют 3НТ в инкубации с тромбоцитами от больных или с алогенными тромбоцитами. Интенсивность реакции, которая эквивалентна реакции бластической трансформации in vitro вследствие действия антигенов, вызывающих реакции позднего типа, прямо пропорциональна степени тяжести данной формы идиопатической тромбоцитопении.
Аутоиммунная тромбоцитопения (идиопатическая тромбоцитопеническая пурпура, болезнь Верльгофа) - причины, клиника
Различают следующие основные виды иммунных тромбоцитопений:
1) аутоиммунная;
2) гетероиммунная;
3) аллоиммунная.
Аутоиммунная тромбоцитопения (идиопатическая тромбоцитопеническая пурпура, болезнь Верльгофа) обусловлена уменьшением продолжительности жизни тромбоцитов и их повышенным разрушением в связи с воздействием антитромбоцитарных аутоантител.
Эта нозологическая форма наиболее распространена среди всех тромбоцитопений и в среднем встречается с частотой 5:100 000 населения в год. Заболевание чаще возникает у женщин 20-40 лет и в большинстве случаев характеризуется длительным индолентным течением (в течение многих месяцев и лет).

Этиология и патогенез аутоиммунных тромбоцитопений
Причиной аутоиммунной тромбоцитопении являются антитромбоцитарные аутоантитела, которые синтезируются преимущественно в селезенке лимфоцитами и плазмоцитами. В 50-80% случаев антитела относятся к IgG, реже IgA или обоим классам иммуноглобулинов. Антитромбоцитарные антитела связываются с антигенами тромбоцитов, расположенными на их мембране (обычно ГП IIb/IIIа и Ib/IX).
Тромбоциты, соединенные с антителами, имеют укороченный период жизни (от десятков минут до 2-3 дней вместо 7-10 дней) и удаляются из кровеносного русла фагоцитами селезенки (реже печени и костного мозга) после соединения с Fc-рецептором. Таким образом, селезенка имеет большое значение в патогенезе аутоиммунной тромбоцитопений:
1) принимает участие в выработке аутоантител;
2) является основным местом деструкции сенсибилизированных тромбоцитов.
При выраженной тромбоцитопений отмечается повышение содержания М-КСФ, стимулирующего фагоцитарную активность макрофагов.
В генезе заболевания имеют значение нарушения клеточного иммунитета, что подтверждается увеличенным уровнем CD8+ и снижением CD4+ лимфоцитов. В ряде случаев (чаще у детей) выявляются аутореактивные Т-лимфоциты, реагирующие с собственными тромбоцитами.
Укорочение жизни тромбоцитов ведет к стимуляции тромбоцитопоэза, в результате чего в костном мозге определяется повышенное количество мегакариоцитов. В тяжелых случаях антитела могут вырабатываться и к мегакариоцитам, обусловливая мегакариоцитарную аплазию.

Клиническая картина аутоиммунной тромбоцитопении
Начало аутоиммунной тромбоцитопении обычно скрытое, без видимой причины. Геморрагический синдром проявляется кожными кровоизлияниями, носовыми кровотечениями, а у женщин, кроме того, — меноррагиями. Кожные кровоизлияния обычно возникают без видимых внешних причин или после незначительных ушибов.
Кровоизлияния имеют вид петехий и экхимозов и чаще возникают на конечностях. При большом количестве экхимозов кожа приобретает характерный внешний вид («шкура леопарда»).
Типичны также кровоизлияния в местах инъекций. Иногда кровоизлияния возникают на лице, губах и конъюнктиве. Появление таких геморрагий свидетельствует о риске развития кровоизлияния в головной мозг и требует своевременной и адекватной терапии.
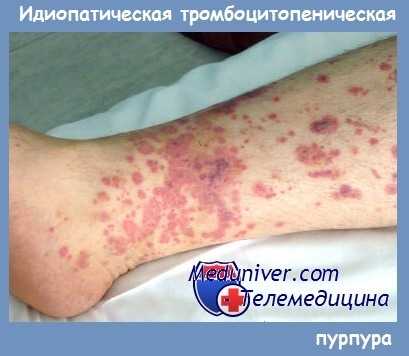
Нередко у больных наблюдаются кровотечения при экстракции зубов, которые начинаются сразу же после вмешательства, могут продолжаться несколько часов или даже дней. После остановки, в отличие от гемофилии, кровотечения не рецидивируют.
При объективном обследовании выявляются положительные пробы на ломкость капилляров («щипка», «жгута»). Увеличения размеров лимфатических узлов, печени и селезенки не отмечается (в отличие от ряда симптоматических тромбоцитопений).
При тяжелых и длительных кровотечениях может развиваться анемический синдром (слабость, быстрая утомляемость, одышка при физических нагрузках, усиленное сердцебиение и др.), выраженность которого зависит от тяжести анемии.
Течение аутоиммунной тромбоцитопений, как правило, волнообразное, с периодами обострений и ремиссий, во время которых уровень тромбоцитов может нормализоваться. В ряде случаев заболевание компенсировано и манифестирует только при воздействии провоцирующих факторов, чаще всего на фоне инфекции.
Тромбоцитопения
Информацию из данного раздела нельзя использовать для самодиагностики и самолечения. В случае боли или иного обострения заболевания диагностические исследования должен назначать только лечащий врач. Для постановки диагноза и правильного назначения лечения следует обращаться к Вашему лечащему врачу.
Тромбоцитопения: причины появления, при каких заболеваниях возникает, диагностика и способы лечения.
Определение
Тромбоциты – клетки крови, имеющие форму пластинки, которые участвуют в процессах свертывания крови. Их основная функция – закрытие раны при кровотечении путем образования тромба, или сгустка крови. Тромбообразование является естественным процессом защиты от массивной кровопотери при любых травмах. Дефицит тромбоцитов в крови называется тромбоцитопенией. Данное состояние достаточно часто протекает бессимптомно, однако может являться опасным для жизни при значительном уменьшении числа тромбоцитов крови.
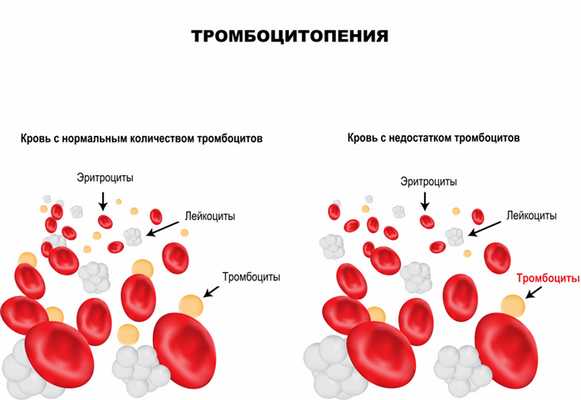
Помимо остановки кровотечения (гемостаза), тромбоциты выполняют ряд важных функций в организме человека: выделение веществ, суживающих сосуды при кровотечении; стимуляция восстановления тканей при любой травме; регулирование процессов местного воспаления и иммунитета.
Эти функции активизируются при любом повреждении эндотелия (внутреннего слоя, покрывающего стенки сосудов). Недостаток тромбоцитов приводит к нарушению системы свертывания крови и, как результат, повышенной кровоточивости, гематомам (синякам) и темно-красной сыпи на коже и слизистых (при надавливании такая сыпь не исчезает).
Продолжительная кровоточивость десен, большой объем кровотечений из маленьких ран и при менструациях – тревожный сигнал, говорящий о возможной проблеме системы свертывания крови.
Разновидности тромбоцитопении
Под тромбоцитопенией понимают уменьшение количества тромбоцитов в периферической крови ниже 150 тыс./мкл. Среди всех тромбоцитопений выделяют следующие состояния:
- Тромбоцитопения разведения – возникает при массивных кровотечениях и восполнении объема циркулирующей крови растворами.
- Тромбоцитопения распределения – часто возникает при избыточной патологической утилизации тромбоцитов в увеличенной селезенке.
- Продуктивная тромбоцитопения – возникает при нарушении функции костного мозга в результате различных заболеваниях или лучевой терапии.
- Тромбоцитопения потребления – возникает при ДВС-синдроме (диссеминированном внутрисосудистом свертывании крови – патологическом состоянии, когда образуются тромбы в кровеносном русле многих органов) или при постоянном аутоиммунном повреждении эндотелия сосудов. Происходит патологическая активация тромбоцитов и их быстрое расходование (потребление) организмом.
- Псевдотромбоцитопения – возникает при нарушении техники проведения анализа с развитием агрегации тромбоцитов.
Одной из частых причин тромбоцитопении является избыточное потребление тромбоцитов в организме, например, при ДВС-синдроме.
Иммунная форма тромбоцитопении считается самой частой иммунной патологией крови. Развивается быстро, с подъемом температуры тела и появлением обильной сыпи на коже нижних конечностей, ягодиц, вокруг крупных суставов, иногда достигая лица. Сыпь представляет собой мелкие кровоизлияния в кожу, часто сопровождается болью в суставах, отеками и нарушением движения в пораженных суставах. Иногда проявляется схваткообразной болью в животе, тошнотой, рвотой и жидким стулом. Описаны случаи появления крови в моче.
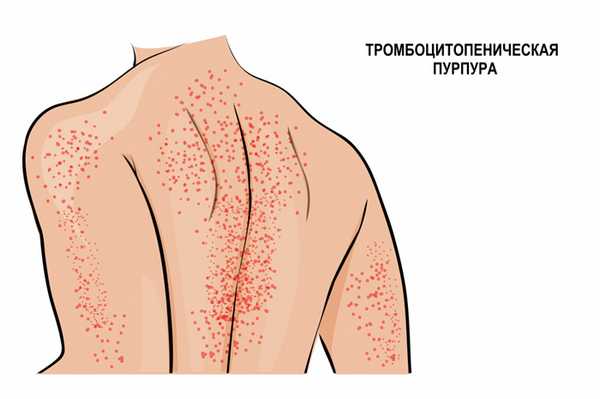
Аутоиммунная тромбоцитопения (идиопатическая тромбоцитопеническая пурпура, болезнь Верльгофа) вызвана уменьшением продолжительности жизни тромбоцитов из-за воздействия антитромбоцитарных аутоантител. Такая тромбоцитопения может протекать волнообразно – с чередованием периодов обострения и ремиссии. Нередко заболевание дает о себе знать на фоне инфекционных заболеваний: гриппа, вируса иммунодефицита человека (ВИЧ), вируса Эпштейна–Барр (ВЭБ), парвовируса В19, цитомегаловирусной инфекции (ЦМВ), вирусных гепатитов В и С.
Среди продуктивных тромбоцитопений особое место занимают апластические анемии, опухолевые процессы в костном мозге, лучевые поражения.
Для всех перечисленных состояний характерно резкое снижение гемопоэтической (кроветворной) функции костного мозга за счет тех или иных структурных изменений.
Апластическая анемия характеризуется уменьшением продукции всех трех ростков кроветворения: эритроцитов, лейкоцитов и тромбоцитов. Каждый росток отвечает за определенные функции в организме, и уменьшение производимых клеток приводит к появлению соответствующих симптомов. Уменьшение тромбоцитов ведет к повышенной кровоточивости, снижение количества эритроцитов говорит о признаках анемии (бледность, утомляемость, ломкость волос, боль за грудиной), а уменьшение лейкоцитов ведет к инфекционным осложнениям в виде рецидивирующих ангин, пневмоний и др. В некоторых случаях костный мозг замещается жировой тканью, что также нарушает образование клеток крови.
При В12- и фолиеводефицитной анемиях происходит нарушение созревания будущих тромбоцитов, они погибают еще до стадии созревания. Заболевание проявляется бледностью кожи, учащенным сердцебиением, одышкой. При выраженном дефиците витамина В12 возможны нарушение чувствительности, парезы и параличи.
Различные виды лейкозов приводят к появлению опухолевых клеток, которые делятся с огромной скоростью и вскоре замещают собой костный мозг. При этом нарушается функция всех трех ростков кроветворения. В костном мозге и крови появляются незрелые клетки, неспособные выполнять свою функцию.
Медикаментозная тромбоцитопения может развиться в результате приема некоторых лекарственных препаратов, например, цитостатиков, которые угнетают образование тромбоцитов в костном мозге.
Заболевания, сопровождающиеся увеличением размера селезенки (спленомегалией), способны привести к повышенному разрушению тромбоцитов, или гиперспленизму (увеличению утилизации тромбоцитов селезенкой). Помимо тромбоцитов также разрушаются эритроциты, что ведет к развитию не только тромбоцитопенического состояния, но и к гемолитической анемии.
К таким заболеваниям относят цирроз печени, в том числе алкогольной этиологии, хроническую сердечную недостаточность, лимфопролиферативные заболевания.
К каким врачам обращаться при тромбоцитопении
Диагноз «тромбоцитопения» устанавливается с помощью лабораторных исследований. Чаще всего пациенты, у которых впоследствии обнаруживается тромбоцитопения, обращаются к терапевту с жалобами на повышенную кровоточивость, сыпь, недомогание, усталость. При обнаружении снижения количества тромбоцитов терапевт назначит консультацию гематолога. В некоторых случаях требуется консультация онколога , гепатолога, ревматолога.
Диагностика и обследования при тромбоцитопении
При выявлении признаков тромбоцитопении врач назначит комплекс лабораторно-инструментальных методов исследования:
- клинический анализ крови: общий анализ с подсчетом тромбоцитов, лейкоформула, СОЭ (с микроскопией мазка крови при наличии патологических сдвигов);
Синонимы: Общий анализ крови, ОАК. Full blood count, FBC, Complete blood count (CBC) with differential white blood cell count (CBC with diff), Hemogram. Краткое описание исследования Клинический анализ крови: общий.
Читайте также:
- Омская геморрагическая лихорадка. Клиника и диагностика омской геморрагической лихорадки
- Лучевая анатомия (рентген, КТ анатомия) пищевода
- Инсулиномы. Диагностика инсулином. Признаки инсулином.
- Профилактика атеросклероза. Первичная и вторичная профилактика атеросклероза.
- Описторхоз: симптомы, возбудитель, диагностика и лечение
