Лучевая диагностика регенераторных и диспластических узлов печени
Добавил пользователь Дмитрий К. Обновлено: 30.01.2026
2 ГБОУ ВПО «Российский национальный исследовательский медицинский университет им. Н.И. Пирогова» Минздрава России
Приведены данные литературы, посвященные морфологическим изменениям клеток при гепатоканцерогенезе. Согласно международному консенсусу выделяют следующие узелковые образования: диспластические фокусы, диспластические узелки, а также ранний рак и прогрессирующий рак, – отражающих прогрессирующие этапы онкогенеза при циррозе печени. Представлены морфологические особенности клеток, нарушений архитектоники и васкуляризации, лежащие в основе дифференциальной диагностики узелковых образований. Диспластические фокусы и диспластические узелки низкой степени являются проявлением реактивных (регенеративных) изменений. Характерным признаком диспластических узелков считается развитие непарных артерий на фоне уменьшения количества ветвей воротной вены. Диспластические узелки высокой степени, характеризующиеся наличием признаков тканевого и клеточного метаболизма, недостаточных для постановки диагноза рак, следует трактовать как предопухолевые изменения с обязательным указанием в морфологическом заключении.
1. Состояние онкологической помощи населению России в 2015 году / Под ред. А.Д. Каприна, В.В. Старинского, Г.В. Петровой. М.: МНИОИ им. П.А. Герцена – филиал ФГБУ «НМИРЦ» Минздрава России, 2016. – 236 с.
2. Туманова У.Н., Кармазановский гг., Дубова Е.А., Щеголев А.И. Сравнительный анализ степени васкуляризации гепатоцеллюлярного рака и очаговой узловой гиперплазии печени по данным компьютерно-томографического и морфологического исследований // Вестник Российской академии медицинских наук. – 2013. – № 12. – С. 9–15.
3. Туманова У.Н., Кармазановский гг., Щеголев А.И. Денситометрические характеристики гепатоцеллюлярного рака при спиральной компьютерной томографии // Медицинская визуализация. – 2012. – № 6. – С. 42–49.
4. Туманова У.Н., Кармазановский Г.Г., Яшина Н.И., Щеголев А.И. Диагностическая значимость компьютерно-томографических характеристик узлов гепатоцеллюлярного рака в зависимости от размера // REJR. – 2016. Т. 6. № 4. – С. 44–55.
5. Туманова У.Н., Щеголев А.И. Ангиогенез при гепатоцеллюлярном раке // Успехи современной биологии. – 2015. – Т. 135. № 2. – С. 164–176.
6. Туманова У.Н., Щеголев А.И. Васкуляризация гепатоцеллюлярного рака // Архив патологии. – 2015. – № 2. – С. 50–55.
8. Anthony P.P., Vogel C.L., Barker L.F. Liver cell dysplasia: a premalignant condition // J. Clin. Pathol. – 1973. – V. 26. – P. 217–223.
9. Borzio M., Fargion S., Borzio F. et al. Impact of large regenerative, low grade and high grade dysplastic nodules in hepatocellular carcinoma development // J. Hepatol. – 2003. – V. 39. – P. 208–214.
10. El-Sayed S.S., El-Sadany M., Tabll A.A. et al. DNA ploidy and liver cell dysplasia in liver biopsies from patients with liver cirrhosis // Can. J. Gastroenterol. – 2004. – V. 18. – P. 87–91.
11. Hytiroglou P., Park Y.N., Krinsky G., Theise N.D. Hepatic precancerous lesions and small hepatocellular carcinoma // Gastroenterol. Clin. North. Am. – 2007. – V. 36. – P. 867–887.
12. International Consensus Group for Hepatocellular Neoplasia. Pathologic diagnosis of early hepatocellular carcinoma: a report of the international consensus group for hepatocellular neoplasia // Hepatology. – 2009. – V. 49. – P. 658–664.
13. International Working Party. Terminology of nodular hepatocellular lesions // Hepatology. – 1995. – V. 22. № 3. – P. 983–993.
14. Kim H., Oh B.K., Roncalli M. et al. Large liver cell change in hepatitis B virus-related liver cirrhosis // Hepatology. – 2009. – V. 50. – P. 752–762.
15. Lee R.G., Tsamandas A.C., Demetris A.J. Large cell change (liver cell dysplasia) and hepatocellular carcinoma in cirrhosis: matched case-control study, pathological analysis, and pathogenetic hypothesis // Hepatology. – 1997. – V. 26. – P. 1415–1422.
16. Libbrecht L., Craninx M., Nevens F. et al. Predictive value of liver cell dysplasia for development of hepatocellular carcinoma in patients with non-cirrhotic and cirrhotic chronic viral hepatitis // Histopathology. – 2001. – V. 39. – P. 66–73.
17. Natarajan S., Theise N.D., Thung S.N. et al. Large-cell change of hepatocytes in cirrhosis may represent a reaction to prolonged cholestasis // Am. J. Surg. Pathol. – 1997. – V. 21. – P. 312–318.
18. Plentz R.R., Park Y.N., Lechel A. et al. Telomere shortening and inactivation of cell cycle checkpoints characterize human hepatocarcinogenesis // Hepatology. – 2007. – V. 45. – P. 968–976.
19. Roncalli M., Roz E., Coggi G. et al. The vascular profile of regenerative and dysplastic nodules of the cirrhotic liver: implications for diagnosis and classification // Hepatology. – 1999. – V. 30. – P. 1174–1178.
20. Watanabe S., Okita K., Harada T. et al. Morphologic studies of the liver cell dysplasia // Cancer. 1983. – V. 51. – P. 2197–2205.
21. Zhao M., Zhang N.X., Du Z.Y. et al. Three types of liver cell dysplasia (LCD) in small cirrhotic nodules are distinguishable by karyometry and PCNA labelling, and their features resemble distinct grades of hepatocellular carcinoma // Histol. Histopathol. – 1994. – V. 9. – P. 73–83.
22. Zondervan P.E., Wink J., Alers J.C. et al. Molecular cytogenetic evaluation of virus-associated and non-viral hepatocellular carcinoma: analysis of 26 carcinomas and 12 concurrent dysplasias // J. Pathol. – 2000. – V. 192. – P. 207–215.
Гепатоцеллюлярная карцинома (ГЦК) является одним из наиболее частых онкологических заболеваний во всем мире с высокими показателями летальности. Наиболее высокие показатели заболеваемости ГЦК отмечаются в странах Азии и Африки. В России на конец 2015 года на учете находилось 7360 пациентов с ГЦК, летальность составила 43,6 % [1].
Чаще всего ГЦК развивается на фоне хронических заболеваний печени, в частности, цирроза [7]. При этом одной из основных причин смерти больных, страдающих циррозом печени, является ГЦК.
Согласно данным литературы [12], развитие ГЦК на фоне цирроза печени представляет собой многоступенчатый процесс в виде прогрессирования процессов тканевого и клеточного атипизма гепатоцитов, а также изменений васкуляризации новообразованных узелков. В этой связи актуальной задачей является выяснение морфологических особенностей предопухолевых узелковых образований печени, необходимых для их дифференциальной диагностики и определения прогноза заболевания.
Цель работы: анализ терминологии и описаний морфологических характеристик узелковых гепатоцеллюлярных образований печени.
Основные определения и морфологические критерии диагностики были опубликованы Международной рабочей группой по изучению узелковых образований в печени в 1995 году [13]. В дальнейшем эти определения и диагностические возможности неоднократно уточнялись и расширялись. Так, в 2002 году в Японском городе Куруме была создана специальная группа исследователей, так называемая «International Consensus Group for Hepatocellular Neoplasia (ICGHN)», по уточнению гистологических критериев диспластических узелков и ранней карциномы печени. В настоящее время данная группа ICGHN, включающая в себя 34 патологоанатомов и 2 врачей-клиницистов из 13 стран, продолжает работать. Согласно современным представлениям, морфологическими образованиями, отражающими этапы гепатоканцерогенеза, являются диспластические изменения (фокусы и узелки) и маленькие, не более 2 см в диаметре, опухолевые образования (ранняя ГЦК и маленькая прогрессирующая ГЦК) (табл. 1) [12].
Диспластические фокусы (или очаги) развиваются при хронических заболеваниях печени, особенно при циррозе, и представляют собой микроскопические (размером менее 1 мм) скопления диспластичных гепатоцитов. Данный термин был введен международным консенсусом в 1995 году [13]. Критериями размеров фокусов явилось то, что они отмечаются, как правило, в пределах одной печеночной дольки или одного узелка при циррозе печени. В этой связи диспластические фокусы выявляются лишь при микроскопическом исследовании биопсийного или операционного материала.
Классификация гепатоцеллюлярных узелковых образований печени
В зависимости от преобладающего вида составляющих клеток диспластические фокусы подразделяют на мелкоклеточные, крупноклеточные фокусы, а также фокусы с отсутствием железа. При этом диспластичные гепатоциты представляют мелкоклеточные изменения или крупноклеточные изменения.
Мелкоклеточные изменения, первоначально называемые как мелкоклеточная дисплазия [20], характеризуются уменьшенным размеромом гепатоцитов, повышенным ядерно-цитоплазматическим отношением, слабовыраженным полиморфизмом и гиперхромностью ядер и базофилией цитоплазмы.
Подобные мелкоклеточные изменения клеток сопровождаются более высокими показателями пролиферативной активности по сравнению с окружающими нормального вида гепатоцитами. При этом в диспластичных гепатоцитах отмечается укорочение теломер, повышенное образование микроядер, свидетельствующее о хромосомной нестабильности, а также потеря или увеличение хромосом [18]. Подобные мелкоклеточные изменения расценивались как предопухолевые. В пользу чего также свидетельствовали выявления аналогичных изменений клеток при ГЦК.
В то же время, диффузные мелкоклеточные изменения отражают процессы регенерации, а не дисплазии гепатоцитов [22]. Поскольку дифференциальная диагностика предопухолевых и регенеративных мелкоклеточных изменений очень затруднена, то остается неоднозначной и их роль в развитии ГЦК: одни исследователи указывают на их связь с ГЦК, другие ее не поддерживают [16].
Крупноклеточными изменениями клеток, первоначально называемыми клеточной дисплазии печени [8], обозначали скопления гепатоцитов с увеличенным объемом и ядра и цитоплазмы (вследствие этого ядерно-цитоплазматическое отношение не изменялось), полиморфизмом и гиперхромностью ядер, иногда с наличием многоядерных гепатоцитов.
К сожалению, единого мнения о биологической роли крупноклеточных изменений так и не достигнуто. В пользу того, что крупноклеточные изменения отражают реактивные процессы при хроническом повреждении или старении, свидетельствуют показатели низкой пролиферативной активности и повышенный апоптоз, отсутствие их в наблюдениях ГЦК [15] и, наоборот, появление при холестазе [17].
Вместе с тем, в таких гепатоцитах выявлено повышенное количество ядрышковых организаторов по сравнению с окружающими нормальными клетками, ненормальное содержание ДНК [10], хромосомные аберрации и потери хромосом [22], что трактуется как предопухолевые изменения. Кроме того, крупноклеточные изменения, наблюдающиеся при крупноузловом циррозе печени, характеризуются моноклональностью, что характерно для гепатоканцерогенеза.
Интересным фактом служат данные H. Kim с соавт. [14] об укорочении теломер, повышении индекса пролиферации и увеличении повреждения ДНК в крупноклеточных изменениях при циррозе печени, вызванном вирусным гепатитом В, и отсутствие таких поражений при крупноклеточных изменениях на фоне хронического холестаза. Подобные сведения свидетельствуют, видимо, о том, что крупноклеточные изменения бывают двух типов: один тип является отражением реактивных (регенераторных) процессов и не связан с онкогенезом, а второй относится к предопухолевых изменениям (дисплазии), являясь звеном гепатоканцерогенеза.
Вместе с тем, по мнению ряда исследователей, выявление крупноклеточных изменений при циррозе печени, развившемся на фоне вирусного гепатита В или С, является фактором риска для последующего развития ГЦК. В то же время укорочение теломер, хромосомная нестабильность и повреждения ДНК выражены в большей степени при мелкоклеточных изменениях по сравнению с крупноклеточными на фоне хронических болезней печени и максимальны при ГЦК [18]. То есть крупноклеточные изменения при вирусном гепатите В или С могут рассматриваться в качестве первого предопухолевого этапа, а мелкоклеточные изменения как последующего, второго.
Диспластические узелки (ДУ) обнаруживаются в основном при циррозе печени, хотя иногда встречаются и при других хронических болезнях печени [12]. ДУ представляют собой более или менее четкое узелковое образование диаметром до 1 см, отличающееся от окружающей паренхимы печени цветом, внешним видом, размером. Они могут быть единичными и множественными (обычно менее 10) [11].
Согласно международному консенсусу [13], в зависимости от морфологических изменений и прогноза их течения все ДУ подразделяются на два вида: диспластические узелки низкой степени и высокой степени (табл. 2).
При микроскопическом исследовании диспластические узелки низкой степени (ДУНС) характеризуются однотипностью изменений с окружающей паренхимой с незначительным увеличением (не более чем 1,3 раза) плотности клеток по сравнению с окружающей паренхимой. ДУНС отличает также клональность клеток в виде диффузного отложения железа или меди, а также признаков стеатоза при отсутствии жировой дегенерации клеток печени. Клеточный атипизм выражен слабо. Могут встречаться крупноклеточные изменения. При этом отсутствуют псевдожелезистые образования гепатоцитов.
В диспластических узелках высокой степени (ДУВС) отмечаются признаки тканевого и клеточного атипизма, но недостаточные для постановки диагноза карциномы. Чаще всего наблюдается увеличение плотности клеток в 1,3–2 раза по сравнению с окружающей тканью печени. Достаточно часто определяются и вышеописанные мелкоклеточные изменения.
Морфологические характеристики гепатоцеллюлярных узелковых образований печени
Лучевая диагностика регенераторных и диспластических узлов печени
КТ, МРТ, УЗИ признаки нодулярной регенераторной гиперплазии печени
а) Терминология:
1. Сокращения:
• Нодулярная регенераторная гиперплазия (НРГ)
2. Синонимы:
• Узловая трансформация, нецирротические узловые изменения
3. Определения:
• Редко распознаваемое заболевание, характеризующееся диффузной мелко- и крупноузловой трансформацией паренхимы печени при отсутствии фиброзных перегородок между очагами
• Очаги большего размера называются мультиацинарными (крупными) регенераторными узлами
б) Визуалазиация:
1. Общая характеристика:
• Лучший диагностический критерий:
о Мультиацинарные регенераторные узлы представляют собой множественные гиперваскулярные очаги размером до 5 см, с персистирующим отсроченным усилением на МРТ с использованием гепатобилиарного контраста
• Локализация:
о Диффузное поражение; микроскопические узелки располагаются преимущественно в перипортальной области
• Размер:
о Моноацинарные узлы при нодулярной регенераторной гиперплазии чаще всего имеют размер около 1 мм в диаметре, сгруппированные узлы достигают 10 мм
о Мультиацинарные узлы: 0,5-5 см в диаметре
• Ключевые моменты:
о Диффузная НРГ и мультиацинарные регенераторные узлы возникают на фоне различных предшествующих состояний и имеют разные лучевые признаки
(Слева) На Т1 ВИ МР томограмме у мужчины 63 лет с миелопролиферативным заболеванием определяется выраженное увеличение селезенки, скорее всего, обусловленное, экстрамедуллярным гемопоэзом. Диффузных или очаговых патологических изменений со стороны печени не определяется, тем не менее, при биопсии подтвердилась диффузная нодулярная гиперплазия — известное осложнение миелодис-плазии, а также побочный эффект приема лекарств, используемых с целью терапии при этом заболевании.
(Справа) Т1 ВИ МР томограмме у этого же пациента с подтвержденной при биопсии нодулярной регенераторной гиперплазией также не определяется каких-либо изменений со стороны печени. (Слева) На аксиальной Т1 ВИ МР томограмме с контрастным усилением у пациента с синдромом Бадда-Киари визуализируются многочисленные гиперинтенсивные очаги размером около 2 см. Обратите внимание на гипоинтенсивное «гало» вокруг некоторых из крупных регенераторных узлов, — типичная, но не частая находка.
(Справа) На аксиальной Т2 ВИ МР томограмме у этого же пациента визуализируются гипоинтенсивные очаги (мультиацинарные регенераторные гиперпластические узлы) в правой доле печени (в меньшем количестве и не столь наглядно). (Слева) На фотографии среза макропрепарата печени, эксплантированной у пациента с синдромом Бадда-Киари, нарушена ее морфология: гипертрофирована хвостатая доля на фоне атрофии латерального сегмента. Визуализируются также множественные мультиацинарные регенераторные узлы оранжевого цвета.
(Справа) На аксиальной КТ с контрастным усилением у мужчины с хронически протекающим синдромом Бадда-Киари визуализируются многочисленные гиперваскулярные крупные регенераторные узлы (макроскопическая форма нодулярной регенераторной гиперплазии).
2. КТ признаки нодулярной регенераторной гиперплазии:
• КТ без контрастного усиления:
о Плотность узелков соответствует плотности печеночной паренхимы
о На фоне диффузного снижения плотности печени при синдроме Бадда-Киари или стеатозе узелки становятся гиперденсными
• КТ с контрастным усилением:
о Диффузная нодулярная регенераторная гиперплазия:
- Сливные образования отсутствуют; патологических изменений со стороны печени не определяется, либо обнаруживается нарушение ее морфологии
- Часто имеют место признаки портальной гипертензии (более чем в 50% случаев):
Спленомегалия, асцит, варикозное расширение вен
о Мультиацинарные регенераторные узлы:
- Множественные (от двух до сотни) образования в печени сливного характера:
Размер узлов составляет 0,5-5 см
Равномерно гиперваскулярны в артериальную и портально-венозную фазу, «вымывание» контраста отсутствует
В центре узлов возможно наличие рубца; по периферии - гипо- или гиперденсное гало
Признаки причинного заболевания (например, при синдроме Бадда-Киари-тромбоз печеночных вен и нижней полой вены, гипертрофия центральных отделов печени и атрофия периферических)
Признаки портальной гипертензии более чем в 50% случаев
3. МРТ признаки нодулярной регенераторной гиперплазии:
• Т1 ВИ:
о Мультиацинарные регенераторные узлы гиперинтенсивны в 75% случаев
• Т2 ВИ:
о Изо- или гипоинтенсивны; обнаруживается меньшее количество узлов
о Могут выглядеть гиперинтенсивными (на фоне инфаркта)
о Симптом гало: обусловлен участками пелиоза вокруг узелков
• Многофазная МРТ с контрастным усилением:
о Равномерное, выраженное контрастное усиление в артериальную и портально-венозную фазу
о Возможно контрастное усиление по типу кольца (гало), а также наличие центрального рубца
• МРТ с гепатобилиарным контрастом (например, препаратами гадоксетовой кислоты): накопление и длительное удержание контраста:
о Позволяет подтвердить доброкачественную природу узлов о Выраженное (равномерное или периферическое) контрастное усиление
о Имитирует проявления очаговой узелковой гиперплазии (ОУГ), как и изменения при гистологическом исследовании
4. УЗИ признаки нодулярной регенераторной гиперплазии:
• Серошкальное УЗИ:
о Гипоэхогенные узлы (38%), изоэхогенные (10%), гиперэхогенные (53%)
• Цветовая допплерография:
о Выраженный артериальный кровоток
5. Рекомендации по визуализации:
• Лучший метод диагностики:
о Многофазная КТ или МРТ
• Выбор протокола:
о МРТ с контрастным усилением (гадобенат димеглюмин или препараты гадоксетовой кислоты):
- Позволяет наиболее точно диагностировать мультиацинарные регенераторные узелки
(Слева) На аксиальной КТ с контрастным усилением визуализируется один из нескольких гиперваскулярных узлов с гиподенсным «ободком» («гало»). При исследовании биоптата была обнаружена гиперплазия ткани печени доброкачественного характера, с наличием крупных (мультиацинарных) регенераторных узлов.
(Справа) На КТ с контрастным усилением у этого же пациента определяются признаки хронической окклюзии и кавернозной трансформации воротной вены. Крупные (мультиацинарные) регенераторные узлы возникают в печени почти исключительно на фоне хронической сосудистой недостаточности (тромбоз воротной вены или синдром Бадда-Киари). (Слева) На Т1 ВИ МР томограмме в артериальную фазу контрастного усиления визуализируются многочисленные гиперваскулярные очаги, некоторые из них с гипоинтенсивным «ободком», другие — с гипоинтенсивным центральным рубцом (изменения типичны для ОНГ— очаговой узелковой гиперплазии).
(Справа) На МР томограмме в отсроченной фазе контрастного усиления у этого же пациента после внутривенного введения гадобената димеглюмина определяется захват и персистирующее накопление контрастного вещества узлами, что является признаком наличия функционирующих гепатоцитов и доброкачественности изменений. (Слева) На аксиальной Т1 ВИ МР томограмме у женщины 43 лет с синдромом Бадда-Киари визуализируются многочисленные, гиперваскулярные, мультиацинарные регенераторные узлы, как минимум в одном из которых имеется центральный рубец.
(Справа) На фотографии макропрепарата виден большой регенераторный узел, резецированный у этой же пациентки; визуализируется также фиброзный рубец изменения, которые обычно присущи ОНГ—заболевания, имеющего практически одинаковые гистологические и лучевые признаки.
в) Дифференциальная диагностика нодулярной регенераторной гиперплазии печени:
1. Мультифокальный гепатоцеллюлярный рак (ГЦР):
• Неравномерно гиперденсное образование (на КТ или МРТ в артериальную фазу) с быстрым вымыванием контраста
• Часто приводит к поражению печеночной или воротной вены; может иметь капсулу
• Узлы ГЦР гипоинтесивны на Т1 ВИ, гиперинтенсивны на Т2 ВИ:
о Крупные регенераторные узлы гиперинтенсивны на Т1 ВИ, изо- или гипоинтенсивны на Т2 ВИ
• Обычно не захватывают и не накапливают гепатобилиарный МР-контраст:
о В некоторых случаях высокодифференцированный ГЦР может неравномерно накапливать гепатобилиарный контраст
2. Множественная очаговая узелковая гиперплазия:
• Лучевые и гистологические признаки идентичны мультиацинарным регенераторным узлам
• Клиническая картина отлична:
о ОНГ является изолированным поражением и возникает у здоровых молодых женщин, у которых отсутствуют другие патологические изменения со стороны печени
(Слева) На аксиальной КТ с портально-венозную фазу контрастного усиления определяются изменения, типичные для синдрома Бадда-Киари и мультиацинарных регенераторных узлов. Обратите внимание на стент в нижней полой вене, на правую печеночную вену с признаками окклюзии, а также многочисленные мультиацинарные регенераторные узлы, длительно удерживающие контраст.
(Справа) На фотографии микропрепарата виден резецированный мультиацинарный регенераторный узел с окрашенными в зеленый цвет ретикулярными волокнами что позволяет отчетливо визуализировать периферический и центральный рубец, наблюдаемый в некоторых крупных регенераторных узлах, и крайне схожий с таковым при ОНГ. (Слева) На КТ в артериальную фазу контрастного усиления у мужчины 35 лет с синдромом Бадда-Киари визуализируются множественные мультиацинарные регенераторные узлы, накапливающие контраст, в т. ч. некоторые из них — с «гало» по периферии, а другие — с центральным «рубцом».
(Справа) На КТ срезе у этого же пациента определяются другие регенераторные узлы. Обратите также внимание на внепеченочный сосудистый стент-графт. (Слева) На аксиальной КТ с контрастным усилением у этого же пациента (после стентирования НПВ) визуализируется стент в нижней полой вене. Определяется уменьшение размеров и количества всех регенераторных узлов.
(Справа) На другом КТ срезе у этого же пациента (после стентирования НПВ) определяется уменьшение количества и размеров регенераторных узлов.
г) Патология:
1. Общая характеристика:
• Этиология:
о Этиология диффузной НРГ неизвестна, существуют различные теории ее возникновения:
- Гиперплазия гепатоцитов, скорее всего, в ответ на хроническую ишемию
о Мультиацинарные регенераторные узлы возникают из-за патологических изменений кровотока в печени (уменьшения кровотока по воротной и печеночной венам)
- Что позволяет объяснить увеличение частоты появления узлов при синдроме Бадца-Киари и у пациентов с тромбозом воротной вены
- Мультифокальная дилатация печеночных артерий — очаговая гиперплазия и пролиферация гепатоцитов:
Позволяет объяснить схожесть лучевых и гистологических признаков с ОНГ
о Диффузная или очаговая форма НРГ не обладает злокачественным потенциалом
• Ассоциированные патологические изменения:
о Диффузная НРГ может быть ассоциирована с множеством других заболеваний и состояний:
- Трансплантация солидного органа или костного мозга
- Миелопролиферативные заболевания (например, полицитемия, лимфома, миелома)
- Химиотерапия
- Аутоиммунные болезни (например, системная красная волчанка, ревматоидный артрит, полиартериит)
- Заболевания сердца, констриктивный перикардит
- Неблагоприятная наследственность (редко)
- Пожилой возраст (РНГобнаруживается у 5% пожилых людей)
о Крупные регенераторные узлы:
- Синдром Бадца-Киари (более чем в 70% случаев)
- Заболевания сердца (особенно врожденные)
- Хронический тромбоз воротной вены
- Цирроз печени различной этиологии, в особенности, обусловленный аутоиммунным гепатитом
2. Микроскопия:
• Диффузная НРГ: моноацинарные узлы в неизмененной в целом печени (без признаков фиброза, цирроза)
• Крупные регенераторные узлы: мультиацинарные, образованы гепатоцитами различного размера, расположенными в 1-2 ряда, с сужением синусоидов:
о Между узлами находятся участки центрилобулярной атрофии, где располагаются извитые, расширенные синусоиды, выражены застойные изменения, а также обнаруживается «сеть» фиброзных тяжей
о В узлах может присутствовать центральный рубец, неотличимый от такового при ОНГ
о Возможна пролиферация мелких желчных протоков либо мета пластическая трансформация гепатоцитов в них
• В обоих случаях возникает облитерация мелких печеночных вен, возможно, также воротной вены:
о Что приводит к ишемии и атрофии, а затем-вторичной гиперплазии в областях наиболее сохранного кровотока
о Относительно легкие диффузные ишемические изменения приводят к формированию диффузной формы НРГ
д) Клинические особенности:
1. Проявления нодулярной регенератоной гиперплазии печени:
• Наиболее частые признаки/симптомы:
о Заболевание чаще всего протекает бессимптомно, однако может приводить к нецирротической портальной гипертензии (варикозному расширению вен и т. д.)
• Другие признаки/симптомы:
о Обусловлены причинным заболеванием, например, синдромом Бадца-Киари, заболеваниями сердца, аутоиммунными болезнями и т.д.
• Диагноз устанавливается на основании данных биопсии мультиацинарного регенераторного узла (гиперплазия ткани печени, ± воспалительные изменения, рубец: изменения аналогичны таковым при ОНГ):
о Патолог имеет меньше возможностей в дифференциальной диагностике, чем рентгенолог, знающий лучевые и клинические признаки в каждом отдельном случае:
- При гистологическом исследовании, особенно в случае тонкоигольной аспирации, РНГ сложно отличить от ОНГ аденомы и даже от ГЦР
2. Демография:
• Возраст:
о Чаще встречается у взрослых, заболеваемость увеличивается с возрастом
• Пол:
о Половая предрасположенность отсутствует
• Эпидемиология:
о Заболевание нечасто распознается, однако не является редким
о Возможная гиподиагностика связана с плохим распознаванием заболевания и вероятным отсутствием изменений в материале полученном при биопсии
3. Течение и прогноз:
• Мультиацинарные регенераторные узлы могут увеличиваться в размерах, реже подвергаются ишемическим изменениям:
о Не трансформируются в ГЦР
• Диффузная НРГ обычно протекает бессимптомно:
о Может приводить к прогрессирующей портальной гипертензии (и, например, к кровотечению из варикозно расширенных вен пищевода), реже-к печеночной недостаточности
• В обоих случаях симптоматика обусловлена причинными заболеваниями
• Прогноз зависит от выраженности изменений, обусловленных портальной гипертензией, и тяжести сочетанных заболеваний
4. Лечение:
• Направлено на коррекцию портальной гипертензии и устранение кровотечения из варикозно расширенных вен
• При прогрессирующей печеночной недостаточности и далеко зашедшем поражении печени показана ортотопическая трансплантация
е) Диагностическая памятка:
1. Следует учесть:
• Диффузная НРГ может становиться причиной кровотечения из варикозно расширенных вен при отсутствии цирроза
• Крупные регенераторные узлы в печени на фоне нарушения ее морфологии могут быть ошибочно приняты за иные объемные образования, например, ГЦР
о Важно распознать причинное заболевание (например, синдром Бадда-Киари) и характерный вид мультиацинарных регенераторных узлов
2. Советы по интерпретации изображений:
• Лучевые признаки практически идентичны ОНГ
• Множественные гиперваскулярные образования, для которых нетипично «вымывание» контраста, обнаруженные у пациента с синдромом Бадда-Киари, представляют собой мультиацинарные регенераторные узлы, а не ГЦР
КТ, МРТ, УЗИ признаки регенераторных и диспластических узлов печени
а) Терминология:
1. Аббревиатуры:
• Диспластический узел (ДУ)
• Регенераторный узел (РУ)
2. Синонимы:
• Цирротический узел
3. Определения:
• Ограниченная пролиферация паренхимы печени на фоне цирроза, возникающая в ответ на ее повреждение:
о При прогрессировании возникают изменения диспластического характера или происходит озлокачествление
б) Визуализация:
1. Общая характеристика:
• Лучший диагностический критерий:
о РУ: множественные мелкие узелки в цирротически измененной печени, гипоинтенсивные на Т2 ВИ и GRE
о ДУ: обнаруживаются в меньшем количестве, имеют меньший размер; гиперинтенсивны на Т1 ВИ и гипоинтенсивны на Т2 ВИ
• Локализация:
о Равномерное распределение во всех отделах печени
• Размер:
о Размер регенераторных узлов обычно не превышает двух сантиметров:
- Поперечный размер диспластических узлов 2-4 см
• Морфология:
о РУ: множественные:
- ДУ: немногочисленные или единичные
о Округлые, четко отграниченные
2. Рекомендации по визуализации:
• Лучший метод диагностики:
о МРТ
• Выбор протокола:
о Т1 и Т2 ВИ; Т1 ВИ с контрастным усилением для оценки васкуляризации
о Препараты гадоксетовой кислоты (Eovist, Primovist) или гадо-беновой кислоты для дифференциальной диагностики узлов в печени:
- РУ и ДУ ожидаемо накапливают и удерживают контрастное вещество в отсроченной фазе
- Узлы ГЦР не накапливают и не удерживают контрастное вещество:
Диспластические узлы (высокой степени дисплазии) также могут не накапливать и не удерживать контраст
В некоторых случаях ГЦР показывает неравномерный («географический», «пятнистый») характер накопления контраста
(Слева) На Т1 ВИ МР томограмме у мужчины 50 лет, страдающего циррозом печени, определяется гиперинтенсивное объемное образование округлой формы, с четкими краями, с «выпадением» сигнала на Т1 ВИ GRE в «противофазе» (томограммы не продемонстрированы).
(Справа) На Т2 ВИ МР томограмме у этого же пациента образование выглядит гипоинтенсивным, что типично для диспластического узла и не характерно для гепатоцеллюлярного рака (ГЦР). (Слева) На Т1 ВИ МР томограмме в поздней артериальной фазе (этот же пациент) определяется минимальная васкуляризация (контрастное усиление) образования.
(Справа) Т1 ВИ МР томограмме в венозной фазе (этот же пациент) визуализируется образование (диспластический узел), гипоинтенсивное по сравнению с паренхимой печени; низкая интенсивность сигнала, скорее всего, обусловлена повышенным контрастным усилением печени, чем «вымыванием» контраста из узла. (Слева) На сонограмме у этого же пациента визуализируется гипоэхогенный узел; под контролем УЗИ была выполнена его биопсия. Несмотря на то, что при МР-исследовании определяются изменения, типичные для диспластического узла, важным моментом является подтверждение природы образования путем его биопсии под контролем УЗИ. При исследовании биоптата были обнаружены диспластические изменения без признаков ГЦР.
(Справа) На фотографии микропрепарата диспластического узла высокой степени дисплазии визуализируется непарная артериола. Определяется также дуктуляр-ная реакция (внутри и по периферии желчных протоков).
3. КТ признаки регенераторных и диспластических узлов:
• КТ без контрастного усиления:
о Большинство регенераторных узлов достоверно не определяются на КТ или MPT (Т1 ВИ)
о Мелкие узелки изоденсны паренхимы печени, вследствие чего их невозможно обнаружить
о Регенераторные узлы могут выглядеть более плотными по сравнению с окружающей их паренхимой печени:
- Вследствие повышенного содержания железа или гликогена
- Или за счет наличия «гало», обусловленного гиподенсными участками фиброза, окружающими узлы
• КТ с контрастным усилением:
о Регенераторные узлы накапливают контраст несколько хуже по сравнению с тканью печени:
- В результате чего они становятся неразличимыми, «исчезают»
о Диспластические узлы изо- или гиперденсны в артериальную фазу:
- Большинство из них не являются гиперваскулярными
- Избыточная васкуляризация является признаком, подозрительным на ГЦР
(Слева) На аксиальной Т1 ВИ МР томограмме с контрастным усилением у женщины 67 года, страдающей циррозом, определяются типичные для цирроза изменения: узлы в печени, а также расширение фиссур. Не очень отчетливо визуализируются множественные, мелкие регенераторные узелки.
(Справа) На аксиальной Т2 ВИ МР томограмме у этой же пациентки лучше видны цирротические узелки, внешний вид которых (гипоинтенсивные очаги субсантиметрового диапазона) типичен для доброкачественных регенераторных узлов. (Слева) На аксиальной Т1 ВИ МР томограмме у этой же пациентки в латеральном сегменте определяется гиперинтенсивное образование с четкими контурами, которое было верифицировано как диспластический узел.
(Справа) На другой аксиальной Т1 ВИ МР томограмме у этой пациентки определяется гипоин-тенсивный очаг в шестом сегменте печени — верифицированный ГЦР. (Слева) На аксиальной Т2 ВИ МР томограмме (эта же пациентка) визуализируется диспластический узел, относительно гипоинтенсивный, что является характерной чертой узловых изменений этого типа.
(Справа) На другой аксиальной Т2 ВИ МР томограмме у этой же пациентки визуализируется относительно гиперинтенсивный узел ГЦР (повышение интенсивности сигнала типично для злокачественного узла или объемного образования).
4. МРТ признаки регенераторных и диспластических узлов:
• Т1 ВИ:
о Регенераторные узлы:
- Характеризуются вариабельной интенсивностью сигнала
- Обычно изоинтенсивны по отношению к паренхиме печени (вследствие чего не визуализируются)
о Диспластические узлы:
- Сигнальные характеристики вариабельны
- Обычно изо- или гиперинтенсивны по отношению к печени
• Т2 ВИ:
о Регенераторные узлы:
- Низкая интенсивность сигнала по сравнению с печенью (из-за содержания железа)
- Узлы высокой степени дисплазии могут быть немного более гиперинтенсивными по сравнению с печенью
о Повышение интенсивности сигнала коррелируете высокой степенью дедифференцировки и подозрительно на ГЦР
• DWI:
о Для РУ и ДУ низкой степени дисплазии нетипично ограничение диффузии (узлы не «светятся»)
о ДУ высокой степени дисплазии и ГЦР обычно «светятся» на DWI
• Т1 ВИ с контрастным усилением:
о РУ:
- Изоинтенсивны печени (не обнаруживаются) либо слегка гипоинтенсивны
о ДУ:
- Вариабельно гиперинтенсивны по отношению к печени:
Увеличение васкуляризации подозрительно на злокачественную трансформацию диспластического узла
• На МРТ сдимеглюмина гадобенатом или препаратами гадоксетовой кислоты регенераторные и диспластические узлы интенсивно накапливают и удерживают контрастное вещество:
о Что означает наличие функционирующих гепатоцитов
о И свидетельствует о доброкачественности изменений (РУ):
- В диспластических узлах высокой степени дисплазии и ГЦР нет функционирующих гепатоцитов, экскреция желчи отсутствует:
Вследствие чего накопления контраста не происходит (узлы гипоинтенсивны в отсроченную фазу)
5. УЗИ признаки регенераторных и диспластических узлов:
• Узлы могут выглядеть гипо-, изо- или гиперэхогенными:
о Большинство регенераторнных и диспластических узлов не очевидны на УЗИ
(Слева) На аксиальной Т1 ВИ МР томограмме в артериальной фазе определяется минимальное накопление контраста диспластическим узлом, что ха рактерно для узловых изменений этого типа.
(Справа) На другой Т1 ВИ МР томограмме в артериальную фазу у этой же пациентки определяется типичное неравномерное накопление контраста узлом ГЦР. (Слева) На аксиальной Т1 ВИ МР томограмме в отсроченной фазе контрастного усиления (с использованием гепатобил парного контраста) определяется накопление и длительное удержание препарата гадоксетовой кислоты (Еоvist) диспластическим узлом и большей частью регенераторных узлов.
(Справа) На другой Т1 ВИ МР томограмме в отсроченную фазу (эта же пациентка) накопление контраста в узле ГЦР не определяется. (Слева) На аксиальной диффузионно-взвешенной томограмме (эта же пациентка) не определяется рестрикции диффузии в диспластическом узле (узел выглядит «темным»).
(Справа) На другой диффузионно взвешенной томограмме (эта же пациентка) определяется рестрикция диффузии в узле ГЦР (узел выглядит «ярким»), что типично для злокачественных новообразований.
в) Дифференциальная диагностика регенераторных и диспластических узлов печени:
1. Гепатоцеллюлярный рак:
• Плотность ГЦР ниже по сравнению с плотностью печени при нативной КТ и при КТ в отсроченную фазу контрастного усиления
• Узлы ГЦР неравномерно гиперваскулярны в артериальную фазу; «вымывание» контраста в венозную и отсроченную фазу является характерным признаком гепатоцеллюлярного рака
• Для ГЦР типичен вариабельно гипоинтенсивный сигнал на Т1 ВИ, гиперинтенсивный на Т2 ВИ; опухоль «светится» на DWI
• Размер обычно превышает 20 мм
• Другие характерные признаки: неоднородная структура, множественность поражения, наличие капсулы, прорастание в вены
2. Нодулярная регенераторная гиперплазия:
• Диффузная мелкоузловая трансформация паренхимы печени без фиброзных септ между узлами
• Обнаруживается в цирротически не измененной печени
• Очаговая форма: «крупные регенераторные узлы»:
о Отдельная нозологическая (патологическая) форма, а не просто цирротические регенераторные узлы, имеющие размер больше обычного
о Ассоциирована с (в порядке уменьшения частоты): синдромом Бадда-Киари, врожденными заболеваниями сердца, другими состояниями
• Узлы обычно гиперинтенсивны на Т1 ВИ и изо- или гипоинтенсивны на 12 ВИ
• Возможно появление «кольца» или «гало» на МРТ с контрастным усилением
• На КТ и МРТ с контрастным усилением узлы интенсивно накапливают контраст, в венозную фазу повышение плотности сохраняется
• Узлы обычно множественные, имеют размер 1,5-5 см
(Слева) На аксиальной КТ без контрастного усиления у женщины 78 лет, страдающей хроническим гепатитом С, в латеральном сегменте печени определяется образование, состоящее из двух различных компонентов: жировой плотности (слева), и мягкотканной плотности (справа).
(Справа) На аксиальной Т1 ВИ МР томограмме с жироподавлением у этой же пациентки определяется, что мягкотканный компонент (справа) относительно гиперинтенсивен, что типично для диспластического узла. Интенсивность сигнала от левой части образования снижается при использовании программы жиро-подавления, что типично для опухолей, содержащих жир, и подозрительно на ГЦР. (Слева) На аксиальной Т2 В И МР томограмме у этой же пациентки определяется снижение интенсивности сигнала от диспластического узла и гиперинтенсивный сигнал от ГЦР. Эти изменения являются примером ГЦР, развившегося внутри диспластического узла (и иллюстрируют картину «узла в узле»).
(Справа) На аксиальной МР томограмме (opposed-phase GRE) у этой же пациентки определяется подавление сигнала от участка ГЦР, содержащего жир, и гипоинтенсивный сигнал от диспластического узла. (Слева) Микропрепарат: гепатоцеллюлярный узел с признаками дисплазии высокой степени выраженности, при этом инфильтрация нормальной паренхимы печени по периферии узла указывает на ГЦР ранней стадии. Инвазия стромы является ключевым моментом в дифференциальной диагностике ГЦР на ранней стадии и диспластических узлов высокой степени дисплазии.
(Справа) Микропрепарат: гепатоцеллюлярный узел с признаками дисплазии высокой степени определяется инфильтрация портального тракта и фиброзной перегородки на периферии узла, что является диагностическим признаком ГЦР на ранней стадии.
1. Общая характеристика:
• Ассоциированные патологические изменения:
о Цирроз печени
• Регенераторные узлы являются доброкачественными, некоторые могут прогрессировать и становиться диспластическими
• Диспластические узлы высокой степени дисплазии представляют собой предопухолевые изменения, однако процесс их злокачественной трансформации протекает достаточно медленно
2. Стадирование, градация и классификация регенераторных и диспластических узлов печени:
• Регенераторные узлы подразделяются на малые (меньше 3 мм) и большие (3 мм и больше)
• Диспластические узлы классифицируются в зависимости от степени выраженности дисплазии (низкая или высокая)
3. Макроскопические и хирургические особенности:
• Регенераторные узлы:
о Функция гепатоцитов в регенераторных узлах не нарушена, клетки Купфера имеют нормальную плотность
о Имеют округлую форму, четкие контуры, размер большинства узлов не превышает 2 см
о Множественные, с диффузным распределением по всей печени
• Диспластические узлы:
о Для ДУ высокой степени дисплазии характерна преимущественно артериальная перфузия вследствие ангиогенеза
о По мере дедифференцировки функция гепатоцитов снижается, уменьшается плотность клеток Купфера
• Перфузия регенераторных узлов и диспластических узлов низкой степени дисплазии преимущественно портальная
• В узлах отсутствуют некротические изменения, кровоизлияния, признаки локальной инвазии
4. Микроскопия:
• Ограниченная пролиферация гепатоцитов и стромы, окруженных фиброзными перегородками
• Дифференциальная диагностика регенераторных и диспластических узлов затруднительна даже на микроскопическом уровне
• Регенераторные узлы:
о Нормальная васкуляризация, интактная ретикулярная «сеть» о Сохранная архитектоника гепатоцитов
о Отсутствие митотической активности
о Увеличение числа гепатоцитов с двумя и большим количеством ядер
• Диспластические узлы:
о Нарушение архитектоники
о Атипия, сгруппированность ядер
о ДУ низкой степени дисплазии напоминают регенераторные узлы и представляют сложность в плане дифференциальной диагностики
о ДУ высокой степени дисплазии напоминают высокодифференцированный ГЦР
(Слева) На аксиальной КТ в артериальную фазу контрастного усиления у мужчины 50 лет, страдающего циррозом, визуализируется узел в правой доле печени, содержащий гиперваскулярные очаги, накапливающие контраст.
(Справа) На КТ в венозной фазе контрастного усиления у этого же пациента достоверно не определяется «вымывание» контраста из узла, однако становится видна капсула, что в данных условиях подозрительно на ГЦР. Обратите внимание на спленомегалию, варикозное расширение вен и цирротическую морфологию печени. (Слева) На аксиальной Т1 ВИ МР томограмме у этого же пациента образование имеет вид «узла в узле», при этом правая часть образования (ГЦР) выглядит гипоинтенсивной, а левая часть -гиперинтенсивной, что типично для диспластического узла.
(Справа) На аксиальной Т2 ВИ МР томограмме у этого же пациента определяется гиперинтенсивный сигнал от правой половины образования, типичный для ГЦР, и сигнал пониженной интенсивности от левой части, характерный для диспластическо -го узла. В этом случае ГЦР, дающий картину «узла в узле» развился внутри диспластического очага. (Слева) На Т1 ВИ МР томограмме в артериальную фазу контрастного усиления у этого же пациента определяется накопление контраста васкуляризованным ГЦР, и минимальное усиление диспластического узла.
(Справа) На МР томограмме в отсроченную фазу контрастного усиления у этого же пациента определяется «вымывание» контраста, визуализируется также незамкнутая капсула вокруг образования — типичные признаки ГЦР, не характерные для простых цирротических регенераторных и диспластических узлов. При исследовании резектата был подтвержден гепатоцеллюлялрный рак внутри диспластического узла.
1. Проявления:
• Другие признаки/симптомы:
о Проявления цирроза и портальной гипертензии:
- Увеличение живота, желтуха, асцит, варикозное расширение вен и др.
2. Демография:
• Возраст:
о Взрослые люди
• Пол:
о Половая предрасположенность отсутствует:
- Алкогольный цирроз печени чаще встречается у мужчин
3. Течение и прогноз:
• Уровень трансформации диспластических узлов в ГЦР относительно невысокий
• Ведение и лечение пациентов с диспластическими узлами в печени не должно быть таким же, как и у пациентов с новообразованиями
• По мере увеличения размера узла возрастает вероятность диспластических изменений высокой степени выраженности или озлокачествления:
о Высокая степень дисплазии крайне нехарактерна для узлов размером меньше 2 см
1. Советы по интерпретации изображений:
• Лучший метод визуализации - МРТ, особенно с использованием гепатобилиарного контраста (препаратов гадоксетовой кислоты-Eovist, Primovist):
о Позволяет подтвердить диагноз при наличии очага размером 3 см и больше
2. Необходимо отразить в заключении:
• Параметры плотности и интенсивности узлов в цирротически измененной печени во всех фазах контрастного усиления:
о Также необходимо оценить васкуляризацию узлов и «вымывание» контраста
Лучевая диагностика гепатоцеллюлярного рака

Гепатоцеллюлярный рак является наиболее распространённой первично злокачественной опухолью печени. Он чаще всего возникает на фоне цирроза как алкогольной, так и вирусной этиологии. ГЦР является пятым по распространённости злокачественным новообразованием в мире и третьей по частоте причиной смерти от рака (после рака лёгких и желудка). Заболеваемость ГЦР растет, что в значительной степени объясняется повышением уровня инфицированности гепатитом С.
К факторам риска относятся:
- инфицированность гепатитом B (HBV): 10% 5-летний кумулятивный риск;
- инфицированность гепатитом С (HCV): 30% 5-летний совокупный риск;
- алкоголизм: 8% 5-летний кумулятивный риск;
- билиарный цирроз: 5% 5-летний кумулятивный риск;
- врождённая атрезия желчных путей;
- контакт с некоторыми токсическими веществами (афлотоксины), а также потребление лекарственных средств (метилдофа, изониазид, цитостатики и т. д.);
- врождённые нарушения обмена веществ:
- гемохроматоз: 20% 5-летний кумулятивный риск,
- дефицит альфа-1-антитрипсина,
- дефицит галактозо-1-фосфат-уридилтрансферазы,
- болезни накопления гликогена типа 1,
- болезнь Вильсона,
- тирозинемия типа I;
ГЦР обычно диагностируется в среднем возрасте или у пожилых (в среднем 65 лет) и чаще встречается у мужчин (в 75% случаев). Однако опухоль также может встречаться в педиатрической практике; это вторая по распространённости у детей первично-злокачественная опухоль печени после гепатобластомы. Так как ГЦР чаще всего проявляется на фоне цирроза, не лишним будет описать типичную КТ/МРТ картину этого заболевания.
Общими для всех методов признаками являются:
- гетерогенность структуры по типу мелко-/крупноочаговой нодуллярности (за счёт присутствия регенераторных узлов) или септальной перестройки;
- сегментарная гипертрофия/атрофия:
- гипертрофия хвостатой доли и боковых сегментов левой доли (сегменты II и III),
- атрофия задних сегментов (VI и VII) правой доли;
При КТ:
- регенераторные узлы (большинство) изоденсны остальной ткани печени;
- сидерические узлы (меньшинство) гиперденсы вследствие накопления в них железа;
- может определяться неровность края печени;
- признаки портальной гипертензии:
- расширение портальной вены;
- портальный венозный тромбоз.
При МРТ:
- на T1 обычно изоинтенсивны, иногда слегка гиперинтенсивны, не наблюдается артериального накопления и «вымывания»;
- на T2 : обычно изоинтенсивны, гипоинтенсивные сидерические узлы;
- узлы низкой степени дисплазии будут напоминать регенераторные узлы;
- узлы высокой степени дисплазии очень схожи с высокодифференцированым ГЦР небольших размеров — отличить их бывает невозможно даже при гистологическом исследовании.
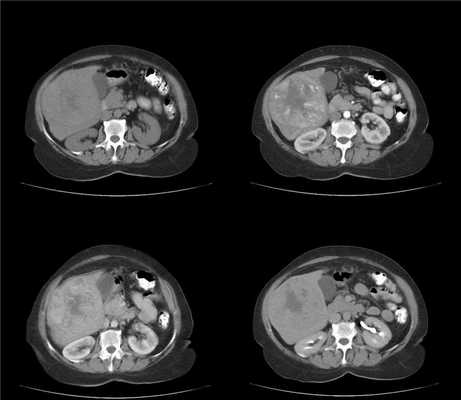
На фоне нерезко выраженых цирротических изменений в виде гетерогенности структуры и неровности контуров печени визуализуется крупное (более 2 см) образование, изоденсное в нативную фазу. В артериальную фазу оно демонстрирует гетерогенное накопление контраста (выше чем паренхима печени). Структура мозаичная, в центре образования участок пониженной плотности - вероятно, центральный некроз. Вокруг образования гиперденсный ободок, выраженый в портовенозную фазу. В отсроченной фазу образование гиподенсно по отношению к окружающей паренхиме печени.
Морфологически ГЦР может быть представлен очаговой, многоочаговой и диффузной формами. В большинстве случаев он не проявляется какими-либо симптомами на фоне уже имеющихся симптомов цирроза. Поэтому важно скрининговое наблюдение для пациентов с циррозом и гепатитами С и В — оно позволяет выявлять ГЦР на ранней стадии.
Радиологами часто используется система LI-RADS (Liver Imaging Reporting and Data System), которая содержит стандартную терминологию и специально разработана для определения рисков ГЦР и дифференциальной диагностики ГЦР с другими злокачественными образованиями (в частности, с внутрипечёночной холангиокарциномой) у пациентов с циррозом печени. В LI-RADS выделяют основные и дополнительные критерии. Основные критерии:
гиперинтенсивность (накопление) в артериальную фазу, или изо- или гипоинтенсивность в артериальную фазу;
надпороговое увеличение диаметра.
Как их правильно определять?
Накопление контрастного вещества в артериальную фазу подразумевает, что образование в артериальную фазу контрастирования становится гиперденсным (КТ) или гиперинтенсивным (МРТ) по отношению к остальной паренхиме печени в эту же фазу. Если образование в артериальную фазу становится гиперинтенсивным по сравнению с тем же образованием в нативную фазу, это не считается накоплением. Накопление контрастного вещества отслеживают в позднюю артериальную фазу, т.е. когда контрастирована брюшная аорта, ветви печёночной артерии и ветви портальной вены; ветви печёночной вены не контрастированы. Трудности с измерением диаметра могут возникнуть, если образование мозаичной структуры, структуры «узел-в-узле» или «узлы-в-узле», и при наличии «капсулы».
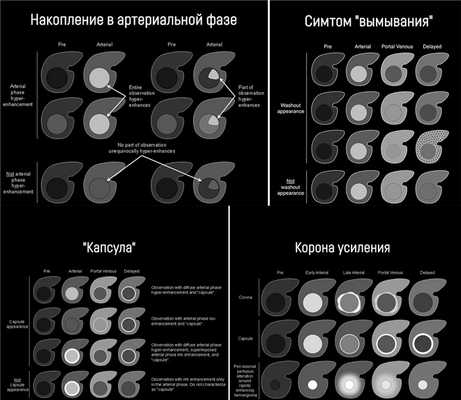
Симптом «вымывания» означает, что в портовенозную (во время наиболее выраженного контрастирования портальной вены; пикового контрастного накопления паренхимой печени и начального контрастирования ветвей печёночной вены) или отсроченную (в которой умеренно контрастированы вены печени и её паренхима) фазы образование становится гипоинтенсивным на фоне окружающей паренхимы печени. Здесь действует то же правило: если образование стало менее интенсивно по сравнению с собой в артериальную фазу, но не по отношению к паренхиме — это не симптом «вымывания».
Если образование накопило контраст в артериальную фазу, а в более поздние фазы выглядит изоинтенсивно паренхиме печени, это называют симтомом «выцветания» (fade). Термин «капсула» при визуализации соотносится с наличием как капсулы, так и псевдокапсулы у опухоли. «Капсула» визуализируется как ровный гладкий ободок по периферии образования, который усиливается в портовенозной или отсроченной фазе и является более толстым или более заметным, чем у ободки фоновых цирротических узелков.
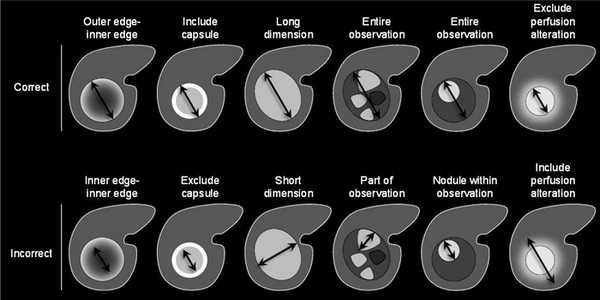
Надпороговое увеличение диаметра означает:
увеличение диаметра ≥50% менее чем за 6 месяцев,
увеличение ≥100% более чем за 6 месяцев,
появление нового образования размером 10 мм и более,
критерий увеличения выше пороговых значений не применим к диффузному поражению,
при сравнении измерения должны проводиться в одинаковых последовательностях/фазах, например, сравнивать Т2 только с другим Т2.
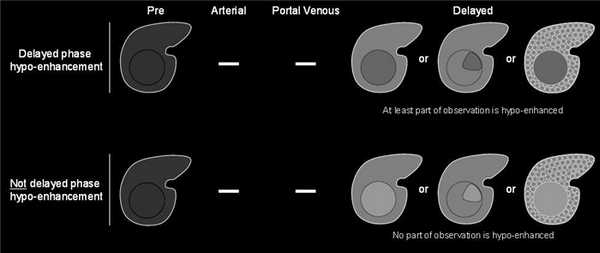
указывающие на ГЦР:
- умеренная гиперинтенсивность на Т2,
- на диффузно-взвешенных изображениях гипоинтенсивность при низких и высоких значениях b-value, гипоинтенсивность на картах ИКД (истинного коэффициента диффузии),
- корона усиления,
- мозаичная структура,
- структура «узла-в-узле»,
- признаки жирового отложения в образовании,
- признаки отложения железа менее выражены в образовании,
- признаки жирового гепатоза менее выражены в образовании,
- признаки кровотечения,
- увеличение диаметра образования, но меньше пороговых значений;
указывающие на доброкачественное образование:
- выраженная гомогенная гиперинтенсивность в Т2,
- выраженная гомогенная гипоинтенсивность в T2 или T2,
- неизменённые сосуды печени,
- образование накапливает контраст параллельно остальной паренхиме печени,
- уменьшение диаметра образования,
- стабильность диаметра на протяжении двух лет и более.
Корона усиления (corona enhancement) обозначает чаще усиление неровных, нечётких контуров вокруг образования, которое проявляется в позднюю артериальную фазу и становится изоденсным в портовенозную или отсроченную фазу. Этот симптом считается отображением раннего вымывания контрастного вещества из образования. Его редко наблюдают во время обычного четырёхфазного сканирования, чаще — при серии сканов в артериальную фазу. Если ободок усиления остается гиперинтенсивным в поздние фазы, его считают капсулой. Корону усиления при ГЦР следует дифференцировать с нарушением перфузии, асоциированном с быстро накапливающей контраст гемангиомой. Если КТ/МРТ картина более типична для гемангиомы, этот симптом не учитывается.
Система классификации
Основные критерии часто приводят непосредственно к присвоению балльной оценки LI-RADS. Если остаются сомнения,картину могут прояснить дополнительные критерии.

Дополнительные критерии, указывающие на ГЦР, могут быть использованы для повышения степени на одну или несколько LR-категорий, но не для присвоения LR5 категории. Это правило введено для того, чтобы сохранить соответствие между классификациями LI-RADS и OPTN (Organ Procurement and Transplantation Network). С помощью дополнительных критериев, указывающих на доброкачественный процесс, можно понизить степень на одну и больше категорий от LR5 до LR1. Эти критерии радиолог использует на свое усмотрение, исходя из общей лучевой и клинической картин.
Категории LI-RADS включают в себя: LR1-LR5, LR5V («опухоль-в-вене»), LR5 TREATED (после лечения) и LR OM (другое злокачественное образование). LR1 (100% вероятность доброкачественного образования) ставится, когда радиолог видит картину, типичную для (например):
сливного фиброза печени;
или другого доброкачественного образования.
Категория LR1 не включает в себя такие доброкачественные образования как фокальная нодуллярная гиперплазия (из-за сложностей её дифференциальной диагностики с ГЦР) и гепатоцелюлярная аденома (так как она крайне редко встречается при циррозе). Образование, которое редуцировалось само по себе в отсутствии лечения, тоже определяется как LR1.
К категории LR2 (вероятно доброкачественное) относятся образования, имеющие несколько нетипичный для доброкачественных вид, но все же не выглядящие злокачественными, например киста с перегородкой. Также категория LR2 присваивается цирроз-ассоциированным узлам печени, которые отвечают всем следующим критериям:
Изоинтенсивный другим фоновым узелкам во всех фазах.
Отличается от фоновых узелов по одному или нескольким из признаков:
отчетливо больше, чем другие фоновые узелки;
умеренно гиперденсны на КТ;
умеренно гиперинтенсивны на Т1;
умеренно гипоинтенсивны на Т2 или Т2* или умеренно или выраженно гиперинтенсивны на T2 или T2.
Узелки, которые не соответствуют всем этим критериям, классифицируются как LR3 или выше.
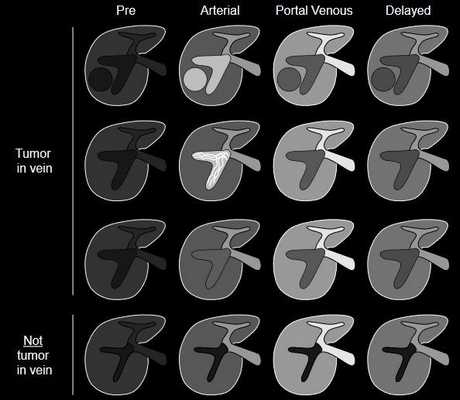
Категория LR5V используется для образования, проросшего в просвет вены. Радиологически оно проявляется как (см. схему):
Оклюзия и расширение вены, гипер- изо- или гиподенсное в артериальную фазу;
Гипо- или изоденсное в портовенозную и отсроченную;
Может присутствовать мягкотканное образование, ассоциированное с окклюзией, но его присутствие необязательно;
Могут определяться гиперденсные полосы в артериальную фазу (симптом “thread-and-streak”).
Опухолевую инвазию следует отличать от не-опухолевого тромбоза, при котором вена не будет выглядеть расширенной и не будет демонстрировать контрастного накопления ни в одну из фаз.
Категория LR5TREATED присваивают в случае:
Подтвержденного ГЦР после эмболизации или абляции, вне зависимости от успешности лечения;
Категория LR5TRAETED не присваивается:
Образованиям категории LR4 и ниже после эмболизации или абляции;
Подтвержденному ГЦР после системной терапии или
Категория OM и дифференциальная диагностика
ГЦР – наиболее распространенное злокачественное образование, возникающее на фоне цирроза. Однако, выявленные изменения следует дифференцировать со следующими злокачественными образованиями:
Посттранплантационная лимфопролиферативная болезнь.
Факторы риска развития холангиокарциномы мало отличаются от таковых для ГЦР. Биохимические маркеры ХГЦ: СА 19-9 (углеводный антиген 19-9) и CEA (карциноидоэмбриональный антиген). При визуализации для ХГЦ характерны:
Только кольцевидное усиление в артериальную фазу;
Усиление в портовенозную и отсроченную фазы;
Нерезко выраженные рестриктивные изменения в DWI;
«Втяжение» ткани печени к образованию;
Билиарная обструкция, при чем степень обструкции не соответствует размерам образования.
Первичные лимфомы печени крайне редки. Чаще встречаются вторичные поражения при системном процессе. Следует помнить, что лимфомы чаще возникают на фоне иммуносупрессии. Увеличение абдоминальных лимфоузлов может навести на правильный диагноз.
Посттранплантационная лимфопролиферативная болезнь – одно из наиболее частых злокачественных новообразований у пациентов с трансплантацией в анамнезе. Ее развитие ассоциировано с иммуносупрессией и инфицированием вирусом Эпштейн-Барра. Печень – наиболее частая локализация экстранодального поражения. Метастазы редко встречаются на фоне цирротического изменения. Необходимо указать первичную опухоль. При визуализации более вероятны следующие признаки:
Усиление в портовенозную/отсроченную фазы;
Частичное или кольцевидное усиление в артериальную фазу;
Центральный некроз или ишемия;
Нерезко выраженные рестриктивные изменения в DWI.
В зависимости от присвоенной категории, ACR рекомендовано:
LR1: продолжать скрининг в обычном режиме;
LR2: продолжать скрининг в обычном режиме;
LR3: тщательное наблюдение: отслеживать изменения размера, стабильности и клинических проявлений;
LR4: тщательное наблюдение, дополнительная визуализация, биопсия или лечение;
LR5: лечение без биопсии, радиологическое ТNM-стадирование.
Применяя LI-RADS в МРТ, следует помнить, что эта классификация разработана для использования внутриклеточных гадолиний-содержащих контрастных веществ (например, Гадавист). Использование гепатобилиарного контраста (Эовист, Примовист) изменит интерпретацию МРТ-картины.
Ведение пациентов выявленными объемными поражениями на фоне цирроза
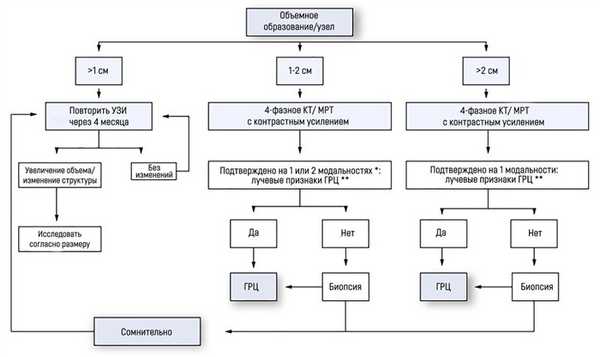
Гайдлайны EASL–EORTC (European Association for the Study of the Liver – European Organisation for Research and Treatment of Cancer) рекомендуют следующую тактику в случае, если УЗИ выявило очаговое поражение у пациента с циррозом:
если найденный узел менее 1 см диаметром, наблюдение каждые 4 месяца на протяжении первого года; затем – каждые 6 месяцев;
при узле 1-2 см диаметром диагноз базируется на неинвазивных методах визуализации или данных биопсии. Если последние оказались неубедительны или паттерн контрастного накопления при КТ/МРТ изменился за время исследования, рекомендована вторая биопсия;
при узле более 2 см диаметром диагностика должна базироваться на неинвазивных методах. Биопсия проводится в случае неубедительных или нетипичных данных КТ/МРТ.
EASL–EORTC называет типичные паттерны, наличия которых при визуализации достаточно для постановки диагноза: образование гиперваскулярно в артериальную фазу и демонстрирует симптом «вымывания» в портовенозную и/или отсроченную фазы. УЗИ с контрастным усилением не рекомендовано для диагностики ГЦР из-за иных характеристик контрастных веществ – они не покидают сосудистое русло. Определение уровня альфа-фетопротеина было исключено из протокола диагностики, так как он редко возрастает на ранней стадии ГЦР.
Источники
Читайте также:
