Маточно - плацентарное кровообращение.
Добавил пользователь Alex Обновлено: 27.01.2026
Допплерометрия (синоним, допплерография) фето-плацентарного кровотока – это исследование состояния кровотока в системе «мать-плацента-плод», которое проводят во время ультразвукового исследования при беременности.
Результаты допплерографии позволяют судить о состоянии маточно–плацентарно–плодового кровотока и косвенно свидетельствуют о внутриутробном состоянии ребенка.
Физический эффект, применяемый в современной медицине для измерения скорости кровотока, открыл в 1842 году Христиан Иоганн Доплер, профессор математики и геометрии. Широкое распространение допплерометрия в акшерстве получила с середины 80 годов 20 века. Наиболее часто применяемые доплеровские методики при сканировании во время беременности следующие: импульсный, цветной (цветовой), энергетический допплеры.
Импульсный допплер.
Сущность эффекта Доплера сводится к тому, что при отражении ультразвуковых волн от движущихся объектов (в нашем случае такими объектами являются кровяные клетки, движущиеся по сосудам) изменяются физические свойства волны. Разница между частотой отраженных и испускаемых ультразвуковых импульсов называется доплеровским сдвигом. Скорость кровотока рассчитывается по математической формуле на основании доплеровского сдвига и затем отмечается светящейся точкой на мониторе. Совокупность этих точек образует рисунок на экране ультразвукового аппарата, который называется кривой скорости кровотока. Кроме того, при проведении допплерометрии слышны звуковые сигналы, которые помогают врачу различать в нужном ли сосуде проводится измерение. Кривую скорости кровотока врач оценивает визуально, а так же, отмечая определенные участки, проводит расчет специальных индексов. Эти индексы называются индексами сосудистого сопротивления и характеризуют состояние кровотока в исследуемом сосуде. Вообще показателей, характеризующих кровоток в сосуде, может быть много, но наиболее популярными в акушерском ультразвуке индексами являются ИР (индекс резистентности), ПИ (пульсационный индекс) и СДО (систало-диастолическое отношение). Значения полученных индексов сопротивления сравниваются с нормативными и, исходя из этого формулируется заключение по состоянию кровотока в сосуде.
Цветной допплер.
Эта методика основана на применении того же частотного сдвига, только после преобразования сигналов на экране монитора появляется изображение сосудов, обычно красного и синего цвета. С помощью этой методики нельзя определить расчетные индексы, но можно охарактеризовать особенности кровотока в органе, проследить ход сосудов.
Часто цветной и импульсный допплер используются в комбинации – цветной для нахождения сосуда, импульсный для оценки скорости кровотока в нем.
При ультразвуковом исследовании во время беременности режим цветного допплера используется очень часто. Так такие опасные состояния как предлежание сосудов плаценты к шейке матки, истинный узел пуповины, многократное обвитие пуповины вокруг шеи плода, рак шейки матки можно диагностировать с помощью этой методики. Кроме этого, цветной допплер применяется при каждом исследовании сердца плода и помогает обнаружить пороки сердца.
Энергетический допплер.
Еще одна из методик оценки кровоснабжения изучаемого объекта. Изменение амплитудных характеристик волны преображается в аппарате и на мониторе видны сосуды обычно оранжевого цвета. Эта методика в акушерстве применяется не часто.
Показания для проведения допплерометрии.
Основными показаниями для оценки кровотока в системе мать-плацента-плод являются:
1.Заболевания матери:
- гестоз, артериальная гипертензия,
- заболевания почек,
- коллагенозы,
- антифосфолипидный синдром и другие аутоиммунные состояния
- врожденные тромбофилии
- сахарный диабет
2.Заболевания плода, плаценты, пуповины:
- отставание в размерах
- маловодие,многоводие
- многоплодная беременность
- нарушение созревания плаценты
- неименная водянка, пороки развития плода, аномалии пуповины, хромосомные аномалии плода
- патологические типы КТГ
- пороки развития и подозрение на хромосомную патологию
3.Отягощённый акушерский анамнез (ЗВРП, гестоз, мертворождения при предыдущих беременностях).
Оценка кровотока в бассейне плаценты.
Оценка плацентарного кровотока включает в себя измерение индексов сопротивления в артерии пуповины и в обеих маточных артериях. Нарушение кровотока в пуповине свидетельствует о неполадках в плодовой части плаценты. Нарушение кровотока в маточных артериях говорит о сбое в работе маточной части плаценты. Необходимо знать, что нормальные показатели кровотока служат достаточно достоверным признаком нормального внутриутробного состояния плода, но полностью не исключают развития определенных осложнений; наличие нарушений кровотока в разных отделах маточно-плацентарно-плодовой системы требует строгого динамического контроля и лечения, в том числе в условиях стационара.
Оценка кровообращения плода.
Гемодинамика малыша обычно оценивается при исследовании кровотока в мозговых сосудах (средняя мозговая артерия), аорте, венозном протоке, сердце.
Классификация нарушений маточно-плацентаро-плодового кровотока.
Наиболее часто применяемая, простая и удобная классификация нарушений плацентарного кровотока изложена ниже.
1 степень
А.Нарушение маточно-плацентарного кровотока при сохранении плодово-плацентарного ( повышены индексы сопротивления в маточных артериях)
Б.Нарушение плодово-плацентарного кровотока при сохранении маточно-плацентарного (повышены индексы сопротивления в артерии пуповины)
2 степень
Одновременное нарушение маточно-плацентарного и плодово-плацентарного кровотока (повышены индексы сопротивления в артерии пуповиныи в маточных артериях)
3 степень
Критическое нарушение плодово-плацентарного кровотока (нарушение кровотока в пуповине) - отсутствует диастолический кровоток в артерии пуповины или даже появляется реверсный (обратный) кровоток.
Проведя оценку кровотока в сосудах плаценты и плода, врач делает соответствующие выводы и формулирует заключение. На основании этого заключения и результатах других методик обследования выбирается тактика ведения беременности.
Необходимо помнить:
* Допплерометрия – это дополнительная методика, которая применяется после проведения ультразвукового исследования.
* Показания к проведению допплерометрии определяет врач. Без показаний такое исследование проводить не стоит.
* Частоту проведения допплерометрии определяет врач. Иногда требуется ежедневный контроль за состоянием кровотока мать-плод
* Нормальные результаты при допплерометрии не отменяют результатов других исследований и не гарантируют отсутствие внутриутробного страдания плода.
Допплерометрия при беременности
Это ультразвуковое исследование, при котором оцениваются параметры кровообращение плода, плаценты, матки и маточных артерий. Допплерометрия помогает определить, как малыш себя чувствует, достаточно ли он получает кислорода. Нарушения в маточно-плацентарном или фетоплацентарном кровотоке приводят к дефициту кровоснабжения плода, что, в свою очередь, может вызвать задержку его развития, внутриутробную гипоксию, осложнения в родах и другие патологические состояния.
Допплеровское картирование на экспертных аппаратах УЗИ в клинике «Геном-Калининград» позволяет получать изображение в полном цвете. При этом можно увидеть гемодинамику матери и плода, оценить состояние пуповины. Инновационное оборудование, опыт и квалификация врача высшей категории обеспечивают максимальную точность результатов диагностики.
Маточно-плацентарный кровоток представлен маточными артериями, которые приносят кровь к плаценте.
Фетоплацентарный кровоток представлен сосудами плаценты, из которых кровь через пуповину поступает непосредственно к плоду.
Таким образом, через плаценту обогащённая кислородом и питательными веществами кровь поступает к плоду, а потом обратно уходит в кровоток матери, насыщенная углекислым газом и продуктами обмена веществ. Далее уже из материнского организма эти вещества выводятся наружу органами выделительной системы.
Допплерометрия выявляет:
- различные расстройства кровообращения в системе мать-плацента-плод. Основное из них – плацентарная недостаточность и обусловленная ею задержка развития плода. Поэтому, прямым показанием для допплер-УЗИ при беременности является несоответствие размеров тела или органов ребенка нормам на данном этапе беременности.
- различные расстройства кровообращения у плода (пороки сердца, гипоксия) и осложнения беременности. Сегодня общепризнано, что причиной токсикозов, гестозов и др. акушерских проблем является нарушение кровотока в маточных артериях и сосудах плаценты.
Допплерометрия оценивает и правильность строения сердца плода. При этом исключается или подтверждается дефект межжелудочковой перегородки. Будущая мама может услышать сердцебиение малыша.
Допплерография несколько раз проводится, если у женщины диагностировали беременность однояйцевой двойней. Это помогает исключить ситуацию, при которой один малыш получает больше притока крови, чем второй (так называемый фето-фетальный трансфузионный синдром).
Допплерография – это та же допплерометрия, только дополнительно ещё ведётся запись показаний на ленте, чтобы проследить за изменением (улучшением/ухудшением) кровотока после проведённого лечения. При доплерометрии врач оценивает кровоток с монитора.
Допплерометрия проводится при плановых УЗИ беременности. Исследование может быть назначено вне плановых сроков в следующих случаях:
- наличие у беременной заболеваний (проблемы с почками, сахарный диабет, повышенное артериальное давление);
- акушерские осложнения беременности (гестоз, маловодие, преждевременное созревание плаценты, резус-конфликт, приращение плаценты, единственная артерия пуповины, аномалии сосудов, пузырный занос);
- патология плода (задержка внутриутробного развития плода, дистресс плода, несоответствие размеров плода сроку беременности);
13 – 14 недель - позволяет прогнозировать дальнейшее течение беременности и риск развития осложнений.
19 – 22 недели - позволяет выявлять осложнения беременности со стороны матери и плода, диагностировать задержку его развития, гипоксию и проч.
30 – 34 недели дает возможность предсказать исход беременности. Если показатели допплерометрии в конце беременности не соответствуют норме, то говорят о риске преждевременных родов, рождения малыша с низкой массой тела.
Маточно - плацентарное кровообращение.
Кафедра акушерства и гинекологии
Кафедра акушерства и гинекологии
Кафедра нормальной физиологии
Кабинет перинатальной диагностики Клиники государственного бюджетного образовательного учреждения высшего профессионального образования "Южно-Уральский государственный медицинский университет" Минздрава РФ, Челябинск
Особенности маточно-плацентарного кровообращения в ранние сроки беременности, осложнившейся при дальнейшем течении преэклампсией
Журнал: Российский вестник акушера-гинеколога. 2014;14(2): 52‑56
Медведев Б.И., Сюндюкова Е.Г., Сашенков С.Л., Кирсанов М.С. Особенности маточно-плацентарного кровообращения в ранние сроки беременности, осложнившейся при дальнейшем течении преэклампсией. Российский вестник акушера-гинеколога. 2014;14(2):52‑56.
Medvedev BI, Siundiukova EG, Sashenkov SL, Kirsanov MS. Maternal-placental circulation in early pregnancy complicated by further preeclampsia. Russian Bulletin of Obstetrician-Gynecologist. 2014;14(2):52‑56. (In Russ.).
Кафедра акушерства и гинекологии
Цель исследования - изучение особенностей маточно-плацентарного кровообращения в ранние сроки беременности, осложнившейся при дальнейшем течении преэклампсией. Материал и методы. Обследованы 74 женщины с неосложненной беременностью, 50 беременных с умеренной и 3 пациентки с тяжелой преэклампсией. В сроки беременности 11-14 нед у этих пациенток изучены допплерометрические показатели кровотока в маточных артериях (систолодиастолическое отношение и индекс резистентности). Проанализированы особенности течения беременности и исходы родов. Результаты. Выявлено повышение индексов периферического сосудистого сопротивления в маточных артериях в сроки 11-14 нед гестации у пациенток, течение беременности у которых в последующем осложнилось преэклампсией. Установлены положительные корреляционные связи показателей систолодиастолического отношения и индекса резистентности в маточных артериях в сроки гестации 11-14 нед с числом случаев развития преэклампсии, плацентарной недостаточности с задержкой развития плода, гипотрофии и асфиксии новорожденного. Заключение. Полученные данные свидетельствуют о возможности использования этих показателей в качестве прогностических факторов указанных акушерских осложнений.
Кафедра акушерства и гинекологии
Кафедра акушерства и гинекологии
Кафедра нормальной физиологии
Кабинет перинатальной диагностики Клиники государственного бюджетного образовательного учреждения высшего профессионального образования "Южно-Уральский государственный медицинский университет" Минздрава РФ, Челябинск
Преэклампсия (ПЭ) остается одной из важнейших причин материнской и перинатальной смертности во всем мире. В настоящее время известно более 30 теорий развития ПЭ. Согласно наиболее признанной гипотезе, причиной ПЭ является нарушение процессов формирования плаценты в самые ранние сроки гестации. При этом нарушение ремоделирования спиральных артерий рассматривается как ранний, но не всегда первичный дефект, вызывающий развитие ПЭ [2, 4, 7, 13]. Вследствие аномальной плацентации и нарушения перфузии в плаценте высвобождаются факторы, вызывающие распространенную дисфункцию эндотелия и синдром системного воспалительного ответа (ССВО), приводящие к полиорганной недостаточности [2, 4, 11]. Таким образом, формирование ПЭ происходит в ранние сроки беременности: ряд предрасполагающих факторов приводит к нарушению инвазии трофобласта, развитию недостаточности маточно-плацентарного кровотока и ишемии плаценты [2, 7, 9].
В настоящее время в акушерстве развивается весьма перспективное направление поиска ранних (I триместр) маркеров, помогающих своевременно прогнозировать развитие ПЭ. В комбинации тестов для оценки степени риска развития ПЭ изучаются начальные этапы маточно-плацентарного кровотока с использованием методики ультразвуковой допплерометрии в маточных артериях [2, 4, 7, 8, 10], которая, по мнению большинства исследователей, наиболее оправдана в сроки 11-14 нед [6]. На протяжении I триместра гестации становление маточного кровотока характеризуется постепенным возрастанием периферического сосудистого сопротивления в маточных артериях до 9 нед с последующим его снижением по мере увеличения срока беременности за счет физиологической гестационной перестройки эндометриальных сегментов спиральных артерий, вызванных инвазией трофобласта [3, 6, 8]. По нашему мнению, установление возможных ранних предикторов развития и нарастания тяжести ПЭ имеет большое клиническое значение.
Цель настоящего исследования - изучение особенностей маточно-плацентарного кровообращения в ранние сроки беременности, осложнившейся при дальнейшем течении ПЭ.
Материал и методы
Нами проведено проспективное исследование у 127 беременных, которые состояли на диспансерном учете в женской консультации Клиники Южно-Уральского государственного медицинского университета Минздрава России. Изучены особенности течения беременности и исходы родов. Критериями включения беременных в исследование явились срок гестации 11-14 нед, отсутствие противопоказаний к беременности, согласие женщины на участие в исследовании. Критерии исключения: срок гестации 15 нед и более, онкологические заболевания, ВИЧ-инфекция, туберкулез, тяжелая соматическая патология, психические заболевания, хронический алкоголизм, наркомания. План исследования соответствует законодательству РФ, международным этическим нормам и нормативным документам исследовательских организаций, а также одобрен этическим комитетом Южно-Уральского государственного медицинского университета Минздрава РФ.
В зависимости от наличия или отсутствия гестационного осложнения - ПЭ и степени ее тяжести [4] выделены группы: 1-я группа (контрольная) - 74 женщины, течение беременности у которых не осложнилось развитием ПЭ; 2-я группа - 50 беременных с умеренной ПЭ; 3-я группа - 3 пациентки с тяжелой ПЭ. Средний возраст женщин 1-й группы составил 27,0±0,8 года, 2-й - 26,3±0,8 года, 3-й - 24,3±2,4 года.
Морфометрические характеристики фетоплацентарного комплекса, допплерометрические параметры кровотока оценивались с помощью диагностических ультразвуковых систем. Кардиомониторирование проводилось с использованием монитора акушерского компьютерного МАК-02-«Ч» «Кроха» с автоматическим анализом по шкалам Fisher, Figo и по показателю КВВ (короткие временные вариации). В сроке 11-14 нед гестации проводилась оценка кривых скоростей кровотока (КСК) в правой и левой маточных артериях методом допплерометрии, использовались систолодиастолическое отношение (СДО - отношение максимальной систолической скорости к конечной диастолической скорости кровотока) и индекс резистентности (ИР - соотношение разности максимальной систолической и конечной диастолической скоростей кровотока к максимальной систолической скорости кровотока). Полученные результаты исследования (СДО и ИР в правой и левой маточных артериях) сгруппированы по максимальному (СДО max и ИР max ) и минимальному (СДО min и ИР min ) числовому значению «уголнезависимых индексов». Гемодинамические нарушения в системе мать-плацента-плод выявлялись во II (с 18 нед гестации) и III триместрах при оценке кривых скоростей кровотока в маточных артериях и артерии пуповины (А.Н. Стрижаков, 1989). С помощью ультразвуковой фетометрии устанавливался диагноз синдрома задержки развития плода (СЗРП), его форма и степень. Оценка физического развития новорожденных проводилась с помощью оценочных таблиц перцентильного типа Г.М. Дементьевой (1984). Состояние новорожденных при рождении оценивалось по шкале Апгар.
Все статистические расчеты были выполнены с помощью пакетов программ: SPSS 12.1, Statistica for Windows 6.0, STADIA 6.3 prof. Для оценки различий между группами обследуемых применен аппарат проверки статистических гипотез с использованием определения критериев Манна-Уитни, &khgr; 2 Пирсона, отношения правдоподобия, линейно-линейной связи, коэффициента сопряженности, симметричная мера, интервальная по интервальной - R Пирсона, корреляции Спирмена при уровне значимости критерия 0,05. Для выявления степени корреляционной зависимости между показателями использовался непараметрический корреляционный анализ с расчетом коэффициента непараметрической корреляции Спирмена.
Результаты и обсуждение
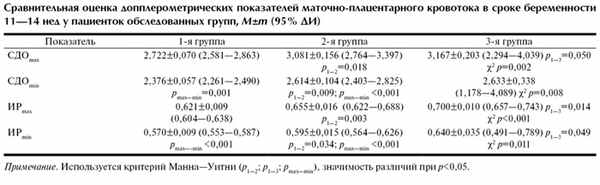
В сроке гестации 11-14 нед проведена допплерометрическая оценка кровообращения в маточных артериях, результаты исследования представлены в таблице. Установлено, что показатели СДО max и СДО min у пациенток, течение беременности у которых в последующем осложнилось ПЭ, оказались достоверно выше, чем в контрольной группе. Установлено, что значения СДО max и СДО min имели достоверные отличия в группе женщин, беременность которых осложнилась умеренной ПЭ, а также в контрольной группе.
Показатели ИР max и ИР min у пациенток 2-й и 3-й групп оказались достоверно выше, чем в контрольной группе. Установлена тенденция к увеличению ИР при нарастании тяжести ПЭ. Выявлены статистически значимые различия между показателями ИР max и ИР min у беременных контрольной группы и женщин с ПЭ умеренной степени.
Таким образом, в результате нашего исследования установлено наличие особенностей кровообращения в маточных артериях уже на ранних этапах гестации (11-14 нед) у пациенток, течение беременности у которых в последующем осложнилось ПЭ умеренной и тяжелой степени; достоверных различий показателей допплерометрического исследования маточного кровотока у беременных с разной степенью тяжести ПЭ мы не выявили, что, возможно, связано с малым количеством выборки в 3-й группе. Такие изменения, вероятно, связаны с нарушением ремоделирования спиральных артерий и инвазии трофобласта на ранних этапах формирования плацентарного комплекса. Это предположение подтверждают результаты исследования Л.А. Агарковой и соавт. [1], которые установили, что повышение индексов периферического сосудистого сопротивления (ИР, пульсационного индекса) в сроки 10-12 нед гестации сочеталось с наличием в гистологической картине незрелых децидуальных клеток, диссоциированного развития котиледонов, отложением солей кальция в межворсинчатом пространстве, ранним приближением фетальных сосудов к покровному эпителию ворсин, наличием в просвете ворсинковых сосудов незрелых форм эритроцитов. Несомненно, это приводит к нарушению перфузии крови в плаценте, развитию гипоксии, запуску ССВО с тотальным повреждением эндотелия сосудов и развитием плацентарной недостаточности с СЗРП и ПЭ [2, 4, 7, 9, 11, 13].
Во II триместре при допплерометрическом исследовании кровотока в маточных артериях и артерии пуповины установлено, что при ПЭ (2-я группа - 8%; 3-я группа - 1 пациентка) чаще, чем в контрольной группе (2,7%), была диагностирована субкомпенсированная форма хронической плацентарной недостаточности (ХПН) (нарушение маточно-плацентарно-плодового кровотока - НМПК - 1А и 1Б степеней), частота выявления увеличивалась при нарастании тяжести ПЭ (критерий Манна-Уитни р 1-3 =0,008; &khgr; 2 Пирсона р=0,046; линейно-линейная связь р=0,020; коэффициент сопряженности р=0,046; R Пирсона р=0,020).
Мы изучили корреляционные связи допплерометрических показателей маточного кровотока в сроке 11-14 нед с частотой и тяжестью НМПК во II и III триместрах гестации и установили следующее:
- показатель СДО max положительно коррелирует с числом случаев НМПК во II (r=0,304; р=0,002) и III (r=0,415; р<0,001) триместрах, НМПК 1А (r=0,193; р= 0,047) и НМПК 1Б (r=0,281; р=0,003) в III триместре;
- показатель СДО min положительно коррелирует с числом НМПК во II (r=0,242; р=0,012) и III (r=0,328; р=0,001) триместрах, НМПК 1Б степени (r=0,201; р=0,039) в III триместре;
Установлено, что при увеличении допплерометрических показателей маточного кровотока (СДО и ИР) в сроке 11-14 нед нарастает число случаев НМПК во II и III триместрах гестации. Таким образом, данные показатели могут быть использованы как прогностические критерии формирования нарушения кровотока в системе мать-плацента-плод во II и III триместрах беременности. В настоящее время остается нерешенным вопрос выбора индекса для оценки состояния периферического сопротивления (СДО, ИР, пульсационный индекс). В результате исследования мы не выявили принципиальных преимуществ в выборе показателя СДО и ИР, однако отмечена большая практическая эффективность использования максимальных числовых значений «уголнезависимых индексов» (СДО max и ИР max ) в сравнении с минимальными (СДО min и ИР min ).
Несомненно, отрицательное влияние на состояние новорожденного оказывают осложнения гестации, возникающие у беременных с ПЭ - суб- и декомпенсированная ХПН с СЗРП, невынашивание, анемия [4, 9]. Для всех этих видов патологии описаны однотипные изменения, характерные для ССВО: активация свободнорадикального окисления, цитокиновый каскад, системная васкулопатия, коагулопатия [2, 7, 9, 12]. С целью оценки физического развития новорожденных использованы оценочные таблицы перцентильного типа Г.М. Дементьевой (1984). Масса новорожденных, родившихся у матерей с ПЭ тяжелой степени, соответствовала перцентилю 12,67±6,48, что было достоверно (критерий Манна-Уитни р 1-3 =0,004, р 2-3 =0,011) меньше по сравнению с этим показателем в 1-й и 2-й группах (59,22±2,59 и 54,42±3,99 соответственно). Число гипотрофичных детей, родившихся у матерей с умеренной ПЭ (18%), оказалось достоверно больше, чем в контрольной группе (6,8%). Установлены достоверные различия по частоте асфиксии новорожденных, у матерей которых была ПЭ, тяжесть асфиксии увеличивалась при ПЭ тяжелой степени (критерий Манна-Уитни р 1-3 р 1-3 рр=0,020; линейно-линейная связь рррр=0,049). Дети, рожденные женщинами с тяжелой ПЭ, достоверно чаще по сравнению с остальными новорожденными имели такие серьезные осложнения течения неонатального периода, как респираторный дистресс-синдром, дыхательная недостаточность, ателектазы легких, внутриутробное инфицирование (ВУИ) новорожденного, что потребовало реанимационных мероприятий с использованием искусственной вентиляции легких. Полученные результаты, несомненно, связаны не только с тяжестью ПЭ у матерей, но и с недоношенностью их новорожденных. Действительно, число преждевременных родов было наибольшим в группе пациенток с тяжелой ПЭ по сравнению с таковым в 1-й (2,7%) и 2-й (4%) группах (&khgr; 2 Пирсона рр=0,009; линейно-линейная связь р=0,001; коэффициент сопряженности рр<0,001).
Мы изучили корреляционные связи показателей допплерометрического исследования маточного кровотока в сроке 11-14 нед с акушерскими осложнениями и установили следующее:
- показатель СДО min положительно коррелирует с частотой развития ПЭ в III триместре (r=0,250; р=0,011); субкомпенсированной формы ХПН - во II (r=0,242; р=0,012) и III (r=0,328; р=0,001) триместрах; СЗРП - в III триместре (r=0,192; р=0,049);
- показатель ИР max положительно коррелирует с частотой развития ПЭ во II (r=0,235; р=0,017) и III (r=0,299; р=0,002) триместрах гестации; ХПН - в III триместре (r=0,270; р=0,005); субкомпенсированной формы ХПН - во II (r=0,294; р=0,002) и III (r=0,418; р<0,001) триместрах; СЗРП - в III триместре (r=0,258; р=0,008), в том числе с СЗРП I степени (r=0,199; р=0,041); гипотрофии новорожденного (r=0,259; р=0,008); асфиксии новорожденного (r=0,237; р=0,016);
- показатель ИР min положительно коррелирует с частотой развития ПЭ в III триместре (r=0,234; р=0,018); субкомпенсированной формы ХПН - во II (r=0,298; р=0,002) и III (r=0,388; р<0,001) триместрах; СЗРП - в III триместре (r=0,199; р=0,041).
Таким образом, при анализе кривых скоростей кровотока в маточных артериях методом допплерометрии в сроке 11-14 нед установлено, что при повышении резистентности маточных артерий увеличивается частота развития ПЭ, субкомпенсированной ХПН, СЗРП, нарушений морфофункциональных показателей новорожденных. Мы не выявили корреляций между величиной значений «уголнезависимых индексов» в маточных артериях и степенью тяжести ПЭ.
Результаты нашего исследования совпадают с данными других авторов. А.Н. Стрижаков (1990) сообщает о четкой зависимости между характером кровотока в маточной артерии и выраженностью клинической картины ПЭ. По данным М.В. Медведева (1991), выявление патологического снижения диастолического кровотока в маточной артерии на 4-16-й неделе предшествует появлению клинических симптомов ПЭ. Т.А. Духина [3] показала, что при различных осложнениях беременности и экстрагенитальных заболеваниях наблюдаются нарушения латерализации кровотока, увеличение индекса пульсации в маточной артерии на стороне прикрепления плаценты, выраженная асимметрия (более 40%) кровотока в правой и левой маточных артериях, монотонное снижение периферического сосудистого сопротивления с увеличением срока беременности. О.В. Коновалова [5] установила, что в группе пациенток высокого риска развития тяжелых форм гестоза прогностически значимыми являются следующие показатели нарушения плацентации: изменение показателей кровотока в маточных артериях (пульсационный индекс >2,25) и РАРР-А [*]
Таким образом, внедрение допплерометрической оценки маточного кровотока в сроке 11-14 нед беременности расширяет возможности ультразвуковой диагностики и способствуют раннему выявлению нарушений в нормальном развитии комплекса мать-плацента-плод, что является ключевым в разработке мероприятий, необходимых для обеспечения эффективной перинатальной охраны плода и новорожденного.
Выводы
1. Выявлено повышение индексов периферического сосудистого сопротивления (систолодиастолическое отношение, индекс резистентности) в маточных артериях на ранних этапах гестации (11-14 нед) у пациенток, течение беременности у которых в последующем осложнилось преэклампсией; достоверных различий показателей допплерометрического исследования маточно-плацентарного кровотока у беременных с разной степенью тяжести преэклампсии не установлено.
2. Во II и III триместрах гестации у обследованных беременных с преэклампсией диагностировалась суб- и декомпенсированная хроническая плацентарная недостаточность с синдромом задержки развития плода.
3. Установлена одинаковая прогностическая значимость показателей систолодиастолического отношения и индекса резистентности, более прогностически значимыми оказались максимальные числовые значения «уголнезависимых индексов» по сравнению с минимальными.
4. Преэклампсия (особенно тяжелая) ассоциируется с низкими ростовесовыми показателями новорожденных и осложнениями течения неонатального периода (респираторный дистресс-синдром, дыхательная недостаточность, ателектазы легких, ВУИ новорожденного).
5. При увеличении допплерометрических показателей маточного кровотока (систолодиастолическое отношение, индекс резистентности) в сроке беременности 11-14 нед увеличивается число случаев нарушения кровотока в системе мать-плацента-плод во II и III триместрах гестации. Установлены положительные корреляционные связи индексов периферического сосудистого сопротивления (систолодиастолическое отношение, индекс резистентности) в маточных артериях в сроках 11-14 нед гестации с частотой развития преэклампсии, субкомпенсированной ХПН, задержки развития плода, гипотрофии и асфиксии новорожденного, что свидетельствует о возможности использования этих показателей в качестве предикторов указанных акушерских осложнений.
Плацентарная недостаточность
Итак, плацента – это важный орган, который образуется только во время беременности. Образуется плацента из хориона - зародышевых оболочек плода. В самом начале беременности ворсины хориона – выросты оболочки - равномерно покрывают всю поверхность плодного яйца, начиная со второго месяца беременности с одной стороны плодного яйца ворсины начинают удлиняться, увеличиваться в размерах и формируют плаценту.
Внутри ворсин течет кровь малыша, а снаружи они омываются кровью матери. Между кровотоком мамы и малыша расположен всего один слой клеток, который и играет роль барьера между организмом матери и ребенка. Благодаря этой мембране кровь матери и плода не смешивается.
Однако в последние годы стало известно, что клетки крови плода все-таки проникают через плацентарный барьер в кровоток матери и благодаря этому стало возможным проведение генетических анализов и определение хромосомных аномалий, резуса фактора и пола плода по крови беременной женщины (неинвазивный пренатальный тест).
В плаценте происходит постоянный обмен веществ между мамой и ребенком. Из материнской крови к плоду поступает кислород и питательные вещества, от плода обратно к матери углекислый газ и продукты обмена, подлежащие выведению из организма.
Плацентарный барьер выполняет иммунологическую функцию, поскольку пропускает некоторые защитные антитела – клетки крови, обеспечивающие борьбу с инфекционными агентами, кроме того он является непроницаемым для некоторых вредных веществ, вирусов и бактерий. К сожалению, плацентарный барьер легко преодолевают наркотические вещества, алкоголь, никотин, компоненты многих лекарств и некоторые вирусы.
Важной функцией плаценты является выработка гормонов и биологически активных веществ. В первую очередь это гормоны, важные для успешного вынашивания беременности, например хорионический гонадотропин, плацентарный лактоген, эстрогены и др.
К сожалению, не всегда все складывается вполне благополучно. В силу самых различных причин на разных сроках беременности могут происходить отклонения в развитии и функционировании плаценты. Изменения эти никогда не проходят бесследно для мамы и малыша, а зачастую имеют грозные последствия.
Если плацента перестает выполнять свои функции в полной мере, развивается так называемая плацентарная недостаточность. По сути, она заключается в ухудшении кровообращения в системе мать-плацента-плод.
Виды и причины плацентарной недостаточности
Врачи различают острую и хроническую плацентарную недостаточность:
Острая плацентарная недостаточность
Это состояние, требующее экстренного вмешательства врачей. Она характеризуется стремительным ухудшением плацентарного кровотока. Острая плацентарная недостаточность возникает в основном в результате отслойки плаценты или гибели отдельных участков ткани плаценты например при образовании тромбов в сосудах. Причиной отслойки может послужить травма живота, антифосфолипидный синдром.
Фосфолипиды – это сложные жиры, которые входят в состав оболочек всех клеток организма. В ряде случаев иммунная система организма вырабатывает большое количество антител к некоторым собственным фосфолипидам и белкам, связывающим эти липиды. Они называются антифосфолипидные антитела и при взаимодействии с клетками организма вызывают повреждение клеток и активацию свертывающей системы крови, что приводит к тромбообразованию.
Антифосфолипидный синдром является самой частой причиной тромботических осложнений при беременности, в том числе причиной отслойки плаценты и острой плацентаной недостаточности.
Вызвать отслойку плаценты может также тяжелое течение гестоза – грозного осложнения второй половины беременности, проявляющееся отеками, повышением давления и появлением белка в моче.
Острая плацентарная недостаточность развивается при отслойке более 2/3 поверхности плаценты.
В случае развития острой плацентарной недостаточности необходимо максимально быстро провести операцию кесарева сечения для сохранения жизни малыша и мамы.
Хроническая плацентарная недостаточность
Значительно чаще у беременных женщин встречается хроническая плацентарная недостаточность. В этом случае происходит нарушение формирования и созревания плаценты, уменьшается маточно-плацентарный и плодово-плацентарный кровотоки, ограничивается газообмен и обмен веществ в плаценте, снижается синтез плацентарных гормонов. Все эти изменения определяют недостаточное поступление кислорода и питательных веществ малышу, вызывают задержку роста и развития плода.
Причинами плацентарной недостаточности чаще всего являются перенесенные аборты, особенно хирургический аборт при первой беременности, курение, при этом количество и крепость выкуриваемых сигарет значения не имеют, поскольку на формировании неполноценных сосудов плаценты негативное действие оказывает табачный дым, а не никотин.
В группу риска по развитию плацентарной недостаточности входят также женщины с хроническими заболеваниями, такими как артериальная гипертензия, железодефицитная анемия, пиелонефрит, сахарный диабет, заболевания щитовидной железы.
В последние годы наблюдается значительный рост плацентарной недостаточности, вызванной бактериями, вирусами, грибами. Причиной этого может быть как острая инфекция, перенесенная будущей мамой во время беременности, так и активация хронического инфекционного процесса в организме беременной женщины.
Немаловажное значение в формировании хронической плацентарной недостаточности играет патология матки: эндометриоз, пороки развития матки (седловидная, двурогая). Фактором риска врачи считают также миому матки. Безусловно, целый ряд лекарственных средств оказывает неблагоприятное влияние на формирование плаценты и развитие плода. В настоящее время определен список препаратов, не разрешенных к применению во время беременности.
Также большое значение в развитии плацентарной недостаточности имеет тромбофилия – повышенная склонность организма к образованию сгустков крови - тромбов в сосудах.
В некоторых случаях плацентарная недостаточность может быть обусловлена наличием хромосомных нарушений у плода, в частности при синдромах Дауна (наличие дополнительной 21 хромосомы у плода) или синдроме Эдвардса (дополнительная 18 хромосома у плода) уже в ранние сроки беременности диагностируется нарушение функции плаценты.
Следует отметить, что среди осложнений беременности, наиболее часто приводящих к развитию хронической плацентарной недостаточности, существенным фактором является преэклампсия (или поздний гестоз) – это осложнения второй половины беременности, проявляющееся отеками, повышением давления и появлением белка в моче.
Независимо от факторов, способствующих развитию плацентарной недостаточности, в основе ее лежат нарушения кровообращения в маточно-плацентарном комплексе, приводящие к нарушению всех функций плаценты. Следовательно, симптомы хронической плацентарной недостаточности будут обусловлены недостатком поступления кислорода и питательных веществ к плоду.
Это прежде всего, задержка внутриутробного развития плода – отставание размеров плода и замедление темпов его роста. Часто имеют место изменение двигательной активности плода. Сначала может быть некоторое усиление движений, а затем уменьшение. Нарушение защитной функции плаценты приводит к внутриутробному инфицированию плода под действием проникающих через плаценту патогенных (болезнетворных) микроорганизмов. Плод, развитие которого происходит в условиях плацентарной недостаточности, в значительно большей степени подвержен риску травматизации в родах, у них отмечается нарушение адаптации к внеутробной жизни, повышенная заболеваемость в первый год жизни.
По времени возникновения врачи разделяют плацентарную недостаточность на раннюю и позднюю.
Ранняя (или первичная) плацентарная недостаточность
Развивается до 16 недель беременности. Она возникает уже на этапе формирования плаценты и связана с заболеваниями беременной женщины, имеющимися до беременности, к примеру с патологией матки, хронической артериальной гипертензией, эндокринологическими заболеваниями. При этом происходит формированием неполноценных сосудов в плаценте.
Поздняя (или вторичная) плацентарная недостаточность
Возникает после 16 недель беременности и чаще всего связана с заболеваниями, возникшими уже во время беременности. Чаще всего это железодефицитная анемия (то есть снижение концентрации гемоглобина и железа в крови), гестационный сахарный диабет (то есть нарушение усвоения организмом глюкозы, возникшее на фоне беременности), перенесенные вирусные и бактериальные инфекции.
Важным является подразделение плацентарной недостаточности на компенсированную и декомпенсированные формы.
Компенсированная плацентарная недостаточность
Развивается, к примеру, при угрозе прерывания беременности и нетяжелых формах позднего гестоза, в случае, если эти осложнения успешно поддаются медикаментозной коррекции.
Декомпенсированная плацентарная недостаточность
Вызывает развитие задержки развития плода, хронической внутриутробной гипоксии, вплоть до гибели плода.
Диагностика плацентарной недостаточности
Лечить уже развившуюся плацентарную недостаточность практически невозможно, поэтому врачи активно стремятся выявлять беременных женщин, угрожаемых в отношении формирования нарушений функции плаценты. Если плацентарная недостаточность выявляется в 3 триместре беременности, эффективного лечения, к сожалению, не существует. Поэтому очень активно в настоящее время применяются все способы выявления в ранние сроки беременности тех женщин, в формировании плаценты которых произошли нарушения.
В первую очередь, при постановке на учет по беременности выявляют максимально значимые факторы риска – курение, перенесенные аборты, отягощенную наследственность (низкий вес при рождении, склонность к тромбозам), наличие хронических заболеваний сердца, сосудов, сахарного диабета.
Профилактические мероприятия против развития плацентарной недостаточности особенно актуальны и необходимы до 16-17 недель беременности, когда происходит формирование структур плаценты.
Значимую помощь в оценке риска развития плацентарной недостаточности оказывает пренатальный скрининг, который проводится в 11-14 недель беременности. Он проводится для выявления синдромов Дауна, Эдвардса и др. хромосомных болезней у плода. В настоящее время самым актуальным является проведение комплексного ранний скрининг беременной на прогнозирование риска развития плацентарной недостаточности, преэклампсии и внутриутробной задержки развития плода. Поскольку данный вид диагностики относится к самым современным и передовым, к сожалению, он пока не включен в перечень услуг, предоставляемых в женской консультации в рамках ОМС, но доступен всем желающим в центрах пренатальной диагностики.
Определение белков, вырабатываемых плацентой
В первую очередь проводят определение белка РАРР-А, он является также маркером хромосомных аномалий плода. Снижение концентрации РАРР-А в крови в 11-14 недель беременности встречается у беременных женщин, имеющих высокий риск плацентарной недостаточности и задержки развития плода.
Второй гормон плаценты, который помогает в оценке рисков плацентарной недостаточности – PIGF (плацентарный фактор роста). Его концентрация в крови снижается задолго до первых проявлений плацентарной недостаточности. Его определение применяют не настолько широко, как PAPP-A, но тем не менее многие лаборатории уже включили данный белок в пренатальный скрининг 1 триместра. Крайне важное значение при проведении скрининга 1 триместра имеет измерение кровотоков в сосудах матки. Однозначно доказано, что сужение сосудов матки, определяемое при исследовании, свидетельствует о неполноценности формирования плаценты, которое будет ухудшаться с увеличением срока беременности и приведет к снижению питания малыша и снабжения его кислородов, то есть к развитию плацентарной недостаточности и задержки развития плода. При нормальных размерах маточных сосудов в 11-14 недель беременности риск тяжелой плацентарной недостаточности ничтожно мал.
Следующее обязательное скрининговое ультразвуковое исследование проводится в 20-21 неделю беременности. При этом обязательно проводят измерения плода, чтобы оценить, нет ли отставания в росте. Ведь при кислородном голодании замедляются темпы роста плода и размеры его начинают отставать от нормы для каждого срока беременности. Кроме того врач обязательно оценивает состояние и зрелость плаценты. Во время УЗИ проводится также допплерометрия сосудов матки для выявления ранних изменений, предшествующих клиническим проявлениям плацентарной недостаточности.
У пациенток, относящихся к группе высокого риска кроме УЗИ и допплерометрии проводят также суточное мониторирование колебаний артериального давления, определение количества белка в анализе мочи, собранном за сутки, оценивают показатели системы свертывания крови.
Третье УЗИ проводится всем будущим мамам в 30–34 недели беременности. Врач измеряет окружность головы и живота крохи, длину костей его ручек и ножек, и вычисляет предполагаемый вес плода. Эти измерения позволяют доктору убедиться в том, что малыш развивается нормально. Также имеет значение строение плаценты, наличие в ней признаков старения, вследствие чего она обычно перестает полноценно снабжать малыша кровью, а, значит, ему перестает хватать кислорода и питательных веществ и развитие ребенка нарушается. Во время УЗИ оценивается количество и вид околоплодных вод, которые также могут изменяться при внутриутробном страдании плода.
Допплерометрия
Допплерометрия сосудов плаценты и пуповины (метод исследования скоростей кровотоков в этих сосудах) так же позволяет оценить самочувствие малыша. Доктор исследует кровоток в артериях матки, пуповины, сердца и мозга ребенка. Это исследование позволяет определить, хорошо ли работает плацента, нет ли признаков нехватки кислорода у малыша, или развития гестоза у мамы. При снижении скорости кровотока в каком-либо сосуде можно говорить о нарушениях питания плода различной степени тяжести.
Вовремя проведенное обследование позволяет выявить начальные стадии дефицита кровоснабжения. В таких случаях лечение сможет предотвратить грозные осложнения, такие как гипоксия и внутриутробная задержка развития малыша. Допперометрию проводят в 20–21 неделю и в 30-32 недели беременности, при наличии изменений, контроль осуществляют минимум каждые две недели.
Кардиотокография
Это важный метод оценки состояния плода. Проводится КТГ при сроке беременности 33 недели и более, поскольку только на этом этапе внутриутробного развития малыша устанавливается полноценная регуляция деятельности сердечно-сосудистой системы плода центрами спинного и головного мозга. Запись сердцебиений плода проводят в течение 20–40 минут, а при необходимости исследование может быть продлено до 1,5 часов.
Аппарат регистрирует и записывает частоту сердцебиений малыша. Врач акушер-гинеколог оценивает кривую записи сердцебиений, эпизоды урежения и резкого учащения частоты сердечных сокращений плода и на основании этих данных делает заключение о том, насколько комфортно малыш чувствует себя в животе у мамы. К примеру, при снижении концентрации кислорода в крови плода, уменьшается и его поступление к клеткам нервной системы, что в свою очередь отражается на частоте сердечных сокращений. При нормальном течении беременности КТГ проводят после 33 недели 1 раз в 10–14 дней, иногда чаще. В некоторых клиниках в настоящее время предлагается услуга постоянного КТГ-мониторирования, что приобретает актуальность при наличии признаков плацентарной недостаточности. Беременной женщине выдается мониторчик, который регистрирует изменения сердечной деятельности малыша и эти данные по интернету передаются лечащему врачу.
Лечение плацентарной недостаточности
Специфических способов лечения плацентарной недостаточности в настоящее время не существует, поскольку нет лекарственных препаратов, которые избирательно улучшают маточно-плацентарный кровоток. Именно поэтому все меры борьбы с плацентарной недостаточностью направлены на профилактику. Если пациентка относится к группе высокого риска по развитию плацентарной недостаточности, с раннего срока беременности ей назначают лекарственные препараты, эффективность которых хорошо доказана и которые предупреждают раннее развитие выраженных нарушений функции плаценты.
Если во время проведения дополнительных методов оценки состояния плода выявляются начальные нарушения поступления кислорода к малышу, проводится медикаментозное лечение, направленное на увеличение притока крови и кислорода через плаценту и обязательные контрольные обследования на фоне проводимой терапии. Если изменения серьезные и малыш испытывает выраженный дефицит кислорода и питательных веществ, состояние его страдает, то в таких случаях проводится экстренное родоразрешение.
Маточно - плацентарное кровообращение.
Э. С. Манелис, Л. И. Калакутский, О. Л. Крылова, Л. Г. Чаплыгина (г. Самара)
Нарушениям маточно-плацентарного кровотока (МПК) в последнем триместре беременности принадлежит ведущая роль в развитии патологии внутриутробного плода, обусловливающей высокую частоту показателей перинатальных осложнений. Коррекция МПК заключается прежде всего в нормализации базального маточного тонуса, системной и органной гемодинамики, реологичеоких свойств крови и микроциркуляции плаценты. Медикаментозная терапия включает целый комплекс препаратов, действующих на указанных уровнях, что создает значительную лекарственную нагрузку на организм матери и плода, нередко сопровождающуюся рядом побочных эффектов (непереносимость, аллергия и др.).
Для снижения медикаментозной нагрузки при коррекции маточного тонуса и нарушений МПК нами дополнительно использовался метод чрескожной электронейростимуляции (ЧЭНС) с помощью сетевого аппарата "Элиман-401" и портативного батарейного прибора "Элиман-206". Подача тока осуществлялась через накожнне электроды,, расположенные паравертебрально на уровне D . L , длительность сеанса 20. 30 мин, число сеансов 3. 8.
Обследовано 40 беременных с угрозой невынашивания беременности при сроке гестации 34. 37 нед, а также 30 беременных с сочетанным гестозом 1-2 ст. на фоне анемии с хронической фетоплацентарной недостаточностью, хронической внутриутробной гипоксией плода.
Оценка вазотропного эффекта ЧЭНС (сравнение результатов до и после сеанса) проводилась методами интегральной реографии тела по Тищенко, реогистерографии (отведение "шейка матки - проекция дна матки на переднюю брюшную стенку"), реовазографии голени, фотоплетизмографии пальцев стопы, допплерографии маточных артерий и сосудов пуповины. Одновременно проводились кардиофетомониторинг и наружная токография, вариационная пульсометрия беременной и плода.
У всех беременных отмечалось клиническое улучшение после 1. 3 сеансов ЧЭНС: нормализовался маточный тонус, улучшались тембр и звучность тонов плода, улучшалось самочувствие беременных, нормализовались сон и диурез. Имелись положительные сдвиги показателей кардиофетомониторинга - исчезновение признаков гипоксии или их сдвиг от внутриутробной гипоксии до угрозы гипоксии за счет нормализации базальной частоты и возрастания вариабельности сердечных сокращений.
Потребность в медикаментах (токолитики, гипотензивные, седативные и др. средства)
снижалась в 3-5 раз.
Все обследованные беременные родили в срок, роды протекали без осложнений, масса плодов 2700 . 3800 г, оценка состояния здоровья по шкале Апгар 7-8 баллов.
При визуальном анализе реограмм, записанных после сеанса ЧЭНС, отмечена благоприятная динамика: высота систолической волны увеличивалась анакрота становилась более крутой, вершина волны приобретала умеренно закругленную форму. Достоверно увеличивались реографический индекс в амплитудно-частотный показатель, свидетельствующие о возрастании объемного кровотока в матке и нижних конечностях. Уменьшались функциональные нарушения сосудистой системы матки, улучшался артериальный приток и условия венозного оттока.
По данным допплерографии, в процессе ЧЭНС в маточных артериях происходит увеличение скоростей движения крови как во время систолы, так и диастолы, достоверно снижалось систоло-диастолическое отношение, пульсационный индекс и индекс резистентности, что свидетельствует об уменьшении сосудистого сопротивления в бассейне кровоснабжения маточных артерий. В артерии пуповины обнаружена тенденция к снижению резистентности микроваскуляторной сети плодовой части плаценты.
Таким образом, по данным рео- и допплерографии под влиянием ЧЭНС наступает увеличение регионарного кровотока в органах малого таза и нижних конечностей за счет ликвидации сосудистого спазма и децентрализации кровообращения.
Увеличение производительности сердца при проведения ЧЭНС носит компенсаторный характер в ответ на регинарную вазодилятацию и возможно при отсутствии выраженной гиповолемии.
Достигаемая в процессе ЧЭНС коррекция МПК служит предпосылкой к улучшению плацентарного газообмена. Это подтверждается более глубоким насыщением закисью азота крови плодов, извлеченных путем кесарева сечения в той группе наблюдений, где в качестве дополнительного компонента премедикации и наркоза использовалась. ЧЭНС. Забор крови производился в момент извлечения плода из вены матери и сосудов пуповины до появления первого вдоха ребенка. Концентрация N O в крови определялась методом газовой хроматографии с последующим определением коэффициентов плацентарного перехода анестетика.
Клинические наблюдения свидетельствуют, что правильно выбранные параметры ЧЭНС можно использовать для коррекции сократительной деятельности матки в родах и состояния внутриутробного плода. Для усиления родовой деятельности следует выбирать субпороговые величины тока (5-20 мА), вызывающие незначительные ощущения под электродами. Для торможения сократительной деятельности матки и умеренного снижения базального тонуса миометрия целесообразны субболевые (45-80 мА) параметры тока. При этом состояние внутриутробного плода (при отсутствии механических препятствий кровотоку, например, пережатия пуповины) обычно улучшается, тоны становятся более ясными, ритмичными, улучшаются показателя кардиофетомониторинга. Данные вариационной пульсометрии выявляют снижение индекса напряженности. Это свидетельствует об улучшения состояния внутриутробного плода.
У 22 из 24 рожениц со слабостью родовой деятельности улучшение показателей кардиотахограммы и вариационной пульсометрии плода наступило через 5-15 мин от начала ЧЭНС на фоне проводимой медикаментозной стимуляции родовой деятельности окситоцином. 20 родов закончились через естественные пути, 4- операцией кесарева сечения. Получено 24 ребенка массой тела 2900. 3950 г, оценка состояния здоровья по шкале Апгар 7-8 баллов.
Наиболее отчетливо положительный клинический эффект ЧЭНС наблюдался у 5 из 6 рожениц с хорионамнионитом (безводный период 32. 104 ч). Сердечные тоны плодов при поступлении в роддом едва прослушивались, были аритмичными, колебались в пределах 60-90 мин. В процессе ЧЭНС, начатом без дополнительной медикаментозной терапии, у 5 из 6 плодов сердечные тоны на 2-5 мин -сеанса ЧЭНС стали более ясными,
ритмичными, частотой 110-136 ударов в минуту. В одном наблюдении ни ЧЭНС, ни медикаментозная терапия плода эффекта не дали, плод погиб внутриутробно. При гистологическом исследовании плаценты выявлена абсолютная плацентпрная недостаточность 4 стадии.
Полученные данные совпадают с результатами работ E.Kubista, K.Philipp (1978), обнаруживших увеличение МПК под влиянием ЧЭНС с помощью сцинтиграфии плаценты. Аналогичные данные приводят Т.Н.Лысая и др. (1987). В.А.Мельников и др. (I987). Механизмами, вызывающими вазоплегию, служат активация парасимпатического и снижение активности симпатического тонуса, выработка вазоактивного кишечного полипептида (Caada , 1983), снижение агрегации тромбоцитов и ускорение каллекреин-зависимого фибринолиза (Г.Е.Слуцкер, 1990).
При неправильном подборе параметров ЧЭНС (неприятные ощущения под электродами) вместо вазоплегии возможна активация симпатического тонуса и усиление вазоспазма. Плавное изменение амплитуды тока под контролем ощущений беременной позволяет избежать данного осложнения. Противопоказаниями к проведению ЧЭНС могут служить индивидуальная непереносимость тока, заболевания кожи в местах наложения электродов, декомпенсированная кровопотеря, выраженная гипотония, эклампсия, преэклампсия, а такте общие акушерские противопоказания в родах (поперечное положение плода, неполноценный рубец на матке и др.).
Таким образом, ЧЭНС оказывает отчетливое коррегирующее влияние на тонус миометрия, маточно-плацентарное кровообращение и состояние внутриутробного плода, целесообразно включение ЧЭНС в повседневную акушерскую практику.
Читайте также:
- Распространенность предменструального синдрома. Критерии ПМС
- Эпидемиология (распространенность) аллергических заболеваний - атопий
- Отравление инсектицидами
- Столбняк. Возбудитель столбняка. Clostridium tetani. Эпидемиология столбняка. Морфология столбняка. Тинкториальные свойства столбняка.
- Анемия у новорожденных
