Миелодиспластические синдромы
Добавил пользователь Валентин П. Обновлено: 27.01.2026
Термин « миелодиспластический синдром » (сокращённо МДС) объединяет различные патологии, при которых обнаруживаются цитопения (понижение концентрации форменных элементов крови), дисплазия (неправильное развитие) гемоцитобластов (предшественников кровяных клеток), гипоклеточность или гиперклеточность костного мозга.
Причины болезни
Ученые предполагают, что спровоцировать миелоидный синдром способен также парвовирус В19.
Повышают риск возникновения патологии постоянная работа с некоторыми химическими веществами (пестицидами, бензином, органическими растворителями), неблагоприятная экологическая ситуация, курение, некоторые врожденные и наследственные болезни.
Под влиянием повреждающих факторов в стволовых клетках возникают мутации, которые способствуют развитию МДС. Постепенно они накапливаются, способствуя переходу болезни в лейкоз.
Симптомы патологии
Признаки МДС зависят от того, дефицит каких кровяных клеток испытывает организм.
Выделяют 3 группы клинических проявлений:
- Анемический синдром . Наблюдается при пониженной концентрации эритроцитов либо гемоглобина. Кожа и слизистые приобретают бледный окрас, в ушах появляется шум. Человек страдает от головокружений и одышки. Он становится раздражительным, быстро устает, даже минимальные физические нагрузки причиняют усиленное сердцебиение.
- Геморрагический синдром . Следствие уменьшения числа тромбоцитов. Сопровождается усиленной кровоточивостью: носовыми, десневыми, желудочно-кишечными, маточными кровотечениями, кровоизлияниями.
- Лейкопения . Развивается при снижении уровня лейкоцитов. В результате ослабляется иммунная система, что способствует присоединению различных инфекций, повышению температуры тела.
У некоторых пациентов в число симптомов миелодиспластического синдрома входят увеличение размеров селезенки (спленомегалия) и печени (гепатомегалия).
Диагностика МДС
Основной метод диагностики миелодиспластического синдрома – исследование крови. При МДС возможно понижение как одного показателя, так и их комбинация. Диагноз ставят только при устойчивой (не менее полугода) цитопении, если не найдены другие причины.
Если возникает подозрение на миелодиспластический синдром, делают трепанобиопсию и пункцию костного мозга. Полученный биоматериал подвергают гистологическому и цитологическому исследованию.
Чтобы исключить другие причины цитопении, пациента направляют на дополнительные лабораторные и инструментальные исследования, которые могут включать:
- биохимическое исследование крови;
- определение маркеров воспаления;
- исследование концентрации гормонов щитовидной железы;
- ультразвуковое исследование щитовидной железы, простаты, органов, расположенных в брюшной полости и в области малого таза; ; ;
- эзофагогастродуоденоскопию.
Цитопения сопровождает различные заболевания. Поэтому важно исключить другие причины: рак, аутоиммунные заболевания, хронические инфекции, нарушение гемопоэза, отравление бензином или тяжелыми металлами, нехватку меди, избыток цинка, побочное действие лекарств.
Лечение МДС
Выбор способа лечения зависит от степени и прогрессирования цитопении, группы риска, имеющихся сопутствующих заболеваний.
В зависимости от числа бластов, цитопений , выявленных генетических изменений выделяют 4 группы риска: высокий, промежуточный 1, промежуточный 2, низкий.
Единственный действенный метод лечения, обеспечивающий лечение , – пересадка костного мозга.
Все остальные способы направлены на ослабление неприятной симптоматики, предотвращение осложнений, улучшение качества жизни. Но из-за высокого риска осложнений, включая возможность смертельного исхода, отсутствия доноров трансплантацию предлагают только 5-10% больных. Обычно пересадку стволовых клеток рекомендуют пациентам моложе 65 лет с промежуточным -2 и высоким риском при наличии идентичного донора.
Выделяют 3 основные способа лечения:
- Высокоинтенсивная терапия, включающая пересадку стволовых клеток и полихимиотерапию . Назначают пациентам, входящим в группу высокого или промежуточного риска 2. При проведении химиотерапевтической терапии применяют эпигенетические модуляторы Азацитидин и Децитабин (облегчают симптоматику, предотвращают переход в острый миелолейкоз), иммуномодулятор Леналидомид ( блокирует ангиогенез опухолевых клеток , уменьшает потребность в переливании крови).
- Низкодозная химиотерапия в комбинации с заместительной и иммуносупрессивнойтерапией . Проводят при низком и промежуточном риске 1.
- Симптоматическое и поддерживающее лечение . Позволяет повысить качество жизни и увеличить ее продолжительность.
o При анемическом синдроме назначают эритропоэтины , вливают эритроцитарную массу. Но при неоднократном проведении процедуры возможна перегрузка железом, что требует хелатной терапии.
o Чтобы купировать либо предотвратить кровоточивость, прибегают к трансфузии тромбоцитов.
o При гипопластическом типе кроветворения эффективное действие оказывают иммунодепрессанты, которые защищают костный мозг от иммунной атаки.
В клинике Спиженко лечение подбирают индивидуально для каждого пациента в соответствии с международными рекомендациями и утвержденными протоколами.
Миелодиспластические синдромы
Вам поставили диагноз: Миелодиспластические синдромы
Наверняка Вы задаётесь вопросом: что же теперь делать?
Подобный диагноз всегда делит жизнь на «до» и «после». Все эмоциональные ресурсы пациента и его родных брошены на переживания и страх. Но именно в этот момент необходимо изменить вектор «за что» на вектор «что можно сделать». Очень часто пациенты чувствуют себя безгранично одинокими вначале пути. Но вы должны понимать - вы не одни.
Предлагаем вашему вниманию краткий, но очень подробный обзор данного заболевания.
Его подготовили высоко квалифицированные специалисты Отдела лекарственного лечения злокачественных новообразований МРНЦ имени А.Ф. Цыба и Отдела лекарственного лечения опухолей МНИОИ имени П.А. Герцена – филиалов ФГБУ «НМИЦ радиологии» Минздрава России под редакцией заведующих отделами, д.м.н. ФАЛАЛЕЕВОЙ Н.А. и д.м.н. ФЕДЕНКО А.А.
Филиалы и отделения, где лечат миелодиспластические синдромы
МНИОИ им. П.А. Герцена – филиал ФГБУ «НМИЦ радиологии» Минздрава России.
Отдел лекарственного лечения опухолей
Заведующий отделом, д.м.н. ФЕДЕНКО Александр Александрович
тел: 8 (494) 150 11 22
МРНЦ им. А.Ф. Цыба – филиал ФГБУ «НМИЦ радиологии» Минздрава России.
Отдел лекарственного лечения злокачественных новообразований
Заведующая отделом, д.м.н. ФАЛАЛЕЕВА Наталья Александровна
тел: 8 (484) 399 – 31-30
Миелодиспластические синдромы
(МДС) – разнородная группа заболеваний системы кроветворения, сопровождающаяся нарушением созревания кроветворных клеток с нарушениями их строения (дисплазией) и функции, а также повышенным риском развития острого лейкоза. МДС чаще всего сопровождаются снижением показателей общего анализа крови – цитопенией. Снижение уровня гемоглобина и числа эритроцитов обозначают термином анемия; числа лейкоцитов/нейтрофилов – лейкопенией/нейтропенией; уровня тромбоцитов – тробоцитопенией. Изредка может быть и увеличение числа лейкоцитов и/или тромбоцитов.
Ежегодная заболеваемость МДС в среднем составляет 3-4 случая на 100000 населения и увеличивается с возрастом. Основной контингент больных МДС представлен пожилыми людьми (средний возраст – 70 лет). В отдельную группу относят МДС, развившиеся после химиотерапии и/или лучевой терапии предшествующих заболеваний (преимущественно онкологических). Они составляют 10-15% от ежегодно выявляемых случаев МДС и называются вторичными МДС.
В связи с гетерогенностью заболевания возникает вопрос о выборе оптимальной терапии. Одним из основных факторов для решения этой задачи является определение прогностической группы (группы риска), к которой относится конкретный больной.
Каждый прогностический признак оценивается в баллах. В соответствии с суммарным числом баллов больных объединяют в 4 группы: низкого (0 баллов), промежуточного-1 (0,5-1,0 балл), промежуточного-2 (1,5-2,0 балла) и высокого (2,5 балла и выше) риска. Первые 2 группы (низкого и промежуточного-1 риска) характеризуются принципиально благоприятным прогнозом, а 2 остальные (промежуточного-2 и высокого риска) — неблагоприятным прогнозом. Определение прогноза необходимо для выбора лечения.
Существует несколько основных направлений в лечении МДС:
Химиотерапия: на протяжении последних 20 лет для лечения больных МДС с увеличенным числом бластных клеток, то есть преимущественно в группе принципиально неблагоприятного прогноза, используются схемы терапии острого миелоидного лейкоза. Применение стандартной химиотерапии позволяет получить высокую частоту полных ремиссий – 50-70%. Однако продолжительность ремиссий относительно короткая (как правило, менее 1,5 лет), а лечение сопровождается высокой токсичностью.
Трансплантация гемопоэтических стволовых клеток (трансплантация костного мозга): единственным методом лечения, позволяющим существенно увеличить продолжительность жизни больных МДС, является аллогенная трансплантация гемопоэтических стволовых клеток (аллоТГСК). Аллогенная ТГСК также позволяет получить наилучшие результаты по сравнению с другими методами лечения при вторичных МДС. Однако выполнение аллоТГСК не всегда возможно в связи с пожилым возрастом большинства больных и отсутствием идентичного родственного донора.
Иммуносупрессивная терапия: использование иммуносупрессивных препаратов, таких как циклоспорин А, демонстрирует наибольшую активность при гипопластическом варианте МДС, при отсутствии увеличения числа бластных клеток в костном мозге, нормальном кариотипе (без отклонений в наборе хромосом), наличии лимфоидных узелков (очаговых скоплений лимфоидных клеток) в трепанобиоптате, наличии клона клеток, составляющих субстрат пароксизмальной ночной гемоглобинурии (ПНГ-клон), и у HLA-DR-15 – позитивных молодых больных.
Терапия колониестимулирующими препаратами: эритропоэз-стимулирующие препараты – эритропоэтины (препараты, направленные на лечение анемии) фигурируют практически во всех рекомендациях по лечению МДС. Практически все специалисты сходятся во мнении о необходимости определения уровня эндогенного (собственного, вырабатываемого организмом) эритропоэтина до начала лечения. При уровне эндогенного эритропоэтина свыше 500 ед/л лечение эритропоэтином не показано, большая эффективность наблюдается при уровне эндогенного эритропоэтина в пределах 200 ед/л.
Сопроводительная (симптоматическая) терапия : к сопроводительной терапии при МДС относят гемотрансфузии (переливания) эритроцитов и тромбоцитов, антимикробную терапию, в том числе в комбинации с Г-КСФ или ГМ-КСФ, использование комплексонов (хелаторов) железа.
Программа лечения МДС основана на риск-адаптированном подходе в зависимости от групп прогноза, возраста, общего состояния больного. Иными словами, назначается индивидуальная терапия в зависимости от результатов полностью проведенного обследования. В некоторых случаях, когда проявления заболевания незначительны, может быть предложено только наблюдение у врача. Лечение некоторыми препаратами может проводиться как в условиях стационара, так и дома.
Филиалы и отделения Центра, в которых лечат миелодиспластические синдромы
ФГБУ «НМИЦ радиологии» Минздрава России обладает всеми необходимыми технологиями лучевого, химиотерапевтического и хирургического лечения, включая расширенные и комбинированные операции. Все это позволяет выполнить необходимые этапы лечения в рамках одного Центра, что исключительно удобно для пациентов.
Отдел лекарственного лечения злокачественных новообразований МРНЦ имени А.Ф. Цыба – филиал ФГБУ «НМИЦ радиологии» Минздрава России
Заведующая отделом, д.м.н. ФАЛАЛЕЕВА Наталья Александровна
8 (484) 399 – 31-30, г. Обнинск, Калужской области
Отдел лекарственного лечения опухолей МНИОИ имени П.А. Герцена –филиал ФГБУ «НМИЦ радиологии» Минздрава России
Заведующий отделом, д.м.н. ФЕДЕНКО Александр Александрович
Миелодиспластические синдромы
Миелодиспластические синдромы (МДС) — группа заболеваний, которые характеризуются нарушениями кроветворения миелоидной линии. В результате этих нарушений возможность выработки зрелых клеток крови частично сохраняется, но наблюдается дефицит тех или иных их видов, а сами клетки при этом изменены и плохо функционируют.
У значительной части больных МДС через некоторый промежуток времени, обычно от нескольких месяцев до нескольких лет, развивается острый миелоидный лейкоз.
МДС в обиходе иногда называют «предлейкемией», ранее применялись также термины «малопроцентный лейкоз», «тлеющий лейкоз» или «дремлющий лейкоз». Это связано с содержанием бластных клеток в костном мозге: если их более 20% (согласно классификации Всемирной организации здравоохранения) или более 30% (согласно франко-американо-британской классификации FAB), то речь уже идет о миелоидном лейкозе, если же их уровень ниже порогового значения, то может быть диагностирован МДС.
Под термином «миелодиспластический синдром» в настоящее время подразумевается целая группа заболеваний, различающихся по частоте встречаемости, клиническим проявлениям, а также по вероятности и ожидаемым срокам трансформации в лейкоз. Специалисты используют две классификации МДС: франко-американо-британскую (FAB) и классификацию Всемирной организации здравоохранения (ВОЗ). Рассмотрим классификацию FAB:
Рефрактерная анемия (РА). Термин «рефрактерная» здесь означает, что анемия не поддается лечению препаратами железа и витаминами. В костном мозге менее 5% миелобластов, аномалии в основном касаются предшественников эритроцитов.
Рефрактерная анемия с кольцевыми сидеробластами (РАКС): миелобластов в костном мозге менее 5%, но не менее 15% предшественников эритроцитов представлены особыми аномальными клетками — так называемыми кольцевыми сидеробластами. Это клетки с кольцеобразными «отложениями» железа, которые не могут обеспечивать эффективный транспорт кислорода.
Рефрактерная анемия с избытком бластов (РАИБ): миелобластов в костном мозге 5–20%. В классификации ВОЗ дополнительно подразделяется на РАИБ-I (5–9% бластов) и РАИБ-II (10-19% бластов).
Рефрактерная анемия с избытком бластов на стадии трансформации (РАИБ-T): миелобластов 21–30% (по классификации ВОЗ это уже острый миелоидный лейкоз).
Хронический миеломоноцитарный лейкоз, ХММЛ (по классификации ВОЗ относится к миелодиспластическим-миелопролиферативным заболеваниям).
Частота встречаемости, факторы риска
Общая частота МДС составляет 3-5 случаев на 100 000 населения. Однако у детей и молодых взрослых это заболевание встречается во много раз реже: более 80% случаев МДС фиксируется после 60 лет, причем несколько чаще у мужчин, чем у женщин.
В большинстве случаев МДС возникает без какой-либо известной причины, но иногда его развитие может быть спровоцировано предшествующей химиотерапией или лучевой терапией по поводу какой-либо опухоли - например, лимфомы Ходжкина или неходжкинской лимфомы. В этих случаях говорят о вторичном МДС.
Частота МДС (как и острого миелоидного лейкоза) повышена у людей с определенными генетическими аномалиями, такими как синдром Дауна, анемия Фанкони, нейрофиброматоз и некоторые другие.
Изучается роль и других факторов в возникновении этого заболевания — например, воздействия некоторых вредных химических веществ. Но у детей и молодых взрослых эти факторы не играют существенной роли.
Признаки и симптомы
Симптомы и степень их выраженности могут различаться в зависимости от разновидности МДС и конкретного случая. Но большинство наблюдаемых проявлений возникает в результате цитопении, то есть дефицита нормальных клеток крови.
Анемия (недостаток эритроцитов, сниженный уровень гемоглобина) характерна для подавляющего большинства случаев МДС; она проявляется бледностью, утомляемостью, плохой переносимостью физических нагрузок; могут также возникнуть одышка, головокружения, боли в груди и т.п.
Примерно у половины больных встречается нейтропения (то есть пониженное содержание зрелых функциональных нейтрофилов) и поэтому снижена сопротивляемость инфекциям. Нередко наблюдается и тромбоцитопения, то есть недостаточное содержание тромбоцитов, что ведет к возникновению кровотечений, синяков, петехий (мелкоточечных подкожных кровоизлияний). Возможны и другие симптомы.
Впрочем, в некоторых случаях пациенты с МДС долгое время не замечают существенного ухудшения самочувствия, и тогда проблемы обнаруживаются только в ходе обычного медосмотра по отклонениям от нормы в клиническом анализе крови.
Диагностика
Как правило, поводом к медицинскому осмотру служат жалобы на симптомы, связанные с анемией, причем эта анемия не поддается обычному лечению препаратами железа и витаминами. В клиническом анализе крови снижено количество эритроцитов, может быть также снижено количество лейкоцитов (нейтрофилов) и/или тромбоцитов. Характерно, что при уменьшении числа эритроцитов их размеры и цветовой показатель крови могут быть увеличены. Полезен также подсчет числа ретикулоцитов — незрелых эритроцитов, так как он дает информацию об интенсивности образования новых красных клеток крови.
Для точной диагностики и определения конкретного варианта МДС необходимо детальное исследование образца костного мозга, взятого в ходе трепанобиопсии: анализируются характер расположения различных клеток («архитектоника» костного мозга), число бластных клеток, содержание кольцевых сидеробластов и других аномальных клеток, степень изменений во всех ростках кроветворения — то есть среди предшественников эритроцитов, гранулоцитов и тромбоцитов, изменения стромы — соединительной ткани костного мозга. Выявленные нарушения могут быть очень разнообразными.
Так как развитие МДС нередко связано с известными хромосомными аномалиями, определенную роль в диагностике и прогнозе играют цитогенетические исследования.
Лечение
Лечение МДС зависит от его конкретной формы. Так, если речь идет об относительно «доброкачественных» разновидностях МДС с небольшим числом бластных клеток, то больные из групп низкого риска могут длительное время сохранять нормальное качество жизни, просто время от времени получая заместительную терапию компонентами крови — эритроцитами и, возможно, тромбоцитами. При перегрузке железом после множественных переливаний необходима соответствующая терапия. Иногда для стимуляции кроветворения используют факторы роста. При инфекционных осложнениях требуется антибактериальная и противогрибковая терапия. В ряде случаев применяют и другие лекарственные средства.
Если же речь идет о формах болезни, связанных с более высоким риском, то вопрос о лечении таких пацентов достаточно сложен. Химиотерапия с использованием обычных цитостатиков (цитарабин и т.п.) малоэффективна и не приводит к долговременной ремиссии. Общепринятых стандартов химиотерапии при МДС практически не существует. Есть и новые лекарства; в частности, обнадеживающие результаты показало применение гипометилирующих препаратов, таких как «Дакоген» (децитабин) и «Вайдаза» (азацитидин). Иногда может применяться иммуносупрессивная терапия и другие методы.
Единственным радикальным методом, позволяющим в случае успеха рассчитывать на полное излечение больных с МДС, является аллогенная трансплантация костного мозга — особенно у молодых пациентов, которые лучше переносят эту процедуру и связанные с ней осложнения. Однако аллогенная трансплантация по поводу МДС, как и по поводу других заболеваний, связана с проблемой поиска совместимого донора и с опасностью жизнеугрожающих осложнений.
При трансформации МДС в острый миелоидный лейкоз проводится химиотерапия этого лейкоза. Однако вторичный лейкоз, развившийся из МДС, обычно плохо поддается терапии. В этой ситуации, как правило, также показано проведение аллогенной трансплантации костного мозга, особенно у молодых больных.
Прогноз
Развитие МДС происходит с разной скоростью в зависимости от конкретной разновидности болезни. Если при некоторых формах МДС пациенты могут, особенно при наличии поддерживающей терапии (переливания компонентов крови и т. д.), жить достаточно долго и полноценно, то при более «активных» и злокачественных разновидностях заболевания средняя продолжительность жизни составляет не более года. Особенно плохой прогноз при вторичном МДС. Пациенты могут погибнуть как от проявлений самого МДС, так и от развившегося на его основе острого миелоидного лейкоза.
При использовании аллогенной трансплантации костного мозга можно добиться нормализации кроветворения и стойкой ремиссии болезни у большинства молодых пациентов. Иными словами, в случае успеха трансплантация приводит к выздоровлению. Однако надо помнить о высокой вероятности жизнеугрожающих осложнений (таких как реакция «трансплантат против хозяина», инфекции и др.) и рецидивов после трансплантации.
Миелодиспластические синдромы
Когда ставят диагноз "миелодиспластический синдром", то всегда помнят о том, что существует множество других болезней, способных ухудшить кровь и изменить костный мозг: это хронические инфекции (туберкулез, токсоплазмоз…), аутоиммунные заболевания (системная красная волчанка, ревматоидный артрит…), разнообразные опухоли. Вот почему пациента нужно всесторонне обследовать, а МДС является, скорее, диагнозом исключения, то есть его ставят тогда, когда все другие причины изменения крови исключены. МДС – болезнь пожилых, средний возраст пациентов составляет 70 лет.
Всем клеткам крови человека дает начало стволовая клетка. По мере взросления ее потомков выделяются 3 основных ветви, или ростка: красный росток (эритроидный), белый росток (лейкоцитарный) и тромбоцитный (тромбоцитарный). И хотя ростков всего три, весь процесс кроветворения очень сложен и многогранен. Воспроизводство крови подобно «оркестру», который в течение всей жизни человека, подстраиваясь под нужды организма, играет, тем не менее, по очень точным и сложным нотам.
Термин «миелодиспластический» состоит из трех частей: «миело-» – греческая приставка, обозначающая связь с костным мозгом, «дис-» – приставка, обозначающая «нарушение», и «-плазия» – конечная часть сложных слов, обозначающая «развитие». Термином «синдром» называют совокупность связанных между собой признаков. Таким образом, из самого названия следует, что в организме произошла какая-то поломка, которая привела к тому, что нарушено созревание (развитие) клеток костного мозга. Причины ученым еще предстоит выяснить, но из-за нарушения на тех или иных этапах взросления клеток кровь начинает меняться. Вначале страдает один росток крови, чаще всего эритроидный. У человека постепенно в крови снижается гемоглобин, больной начинает чувствовать слабость, нарастающее недомогание, привычная работа оказывается не по силам, а отдых не приносит облегчения. Это происходит потому, что, когда в крови уменьшается количество гемоглобина (основного переносчика кислорода) и вдыхаемый из воздуха кислород не попадает в органы и ткани, у них начинается кислородное голодание. Пациент чувствует слабость.
Диагноз «миелодиспластический синдром» (МДС) поставить довольно сложно. Здесь лечащий врач, как никогда, нуждается в помощи врачей-лаборантов: цитолога и цитогенетика с хорошей лабораторией. Врач-цитолог, глядя в микроскоп, тщательно анализирует костный мозг, капелька которого нанесена на специальное маленькое стекло и делает заключение о том, есть ли внешние признаки нарушения работы костного мозга. Этот метод относится к одному из самых технически простых, однако специалистов-цитологов, способных выявить и оценить «неправильные» клетки, в городе очень мало. Врач-цитогенетик с помощью сложной аппаратуры анализирует делящиеся клетки костного мозга и ищет типичные изменения в генах, которые очень важны для диагноза, прогноза, выбора лечения и контроля за ним.
Когда ставят диагноз МДС, то всегда помнят о том, что существует множество других болезней, способных ухудшить кровь и изменить костный мозг: это хронические инфекции (туберкулез, токсоплазмоз…), аутоиммунные заболевания (системная красная волчанка, ревматоидный артрит…), разнообразные опухоли. Вот почему пациента нужно всесторонне обследовать, а МДС является, скорее, диагнозом исключения, то есть его ставят тогда, когда все другие причины изменения крови исключены. МДС – болезнь пожилых, средний возраст пациентов составляет 70 лет.
Чем же опасен миелодиспластический синдром, кроме низкого гемоглобина? Одним из самых неприятных и опасных следствий является постепенное накапливание поломок в кроветворении, поскольку первая поломка в зрелых клетках «тянет» за собой другие поломки и уже в более молодых клетках. Со временем заболевают все более и более активные клетки, и возникает болезнь «острый лейкоз». Наблюдая за пациентами, а также анализируя картину их болезни, врачи научились примерно предсказывать его появление. Риск перехода МДС в острый лейкоз записывают специальными прогностическими индексами (IPSS, WPSS и другими), которые обычно указывают в диагнозе.
Миелодисплатический синдром существует в нескольких видах:
Мировая статистика показывает, что в зависимости от разных факторов пациенты с МДС живут от одного-двух месяцев до нескольких лет.
Миелодиспластические синдромы (МДС)
Миелодиспластические синдромы (МДС) – разнородная группа хронических заболеваний крови, при которых происходит нарушение созревания клеток крови, с возможным переходом в лейкоз.
- цитопения (снижение клеток крови - эритроцитов, тромбоцитов, лейкоцитов) в периферической крови;
- качественные изменения всех ростков кроветворения;
- высокий риск перехода в острый лейкоз.
Ранее МДС имел различные названия (малопроцентный острый лейкоз, предлейкоз, тлеющая лейкемия и др.).
Заболеваемость МДС составляет 3-5 случаев на 100 тысяч населения в год. Более 85% пациентов старше 60 лет, причем риск развития заболевания с возрастом увеличивается. В 2/3 случаев МДС носит вторичный характер и развивается на фоне других заболеваний крови (множественная миелома, лимфогранулематоз, неходжкинские лимфомы, хронический лимфолейкоз) и после цитостатической терапии при ревматоидном артрите, системной красной волчанке, хроническом гломерулонефрите.
Причина заболевания окончательно не выяснена, определенную роль играют ионизирующее излучение, прием цитостатические препараты, производные бензола.
- одышка, затрудненное дыхание
- слабость, чувство усталости
- появление “синячков” и кровоизлияний на коже, носовые и десневые кровотечения
- лихорадка, частые инфекции
ДИАГНОСТИКА
Клинический анализ крови позволяет выявить анемию (малокровие), которая является самым частым симптомом МДС и обнаруживается в 85-90% случаев, лейкопению (снижение числа лейкоцитов), выявляемую у 50% больных и тромбоцитопению (снижение количества тромбоцитов), проводящую к кровотечениям.
Мазок периферической крови выявляет количественные и качественные изменения клеток крови их тип, форму и размеры, что является важным критерием в диагностике МДС .

Цитогенетический анализ позволяет определить изменения в хромосомном аппарате клеток крови и является ключевым методом диагностики и определения прогноза заболевания.
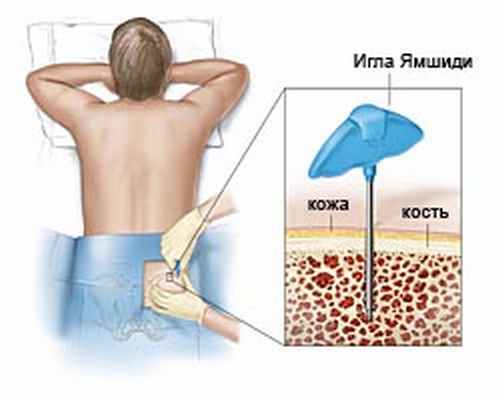
Аспирация (пункция костного мозга) и биопсия (трепанобиопсия) костного мозга – получение небольшого количества (0,2-0,5 мл) аспирата костного мозга и небольшого фрагмент кости. Процедура абсолютно безопасна и выполняется под местной анестезии в течение 2-5 мин. Может также проводиться амбулаторно. Исследования материала биопсий позволяют выявить изменения в костном мозге характерные для МДС.
У 20% пациентов можно выявить увеличение размеров селезенки, печени.
Диагноз МДС основывается исключительно на морфологической диагностике - обнаружении качественных и количественных нарушений кроветворения в одном или нескольких ростках гемопоэза (дизэритропоэз, дизгрануломоноцитопоэз, дизмегакариоцитопоэз), данных цитогенетических исследований.
Выбор лечения определяется вариантом заболевания, прогнозом а также наличием сопутствующих заболеваний, которые могут существенно повлиять на терапию.
Основная цель лечения - получение ремиссии и сохранение качества жизни пациентов.

- Химиотерапия (цитозар, дакоген, мельфалан и др.)
- Трансплантация костного мозга
- Иммуносупрессивная терапия ( антитимоцитарный глобулин и др.)
- Ингибиторы естественной гибели клеток костного мозга (сандиммун, весаноид)
- Ингибиторы ангиогенеза (развития кровеносных сосудов) (талидамид, ревлимид и др.)
- Комбинации указанных методов
При благоприятном прогнозе и минимальных проявлениях заболевания можно ограничиться наблюдением за больным, пока показатели крови и костного мозга остаются стабильными.
При выраженном малокровии (анемии) показано переливание эритроцитарной массы, а при повышенной кровоточивости переливание тромбомассы. В ряде случаев возможно применение ростовых факторов (колониестимулирующие факторы).
Единственным методом лечения, позволяющим существенно увеличить продолжительность жизни больных МДС, является аллогенная трансплантация костного мозга/периферических стволовых клеток, Однако применение аллогенной трансплантации не всегда возможно в связи с пожилым возрастом большинства больных и отсутствием идентичного родственного донора.
До настоящего времени результаты лечения больных МДС остаются неудовлетворительными, в связи с этим не существует общепринятых стандартов лечения, а определены лишь общие подходы к терапии для разных групп больных при разных вариантах заболевания. Поэтому сохранение качества жизни пациентов с МДС в большинстве случаев, выходит на первый план при проведении лечения.
© 2022 ФГБУ «НМХЦ им. Н.И. Пирогова» Минздрава России. Использование материалов сайта полностью или частично без письменного разрешения строго запрещено.
Читайте также:
