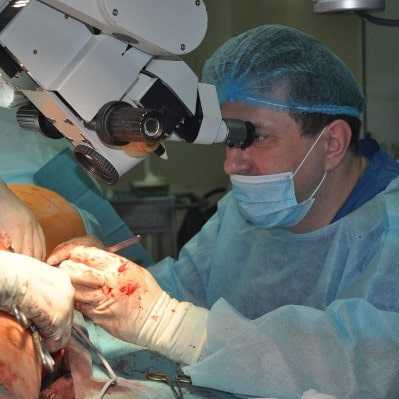
Микрохирургия кровеносных сосудов. Микрохирургическая сосудистая техника
Добавил пользователь Дмитрий К. Обновлено: 30.01.2026
Реконструктивные операции на сосудах. Методы реконструктивных операций на артериях
История реконструктивной хирургии окклюзионных поражений артерий сравнительно невелика. В 1947 г. португальский хирург Дос Сантос сообщил о первой выполненной им эндартерэктомии из бедренной артерии. В настоящее время оперативные вмешательства при облитерируютих заболеваниях артериальных стволов получили распространение почти во всех странах мира. Операции на сосудах отличаются определенным своеобразием и специфичностью. Для их выполнения требуются специальные инструменты и различного размера атравматические иглы. Шовным материалом является пластмассовая нить, составляющая одно целое с иглой.
Для восстановления магистрального кровотока при окклюзионных поражениях артерий используют в основном три вида реконструкций:
1) эндартерэктомию — удаление организованного тромба или атероскле-ротической бляшки вместе с патологически измененной ннтнмой сосуда;
2) протезирование — резекцию окклюзированного сосуда и замещение его тем или иным трансплантатом; 3) шунтирование — восстановление магистрального кровотока с помощью трансплантата в обход пораженного сосуда. Выбор реконструктивной операции при окклюзионных поражениях сосудов зависит от многих факторов. Основными из них являются: локализация и распространенность закупорки, травматичность и длительность операции, общее состояние больного, а также опыт оперирующего хирурга в выполнении того или иного вмешательства. При выборе операции обязательно учитывают этиологию окклюзионного заболевания. Так, при эндартериите (артериите) методом выбора всегда является протезирование или шунтирование, так как результаты эндартерэктомии при этой форме патологии весьма неблагоприятны.
В биологическом отношении наиболее приемлема эидартерэктомия, ибо при таком типе реконструкции сохраняются естественные артериальные магистрали и используется только аутогенная ткань. Эта операция наиболее оправдана при сегментарных стенозах и сравнительно небольших по протяжению (5—10 см) окклюзиях артерий. Существует «открытый» метод эндартерэктомии, при котором операцию производят на глаз, для чего рассекают иа всем протяжении стенку сосуда над пораженным его отделом. Большее распространение получила «полузакрытая» эидартерэктомия, которая проводится из нескольких продольных или поперечных разрезов реконструируемого сосуда. В этих случаях для удаления патологически измененной интимы применяют различные инструменты и приспособления: лопаточки, кольца, петли, специальные баллонные катетеры. Некоторые хирурги с целью уменьшения травматизации стенки артерии используют для эндартерэктомии поток углекислого газа под давлением, который подастся через специальный инструмент между средней и внутренней оболочками сосуда, тем самым разделяя их.
Во Всесоюзном научном центре хирургии разработан и впервые применен в клинической практике метод ультразвуковой эндартерэктомии. Сущность метода заключается в том, что эндартерэктомию производят с помощью специальных волноводов с рабочей частью в виде колец или лопаточек, на которые подаются ультразвуковые колебания, значительно облегчающие удаление патологически измененной интимы. Наиболее радикальным является эверсионный вариант эндартерэктомни, при котором всю измененную интиму под контролем зрения удаляют при выворачивании резецированного сосуда (рис. 1С7).
Наиболее травматичной при распространенных окклюзиях, а в техническом отношении наиболее простой операцией считается шунтирование. Проксимальный и дистальиый анастомозы используемого для шунтирования трансплантата накладывают с артериальной магистралью конец в бок. Принципиально важное значение имеет тот факт, что при этой операции сохраняется кровоток в системе коллатералей пораженных сосудов, в обход которых накладывают шунт.
Операция протезирования по сравнению с эндартерэктомией и шунтированием получила более ограниченное распространение. Это вмешательство наиболее оправдано при небольших по протяжению (5—7 см) закупорках сосудов на почве эндартериита (артериита) или при гипоплазии окклюзированных сосудов. При операциях шунтирования н протезирования в настоящее время в качестве трансплантатов используют в основном синтетические протезы или аутовены. Сосудистые протезы из полимеров вполне себя оправдывают при пластике артериальных стволов диаметром более 7—8 мм (аорта, подвздошные артерии, плечеголов-ной ствол, сонные и подключичные артерии). За рубежом, в частности в США, чаще используют вязаные дакроновые трансплантаты, в СССР-отечественные тканые или плетеные протезы из лавсана или фторлон-лавсана. Основные требования к протезам заключаются в следующем: материал пластмассы по отношению к тканям организма должен быть интактным, стенки протеза должны быть достаточно пористыми, а протез — гофрированным, эластичным и неперегибающимся.
Кроме лавсановых протезов, во Всесоюзном научном центре хирургии используются и другие виды оригинальных отечественных синтетических трансплантатов, в частности полубиологические. Преимущество таких комбинированных протезов заключается в том, что после имплантации пропитывающий стенку крупнопористого трансплантата коллаген рассасывается. По мере его рассасывания окружающие ткани быстро прорастают протез через освобождающиеся поры. Это обеспечивает сравнительно высокую скорость образования неоинтимы трансплантата.
Синтетические протезы непригодны для замещения сосудов диаметром менее 6—7 мм. В этих случаях, как правило, быстро наступает тромбоз. Лучшим пластическим материалом в подобной ситуации является аутовена — большая подкожная вена бедра. Применяемые для протезирования артерий конечностей отдельными хирургами лнофилизированные артерии, взятые у трупа, себя не оправдали, а использование специально обработанных с целью ликвидации антигенных свойств ксенотрансплантатов (гетероартернн) еще не вышло за рамки клинического эксперимента и не может быть рекомендовано для широкого использования.
Информация на сайте подлежит консультации лечащим врачом и не заменяет очной консультации с ним.
См. подробнее в пользовательском соглашении.
Микрохирургия кровеносных сосудов. Микрохирургическая сосудистая техника
Микрохирургия представляет собой новое направление хирургии, которое характеризуется использованием систем оптического увеличения, специального инструментария и шовного материала, применяемого для опсрацнй на структурах весьма малого размера, например на сосудах диаметром менее 2 мм. Благодаря использованию микрохирургической техники значительно расширились возможности реконструктивной хирургии артерий и вен малого диаметра, лимфатических сосудов и нервов, появилась возможность выполнять реплантацию пальцев и кисти при их травматической ампутации. До появления метода микрохирургии такие операции были крайне трудны и даже невозможны.
В Советском Союзе отделение микрохирургии сосудов было создано во Всесоюзном научном центре хирургии (в то время Всесоюзном научно-исследовательском институте клинической и экспериментальной хирургии) по нашей инициативе. Основное направление отделения — реплантация пальцев и кисти средствами микрохирургии. В течение 2 последних лет в стране открылось еще несколько новых центров микрохирургии.
Операционный микроскоп обеспечивает одновременное видение операционного поля дли двух или трех хирургов, снабжен трансфокатором, фотографической и телевизионной камерами. Микрохирургические инструменты нежные, высокоточные; рабочие бранит их выполнены под микроскопом. Особо важными инструментами дли микрохирургических операций являются специальные ножницы, микроскальпель-копьс, прецизионные пинцеты для завязывания нитей, специальные иглодержатели, клипсы для пережатия сосудов малого диаметра и пинцеты для электро-коагуляции. Шовный материал для операций на сосудах малого диаметра имеет толщину 20—25 мкм.
Непременным элементом работы каждого хирурга, занимающегося микрохирургией, является эксперимент. Экспериментальная работа в микрохирургии имеет целью не только отработку и совершенствование технических навыков хирурга, испытание существующих инструментов. создание и отработку новых инструментов, но и создание с помощью микрохирургии принципиально новых биологических моделей на мелких лабораторных животных. Например, во Всесоюзном научном центре хирургии средствами микрохирургии выполнено более 500 экспериментов на нелинейных и линейных крысах: на них производились опыты но наложению швов на брюшную аорту, каудальную вену, по пересадке почки. В настоящее время имеются одно-, трех- и четырехпочечная модели пересадки почки у крыс. Успешно проведен сложный эксперимент с применением микрохирургии на обезьянах — пересадка пальца со стоны на кисть с хорошими отдаленными результатами, открывшие путь, для успешного применения этой операции в клинике.
Одной из областей применения микрохирургической техники в клинике стало выполнение микрососудистых анастомозов на артериях голени у больных с окклюзнонными заболеваниями сосудов нижних конечностей. Малый диаметр этих артерий (1,5—2 мм) делает крайне трудным выполнение сосудистого анастомоза без оптического увеличения.
Применение микрохирургической техники позволяет накладывать анастомоз между трансплантатом (аутовеиой) и артериями голени весьма точно, прецизионно и тем самым обеспечивать его проходимость и наилучшую функцию. Как уже указывалось, микрохирургия сделала возможной реплантацию пальцев и кисти.
Реплантация пальцев и кисти, отторгнутых в результате травмы, выполняется пока в немногих микрохирургических центрах мира из-за сложности и длительности этой многочасовой операции. Для развития этого направления хирургии особенно важное значение приобретают вопросы создания специализированных высокооснашенных отделений, а также пропаганда соответствующих знаний как среди медицинских работников, так и среди населения. Операция реплантации пальца (кисти) может быть разделена на три этана: 1) предварительный (организационные основы); 2) саму операцию реплантации; 3) послеолерационный период (реабилитация).
Особо важное значение имеет быстрое обеспечение «холодовой ишемии», предшествующей реплантации, т. е. помещение ампутированного пальца или сегмента конечности в изотонический раствор хлорида натрия температуры 4°С. Следующий этап — первичная обработка раны и будущего трансплантата с обязательной маркировкой клипсами артерий, вен и нервов. Непосредственно сама операция реплантации пальца (кисти) может быть разделена на: 1) травматологический этап (обработка и укорочение костей, остеосинтез, шов сухожилий разгибателей и сгибателей); 2) сосудистый этан (шов артерии пальца и двух вен); 3) шов нервов и кожную пластику. В послеоперационном периоде после восстановления в реплантированном пальце кровообращения больному вводят растворы рсополиглюкнна, гепарина, а позднее антикоагуляиты непрямого действия. Назначают строгий постельный режим не менее чем на 10 дней после операции. Используется гипербарическая оксигенация.
Опыт отделения микрохирургии Всесоюзного научного центра хирургии на I мая 1980 г. составил 228 операций реплантации пальцев у 156 больных и 13 реплантаций кисти. Прижили после реплантации 135 пальцев и 7 кистей. Принятое до сих лор деление на полную и неполную (сохранение кожного лоскута) ампутации утратило категоричность, так как палец с полным перерывом артериального кровообращения, хотя бы и с сохраненным кожным мостиком, является полностью нежизнеспособным. Факт перерыва магистрального кровотока достоверно доказывается методом ультразвуковой флоуметрии.
Микрохирургия. Общие принципы микрохирургической техники.
Микрохирургия как новый метод оперативной техники возникла на I основе соединения обычных хирургических приемов с новыми принципами оперирования, связанными с применением специального микрохирургического инструментария и различных оптических средств. В качестве оптических средств для увеличения объекта операции используют очки, лупы, операционные микроскопы, дающие увеличение от 1,5 до 40 раз. Для выполнения манипуляций под таким увеличением в нашей стране и зарубежом созданы специальные наборы инструментов. Для разъединения тканей применяют глазные скальпели, скальпели с алмазным лезвием, микрохирургические ножницы, рабочая поверхность которых уменьшена, а кольца заменены пружинным механизмом. Микрохирургические иглодержатели отличаются от обычных размерами рабочей поверхности (ее длина не превышает 1 см, а ширина — 1 мм), а также наличием пружинного механизма. Созданы также иглодержатели, которые удерживают иглу с помощью пневматического или гидравлического механизма. Для фиксации тканей созданы различные микрокрючки, пинцеты. цапки, микроподъемники.
Шовный материал должен отвечать особым требованиям. Предел прочности на разрыв шовной нити должен быть достаточным для того, чтобы с помощью шва сблизить сшиваемые ткани и предупредить их расхождение. Применяют синтетические нити толщиной 15—55 мкм (7/0 11/0). Нить, окрашенная в темный цвет, должна быть абсолютно гладкой, обладать высокой степенью несмачиваемости, ареактивностью, легко завязываться с помощью инструментов.
Атравматические иглы, которые применяют в микрохирургии, по диаметру приближаются к шовному материалу, они острые и изогнуты на 3/4 окружности. Часто используются прямые иглы.

При выполнении операции под операционным микроскопом хирург сидит в кресле с подлокотниками, что обеспечивает фиксацию предплечья и кисти, возможность выполнять тонкие и точные движения только пальцами. Для предохранения операционного поля от высыхания его постоянно орошают, а затем жидкость отсасывают тонкими трубками. Кровотечение из мелких сосудов останавливают с помощью электрокоагулятора.
Микрохирургическая техника при соединении мелких кровеносных сосудов. Методика восстановления целости артерий и вен такая же. как и методика наложения обычного ручного сосудистого шва. Чаще применяют круговой шов с двумя фиксирующими лигатурами. При этом он может быть как непрерывным, так и узловым.
Для предупреждения сужения диаметра соединяемых сосудов в месте их соединения в стенку формируемого анастомоза часто вшивают «заплатку» из вены. Для этого на протяжении 4—5 мм продольно рассекают переднюю стенку обоих концов сосуда. Заднюю стенку анастомоза сшивают непрерывным швом, а в оставшийся овальный дефект по передней поверхности сосудов вшивают «заплатку» из аутовены. Увеличить диаметр соединяемых сосудов можно также путем косого пересечения сосудов.
Часто при наложении анастомоза на очень мелкие кровеносные сосуды в месте бифуркации образуют кромку из их ветвей.
В нейрососудистой хирургии, хирургии коронарных артерий, приреконструктивных операциях на сосудах голени применяют шунтирование мелких кровеносных сосудов.
Обычно для наложения обходного анастомоза используют аутовену. Применение микрохирургической техники при шунтировании обеспечивает точность выполнении самого сосудистого шва, минимальное травмирование стенки артерии и аутовены, что значительно повышает эффективность функционирования шунта.
ННИИПК им. акад. Е.Н. Мешалкина Минздравсоцразвития РФ
ФГБУ «Национальный медицинский исследовательский центр им. акад. Е.Н. Мешалкина» Минздрава России, Новосибирск, Россия
ФГБУ «Национальный медицинский исследовательский центр кардиологии» Минздрава РФ, Москва, Россия
- SPIN РИНЦ: 6756-8930
- Scopus AuthorID: 7006967737
- ResearcherID: B-7762-2019
Институт клинической кардиологии им. А.Л. Мясникова ФГБУ «НМИЦ кардиологии» Минздрава России, Москва, Россия
- SPIN РИНЦ: 8710-6679
- Scopus AuthorID: 7006804867
- ResearcherID: O-8009-2018
ФГУ ННИИПК им. акад. Е.Н. Мешалкина Минздравсоцразвития России
Новосибирский НИИ патологии кровообращения им. акад. Е.Н. Мешалкина;
Российский кардиологический научно-производственный комплекс Минздравсоцразвития России, Москва
ФГБУ «Национальный медицинский исследовательский центр им. акад. Е.Н. Мешалкина» Минздрава России, Новосибирск, Россия, ФГБУ «Национальный медицинский исследовательский центр кардиологии» Минздрава России, Москва, Россия
Микрохирургия коронарных артерий с использованием операционного микроскопа
Журнал: Хирургия. Журнал им. Н.И. Пирогова. 2019;(1): 60‑64
Представлен мировой опыт использования операционного микроскопа при коронарном шунтировании. Приведены данные, свидетельствующие о важной роли применения операционного микроскопа и микрохирургической техники для выполнения коронарных анастомозов. Благодаря высокому оптическому увеличению формирование коронарных анастомозов стало более точным, что положительно сказывается на послеоперационной проходимости шунтов.
В настоящее время заболевания сердечно-сосудистой системы являются ведущей причиной смертности как в Российской Федерации, так и во всем мире [1—3]. Существенную часть заболеваний системы кровообращения с высокой заболеваемостью и смертностью составляет ишемическая болезнь сердца (ИБС) [2, 3]. Основной метод хирургического лечения ИБС — коронарное шунтирование (КШ), которое остается эффективным способом лечения ее наиболее тяжелых форм. Без сомнения, вопросы совершенствования основного хирургического метода лечения такой эпидемиологически значимой болезни, как ИБС, являются сегодня актуальными и даже приоритетными.
Цель исследования — освещение опыта коронарной хирургии с использованием операционного микроскопа, а также обоснование более тщательного изучения и возможности более широкого применения данного метода оптического увеличения при выполнении КШ.
История коронарной микрохирургии
Для создания применяемой в настоящее время технологии прямой реваскуляризации миокарда медицинская наука прошла путь более чем в 100 лет. Прежде всего следует упомянуть выдающегося исследователя A. Carrel, который в 1902 г. описал методику сосудистого шва, за которую он был удостоен Нобелевской премии в 1912 г. [4, 5]. Помимо этого, в 1910 г. A. Carrel провел эксперименты по аортокоронарному шунтированию (АКШ) на животных. Несмотря на неудачные результаты эксперимента, нельзя не признать, что А. Carrel внес огромный вклад в хирургию ИБС.
Первое успешное аутовенозное АКШ выполнил R. Favaloro [6] в 1967 г. За несколько лет до этого произвести аутовенозное АКШ пытались D. Sabiston, H. Garret, D. Kann, M. DeBakey, но систематическое внедрение аутовенозного АКШ в хирургию ИБС принадлежит R. Favaloro [5—8]. В нашей стране первое АКШ выполнил М.Д. Князев в 1970 г. во Всесоюзном научном центре хирургии. В том же году в Институте сердечно-сосудистой хирургии им. А.Н. Бакулева АМН СССР А.В. Покровский успешно произвел первую операцию аутовенозного АКШ в сочетании с аневризморафией левого желудочка [5].
Как известно, аутовенозное АКШ с момента внедрения в клиническую практику долгое время было преобладающим методом коронарной реваскуляризации. Более 20 лет микрохирургическая техника и оптическое увеличение практически не использовались в коронарной хирургии, так как аутовенозное шунтирование чаще всего не требовало значительного увеличения операционного поля [5, 9].
Первое успешное маммарно-коронарное шунтирование (МКШ) выполнил В.И. Колесов [10] в 1964 г. Он разработал технику МКШ и внедрил ее в коронарную хирургию. В.И. Колесов проводил операции МКШ на работающем сердце, в качестве доступа используя левостороннюю торакотомию. К 1971 г. В.И. Колесов сделал по своей методике более 400 операций у тяжелых больных, в большинстве случаев результаты были хорошими [5, 10].
Вскоре процедуру МКШ ввел в широкую практику G. Green [11—14], он первым применил операционный микроскоп и микрохирургические инструменты для проведения КШ и один из первых показал эффективность и безопасность использования внутренней грудной артерии в качестве коронарного шунта. Процедура МКШ стала стандартом реваскуляризации миокарда, однако методика с использованием микрохирургической техники и операционного микроскопа не получила широкого распространения в коронарной хирургии.
Операционный микроскоп появился в медицине гораздо раньше, чем был внедрен в коронарную хирургию. Микроскоп был введен в клиническую практику C. Nylen [15] в 1921 г., который превратил обычный лабораторный микроскоп в операционный микроскоп для использования в микрохирургии уха. Начиная с 1946 г., операционный микроскоп стал широко применяться хирургами в офтальмологии, началось производство специальных микрохирургических инструментов [4, 16, 17].
Известный опыт использования операционного микроскопа в хирургии ИБС ограничен несколькими центрами. Впервые возможности операционного микроскопа в коронарной хирургии представил G. Green [20] в эксперименте на животных. Он же показал, что использование высокого оптического увеличения посредством операционного микроскопа является важным условием качества формирования коронарных анастомозов [11—14]. Хирург из Японии K. Katsumoto [21] в 90-х годах описал успешное применение операционного микроскопа в ряде операций К.Ш. Операционный микроскоп для выполнения шунтирования коронарных артерий используют в больнице St Luke’s-Roosevelt Hospital Center, Нью-Йорк, США [22].
В нашей стране операционный микроскоп в микрохирургии коронарных артерий используется в Национальном медицинском исследовательском центре кардиологии, Москва (Р.С. Акчурин, А.А. Ширяев) [9, 23, 24], Национальном медицинском исследовательском центре им. акад. Е.Н. Мешалкина, Новосибирск (С.А. Альсов), Федеральном центре сердечно-сосудистой хирургии, Хабаровск (А.Н. Семченко) [25] и Российском научном центре хирургии им. акад. Б.В. Петровского, Москва (А.В. Лысенко, Ю.В. Белов) [26].
Важность применения операционного микроскопа в коронарной хирургии
Успех КШ напрямую зависит от ранней и отдаленной проходимости шунта коронарной артерии, характера поражения коронарного русла и диаметра шунтируемых артерий в зоне анастомозирования [27]. Как известно, наибольшая часть окклюзий, приводящих к послеоперационной дисфункции шунта, случается в ближайшем периоде после операции [28]. Причиной ранней окклюзии, как правило, является тромбоз шунта, возникающий в раннем послеоперационном периоде [29—32]. Согласно данным литературы [28, 31, 33—35], окклюзия шунта, обусловленная тромбозом, происходит в срок от первых суток после выполнения вмешательства и до 1 мес послеоперационного периода. В последних исследованиях [29, 32, 36] показано, что основными причинами ранней (до 1 мес) и среднеотдаленной (до 1 года) дисфункции аутовенозных шунтов являются тромбоз шунта, гиперплазия интимы и технические ошибки наложения анастомоза, приводящими к тромбозу графта.
Влияние использования операционного микроскопа на результаты коронарной и сосудистой микрохирургии
Применение операционного микроскопа целесообразно при формировании анастомозов сосудов малого диаметра. D. Pieptu [50] сообщает о необходимости использования операционного микроскопа в реконструктивной хирургии и нейрохирургии, но для микрохирургии сосудов размером более 2 мм предлагает использовать только хирургические лупы. Некоторые экспериментальные и клинические исследования конца прошлого века также рекомендуют считать низшим пределом возможности использования хирургических луп сосуды диаметром 2 мм [48, 49]. D. Ross и соавт. [51] в ретроспективном анализе опыта 151 операции пересадки свободного тканевого лоскута не нашли различий в частоте осложнений между группами с применением хирургических луп и операционного микроскопа, но сообщили о необходимости применения операционного микроскопа, если диаметр анастомозируемых сосудов составляет менее 1 мм. Необходимость использования операционного микроскопа при операциях на сосудах менее 1 мм показана и в других работах [12, 52]. P. Andrades [53] в эксперименте на животных показал, что при формировании анастомоза сосудов диаметром 1,5 мм целесообразнее использовать операционный микроскоп, чем хирургические лупы, так как применение микроскопа в этом случае статистически значимо сокращало время манипуляции и увеличивало 24-часовую проходимость сосудов. Клинические исследования в таких областях, как реконструктивная, детская, сосудистая хирургия, также показывают необходимость применения операционного микроскопа при вмешательствах на сосудах менее 1,5 мм [47, 54, 55].
G. Green [11, 12], накопив большой опыт в микрохирургии коронарных артерий, показал важность использования операционного микроскопа в формировании дистального маммарно-коронарного анастомоза. G. Green [13] назвал микроскоп основой успеха результатов маммарно-коронарного шунтирования. В исследовании, посвященном 20-летнему опыту использования внутренней грудной артерии для шунтирования коронарных артерий, отмечено, что использование операционного микроскопа можно рассматривать в качестве независимого предиктора смертности, при этом достоверно снижается смертность при КШ с отношением рисков 0,76 [14]. G. Green [13, 14] был убежден, что использование операционного микроскопа с 8—12-кратным увеличением необходимо для проведения как аутоартериального, так и аутовенозного КШ.
Наибольший в мире опыт применения операционного микроскопа — около 7000 операций с 1986 г. — имеют Р.С. Акчурин и А.А. Ширяев и соавт. В их исследованиях показано, что применение микрохирургических методов и операционного микроскопа достоверно повышает выживаемость и эффективность коронарной хирургии в отдаленном периоде [9, 27]. Авторы выявили, что в случае использования операционного микроскопа интраоперационно снижается количество эндартерэктомий и увеличивается количество подвергшихся шунтированию коронарных артерий диаметром менее 1,5 мм [9]. При использовании операционного микроскопа и микрохирургической техники наблюдаются более низкая летальность, меньшая заболеваемость нефатальным инфарктом миокарда, сердечной недостаточностью и меньшая частота повторных вмешательств в отдаленном периоде [9, 23].
Крупный опыт использования операционного микроскопа в микрохирургии коронарных артерий имеет С.А. Альсов и соавт. — около 1500 операций с 2006 г. Используемое рабочее увеличение для формирования дистальных анастомозов составляет 4—10 крат, для проксимальных анастомозов — 2—4 крат. Установлено, что в рутинной практике для выполнения вмешательств большее увеличение, как правило, не требуется (хотя технически это возможно). Данное увеличение позволяет проводить шунтирование коронарных артерий малого диаметра пациентам женского пола, пациентам с сахарным диабетом и диффузным коронарным атеросклерозом, которых ранее признавали неоперабельными.
В последние годы свой опыт использования операционного микроскопа в хирургии коронарных артерий опубликовали А.Н. Семченко и соавт. [25]. Они показали, что применение микрохирургической техники и операционного микроскопа при КШ безопасно, исключает риск технической ошибки как возможной причины окклюзии шунта в ближайшие сроки после операции, не увеличивает частоту сердечно-сосудистых осложнений на госпитальном этапе. В опыте первых 100 операций с применением операционного микроскопа 82 (82%) пациентам в раннем послеоперационном периоде оценена проходимость шунтов, выявлена проходимость 93,4% шунтов. В послеоперационном периоде получен приемлемый уровень летальности, сердечно-сосудистых и неспецифических осложнений, не превышающий 2% [56].
Опыт использования операционного микроскопа имеют хирурги РНЦХ им. акад. Б.В. Петровского во главе с А.В. Лысенко и Ю.В. Беловым. Анализируя свой опыт 17 операций, они пришли к выводу, что применение операционного микроскопа позволяет уверенно формировать дистальные анастомозы с артериями, диаметр которых составляет 1 мм и менее, в том числе пациентам, которым в других учреждениях отказано в оперативном вмешательстве ввиду малого диаметра и диффузного дистального поражения коронарных артерий. Хорошие результаты процедуры КШ у пациентов с тяжелым многососудистым поражением коронарного русла отмечены в [26].
Таким образом, несмотря на то что в коронарной хирургии приходится работать с сосудами диаметром 1—2 мм, применение операционного микроскопа в этой области медицины до сих пор не распространено. По словам основоположника коронарной микрохирургии G. Green [13], парадоксально, что кардиоторакальная хирургия, которая стоит в авангарде столь большого количества инноваций, станет последней из хирургических специальностей, которая признает важность использования микроскопа. Как показано в данном обзоре, использование операционного микроскопа может влиять на хирургическую технику выполнения дистального коронарного анастомоза и раннюю проходимость шунтов, но опыт его применения в коронарной хирургии очень ограничен. Безусловно, сегодня необходимо более тщательное изучение результатов применения операционного микроскопа при шунтировании коронарных артерий, но также целесообразно широкое внедрение микроскопа в клиническую практику.
Шунтирование артерий голени и стопы при гангрене
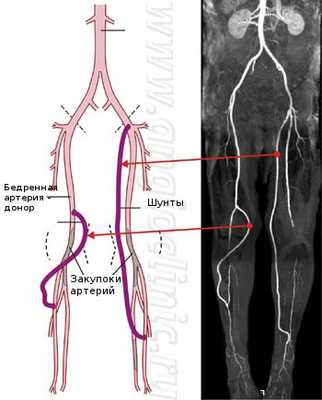
Шунтирование сосудов (Bypass) - операция создания обходного пути, при закупорке сосуда атеросклеротическими бляшками или тромбами. Шунтирование артерий применяется при тяжелых формах недостаточности артериального кровообращения. Операция шунтирования позволяет сохранить конечность при гангрене. Шунт проводится от артерии, расположенной выше закупорки к артерии ниже поражения, полностью восстанавливая кровоснабжение пораженного органа.
Чаще всего для шунтирования артерий нижних конечностей используются собственные подкожные вены пациента, которые обрабатываются таким образом, чтобы нести кровь к ноге, а не обратно.
Преимущества лечения в Инновационном сосудистом центре
Инновационный сосудистый центр - единственная в нашей стране клиника, где комплексно применяются уникальные микрохирургические, эндоваскулярные и пластические методы для лечения больных с начавшейся гангреной и диабетической стопой.
Сосудистые хирурги нашей клиники успешно применяют метод восстановления кровообращения в конечности с помощью микроскопа, разработанный в университетской клинике г. Аахена (Германия), для пациентов с поражением мелких артерий голени и стопы.
Это микрохирургическое шунтирование артерий голени и стопы с помощью собственной подкожной вены пациента. Микрохирургия позволяет выполнять успешное соединение венозных шунтов и мельчайших сосудов с высоким качеством. Это дает возможность врачам нашей клиники сохранять конечности больным, уже приговоренным к ампутациям.
С 2011 года наша клиника является лидером в России по применению шунтирования артерий голени и стопы и имеет самые лучшие результаты по сохранению конечностей на фоне атеросклероза малых артерий.
Показания к шунтированию
На шунтирование отбираются пациенты, сохранные по общему состоянию. Поэтому проводится детальная оценка сопутствующих заболеваний, ожирения и других факторов риска для жизни. Только непосредственная угроза жизни является поводом для риска у больных с тяжелыми сопутствующими заболеваниями.
Необходимо детально оценить сосудистое русло с помощью УЗИ диагностики и ангиографии, чтобы сформулировать четкую концепцию для операции.
Необходима тщательная оценка подкожных вен, так как от их качества зависит успех шунтирования и продолжительность работы шунта. Использование в качестве шунтов искусственных протезов является операцией отчаяния, так как такие шунты закрываются в половине случаев в течение 2 лет.
Предоперационная подготовка
Для определения показаний к операции бедренно-тибиального шунтирования пациента необходимо обследовать с точки зрения сосудистых поражений и общего состояния здоровья.
Для диагностики сосудистых поражений применяют следующие методы:
- УЗИ артерий нижних конечностей с измерением давления на лодыжках
- Мультиспиральная компьютерная томография с контрастированием аорты и артерий нижних конечностей
- Рентгеновская контрастная ангиография - чаще всего используется для точного определения возможности ангиопластики, вместо шунтирования
- Дуплексное сканирование подкожных вен - для определения пригодности их в качестве шунта
Общая диагностика пациента включает в себя:
- Общие анализы крови и мочи
- Биохимический анализ крови
- Анализы крови на сифилис, ВИЧ и гепатиты
- Электрокардиограмма (ЭКГ)
- УЗИ сердца (эхокардиография)
- УЗИ сонных артерий
- ЭГДС (гастроскопия желудка)
- Рентгенография грудной клетки
Собственно подготовка к операции заключается в уменьшении отека больной ноги. Для этого пациенту предварительно устанавливают продленную перидуральную анестезию (чтобы он мог лежать). Перед операцией в мочевой пузырь устанавливают катетер, для контроля за выделением мочи. С целью введения лекарственных препаратов устанавливают внутривенный катетер в подключичную вену.
Накануне операции пациенту даются успокоительные препараты, которые дополняются премедикацией непосредственно перед подачей больного в операционную.
Обезболивание при шунтировании
Операции на артериях нижних конечностей в нашей клинике проводятся под эпидуральной анестезией. Последняя подразумевает введение анестезирующего препарата в область эпидурального пространства позвоночника. Такой вид обезболивания позволяет эффективно устранить болевые ощущения во время операции и в раннем послеоперационном периоде.
Для контроля за состоянием сердечно-сосудистой системы мы используем следящие мониторы, которые подключаются к грудной клетке для снятия ЭКГ и к плечу для контроля артериального давления. С целью улучшения насыщения крови кислородом пациенту дается кислородная маска.
![]()
Ход операции
Пациент укладывается в операционной на спину. Под колено оперируемой ноги подкладывается специальный валик.
Начинается операция с ревизии (оценки) артерий голени, к которым должен подойти шунт. Для доступов к артериям голени используются разрезы длиной 4-6 см в паховой области и на голени (стопе). Затем проводится доступ к артерии на бедре, чтобы оценить ее пригодность в качестве донора для шунта.
После оценки артерий хирург приступает к подготовке венозного шунта. Через небольшие разрезы выделяется подкожная вена на голени, затем на бедре.
Первым выполняется соединение большой подкожной вены с бедренной артерией. После сшивания анастомоза запускается кровоток. Пульсация шунта возможна до первого венозного клапана.
Затем специальный инструмент вальвулотом проводится в венозный шунт и производится иссечение клапанов. Это необходимо, чтобы кровоток мог пойти по этой вены из бедренной артерии к артерии голени. Без рассечения клапанов кровоток по шунту не пойдет.
После удаления клапанов хирург оценивает вену на УЗИ и находит сбросы крови по шунту в боковые ветви. Перевязка этих ветвей производится через отдельные маленькие разрезы. Это необходимо для того, чтобы кровь по венозному шунту двигалась в направлении стопы, а не уходила в боковые ветви.
Когда будут перевязаны все сбросы по венозному шунту мы приступаем к сшиванию шунта и артерии на голени или стопе под микроскопом. Большое увеличение на этом этапе необходимо для успеха, так как любая ошибка в приведет к неудаче всей операции шунтирования.
Затем запускается кровоток и проверяется работа шунта по УЗИ. Если кровообращение восстановлено, то операция заканчивается ушиванием ран. Если есть сомнения, то выполняется контрольная ангиография и, при необходимости, ангиопластика измененной артерии ниже шунта.
Варианты операции
Этот метод предполагает использование собственной большой подкожной вены пациента, которая остается на своем привычном месте, однако с помощью особых приемов по ней пускается артериальный кровоток в мелкие артерии на голень и стопу. Бедренно-тибиальное шунтирование является основным способом лечения критической ишемии и угрожающей гангрены. Успех ,при правильных показаниях к операции, достигается у 90% больных с начинающейся артериальной гангреной (некрозы пальцев, артериальные трофические язвы). Сохраняется возможность ходить на своей ноге.
Венозный шунт можно делать из вен ног или рук, если не сохранена основная подкожная вена.
Самая маленькая артерия голени меньше всего поражена атеросклеротическим процессом. Однако ее емкости часто не хватает для полноценной работы аутовенозного шунта, что приводит к тромбозу. Особенностями операций на малоберцовых артериях является необходимость четко оценить объем кровотока. Для разгрузки артерии нередко используются специальные приемы - разгрузочные фистулы с венами далеко от анастомоза.
Часто пациентам отказывают в сохранении ноги по причине отсутствия хорошей длиной и проходимой артерии на голени, однако при этом, мы нередко видим отдельные участки и ветви артерий с сохраненным кровотоком. Нашим ведущим сосудистым хирургом Калитко И.М. для таких ситуаций разработана методика многоэтажного шунтирования артерий голени. Нередко выполняется несколько коротких шунтов к отдельным проходимым сегментам артерий. Важным условием для нормальной работы такой сложной реконструкции является достоверная оценка приходящего и распределяющегося объема крови. При перегрузке шунтов могут использоваться разгрузочные фистулы.
Возможные осложнения после шунтирования
- Кровотечение во время операции - редкое явление, обычно кровопотеря составляет 300-500 мл и не требует восполнения.
- Нагноение послеоперационных ран - может наблюдаться у ослабленных пациентов с диабетом и гнойным процессом на стопе. Чаще всего протекает благоприятно, но задерживает выздоровление пациента.
- Реперфузионный синдром - состояние конечности, связанное с восстановлением кровотока на фоне критической ишемии. Характеризуется резким отеком конечности, болевыми ощущениями, гиперемией. Обычно проходит через 2-3 недели после операции.
- Лимфорея - продолжительное истечение лимфы из разрезов. Редкое осложнение в нашей клинике, причиной которого бывает повреждение увеличенных лимфоузлов в паховой области при хирургическом доступе к бедренной артерии.
- Образование ложных микотических аневризм шунта - редкое осложнение, которое наблюдается при присоединении инфекции к аутовенозному шунту. Является опасным состоянием, так как может привести к позднему разрыву шунта или его тромбозу.
- Тромбоз аутовенозного шунта может быть ранним или поздним. Ранние тромбозы связаны с недостаточным оттоком по шунту из-за плохих артерий ниже шунта или с высокой свертываемостью крови. Поздние тромбозы связаны с прогрессированием атеросклероза в артериях оттока или притока и рубцеванием самого шунта. Использование антикоагулянтов и контрольной ангиографии после шунтирования позволяет устранить причины ранних тромбозов. Для предупреждения поздних необходимо наблюдение у сосудистого хирурга.
Наблюдение и прогноз после шунтирования
Успех операции бедренно-дистального шунтирования зависит от очень большого количества факторов. Помимо ювелирной техники исполнения, грамотной интраоперационной оценки состояния артерий и знания причин послеоперационных тромбозов очень важным элементом успеха является тщательное послеоперационное наблюдение.
Перед выпиской больного из стационара мы обязательно проводим ультразвуковое исследование шунта. При выявлении оставшихся венозных сбросов мы немедленно их устраняем.
Через месяц, полгода и год после операции пациент приглашается на контрольные осмотры сосудистого хирурга с обязательным выполнением УЗИ. Если при УЗИ диагностике выявляются проблемы в функции шунта, то мы проводим пациенту мультиспиральную компьютерную томографию шунта и артерий ног.
При своевременном выявлении сужений мы можем устранить их с помощью ангиопластики и стентирования.
Успех операции шунтирования артерий нижних конечностей составляет в нашей клинике 95%. Через год проходимы 85% шунтов. Первичная проходимость в течение 3лет составила 70%, вторичная проходимость (после дополнительных вмешательств) - 88% шунтов. Сохранить конечность в течение 3-х лет наблюдений нам удалось у 88% пациентов.
Читайте также:
- Клиника и диагностика аллергического ринита
- Жировые клетки, коллагеновые волокна при лучевой болезни. Лучевое поражение скелетных мышц
- Диагностика острой сердечной недостаточности. Лечение острой сердечной недостаточности.
- Применение ингибиторов протонной помпы в интенсивной терапии и реанимации
- Симптомы риносинусита с ВИЧ и его лечение