Морфология опухолей надпочечников. Андростеромы
Добавил пользователь Владимир З. Обновлено: 27.01.2026
Первичные опухоли надпочечников относятся к одному из важных и трудных в диагностическом и лечебном плане разделов клинической онкологии. Эти заболевания объединяют группу различных вариантов опухолей, в число которых входят и гормональноактивные опухоли надпочечников. Общепринято классифицировать опухоли надпочечников на доброкачественные и злокачественные. Это имеет важное практическое значение относительно прогноза заболевания, так как хирургическое удаление доброкачественной опухоли ведет к полному выздоровлению, тогда как прогноз при злокачественных новообразованиях сомнителен. При этом морфологические признаки злокачественности опухолей надпочечников дискутируются до настоящего времени [13,17].
Литература
1. Авдеева Т.Ф., Казеев К.Н., Демидов В.Н., Артемова A.M. Возможности неинвазивных методов исследования в топической диагностике гормонально–активных опухолей надпочечников // Хирургия надпочечников. Материалы I Всесоюзного симпозиума.–Сн.–Петербург.–1992.–С.54–56.
2. Баронин А.А. Первичные и метастатические опухоли надпочечников (клиника, диагностика, лечение, морфологические и биологические факторы прогноза). // Дисс. . докт. мед. наук. Росс. АМН. РОНЦ им. Н.Н. Блохина М.; 2003
3. Бирюкова М.С. Эндокринные заболевания и синдромы. Вирилизм. –Знание. – М. – 2000. –с. 165.
4. Блинова Л.И. Лимфатическая и кровеносная система надпочечников человека в возрастном аспекте // Автореф. дисс. . канд. мед. наук. –Иваново.–1971.–С.24.
5. Бондарь Ю.С., Котова Л.Н., Кулагин СВ. и соавт. Феохромоцитома злокачественного течения с множественными тромбоэмболическими проявлениями // Пробл. эндокринол.–1988.–т.34,№5.–с.43–45.
6. Григорян СВ., Кучинский Т.А., Молчанов Г.В. Особенности клинического течения и диагностики гигантских опухолей коры надпочечников // Тер.архив.–1989.–№ 1.–е. 124–128
7. Зографски Ст. Эндокринная хирургия. София.–1977.–с.594.
8. Казанцева И.А., Калинин А.П., Полякова Г.А. и др. Клиническая морфология кортикальных опухолей гиперплазии надпочечников // Пособие для врачей.– М.–1998.–с.З–18
9. Калинин А.П., Давыдова И.В. Феохромоцитома и сердечно–сосудистая система // Тер.архив.–1982.–т.54.–№5.–с. 143–148.
10. Керцман В.П. Клиника и лечение гормонпродуцирующих опухолей коры надпочечника // Ереван–Айастан.–1977.–с.319
11. шаткин Н.А. О редких формах феохромоцитомы // Урология.– 196О. – №2. –с.42–46.
12. Петров Ю.Л., Стебакова Л.Н. СИФ–клетки и их отношение к APUD–системе (некоторые вопросы функциональной морфологии в норме и при экспериментальных гипертензиях) // APUD–система: онкорадиологические и общепатологические аспекты.–Обнинск.–1988.–с.18–19.
13. Пилькевич О.Я. Методические аспекты эндохирургических вмешательств при новообразованиях надпочечников // Автореф.дисс.канд.мед.наук. Сн.–Петербург.–2000.–с.23.
14. Полякова Г.А., Безуглова Т.В., Богатырев О.П. и соавт. К морфологической характеристике феохромоцитом. Мат. 4–го Российского симпозиума по хирургической эндокринологии «Хирургия эндокринных желез».–Уфа.–1995.–с. 107–111.
15. Фромен Л.А., Фелиг Ф., Бродус А.Е., Бакстер Дж.Д. Клиничесие проявления эндокринных заболеваний. Эндокринология и метаболизм. (Под ред. Фелига Ф., Бакстера Дж.Д., Бродуса А.Е., Фромена Л.А.) // М.–Медицина.–1985.–т.1.–с.11–34.
16. Chinnaiyan A.M., O’Rourke К., Yu G.L., Lyons R.H., Garg M., Duan D.R., Xing L., Gentz R., Ni J., Dixit V.M. Signal transduction by DR–3, a death domain–containing receptor related to TNFR–1 and CD95. Science.–1996.–Vol.274.–p.990–992.
17. Darmon A.J., Nicholson D.W., Bleackley R.C. Activation of the apoptotic protease CPP32 by cytotoxic T–cell–derived granzyme B. Nature.–1995.–Vol.377.–p.446–448.
18. Enari M., Talanian R.V., Wong W.W., Nagata S. Sequential activation of ICE–like and CPP32–like proteases during Fas–mediated apoptosis. Nature.– 1996. –V ol.380. – p.723–726.
19. Gajewski T.F., Thompson CD. Apoptosis meets signal transduction: elimination of BAD influence. Cell.–1996.–Vol.87.–p.589–592.
20. Grimelius L. The argirophil reaction in islet cells of adult human pancreas studied with a new silver procedure. Acta Soc.Med.Upsal.–1968.–Vol.73.–p.271–294.
21. Heller R.A., Song K., Onasch M.A., Fischer W.H., Chang D., Ringold G.M. Complementary DNA cloning of a receptor for tumor necrosis factor and demonstration of a shed form of the receptor. Proc. Natl. Acad. Sci. USA.–1990.–Vol.87.–p.6151–6155.
22. Kakeji Y., Machara Y., Orita H. et al. Argyrophilic mucleolar organizer region in endoscopically obtained biopsy tissue: A useful predictor of nodal metastasis and prognosis in»carcinoma of’the stomach //J.Am.College of Surgeons.–1996.–Vol. 182.–N6.–p.482–487.
23. Knudson СМ., Tung K.S., Tourtellotte W.G., Brown G.A., Korsmeyer S.J. Bax–deficient mice with lymphoid hyperplasia and male germ cell death. Science.–1995. –Vol.270.–p.96–99.
24. Masson C, Andre C, Arnoult J., Geratid G., Herman–dez–Verdun D. Nucleolur antigen specific for the dense fibrillar component of nucleoli. J.Cell.Sci. – 1990. – Vol.95. –p.371–381.
25. Medeiros L J., Weiss L.M. New developments in the pathologic diagnosis of adrenal cortical neoplasms // A review Am.J.Clin.Pathol.–1992.–Vol.97.–p.–73–83.
26. Nagata S. Apoptosis by Death Factor. Cell.–1997.–Vol.88.–p.355–365.
27. Ochs R.Z., Lischwe M.A., Spohn W.H., Busch H. Fibrillarin: a new protein of the nucleolus indentified by autoimmune sera//Biol. Ctll.–1985.–Vol.54.–p.123–134.
28. Patel Т., Gores G.J. Apoptosis and hepatobiliary diseases // Hepatol. – 1995. – Vol.21.–p.l725–1741.
29. Sirri R., Pession A., Trere D. et al. Proportionally constant quantitative transmission of nucleolin and protein В 23 in cycling cancer cells // J.Clin. Pathol. – 1995. – Vol.48.–p.264–368.
30. Tokano Y., Miyake S., Kayagaki N., Nozawa K., Morimoto S., Azuma M., Yagita H., Takasaki Y., Okumura K., Hashimoto H. Soluble Fas Molecule in the Serum of Patients with Systemic Lupus Erythematosus. J.Clin.Immunol.–1996.–Vol.l6.–p.261–265.
31. Zhang J., Cado D., Chen A., Kabra N., Winoto A. Fas–mediated apoptosis and activation–induced T–cell proliferation are defective in mice lacking FADD/Mortl. Nature.–1998.–Vol.392.–p.296–299.
Контент доступен под лицензией Creative Commons «Attribution» («Атрибуция») 4.0 Всемирная.
Андростерома
Андростерома – одна из редко встречающихся гормонально активных опухолей надпочечников, является вирилизирующей опухолью (опухоль, при которой происходит «омужествление» – появление у женщин и усиление у мужчин мужских признаков). Андростеромы в 2 раза чаще наблюдаются у женщин, чем у мужчин. Андростеромы нередко встречаются на первом году жизни.
Локализуется опухоль либо в одном из надпочечников, либо в зонах размещения добавочной надпочечниковой ткани - в яичниках или широкой маточной связке. Опухоль выделяет большое количество андрогенов, что и определяет клиническую картину. Андростеромы могут быть доброкачественными (аденомы) и злокачественными (карциномы), но отличить их можно только при помощи изучения данных гистологического исследования. Опухоли, диаметр которых превышает 5 см, чаще всего злокачественной природы, с метастазами в легкие, печень, лимфатические узлы забрюшинного пространства и другие органы. В детском возрасте вирилизирующие опухоли обычно злокачественные.
В основе клинических признаков заболевания лежит чрезмерная выработка андростеромой андрогенов - мужских половых гормонов. Поэтому симптоматика андростеромы характеризуется активным "омужествлением" - вирилизацией.
Степень вирилизации у больных с андростеромой может быть различна, что связано с индивидуальными особенностями гормональной активности опухоли и продолжительности течения опухолевого процесса.
У детей появляются преждевременное половое оволосение, нечистота и сальность кожи, угри, наращение мышечной ткани, гипертрихоз. У девочек вирилизируется и увеличивается клитор при нормальном входе во влагалище, не развиваются или гипоплазируются молочные железы, прекращается менструация, голос становится низким. У мальчиков увеличивается половой член при отсутствии изменений яичек, появляется эрекция. У мужчин клинические проявления вирилизации менее выражены, поэтому андростерома может стать случайной находкой. У детей обоего пола ускоряются рост и скелетное созревание. Иногда выявляется гипертензия.
Общее самочувствие больных на ранних стадиях заболевания не изменяется. Порой женщины отмечают прилив сил, увеличение работоспособности, повышение полового влечения. Однако, впоследствии больные становятся раздражительными, лабильными, а иногда впадают в тяжелое депрессивное состояние. Когда опухоль достигает внушительных размеров, сдавление близлежащих нервных окончаний может приводить к болям.
Диагноз "андростерома" ставят на основании клинических признаков, данных лабораторной и инструментальной диагностики с проведением тщательного дифференцирования заболевания с другими патологическими процессами, сопровождаемыми вирилизацией (например, опухоли яичка или яичника, печени).
В настоящее время широко используется УЗИ, КТ или МР-томография для выявления расположения опухоли надпочечника, наличия метастазов.
Лабораторное исследование крови и мочи у больных с андростеромой позволяет выявить многократное увеличение концентрации андрогенов и их метаболитов. Выполняют пробы с введением адренокортикотропного гормона и дексаметазона, с целью дифференциальной диагностики с врожденной двусторонней гиперплазией и дисфункцией надпочечников.
Лечение хирургическое — удаление опухоли вместе с пораженным надпочечником. В случае метастазов операция сочетается с лучевой и химиотерапией. В отличии от лечения кортикостеромы, дальнейшей заместительной гормональной терапии обычно не требуется, так как второй надпочечник не подвергается атрофии, и сохраняет свою функцию.
Если злокачественная андростерома диагностирована в поздние сроки, когда обнаруживаются отдаленные метастазы, лечение опухоли - симптоматическое (обезболивание, химиотерапия, лучевая терапия), а прогноз - неблагоприятный.
Прогноз при своевременной диагностике и хирургической коррекции доброкачественных андростером благоприятный.
Андростерома Текст научной статьи по специальности «Клиническая медицина»
Аннотация научной статьи по клинической медицине, автор научной работы — Ахметзянова Т. Н., Гильмуллин И. Ф., Фаттахова Д. С.
Андростерома гормонально-активная опухоль коры надпочечника, исходящая в основном из ее сетчатой зоны, избыточно выделяющая кортикостероиды, но преимущественно андрогены, и характеризующаяся клинической картиной, сходной с врожденной дисфункцией коры надпочечников . Заболевание может встречаться в любом возрасте у лиц обоего пола. Решающее значение при постановке диагноза андростеромы имеют данные компьютерной томографии надпочечников. Представлен клинический случай, обучающий основам клиники, дифференциальной диагностики и лечения андро-стеромы.
Похожие темы научных работ по клинической медицине , автор научной работы — Ахметзянова Т. Н., Гильмуллин И. Ф., Фаттахова Д. С.
Неклассическая форма врожденной дисфункции коры надпочечников, обусловленная дефицитом 11β-гидроксилазы: описание 3 клинических случаев
Развитие синдрома поликистозных яичников у пациентки с классическим синдромом врожденной дисфункции коры надпочечников
Androsteroma
Androsteroma is a hormonal-active tumour of the adrenal cortex, that primarily includes cells from her reticular zone and secrets excess number of corticosteroids, but mainly androgens, and is characterized by a clinical picture similar to that of congenital adrenal hyperplasia. The disease can occur at any age in both sexes. Crucial in the diagnosis androsteromy have data computed tomography adrenal glands. Presents a case of teaching the basics of the clinic, differential diagnosis and treatment androsteromа.
Текст научной работы на тему «Андростерома»
Т.Н. АХМЕТЗЯНОВА, И.Ф. ГИЛЬМУЛЛИН, Д.С. ФАТТАХОВА УДК б1б.453-оое
Республиканская клиническая больница М3 РТ, г. Казань Казанский государственный медицинский университет
I Ахметзянова Талия Нурулловна
эндокринолог диабетологического центра
Андростерома - гормонально-активная опухоль коры надпочечника, исходящая в основном из ее сетчатой зоны, избыточно выделяющая кортикостероиды, но преимущественно андрогены, и характеризующаяся клинической картиной, сходной с врожденной дисфункцией коры надпочечников. Заболевание может встречаться в любом возрасте у лиц обоего пола. Решающее значение при постановке диагноза андростеромы имеют данные компьютерной томографии надпочечников. Представлен клинический случай, обучающий основам клиники, дифференциальной диагностики и лечения андро-стеромы.
Ключевые слова: андростерома, врожденная дисфункция коры надпочечников, аменорея.
T.N. AKHMETZYANOVA, I.F. GILMULLIN, D.S. FATTAKHOVA
Republican Clinical Hospital of Ministry of Health Care of the Republic of Tatarstan, Kazan Kazan State Medical University
Androsteroma is a hormonal-active tumour of the adrenal cortex, that primarily includes cells from her reticular zone and secrets excess number of corticosteroids, but mainly androgens, and is characterized by a clinical picture similar to that of congenital adrenal hyperplasia. The disease can occur at any age in both sexes. Crucial in the diagnosis androsteromy have data computed tomography adrenal glands. Presents a case of teaching the basics of the clinic, differential diagnosis and treatment androsteromа.
Keywords: androsteroma, congenital adrenal disfunction, amenorrhea.
Андростерома — вирилизирующая, гормонально активная опухоль коры надпочечника, исходящая в основном из ее сетчатой зоны, избыточно выделяющая кортикостероиды, но преимущественно андрогены, и характеризующаяся клинической картиной сходной с врожденной дисфункцией коры надпочечников. Заболевание может встречаться в любом возрасте, как у лиц женского, так и мужского пола [1].
Патогенез андростеромы обусловлен повышением продукции гормонов, в основном андрогенов, тканью опухоли. При патологоанатомическом исследовании обнаруживают опухоль коры надпочечника. Обычно она мягкой консистенции, инкапсулирована. Гистологически в опухоли обнаруживают, главным образом, темные клетки, характеризующиеся выраженным полиморфизмом. В ряде случаев гистологическая картина опухоли напоминает строение сетчатой зоны коры надпочечников. При злокачественной андростероме отмечают выраженный полиморфизм, клеточную атипию, инфильтратив-ный рост опухолевых клеток, множество очагов некроза. При злокачественной андростероме может происходить метаста-зирование в забрюшинное пространство, печень, легкие [2]. Клиника андростеромы характеризуется быстрым развитием вирилизации, особенно резкой при злокачественной андросте-
роме. Иногда появляются отдельные симптомы, характерные для болезни Иценко-Кушинга, что обусловлено гиперпродукцией глюкокортикоидов. С целью визуализации надпочечников используется РКТ, при этом выявляется чаще односторонняя опухоль надпочечника. Данные РКТ имеют решающее значение при постановке диагноза андростеромы. Дифференциальную диагностику следует проводить с двусторонней вирилизирую-щей гиперплазией надпочечников. Для этого проводят пробы с введением АКТГ и дексаметазона. В связи с определенной автономностью опухоли, т. е. независимостью ее функции от регулирующего влияния гипофиза, введение АКТГ и декса-метазона не сопровождается изменением экскреции 17-КС. Рентгенологическое исследование (супраренографию) сочетают с ретроградной или инфузионной пиелографией. Из других заболеваний, сопровождающихся вирилизацией, следует помнить об опухолях яичников, продуцирующих андрогены, адренобластомах. В этих случаях экскреция 17-КС не изменена или умеренно повышена неадекватно степени вирилизации. Методом диагностики служит гинекологический осмотр и рентгенодиагностика (оксипельвиография). Увеличение яичника с одной стороны дает основания подозревать опухоль. Описаны отдельные случаи развития вирильного синдрома на почве
АКТУАЛЬНЫЕ ПРОБЛЕМЫ МЕДИЦИНЫ I ТОМ 1
липоидоклеточной опухоли яичника при эктопированной опухоли коры надпочечников в яичник. Применяются те же диагностические тесты, включая геникографию. При гормональных исследованиях у женщин с опухолями яичников определяется повышение секреции андростерона, этиохоланолона, прегнан-триола и тестостерон-глюкуронида. При введении метапирона или хорионического гонадотропина отмечается заметное повышение этих стероидов. У мальчиков андростерому следует отличать от преждевременного полового созревания, связанного с поражением центральной нервной системы, опухолью эпифиза, опухолью яичек. При всей этой патологии экскреция 17-кетостероидов не достигает такого высокого уровня, как при андростероме. При внутримозговых процессах имеется неврологическая симптоматика. При ранней диагностике и своевременном оперативном лечении доброкачественной андростеромы прогноз благоприятный. При злокачественной андростероме и наличии метастазов прогноз неблагоприятный. Лечение. Лечение только оперативное — удаление пораженного опухолью надпочечника [3, 4].
Пациентка Г.Н., 1987 г.р., обратилась к эндокринологу РКП РКБ летом 2011 г. с жалобами на рост волос по всему телу в течение последних 2-3 лет, отсутствие менструаций в течение последних трех месяцев, снижение массы тела на 10 кг за последние 2 года, повышенную чувствительность, необъяснимую агрессию, лабильность настроения, постоянную слабость.
Считает себя больной около 2-3 лет, когда стала замечать снижение веса на фоне хорошего аппетита, появление усиленного роста волос на теле, нерегулярный менструальный цикл. Последние несколько месяцев указанные симптомы усугубились, менструации полностью прекратились. К врачу обратилась впервые.
Наследственность по эндокринологическим заболеваниям не отягощена. Гинекологический анамнез: менструации с 14 лет, регулярные, необильные, безболезненные. В настоящее время — аменорея. Беременностей не было.
При осмотре состояние удовлетворительное. Рост - 168 см, вес - 52 кг, ИМТ - 18 кг/м2. Телосложение нормостеническое. Рост волос по мужскому типу. Кожа сухая. Видимые слизистые чистые, бледные, гиперпигментации нет. Щитовидная железа не пальпируется. В легких дыхание везикулярное, хрипов нет. Границы относительной тупости сердца в пределах возрастной
нормы. Частота сердечных сокращений увеличена (96 уд/мин.), тоны сердца приглушены. АД 100/60 мм рт. ст. (в положении сидя). Ортостатическая проба отрицательная. Пульс удовлетворительного наполнения, дефицита пульса нет. Живот мягкий, безболезненный. Печень не увеличена, размеры по Курлову 9х8х7 см. Селезенка не увеличена. Периферических отеков, пастозности нет.
ДГЭА-С =1460.7 (Ы-80,2-511,7мкг/дл), Тестостерон = 13.4 (N 0.17-4.13 нмоль/л), Кортизол =8.2 (N 3,7-24,0мкг/дл), АКТГ =14.2 (N-0-46 пг/мл). Содержание ЛГ, ФСГ, СТГ, 17-оксипрогестерона, эстрадиола, соматомедина-с в пределах нормы.
Компьютерная томография — множественные узловатые образования обоих надпочечников. Аденомы. При гистологическом исследовании биоптата — темно-клеточная аденома коры надпочечников с массивными кровоизлияниями. УЗИ матки и придатков — состояние соответствует гипоэстрогении.
На основании анамнеза и клинико-лабораторных данных поставлен клинический диагноз: Андростерома обоих надпочечников.
Больной проведена адреналэктомия слева и резекция правого надпочечника. В течение месяца послеоперационного периода пациентка отмечает восстановление менструального цикла, стабилизацию веса, стабилизацию настроения, качественное улучшение самочувствия. Результаты обследования в послеоперационном периоде: ДГЭА-С =161.3 мкг/дл, Тестостерон = 1.27 нмоль/л.
1. Бирюкова М.С.Эндокринные заболевания и синдромы. Вирилизм // WORD. — 2000. —165 с.
2. Керцман В.П. Клиника и лечение гормонпродуцирующих опухолей коры надпочечника // Ереван-Айастан. — 1977. — С. 319.
3. Казанцева И.А., Калинин А.П., Полякова Г.А. и др. Клиническая морфология кортикальных опухолей гиперплазии надпочечников. Пособие для врачей. — М. — 1998. — С. 180.
4. Medeiros L. J., Weiss L.M. New developments in the pathologic diagnosis of adrenal cortical neoplasms // A. review Am. J. Clin. Pathol. — 1992. — Vol. 97.
Морфология опухолей надпочечников. Андростеромы
Морфология опухолей надпочечников. Андростеромы
Опухоль, обусловливающая возникновение адрено-генитального синдрома, наиболее часто развивается из сетчатой зоны коркового слоя надпочечников. Клубочковая зона коры надпочечников при этом синдроме, как правило, мало изменяется, либо в отдельных случаях несколько гиперплазирована. Однако описываются случаи адрено-генитального синдрома с явлениями гиперплазии всех трех зон коркового слоя надпочечников. До недавнего времени эти опухоли но выделяли в отдельную группу; их обычно относили к истинным гипернефромам или гормональноактивным аденомам коркового вещества надпочечных желез.
Однако учитывая характер возникновения этих опухолевых процессов, а главное, источник их роста, которым обычно является сетчатая зона коры надпочечников, продуцирующая именно андрогенные стероидные гормоны, О. Н. Николаев и Е. И. Тараканов выделили эти опухоли в отдельную группу, дав им название андростером. Основным патогенетическим фактором в возникновении и течении адрено-генитального синдрома является выраженное проявление андрогенной функции надпочечников.
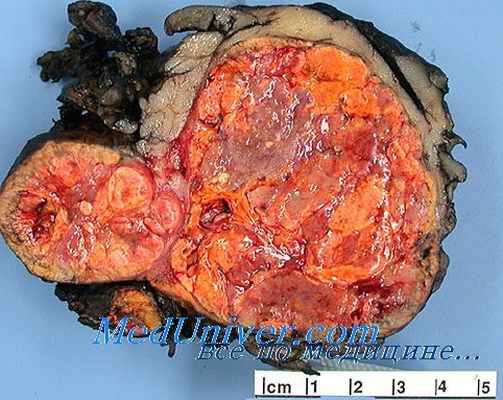
Такие опухоли надпочечных желез бывают сравнительно небольших размеров, мягкой или эластической консистенции, имеют округлую или яйцевидную форму и, как правило, окружены плотной соединительнотканной капсулой, отделяющей андростеро-му от окружающей паренхимы железы. Однако нередко весь пораженный надпочечник представляет собой сплошной опухолевый конгломерат, в котором невозможно различить не только отдельные зоны железы, но даже отдифференцировать корковое и мозговое вещество. На разрезе в толще опухоли определяется множество мелких оранжевого цвета включений на фоне бурого однородного мелкодольчатого строения паренхимы новообразования. Иногда в андростероме можно обнаружить мелкие петрификаты, а также мощные соединительнотканные тяжи, пронизывающие опухоль в различных направлениях.
Андростеромы имеют отчетливо выраженную структуру: построены они преимущественно из темных клеток сетчатой зоны коркового слоя надпочечников и отличаются выраженным полиморфизмом в отношении их формы и размеров. Большинство ядер этих опухолевых клеток гиперхромцы, однако изредка встречаются светлые ядра, которые крупнее, чем темные. Нередко светлые ядра этих эпителиальных клеток вакуолизированы и содержат несколько ядрышек. Иногда встречаются фигуры нормального митоза.
В некоторых андростеромах клетки коркового слоя надпочечников тесно прилежат друг к другу, образуя тяжи или балки, отдельные балочки, напоминающие своей микроскопической структурой сетчатую зону коркового вещества надпочечников. Иногда обнаруживаются небольшие липоидные скопления в участках опухолевой паренхимы, подвергшейся некробиотическим изменениям.
При электронномикроскопическом исследовании таких гормональноактивных опухолей обнаруживаются эпителиальные клетки, характерные для сетчатой зоны коркового слоя надпочечников. В цитоплазме этих опухолевых клеток выявляется как гранулярный, так и аграиулярпый эндоплазматический ретикулум, среди которого встречается большое количество мелких липоид-ных капель. Ядра этих клеток крупные, овальной или округлой формы. Ядерпый материал концентрируется преимущественно у внутренней поверхности ядерной мембраны. Ядрышко располагается чаще эксцентрически и значительно гипертрофировано. Наружная ядерная мембрана опухолевых клеток имеет утолщения, околоядерное пространство несколько расширено. Митохондрии набухшие, четко контурируются кристы, располагающиеся несколько под углом к мембране.
Некоторые кристы в этих клетках имеют колбовидные вздутия, встречаются также отдельные митохондрии с разрушенными или деформированными кристами.
На мембранах ретикулума в свободном состоянии определяется большое количество полирибосом (J. Orban, G. Kelenyi, А. Goll).
Андростеромы иногда подвергаются злокачественному перерождению; при этом морфологическими критериями их озлокачествления являются: выраженный полиморфизм и клеточная атипия; наличие значительного количества амнтотических форм деления с образованием двух- и многоядерных гигантских клеток; обилие мелких и крупных очагов некроза, а также явные признаки инфильтративного роста опухолевых эпителиальных клеток. Злокачественные андростеромы нередко инкапсулированы, а иногда интенсивно прорастают капсулу и дают ранние и дистантные метастазы.
Они сравнительно быстро метастазируют во второй надпочечник, лимфатические узлы, печень, легкие, почки, в забрюшинное пространство, кости и головной мозг. Описаны случаи адрено-генитального синдрома (В. И. Левенсон, Я. В. Оберемченко и Л. Л. Лихт), когда причиной заболевания были злокачественные андростеромы огромных размеров (весом до 2 кг), метастазировавшие в легкие, печень и регионарные лимфатические узлы. Микроскопически дифференцировать доброкачественную апдростерому от злокачественной чрезвычайно трудно, так как есть ряд переходных форм.
При адрено-генитальном синдроме у мальчиков наступает макрогенитосомия (раннее оволосение по мужскому типу, преждевременный рост половых органов, ускоренный рост тела); у девочек возникают признаки гирсутизма, ложный гермафродитизм (избыточный рост волос, преждевременное возникновение вторичных половых признаков, увеличение клитора). У женщин при адрено-генитальном синдроме появляется ряд мужских вторичных признаков (А. П. Преображенский, Д. А. Архипов).
При вскрытии женщин, умерших от метастатических поражений внутренних паренхиматозных органов злокачественными вариантами андростером, как правило, обнаруживается выраженная атрофия яичников с явлениями гипоплазии матки и атрофическими изменениями слизистой оболочки влагалища и яйцеводов (И. В. Голубева). При микроскопическом исследовании таких яичников обнаруживается полное отсутствие примордиальных и атретических фолликулов. Вместо с тем иногда можно наблюдать склерокистозные поражения яичников с наличием большого количества мелких кист и значительным утолщением белочной оболочки.
У мужчин с адрено-генитальным синдромом, умерших от метастазов первичной опухоли, можно наблюдать атрофические изменения в семенниках с угнетением сперматогенеза, исчезновением интерстициальпых клеток. Иногда у мальчиков при этом синдроме можно обнаружить в яичках выраженную гиперплазию добавочной надпочечниковой паренхимы. В периферической крови больных нередко отмечается эозинопения, а также возникновение отеков туловища и конечностей в связи с резким нарушением электролитного баланса.
Морфология опухолей надпочечников. Андростеромы




ОПУХОЛИ НАДПОЧЕЧНИКОВ – доброкачественные (кисты, аденомы) или злокачественные образования из клеток коркового или мозгового слоев надпочечников, имеющие разную морфологическую структуру, гормональную активность и клинические проявления.Опухоли надпочечника наблюдаются у 3-4% обследуемых пациентов в возрасте 40-60 лет, у женщин выявляются в 2 раза чаще, чем у мужчин. Гормональную активность проявляют только 10% опухолей. Среди всех выявленных опухолей надпочечников рак встречается в 2-4% случаев. К опухолям надпочечника, которые требуют хирургического вмешательства относятся: феохромоцитома, альдостерома, адренокортикальный рак, аденома надпочечника (гормонально активная и неактивная), большие миелолипомы и кисты надпочечников.
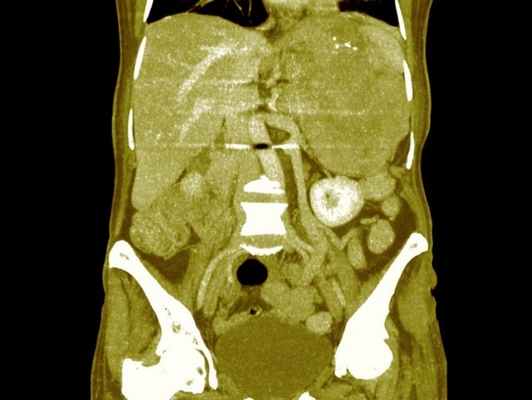
Клинические проявления опухолей надпочечников различаются в зависимости о т морфологического строения опухоли, потенциала злокачественности, наличия или отсутствия гормональной активности.
Киста надпочечника определяется чаще в виде одиночного, одностороннего образования, почти всегда гормонально-неактивна, безболезненна и выявляется, как правило, случайно, при УЗИ или КТ органов брюшной полости. Формируется киста надпочечников в эмбриональном периоде и на протяжении многих лет человек не знает о ее существовании из-за отсутствия каких-либо специфических признаков.
Аденомы надпочечника — доброкачественные образования коры надпочечника с твердой капсулой и однородным содержимым. Аденомы надпочечника чаще гормонально неактивны, составляют 98% всех выявленных образований и не проявляют себя никакими симптомами. Гормонально-активные аденомы надпочечника встречаются в 2% случаев и проявляются разнообразными симптомами, которые зависят от вырабатываемого гормона.
При кортикостероме , кортизол-вырабатывающей аденоме коры надпо чечника, формируется «синдром Иценко-Кушинга», чаще встречается у женщин 20-40 лет. Основным симптомом является специфическое ожирение кушингоидного типа - жир откладывается на груди, животе, шее, формируется типичное округлое лицо. У большинства пациентов отмечается атрофия мышц ягодиц, ног, передней брюшной стенки («лягушачий живот»). Характерным симптомом является атрофия и истончение кожи, появление стрий – багрово-красных или фиолетовых полос растяжений на коже живота, внутренней поверхности бедер и плеч, на молочных железах. Характерно возникновение мелких кровоизлияний в подкожной клетчатке. Частым осложнением является остеопороз – ослабление костной ткани, связанное с потерей минеральных солей. Развитие остеопороза приводит к появлению тяжелых переломов, из которых наиболее опасными являются перелом шейки бедра и переломы позвоночника. Наблюдаются нарушения нервной системы – депрессия , заторможенность, психотических реакций. У 10-20% пациентов с кортикостеромой встречается стероидный сахарный диабет . У женщин при развитии синдрома Иценко-Кушинга встречается гирсутизм - избыточный рост волос на теле и аменорея - нарушение менструального цикла.
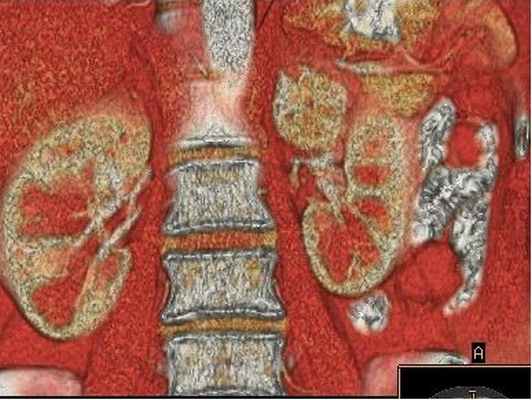
При феохромоцитоме – опухоли, вырабатывающей адреналин или норадреналин, наблюдается артериальная гипертония с кризовым течением. Наиболее характерна классическая триада симптомов катехоламиновых кризов: внезапная сильная головная боль, повышенное потоотделение и сердцебиение.
При альдостероме – аденоме, вырабатывающей альдостерон, развивается первичный гиперальдостеронизм, «синдром Конна», повышение артериального давления в результате задержки в организме натрия и увеличения объема циркулирующей крови. Развиваются мышечная слабость, миоплегия, судороги, парестезии, связанные с повышенным выведением калия с мочой и снижением уровня калия в крови.
При андростероме - аденоме, вырабатывающей андростерон – мужской половой гормон, наблюдается развитие мужских половых признаков у женщин - выраженной мускулатуры, грубого голоса, появление роста волос на теле, лице, уменьшение размера молочных желез, нарушение менструального цикла. Проявления андростеромы у мужчин незаметны, что ведет к поздней диагностике этой опухоли.
Инсиденталома надпочечника (от incidental – случайный) - случайно обнаруженная опухоль надпочечника на УЗИ, КТ или МРТ брюшной полости, не проявляющая себя клинически. Инсиденталомы могут быть по своему строению аденомами надпочечника, феохромоцитомами, кистами, липомами, миелолипомами, гемангиомами, тератомами, нейрофибромами, раком надпочечника, саркомами, метастазами других опухолей в надпочечник. Поэтому при выявлении опухоли надпочечника необходимо тщательное обследование для уточнения диагноза в специализированном учреждении по эндокринной хирургии.
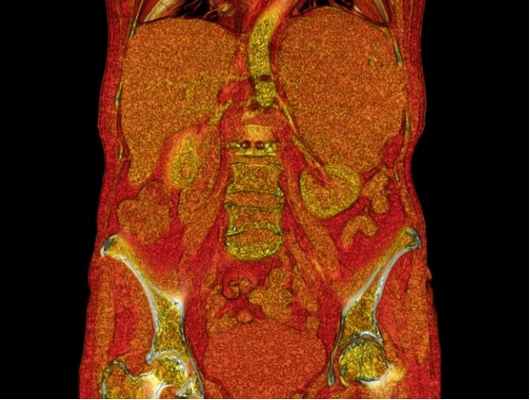
Адренокортикальный рак - злокачественная опухоль надпочечника, характеризующаяся быстрым, агрессивным ростом с высокой склонностью к метастазированию в регионарнарные лимфатические узлы и отдаленные органы (легкие, кости). Выявляется у 1% пациентов с опухолями надпочечника. При раке надпочечников у 60% пациентов наблюдается автономная неконтролируемая выработка разных гормонов, что может проявляться синдромом Кушинга, вирилизацией, преждевременным половым созреванием, феминизацией, первичным гиперальдостеронизмом, катехоламиновыми кризами. Отмечаются также симптомы типичные для всех злокачественных опухолей – снижение аппетита, похудание, нарушение пищеварения, диспепсические явления, локализированная или разлитая боль, зависимо от миграции метастазов, депрессивные расстройства, анемический синдром. Разнообразие клинических проявлений рака надпочечника приводит к выявлению опухоли на поздних стадиях у 80% пациентов, когда опухоль имеет значительный размер - более 4 см.
Инструментальные методы исследования
Дополнительные методы исследования
При подозрении на рак надпочечников для исключения метастазов опухоли проводятся компьютерная томография легких и брюшной полости, магнитно-резонансная томография головного мозга. Исследуется компьютерный фенотип опухоли. Цитоплазма клеток аденом и миелолипом надпочечника характеризуется высоким содержанием липидов в отличие от зрелых опухолей. Это свойство используется при денситометрии опухоли. Оценивается плотность жировых и нежировых структур в неконтрастную фазу. Нативная плотность образования менее 10 HU характерна для доброкачественных аденом, альдостером, липом, кист, гематом, абсцессов. Повышение плотности более 10 HU возможно при адренокортикальном раке, феохромоцитоме, метастазах, нейрогенных опухолях, лимфомах. При исследовании плотности на разных фазах выведения контрастного вещества аденомы быстро снижают показатели плотности, злокачественные опухоли имеют тенденцию к задержке контрастного вещества. Разделительная точка – вымывание 50% контраста за 10 минут.
Лабораторные методы исследования
При выявлении любой опухоли надпочечника диаметром 1 см и более необходимо проведение гормонального обследования, которое включает определение следующих показателей в крови и моче:
Кортизол в суточной моче - позволяет оценить базовую выработку кортизола надпочечниками. Важно помнить, что определение уровня кортизола в крови не позволяют четко определить гормональную функцию надпочечников в связи со значительными колебаниями в течение дня.
Малая дексаметазоновая проба - позволяет выявить у пациента даже слабо выраженные признаки синдрома Иценко-Кушинга. При проведении пробы в первый день пациенту утром берется кровь на уровень кортизола. В 24 часа этого же дня пациент принимает таблетку дексаметазона в дозировке 1 мг. Утром следующего дня пациенту берется анализ крови на кортизол. В норме уровень кортизола утром второго дня снижается более чем в 2 раза по сравнению с первым днем. При отсутствии подавления уровня кортизола крови можно сделать вывод о наличии автономной неконтролируемой выработки кортизола.
Дексаметазоновый подавляющий тест. Для проведения подавляющего теста пациент принимает 1 мг дексаметазона между 23 и 24 часами, после чего производится определение кортизола в крови, взятой между 8 и 9 часами утра. Можно с уверенностью говорить об отсутствии у пациента избыточной выработки кортизола опухолью надпочечника, если утренний уровень кортизола крови составил менее 50 нмоль/л.
АКТГ крови в утренние часы. Если уровень АКТГ находится на низких значениях – это позволяет исключить диагноз АКТГ-продуцирующей опухоли гипофиза и более уверенно склониться к диагнозу опухоли надпочечника, вырабатывающей кортизол.
Метанефрины в суточной моче - фракционированное определение метилированных производных катехоламинов при диагностике феохромоцитомы. Повышает специфичность диагностики неоднократные исследования метанефринов. Сейчас стала доступна сцинтиграфия с метайодбензилгуанидином - I 123 (MIBG - I 123 ) и определение неспецифического маркера нейроэндокринных опухолей - хромогранина А.
Альдостерон-рениновое соотношение - скрининг при синдроме артериальной гипертензии для диагностики первичного альдостеронизма. Чувствительность повышается исследованием альдостерона в динамике. Возможно использование верифицирующего функционального теста с натриевой нагрузкой. При гиперпластических формах с целью латерализации источника гиперпродукции альдостерона – сравнительный селективный забор венозной крови из надпочечниковых вен .
Основные методы лечения
Выбор лечения зависит от клинических, рентгенологических, гормональных харатеристик выявленной опухоли.
Гормонально неактивные опухоли менее 4см без косвенных признаков злокачественного роста не требуют оперативного вмешательства. Рекомендуется динамическое наблюдение , контроль УЗИ, МРТ, КТ и гормональных анализов через 6, 12 и 24 месяца (при подозрительных данных через 3 месяца).
При гормонально-активных опухолях надпочечников, новообразованиях более 3 см, не проявляющих функциональной активности проводится - адреналэктомия , удаление всего пораженного надпочечника, в некоторых случаях производится удаление части надпочечника с опухолью.
При опухоли надпочечника с признаками малигнизации проводится адреналэктомия с удалением регионарных лимфатических коллекторов.
Читайте также:
