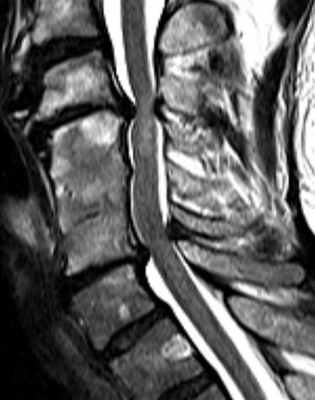
МРТ при лучевой миелопатии
Добавил пользователь Skiper Обновлено: 27.01.2026
Если происходит повреждение нервной ткани в спинном мозге шейного или грудного отделов позвоночника, мы говорим о миелопатии. Слово «миелопатия» состоит из древнегреческих частей Myelon – «спинной мозг» и Pathos – «болезнь, повреждение». Внутри позвоночника находится спинномозговой канал, в нем проходит спинной мозг, а в нижнем отделе позвоночника - нервные волокна. Между телами позвонков нервы покидают спинномозговой канал и выходят далее в руки, в туловище или ноги. Если постоянно происходит массивное давление на спинной мозг, например, при межпозвоночной грыже, стенозе позвоночного канала, опухоли или нарушении кровообращения, то ткани спинного мозга теряют свою витальность, и со временем это приводит к отмиранию нервной ткани с потерей ее функций. Поскольку нервные клетки в этом отделе не могут регенерироваться или размножаться, последствия заболевания остаются навсегда или только ухудшаются.
В зависимости от причины повреждения спинного мозга различаются разные формы миелопатии. Решающим является локализация повреждения спинного мозга, то есть, затронут ли спинной мозг в шейном или в грудном отделе.
Частота - мужчины болеют в два раза чаще, чем женщины
По опыту известно: мужчины страдают от этой проблемы в два раза чаще, чем женщины. Дегенеративные изменения шейного отдела позвоночника преимущественно затрагивают людей среднего и пожилого возраста. Половина всех людей старше 50 лет и три четверти всех людей старше 65 лет имеют признаки цервикальной миелопатии. Возможно, вам будет интересно: в японском исследовании в одном районе с населением 2,26 миллиона человек 1155 пациентов были прооперированы из-за цервикальной (шейной) миелопатии. Большинство пациентов были в возрасте от 60 до 70 лет. В 30% случаев присутствовал стеноз спинномозгового канала.
У миелопатии есть разные причины
Естественно, что вы хотите и должны знать причины возникновения миелопатии.
И вот ответы. Принципиальное правило: повреждение спинного мозга может быть вызвано разными механизмами. Однако в подавляющем большинстве случаев она приобретается в течение жизни. Если спинной канал слишком сильно сужен, то это может привести к серьезным отказам в работе рук и ног с нарушением мелкой моторики, чувствительности, силы мышц и походки. Неполный или полный поперечный паралич может быть результатом, если не расширить позвоночный канал.
Как можно «заработать» миелопатию? Сужение (стеноз) спинного мозга и вытекающие отсюда повреждения нервных путей и нервных корешков могут возникнуть из-за острых травмирующих обстоятельств, например, аварии, межпозвоночной грыжи или падения, но также в силу изменения тканей при/после воспалений, а также опухолей или кист. Различные причины вызывают различные варианты миелопатии.
Существуют три формы заболевания! Первая форма – это компрессионная миелопатия. Она может возникнуть в результате опухоли, метастазов в позвоночнике и оболочках спинного мозга, а также посттравматически, например, после перелома позвонков, после межпозвоночной грыжи, из-за стеноза позвоночного канала, спондилеза (износа). Помимо компрессионной миелопатии снижение кровообращения также приводит к повреждению нервных клеток спинного мозга. Нарушение кровообращения происходит при сосудистых пороках или сосудистых сужениях (стенозах). Острая кровопотеря также может привести к недостаточному снабжению спинного мозга (шоковая симптоматика). Если присутствуют эти причины, то мы говорим о сосудистой миелопатии. Вы наверняка уже слышали о радиационном поражении. Действительно, в рамках лучевой терапии может произойти повреждение спинного мозга. Если это так, то мы говорим о лучевой миелопатии.
При миелопатии симптомы развиваются медленно
Миелопатия привлекает к себе внимание различными симптомами. Они зависят в первую очередь от области повреждения спинного мозга. Симптомы, как правило, развиваются вялотекуще. При чистых компрессиях спинного мозга, которые обычно безболезненны, могут пройти годы от появления первого симптома до постановки диагноза. Первыми признаками могут быть расстройства чувствительности в руках или подошвах ног, неловкость рук и неуверенность при ходьбе в темноте. Для всех форм миелопатии действует правило, что поврежденные участки спинного мозга больше не могут правильно выполнять свою функцию в нервной системе, поэтому возникают неврологические расстройства.
Некоторые пациенты жалуются на боли в шее, которые отдают в руки, или онемение, вплоть до потери силы в руках. Важными признаками миелопатии является даже не боль, а неврологические расстройства. Типичным является также «засыпание» рук во время ночного сна. Первоначальные симптомы могут включать нарастающую ригидность (жесткость) шеи с болью при повороте головы влево и вправо. При повреждении спинного мозга симптомы могут отдавать в ноги, а также вызывать неуверенность походки и потерю контроля над мочевым пузырем или кишечником. Нарушения мелкой моторики рук могут усиливаться, почерк становится угловатым и похожим на каракули, предметы могут чаще выпадать из рук. Становится труднее застегивать пуговицы на рубашке и блузке. Шейная миелопатия имеет прогрессирующую форму течения. В начале заболевания возникают легкие двигательные сбои (нарушения походки) и сбои функций верхних и/или нижних конечностей. Из-за одностороннего сжатия могут возникать нарушения ощущений и нарастающие двигательные проблемы (синдром Броун-Секара).
Миелопатии грудного отдела позвоночника (грудные миелопатии) имеют такие же типичные симптомы, как и миелопатии в области ШОП. Симптомы возникают медленно и являются результатом потери функции каждого из пораженных спинномозговых участков. Характерны тугоподвижность в ногах, слабость в мышцах рук, затрудненное дыхание, атрофия мышц рук или кистей, нарушения чувствительности рук, нарушения походки, нарушения чувствительности, параличи, нарушения функций мочевого пузыря и кишечника.
Сосудистые миелопатии проявляются в различных функциональных сбоях в зависимости от пораженного сосуда. Больные жалуются на слабость, онемение, нарушения мелкой моторики, нарушения опорожнения мочевого пузыря, равновесия и половой функции, а также на жесткость мышц. На продвинутой стадии заболевания может возникнуть атрофия тканей и затруднение дыхания.
Врачу сложно диагностировать миелопатию
Принципиально надо сказать две вещи по теме диагностки миелопатии:
- Точная постановка диагноза – предпосылка для подходящего лечения.
- Чем раньше поставлен диагноз, тем лучше прогноз на полное выздоровление. Это очевидно, и возможно, что вы сами уже испытали это на себе. Девиз: быстро распознать – быстро устранить!
Однако миелопатия затрудняет врачу диагностику, и для этого есть причина: нет специфических ранних признаков для ее выявления. Другими словами, болезненный процесс очень часто протекает незаметно и неприметно, так что диагноз часто ставится только при прогрессирующей картине болезни. Это, помимо болезни как таковой, самое коварное в миелопатии.
Поэтому при диагностике особенно важно «ехать по дороге с двусторонним движением». Иными словами, это означает разговор с врачом и клиническое обследование. Во-первых, врач спросит вас о характере симптомов (отказы некоторых функций организма, боли, нарушения функций мочевого пузыря или прямой кишки). Во-вторых, он спросит об известных ранее имевшихся заболеваниях: болезнь Бехтерева, спондилоартроз, остеопороз, грыжи межпозвоночного диска, нарушения артериального кровообращения или проведенная лучевая терапия.
Далее следует неврологический статус с проверкой походки, анализами на патологические рефлексы и на нарушения ощущений (потеря чувствительности).
Затем используется визуализационная диагностика, такая как МРТ (магнито-резонансная томография). Обычные рентгеновские снимки также могут хорошо представлять костные изменения. Дополнительные функциональные снимки всегда должны быть сделаны, чтобы определить возможные нестабильности.
Магнито-резонансная томография является важнейшим методом исследования для определения миелопатии. В послойных снимках магнито-резонансной томографии четко видна миелопатия. Таким образом, именно ОНА является методом выбора для диагностики. Во-первых, это позволяет увидеть сжимающие спинной мозг структуры, такие как грыжа межпозвоночного диска или опухоли. С другой стороны, поврежденные области спинного мозга на МРТ можно отличить от здоровой нервной ткани. Электрофизиологические измерения (скорость проведения нервного испульса, вызванные потенциалы и т. д.) дают важную информацию о функциях спинного мозга.
Обычно врач также направляет пациента на лабораторный анализ крови, чтобы выявить возможные воспалительные процессы в организме.
Существуют различные степени миелопатии. Ниже приведена Европейская миелопатическая шкала. Посмотрите, как дела обстоят у вас:
Миелопатия
Миелопатия является собирательным термином, обозначающим любое повреждение спинного мозга имеющее различный генез. Например, миелопатия может быть канцероматозная (связана с дегенерацией спинного мозга, связанная с раковым процессом) компрессионная (вследствие давления на спинной мозг гематомы или тканей), радиационная миелопатия (происходит разрушение спинного мозга от воздействия ионизирующего излучения – к примеру, при лучевой терапии). Когда причиной повреждения спинного мозга являются заболевания, то миелопатия носит название этого заболевания – например диабетическая миелопатия.
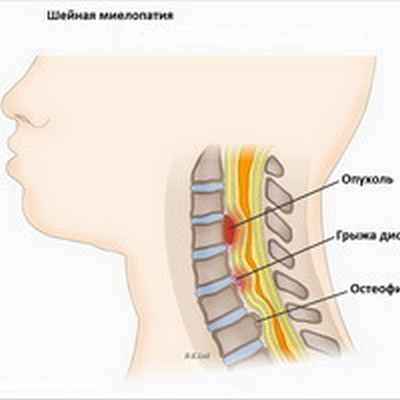
Миелопатия может быть вызвана травмой спинного мозга (перелом или вывих позвонков), грыжей межпозвоночного диска (межпозвонковый диск оказывает компрессионное воздействие на спинной мозг), остеоартрозом позвоночника (спондилез) или объемными поражениями, такими как опухоли. Миелопатия также может быть клиническим проявлением инфекционных или воспалительных процессов, а также нарушений кровообращения в сосудах спинного мозга о (спинальный инсульт). Синдром, который является результатом компрессии спинного мозга с одной стороны спинного мозга на уровне 10 грудного позвонка и сопровождающийся спастическим парезом на стороне повреждения спинного мозга и потерей проприорецепции и болевой и температурной чувствительности на противоположной стороне - называется Броун-Секаровским синдромом и тоже считается разновидностью миелопатии. Причинами миелопатии могут быть также вирусы, иммунные реакции, недостаточность кровообращения в сосудах спинного мозга. Кроме того миелопатия может развиться вследствие демиелинизации (потери нервным волокном защитной оболочки) или как реактивное осложнение на такие прививки как оспа, корь, ветрянка.
Факторы риска
Миелопатия вследствие травмы или заболевания может произойти в любом возрасте как у мужчин, так и у женщин. Степень нарушения функций зависит от уровня поражения спинного мозга.
Чаще всего первичные опухоли спинного мозга встречаются у людей в возрасте от 30 до 50 лет.
Травмы спинного мозга чаще встречаются у мужчин в возрасте от 15 до 35 лет.
Шейная спондилогенная миелопатия является наиболее распространенным повреждением спинного мозга в лиц в возрасте 55 лет и старше. Повышенный риск развития шейной спондилогенной миелопатии имеют люди, которые подвержены повторяющимся травмам - работа связана с переносом тяжестей или занятия такими видами спорта, как гимнастика. Пациенты с наличием сосудистых заболеваний подвержены большему риску закупорки спинальных артерий. Также у пациентов с рассеянным склерозом возможно развитие симптомов миелопатии.
Заболеваемость: Точной информации о частоте миелопатии на сегодняшний день нет. Тем не менее, информация о некоторых распространенных причинах миелопатии существует. К примеру, в США происходит от 12 до 15 000 травм спинного мозга ежегодно. Считается, что у 5% - 10% пациентов с раком велика вероятность роста опухолей в эпидуральное пространство, что приводит к более 25000 случаям миелопатии в год, из них 60% будет возникать в грудном отделе позвоночника, и 30% в пояснично-крестцовом отделе позвоночника.
Распространенность шейной спондилогенной миелопатии составляет 50% среди мужчин и 33% женщин в возрасте старше 60 лет.
Различные опухоли могут привести к компрессии спинного мозга, но первичные опухоли спинного мозга встречаются достаточно редко.
Симптомы и диагностика
История болезни: симптомы миелопатии варьируют в зависимости от причин, тяжести состояния, и является ли состояние являющейся причиной миелопатии острым или хроническим. В случае, когда причиной являются опухоли спинного мозга, компрессия или травмы могут быть боли (которые также могут иррадиировать в руки или ноги), нарушения чувствительности или движений, и / или контрактуры с одной, или с противоположной стороны тела. Если причиной является остеоартрит, могут быть жалобы на боли и болезненность, снижение амплитуды движений в позвоночнике, слабость, возможны деформации позвоночника. Миелопатия может также проявляться нарушением функции мочевого пузыря или кишечника или потерей чувствительности или онемением в области гениталий. Инфекции, вызывающие миелопатию, могут вызвать повышение температуры, покраснение, припухлость, повышенную болезненность. Если у человека синдром Броун-Секара, то может быть спастический паралич на стороне повреждения спинного мозга и потеря проприорецепции и боль, чувство жара на другой стороне тела.
Осмотр
Стандартный неврологический осмотр может выявить заболевания, связанные с компрессией корешков (например, шейная радикулопатия) или наличие спастичности в ногах. Клонусы мышц могут быть признаками расстройств верхнего двигательного нейрона в спинном мозге. Изучение рефлекторной активности позволяет отметить изменения рефлексов (которые могут быть повышенными или сниженными в зависимости от причины), а также потери или изменения чувствительности. Проверка сенсорной чувствительности (от нижних конечностей до лица) может быть необходима для определения уровня нарушений чувствительности. Кроме того, полезно определение активности брюшных рефлексов, что также позволяет уточнить уровень поражения. Также может быть паралич и / или уменьшение чувствительности в различных частях тела. Возможно также снижение объема произвольных движений. Оценка функции прямой кишки тоже имеет важную роль в диагностике миелопатии.
Диагностические методы
Диагностические методы зависят от истории заболевания и физикального обследования. Рентгенография, денситометрия, компьютерная томография (КТ) или магнитно-резонансная томография (МРТ) спинного мозга может обнаружить повреждения в пределах или вблизи спинного мозга. Лабораторные исследования могут быть назначены, чтобы исключить другие возможные причины (например, дефицит витамина В12 или отравления солями тяжелых металлов). Повышенное количества белых кровяных телец (лейкоцитов) предполагает наличие инфекции (менингит или остеомиелит позвоночника). Повышенная скорость оседания эритроцитов крови (СОЭ) может быть признаком воспаления, инфекции или опухоли. Спинномозговая пункция может быть проведена для получения спинномозговой жидкости (ликвора) для лабораторных исследований при подозрении на менингит или рассеянный склероз. Другие диагностические процедуры могут включать биопсию костной ткани или мягких тканей, а также посев культуры крови и цереброспинальной жидкости.
Лечение
Лечение зависит от причины миелопатии. Для перелома или вывиха позвонков - обезболивающие (анальгетики), тракция, иммобилизация в течение нескольких недель, и реабилитационная терапия (физиотерапия, ЛФК, массаж). Хирургическое лечение для исправления деформации позвоночника может включать в себя удаление части поломанного позвонка и / или фиксация отломков позвонков. Анальгетики, НПВС, (стероиды), и, возможно, физиотерапия может быть использована для лечения проблем связанных с артритом. Лекарственные препараты для лечения рассеянного склероза могут быть полезными, в том числе новые лекарственные препараты или стероиды. Инфекции требуют применения препаратов для устранения инфекции (антибиотики), для снижения температуры (жаропонижающие), и, возможно, противовоспалительные препараты (стероиды), чтобы минимизировать воспаление. Для лечения миелопатии в результате компрессии спинного мозга может потребоваться операция по удалению опухоли или грыжи межпозвонкового диска (ламинэктомия).
Прогноз
Прогноз зависит от причины миелопатии и наличия стойкого повреждения нервных структур. Тракция и иммобилизация могут привести к полному выздоровлению, если не было повреждения спинного мозга. Полное излечение возможно и при инфекциях. При хронических заболеваниях таких, как артрит или остеопороз, эффект от лечения может быть временным или если заболевание прогрессирует, то возможно стойкая потеря трудоспособности вплоть до инвалидной коляски Травма спинного мозга или компрессия может привести к необратимым изменениям в спинном мозге, включая потерю чувствительности в различных частях тела, а также потерю произвольных движений в конечностях. Восстановление после удаления опухоли зависит от остаточного повреждения и если это раковая опухоль, то от метастазирования. Восстановление после удаления грыжи диска (дискэктомия) дает хороший результат, но только если спинной мозг не подвергся необратимым изменениям в результате компрессии. Осложнениями миелопатии может быть зависимость от обезболивающих, постоянная нарушение чувствительности и / или произвольных движений, деформации позвоночника и нарушения функции мочевого пузыря и кишечника.
Использование материалов допускается при указании активной гиперссылки на постоянную страницу статьи.
МАГНИТНО-РЕЗОНАНСНАЯ ТОМОГРАФИЯ ПРИ КОМПРЕССИОННОЙ МИЕЛОПАТИИ У ПАЦИЕНТОВ С ИНФЕКЦИОННЫМИ СПОНДИЛИТАМИ
Изучены клинико-неврологический статус и результаты магнитно-резонансной томографии (МРТ) позвоночника последовательно обследованных 100 пациентов с подозрением на инфекционный спондилит. Дизайн исследования — проспективная моноцентровая когорта с периодом набора материала 2015–2017 гг. Уровень доказательности — III. Выявлено преобладание интрамедуллярных изменений в виде глиоз/миелоишемия-отек в сравнении с другими вариантами выявляемых изменений; доказано наличие более высокой степени сагиттального стеноза позвоночного канала (SCSs) и вершинного угла деформации спинного мозга (SCK) и также среднего числа пораженных позвонков при туберкулезном спондилите, чем при неспецифическом. У ВИЧ-положительных пациентов отмечены более высокие значения степени максимального сагиттального стеноза позвоночного канала (SCSs), чем у ВИЧ-отрицательных. Не доказана статистическая зависимость между оцененной по шкале Frankel тяжестью неврологических расстройств с этиологией процесса и с конкретными вариантами структурных изменений спинного мозга. Показатели тактильной и болевой чувствительности достоверно выше у пациентов с интрамедуллярными изменениями в виде глиоза/миелоишемии-отека, чем при миеломаляции.
Ключевые слова
Об авторах
Санкт-Петербургский научно-исследовательский институт фтизиопульмонологии
Россия
Макогонова Марина Евгеньевна — заведующая кабинетом магнитно-резонансной томографии ФГБУ «Санкт-Петербургский НИИ фтизиопульмонологии» Минздрава России; 194064, Санкт-Петербург, Политехническая ул., д. 32
Санкт-Петербургский научно-исследовательский институт фтизиопульмонологии
Россия
Трофимова Татьяна Николаевна — доктор медицинских наук, профессор, главный врач клиник «АВА-ПЕТЕР» и «Скандинавия», главный специалист по лучевой диагностике Санкт-Петербурга и СЗФО, руководитель Научно-клинического и образовательного центра «Лучевая диагностика и ядерная медицина» Санкт-Петербургского государственного университета, главный научный сотрудник ФГБУН «Институт мозга человека им. Н. П. Бехтеревой» Российской академии наук; 197376, Санкт-Петербург, ул. Академика Павлова, д. 9
Санкт-Петербургский научно-исследовательский институт фтизиопульмонологии
Россия
Мушкин Александр Юрьевич — доктор медицинских наук, профессор, главный научный сотрудник, руководитель клиники детской хирургии и ортопедии, руководитель центра патологии позвоночника, координатор направления «Внелегочный туберкулез» ФГБУ «Санкт-Петербургский НИИ фтизиопульмонологии» Минздрава России; 194064, Санкт-Петербург, Политехническая ул., д. 32
Список литературы
1. Баулин И.А., Советова Н.А., Гаврилов П.В., Демиденко А.В., Тумасова Н.С., Макогонова М.Е. Туберкулезный спондилит // Принципы лучевой диагностики. 2017. № 2. С. 22–34. [Baulin I.A., Sovetova N.A., Gavrilov P.V., Demidenko A.V., Tumasova N.S., Makogonova M.E. Tuberkuleznyj spondilit. Principy luchevoj diagnostiki, 2017, No. 2, рр. 22–34 (In Russ.)].
2. Gupta A.K., Kumar C., Kumar P., Verma A.K., Nath R., Kulkarni C.D. Correlation between neurological recovery and magnetic resonance imaging in Pott’s paraplegia // Indian J. Orthop. 2014. Jul. Vol. 48 (4). Р. 366–373. doi: 10.4103/0019–5413.136228.
3. Труфанов Г.Е., Рамешвили Т.Е., Дергунова Н.И., Митусова Г.М. Лучевая диагностика инфекционных и воспалительных заболеваний позвоночника. СПб.: Элби-СПб, 2011. [Trufanov G.E., Rameshvili T.E., Dergunova N.I., Mitusova G.M. Luchevaya diagnostika infekcionnyh i vospalitel’nyh zabolevanij pozvonochnika. Saint Petersburg: Izdatel’stvo EHlbi-SPb, 2011 (In Russ.)].
4. Лучевая диагностика воспалительных заболеваний позвоночника, осложненных спинномозговыми расстройствами: пособие для врачей-рентгенологов / сост.: Н. А. Советова, Г. М. Митусова, И. Б. Савин, А .З. Некачалова. СПб., 1997. [Luchevaya diagnostika vospalitel’nyh zabolevanij pozvonochnika, oslozhnennyh spinnomozgovymi rasstrojstvami: posobie dlya vrachej-rentgenologov / sost.: N. A. Sovetova, G. M. Mitusova, I. B. Savin, A. Z. Nekachalova. Saint Petersburg, 1997 (In Russ.)].
5. Митусова Г.М., Советова Н.А. Магнитно-резонансная томография в комплексной лучевой диагностике туберкулезного спондилита у взрослых // Проблемы туберкулеза. 1999. № 3. С. 19–22. [Mitusova G.M., Sovetova N.A. Magnitno-rezonansnaya tomografiya v kompleksnoj luchevoj diagnostike tuberkuleznogo spondilita u vzroslyh. Problemy tuberkuleza, 1999, No. 3, рр. 19–22 (In Russ.)].
6. Советова Н.А., Олейник В.В., Митусова Г.М., Некачалова А.З. Клинико-рентгенологические проявления // Проблемы туберкулеза. 2001. № 4. С. 9–13. [Sovetova N.A., Olejnik V.V., Mitusova G.M., Nekachalova A.Z. Kliniko-rentgenologicheskie proyavleniya. Problemy tuberkuleza, 2001, No. 4, рр. 9–13 (In Russ.)].
7. Harkey H.L., Аl-Mefty O., Marawi I., Peeler D.F., Haines D.E., Alexander L.F. Experimental chronic compressive cervical myelopathy: effects of decompression // J. Neurosurg. 1995. Vol. 83. Р. 336–341 [PMID: 7616281].
8. Mamata Н., Jolesz F.A., Maier S.E. Apparent diffusion coefficient and fractional anisotropy in spinal cord: age and cervicalspondylosis-related changes // J. Magn. Reson. Imaging. 2005. Jul., Vol. 22 (l). Р. 38–43.
9. Ohshio I., Hatayama A., Kaneda K., Takahara M., Nagashima K. Correlation Between histopathologic feartures and magnetic resonance images of spinal cord lesions // Spine (PHILA PA 1976). 1993.
10. Yasutaka Matsuda, Kazumi Miyazaki, Kenji Tada, Atsushi Yasuda, Tomitaka Naka. Increased MR signal intensity due to cervical myelopathy. Analysis of 29 surgical cases // Journal of Neurosurgery. 1991. June, Vol. 74, No. 6. P. 887–892.
11. Jain A.K., Aggarwal A., Mehrotra G. Correlation of canal encroachment with neurological deficit in tuberculosis of spine // Int. Ortop. 1999. Vol. 23 Р. 85–86.
12. Jain A.K., Sinha S. Evaluation of paraplegia grading systems in tuberculosis of the spine // Spinal Cord. 2005. Vol. 43 (6). Р. 375–380.
13. Jain A.K., Jena A., Dhameni I.K. Correlation of clinical course with magnetic resonance imaging in tuberculous myelopathy // Neurol. India 2000. Vol. 48. Р. 132–139. Jul. 1S 91. Р. 1140–1149.
14. Ozawa H., Sato T., Hyodo H., Ishii Y., Morozumi N., Koizumi Y., Matsumoto F., Kasama F., Aizawa T., Itoi E., Kokubun S. Clinical significance of intramedullary Gd-DTPA enhancement in cervical myelopathy. Spinal Cord. 2010.
15. Dunn R., Zondagh I., Candy S. Spinal tuberculosis // Spine. Vol. 36, No. 6. Р. 469–473.
16. Hoffman E.B., Grosier J.H., Gremin B.J. et al. Imaging in children with spinal tuberculosis: a comparison of radiography, computed tomography and magnetic resonance // J. Bone Joint Surg. Br. 1993. Vol. 75. Р. 233–238.
17. Вишневский А.А., Трофимова Т.Н., Шулешова Н.В. Спинной мозг. Сопоставления. М.: Фолиант, 2014. 744 с. [Vishnevskij A.A., Trofimova T.N., Shuleshova N.V. Spinnoj mozg. Sopostavleniya. Moscow: Izdatel’stvo Foliant, 2014. 744 р. (In Russ.)].
18. Решетнева Е.В., Мушкин А.Ю., Зимина В.Н. ВИЧ-инфекция и туберкулез позвоночника: Основные аспекты общей проблемы // Инфекционные болезни. 2015. № 4. С. 22–29. [Reshetneva E.V., Mushkin A.Yu., Zimina V.N. VICH-infekciya i tuberkulez pozvonochnika: Osnovnye aspekty obshchej problemy. Infekcionnye bolezni, 2015, No. 4, рр. 22–29 (In Russ.)].
19. Решетнева Е.В., Вишневский А.А., Соловьева Н.С., Олейник В.В. Клинические особенности туберкулезного спондилита у больных ВИЧ-инфекцией // Туберкулез и болезни легких. 2014. № 2. С. 19–21. [Reshetneva E.V., Vishnevskij A.A., Solov’eva N.S., Olejnik V.V. Klinicheskie osobennosti tuberkuleznogo spondilita u bol’nyh VICH-infekciej. Tuberkulez i bolezni legkih, 2014, No. 2, рр. 19–21.
Поздняя постлучевая миелопатия: механизмы возникновения демиелинизации, сложности диагностики Текст научной статьи по специальности «Клиническая медицина»
Аннотация научной статьи по клинической медицине, автор научной работы — Гончарова З.А., Погребнова Ю.Ю., Ярош Н.М.
В статье представлены данные литературы и собственное наблюдение одной из редчайших форм миелопатии постлучевой. Рассмотрены возможные варианты патогенеза, стадии развития, особенности клиники и диагностики лучевого повреждения спинного мозга. Приведен дифференциально-диагностический алгоритм, позволивший поставить окончательный клинический диагноз путем исключения более распространенных миелитов.
Похожие темы научных работ по клинической медицине , автор научной работы — Гончарова З.А., Погребнова Ю.Ю., Ярош Н.М.
Идиопатические воспалительные демиелинизирущие заболевания центральной нервной системы: современный взгляд на классификацию, опыт создания регистра
Дифференциальная диагностика очаговых некомпрессионных поражений спинного мозга шейно-грудной локализации
Late postradiation myelopathy: mechanisms of demyelination, problems of diagnosing
The article presents literature data and own observation of one of the rarest forms of myelopathy post-radiation myelopa-thy. The possible variants of pathogenesis, stages of development, features of clinical picture and diagnosis of radiation damage to the spinal cord are discussed. A differential-diagnostic algorithm is proposed, which allows to make the final clinical diagnosis by excluding the more common myelitis .
Текст научной работы на тему «Поздняя постлучевая миелопатия: механизмы возникновения демиелинизации, сложности диагностики»
З.А. ГОНЧАРОВА, Ю.Ю. ПОГРЕБНОВА, Н.М. ЯРОШ
Ростовский государственный медицинский университет, 344022, г. Ростов-на-Дону, пер. Нахичеванский, д.29
Поздняя постлучевая миелопатия: механизмы возникновения демиелинизации, сложности диагностики
В статье представлены данные литературы и собственное наблюдение одной из редчайших форм миелопатии — постлучевой. Рассмотрены возможные варианты патогенеза, стадии развития, особенности клиники и диагностики лучевого повреждения спинного мозга. Приведен дифференциально-диагностический алгоритм, позволивший поставить окончательный клинический диагноз путем исключения более распространенных миелитов. Ключевые слова: постлучевая миелопатия, миелит, демиелинизация, оптикомиелит Девика.
Z.A. G0NCHAR0VA, Yu.Yu. P0GREBN0VA, N.M. YAR0SH
Rostov State Medical University, 29 Nakhichevanskiy pereulok, Rostov-on-Don, Russian Federation, 344022
Late postradiation myelopathy: mechanisms of demyelination, problems of diagnosing
The article presents literature data and own observation of one of the rarest forms of myelopathy — post-radiation myelopathy. The possible variants of pathogenesis, stages of development, features of clinical picture and diagnosis of radiation damage to the spinal cord are discussed. A differential-diagnostic algorithm is proposed, which allows to make the final clinical diagnosis by excluding the more common myelitis.
Key words: postradiation myelopathy, myelitis, demyelination, Devic's disease.
Опосредованное лучевое воздействие на спинной мозг при лечении онкологических заболеваний является одним из редчайших и очень сложных в диагностическом плане факторов, приводящих к постлучевой миелопатии (миелиту). Клинически и радиологически миелиты подразделяют на «поперечный» и «продольно-распространенный». Если патологический очаг захватывает больше половины поперечника спинного мозга и клинически проявляется парезом различной степени выраженности, проводниковыми чувствительными расстройствами с четкой поперечной границей, вегетативными на-
рушениями, то речь идет о поперечном миелите [1]. Продольно-распространенный миелит располагается по вертикальной оси спинного мозга на 3 сегмента и более, не имея четких границ чувствительных нарушений [2].
По срокам возникновения клинических признаков миелопатии выделяют 3 стадии [3]:
Ранняя: после воздействия очень высоких доз радиации на центральную нервную систему, возникающих, например, при авариях на атомных электростанциях, и проявляющихся тошнотой, дезориентацией и потерей сознания, с последующей
174 ПРАКТИЧЕСКАЯ МЕДИЦИНА
'1 (102) март 2017 г. / Том 1
смертью в течение нескольких дней без клинических признаков повреждения спинного мозга, которые, вероятно, просто не успевают проявиться.
Ранняя опосредованная: проявляется на сроках от 2 до 4 месяцев после лучевого воздействия под-пороговыми дозами. Клинически со стороны спинного мозга выражается в виде синдрома Лермитта с полным регрессом после нескольких месяцев. Факторы риска возникновения данного синдрома включают молодой возраст и большую протяженность облучаемого участка [4].
Поздняя: проявляется после лучевого воздействия через 4 месяца и более (до двух лет) двигательными и чувствительными нарушениями различной степени выраженности, с возможным развитием синдрома Броун — Секара. Поздние ми-елопатии протекают максимально тяжело, с плохим прогнозом для восстановления функций.
Однозначная точка зрения на патогенез поздней постлучевой миелопатии, механизмы отсроченного повреждающего действия радиации на центральную нервную систему (ЦНС) отсутствуют, что затрудняет выбор лечебной тактики и ухудшает прогноз. По данным Coderre J.A. и соавт. (2006), избирательное облучение сосудистой сети может приводить к некрозу белого вещества [2]. Отличительной чертой позднего радиационного поражения спинного мозга является демиелинизация, главная роль в которой отводится олигодендроцитам, ответственным за ре-миелинизацию после повреждений. В исследованиях Chow B.M. и соавт. (2000) было показано, что в течение часа после лучевого воздействия увеличивалась апоптотическая активность олигодендро-цитов и их клеток — предшественников, опосредованных р53 [5]. В то же время, в настоящее время нет никаких доказательств связи апоптоза олиго-дендроглии после лучевой терапии с появлением демиелинизации при поздних лучевых миелопатиях [6]. По данным позитронно-эмиссионной томографии выявляется увеличение поглощения F-2-фтор-2-дезоксиглюкоза в зоне повреждения спинного мозга, что связано с повышенной метаболической активности на месте повреждения [7, 8].
По данным медицинского радиологического Научного центра МЗ РФ (МРНЦ РАМН) города Обнинска в период с 1974 по 200l гг. в отделении хирургического и консервативного лечения лучевых повреждений наблюдались более 8 тыс. онкологических больных с местными лучевыми повреждениями покровных тканей и внутренних органов, развившимися в различные сроки после лучевого или комбинированного лечения болезни Ходжкина. Из них миелитов было всего 27 случаев, включая 3 случая раннего миелита и 24 случая позднего миелита [9].
Несмотря на редкость, патология привлекает внимание практикующих неврологов ввиду отсутствия четких клинических и нейровизуализаци-онных критериев, трудностей дифференциальной диагностики с миелитами другой этиологии (пара-неопластическая миелопатия, оптикомиелит Деви-ка, рассеянный склероз) и выбора тактики лечения. Развитие миелопатии как варианта паранеопласти-ческого синдрома не является характерным для лимфомы Ходжкина [10]. Однако, тем не менее, разграничение паранеопластической и постлучевой (особенно — поздней) миелопатии, по-нашему мнению, весьма условно и базируется только на вероятной причинно-следственной связи лучевой терапии с появлением клинической картины.
В связи с вышеизложенным, представляет интерес описание каждого клинического случая поздней постлучевой миелопатии.
Приводим анализ медицинской документации пациентки Д., 29 лет, страдающей классической лим-фомой Ходжкина (смешанно-клеточный вариант с поражением лимфатических узлов средостения) и находившейся на обследовании в неврологическом отделении клиники Ростовского государственного медицинского университета в октябре 2016 г. и январе 2017 г. На момент обследования у пациентки была стойкая ремиссия по основному заболеванию после комплексного лечения — 6 курсов полихимиотерапии (ПХТ) + конформное облучение. Данный случай вызвал сложности как при проведении дифференциальной диагностики и установлении причины миелопатии, так и при выборе тактики лечения пациентки.
Неврологическая симптоматика в виде нарушения поверхностной чувствительности в правой ноге появилась впервые в апреле 2016 года, спустя 2 года после верификации лимфомы Ходжкина и проведения вышеописанного курса комплексного лечения. Заболевание носило прогрессирующий характер, в течение месяца присоединилась слабость в ногах, тазовые нарушения. Магнитно-резонансная томография (МРТ) грудного отдела позвоночника выявила МР-картину деформирующего спондилеза, остеохондроза, жировую дегенерацию костного мозга, МР-признаки участков миелопатии в спинном мозге на уровне сегментов C5-Th1. Данных, доказывающих опухолевое или метастатическое поражение спинного мозга и его оболочек, не было выявлено. По месту жительства проходила повторные курсы неспецифической метаболической терапии по поводу «миелопатии» (без эффекта). С лета 2016 года присоединилась слабость в левой руке. Проведена МРТ шейного отдела (июль 2016 г.): МР-картина постлучевой спондилопатии C2-Th4 позвонков, миелопатии с уровня C5-Th3. Признаки межпозвонкового остеохондроза шейного отдела позвоночника, протрузии дисков С4-С5, С5-С6. Таким образом, в начале дифференциально-диагностического поиска, по данным МРТ исследования из круга дифференцируемых заболеваний удалось исключить компрессионные повреждения спинного мозга (грыжи дисков, экстрадуральные опухоли, в том числе и лимфому центральной нервной системы), прогрессирование основного заболевания с вовлечением цНс. Первичная спинальная эпидуральная неходжкинская лимфома встречается крайне редко, предпочтительно поражается по-яснично-крестцовый отдел позвоночника, сопровождаясь компрессией спинного мозга.
В диагностике очаговых поражений спинного мозга и в частности, радиационной миелопатии, ведущая роль в настоящее время отводится МРТ. Однозначных нейровизуализационных характеристик для лучевой миелопатии не существует. В доступной нам литературе мы встретили описание нескольких наблюдений, без гистологического подтверждения [8]. МРТ изменения включают в себя области низких сигналов на Т1-взвешенных изображениях, высокочастотных сигналов на Т2 с контрастным усилением. Высокоинтенсивный сигнал на Т2 связан с отеком и сливающимся некрозом, а контрастное усиление является следствием нарушения гематомиелического барьера [11].
На следующем диагностическом этапе на основании критериев McDonald (2010), учитывая дан-
ные анамнеза, клинических проявлении и данных МРТ, был исключен РС. Самым распространенным клиническим проявлением миелита при РС является нарушение вибрационной чувствительности и мышечно-суставного чувства, на втором месте — неярко выраженные асимметричные чувствительные или двигательные нарушения, реже выявляется синдром Броун — Секара, возможно появление симптома Лермитта, «синдрома сенсорно бесполезной руки», которые имеют ремиттирую-щий характер течения [12]. При проведении методов интраскопии очаги предпочтительно располагаются в области задних столбов спинного мозга, не затрагивая серое вещество, и занимают не более 1-2 сегментов спинного мозга [13]. В представленном нами клиническом случае данные анамнеза в виде первично-прогрессирующего течения и отсутствия обострений, клиническая картина заболевания (смешанный тетрапарез, четкая граница нарушения поверхностной чувствительности, без убедительных данных за изменения глубокой чувствительности и тазовые нарушения, клинически советующие полному поперечному миелиту), а так же данные МРТ исследования (распространенность очага по длиннику спинного мозга более чем на 3 сегмента), не соответствовало критериям постановки диагноза РС.
Исключение оптикомиелита Девикаиз круга возможных диагнозов вызвало наибольшие трудности. Обязательным диагностическим признаком в критериях постановки диагноза D.H. Miller и соавт. (2008) является сочетание неврита зрительных нервов и миелита. Критерии D.M. Wingerchuk и соавт. (2014) допускают постановку достоверного заболевания при наличии изолированного миелита [14, 15]. Миелит при болезни Девика имеет ряд характерных клинических особенностей: острое/подострое начало (на протяжении часов-дней) с развитием грубых двигательных, чувствительных и сфинктерных нарушений, что соответствует «полному поперечному миелиту» [16]. Радиологические признаки оптико-миелита: распространенность на протяжении более 3-х сегментов спинного мозга (продольный миелит) с поражением грудного отдела в 80% случаев, очаг поражения имеет центральную или дорсальную локализацию с вовлечением как серого, так и белого вещества, и характеризуется пятнистым (неоднородным) накоплением контрастного вещества [17].
В стационаре пациентке были выполнены исследования общего и биохимического анализа крови, иммунограмма, не выявившие значимых изменений, что позволило исключить системные аутоиммунные заболевания (системную красную волчанку, болезнь Шегрена), но не исключало оптикомиелит Девика. С целью исключения инфекционной или ауто-имунной причины миелита проведена люмбальная пункция, выполненный анализ ликвора отражал вариант нормы, что не противоречило диагнозу оп-тикомиелит Девика. Дополнительно образцы крови и ликвора были направлены для определения антител к аквапорину-4, что на сегодняшний день является патогномоничным для оптикомиелита Девика, результаты которых оказались отрицательными. Таким образом, пациентке был установлен диагноз «Постлучевая миелопатия», проведен курс пульс-терапии солумедролом (курсовая доза — 5 грамм), без какой-либо положительной динамики как в неврологическом статусе, так и по данным МРТ. У пациентки продолжала нарастать выраженность тетрапареза, чувствительных нарушений. МРТ шей-
ного отдела позвоночника, спинного мозга с контрастированием (01.2017 г.): выявлено прогресси-рование очаговых изменений за время наблюдения (существенное увеличение протяженности с момента исследования от апреля 2016 г., формирование зоны некроза с момента исследования от июля 2016 г.). Учитывая прогрессирующее течение, пациентке начат курс иммуносупрессивной терапии (митоксан-трон), проведен курс внутривенной иммуноглобу-линотерапии. Достигнута стабилизация процесса в течение 1 месяца, продолжается динамическое наблюдение.
Постлучевая миелопатия является редкой патологией в практике невролога и, несмотря на анамнез (возможная причинно-следственная связь с курсом лучевой терапии), остается диагнозом исключения. На сегодняшний день нет общепринятой теории патогенеза поздней постлучевой миелопатии, не разработаны схемы терапии, что можно объяснить немногочисленностью пациентов и трудностью проведения полноценных исследований. Для развития заболевания немаловажное значение имеет область приложения лучевой терапии. Большинство выявленных случаев постлучевой миелопатии, включая и описанное нами клиническое наблюдение, являются следствием облучения области шеи и грудной клетки, что требует дополнительного внимания со стороны онкологов и радиологов с целью изучения, коррекции вариантов и доз лучевой терапии данных областей и определения возможностей медикаментозной нейропротекции. Эффективность иммуносупрессивной терапии в лечении постлучевой миелопатии свидетельствует о значимости процессов демиелинизации в патогенезе данной патологии и требует более углубленного анализа. Возможно, поздняя постлучевая и паране-опластическая миелопатия являются одной имму-ноопосредованной нозологической синдромальной формой, что требует прицельного внимания онкологов с целью своевременного возобновления терапии основного заболевания.
2. Coderre J.A., Morris G.M., Micca P.L., et al. Late effects of radiation on the central nervous system: role of vascular endothelial damage and glial stem cell survival // Radiat. Res. — 2006. — 166. — P. 495-503.
3. Wong C.S., Fehlings M.G., Sahgal1 A. Pathobiology of radiation myelopathy and strategies to mitigate injury // Spinal Cord. — 2015. — 53. — P. 574-580.
4. Mul V.E., de Jong J.M., Murrer L.H., et al. Lhermitte sign and myelopathy after irradiation of the cervical spinal cord in radiotherapy treatment of head and neck cancer // Strahlenther Onkol. — 2012. — 188. — P. 71-76.
5. Chow B.M., Li Y.Q., Wong C.S. Radiation-induced apoptosis in the adult central nervous system is p53-dependent // Cell Death Differ. — 2000. — 7. — P. 712-720.
6. Atkinson S., Li Y.Q., Wong C.S. Changes in oligodendrocytes and myelin gene expression after radiation in the rodent spinal cord // Int. J. Radiat. Oncol. Biol. Phys. — 2003. — 57. — P. 1093-1100.
8. Uchida K., Nakajima H., Takamura T., et al. Neurological improvement associated with resolution of irradiation-induced myelopathy: serial magnetic resonance imaging and positron emission tomography findings // J. Neuroimag. — 2009. — 19. — P. 274-276.
9. Бардычев М.С., Курпешева А.К., Пасов В.В., и др. Лучевые повреждения при лечении болезни Ходжкина // Материалы VI Российской онкологической конференции. — М., 2002.
10. Шнайдер Н.А., Дыхно Ю.А., Ежикова В.В., Гончарова З.А.
176 ^tL ПРАКТИЧЕСКАЯ МЕДИЦИНА
'1 (102) март 2017 г. / Том 1
и др. Паранеопластический неврологический синдром. — Новосибирск: Наука, 2016. - 172 с.
11. Philippens M.E., Gambarota G., van der Kogel A.J., Heerschap A. Radiation effects in the rat spinal cord: evaluation with apparent diffusion coefficient versus T2 at serial MR imaging // Radiology. — 2009. — 250. — P. 387-397.
12. Jacob A. An approach to the diagnosis of acute transverse myelitis / A. Jacob, B.G. Weinshenker // Semin Liver Dis. — 2008. — 28 (1). — P. 105-120.
13. Lycklama G., Thompson A., Filippi M., et al. Spinal-cord MRT in multiple sclerosis // Lancet Neurol. — 2003. — 2 (9). — P. 555-562.
14. Miller D.H., Weinshenker B.G., Filippi M., et al. Differential
diagnosis of suspected multiple sclerosis: a consensus approach // Mult. Scler. — 2008. — 14. — P. 1157-1174.
15. Wingerchuk D.M., Banwell B., Bennett J.L., et al. International consensus diagnostic criteria for neuromyelitisoptica spectrum disorders // Neurology. — 2015. — 85. — P. 177-189.
16. Jarius S., Wildemann B., Paul F. Neuromyelitisoptica: clinical features, immunopathogenesis and treatment // Clin. Exp. Immunol. — 2014. — 176. — P. 149-164.
17. Симанив Т.О., Воробьева А.А., Смирнова Н.В. и др. Оптико-миелитиаквапорин-ассоциированные синдромы // Журн. неврол. и психиатр. — 2015. — 2. — С. 31-37.
Миелопатия
Миелопатия – сборное понятие, под которым подразумевают группу заболеваний острых и хронических поражений спинного мозга. Они могут вызваны различными механизмами и патологическими процессами, которые часто протекают вне его – травматическими, дегенеративно-дистрофическими, инфекционными, онкологическими, демиелинизирующими. Именно поэтому выделить основную группу риска невозможно.
Заболевание встречается у детей и людей старшего возраста. Для лечения миелопатии спинного мозга, реабилитации или стабилизации состояния нужно сначала установить ее причины, во многом определяющие прогноз.
Виды и причины миелопатии
Несмотря на то, что определить группу риска нельзя, между возрастом и причинами заболевания есть взаимосвязь. Нарастание дегенеративных изменений в позвоночнике и проблемы с сосудами характерны для пожилых людей. Позвоночно-спинномозговые травмы и новообразования часто приводят к развитию миелопатии в молодом и среднем возрасте от 30 до 50 лет. Из-за инфекций и генетически обусловленных заболеваний она возникает у подростков.
Клиническая картина, возможность и результаты лечения миелопатии зависят от ее локализации и вида.
Дискогенная или спондилогенная
Грыжи межпозвонковых дисков, формирование остеофитов и суженный позвоночный канал на поздних стадиях остеохондроза приводят к компрессии спинного мозга и ухудшению кровообращения.
Атеросклеротическая
Развитие этого вида миелопатии с нарушением спинального кровообращения вызывают сосудистые факторы – атеросклероз и артериальная гипертензия, а также сердечные патологии и эндокринные заболевания (сахарный диабет).
Посттравматическая
К повреждениям спинного мозга и сдавливанию артерий приводят травмы, отеки и нейровоспаления – переломы, смещения дисков в результате резкого хлыстового удара, например во время аварии, или перенос тяжестей, при котором высокие нагрузки прикладываются по оси.
Карциноматозная
Причиной компрессии спинного мозга становятся метастатические опухоли, которые прорастают из пораженных позвонков – лимфомы, саркомы, рак желудка, легких, молочной железы, простаты.
Инфекционная
Миелопатии этого типа возникают на фоне инфицирования золотистым стафилококком и менингита, осложнений туберкулеза, для которых характерны формирование абсцессов, изменения формы и структуры спинного мозга с постепенным вовлечением сосудов.
Демиелинизирующая
В развитии миелопатии играют роль аутоиммунные, генетически обусловленные заболевания, при которых разрушается миелиновая оболочка нервных волокон спинного и головного мозга.
Радиационная или лучевая
В этом случае поражения спинного мозга – гиалиноз и закупорка сосудов обусловлены побочным эффектом лучевой терапии, которая была направлена на находящуюся рядом зону. При отсутствии терапии и тяжелых повреждениях заболевание прогрессирует.
Грамотное комплексное лечение некоторых типов миелопатии – дегенеративной, инфекционной, посттравматической позволяет добиться ремиссии, улучшений неврологических показателей и качества жизни.
Локализация и симптомы миелопатии
Заболевание может затрагивать все отделы позвоночника на одном или нескольких уровнях. Чаще всего встречается шейная и поясничная миелопатия, к которой ведут дегенеративные процессы. Заболевание грудного отдела диагностируется реже. У пациентов наблюдаются:
- слабость, онеменение в ногах и руках с сопутствующими нарушениями мелкой моторики – трудности при письме, застегивании одежды;
- интенсивная боль в спине – тупая или ноющая, постоянная или возникающая при движении;
- снижение температурной и болевой чувствительности, дисфункции тазовых органов – в первую очередь мочеиспускания;
- параличи, спастические парезы и парапарезы, сочетающиеся между собой и вызывающие нарушения походки.
Особенности лечения миелопатии шейного, поясничного, грудного отдела позвоночника зависят от характера повреждений и выраженности симптомов.
Диагностика, лечение и реабилитация при миелопатии
«Золотой стандарт» диагностики миелопатии – МРТ, которая позволяет четко визуализировать очаг и определить тяжесть поражения. Дополнительно выполняют рентген со сгибанием и разгибанием, КТ с двухмерной реконструкцией, чтобы оценить состояние позвоночника – мобильность, физиологический изгиб, наличие остеофитов и компрессию. Для лечения миелопатии используются оперативные и консервативные методы:
- ЛФК для повышения активности, увеличения мышечной силы и амплитуды движений;
- физиотерапия для восстановления чувствительности, уменьшения спастики и болевых ощущений;
- массаж для стимуляции мышц, предупреждения контрактур и улучшения кровоснабжения;
- медикаментозные средства для длительной терапии основного заболевания и курсами;
- хирургическое лечение.
Читайте также:
