МРТ при синдроме Рамсея Ханта (СРХ)
Добавил пользователь Алексей Ф. Обновлено: 07.01.2026
(Ганглионит узла коленца; синдром Рамсея Ханта; вирусный нейронит)
, MD, Columbia University Medical Center and New York Presbyterian Hospital
Опоясывающий лишай уха — вызываемая вирусом опоясывающего герпеса инфекция кластеров нервных клеток (ганглиев), которые контролируют нервы, отвечающие за слух, равновесие (8 пара черепных нервов) и движение мышц лица (7 пара черепных нервов).
Опоясывающий герпес ( опоясывающий лишай Опоясывающий лишай Опоясывающий лишай — это болезненная кожная сыпь, вызванная вирусной инфекцией, которая возникает при реактивации вируса ветряной оспы. Причина, которая приводит к реактивации вируса, неизвестна. Прочитайте дополнительные сведения — вируса, который вызывает ветрянку. После эпизода ветряной оспы этот вирус дремлет в нервных корешках и может реактивироваться, пройдя вниз по нервным волокнам до кожи, где он вызывает болезненные язвы. Как правило, установить причину реактивации не представляется возможным, но иногда это происходит, когда иммунная система ослаблена каким-либо заболеванием, например, раком или СПИДом, или лекарственным препаратом.
Симптомы ганглионита узла коленца
К симптомам ганглионита узла коленца относятся:
сильная боль в ухе;
наполненные жидкостью пузырьки (везикулы) на внешней части уха (ушная раковина) и в ушном канале;
потеря слуха Потеря слуха и глухота , которая может быть постоянной либо полностью или частично восстановиться;
в редких случаях — головная боль, спутанность сознания или ригидность затылочных мышц.
Иногда поражаются другие пары черепных нервов.
Диагностика ганглионита узла коленца
Иногда лабораторные исследования или анализ жидкости из пузырьков
Иногда магнитно-резонансная томография (МРТ)
Как правило, врачи ставят диагноз ганглионита узла коленца, основываясь на результатах физикального обследования. В некоторых случаях врачи берут соскобы везикул для изучения под микроскопом и посева Посев Врачи могут поставить диагноз многих кожных заболеваний путем простого осмотра кожи. Полный осмотр кожи включает исследование волосистой части головы, ногтей и слизистых оболочек. Чтобы лучше. Прочитайте дополнительные сведения ).
Лечение ганглионита узла коленца
Иногда кортикостероидные препараты, например, преднизон, для уменьшения воспаления
В некоторых случаях — противовирусные препараты для лечения инфекции
В редких случаях — хирургическое вмешательство для снижения давления на лицевой нерв
Чтобы облегчить симптомы и вылечить ганглионит узла коленца, врачи могут назначать пациентам лекарственные препараты. Однако эффективность этих препаратов до сих пор не подтверждена. Кортикостероиды, такие как преднизон, назначают, чтобы блокировать воспаление. Противовирусные препараты, например, ацикловир или валацикловир, могут способствовать уменьшению продолжительности инфекции и обычно назначаются людям, иммунная система у которых ослаблена или нарушена. Облегчить приступы головокружения помогает диазепам. Для снятия боли назначают опиаты для приема внутрь. Людям, у которых наблюдается длительная остаточная боль (постгерпетическая невралгия), могут быть назначены другие препараты, например, лечебные кожные пластыри, противосудорожные препараты или трициклические антидепрессанты.
Если у пациента полностью парализовано лицо, требуется оперативное вмешательство, чтобы ослабить давление на лицевой нерв.
ПРИМЕЧАНИЕ: Это — пользовательская версия ВРАЧИ: Нажмите здесь, чтобы перейти к профессиональной версии
Авторское право © 2022 Merck & Co., Inc., Rahway, NJ, США и ее аффилированные лица. Все права сохранены.
МРТ при синдроме Рамсея Ханта (СРХ)
а) Терминология:
1. Аббревиатура:
• Синдром Рамсея Ханта (СРХ)
2. Синоним:
• Опоясывающий герпес с поражением уха
3. Определение:
• СРХ: поражение вирусом опоясывающего герпеса чувствительных волокон ЧН VII и ЧН VIII, а также части наружного уха, иннервируемой ушно-височным нервом
б) Визуализация:
1. Общая характеристика:
• Лучший диагностический критерий:
о Патологическое контрастирование ЧН VII ± ЧН VIII в области дна внутреннего слухового канала, а также перепончатого лабиринта (полное или частичное) на МРТ Т1 С+
• Морфология:
о Линейное или веретеновидное контрастирование ВСК
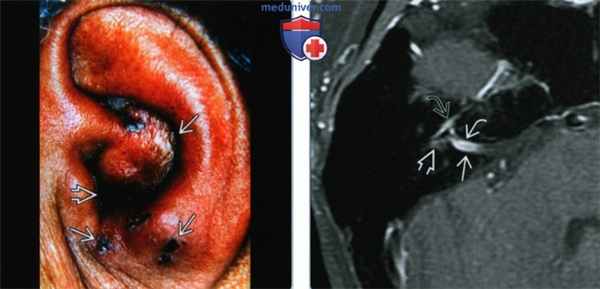
(Слева) На фото наружного уха видна геморрагическая везикулярная сыпь на ушной раковине и в наружном слуховом канале. Наличие такой сыпи, часто болезненной, наряду с нейропатией лицевого и преддверно-улиткового нервов, делает очевидным диагноз синдрома Рамсея Ханта (СРХ).
(Справа) При аксиальной MPT Т1 ВИ С+ FS у пациента с СРХ определяется линейное контрастное усиление ЧН VII в области дна ВСК с распространением на лабиринтный и барабанный сегменты. Верхний преддверный нерв также контрастируется в области дна ВСК и в преддверии.
2. МРТ при синдроме Рамсея Ханта:
• Т2 ВИ:
о Т2 высокого разрешения (- Утолщение ЧН VII и VIII в области дна
- При выраженном утолщении может имитировать фундальную вестибулярную шванному
• FLAIR:
о Нормальная паренхима головного мозга
• Т1 ВИ С+:
о Наружное ухо:
- Контрастирующиеся везикулы наружного уха в сочетании с воспалительными изменениями
о Лицевой нерв в височной кости:
- Обычно контрастируется на всем протяжении:
Достоверно накапливают контраст лабиринтный сегмент ЧН VII и коленчатый ганглий
о Перепончатый лабиринт:
- Выраженное в различной степени поражение улитки, преддверия, полукружных каналов:
Чаще всего контрастируется улитковая часть
- Перепончатый лабиринт может не контрастироваться даже при наличии тугоухости и головокружения
о ВСК:
- Линейное или шаровидное С+ в области дна ВСК (ЧН VII и VIII)
- ВСК может не контрастироваться даже при наличии тугоухости ± головокружения
о Мозговой ствол:
- Ядра лицевого нерва в стволе мозга редко контрастируются при СРХ
3. Рекомендации по визуализации:
• Лучший метод визуализации:
о МРТ головного мозга с контрастным усилением с фокусом на ММУ-ВСК и височную кость
о Изменения лучше всего видны на МРТ Т1 С+ с FS
• Выбор протокола:
о Если везикулярная сыпь в наружном ухе клинически очевидна, лучевая диагностика по поводу сопутствующего паралича ЧН VII ЧН VIII не требуется
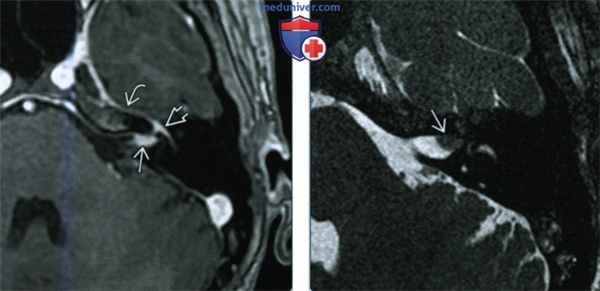
(Слева) При аксиальной МРТ SPGR С+ определяется контрастное усиление дна ВСК слева, а также лабиринтного сегмента, коленчатого ганглия, переднего барабанного сегмента ЧH VII. Накапливает контраст и большой поверхностный каменистый нерв (ветвь ЧH VII), расположенный вдоль переднего края вершины пирамиды.
(Справа) При аксиальной MPT Т2ВИ FS с увеличением у этого же пациента в области дна ВСК визуализируются утолщенные, воспаленные ЧН VII и ЧН VIII, изоинтенсивные головному мозгу.
в) Дифференциальная диагностика синдрома Рамсея Ханта:
1. Паралич Белла:
• Контрастирование ЧН VII; отсутствие контрастирования перепончатого лабиринта или ЧН VIII
• Контрастирующийся «хохолок» в области дна ВСК
• Контрастирование ВСК обычно менее интенсивное, чем при СРХ
2. Менингит:
• Головная боль, ригидность затылочных мышц, лихорадка
• Утолщение, диффузное контрастирование мозговых оболочек
• Анализ ликвора помогает сделать заключение
г) Патология. Общая характеристика:
• Этиология:
о Классическая гипотеза: периодическая реактивация дремлющей вирусной инфекции в коленчатом ганглии:
- Вирус опоясывающего герпеса можно получить из содержимого везикул или слюны
д) Клинические особенности:
1. Проявления:
• Типичные признаки/симптомы:
о Паралич лица и нейросенсорная тугоухость в сочетании с везикулярной сыпью наружного уха
• Другие признаки/симптомы:
о Лихорадка, головокружение, тошнота, рвота
о Глубокая жгучая боль в ухе
2. Течение и прогноз:
• Боль в ухе, затем появление эритематозной везикулярной сыпи на наружном ухе в течение - 7 дней
• Краниальная нейропатия после появления боли в ухе:
о До или после разрыва везикул
о До: лучевая диагностика может применяться для визуализации причин паралича, обусловленного поражением ЧН VII
3. Лечение:
• Вначале консервативное:
о Теплые компрессы и анальгетики
о Уход за роговицей при параличе лица
• Медикаментозное лечение:
о Кортикостероиды ± ацикловир (↓ боли, улучшение функции ЧН VII)
е) Диагностическая памятка. Следует учесть:
• МРТ выполняется только при атипичных клинических проявлениях
Постзостерный синдром Рамсея–Ханта
Представлены литературный обзор по постгерпесной невралгии и клинический случай неблагоприятного исхода ветряной оспы в виде сформировавшегося постзостерного ганглионита лицевого и тройничного нервов — синдрома Рамсея–Ханта, нейропатии большого затылочног
The literature overview on post-herpes neuralgia was given, and a clinical case of adverse outcome of chicken pox as a formed post-zoster ganglionitis of facial and trifacial nerves — Ramsay Hunt syndrome, neuropathy of greater occipital nerve, was presented. The strategy of the therapy was discussed.
Актуальной проблемой современной медицины является постгерпетическая невралгия, что связано с ростом числа герпесвирусных заболеваний с формированием болевого синдрома в случае поражения ганглиев. Частота опоясывающего герпеса после перенесенной ветряной оспы с формированием невралгии в различных странах мира составляет от 0,4 до 1,6 случая заболевания на 1000 пациентов в год в возрасте до 20 лет.
Вирус варицелла-зостер (ВГЧ 3-го типа), вызывая всем хорошо известную детскую инфекцию — ветряную оспу, может приводить к серьезным поражениям периферической нервной системы — ганглионевритам и ганглиорадикулитам.
Доказано, что в условиях даже одного субклона для вирионов характерны полиморфизм и антигенная вариабельность. Поэтому ВГЧ 3-го типа у одних людей вызывает ветряную оспу, а у других — опоясывающий герпес, поражая у одних только кожу, у других — слизистые оболочки, а инфицируя эндоневральные и периневральные клетки ольфакторных волокон и попадая в паренхиматозные клетки обонятельной луковицы, может проникать в центральную нервную систему (ЦНС). Полагают, что такой путь передачи — единственный способ проникновения в ЦНС нейротропных вирусов при инфекциях с низким уровнем вирусемии. Так, первично или после перенесенной ветряной оспы вирус через кожу и слизистые, далее лимфогенным и гематогенным путем проникает в ганглии, межпозвонковые узлы и задние корешки спинного мозга, где долгое время может персистировать в латентном состоянии. Вирус инфицирует ветви обонятельного или тройничного нервов, достигает луковицы обонятельного тракта или гассерова узла, что клинически проявляется острым ганглионитом [4].
При снижении иммунологической реактивности под влиянием различных факторов, таких как иммунодефицитное состояние, обострение хронических заболеваний, прием иммунодепрессантов, интоксикации, латентная инфекция может активизироваться. Активация вируса сопровождается развитием ганглионита (межпозвонковых ганглиев или ганглиев черепных нервов, а также задних корешков). При данном заболевании поражаются региональные, чувствительные ганглии с развитием корешковых болей, парастезий, сегментарных нарушений чувствительности, что отмечается практически у каждого больного [5].
По локализации выделяют поражения: тригеминального (гассерова узла); коленчатого; шейных; грудных; пояснично-крестцовых ганглиев [5].
По МКБ-10 классифицируют:
- опоясывающий лишай с другими осложнениями со стороны нервной системы (B02.2);
- постгерпетический ганглионит узла коленца лицевого нерва (G53.0);
- полиневропатию (G63.0);
- невралгию тройничного нерва (G53.0).
Следствие поражения коленчатого узла (ганглия коленца) вирусом опоясывающего лишая (herpes zoster) описали: в 1907 г. американский невролог J. R. Hunt, а в 1912 г. французские неврологи Dejerine, Souques, Sicard. Проявления заболевания начинаются остро, с общих симптомов интоксикации и повышения температуры. У части больных может наблюдаться поражение лицевого нерва и невралгия тройничного нерва с продолжительностью до нескольких недель. J. R. Hunt (1907) подробно описал четыре клинические формы этого заболевания, которое в дальнейшем стало называться синдромом Ханта. В случаях очень распространенного ушного зостера последний захватывает не только наружный слуховой проход, ушную раковину, сосцевидный отросток, но и барабанную перепонку, которая иногда очень тяжело страдает. В таких случаях поражается область, иннервируемая V, VII и Х парами, причем поражение этих нервов сопровождается поражением ганглиев, соответственных черепных нервов или же анастомозов, связывающих конечные разветвления всех вышеперечисленных нервов [6, 7].
При ганглионите гассерова узла отмечаются мучительные боли и высыпания в зоне иннервации I, II, III или всех ветвей тройничного нерва. По мнению ряда авторов герпетические ганглиониты гассерова узла встречаются чаще, чем ганглиониты межпозвонковых узлов.
У большинства больных с данной локализацией процесса наблюдаются повышение температуры и отек лица на пораженной стороне, а также болезненность в точках выхода тройничного нерва. Невралгия (от др.-греч. νεuρον — жила, нерв +aλγος — боль) — поражение периферических нервов, характеризующееся приступами боли в зоне иннервации какого-либо нерва. В отличие от неврита при невралгии нет двигательных нарушений и выпадения чувствительности [7–9].
Постзостерная (постгерпетическая) невралгия (ПГН) возникает примерно у 10–15% пациентов, страдающих опоясывающим лишаем. Развитию постзостерной невралгии предшествуют одновременно общая нечувствительность пораженного дерматома и сильная боль в начальной фазе опоясывающего лишая. ПГН описывается как постоянная мучительная, жгучая боль различной интенсивности, иногда сопровождаемая внезапными кратковременными приступами дизестезии, такими как пощипывание и пронзительная боль.
Болевой синдром имеет выраженную вегетативную окраску в виде жгучих, приступообразных, резких болей, усиливающихся в ночное время. В дальнейшем боли рецидивируют и беспокоят больного в течение многих месяцев и лет, вызывая потерю трудоспособности, нарушая сон, изменяя его психический и эмоциональный статус, формируя постоянный синдром — постгерпетической невралгии. Затяжной, тяжелый характер заболевания с длительным, выраженным алгическим синдромом способствует формированию личностных расстройств психики [10].
Клинический пример ганглионита, развившегося в результате осложненного течения ветряной оспы
Больная Арина К., 20.06.1992 г. рожд. История болезни № 18230.
Анамнез жизни. Девочка родилась от первой беременности, протекавшей без патологии, срочных родов, весом 3650 г, длиной 53 см. Ранний постнатальный период протекал без патологии, на грудном вскармливании до 6 мес. Развитие соответствовало возрасту. Аллергологический анамнез не отягощен. Прививки проводились согласно НКП, патологических реакций в поствакцинальном периоде не отмечалось. Перенесла в 2,5 года коклюш, в 4 года — энтеровирусную миалгию. Девочка проживала в Краснодарском крае.
Анамнез заболевания. В 7 лет (1999 г.) заболела ветряной оспой, протекавшей с обилием высыпаний на коже и слизистых, которые преимущественно локализовались в области головы, шеи, лица, ушей. Регистрировался гипертермический синдром с последующим длительным субфебрилитетом (в течение 40 дней). На 21-й день от начала заболевания вновь отмечался подъем температуры до 40 °С. Накануне за несколько дней девочка жаловалась на сильную «жгучую» боль в области глазниц, лба, где вновь появились папулезно-везикулезные высыпания. На этом фоне жаловалась на светобоязнь, слезотечение, звукошумовую непереносимость, отмечалась упорная цефалгия. Была госпитализирована.
В стационаре получала антибиотико- и глюкокортикоидную терапию (противовирусная терапия не проводилась). Состояние на фоне лечения улучшилось, исчез болевой синдром. Однако спустя 6 мес появились повторные жалобы на «распирающие», «жгучие» боли в области глаз, ушей, шейной области, что сопровождалось гиперемией и отеком в периорбитальной области. На фоне короткого курса гормональной терапии указанные симптомы купировались. Весной 2000 г. повторились те же жалобы, получала лечение в условиях санатория без особого эффекта, после которого периодически госпитализировалась в неврологическое отделение. Получала симптоматическую терапию.
В 2002 г. на фоне усиления болевого синдрома той же локализации проведена терапия ацикловиром с положительным эффектом. В 2003 г. отмечался очередной приступ более интенсивных и продолжительных болей в области глаз, шеи, ушей, со слезотечением, упорной головной болью. Диагностирован синдром Рамсея–Ханта. Получен кратковременный эффект от терапии ацикловиром внутривенно. Через 2 недели приступ повторился, но меньшей интенсивности. В течение 2003 г. проводилась месячным курсом терапия Вифероном-2, Т-активином, девочка редко посещала школу из-за повторных приступов болевого синдрома. Консультирована была в Москве в Госмедакадемии им. И. М. Сеченова, где психиатром диагностирован ипохондрический синдром.
В феврале 2004 г. обратилась за помощью на нашу кафедру, где при осмотре подтвержден синдром Рамсея–Ханта после перенесенной ветряной оспы и герпес зостер, что требовало исключения других фоновых персистирующих герпесвирусных инфекций и оценки иммунного статуса.
При неврологическом обследовании отмечались жалобы на головокружение, сопровождавшееся тошнотой, боли в затылочно-околоушной и периорбитальной зонах. Отмечены слабость конвергенции, значительная сглаженность носогубной складки справа, гиперестезия в зоне С2-С3 справа; болезненность в области большого затылочного нерва справа; повороты головы в стороны были ограничены; общий тон настроения сниженный, девочка установочно фиксирована была на своих ощущениях.
Рентгенологически в области шейного отдела позвоночника патология не выявлена.
При осмотре окулистом выявлялись спазм аккомодации, приобретенная миопия.
Проведено серологическое и молекулярно-генетическое обследование на весь спектр герпесвирусных инфекций, получены положительные результаты на вирус Эпштейна–Барр, ВГЧ 1-го, 6-го типов при исследовании крови, мочи и слюны методами иммуноферментного анализа (ИФА) и полимеразной цепной реакции (ПЦР), что указывало на медленную персистирующую герпесвирусную инфекцию, включая варицелла-зостерную инфекцию.
ИФА на anti-IgG к вирусу варицелла-зостер — 1:16000; anti-IgG — к HSV1–1:24000; anti-IgG к EBV (к VCAg — 1:160; к EAg — 1:80); в слюне: DNA HHV-6 — положит., DNA EBV — положит., DNA СMV — положит; в моче: DNA HHV-6 — положит., DNA EBV — положит., DNA СMV — положит., DNA HSV1 — положит.; в крови — отр.
В иммунном статусе выявлена недостаточность клеточного иммунитета: снижение CD 19+ , CD 20+ , CD 4+ , ИРИ — до 0,89. Показатели иммуноглобулинов А, М и G в пределах нормы.
Консультирована и обследована иммунологом в НИИ иммунологии РАМН, где установлено вторичное иммунодефицитное состояние на фоне медленно текущей персистирующей герпесвирусной инфекции.
При исследовании общих анализов крови, мочи, биохимического анализа крови патология не выявлена.
Таким образом, с учетом данных анамнеза заболевания и результатов объективного обследования у больной был диагностирован синдром Рамсея–Ханта (ганглионит с поражением ядер лицевого и тройничного нервов, нейропатией большого затылочного нерва), который развился на фоне хронической смешанной персистирующей ГВИ: HVZ, HSV1, СMV и HHV 6-го типа со сформировавшимся вторичным иммунодефицитным состоянием. Сопутствовал астеноипохондрический синдром на фоне хронического болевого синдрома. Следует отметить несвоевременность назначения противовирусной терапии, которая первично не была применена в остром периоде заболевания ветряной оспой, протекавшей тяжело, и в рецидивирующем характере течения, что требовало уточнения фоновой патологии, обусловившей неблагоприятный исход этой инфекции.
Учитывая кратковременность эффекта на предшествующую противовирусную и гормональную терапию, на клинической базе нашей кафедры — в Морозовской городской детской клинической больнице решено было в комплексную терапию включить курс высокоактивных в/в иммуноглобулиновых препаратов (пентаглобина, октагама — 22,5 г на курс), миелопида интраназально, Т-активина 100 мг в/м на 1 мес; с противовоспалительной целью — в/в получала фосфоглив прерывистым курсом — 3 мес, гепон интраназально 2 недели, нейропсихотропные препараты: амитриптилин 1/2 табл. на ночь, Финлепсин 1/2 табл. 2 раза — до 3 мес, Кавинтон 1 табл. 3 раза в сутки 1 мес, Фенибут 1 табл. 3 раза на время стационарного лечения. На фоне указанной терапии состояние больной значительно улучшилось. Так как девочка переехала на постоянное жительство в Москву, было продолжено наблюдение в катамнезе на нашей кафедре и в неврологическом центре. За время 5-летнего наблюдения у девочки интенсивность и частота повторных приступов болевого синдрома значительно уменьшились на фоне повторных курсов нейротропных и иммунотропных препаратов, включая и противовирусную терапию Фамвиром. Это способствовало включению больной в нормальный режим обучения в школе и параллельно в музыкальной школе (чего она была лишена в течение нескольких лет). Обучение продолжила в музучилище.
В современном стандарте и протоколе лечения и профилактики ветряной оспы и опоясывающего герпеса приводятся следующие рекомендации.
Противовирусная терапия
При среднетяжелой и тяжелой формах ветряной оспы или опоясывающего лишая, а также при иммунодефицитных состояниях, в том числе пациентам, получающим иммуносупрессивную терапию цитостатиками или глюкокортикостероидами, страдающим фоновой энцефалопатией, независимо от формы тяжести в качестве этиотропной терапии применяют противовирусные препараты.
Препарат выбора при ветряной оспе:
- Ацикловир внутрь по 0,2 г (детям до 2 лет); по 0,4 г (детям 2–6 лет); по 0,8 г (детям старше 6 лет) 4 раза в сут, 7 дней.
Препарат выбора при опоясывающем лишае:
- Валацикловир внутрь по 1 г 3 раза в сут, 7 дней.
При тяжелой форме противовирусные препараты назначаются парентерально:
- Ацикловир в 100 мл 0,9% раствора хлорида натрия в/в капельно по 5–10 мг/кг.
Препарат выбора при опоясывающем герпесе для местного применения:
- Валацикловир (мазь или крем) на пораженные участки 5 раз в сут с интервалом 4 ч, 5–10 дней + Глицирризиновая кислота (крем) на пораженные участки 5 раз в сут с интервалом 4 ч, 5–10 дней.
Иммунотерапия
При развитии энцефалита или менигоэнцефалита, а также при тяжелых атипичных формах с целью интенсификации этиотропной терапии вводятся стандартные иммуноглобулиновые препараты: иммуноглобулин человека нормальный (IgG + IgA + IgM) в/в капельно 5 мл/кг 3–5 введений (при необходимости через 1 неделю курс повторить) или иммуноглобулин человека нормальный в/в капельно 5–8 мл/кг 1 раз в сут, 3–5 введений.
Проводится терапия антигистаминными препаратами наряду с антипиретиками (парацетамол, ибупрофен), при болевом синдроме назначаются анальгетики.
Вакцинопрофилактика ветряной оспы
В настоящее время используется вакцина Варилрикс, вводится по 0,5 мл подкожно или внутримышечно.
Одна доза вакцины Варилрикс назначается детям в возрасте от 12 месяцев и до 13 лет, а две дозы назначаются подросткам с 13 лет и взрослым с интервалом между дозами 6–10 недель — такая схема вакцинации обеспечивает 95% оптимальную защиту против ветряной оспы.
Вакцина Варилрикс может назначаться одновременно с другими детскими вакцинами, такими как корь–краснуха–паротит, что делает ее прекрасным кандидатом для универсальной массовой вакцинации.
Показана для однократной постэкспозиционной профилактики в период до 96 часов после контакта с вирусом (предпочтительно в течение 72 часов). Это уменьшает тяжесть ветряной оспы и является обоснованной стратегией предотвращения вспышек.
Вакцина Варилрикс™ может храниться в обычном холодильнике при температуре 2–8 °C до 2 лет.
В мире применяется вакцина Зоставакс, которая применяется у взрослых с целью профилактики опоясывающего герпеса.
Заключение
Применение своевременного комплексного системного подхода в лечении основных причин заболевания постзостерного ганглионита с использованием противовирусных, иммунотропных препаратов, нейротропных, а также и препаратов, воздействующих на болевой синдром, позволяет уменьшить степень инвалидизации подобной категории больных.
Существующие мифы о том, что ветряная оспа является легкой детской инфекцией, развеиваются, когда эта инфекция наслаивается на персистирующую другую герпесвирусную инфекцию, на иммунодефицит, органическую сосудистую патологию головного мозга и др., часто предопределяющих неблагоприятный исход заболевания.
Поэтому вопрос о назначении противогерпетической терапии в подобных случаях решается в пользу назначения таковой даже при легкой форме ветряной оспы.
Принципиально важной остается недооценка значимости профилактики этой инфекции, где до настоящего времени существует расхожее, ничем не подкрепленное мнение о том, что:
- ветряная оспа — не опасная инфекция;
- с введением прививок возрастает риск развития опоясывающего лишая;
- вакцина не дает желаемого эффекта;
- введение вакцины чревато высоким риском осложнений и т. д.
Авторам этой статьи очень хочется привлечь внимание педиатров и врачей общей практики к проблеме лечения и профилактики ветряной оспы у детей и взрослых, так как, переболев ею однажды даже в легкой форме, продолжаем в себе носить этот вирус на протяжении всей жизни с огромным риском потерять беременность, родить инвалида или заболеть тяжелой неврологической патологией.
Литература
- Гранитов В. М. Герпесвирусные инфекции. НГМА, 2001. С. 80.
- Деконенко Е. П. Вирус герпеса и поражение нервной системы // Рос. мед. журнал. 2002. № 2. С. 46–49.
- Диагностика герпесвирусных инфекций человека: меморандум совещания ВОЗ // Бюл. ВОЗ. 1991. № 3. С. 11–18.
- Редькин Ю. В., Одокиенко А. Ю. Современные подходы в фармакотерапии рецидивирующей герпетической инфекции // Экспериментальная и клиническая фармакология. 2005. Т. 68, № 6. С. 67–71.
- Опоясывающий герпес / Под ред. А. А. Кубановой. М.: ДЭКС-Пресс, 2010. 24 с.
- Thakur R., Philip A. G. Treating herpes zoster and postherpetic neuralgia: аn evidence-based approach // Journal of Family Practice. 2012. Vol. 61. № 9. S9–15.
- Hunt J. R. On herpetic inflammations of the geniculate ganglion: a new syndrome of its complications // [The] Journal of nervous and mental disease, 1907; 34: 73–96.
- Hunt J. K. The sensory field of the facial nerve: a further contribution to the simptomatology of the geniculate ganglion // Brain. 1915. Vol. 38. P. 418–446.
- Bhupal H. K. Ramsay Hunt syndrome presenting in primary care. Practitioner 2010. 254 (1727). С. 33–53.
- Максимова М. Ю., Синева Н. А., Водопьянов Н. П. Постгерпетические невралгии (невропатии), обусловленные опоясывающим герпесом // Фарматека. 2013. № 10. С. 58–62.
Ф. С. Харламова* , 1 , доктор медицинских наук, профессор
В. Ф. Учайкин*, доктор медицинских наук, профессор, академик РАН
И. М. Дроздова**
А. Е. Анджель**
* ГБОУ ВПО РНИМУ им. Н. И. Пирогова МЗ РФ, Москва
** ГБУЗ Морозовская ДГКБ ДЗМ, Москва
Паралич Белла
Паралич Белла — это форма временного лицевого паралича, вызванного повреждением или травмой лицевых нервов. Лицевой нерв, называемый также седьмым черепным нервом, проходит через узкий костный канал (называемый фаллопиевым каналом) в черепе под ухом к мышцам с каждой стороны лица. Большую часть своего путешествия нерв заключен в эту костную оболочку.
Каждый лицевой нерв направляет мышцы на одной стороне лица, в том числе те, которые контролируют моргание и закрытие глаз, а также выражения лица (улыбку и хмурый взгляд). Дополнительно, лицевой нерв несет нервные импульсы к слезным и слюнным железам, мышцам небольшой кости в середине уха. Лицевой нерв также передает вкусовые ощущения от языка.
Паралич Белла назван в честь сэра Чарльза Белла, шотландского хирурга 19-го века, который описал лицевой нерв и его связь с состоянием. Паралич Белла, который никак не связан с инсультом, является наиболее частой причиной лицевого паралича. Как правило, он поражает только один из двух лицевых нервов, поэтому проявляется только на одной стороне лица, но в редких случаях может воздействовать на обе стороны одновременно.
Признаки и симптомы
Ранние симптомы паралича Белла могут включать:
- небольшую лихорадку (повышение температуры);
- боль за ухом;
- ригидность затылочных мышц;
- слабость и/или скованность на одной стороне лица.
Симптомы могут начаться внезапно и быстро прогрессировать в течение нескольких часов, иногда после воздействия холода или сквозняка. Затронуто может быть часть или все лицо.
В большинстве случаев паралича Белла возникает только лицевая мышечная слабость, и паралич лица является временным. Большинство случаев разрешается через две-три недели. Примерно 80% случаев разрешаются в течение трех месяцев. Однако некоторые случаи сохраняются. Изредка поражается только верхняя или нижняя половина лица.
В тяжелых случаях паралича Белла лицевые мышцы на пораженной стороне полностью парализуются, что приводит к тому, что эта сторона лица становится гладкой, невыразительной и неподвижной. Часто отверстие между верхним и нижним веками (глазная щель) увеличивается и остается открытой во время сна. Это может привести к невозможности закрыть глаз на пораженной стороне. Люди с параличом Белла могут не иметь роговичного рефлекса, следовательно, глаз на пораженной стороне не закрывается при прикосновении к роговице.
Если сжатая область лицевого нерва находится рядом с ветвлением других нервов, может быть снижение выработки слюны и/или слез. Некоторые люди с параличом Белла испытывают потерю вкусовых ощущений на одной стороне рта, слюнотечение и повышенную чувствительность к звуку (гиперакуз) на пораженной стороне головы. В некоторых случаях реакция пострадавшего на укол за ухом также уменьшается.
Восстановление от паралича Белла зависит от степени и серьезности повреждения седьмого черепного нерва. Если паралич лица только частичный, можно ожидать полного выздоровления. Пораженные мышцы обычно возвращаются к своей первоначальной функции в течение одного-двух месяцев.
Если по мере восстановления нервные волокна срастаются с мышцами, отличающимися от тех, которые они первоначально иннервировали, могут появиться произвольные движения мышц лица, сопровождаемые непроизвольными сокращениями других мышц лица (синкинезия). Иногда в результате паралича Белла развивается явление называемое «крокодиловы слезы» (слезы, не вызванные эмоциями), связанные с лицевыми мышечными сокращениями.
Причины и факторы риска
Заболевание возникает в результате воспалительного процесса или сдавливания лицевого нерва; конкретная причина не была идентифицирована, но корреляция с вирусными инфекционными процессами наблюдается в большинстве случаев. На самом деле, у человека, пораженного вирусом, также может возникнуть воспаление лицевого нерва; это вызывает отек, который, в свою очередь, вызывает повышение давления в канале, пересекаемом нервом (так называемый фаллопиев канал), с последующим уменьшением притока крови и кислорода к нервным клеткам. Иногда повреждение влияет только на нервную оболочку (миелиновую оболочку); в этом случае выздоровление от паралича Белла происходит довольно быстро.
Вирусные инфекции, связанные с началом паралича Белла:
- вирус простого герпеса (ответственный за различные заболевания, такие как герпес)
- вирус опоясывающего герпеса (вирусный агент, вызывающий опоясывающий лишай и ветряную оспу) (возбудитель инфекционного мононуклеоза)
Другими сопутствующими вирусами являются те, которые вызывают такие заболевания, как:
Другие патологические состояния включают:
- болезнь Лайма (боррелиоз); (высокое кровяное давление); ; ;
- опухоль головного мозга;
- опухоль околоушной железы.
Травматические события, затрагивающие лицо или череп, также могут быть связаны с началом паралича Белла.
Паралич Белла не является состоянием, связанным с инсультом или транзиторной ишемической атакой (ТИА).
Затронутые группы населения
Паралич Белла является довольно распространенным заболеванием, поражающим мужчин и женщин в равных количествах. По разным оценкам, 25-35 из 100 000 человек страдают параличом Белла. Ежегодно болезнь диагностируется приблизительно у 40 000 человек.
У пожилых людей чаще развивается паралич Белла, чем у детей, но расстройство может поражать людей любого возраста. Однако беременные женщины или люди с сахарным диабетом или заболеваниями верхних дыхательных путей поражаются чаще, чем население в целом.
Диагностика
Диагностика основана на физикальном осмотре, в частности, при наблюдении характерного искажения лица и неспособности двигать мышцами, находящимися на пораженной стороне; однако, лабораторного теста, который мог бы однозначно подтвердить расстройство нет. Следовательно, должны быть исключены другие возможные причины лицевого паралича.
Как правило, требуюется проведение различных клинических исследований, как лабораторных (анализы крови), так и инструментальных тестов (например, магнитно-резонансная томография (МРТ) и компьютерная томография (КТ)) для проверки наличия переломов или опухолевых образований, которые могли повредить VII черепной нерв.
Обследование, оказывающее значительную помощь, — электромиография (ЭМГ), благодаря этому исследованию можно проверить наличие нервных поражений и, в случае положительного результата, определить степень повреждения лицевого нерва.
Схожие по симптомам расстройства
Симптомы следующих расстройств могут быть похожи на симптомы паралича Белла. Сравнения могут быть полезны для дифференциальной диагностики:
Лечение
Паралич Белла лечиться у каждого больного по-разному:
- Некоторые случаи легкие и не требуют лечения, поскольку симптомы имеют тенденцию спонтанно регрессировать в течение двух недель.
- В других случаях применяются лекарства и/или другие терапевтические меры; когда можно отследить точную причину паралича (например, инфекции), очевидно, что будет полезно конкретное лечение.
Недавние исследования показали, что препараты кортизона могут уменьшать воспаление и отек, и поэтому они эффективны и полезны при лечении паралича Белла. Другие лекарства, такие как ацикловир, используемые для борьбы с герпетической инфекцией, могут в определенных случаях сокращать течение заболевания. Обезболивающие, такие как аспирин, ацетаминофен или ибупрофен, могут облегчить боль.
Другим фундаментальным фактором в лечении является защита глаз: Расстройство может нарушить естественную способность глаза к увлажнению, в результате чего драгоценный орган подвергается воздействию сухости и последующего раздражения. Поэтому важно держать глаз смазанным (например, искусственными слезами) и защищать его от пыли и травм, особенно ночью.
Другие методы лечения, такие как физиотерапия, массаж лица или иглоукалывание, могут улучшить функции лицевого нерва и разрешить боли.
Прогноз
Прогноз для больных с параличом Белла, как правило, хороший. Степень повреждения нерва определяет степень восстановления. Улучшение происходит постепенно, а время восстановления меняется. С лечением или без него большинство пациентов начинают поправляться через 2 недели после появления первых симптомов, а большинство полностью восстанавливаются, возвращаясь к нормальной работе в течение 3-6 месяцев. У некоторых, однако, симптомы могут длиться дольше.
В некоторых случаях симптомы могут никогда полностью не исчезнуть.
В редких случаях расстройство повторяется либо на той же, либо на противоположной стороне лица.

Неврологические поражения, вызванные реактивацией varicella zoster virus без высыпаний — 3 Ноября 2014 — Кафедра инфекционных болезней БГМУ
Существование ганглионита без высыпаний поддерживается корешковой болью, предваряющей герпес, так называемой прегерпетической невралгией. Нами были изучены 6 пациентов, у которых боль началась за 7-100 дней и локализовалась как в области дерматомов, на которых позже проявилась сыпь, так и на тех, где сыпи не было (Гилден и соавторы 1991). У двоих пациентов в конце концов развилась распространенная зостерная инфекция с такими неврологическими осложнениями, как зостер-паралич и фатальный зостер-энцефалит; оба принимали пролонгированные стероидные препараты в низких дозах. Третий случай прегерпетической невралгии развился у пациента с предшествующей карциномой с метастазами (в анамнезе), а четвертый – у пациента с ранним эпизодом плечевого неврита. В двух случаях основного заболевания не было. Дальнейшее документирование случаев прегерпетической невралгии определит, является ли очевидная связь с терапией стероидами и развитием серьезных осложнений статистически значимой.
Менингит характеризуется головной болью, лихорадкой и ригидностью мышц шеи. Дополнительное ухудшение высших когнитивных функций, нарушение сознания или его заторможенность указывают на лежащую в основе вовлеченность паренхимы головного мозга (энцефалит). VZV-ассоциированная вовлеченность ЦНС без высыпаний была подтверждена интратекальным синтезом антител к VZV у двоих пациентов с асептическим менингитом (Мартинез-Мартин и соавторы 1985), а затем еще у 4-х пациентов с асептическим менингитом (Эчеваррия и соавторы 1987), и у одного пациента с острым менингоэнцефалитом (Вардаль и соавторы 1987). Поэл и соавторы (1995) доложили о пациенте с менингоэнцефалитом без сыпи, чья ЦСЖ содержала ДНК VZV, а Манкарди и соавторы (1987) описали пациента с энцефаломиелитом без сыпи, у которого в ЦСЖ были обнаружены антитела к VZV. Большинство недавних случаев VZV-ассоциированного менингита с гипогликорахией и без сыпи развивались у иммунокомпетентных женщин (Хабиб и соавторы 2009).
Строгое определение синдрома Рамсея Ханта (CРХ) – это периферический паралич лицевого нерва, сопровождающийся эритематозной везикулярной сыпью на ушной раковине (ушной зостер) или в области рта. СРХ вызывается VZV. У некоторых пациентов развивается периферический паралич лицевого нерва без сыпи в области уха или рта, ассоциированный с четырехкратным возрастанием антител к VZV или наличием ДНК VZV в коже ушной раковины, мононуклеарах крови, жидкости среднего уха или слюне (Хато и соавторы 2000). В исследовании 32 пациентов с изолированным периферическим параличом лицевого нерва, Мураками и соавторы (1998) определили СРХ и zoster sine herpete у 6 из них (19%), основываясь на 4-х кратном увеличении титра антител к VZV в крови; у 4-х из этих 6 пациентов была обнаружена ДНК VZV методом ПЦР при изучении соскобов кожи коленчатого узла. В дальнейшем Морган и Натвани (1992) обнаружили, что 9,3% пациентов с параличом Белла продемонстрировали сероконверсию к VZV, а Терада и соавторы (1998) обнаружили, что кровяные мононуклеары 4-17 пациентов с параличом Белла были положительны на ДНК VZV, определяемой методом ПЦР. Таким образом, у небольшой доли пациентов с параличом Белла (идиопатический периферический паралич лицевого нерва) диагностируется zoster sine herpete.
6 Полиневриты черепно-мозговых нервов
Транзиторные ишемические атаки и очговый неврологический дефицит не являются редкостью после реактивации VZV. Первичный летальный случай прогрессирующей васкулопатии длительностью 314 дней у иммунокомпетентного 73-летнего пациента (Case Records of the Massachusetts General Hospital; Case 5-1995) был подтвержден вирусологически как вызванный VZV (Гилден и соавторы 1996). Ноэм и соавторами в 1998 г. было доложено о другом случае VZV-ассоциированной васкулопатии без сыпи с ее вирусологическим подтверждением. Kleinschmidt-DeMasters et al. (1998) описали ВИЧ-положительного пациента с фатальным энцефаломиелитом и некротизирующим васкулитом без сыпи, патологоанатомически подтвержденным как вызванный VZV. В прошлые два десятилетия было описано множество случаев VZV-васкулопатии без сыпи. На самом деле самое большое исследование вирусологически подтвержденных случаев VZV-васкулопатии выявило, что более чем у трети пациентов сыпь не развивалась. Даже в случае вирусологически подтвержденного инфаркта спинного мозга, вызванного VZV, сыпи не развивалась в течение 3-х дней после начала миелопатии (Орм и соавторы 2007).
Острая VZV-миелопатия обычно характеризуется параличом нижних конечностей и недержанием мочи и кала, что происходит при отсутствие сыпи. Геллером и соавторами в 1990 впервые был описан 31-летний иммунокомпетентный мужчина, у которого развился поперечный миелит с частичным восстановлением. Заболевание было признано как вызванное VZV, основываясь на появление в ЦСЖ антител. В дальнейшем мы столкнулись с 2-мя случаями с VZV-миелопатией при отсутствии сыпи (Гилден и соавторы 1994). У первого пациета спустя 5 месяцев после миелопатии развился зостер, когда в ЦСЖ были обнаружены VZV-антитела методом ПЦР. У второго, не менее примечательного пациента, миелопатия развилась на фоне острой зостерной инфекции. Миелопатия разрешилась, но спустя 6 месяцев рецидивировала. Спустя 5 месяцев после рецидива миелопатии в ЦСЖ пациента были обнаружены не только ДНК VZV, но и антитела к VZV. В другом случае рецидива миелопатии в ЦСЖ были обнаружены антитела IgG к VZV с уменьшенным количеством антител IgG в крови во время рецидива и при отсутствии сыпи (Гилден и соавторы 2009). В целом, спектр VZV-миелопатий является широким, варьирующим от острых до хронических и редко рецидивирующих.
В литературе описывают множественные офтальмологические нарушения воспалительного характера, вызванные VZV при отсутствии сыпи. VZV является основной причиной PORN. Было описано множество случаев PORN, вызванных VZV при отсутствии сыпи (Friedman et al. 1993; Galindez et al. 1996). Случай тяжелой персистирующей глазной боли был определен как вызванный VZV, основываясь на выявлении ДНК VZV в назальных и конъюнктивальных мазках (Goon et al. 2000). Другие случаи, включающие паралич третьей пары черепно-мозговых нервов (Hon et al. 2005),), ретинальный перифлебит (Noda et al. 2001), увеит (Akpel and Gottsch 2000; Hon et al. 2005), иридоциклит (Yamamoto et al. 1995) и дискоидный кератит (Silverstein et al. 1997), все проявляющиеся без сыпи, были подтверждены как вызванные VZV.
11 Примечательные случаи VZV инфекции без высыпаний
Два примечательных случая VZV инфекции заслуживают внимания. Первый и самый яркий пример VZV инфекции нервной системы – случай у 77-летнего пациента с Т-клеточной лимфомой и без зостерной сыпи в анамнезе, у которого развился мененгорадикулит корешков черепно-мозговых нервов и конского хвоста, он умер спустя 3 недели после начала неврологического заболевания; патологоанатомически и вирусологически было подтверждено, что заболевание было вызвано VZV (Дуэленд и соавторы, 1992). Аутопсия выявила геморрагические воспалительные повреждения с включениями Коудри А в мозговых оболочках и нервных корешках, распространяющиеся от корешков черепно-мозговых нервов до конского хвоста. Точно такие же повреждения присутствовали и в веществе головного мозга, хотя и с меньшей протяженностью. Антиген VZV и его ДНК, но не вирус простого герпеса, цитомегаловирус или его ДНК были найдены в поврежденных тканях на всем протяжении нейрональной оси. Таким образом, VZV должен быть включен в дифференциальную диагностику при остром энефаломиелите-радикулопатии, особенно при доступности антивирусной терапии.
Второй случай — иммунокомпетентная 45-летняя женщина с 13-месячным онемением правой половины лица и болью в области иннервации верхнечелюстной ветви правого тройничного нерва, которая носила характер «вспышек молнии». Вначале онемение присутствовало на области между носом и скуловой костью, и легкое прикосновение к правой лобной области вызывало боль (аллодинию) в области всего лица. Неврологическое обследование выявило потерю поверхностной чувствительности в области иннервации верхнечелюстной ветви правого тройничного нерва. Моторная функция нерва и роговичный рефлекс были в норме. В ЦСЖ плейоцитоза не было. Исследование мозга с помощью КТ и МРТ показало норму. Пациентке был назначен невронтин, 900 мг трижды в день, но ее боль усиливалась. Спустя год, и КТ и МРТ показали гомогенную растущую массу на основании мозга справа, в области узла тройничного нерва размерами 0,9*0,9*2 см. В анамнезе пациентки не было упомянуто о зостерной инфекции с сыпью. Опухоль была удалена хирургическим путем. Патологоанатомическое и вирусологическое исследование массы узла тройничного нерва подтвердили VZV-ассоциированный хронический ганглиолит в стадии обострения (Хевнер и соавторы, 2003).
12 Системные заболевания, вызванные реактивацией VZV без сыпи
13 Субклиническая реактивация VZV
В то время как опоясывающий лишай можно диагностировать визуально, все неврологические осложнения, вызванные реактивацией VZV и протекающие без сыпи, требуют вирусологического подтверждения. Доказательство активной VZV инфекции поддерживается положительными результатами любых из следующих тестов: присутствие IgM к VZV антител в сыворотке или ЦСЖ, или IgG антител в ЦСЖ, или обнаружения ДНК VZV в мононуклеарах крови или ЦСЖ. Так как сыворотка почти всех взрослых людей содержит IgG антитела к VZV, серологические исследования на IgG антитела к VZV, без проведения других вирусологических исследований, не имеют ценности. По нашему опыту, самыми диагностически значимыми исследованиями являются те, которые обнаруживают ДНК или IgG антитела к VZV в ЦСЖ. Намного реже IgМ антитела к VZV обнаруживаются в сыворотке крови или ЦСЖ, и еще более редко обнаружение ДНК VZV в мононуклеарах крови в остром периоде заболевания. Некоторые, но не все клинические лаборатории больниц, или проводят исследование на IgG антитела к VZV, или посылают образцы в другие лаборатории. Так как ДНК VZV была найдена в слюне каждого пациента с зостером в исследовании Мехты и соавторов (2008), возможно, что слюна является ценным источником обнаружения VZV у пациентов с неврологическими заболеваниями и при отсутствии сыпи. До сих пор определенное вирусологическое подтверждение требовало исследования крови и ЦСЖ на ДНК VZV и антител к VZV класса M или G. Трудной задачей для врача продолжает оставаться установление диагноза вовремя, когда терапия эффективна.
Читайте также:
