Проксимальная желудочная ваготомия с пилоропластикой. Кровоточащие язвы двенадцатиперстной кишки.
Добавил пользователь Евгений Кузнецов Обновлено: 27.01.2026
А. И. Чернооков*, Б. А. Наумов, Е. С. Сильчук, В. С. Алексеев, Ф. А. Ересько
Кафедра госпитальной хирургии № 2 (зав. – проф. А. И. Чернооков) Московской медицинской академии им. И. М. Сеченова
Для корреспонденции:
* Чернооков Александр Иванович, доктор мед. наук, зав. кафедрой.
119991, Москва, ул. Трубецкая, д. 8, стр. 2.
ТАКТИКА ХИРУРГИЧЕСКОГО ЛЕЧЕНИЯ БОЛЬНЫХ С КРОВОТОЧАЩИМИ ЯЗВАМИ ЖЕЛУДКА III ТИПА ПРИ СОЧЕТАННЫХ ОСЛОЖНЕНИЯХ
Обобщен многолетний опыт хирургического лечения больных с кровоточащими язвами желудка III типа при сочетанных осложнениях. Всего с 1989 по 2009 г. из находившихся на лечении 4651 больного с язвенной болезнью сочетанные осложнения кровоточащих язв желудка III типа выявлены у 140 (3%) больных. Локализацию язв в пилорическом канале наблюдали у 123 (87,9%) и в препилорическом отделе – у 17 (12,1%). Мужчин было 91 (65%), женщин – 49 (35%), соотношение 1,8:1. Средний возраст больных составлял 54,49 ± 7,3 года. Длительность язвенного анамнеза 6,4 ± 0,73 года. Источником кровотечения у 108 (77,1%) больных явилась язва, располагающаяся на задней стенке препилорического отдела желудка и пилорического канала, у 29 (20,7%) – на передней стенке. Кровотечение одновременно из язв передней и задней стенок наблюдали у 3 (2,1%) больных.
Средний размер язв составлял 1,8 ± 0,08 см. При эндоскопическом исследовании у 52 (37,1%) больных при поступлении в клинику выявлено активное кровотечение.
Характер оперативных вмешательств при сочетанных осложнениях кровоточащих язв желудка III типа: паллиативные хирургические вмешательства (иссечение язвы и пилоропластика) – 28 (20%), резекция желудка – 26 (18,57%), стволовая ваготомия с иссечением язвы и пилоропластикой – 23 (16,43%), проксимальная желудочная ваготомия с иссечением язвы и пилоропластикой – 4 (2,86%), задняя стволовая ваготомия в сочетании с передней серомиотомией тела и кардиофундального отдела желудка с иссечением язвы и пилоропластикой – 59 (42,14%).
Продольные пилоропластики (типа Judd–Horsley, Heineke–Miculicz, Finney) выполнены у 18 (20,93%), поперечные пилоропластики (типа Aust, типа Holle, Judd–Rankin) – у 68 (79,07%).
Общая летальность после хирургических вмешательств составила 22,86%. Радикальной операцией выбора у больных с сочетанными осложнениями кровоточащих язв желудка III типа является задняя стволовая ваготомия в сочетании с передней серомиотомией тела и кардиофундального отдела желудка с иссечением язвы и поперечной пилоропластикой.
Ключевые слова: кровоточащие язвы желудка, сочетанные осложнения, хирургическое лечение.
1. Аруин, Л. И. Морфологическая диагностика болезней желудка и кишечника / Л. И. Аруин, Л. Л. Капуллер, B. A. Исаков. – М.: Триада X, 1998. – 483 с.
2. Асташов, В. Л. Хирургическое лечение гастродуоденальных язв, осложненных кровотечением и перфорацией, у лиц пожилого и старческого возраста: автореф. дис. … канд. мед. наук / В. Л. Асташов. – М., 1996. – 25 с.
3. Гончаров, Н. Н. Алгоритм прогнозирования осложнений язвенной болезни желудка и двенадцатиперстной кишки / Н. Н Гончаров // Сингральная хир. – 2002. – № 1. – С. 10–12.
4. Гостищев, В. К. Гастродуоденальные кровотечения язвенной этиологии: руководство для врачей / В. К. Гостищев, М. А. Евсеев. – М.: ГЭОТАР-Медиа, 2008. – 377 с.
5. Исаков, В. А. Хеликобактериоз / В. А. Исаков, И. В. Домарадский. – М.: Медпрактика, 2003. – 109 с.
6. Котаев, А. Ю. Тактика хирургического лечения больных с пептическими язвами желудка и двенадцатиперстной кишки, осложненными кровотечением: дис. … д-ра мед. наук / А. Ю. Котаев. – М., 1999. – 290 с.
7. Крылов, Н. Н. Качество жизни больных язвенной болезнью двенадцатиперстной кишки после хирургического лечения: дис. … д-ра мед. наук / Н. Н. Крылов. – М., 1997. – 269 с.
8. Курыгин, А. А. Ваготомия в хирургической гастроэнетерологии: легенды и действительность / А. А. Курыгин // Вестник хир.
им. И. И. Грекова. – 2006. – Т. 165, № 4. – С. 83–86.
9. Липницкий, Е. М. Эффективность комбинированного эндоскопического гемостаза у больных язвенной болезнью, осложненной кровотечением / Е. М. Липницкий, А. В. Алекберзаде, Г. Р. Рыжов // Вестник Рос. акад. мед. наук. – 2009. – № 6. – С. 28–32.
10. Петров, В. И. Клинико-анатомическое обоснование вариантов проксимальной селективной ваготомии в лечении язвенной болезни двенадцатиперстной кишки и желудка / В. И. Петров, П. А. Романов, В. Н. Горбунов и др. // Хирургия. – 1990. – № 12. – С. 18–23.
11. Постолов, П. М. Целесообразна ли селективная проксимальная ваготомия в лечении кровоточащих язв двенадцатиперстной кишки? / П. М. Постолов, А. А. Полянцев, В. Б. Писарев, Д. А. Кувшинов // Хирургия. – 1991. – № 3. – С. 19–26.
12. Соловьев, Г. М. Концентрат фибриногена как аналог фибринового клея / Г. М. Соловьев, Т. В. Хоробрых, А. Н. Антонов, Г. К. Орлова // Новое в трансфузиологии. – 1994. – № 7–8. – С. 82–84.
13. Cutela, P. Circadian acidity pattern in prepiloric ulcers: a comparison with normal subjects and duodenal ulcer patients / P. Cutela, M. R. Mele, G. Celle // Scand. J. Gastroenterol. – 1993. – Vol. 28. – P. 772–776.
14. De Miguel, J. Pylorectomy and prepyloric antrectomy for gastric ulcer / J. De Miguel // Br. J. Surg. – 1979. – Vol. 66. – P. 48–50.
15. Enders, K. W . Eradication of Helicobacter pylori prevents recurrence of ulcer after simple closure of duodenal ulcer perforation, randomized controlled trial / K. W. Enders, Y. H. Lam, J. Y. Joseph et al. // An. Surg. – 2000. – Vol. 231, № 2. – Р. 1–10.
16. Forrest, J. A. H . Endoscopy in gastrointestinal bleeding / J. A. H. Forrest, N. D. С. Finlayson, D. J. С. Sherman // Lancet. – 1974. – Vol. 2. – P. 394–397.
17. Heberer, G. Recurrence after proximal gastric vagotomy for gastric, pyloric, and prepyloric ulcer / G. Heberer, R. K. Teichmann // World J. Surg. – 1987. – Vol. 11. – P. 283–288.
18. Herrington, J. L. Gastric ulcer / J. L. Herrington, J. L. Sawyers // Curr. Probl. Surg. – 1987. – Vol. 24, № 12. – P. 759–865.
19. Holinshead, J. W. Parietal cell vagotomy: experience with 114 patients with prepyloric or duodenal ulcer / J. W. Holinshead, R. C. Smith, D. J. Gillett // World J. Surg. – 1982. – Vol. 6. – P. 596–602.
20. Johnson, H. D. Gastric ulcers, blood groups and acid secretion / H. D. Johnson, A. H. G. Love, N. S. Roders, A. P. Wyatt // Gut. – 1964. – Vol. 5. – P. 402–411.
21. Johnston, D. A new look at selective vagotomies / D. Johnston, R. L. Blackett // Am. J. Surg. – 1988. – Vol. 156. – P. 416–427.
22. Lausević, D. Surgical perspectives in treatment of bleeding peptic ulcers / D. Lausević, P. M. Pesko, S. N. Krstic et al. //Acta Chir. Iugosl. – 2007. – Vol. 54, № 1. – Р. 157–164.
23. Malfertheiner, P. Current concepts in the management of Helicobacter pylori infection / P. Malfertheiner, F. Megraud, C. O. Morain // The Maastricht III Concensus Report 2005. – Submitted, 2006. – P. 28.
24. Muller, C. Die proximal selective vagotomie in der behandlung der gastroduodenalen ulkuskrankheit / C. Muller, S. Martinoli. – Berlin, Heidelberg, New York: Springer Verlag, 1985.
25. Muller, C. Pyloric and prepyloric ulcers / C. Muller, D. LiebermannMefferrt, M. Allgower // World J. Surg. – 1987. – Vol. 11. – P. 339–346.
26. Peter, S. Modern endoscopic therapy of peptic ulcer bleeding / S. Peter, C. M. Wilcox // Dig Dis. – 2008. – Vol. 26, № 4. – P. 291–299 (Epub. 2009, Jan 30).
27. Skandalakis, L. J. The history and surgical anatomy of the vagus nerves / L. J. Skandalakis, S. W. Gray // Surg. Gynecol. Obstet. – 1986. – Vol. 162. – P. 75–85.
28. Strom, M. Duodenal, prepyloric and combined duodenal prepyloric ulcer disease: three distinct entities of juxtapyloric ulcer disease? / M. Strom, G. Bodemar, R. Goffhard, A. Walan // Scand. J. Gastroenterol. – 1986. – Vol. 21. – P. 1105–1110.
29. Taghavi, S. A. Adrenaline injection plus argon plasma coagulation versus adrenaline injection plus hemoclips for treating high-risk bleeding peptic ulcers: a prospective, randomized trial / S. A. Taghavi, S. M. Soleimani, S. M. Hosseini-Asl et al. // Can. J. Gastroenterol. – 2009. – Vol. 23, № 10. – Р. 699–704.
30. Tsai, J. J. Oral or intravenous proton pump inhibitor in patients with peptic ulcer bleeding after successful endoscopic epinephrine injection / J. J. Tsai, Y. C. Hsu, C. L. Perng, H. J. Lin // Br. J. Clin. Pharmacol. – 2009. – Vol. 67, № 3. – P. 326–332.
31. Visick, A. H. A study of the failures after gasterectomy / A. H. Visick // Ann. Roy. Coll. Surg. Engl. – 1948. – Vol. 3. – P. 266–284.
Проксимальная желудочная ваготомия с пилоропластикой. Кровоточащие язвы двенадцатиперстной кишки.
Проксимальная желудочная ваготомия с пилоропластикой. Кровоточащие язвы двенадцатиперстной кишки.
Проксимальная желудочная ваготомия характеризуется пересечением ветвей блуждающего нерва, иннервирующих гело желудка, с сохранением иннервации антрального отдела и привратника, регуляции желудочной эвакуации и растирания твердой пищи. При проксимальной желудочной ваготомии нет необходимости выполнять дренирующую операцию. В настоящее время проксимальная желудочная ваготомпя выполняется реже из-за высокой частоты рецидивов язвы. Некоторые хирурги доказывают, что если наступил рецидив язвы после этой операции, в качестве повторной операции без затруднений можно выполнить гемигастрэктомию.
Проксимальная желудочная ваготомия с пилоропластикой
Эта операция, предложенная Holle, дополняет проксимальную ваготомию пилоропластикой с целью (по мнению автора) облегчения желудочной эвакуации. Этот метод не улучшает результатов, полученных при применении проксимальной желудочной ваготомии без пилоропластики, и имеет сходную частоту рецидивов.
При выборе наилучшего для данного пациента способа оперативного вмешательства необходимо учитывать такие факторы, как возраст, пол, телосложение, тучность, общее состояние, состояние сердечно-сосудистой системы, неадекватная масса тела, желудочная секреция, психическое состояние, пассаж пищи по кишечнику, наличие диареи или жидкого стула, наличие геморрагии, остеопороза, «трудной» двенадцатиперстной кишки или постбульбарной язвы. Необходимо учесть также опыт хирурга в выполнении резекций желудка и обращении с «трудной» двенадцатиперстной кишкой. Например, тучного пациента можно подвергнуть резекции 2/3 желудка. С другой стороны, эта операция нецелесообразна ухудощавых пациентов, особенно женщин, или у психически нестабильных пациентов, так как у них чаще развиваются демпинг-синдром и другие вазомоторные симптомы.
Стволовую ваготомию не следует рекомендовать пациентам с диареей или жидким стулом. Если оперирующий хирург не имеет опыта резекции желудка или обращения с «трудной» двенадцатиперстной кишкой, он может произвести проксимальную желудочную или стволовую ваготомию с пилоропластикой. Проксимальная желудочная ваготомпя не показана при дуоденальной язве с кровотечением, перфорацией или стенозом. Стволовую ваготомию можно выполнять пожилым пациентам, находящимся в тяжелом состоянии или пациентам с несколькими кровоточащими язвами до тех пор, пока возможен местный гемостаз. Пациентам с активно кровоточащей язвой, которым выполняется резекция желудка, разумно восстанавливать пассаж по кишечнику методом Billroth II, а не Billroth I, потому что первый надежнее для остановки кровотечения. Кроме того, остановку кровотечения производят посредством более надежной перевязки артерий снаружи двенадцатиперстной кишки. Более того, не всегда возможно произвести операцию Billroth I при дуоденальных язвах, пенетрирующих в поджелудочную железу, постбульбарных язвах или выраженных фиброзных деформациях двенадцатиперстной кишки.

Кровоточащие язвы двенадцатиперстной кишки
Пациентов с массивным кровотечением из язвы двенадцатиперстной кишки, потерявших более 2 литров крови, необходимо оперировать. Операция показана также пациентам без массивной потери крови, но с рецидивом кровотечения или с сердечно-сосудистой недостаточностью, особенно пожилым пациентам или при отсутствии достаточного количества крови.
Самой надежной операцией для лечения язв двенадцатиперстной кишки, осложненных кровотечением, является резекция 2/3 желудка или гемигастрэктомия со стволовой ваготомией.
У пожилых пациентов в тяжелом состоянии или при отсутствии у хирурга опыта резекции желудка и операций на «трудной» двенадцатиперстной кишке можно прибегнуть к остановке кровотечения посредством прошивания кровоточащей зоны. Если кровотечение происходит из одной из артерий гастродуоденального комплекса, то, как показали Berne и Rosoff, следует накладывать три шва. Один шов должен быть наложен над язвой для окклюзии желудочно-двенадцатиперстной артерии. Другой шов следует наложить ниже язвы, чтобы перекрыть желудочно-двенадцатиперстную артерию и предотвратить ток крови из правой желудочно-сальниковой и поджелудочно-двенадцатиперстной артерий. Дополнительно левее язвы должен быть размещен другой шов, чтобы перекрыть поперечную поджелудочную артерию. Этот метод будет описан далее. Кровотечения не из гастродуоденального комплекса бывают реже, они обычно не такие массивные, и гемостаз осуществить легче. Местный гемостаз кровоточащей язвы не так надежен, как гемостаз при резекции желудка и восстановлении непрерывности желудочно-кишечного тракта по методу Billroth II. При местном гемостазе отмечается склонность кчастым рецидивам.
При соблюдении всех требований метода Berne и Rosoff вероятность рецидива кровотечения уменьшается. Осуществив местный гемостаз, операцию обычно завершают стволовой ваготомией с пилоропластикой, используя произведенный для гемостаза разрез двенадцатиперстной кишки.
Информация на сайте подлежит консультации лечащим врачом и не заменяет очной консультации с ним.
См. подробнее в пользовательском соглашении.
Проксимальная желудочная ваготомия с пилоропластикой. Кровоточащие язвы двенадцатиперстной кишки.
1 ГБОУ ВПО «Кубанский государственный медицинский университет» Министерства здравоохранения и социального развития Российской Федерации, Краснодар
Наблюдали 196 больных с кровоточащими язвами желудка и дуоденум. Экстренные операции на высоте кровотечения выполнены у 48 (24,5%) пациентов, а еще у 6 (3%) по причине сочетания кровотечения с перфорацией. У 93 (47,7%) же пациентов ее причиной послужил рецидив кровотечения, который возник через 5–18 часов и 1–2 суток после первичного гемостаза. Отсроченные операции осуществлены у 43 (21,9%) пациентов с длительным язвенным анамнезом. У 6 (3%) пациентов с признаками малигнизации язвы выполнены ранние плановые операции. Мостовидная дуоденопластика произведена у 106 (54,1%) пациентов, сегментарная – у 43 (22%), гастропластика – у 35 (17,8%), резекция желудка – у 12 (6,1%). Послеоперационная летальность составила 14,7%.
1. Васильев Ю.В. Язвенная болезнь желудка и двенадцатиперстной кишки, осложненная кровотечением, и Helicobacter pylori // CONSILIUM medicum. - 2002. - № 3. - С. 6-11.
3. Киров М.Ю. Современные аспекты мониторинга гемодинамики в отделении анестезиологии и интенсивной терапии // Интенсивная тер. - 2005. - № 3. - С. 155-159.
4. Кубышкин В.А., Шишин К.В. Эрозивно-язвенное поражение верхних отделов желудочно-кишечного тракта в раннем послеоперационном периоде // CONSILIUM medicum. - 2004. - № 1. - С. 29-31.
5. Кузнецов Н.А. Современные технологии лечения острой кровопотери // CONSILIUM medicum. - 2003. - № 6. - С. 347-357.
6. Маев И.В., Самсонов А.А. Язвенная болезнь двенадцатиперстной кишки: различные подходы к современной консервативной терапии // CONSILIUM medicum. - 2004. - № 1. - С. 6-11.
8. Bone RC Immunologic dissonance: a continuing evolution in our understanding of the systemic inflammatory response syndrome (SIRS) and the multiple organ dysfunction syndromes (MODS) // ANN intern Med. - 1996. - № 8. - P. 680-687.
9. Wang P., Chaudri I.H. Crystalloid resuscitation restores but does not maintain cardiac output following severe hemorrhage // J. Surg. Res. - 1991. - № 50. - P. 163-169.
10. Weil M.H., Henning R.J. New concepts in the diagnosis and fluid treatment of circulatory shock // Anesth. Analg. - 1979. - № 58. - P. 124-132.
Введение. Язвы гастродуоденальной зоны (ЯГДЗ) осложняются острым кровотечением в 5-10% наблюдений. У мужчин, особенно в возрасте старше 40 лет, это осложнение встречается в 5-6 раз чаще, чем у женщин. У пожилых же пациентов вероятность кровотечения достигает уже 70-90%. У 12-33% больных в среднем через 164 дня (от 1 и до 1024 суток) наблюдаются рецидивы кровотечений [1].
К причинам развитие данного осложнения относят: 1) патоморфологические особенностями язвенного дефекта слизистой оболочки (длительно не рубцующаяся язва с зияющими сосудами и др.); 2) погрешность в хирургической коррекции кислотно-пептической агрессии (отказ от ваготомии, прошивание в язве кровоточащего сосуда и др.); 3) неадекватность медикаментозной терапии; 4) тяжесть нарушений свертывающей системы крови и развитие других патологических состояний на фоне геморрагического шока (острая сердечная, почечная и печеночная недостаточность, респираторный дистресс-синдром, ДВС-синдром, синдром массивного кровезамещения и др.) [1; 4; 6].
При кровоточащих язвах гастродуоденальной зоны (КЯГДЗ) воздействовать на систему гемостаза предлагают лишь тогда, когда происходит потеря факторов свертывания крови, и при нестабильном локальном гемостазе с высокой угрозой рецидива кровотечения. В таких случаях показана трансфузия свежезамороженной плазмы, и она должна продолжаться до тех пор, пока глобальные коагуляционные тесты не нормализуются [5]. Однако переливание ее больным, находящимся в критических состояниях, сопровождается у 6,8% из них рецидивом кровотечения, а еще у 18% наступает и острое повреждение легких. Если же плазма не переливается, то указанные осложнения соответственно возникают только у 2,8 и 4% больных [8; 9].
Цельную кровь и эритроцитарную массу сейчас считают очень опасными. Так, например, заместительные трансфузии эритромассы сопровождаются фатальными реакциями 1 : 1 000, трансфузионными поражениями легких и почек - 1 : 5 000, бактериальной контаминацией (в том числе фатальным сепсисом) - 1 : 10 000, передачей вирусов гепатита В - 1 : 30 000, гепатита С и вируса иммунодефицита человека - 1 : 1 000 000, при этом многие потенциально опасные вирусные инфекции у доноров вообще не тестируются [8; 10]. Повторные переливания крови увеличивают опасность развития у пациентов гнойно-некротических осложнений [1; 6].
Вместо крови и плазмы ныне предлагают использовать гидроксиэтилированный крахмал («Инфукол ГЭК» 6% и 10%) и перфторан. Переливать же альбумин пациентам с повышенной проницаемостью капилляров не рекомендуют, так как он проникает в интерстиций, что сопровождается развитием отека органов и тканей. Назначение тромбоцитарной массы показано только при падении уровня тромбоцитов ниже 50 000. Медикаментозная терапия оказывается эффективной у 80-85% больных с КЯГДЗ, а у 15-20% - требуется хирургическое лечение [2; 3; 5].
Рациональная инфузионно-трансфузионная терапия предусматривает проведение мероприятий, направленных как на коррекцию абсолютной и относительной гиповолемии с восстановлением нормального распределения жидкости между секторами организма, так и на снижение концентрации медиаторов септического каскада и токсических метаболитов, но это требует поддержания адекватного уровня коллоидно-осмотического давления плазмы. Неадекватная перфузия тканей на фоне гиповолемии и гипотензии усиливает метаболические нарушения. Увеличение же концентрации сывороточного лактата до 4 ммоль/л и более является прямым показанием для проведения инфузионной терапии. Чтобы восстановить тканевую перфузию, объем инфузии кристаллоидных или коллоидных растворов должен быть не менее 20 мл/кг в сутки [5]. Сбалансированной же объем инфузионной терапии определяется индивидуально - в первую очередь на основании оценки показателей АД, пульса, ЦВД и диуреза. Во избежание развития отека легких трансфузионную терапию необходимо осуществлять так, чтобы разница между коллоидно-осмотическим давлением плазмы и давлением заклинивания в легочных капиллярах (осмотический - гидростатический градиент) была не ниже 12 мм рт. ст. Для этого нужно в первую очередь рассчитать общее суточное количество жидкости. Эта величина определяется путем сложения суточных физиологических потребностей (1500 мл/кв. м) + дефицит воды на момент расчета + необычные ее потери (во время рвоты, выделения экссудата через дренажные трубки, усиленное потоотделение, гипервентиляция). На каждый один градус повышения температуры тела выше нормальной величины требуется дополнительное введение 500 мл воды. Если возникают трудности в определении потерь электролитов, то нужно нормальную суточную их потребность (калия - 1 ммоль/кг, натрия - 2 ммоль/кг, хлора - 1,5 ммоль/кг) увеличить в 2-3 раза.
Трансфузионных средств довольно много, и по этой причине каждое из них следует назначать индивидуально с учетом необходимости для коррекции гомеостаза. Данные литературы свидетельствуют о том, что эффективность кристаллоидных и коллоидных растворов примерно одинакова. Однако для достижения нужных результатов лечения требуется гораздо больший объем кристаллоидов, чем коллоидов, а это сопровождается повышением экстравазации жидкости и формированием генерализованного отека тканей, который в свою очередь ухудшает транспорт кислорода и тем самым поддерживает полиорганную дисфункцию [5; 9].
Большинство кристаллоидных растворов изотоничны плазме и по данной причине свободно проникают через эндотелий капилляров, что сопровождается снижением онкотического давления. Распределение кристаллоидов после инфузии определяется коллоидно-осмотическим давлением плазмы и интерстициального пространства. В условиях выраженной капиллярной «утечки» объем инфузии кристаллоидов в 3-4 раза превышает эквивалентный объем коллоидов, при этом их эффект весьма не продолжителен. Кроме этого, они хотя и восстанавливают сердечный выброс, но не поддерживают его и не способствуют восстановлению микроциркуляции [2; 10]. Использование у пациентов с органной дисфункцией значительных объемов 0,9%-ного раствора хлорида натрия (осмолярность его составляет 308 мосм/л, тогда как у плазмы крови всего 285-295 мосм/л) или лактата Рингера (осмолярность 273-254 мосм/л) может привести к внутриклеточному отеку внутренних органов и головного мозга с резким возрастанием внутричерепного давления. Следует помнить и о том, что у физиологического раствора рН около 7,0, что может серьезно усилить имеющийся в больных ацидоз. Раствор Рингера - Локка и Лактасол более физиологичны, чем 0,9%-ный раствор хлорида натрия. Они способствуют восстановлению кислотно-основного состояния организма и улучшают гемодинамику. К числу регуляторов кислотно-основного состояния относятся также 5-7%-ный раствор гидрокарбоната натрия, но он эффективен не более чем 4 часа от момента изготовления, и 3,66%-ный раствор трисамина.
Коллоидные инфузионные среды при коррекции волемических расстройств в меньшей степени вероятности способствуют развитию отечного синдрома и значительно улучшают микроциркуляцию. Однако они могут вызвать аллергическую реакцию, отрицательно влияют на гемостаз и повреждают нефрон. Наиболее безопасными являются среднемолекулярные крахмалы (гидроксиэтилкрахмал с молекулярной массой 130±20 кДа) и растворы модифицированного жидкого желатина. Они значительно улучшают реологические свойства крови, снижают капиллярную утечку (за счет ингибирования активации эндотелиоцитов и «запечатывающего эффекта»), снижают как выброс ксантин-оксидазы после ишемии-реперфузии, так и системную воспалительную реакцию. Например, волемический эффект гидроксиэтилкрахмала (ГЭК 130/0,4) достигает 100% и продолжается около 4 часов, при этом даже при инфузии препарата 75 мл/кг не отмечается кумуляции его в плазме. Инфузионно-трансфузионную терапию проводят на фоне обязательного постоянного вдыхания увлажненного кислорода.
Профилактика тромбоэмболических осложнений проводится путем: эластической компрессии тканей нижних конечностей эластическими чулками, возвышенного положения ног с пассивными и активными сгибаниями стоп, лечебной гимнастики и массажа, местного применения троксевазина. После устранения язвенного кровотечения оперативным путем с этой целью используют подкожное введение сниженных доз или обычного нефракционированного гепарина (НФГ), или низкомолекулярного гепарина (НМГ), а также непрямые антикоагулянты после восстановления перистальтики кишечника. Первая доза гепарина вводится через 4-6 часов после операции. Этот препарат улучшает реологические свойства крови, предотвращает коагулопатию, улучшает микроциркуляцию и тем самым способствует восстановлению моторной деятельности желудочно-кишечного тракта. Эффект усиливается, если одновременно внутривенно вводится реополиглюкин. В последнее время в международной клинической практике для профилактики тромбоэмболических осложнений предпочтение отдается НМГ - его применять удобнее, чем НФГ, а число геморрагических осложнений при нем ниже. Обычно используют малые дозы НМГ: 20 мг клексана 1 раз в сутки под кожу живота либо 0,3 мл фраксипарина 1 раз в сутки, либо 2500 МЕ фрагмина 1 раз в сутки. Лечебное действие клексана продолжается 24 часа, а фрагмина и фраксипарина - 18 часов. Однако если проводится консервативное лечение, то применение гепарина и непрямых антикоагулянтов противопоказано даже в стадии рубцевания и эпителизации язв.
При лечении КЯГДЗ общепризнанной является активно-выжидательная тактика. Операцией выбора при язвах ДПК является дуоденопластика (или сегментарная, или мостовидная), а желудка - гастропластика [7]. Без коррекции секреции соляной кислоты любая из них будет обречена на неудачу [6]. Летальность при КЯГДЗ остается в пределах 10-25%. Сравнительный анализ результатов выживаемости различных групп пациентов проводят с учетом балльной оценки индекса тяжести по APACHE - 11. В него включают 8 факторов. При третьей степени тяжести (более 30 баллов) летальность достигает 100%.
Цель работы: изучение причинных факторов рецидива КЯГДЗ.
Материалы и методы. В хирургических отделениях КГЦ БСМП с 2001 по 2007 год (включительно) находилось на лечении 2444 пациента с кровоточащими язами гастродуоденальной зоны, из которых у 1808 (78,4%) было проведено консервативное лечение (умерло 59 человек, или 3,2%), а у 557 (21,6%) - оперативное (умерло 67 человек, или 12%). Спустя сутки от начала заболевания (кровотечения) в больницу поступило 925 (37,8%)человек, из которых у 75% осуществлено консервативное лечение (из 694 пациентов умерло 25, или 3,6%), а у 25% была произведена операция (из 231 пациента умерло 24, или 10,3%).
Из 577 пациентов, подвергнутых оперативному лечению, у 231 (40%) кровотечение возникло из язвы желудка, а у 346 (60%) -из язвы двенадцатиперстной кишки. Из числа больных с язвой желудка женщин было 27,5%, а мужчин - 72,5%., а с язвой двенадцатиперстной кишки - соответственно 24 и 76%, то есть у мужчин язвы обеих локализаций наблюдались примерно одинаково и встретились в 3,5 раза чаще, чем у женщин. Возраст больных с язвой желудка был от 22 и до 92 лет, а двенадцатиперстной кишки - от 15 и до 89 лет. Однако возрастной состав больных в этих двух группах наблюдений несколько отличался друг от друга. Так, язва желудка в возрасте до 20 лет вообще не наблюдалась, а двенадцатиперстной кишки - 2,3% наблюдений. На возраст 21-30 лет соответственно пришлось 2,5 и 11,8%; 31-40 лет - 10,6 и 13,3%; 41-50 лет - 21,8 и 17,1%; 51-60 лет - 23,1 и 17,2%; 61-70 лет - 25,6 и 22,9%; 71-80 лет - 11,3 и 12,3%; старше 80 лет - 5,1 и 3,1%. Таким образом, язва двенадцатиперстной кишки наблюдалась в более молодом возрасте по сравнению с язвой желудка. Среди умерших женщин было 29,1%, а мужчин - 70,9%. Эти данные не подтверждают бытующее мнение о том, что язвенная болезнь у женщин протекает тяжелее, чем у мужчин. Летальность в возрасте до 20 лет составила 16,6%; от 21 до 30 лет - 5,7%; от 31 до 40 лет - 1,9%; от 41 до 50 лет - 8,8%; от 51 до 60 лет - 8,5%; от 61 до 70 лет - 17,8%; от 71 до 80 лет - 20%; старше 81 года - 25%. Следовательно, на прогноз заболевания влияет возраст больных. Если у лиц до 20 лет высокую летальность в основном можно объяснить наследственным фактором, то у пациентов старше 40 лет уже отчетливо просматриваются социальные факторы - это вредные привычки, характер трудовой деятельности и диеты и др. С возрастом отмечается кумуляция повреждающих факторов, что отражается на тяжести течения заболевания.
Из 557 пациентов, подвергшихся оперативному лечению, у 153 (27,4%) операции по сроку выполнения можно отнести к числу экстренных (через 2-3 часа после поступления пациентов в стационар на высоте профузного кровотечения и геморрагического шока им осуществлялось хирургическое вмешательство, а дообследование проводилось на операционном столе). У 267 (47,9%) больных они были неотложными - рецидив кровотечения у них возник или через 5-18 часов, или через 1-2 суток после первичного гемостаза, а у 122 (21,9%) отсроченными - выполнены через 2-3 суток при эндоскопических признаках явной угрозы рецидива кровотечения. Ранние плановые операции осуществлены всего у 15 (2,8%) человек (на 7-14 сутки после остановки кровотечения при явных признаках малигнизации тканей).
В таблице 1 приводятся сведения о характере произведенных операций.
Таблица 1 - Характер выполненных операций у больных с кровоточащими язвами
Техника лапароскопической селективной проксимальной ваготомии и фундопликации при язвенной болезни двенадцатиперстной кишки и эрозивном рефлюкс-эзофагите
Положение больного на столе, места введения троакаров, расположение операционной бригады и монитора должны максимально обеспечивать комфортные условия для работы хирурга, качественную визуализацию операционного поля и возможность проведения необходимых манипуляций в зоне вмешательства. Естественно, что на вышеперечисленные установки оказывает влияние состояние конкретного пациента (вес, характер заболевания, наличие послеоперационных рубцов на брюшной стенке и т. д.), привычки оператора и особенности хирургической школы.
Лапароскопические оперативные вмешательства по поводу язвенной болезни ДПК, грыжи пищеводного отверстия диафрагмы и рефлюкс-эзофагита мы обязательно проводим под интубационным наркозом с применением миорелаксантов.
В нашей клинике используется следующее положение больного на операционном столе: пациент лежит на спине, с разведенными и полусогнутыми в коленных суставах ногами.
Головной конец стола приподнимаем до 30-40º. Отведенную левую руку помещаем на подставку, другую руку закрепляем вдоль туловища. Высота операционного стола определяется ростом хирурга и должна обеспечивать его работу без физического напряжения в области плечевого пояса. Спина должна быть прямая, а плечи опущены. Следует отметить, что за счет изменения положения стола на 30 градусов после введения троакаров брюшная стенка дополнительно опускается на 15-20 см.
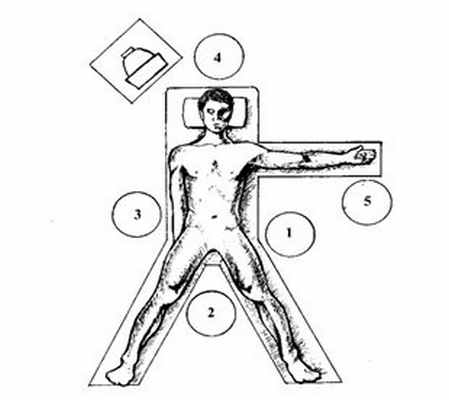
Рис. 1. Положение больного на операционном столе и расположение операционной бригады. 1 – хирург, 2 – 1-й ассистент (видео оператор), 3 – 2-й ассистент, 4 – анестезиолог, 5 – операционная сестра.
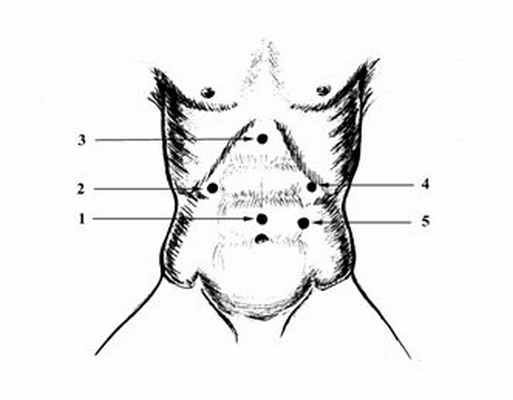
Рис. 2. Оптимальные точки для введения троакаров при выполнении лапароскопической операции при ЯБДПК и ГПОД.
Рис. 3. Положение больного на операционном столе (вид сбоку), положение Фовлера (30°).
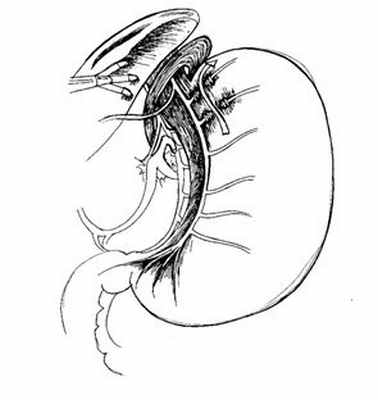
Рис 4. Начальный этап мобилизации пищеводно-желудочного перехода, пересечение первых ветвей переднего вагуса и выделение передней стенки пищевода.
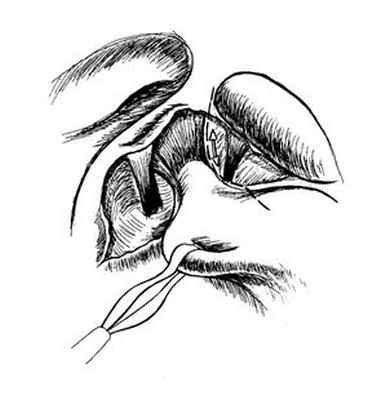
Рис. 5. Рассечение фундально-диафрагмальной связки.
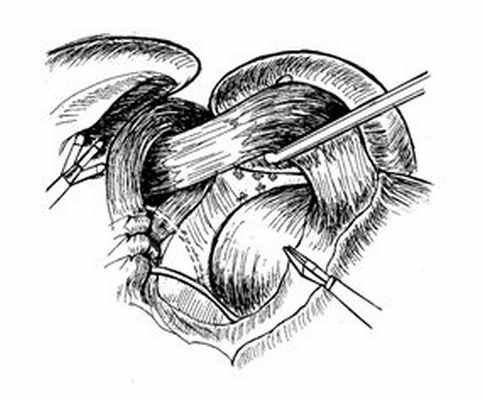
Рис. 6. Ретрактором осуществляется тракция кардиального отдела желудка влево. Этап лигирования коротких желудочных сосудов под пищеводом.
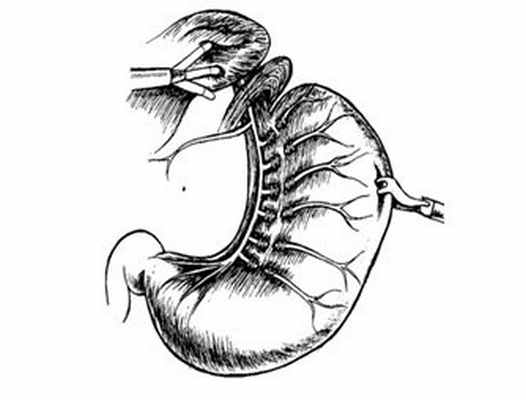
Рис. 7. Этап лапароскопической селективной проксимальной ваготомии - пересечение веточек переднего блуждающего нерва.
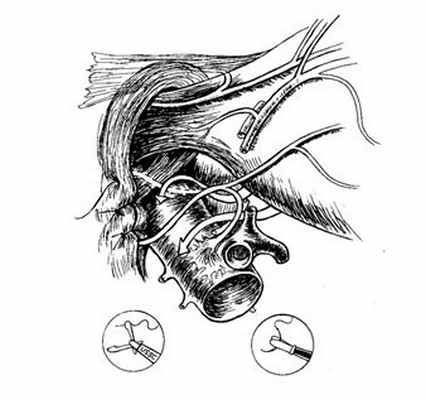
Рис. 8. Лапароскопическое сшивание ножек диафрагмы (крурорафия) и варианты расположения заднего блуждающего нерва после нее.
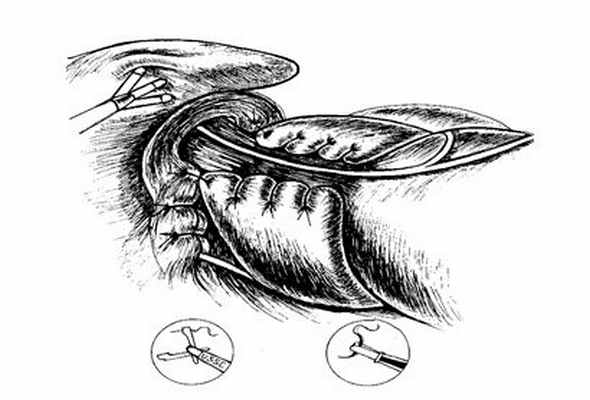
Рис. 9. Окончательный вид физиологической 2-х сторонней фундопликации по Toupet в нашей модификации.
Располагается операционная бригада следующим образом: хирург стоит у левой ноги пациента, 1-й ассистент – между ног, 2-й ассистент – справа от больного, эндоскопическая стойка с оборудованием – у его правого плеча. Анестезиолог и наркозно-дыхательная аппаратура располагаются у головы пациента, а анестезиологическая медицинская сестра с инструментальным столиком - у его левой руки. Операционная сестра и инструментальный столик находятся справа от хирурга, так как это позволяет менять хирургические инструменты без поворота по своей оси, не вовлекая левую руку оператора (Рис.1).
Для четкого разделения рабочей зоны между анестезиологической и операционной сестрами дополнительно натягиваем стерильную простыню, которую фиксируем бельевыми цапками к анестезиологической дуге и стойке для внутривенной инфузии у левой руки пациента.
Такое положение операционной бригады, по нашему мнению, является наиболее удобным, так как глаза хирурга, руки, лапароскоп, зона оперативного вмешательства и монитор находятся на одной линии, а ассистент, манипулируя оптикой, не мешает оператору.
Следует отметить, что максимальные возможности данного расположения операционной бригады проявляются при использовании 30 градусной оптики, способной помочь ассистенту визуализировать объект с любой стороны.
После интубации выполняем обработку операционного поля, границами которого являются среднеподмышечные линии с двух сторон, средняя треть грудины и лонный бугор. Места введения троакаров отграничиваем стерильным бельем и приступаем к соединению аппаратуры с инструментами.
На рисунке показаны оптимальные точки для введения троакаров при выполнении оперативного вмешательства по поводу грыжи пищеводного отверстия диафрагмы (Рис. 2): 1 – 10 мм - для лапароскопа, 2- 10 мм - дополнительный порт для введения печеночного ретрактора, 3 - 5 мм - для введения мягкого зажима (для работы хирурга левой рукой), 4 - 10 мм - основной рабочий порт для введения ножниц, диссектора, клипсаппликатора, иглодержателя, инструмента EndoStitch, инструмента LigaSure, 5 - 10 мм - дополнительный порт для введения инструмента ЭндоБебкок и фиксации желудка и введения пищеводного ретрактора.
Отметим, что места введения троакаров могут варьировать, но всегда остается необходимость отводить печень, натягивать фундальный отдел желудка, вводить оптику и выполнять основные приемы двумя руками. Для решения этих задач необходимо пять доступов.
Оперативное вмешательство начинаем с инсуфляции углекислого газа в брюшную полость через иглу Вереша, введенную в параумбиликальную область. Скорость подачи газа - 1,5 литра в минуту, давление - 12 мм. рт. ст. Критерием проникновения иглы в брюшную полость является характерный щелчок выскочившей защиты. Для точного определения положения иглы Вереша всегда выполняем водную пробу. Затем вводим первый 10 мм троакар(стальной «Karl Storz»). Для большей безопасности мы фиксируем брюшную стенку в области прокола двумя бельевыми «цапками». Направление введения троакара должно быть строго вертикальным. Очень важно, чтобы стилет у первого из них имел пирамидальную, а не коническую форму, в этом случае при фиксированной брюшной стенке ткани легко рассекаются и отсутствует не контролируемый эффект «провала» в брюшную полость. С целью контроля за «провалом» в брюшную полость следует также вдоль троакара выпрямлять указательный палец правой руки, который будет ограничивать продвижение стилета по тканям брюшной стенки.
При выполнении симультанных операций на верхнем этаже брюшной полости, связанных с извлечением органов (например – лапароскопическая холецистэктомия с фундопликацией и ваготомией), мы используем поперечный разрез по вворачивающемуся краю пупка длиной 10 мм для возможного его расширения до необходимого размера с соблюдением элементов косметики. Если оперативное вмешательство не сопровождается извлечением органов из брюшной полости, более удобным будет выполнение разреза для введения оптики на 4-5 см выше пупка по средней линии (особенно это важно у высоких пациентов с большим расстоянием от мечевидного отростка до пупка).
У пациентов, перенесших ранее лапаротомные оперативные вмешательства, как правило, органы брюшной полости оказываются припаянными к послеоперационному рубцу, что может сопровождаться их повреждением при введении иглы Вереша или первого троакара. В этой ситуации мы обычно используем оптический троакар VISIPORT компании Covidien (Швейцария), который позволяет под контролем зрения строго дозировано (по 1 мм) послойно рассекать ткани брюшной стенки. При отсутствии подобного инструмента может быть использована методика «открытой» лапароскопии по Hasson.
После введения лапароскопа в брюшную полость выполняем обзорную лапароскопию для получения дополнительной информации о состоянии органов брюшной полости и наличия спаечного процесса. Для улучшения изображения торцевой конец лапароскопа должен быть согрет до 50 градусов в стерильном физиологическом растворе или обработан салфеткой, смоченной специальным составом Anti-Fog (KARL STORZ). Далее операционный стол переводим в положение Фовлера (30°), в желудок вводим толстый зонд диаметром – 20 - 24 мм (Рис. 3).
Под контролем зрения устанавливаем остальные троакары, начиная их введение с левого подреберья по часовой стрелке. После установки второго троакара в брюшную полость помещаем печеночный ретрактор, которым отводим круглую связку печени вправо для облегчения введения третьего, 5- мм троакара. Затем поочередно вводим четвертый и пятый 10 мм троакары, обязательно учитывая ход крупных сосудов для профилактики их повреждения.
Как правило, для работы в первом и четвертом доступах мы используем стальные троакары «Karl Storz», во втором и пятом - пластиковые троакары Covidien (Швейцария). В третьем доступе очень удобен пластиковый троакар компании Covidien (Швейцария) с фиксатором.
При введении инструментов следует соблюдать ряд рекомендаций. Выполнение лапароскопической СПВ и фундопликации осуществляется главным образом через два основных манипуляционных троакара – в третьем и четвертом доступах. Операционный угол между двумя инструментами, введенными через них, при сближении в области абдоминального отдела пищевода должен быть не менее 80 – 70 градусов. Направление троакаров при их введении - строго радиальное по отношению к зоне оперативного действия. Это, с одной стороны, облегчит подведение инструментов «вслепую» к месту операции, а с другой – не будет изменять тактильное ощущение хирурга, связанное с приложением усилия по коррекции неправильного выбранного угла.
После установки троакаров через второй доступ мы вводим печеночный ретрактор и отводим левую долю печени вверх и вправо. Через пятый доступ инструментом «ЭндоБебкокк» захватываем фундальный отдел желудка. В третий доступ вводим мягкий 5 мм зажим, а через 4 - 5 мм ножницы. Использование пластиковых 5 мм мягких зажимов с фиксатором значительно облегчает работу на тонких структурах малого сальника, так как, с одной стороны, эти инструменты имеют удобные кремальеры для экстренного захвата кровоточащего сосуда, а с другой – их малый вес позволяет выпустить инструмент из рук, не боясь отрыва тканей в зоне оперативного вмешательства. В области малого сальника очень удобно использование изогнутых пластиковых ножниц компании Covidien (Швейцария), так как длина бранш соответствует размеру выделенных тканей под средне-большие клипсы или инструмент LigaSure, а их кривизна позволяет выделять сосуды без применения диссектора.
Для обеспечения легкой и безопасной работы в области пищеводно-желудочного перехода и малого сальника необходимо адекватное натяжение тканей, которое создается инструментом «Эндобебкокк» через пятый доступ.
В отличие от техники селективной проксимальной ваготомии, выполняемой открытым способом, когда скелетирование малой кривизны желудка начинается от «вороньей лапки» нерва Летарже и продолжается вверх, при лапароскопической ваготомии мобилизацию малой кривизны желудка лучше начинать с пищевода и продолжать вниз (Рис. 4).
В этом случае структуры, подлежащие лигированию и пересечению, постоянно находятся в состоянии натяжения. Пищевод мобилизуем медиально от левого блуждающего нерва с использованием LigaSure Atlas, и после вскрытия сальниковой сумки и рассечения фундально-диафрагмальной связки (рис. 5) под пищеводом ретрактором осуществляем тракцию кардиального отдела желудка влево (Рис. 6).
Этим приемом мы значительно облегчаем манипуляции в области малого сальника. Далее сверху вниз послойно выполняем диссекцию нервно-сосудистых образований между левым блуждающим нервом и желудочной стенкой, используя мягкий 5 мм зажим, ножницы и 5 мм аппарата LigaSure (Рис.7).
По мере продвижения к «вороньей лапке» для сохранения натяжения структур в зоне оперативного действия, зажим «ЭндоБебкокк» передвигаем вниз по малой кривизне. Отсутствие клипс, надежный гемостаз и одновременное рассечение тканей на этом этапе делают преимущества аппарата LigaSure очевидными.
После окончания селективной проксимальной ваготомии выполняем диссекцию тканей в области правой и левой диафрагмальных ножек, крурорафию (Рис. 8) и фундопликацию (Рис. 9).
Ушивание десерозированного участка малой кривизны желудка не целесообразно. Далее проводим смену желудочных зондов и лаваж брюшной полости стерильным физиологическим раствором. Мы крайне редко оставляем страховой дренаж, так как в этом нет необходимости. Раны брюшной стенки ушиваем послойно иглой Endo close.
Список работ опубликованных профессором Пучковым К.В. по теме хирургия желудка и двенадцатиперстной кишки
Отзывы пациентов
06.07.2020 09:25:00 Владимир и Ольга Литовченко
Тест по лечебному делу

2. Какой из перечисленных гормонов и гуморальных факторов не имеет отношения к регуляции кислотопродукции?
- 1. холецистокинин;
- 2. гастрин;
- 3. ацетилхолин;
- 4. глюкагон;
- 5. секретин.
- 1. а, б;
- 2. б, в;
- 3. все ответы правильные;
- 4. б, г;
- 5. в, г.
- 1. а, б;
- 2. б, в;
- 3. а, г;
- 4. б, д;
- 5. в, д.
- 1. соляная кислота;
- 2. пепсин;
- 3. хеликобактер пилори;
- 4. нестероидные протововоспалительные средства;
- 5. бикарбонаты.
- 1. а, б, в;
- 2. а, б, г, д;
- 3. б, в, г, д;
- 4. в, д;
- 5. б, в, г.
- 1. а, б;
- 2. в, д;
- 3. б, г;
- 4. г, д;
- 5. б, д.
8. После тщательного клинического обследования больному поставлен диагноз: синдром Золлингера-Эллиссона. Какое из утвер-ждений можно считать верным в отношении этого синдрома?
- 1. данный синдром является послеоперационным осложнением хирургических вмешательств по поводу язвенной болезни и приводит к устойчивым рвотам после приема пищи;
- 2. данный синдром известен также как синдром верхней бры¬жеечной артерии;
- 3. данный синдром состоит в нарушении проходимости дистальных отделов желудка, обусловленном язвенной деформацией;
- 4. это форма тяжелого течения язвенной болезни, вызванной гастринпродуцирующей опухолью поджелудочной железы;
- 5. встречается в психиатрической практике у больных, часто глотающих инородные тела.
9. У больного 48 лет с гигантской язвой желудка с рецидивирующим течением (язвенной болезнью страдает на протяжении 11 лет) выявлена гистаминорефрактерная ахлоргидрия. Какова лечебная тактика?
- 1. стационарное консервативное лечение в течение 8 недель и выписка больного;
- 2. стационарное лечение до заживления язвы и выписка больного;
- 3. консервативное лечение в стационаре и последующее сана¬торно-курортное лечение;
- 4. противоязвенная терапия перед плановой операцией в рам¬ках предоперационной подготовки;
- 5. экстренная операция.
- 1. б, в, д;
- 2. б, в, г;
- 3. в, г, д;
- 4. а, в, д;
- 5. а, б, в.
11. У больного 48 лет сочетанная форма язвенной болезни (выраженная рубцовоязвенная деформация луковицы двенадцатиперстной кишки с субкомпенсированным пилоробульбарным стенозом и хроническая язва угла желудка). Какая операция показана больному?
- 1. резекция желудка;
- 2. селективная проксимальная ваготомия;
- 3. стволовая ваготомия с пилоропластикой;
- 4. гастроэнтеростомия;
- 5. ваготомия с гемигастрэктомией.
- 1. а, б, в;
- 2. б, в, г;
- 3. б, г, д;
- 4. а, г, д;
- 5. в, г, д.
- 1. а, б, в;
- 2. б, в, г;
- 3. все ответы правильные;
- 4. в, г, д;
- 5. все ответы неправильные.
14. У практически здорового пациента, злоупотребляющего алкоголем, после многократной рвоты без примеси крови началось массивное кровотечение из верхних отделов ЖКТ. Указания на язвенную болезнь в анамнезе отсутствуют. Что, скорее всего, послужило причиной кровотечения?
- 1. хиатальная грыжа;
- 2. рак желудка;
- 3. язва двенадцатиперстной кишки;
- 4. синдром Меллори-Вейсса;
- 5. гастрит.
- 1. желудочная язва;
- 2. дуоденальная язва;
- 3. рак желудка;
- 4. синдром Меллори-Вейсса;
- 5. геморрагический гастрит.
16. Какой из методов наиболее достоверен в определении точной локализации источника кровотечения из верхних отделов ЖКТ?
- 1. энтерография;
- 2. компьютерная томография;
- 3. эндоскопическая эзофагогастродуоденоскопия;
- 4. артериография;
- 5. радионуклидное сканирование.
- 1. а, б;
- 2. б, в;
- 3. в, г;
- 4. г, д;
- 5. а, д.
18. У больного 44 лет, поступившего в стационар через 6 часов после начала массивного желудочно-кишечного кровотечения, проявившегося рвотой алой кровью и коллапсом, произведена ЭГДС. Установлен источник кровотечения - дуоденальная язва - и выполнена эндоскопическая коагуляция сосудов в дне язвы, после чего кровотечение остановилось. В ходе интенсивной терапии в отделении реанимации через 8 часов после ЭГДС наступил рецидив кровотечения. Что из нижеперечисленного показано данному больному?
- 1. экстренная лапаротомия;
- 2. внутривенное введение вазопрессина;
- 3. повторное эндоскопическое исследование;
- 4. введение назогастрального зонда и промывание желудка ле¬дяной водой;
- 5. наблюдение и продолжение консервативных мероприятий.
- 1. а, б, ж;
- 2. а, б, в;
- 3. б, в, г;
- 4. в, г, д;
- 5. д, е, ж.
- 1. а, б, в;
- 2. а, в, д;
- 3. в, г, д;
- 4. б, г, д;
- 5. б, в, г.
21. Молодой мужчина поступил в приемное отделение с жалобами на сильнейшие боли в животе. Страдает язвенной болезнью несколько лет. АД - 90/60 мм рт. ст., пульс - 100 ударов в 1 мин, анурия. Пальпаторно: передняя брюшная стенка резко напряжена. Диагноз, скорее всего, будет поставлен на основании:
- 1. подсчета лейкоцитов в периферической крови;
- 2. обзорной рентгенографии брюшной полости в положении стоя;
- 3. уровня СОЭ;
- 4. контрастной рентгенографии желудка;
- 5. контрастного рентгенологического исследования толстой кишки.
22. Молодой мужчина поступил в приемное отделение с жалобами на сильнейшие боли в животе. Страдает язвенной болезнью несколько лет. АД - 90/60 мм рт. ст., пульс - 100 ударов в 1 мин, анурия. Пальпаторно: передняя брюшная стенка резко напряжена. Показания к неотложной операции у этого больного менее всего будут зависеть от следующего фактора:
- 1. общего состояния больного;
- 2. срока от начала заболевания;
- 3. степени распространенности перитонита;
- 4. длительности язвенного анамнеза;
- 5. цифр артериального давления.
- 1. а, б, в, г;
- 2. все правильно;
- 3. а, г, д;
- 4. б, в, г;
- 5. б, в, г, д.
24. Что из перечисленного является наиболее предпочтительным для больного молодого возраста с перфоративной дуоденальной язвой при отсутствии предшествующего язвенного анам-неза и других осложнений, присущих язвенной болезни?
- 1. метод Вангенстина-Тейлора;
- 2. ваготомия с дренирующей желудок операцией;
- 3. резекция желудка;
- 4. лапароскопическое ушивание перфоративной язвы;
- 5. традиционное ушивание перфоративной язвы.
25. Женщина 75 лет поступила с картиной разлитого перитонита 3-суточной давности. Длительный язвенный анамнез. При обзорной рентгенографии брюшной полости выявлен «свободный газ». Данной больной показана:
- 1. эндоскопическая эзофагогастродуоденоскопия;
- 2. рентгеноскопия желудка с барием;
- 3. неотложная лапаротомия;
- 4. наблюдение;
- 5. УЗИ.
26. Мужчина 55 лет поступил в стационар с жалобами на рвоту пищей в течение недели. Длительный язвенный анамнез. В последние полтора года - частые рвоты съеденной накануне пищей. Похудание на 20 кг. Гематокрит - 55%. Какое лечение нецелесообразно?
- 1. выполнение эзофагогастродуоденоскопии с проведением зон¬да в тонкую кишку для энтерального питания;
- 2. регулярное промывание желудка;
- 3. катетеризация центральной вены;
- 4. назначение метоклопрамида для стимуляции эвакуаторной функции желудка;
- 5. назначение Н2-блокаторов внутривенно.
27. Мужчина 55 лет поступил в стационар с жалобами на рвоту пищей в течение недели. Кожные покровы и слизистые оболочки сухие. Гематокрит - 55%. В анамнезе отмечен постоян-ный болевой синдром, сменяющийся в последнее время чувством тяжести в эпигастральной области. Ранее не обследовался. При рентгеноскопии желудка выявлен значительно увеличенный желудок. Укажите патологическое состояние, чаще других встречающееся при наличии указанных симптомов:
- 1. гипертензия;
- 2. водно-электролитные нарушения;
- 3. лихорадка;
- 4. нарушение функции печени;
- 5. гипергликемия.
- 1. а, б, в;
- 2. а, б, г;
- 3. б, в, г;
- 4. а, б, д;
- 5. б, г, д.
29. У больного - декомпенсированный стеноз пилоро-бульбарной области на фоне 10-летнего язвенного анамнеза. В среднетяжелом состоянии он поступил с жалобами на многократную рвоту и отрыжку тухлым. Отмечает выраженную слабость. Истощен. Какой симптом является патогномоничным для данной категории больных?
- 1. симптом «падающей капли» и вздутия живота;
- 2. «кинжальная боль» в эпигастральной области и ригидность брюшной стенки;
- 3. симптом «шума плеска»;
- 4. отсутствие перистальтики, стул в виде «малинового желе»;
- 5. локальная болезненность при пальпации в правом подребе¬рье и высокий лейкоцитоз.
30. У больного - декомпенсированный стеноз пилоро-бульбарной области на фоне 10-летнего язвенного анамнеза. В среднетяже-лом состоянии он поступил с жалобами на многократную рвоту и отрыжку тухлым. Отмечает выраженную слабость. Истощен. Какое метаболическое нарушение является причиной состояния этого больного при поступлении?
- 1. ни одно из перечисленных ниже нарушений;
- 2. дыхательный ацидоз;
- 3. метаболический ацидоз;
- 4. дыхательный алкалоз;
- 5. метаболический алкалоз.
31. У больного — декомпенсированный стеноз пилоро-бульбарной области на фоне 10-летнего язвенного анамнеза. В среднетяжелом состоянии он поступил с жалобами на многократную рвоту и отрыжку тухлым. Отмечает выраженную слабость. Истощен. После стабилизации метаболических показателей и общего состояния больной дал согласие на оперативное лечение. При дообследовании выявлено, что больной - гипосекретор, имеются эндоскопические признаки выраженного гастрита во всех отделах желудка. Выберите метод операции:
- 1. селективная проксимальная ваготомия;
- 2. ваготомия с дренирующей желудок операцией;
- 3. резекция желудка по Бильрот II;
- 4. наложение гастростомы по Витцелю;
- 5. фундопликация по Ниссену.
32. Выберите наиболее частую причину рецидива язвы после ор-ганосохраняющей операции с ваготомией при адекватном снижении кислотопродукции после операции:
- 1. синдром Золлингера-Эллисона;
- 2. неполная ваготомия;
- 3. дуоденогастральный рефлюкс желчи;
- 4. гастрит оперированного желудка;
- 5. чрезмерное употребление алкоголя.
- 1. а, б, в;
- 2. в, г, д;
- 3. б, в, г;
- 4. а, в, г;
- 5. б, в, д.
- 1. все ответы правильные;
- 2. а, б;
- 3. б, в;
- 4. в, г;
- 5. г.
- 1. а, б;
- 2. б, в;
- 3. в, г;
- 4. а, в;
- 5. б, г.
36. На 9 сутки у больного после ваготомии с пилоропластикой по Финнею проконтролировали адекватность моторной и эвакуаторной функций желудка. В результате диагностирована задержка эвакуации желудочного содержимого. Какой рутинный метод из нижеперечисленных мог натолкнуть на предположение о данном осложнении до рентгенологического исследования?
- 1. зондовые пробы;
- 2. развернутый клинический анализ крови;
- 3. эндоскопическая гастродуоденоскопия;
- 4. ирригоскопия;
- 5. ЯМР-томография верхнего этажа брюшной полости.
- 1. а, б, в;
- 2. а, в, г;
- 3. б, в, г;
- 4. а, б, г;
- 5. все ответы правильные.
- 1. б, в, г
- 2. а, б, в
- 3. б, в, д
- 4. а, г, д
- 5. в, г, д
- 1. б, в;
- 2. а, б;
- 3. а, г;
- 4. б, г;
- 5. г, д.
- 1. наблюдение без противоязвенной терапии;
- 2. наблюдение с проведением противоязвенной и антихелико-бактерной терапии;
- 3. ваготомия с дренирующей желудок операцией через 2-3 месяца;
- 4. резекция желудка через 2-3 месяца;
- 5. гастрэктомия после обследования.
- 1. а, б, в;
- 2. б, в, г;
- 3. в, г, д;
- 4. а, г, д;
- 5. а, б, д.
- 1. все ответы правильные;
- 2. а, б;
- 3. б, в;
- 4. в, г;
- 5. г, д.
- 1. яичники;
- 2. печень;
- 3. надключичные лимфоузлы;
- 4. трубчатые кости бедра;
- 5. дугласово пространство.
44. У больного 70 лет опухоль с тотальным поражением желудка, полностью стенозирующая выход из желудка. Диагноз установлен с помощью ЭГДС. При поступлении взята биопсия. При УЗИ - метастазы в печени, асцит. Какой метод хирургического лечения наиболее обоснован у данного больного?
Читайте также:
